Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Tarea. Esterificación en Medio Basico DMAP Ó DMAP-DCC R.L
Cargado por
Reynel A. Lugo0 calificaciones0% encontró este documento útil (0 votos)
63 vistas2 páginasTítulo original
Tarea. Esterificación en medio Basico DMAP ó DMAP-DCC R.L
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
63 vistas2 páginasTarea. Esterificación en Medio Basico DMAP Ó DMAP-DCC R.L
Cargado por
Reynel A. LugoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
Métodos de síntesis Orgánica
Esterificación en medio básico (DMAP – DMAP/DCC)
Esta reacción tiene lugar generalmente, a temperatura ambiente. Un disolvente adecuado es el
diclorometano. Debido a que la reacción es leve, se pueden obtener ésteres que son inaccesibles
por medio de otros métodos, por ejemplo, los ésteres del ácido 2,4-dihidroxibenzoico. Con
aminas, la reacción procede sin problema alguna a la correspondiente amida, debido a que las
aminas son mejores nucleófilos. Si la reacción es lenta, puede ocurrir una reacción secundaria,
disminuyendo el rendimiento final o complicando la purificación del producto. Esta reacción es
un reordenamiento 1,3 del intermediario O-acilo a una N-acilurea, la cual no es capaz de
reaccionar con el alcohol y dar el producto deseado. El DMAP suprime esta reacción actuando
como un reactivo de transferencia de acilo.
Mecanismo general de la reacción
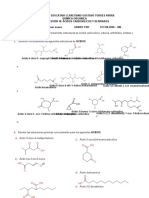
Síntesis de derivados del éster proveniente del ácido (E)-cinámico
Condiciones de reacción
La esterificación de Steglich utiliza tradicionalmente N,N-diciclohexilcarbodiimida (DCC) con
N-dimetilamino piridina (DMAP) como catalizadores y emplea diclorometano como solvente.
Acá se modificaron condiciones, se trabajó con carbodiimida junto con DMAP en vez de DCC, y
como solvente se empleó acetonitrilo. En esta reacción, el ácido se activa primero por la
carbodiimida, para formar un intermediario de O-acilisourea. Para la síntesis de ésteres, la adición
de DMAP es importante, porque minimiza la formación de un subproducto de migración 1,3 del
intermediario O-acilo a una N-acilurea, la cual no es capaz de reaccionar con el alcohol y dar el
producto deseado, el cual compite con el ataque nucleofílico del alcohol en el intermediario. La
formación del subproducto de migración de acilo intramolecular es lenta en comparación con un
ataque nucleofílico por parte de los grupos amino.
Las condiciones en el experimento, además del empleo de acetonitrilo; se trabajo en condiciones
de 40-45ªC, las cuales fueron elegidas para permitir un comportamiento similar a la del
diclorometano a temperatura ambiente, fueron empleados una gran variedad de alcoholes para
evaluar la influencia de los efectos estéricos y electrónicos respecto al alcohol. Con este método
en mente, se sintetizaron una gran variedad de derivados de éster del ácido (E)-cinámico. Los
derivados de alcoholes alifáticos primario y secundarios y de alcoholes bencílicos y alílicos
formaron el éster correspondiente fácilmente bajos las condiciones ya mencionadas. Los fenoles
que contiene sustituyentes tanto donadores como aceptores de electrones también pueden
reaccionar fácilmente con el ácido (E)-cinámico bajo las mismas condiciones. Para alcoholes
bencílicos más impedidos estéricamente se necesitó de calor adicional para permitir un
rendimiento notable en tiempos de reacción de 45 minutos. Ahora bien, con respecto a los
rendimientos moderados bajo las condiciones empleadas, se pueden mejorar con tiempos de
reacción mayores (24h para Temperatura ambiente) o a temperaturas más altas (60ªC). En lo que
respecta a los alcoholes terciarios, no pudo aislarse bajo estás condiciones el producto lo cual es
una desventaja en cuanto se emplea solventes clorados.
Reynel Lugo
También podría gustarte
- Previo 9 Org IIDocumento6 páginasPrevio 9 Org IIPipö Lopz LömbardoAún no hay calificaciones
- Quimica Biorganica p2Documento5 páginasQuimica Biorganica p2Juan AntonioAún no hay calificaciones
- Informe Condensacion AldolicaDocumento7 páginasInforme Condensacion AldolicaDayan OcampoAún no hay calificaciones
- Practica Aldehidos y CetonasDocumento11 páginasPractica Aldehidos y CetonasAlejandra Yauri Tintaya0% (3)
- Butiraldehido 1Documento4 páginasButiraldehido 1Ar RaAún no hay calificaciones
- Reacción Reimer-Tiemann para formilar fenolDocumento6 páginasReacción Reimer-Tiemann para formilar fenolJESUS ALBERTO HERNANDEZ SUAREZAún no hay calificaciones
- DibenzalacetonaDocumento5 páginasDibenzalacetonaKevin Alejandro OMAún no hay calificaciones
- Practica 7 DibenzalacetonaDocumento6 páginasPractica 7 DibenzalacetonaÓscar AguirreAún no hay calificaciones
- Reacciones de Alcoholes y FenolesDocumento58 páginasReacciones de Alcoholes y FenolesRODRIGO DE JESUS RUBIO ROSASAún no hay calificaciones
- Acido CinamicoDocumento18 páginasAcido CinamicoHector Orozco GutierrezAún no hay calificaciones
- Informe OrganicaDocumento18 páginasInforme OrganicaCRQ_1994Aún no hay calificaciones
- Reacciones de aldehídos y cetonas: haloformo, Cannizzaro y condensación aldólicaDocumento6 páginasReacciones de aldehídos y cetonas: haloformo, Cannizzaro y condensación aldólicaSabadoGrisAún no hay calificaciones
- Condensación de Knoevenagel QuimicaDocumento8 páginasCondensación de Knoevenagel QuimicaFernanda Garcia HernandezAún no hay calificaciones
- Sintesis Organica FundamentalDocumento49 páginasSintesis Organica FundamentalMarco Antonio MorenoAún no hay calificaciones
- Practica 6Documento19 páginasPractica 6Duul Fuentes SosaAún no hay calificaciones
- Informe 4. Condensacion de Claisen-Schmidt y KnoevenagelDocumento8 páginasInforme 4. Condensacion de Claisen-Schmidt y KnoevenagelDiego Molina RoaAún no hay calificaciones
- Síntesis de CiclohexanonaDocumento4 páginasSíntesis de Ciclohexanonavicky gonzalezAún no hay calificaciones
- AcroleinaDocumento83 páginasAcroleinaRuben Dario100% (1)
- Informe Acido CinamicoDocumento7 páginasInforme Acido CinamicoAlina Constanza Silva RicardoAún no hay calificaciones
- Práctica 7 AldehídoDocumento6 páginasPráctica 7 AldehídoJulio Cesar Jimenez BautistaAún no hay calificaciones
- Practica 7 de OrganicaDocumento8 páginasPractica 7 de OrganicaHéctor Velázquez CastroAún no hay calificaciones
- Preinforme Aldehidos y CetonasDocumento25 páginasPreinforme Aldehidos y CetonasRoly Neftal Paniagua MurilloAún no hay calificaciones
- Conductividad Térmica NylonDocumento5 páginasConductividad Térmica NylonPame FlowersAún no hay calificaciones
- Síntesis de Ácido CinámicoDocumento4 páginasSíntesis de Ácido CinámicoAngelo MolinaAún no hay calificaciones
- PREPARACIÓN AnilinaDocumento8 páginasPREPARACIÓN AnilinaChurio Silvera OscarAún no hay calificaciones
- Ruta y SeparaciónDocumento5 páginasRuta y SeparaciónEric BaizánAún no hay calificaciones
- Reacciones de Adición NuDocumento131 páginasReacciones de Adición NuAle GutiérrezAún no hay calificaciones
- 8 Aldehídos y CetonasDocumento7 páginas8 Aldehídos y Cetonassaulcarvajal23Aún no hay calificaciones
- Obtención de ácido cinámico por microondasDocumento12 páginasObtención de ácido cinámico por microondasRaúl Jair Cortés CabañasAún no hay calificaciones
- Reactividad Aldehidos y Cetonas V.2Documento32 páginasReactividad Aldehidos y Cetonas V.2emstorAún no hay calificaciones
- Síntesis de piperonal mediante oxidación selectiva de alcoholDocumento8 páginasSíntesis de piperonal mediante oxidación selectiva de alcoholJuan100% (1)
- AnilinaDocumento10 páginasAnilinahairmonAún no hay calificaciones
- Reacción de Knoevenagel para obtener ácido cinámicoDocumento12 páginasReacción de Knoevenagel para obtener ácido cinámicoKatherine RamírezAún no hay calificaciones
- Practica Reacciones de Aldehídos y Cetonas. Obtención de La CanforoximaDocumento7 páginasPractica Reacciones de Aldehídos y Cetonas. Obtención de La Canforoximalameramocha50% (2)
- Practica 6 de ReaccionDocumento7 páginasPractica 6 de Reaccionclaudia vasquezAún no hay calificaciones
- Anhidrido MaleicoDocumento10 páginasAnhidrido MaleicoAlejandro Vergel UsecheAún no hay calificaciones
- Síntesis de salicilaldehido en UNAMDocumento6 páginasSíntesis de salicilaldehido en UNAMNadia AuzsaAún no hay calificaciones
- Haluros de Alquilo A Aldehídos y CetonasDocumento6 páginasHaluros de Alquilo A Aldehídos y CetonasJorge Alberto Estrada TorresAún no hay calificaciones
- Síntesis y Análisis de Una Imina y Una Amina VersátilesDocumento4 páginasSíntesis y Análisis de Una Imina y Una Amina VersátilesAylin LezmesAún no hay calificaciones
- ThiokolDocumento20 páginasThiokolCinthiaFabiánMesiasAún no hay calificaciones
- Acetilación Anilina Rendimiento 42Documento14 páginasAcetilación Anilina Rendimiento 42DavidAún no hay calificaciones
- Oxidación de Aldehídos y CetonasDocumento11 páginasOxidación de Aldehídos y CetonasCrowley Nightray WaylandAún no hay calificaciones
- Organica 6Documento10 páginasOrganica 6maikol0% (1)
- AlquilacionDocumento4 páginasAlquilacionjustislaura_Aún no hay calificaciones
- Práctica 3 OrgánicaDocumento6 páginasPráctica 3 OrgánicaEsmeralda Galvan SixtoAún no hay calificaciones
- La Oxidación Perácida de IsosafrolDocumento7 páginasLa Oxidación Perácida de IsosafrolJorge Alberto Estrada TorresAún no hay calificaciones
- Diapositiva FinalDocumento42 páginasDiapositiva Finalroyer torrezAún no hay calificaciones
- ExposiciónDocumento12 páginasExposiciónXAVIER ISRAEL CHANCUSIG QUILUMBAAún no hay calificaciones
- ImformeDocumento5 páginasImformeAnonymous MVMOeliIRzAún no hay calificaciones
- Síntesis dibenzalacetonaDocumento5 páginasSíntesis dibenzalacetonaLuis RomeroAún no hay calificaciones
- Condensación de ClaisenDocumento7 páginasCondensación de ClaisenJorge RomeroAún no hay calificaciones
- Modificacion de Verley-DobnerDocumento18 páginasModificacion de Verley-DobnerLaura TrujilloAún no hay calificaciones
- Reacciones de Sustitución Nucleofilica SN Síntesis de Cloruro de Terc-ButiloDocumento8 páginasReacciones de Sustitución Nucleofilica SN Síntesis de Cloruro de Terc-ButiloJonathan ReyesAún no hay calificaciones
- Metodos de ObtenciónDocumento9 páginasMetodos de ObtenciónSharyn CruzAún no hay calificaciones
- Etapas Del PardeamientoDocumento4 páginasEtapas Del PardeamientoMonica PugaAún no hay calificaciones
- Act Previas MetilnaftilicoDocumento6 páginasAct Previas MetilnaftilicodanielAún no hay calificaciones
- Informe 3 de Organica 2Documento8 páginasInforme 3 de Organica 2David JuniorAún no hay calificaciones
- Manual técnico de refrigerantesDe EverandManual técnico de refrigerantesCalificación: 4 de 5 estrellas4/5 (4)
- Reflexión Del Pensamiento Complejo. Edgar Morin Reynel Lugo 24334505Documento3 páginasReflexión Del Pensamiento Complejo. Edgar Morin Reynel Lugo 24334505Reynel A. LugoAún no hay calificaciones
- TAREA #1. Tecnología de Vacío (Bombas y Medidores) Reynel Lugo 24334505Documento9 páginasTAREA #1. Tecnología de Vacío (Bombas y Medidores) Reynel Lugo 24334505Reynel A. LugoAún no hay calificaciones
- Reynel Lugo 24334505. Mapa Mental Unidad 1. Desarrollo Manipulación y Aprendizaje.Documento2 páginasReynel Lugo 24334505. Mapa Mental Unidad 1. Desarrollo Manipulación y Aprendizaje.Reynel A. LugoAún no hay calificaciones
- Observación de un proceso instruccional en Educación Media GeneralDocumento19 páginasObservación de un proceso instruccional en Educación Media GeneralReynel A. LugoAún no hay calificaciones
- VivirBienResumenDocumento14 páginasVivirBienResumenReynel A. LugoAún no hay calificaciones
- Escalamiento, Desde Escala Laboratorio Hasta Planta Piloto Del Proceso de Reacción de Nitrato de Plomo (II) Con Yoduro de PotasioDocumento7 páginasEscalamiento, Desde Escala Laboratorio Hasta Planta Piloto Del Proceso de Reacción de Nitrato de Plomo (II) Con Yoduro de PotasioReynel A. LugoAún no hay calificaciones
- Proyecto. La Neurociencia en El Camino Hacia La Neuroeducación, Inteligencias Múltiples y La Producción Escrita Como Expresión Del SerDocumento20 páginasProyecto. La Neurociencia en El Camino Hacia La Neuroeducación, Inteligencias Múltiples y La Producción Escrita Como Expresión Del SerReynel A. LugoAún no hay calificaciones
- Reynel Lugo V-24334505. Actividad 1. Análisis Zoom by Istvan BanyaiDocumento1 páginaReynel Lugo V-24334505. Actividad 1. Análisis Zoom by Istvan BanyaiReynel A. LugoAún no hay calificaciones
- Actividad Tema 4. Análisis EconómicoDocumento4 páginasActividad Tema 4. Análisis EconómicoReynel A. LugoAún no hay calificaciones
- Prueba Unidad 1 Reynel Lugo 24334505. Componente DocenteDocumento4 páginasPrueba Unidad 1 Reynel Lugo 24334505. Componente DocenteReynel A. LugoAún no hay calificaciones
- Asignación 3. DFP Producción Formaldehído - Rutas Primarias.Documento7 páginasAsignación 3. DFP Producción Formaldehído - Rutas Primarias.Reynel A. LugoAún no hay calificaciones
- Actividad 1 R. L. 24334505Documento2 páginasActividad 1 R. L. 24334505Reynel A. LugoAún no hay calificaciones
- Asignación 2. Diagrama de Bloques FormalinaDocumento4 páginasAsignación 2. Diagrama de Bloques FormalinaReynel A. LugoAún no hay calificaciones
- Ensayo. Tiempo Fuera de La Mente. Reynel Lugo 24334505Documento7 páginasEnsayo. Tiempo Fuera de La Mente. Reynel Lugo 24334505Reynel A. LugoAún no hay calificaciones
- Actividad 7. Cuestionario. Reynel Lugo 24334505Documento13 páginasActividad 7. Cuestionario. Reynel Lugo 24334505Reynel A. LugoAún no hay calificaciones
- Asignacion 1 DFP de La FormalinaDocumento1 páginaAsignacion 1 DFP de La FormalinaReynel A. LugoAún no hay calificaciones
- Proceso formalina UCVDocumento6 páginasProceso formalina UCVReynel A. LugoAún no hay calificaciones
- Tarea. Ácdio-Base Blando-Duro R.LDocumento2 páginasTarea. Ácdio-Base Blando-Duro R.LReynel A. LugoAún no hay calificaciones
- Asignación Tema 9. Descontaminación Reynel Lugo 24334505Documento2 páginasAsignación Tema 9. Descontaminación Reynel Lugo 24334505Reynel A. LugoAún no hay calificaciones
- Asignación 7. Resumen AlquimiaDocumento6 páginasAsignación 7. Resumen AlquimiaReynel A. LugoAún no hay calificaciones
- Tarea Reacción Ritter R.LDocumento2 páginasTarea Reacción Ritter R.LReynel A. LugoAún no hay calificaciones
- Actividad 2 R. L. 24334505Documento2 páginasActividad 2 R. L. 24334505Reynel A. LugoAún no hay calificaciones
- Monografía Final de Síntesis. Sirolimus R.L.Documento22 páginasMonografía Final de Síntesis. Sirolimus R.L.Reynel A. LugoAún no hay calificaciones
- Metodos CineticosDocumento21 páginasMetodos CineticosReynel A. LugoAún no hay calificaciones
- Monografía Grupos Protectores Ac. Carboxílicos, Aldehídos y CetonasDocumento24 páginasMonografía Grupos Protectores Ac. Carboxílicos, Aldehídos y CetonasReynel A. LugoAún no hay calificaciones
- Tarea Reducción de Nitrocompuestos A Aminas R.LDocumento3 páginasTarea Reducción de Nitrocompuestos A Aminas R.LReynel A. LugoAún no hay calificaciones
- Tarea Esterificación en Medio Básico N-Metilimidazol R.LDocumento2 páginasTarea Esterificación en Medio Básico N-Metilimidazol R.LReynel A. LugoAún no hay calificaciones
- Tarea. Transformación de Nitrocompuestos A Carbonilo R.LDocumento1 páginaTarea. Transformación de Nitrocompuestos A Carbonilo R.LReynel A. LugoAún no hay calificaciones
- Métodos de síntesis orgánica: oxidación de SwernDocumento4 páginasMétodos de síntesis orgánica: oxidación de SwernReynel A. LugoAún no hay calificaciones
- Laboratorio de ProteínaDocumento4 páginasLaboratorio de ProteínaMaryorisAún no hay calificaciones
- 5 - Estructura de Proteinas 20-11-18Documento55 páginas5 - Estructura de Proteinas 20-11-18Yessenia FloresAún no hay calificaciones
- Ácidos Carbocilicos y DerivadosDocumento10 páginasÁcidos Carbocilicos y DerivadosJairo Rodriguez SuazaAún no hay calificaciones
- 005 Apunte - Materiales Org - Inorg - VGVDocumento6 páginas005 Apunte - Materiales Org - Inorg - VGVfotoseuro23Aún no hay calificaciones
- Proyecto de Los Cursos de Hidraulica Gutnar Fernando Peñaloza MolinaDocumento55 páginasProyecto de Los Cursos de Hidraulica Gutnar Fernando Peñaloza MolinaHenry CañotoAún no hay calificaciones
- ALCOHOLES, FENOLES, CETONEAS InformeDocumento22 páginasALCOHOLES, FENOLES, CETONEAS InformeCinthia Bustos AguilarAún no hay calificaciones
- Mapa Mental Quimica oDocumento1 páginaMapa Mental Quimica obrayan criolloAún no hay calificaciones
- Hidrocarburos no convencionales BoliviaDocumento13 páginasHidrocarburos no convencionales BoliviaDavid DelgadilloAún no hay calificaciones
- Sikabond ConstructionadhesiveDocumento3 páginasSikabond ConstructionadhesiveRandol RiveroAún no hay calificaciones
- Aminoácidos, péptidos y proteínas esencialesDocumento20 páginasAminoácidos, péptidos y proteínas esencialesDiego CorboAún no hay calificaciones
- Biosintesis de Purinas y NovoDocumento14 páginasBiosintesis de Purinas y NovoDBZ GOKU47Aún no hay calificaciones
- Capitulo 7-Biol-Unmsm-2013Documento24 páginasCapitulo 7-Biol-Unmsm-2013mike kaiser romanovAún no hay calificaciones
- Agua SupercriticaDocumento8 páginasAgua SupercriticaJose Miguel Pariguana QuispeAún no hay calificaciones
- Ejercicios de Equilibrio Químico KcDocumento2 páginasEjercicios de Equilibrio Químico KcJuan Camilo CamachoAún no hay calificaciones
- Porcentaje de Materia Organica-3roaDocumento18 páginasPorcentaje de Materia Organica-3roaMichelle RodriguezAún no hay calificaciones
- Laboratorio Quimica - Informe 1Documento14 páginasLaboratorio Quimica - Informe 1Alberto CuevaAún no hay calificaciones
- PIRIDINADocumento95 páginasPIRIDINAMario Leonardo Guevara EscalanteAún no hay calificaciones
- Catalogo General Mapa Professional 2020 - GUANTESDocumento31 páginasCatalogo General Mapa Professional 2020 - GUANTESCarlosAún no hay calificaciones
- Semana 11 AldehidosDocumento5 páginasSemana 11 Aldehidossamantha vidalAún no hay calificaciones
- Qué Es El XilenoDocumento4 páginasQué Es El XilenoOscar Lopez AguilarAún no hay calificaciones
- Neurotransmisores convencionales y no convencionalesDocumento2 páginasNeurotransmisores convencionales y no convencionalesRoger PerezAún no hay calificaciones
- Las PinturasDocumento18 páginasLas PinturasPedro Jose Ardila GomezAún no hay calificaciones
- Ue Ames Tarea Ev 4120 50547 20231130205107Documento14 páginasUe Ames Tarea Ev 4120 50547 20231130205107emilydannyvintimillaAún no hay calificaciones
- Informe 11Documento5 páginasInforme 11ClaudiaEcheverryVivesAún no hay calificaciones
- Todo sobre los plásticos: tipos, usos, impacto ambiental y cómo reciclarlosDocumento5 páginasTodo sobre los plásticos: tipos, usos, impacto ambiental y cómo reciclarlosMARCELINO RUBEN MERINO CONDARCOAún no hay calificaciones
- Avances Tecnologicos A Base de CarbonDocumento37 páginasAvances Tecnologicos A Base de CarbonJesús Ruiz100% (1)
- Exposicion Final Compuestos CarbonilicosDocumento14 páginasExposicion Final Compuestos Carbonilicoslaura camila ussa vidalAún no hay calificaciones
- TRANSCRIPCION GeneralidadesDocumento14 páginasTRANSCRIPCION GeneralidadesFacundo Exequiel CorreaAún no hay calificaciones
- Técnicas de SeparaciónDocumento24 páginasTécnicas de SeparaciónJairArmandoGomezPerez0% (1)
- Nitración de Benzoato de Metilo (Virtual)Documento35 páginasNitración de Benzoato de Metilo (Virtual)Fa kochoAún no hay calificaciones