Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Altv J65397 Es I 3
Cargado por
Papeleria Diseño y ArteTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Altv J65397 Es I 3
Cargado por
Papeleria Diseño y ArteCopyright:
Formatos disponibles
INSTRUCCIONES DE USO ALTV
Slides VITROS Chemistry Products ALTV Alanina aminotransferasa
684 4288
Aplicación
Solo para uso diagnóstico in vitro.
Los Slides VITROS Chemistry Products ALTV determinan cuantitativamente la actividad de la alanina aminotransferasa
(ALT) en el suero y plasma utilizando los sistemas VITROS 250/350/5,1 FS/4600/XT 3400 Chemistry System y los
sistemas VITROS 5600/XT 7600 Integrated System. La determinación del nivel de alanina aminotransferasa se utiliza en el
diagnóstico y tratamiento de determinadas enfermedades hepáticas (por ejemplo, hepatitis y cirrosis) y enfermedades
cardiacas.
Resumen y explicación
La alanina aminotransferasa (ALT), una enzima involucrada en el metabolismo de aminoácidos, se encuentra en muchos
tejidos, como en el hígado, el músculo cardiaco y esquelético, los riñones y el páncreas. Por tanto, las elevaciones de ALT
se asocian con trastornos tanto hepáticos como no hepáticos, por ejemplo, la hepatitis, la cirrosis, los tumores hepáticos, la
obstrucción biliar, el síndrome de Reye, la rabdomiólisis, la miositis, la miocarditis y el infarto de miocardio. Debido a su
distribución principalmente hepática, las elevaciones de ALT son muy útiles a la hora de detectar el daño hepático 1, 2 y las
mediciones de ALT son especialmente útiles en el diagnóstico y gestión de una enfermedad hepática.
Principios del procedimiento
El Slide VITROS ALTV es un elemento analítico multicapa incorporado a un soporte de poliéster. En el slide se deposita
una gota de muestra del paciente, que se distribuye uniformemente desde la capa difusora a las capas subyacentes. La
capa difusora contiene los sustratos de la ALT, L-alanina y α-cetoglutarato sódico. La alanina aminotransferasa cataliza la
transferencia del grupo amino de L-alanina a α-cetoglutarato en presencia de piridoxal-5-fosfato (P-5-P) para producir
piruvato y glutamato. La piruvato oxidasa oxida al piruvato en acetilfosfato y peróxido de hidrógeno. El paso final de la
reacción implica la oxidación catalizada por la peroxidasa de un leucoderivado para dar un pigmento coloreado. La
frecuencia de oxidación del leucoderivado se monitoriza por espectrofotometría de reflectancia. La frecuencia de cambio
en la densidad de reflectancia es proporcional a la actividad enzimática en la muestra. El filtro de corte de la longitud de
onda corta presente en la montura del slide minimiza los efectos de frecuencia del blanco de la luz incidente durante el
desarrollo del colorante.
Tipo y condiciones del ensayo
Tiempo Volumen de
aproximado de Longitud de muestra de
Tipo de ensayo Sistema VITROS incubación Temperatura onda reacción
5600, 4600, 5,1
Cinética
FS, 250/350, XT 5 minutos 37 °C 670 nm 7 μL
multipunto
7600, XT 3400
No todos los productos y sistemas se comercializan en todos los países.
Esquema de la reacción
ALT
alanina + α-cetoglutarato piridoxal-5–fosfato
piruvato + glutamato
piruvato oxidasa peróxido de hidrógeno + acetilfosfato +
piruvato + fosfato + O2
CO2
peroxidasa
peróxido de hidrógeno + leucoderivado colorante
Versión 4.0 N.º de pub. J65397_ES 1 de 13
ALTV INSTRUCCIONES DE USO
Alanina aminotransferasa Advertencias y precauciones
Advertencias y precauciones
Solo para uso diagnóstico in vitro.
ADVERTENCIA: Tome precauciones cuando manipule materiales y muestras de origen humano.
Como ningún método de ensayo puede ofrecer una seguridad completa sobre la
ausencia de agentes infecciosos, considere todas las muestras, controles y
calibradores clínicos como potencialmente infecciosos. Manipule las muestras,
los residuos sólidos y líquidos, así como los componentes del ensayo, de
acuerdo con las normativas locales y la directriz M29 3 del CLSI u otras pautas
de seguridad publicadas en relación con los riesgos biológicos.
Encontrará advertencias y precauciones específicas de los distintos calibradores, así como de los materiales de control de
calidad y otros componentes en las instrucciones de uso del producto correspondiente y en cualquier otra documentación
del producto facilitada por el fabricante.
Reactivos
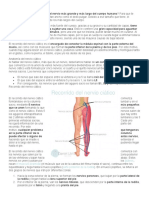
Diagrama del slide
Ingredientes del slide 1. Montura superior del slide
2. Capa difusora (BaSO4)
Ingredientes reactivos por cm2 • α–cetoglutarato sódico
• L-alanina
α-cetoglutarato sódico 0,204 mg; L-alanina 0,108 mg; 2-(3,5- 3. Capa reactiva
dimetoxi-4-hidroxifenil)-4,5-bis(4-dimetilaminofenil) imidazol 37,5 • tampón de pH 7,35
• leucoderivado
µg; fosfato sódico 42 µg; sodio piridoxal-5-fosfato 22 µg; piruvato • fosfato de sodio
oxidasa (Aerococcus sp.) 0,2 U; y peroxidasa (raíz de rábano • piruvato oxidasa
• peroxidasa
picante) 0,5 U. • piridoxal-5-fosfato sódico
4. Soporte
Otros ingredientes 5 Filtro: filtro de corte de la luz
Ligantes, tampones, pigmento, estabilizantes, depurador, de longitud de onda corta
cofactores enzimáticos, solubilizante de colorante, agente 6 Montura inferior del slide
reticulante de polímeros y colorantes de filtros.
Manipulación de los reactivos
Atención: No utilice cartuchos de slide cuyo envoltorio presente daños o un sellado
incompleto.
• Inspeccione el envoltorio para comprobar la ausencia de daños.
• Cuando abra el envoltorio externo con un instrumento afilado, preste atención para no dañar el envoltorio individual del
producto.
Preparación del reactivo
IMPORTANTE: El cartucho de slide debe alcanzar la temperatura ambiente, 18–28 ° C, antes de
extraerlo de su envase y cargarlo en el tambor de reactivos.
1. Retire los cartuchos de slide de su lugar de almacenamiento.
2. Con el cartucho aún en el envoltorio, espere a que alcance la temperatura ambiente (30 minutos si estaba en un
refrigerador, o 60 minutos si estaba en un congelador).
3. Desenvuelva el cartucho y cárguelo en el tambor de reactivos.
Nota: Cargue los cartuchos dentro de las 24 horas siguientes de alcanzar la
temperatura ambiente, 18–28 ° C.
Conservación y estabilidad de los reactivos
Cuando se conservan y manipulan según las indicaciones correspondientes, los Slides VITROS ALTV se mantienen
estables hasta la fecha de caducidad que figura en el envase. No los utilice después de la fecha de caducidad.
Reactivo Condiciones de conservación Estabilidad
Sin abrir Refrigerado 2–8 °C ≤ 3 meses
Congelado ≤ -18 °C Hasta la fecha de
caducidad
Abierto En el analizador Sistema encendido ≤ 2 semanas
En el analizador Sistema apagado ≤ 2 horas
Utilice materiales de control de calidad para verificar el rendimiento:
2 de 13 N.º de pub. J65397_ES Versión 4.0
INSTRUCCIONES DE USO ALTV
Recogida, preparación y almacenamiento de las muestras Alanina aminotransferasa
• Cuando el sistema haya permanecido apagado más de 2 horas.
• Tras volver a cargar cartuchos que se hayan retirado del tambor de reactivos y se hayan almacenado para su uso
posterior.
Recogida, preparación y almacenamiento de las muestras
Muestras recomendadas
• Suero
• Plasma: heparinizado
IMPORTANTE: Se ha descrito que ciertos dispositivos de recogida de muestras pueden afectar
a otras pruebas y analitos. 4 Debido a la variedad de dispositivos
comercializados para la recogida de muestras, Ortho Clinical Diagnostics no
puede proporcionar una declaración final acerca del rendimiento de sus
reactivos con cada uno de estos dispositivos. Confirme que sus dispositivos de
recogida sean compatibles con esta prueba.
Muestras no recomendadas
• K2 Plasma en EDTA
Suero y plasma
Obtención y preparación de las muestras
Recoja las muestras utilizando los procedimientos de laboratorio estándar. 5, 6
Nota: Encontrará información detallada sobre los requisitos de volumen de llenado
mínimo en las instrucciones de funcionamiento de su analizador.
Preparación del paciente
No se requiere ninguna preparación especial del paciente.
Precauciones especiales
Centrifugue las muestras y retire el suero o plasma del material celular dentro de un plazo de 3 días tras la recogida. 7
Manipulación y conservación de las muestras
• Manipule y conserve las muestras en contenedores tapados para evitar su posible contaminación o evaporación.
• Mezcle las muestras por inversión suave y espere a que alcancen la temperatura ambiente, 18–28 ° C, antes del
análisis.
IMPORTANTE: No congele la muestra.
Conservación y estabilidad de las muestras
Conservación Temperatura Estabilidad
Temperatura ambiente 18–28 °C ≤ 18 horas
Refrigerado 2–8 °C ≤ 1 semana
Congelado ≤ -18 °C No se recomienda
Procedimiento del ensayo
Materiales suministrados
Slides VITROS Chemistry Products ALTV
Materiales necesarios no suministrados
• VITROS Chemistry Products Calibrator Kit 3.
• Materiales de control de calidad, tales como el VITROS Chemistry Products Performance Verifier I y II
• VITROS Chemistry Products 7% BSA
• VITROS Chemistry Products FS Diluent Pack 2 (BSA/Saline) (en el modo dilución en el analizador)
Instrucciones de funcionamiento
• Compruebe los inventarios de reactivo al menos una vez al día para asegurarse de que las cantidades existentes sean
suficientes para la carga de trabajo prevista.
• Para obtener más información, consulte las instrucciones de funcionamiento de su sistema.
Versión 4.0 N.º de pub. J65397_ES 3 de 13
ALTV INSTRUCCIONES DE USO
Alanina aminotransferasa Calibración
IMPORTANTE: Espere a que todos los fluidos y las muestras alcancen la temperatura ambiente,
18–28 ° C, antes del análisis.
Dilución de la muestra
Si la actividad de la alanina aminotransferasa excede el intervalo de medición (comunicable o dinámico) del sistema:
Dilución de la muestra en el analizador (solo sistemas VITROS 5600/XT 7600 Integrated y VITROS 250/350, 5,1 FS/
4600/XT 3400 Chemistry System)
Para obtener más información sobre el procedimiento de dilución en el analizador, consulte las instrucciones de
funcionamiento de su analizador. Para los sistemas VITROS 5600/XT 7600 Integrated y VITROS 5,1 FS/4600 Chemistry
System, use VITROS Chemistry Products FS Diluent Pack 2 para la dilución.
Para los sistemas VITROS 250/350 y VITROS XT 3400 Chemistry System, use VITROS 7% BSA para la dilución.
Dilución manual de la muestra
1. Diluya la muestra con VITROS 7% BSA.
2. Repita el análisis.
3. Multiplique los resultados por el factor de dilución para obtener un cálculo de la concentración de alanina
aminotransferasa en la muestra original.
Calibración
Calibradores necesarios
VITROS Chemistry Products Calibrator Kit 3.
Preparación, manipulación y conservación de los calibradores
Consulte las Instrucciones de uso correspondientes al VITROS Calibrator Kit 3.
Procedimiento de calibración
Consulte las instrucciones de funcionamiento de su sistema.
Cuándo calibrar
Realice una calibración en las siguientes circunstancias:
• Cuando cambie el número de lote de los slides.
• Cuando se sustituyan piezas esenciales del sistema durante un procedimiento de mantenimiento o reparación.
• Cuando así lo requieran las normativas gubernamentales.
Por ejemplo, en EE.UU., las normas de la CLIA exigen que la calibración se realice o se compruebe al menos una vez
cada seis meses.
También puede ser necesario calibrar el ensayo VITROS ALTV:
• Si los resultados de control de calidad están consistentemente fuera del intervalo aceptable.
• Tras llevar a cabo determinados procedimientos de mantenimiento.
Para obtener más información, consulte las instrucciones de funcionamiento de su sistema.
Cálculos
Tomando como base lecturas secuenciales de la reflectancia del slide a 670 nm durante el periodo de incubación definido,
se determina el porcentaje de cambio de la reflectancia. Esta frecuencia se utiliza en el modelo de calibración de cinética
multipunto residente en el software para calcular la actividad enzimática. Después de haberse establecido la calibración de
cada lote de slides, puede determinarse la actividad de la alanina aminotransferasa en muestras desconocidas a partir de
la frecuencia de cambio en la reflectancia medida en cada uno de los slides de ensayo desconocidos.
Validez de la calibración
Los parámetros de calibración los evalúa automáticamente el sistema por comparación con un conjunto de parámetros de
calidad que se detallan en la pantalla de coeficientes y límites de los sistemas VITROS 250/350 System (en los sistemas
VITROS 5600/XT 7600 Integrated y VITROS 5,1 FS/4600/XT 3400 System, consulte la pantalla Revisar datos de la
prueba). Si se incumple alguno de los parámetros de calidad predefinidos, la calibración fallará. El informe de calibración
debe usarse conjuntamente con los resultados de control de calidad para determinar la validez de la calibración.
Intervalo de medición (comunicable o dinámico)
Unidades convencionales y SI Unidades alternativas
(U/L) (μkat/L)
4–750 0,07–12,53
Para muestras fuera del intervalo, consulte el apartado“Dilución de la muestra”.
4 de 13 N.º de pub. J65397_ES Versión 4.0
INSTRUCCIONES DE USO ALTV
Control de calidad Alanina aminotransferasa
Trazabilidad de la calibración
Los valores asignados al VITROS Chemistry Products Calibrator Kit 3 en el ensayo de alanina aminotransferasa pueden
rastrearse al método de la alanina aminotransferasa recomendado por la Federación Internacional de Química Clínica
(IFCC). 8
Control de calidad
Selección de materiales de control de calidad
IMPORTANTE: Se recomienda utilizar los VITROS Performance Verifiers siempre que se trabaje
con VITROS de Bioquímica y VITROS Integrated Systems. Antes de utilizar
cualquier otro líquido de control comercial, evalúe su compatibilidad con el
ensayo.
• Los materiales de control distintos de los verificadores del rendimiento VITROS pueden mostrar diferencias en
comparación con otros métodos aplicables a la alanina aminotransferasa si:
– No corresponden a una matriz verdaderamente humana.
– Contienen altas concentraciones de conservantes, estabilizantes u otros aditivos no fisiológicos.
• La actividad de la enzima también puede variar dependiendo del origen de la enzima, la temperatura del diluyente y el
tiempo de activación durante la reconstitución.
• No utilice materiales de control estabilizados con etilenglicol.
Recomendaciones sobre los procedimientos de control de calidad
• Elija niveles de control apropiados para verificar el intervalo pertinente desde el punto de vista clínico.
• Analice los materiales de control de calidad del mismo modo que las muestras de pacientes, antes o durante el
procesamiento de las muestras.
• Para verificar el rendimiento del sistema, analice los materiales de control:
– Tras realizar una calibración.
– De acuerdo con las normativas locales y, al menos, una vez cada día que se realice el ensayo.
– Tras realizar los procedimientos de reparación especificados. Consulte las instrucciones de funcionamiento de su
sistema.
• Si los resultados del control están fuera del rango aceptable, investigue las causas antes de decidir si se va a informar o
no de los resultados del paciente.
• Encontrará recomendaciones genéricas sobre el control de la calidad en CLSI Statistical Quality Control for Quantitative
Measurements: Principles and Definitions; Approved Guideline-Third Edition 9 u otras directrices publicadas.
• Para obtener más información, consulte las instrucciones de funcionamiento de su sistema.
Preparación, manipulación y conservación del material de control de calidad
Consulte las instrucciones de uso del VITROS Chemistry Products Performance Verifier I y II u otra documentación del
producto facilitada por el fabricante.
Resultados
Unidades de medida y conversión de unidades
Los VITROS de Bioquímica y VITROS Integrated Systems pueden programarse para expresar los resultados de ALTV en
unidades convencionales, SI y alternativas.
Unidades convencionales y SI Unidades alternativas
U/l µkat/l (U/l x 0,0167)
Limitaciones del procedimiento
Interferencias conocidas
Suero y plasma
El método de Slides VITROS Chemistry Products ALTV ha sido analizado para la detección de sustancias interferentes
según el protocolo EP07 del CLSI. 10 Las sustancias enumeradas en la tabla produjeron las desviaciones mostradas
cuando se analizaron en las concentraciones indicadas.
Para saber las sustancias que se analizaron sin que se detectaran interferencias, consulte el apartado “Especificidad”.
Versión 4.0 N.º de pub. J65397_ES 5 de 13
ALTV INSTRUCCIONES DE USO
Alanina aminotransferasa Valores esperados
Actividad alanina
aminotransferasa Desviación
Interferente* Concentración del interferente Unidades Unidades
Unidades conv. alternativas conv. y SI Unidades alternativas
y SI (U/L) (µkat/L) (U/L) (µkat/L)
49 mg/dL 3,0 mmol/L 62 1,04 -8 -0,13
N-acetilcisteína**
38 mg/dL 2,3 mmol/L 298 4,98 -25 -0,42
11 mg/dL 0,353 mmol/L 64 1,07 -8 -0,13
Tolazamida
10 mg/dL 0,321 mmol/L 291 4,86 -24 -0,40
*Es posible que haya otras sustancias que presenten interferencias. Estos resultados son representativos; no obstante, sus resultados
pueden diferir ligeramente debido a la variación entre ensayos. El grado de interferencia para concentraciones distintas de las indicadas
puede no ser predecible.
**
N-acetilcisteína a 15 mg/dL, que corresponde al triple del nivel de suero tras dosis orales de hasta 14000 mg o una dosis IV de 600
mg, no causa ninguna desviación.
Otras limitaciones
• Niveles elevados de piruvato pueden provocar la aparición de indicadores TR o DP. Estas muestras deberán diluirse en
1 parte de muestra con 2 partes de BSA al 7% (3x) y repetirse. Si el código DP fue causado por un piruvato, el resultado
final de ALT puede ser normal o predecible dentro del intervalo del sistema.
• Se sabe que ciertos fármacos y afecciones clínicas alteran las concentraciones de ALT in vivo. Si desea más
información, consulte alguno de los resúmenes publicados. 11, 12
Valores esperados
Intervalo de referencia 13
Unidades convencionales y SI (U/L) Unidades alternativas (µkat/L)
Mujeres <35 <0,58
Varones <50 <0,84
Cada laboratorio debe confirmar la validez de estos intervalos para la población que atiende.
Características de rendimiento
Comparación de métodos
Los gráficos y la tabla muestran los resultados de comparar las muestras de suero analizadas en VITROS 5600 Integrated
System con las analizadas utilizando el método comparativo de IFCC. 8 Los ensayos se basan en el protocolo EP09 14 del
CLSI.
La tabla también muestra los resultados de las comparaciones de muestras de suero en los analizadores VITROS
250/350,5,1 FS y 4600 de Bioquímica con el VITROS 5600 Integrated System. Los ensayos se basan en el protocolo
EP09 14 del CLSI.
6 de 13 N.º de pub. J65397_ES Versión 4.0
INSTRUCCIONES DE USO ALTV
Características de rendimiento Alanina aminotransferasa
Unidades convencionales y SI Unidades alternativas
Sistema VITROS 5600 (µkat/L)
Sistema VITROS 5600 (U/L)
Método comparativo: IFCC Método comparativo: IFCC
(U/L) (μkat/L)
Unidades convencionales y SI
(U/L) Unidades alternativas (µkat/L)
Intervalo Intervalo
de de
Coeficiente actividad actividad
Pendi- de de de
n ente correlación muestra Intersección Sy.x muestra Intersección Sy.x
5600†† frente al método
comparativo 124 1,01 0,999 6–728 1,5 8,0 0,10–12,16 0,024 0,13
350 frente a 5600†† 127 1,00 1,000 9–733 0,2 3,5 0,15–12,24 0,002 0,06
4600 frente a 5600†† 127 1,00 1,000 9–733 –0,1 2,9 0,15–12,24 -0,002 0,05
5,1 FS† frente a 5600†† 127 0,99 1,000 9–733 0,4 3,7 0,15–12,24 0,006 0,06
† Las características de rendimiento de VITROS 5,1 FS System son válidas para VITROS 4600 System.
†† Las características de rendimiento de VITROS 5600 System son válidas para los sistemas VITROS XT 3400 y XT 7600 System.
Precisión
La precisión se evaluó con materiales de control de calidad y tres pools de muestras de pacientes en los analizadores
VITROS 350, VITROS 5,1 FS y VITROS 4600 de Bioquímica y el VITROS 5600 Integrated System conforme al protocolo
EP05 del CLSI. 15
Los datos facilitados son una representación del rendimiento del ensayo y se ofrecen a modo de orientación. Variables
tales como la manipulación y la conservación de muestras y reactivos, el entorno del laboratorio y el mantenimiento del
sistema pueden afectar a la reproducibilidad de los resultados del ensayo.
Unidades convencionales y SI (U/L)
Actividad Repetibilidad* Intradía** Intralab. *** N.º de N.º de
Sistema media DE CV% DE CV% DE CV% observ. días
14 0,1 0,7 0,1 0,7 0,3 2,1 80 20
32 0,2 0,6 0,3 0,9 0,6 1,9 80 20
350 168 1,2 0,7 1,5 0,9 2,6 1,5 80 20
343 2,1 0,6 2,7 0,8 4,7 1,4 80 20
572 3,3 0,6 4,8 0,8 6,2 1,1 80 20
14 0,1 0,7 0,1 0,7 0,2 1,4 88 22
32 0,2 0,6 0,3 0,9 0,4 1,3 88 22
4600 166 1,0 0,6 1,6 1,0 1,8 1,1 88 22
339 1,6 0,5 1,7 0,5 3,3 1,0 88 22
562 3,8 0,7 4,9 0,9 6,8 1,2 88 22
Versión 4.0 N.º de pub. J65397_ES 7 de 13
ALTV INSTRUCCIONES DE USO
Alanina aminotransferasa Características de rendimiento
Unidades convencionales y SI (U/L)
Actividad Repetibilidad* Intradía** Intralab. *** N.º de N.º de
Sistema media DE CV% DE CV% DE CV% observ. días
14 0,1 0,7 0,1 0,7 0,3 2,1 88 22
32 0,2 0,6 0,3 0,9 0,6 1,9 88 22
5600†† 168 0,9 0,5 1,1 0,7 2,3 1,4 88 22
343 1,7 0,5 2,2 0,6 3,6 1,0 88 22
566 3,2 0,6 4,7 0,8 6,4 1,1 88 22
14 0,1 0,7 0,2 1,4 0,2 1,4 88 22
32 0,2 0,6 0,3 0,9 0,4 1,3 88 22
5,1 FS† 166 0,9 0,5 1,3 0,8 1,4 0,8 88 22
341 2,0 0,6 2,5 0,7 3,4 1,0 88 22
565 3,8 0,7 4,6 0,8 5,6 1,0 88 22
* La repetibilidad (anteriormente conocida como precisión intraserie) se determina utilizando dos repeticiones por análisis.
** La precisión intradía se determinó a partir de dos análisis por día con dos repeticiones.
*** La precisión intralaboratorio se determinó utilizando un único lote de slides y efectuando una calibración semanal.
† Las características de rendimiento de VITROS 5,1 FS System son válidas para VITROS 4600 System.
†† Las características de rendimiento de VITROS 5600 System son válidas para los sistemas VITROS XT 3400 y XT 7600 System.
Unidades alternativas (µkat/L)
Actividad Repetibilidad* Intradía** Intralab. *** N.º de N.º de
Sistema media DE CV% DE CV% DE CV% observ. días
0,23 0,002 0,7 0,002 0,7 0,005 2,1 80 20
0,53 0,003 0,6 0,005 0,9 0,010 1,9 80 20
350 2,81 0,020 0,7 0,025 0,9 0,043 1,5 80 20
5,73 0,035 0,6 0,045 0,8 0,078 1,4 80 20
9,55 0,055 0,6 0,080 0,8 0,104 1,1 80 20
0,23 0,002 0,7 0,002 0,7 0,003 1,4 88 22
0,53 0,003 0,6 0,005 0,9 0,007 1,3 88 22
4600 2,77 0,017 0,6 0,027 1,0 0,030 1,1 88 22
5,66 0,027 0,5 0,028 0,5 0,055 1,0 88 22
9,39 0,063 0,7 0,082 0,9 0,114 1,2 88 22
0,23 0,002 0,7 0,002 0,7 0,005 2,1 88 22
0,53 0,003 0,6 0,005 0,9 0,010 1,9 88 22
5600†† 2,81 0,015 0,5 0,018 0,7 0,038 1,4 88 22
5,73 0,028 0,5 0,037 0,6 0,060 1,0 88 22
9,45 0,053 0,6 0,078 0,8 0,107 1,1 88 22
0,23 0,002 0,7 0,003 1,4 0,003 1,4 88 22
0,53 0,003 0,6 0,005 0,9 0,007 1,3 88 22
5,1 FS† 2,77 0,015 0,5 0,022 0,8 0,023 0,8 88 22
5,69 0,033 0,6 0,042 0,7 0,057 1,0 88 22
9,44 0,063 0,7 0,077 0,8 0,094 1,0 88 22
* La repetibilidad (anteriormente conocida como precisión intraserie) se determina utilizando dos repeticiones por análisis.
** La precisión intradía se determinó a partir de dos análisis por día con dos repeticiones.
*** La precisión intralaboratorio se determinó utilizando un único lote de slides y efectuando una calibración semanal.
† Las características de rendimiento de VITROS 5,1 FS System son válidas para VITROS 4600 System.
†† Las características de rendimiento de VITROS 5600 System son válidas para los sistemas VITROS XT 3400 y XT 7600 System.
Especificidad
Sustancias que no interfieren
Las sustancias indicadas en la tabla a continuación se analizaron con slides VITROS ALTV según el protocolo CLSI
EP07 10 y se vio que no interferían, con una desviación de < 8 U/L, a 60 U/L y una desviación de < 24 U/L a 300 U/L, en la
concentración mostrada.
8 de 13 N.º de pub. J65397_ES Versión 4.0
INSTRUCCIONES DE USO ALTV
Bibliografía Alanina aminotransferasa
Compuesto Concentración Compuesto Concentración
Acetaminofeno/
20 mg/dL 1319 μmol/L 50 mg/dL 2424 μmol/L
paracetamol Ibuprofeno
Adefovir dipivoxil 7,4 μg/dL 0,148 μmol/L Intralípidos 800 mg/dL 8 g/L
Alprazolam 0,20 mg/dL 6,48 μmol/L Isoniazida 4 mg/dL 292 μmol/L
Ácido 5-aminosalicílico 0,4 mg/dL 26,1 μmol/L Lamivudina 2,1 mg/dL 91,6 μmol/L
Besilato de amlodipina 14 μg/dL 247 nmol/L Levodopa 0,98 mg/dL 49,7 μmol/L
Amoxicilina 7,53 mg/dL 206 μmol/L Levotiroxina 100,2 μg/dL 1,29 μmol/L
Ácido ascórbico 100 mg/dL 5,7 mmol/L Metotrexato 94,5 mg/dL 2 mmol/L
Aspartato
750 U/L 12,5 μkat/L 12 mg/dL 701μmol/L
aminotransferasa (AST) Metronidazol
Calcio de atorvastatina
72,6 mg/dL 600 µEq/L 54,9 mg/dL 2173 μmol/L
(trihidrato) Naproxeno sódico
Benazepril (HCI) 2,21 mg/dL 48 μmol/L Omeprazol 0,60 mg/dL 17,4 μmol/L
Bilirrubina, conjugada 57,64 mg/dL 684 μmol/L Oxicodona 0,05 mg/dL 1,59 μmol/L
Peginterferón alfa-2b
40 mg/dL 684 μmol/L (como Interferón 0,216 μg/dL 0,112 nmol/L
Bilirrubina, no conjugada alfa-2b)
Boceprevir 0,54 mg/dL 10,4 μmol/L Propranolol (HCl) 0,23 mg/dL 7,78 μmol/L
Calcio dobesilato 2,3 mg/dL 55 μmol/L Pseudoefedrina (HCI) 1,221 mg/dL 60,5 μmol/L
Cefazolina sódica 126,1 mg/dL 2647 μmol/L Ribavirina 1,07 mg/dL 43,8 μmol/L
Cefoxitina sódica 69,5 mg/dL 1547 μmol/L Rifampicina 6,43 mg/dL 78,1 μmol/L
Ceftriaxona disódica Calcio de
87,45 mg/dL 1322 μmol/L 6,2 μg/dL 61,9 nmol/L
hemi(heptahidratada) rosuvastatina
Cefuroxima 60 mg/dL 1414 μmol/L Ácido salicílico 45 mg/dL 3,258 mmol/L
Colesterol 500 mg/dL 13 mmol/L Simeprevir 3,44 mg/dL 45,9 μmol/L
Sofosbuvir (como
0,563 mg/dL 4,68 μmol/L metabolitos 0,42 mg/dL 16,14 μmol/L
Ciclosporina-a GS311007)
Dextrano 40 6 g/dL 60 g/L Espironolactona 0,06 mg/dL 1,44 μmol/L
Difenhidramina (HCI) 0,57 mg/dL 19,5 μmol/L Sulfapiridina 29,9 mg/dL 1200 μmol/L
Dipirona sódica
19 mg/dL 570 μmol/L 30 mg/dL 753 μmol/L
(Metamizol sódico) Sulfasalazina
Dobutamina (HCI) 26,7 μg/dL 0,886 μmol/L Sodio de suramina 30 mg/dL 210 μmol/L
Dopamina (HCI) 111,6 μg/dL 5,89 μmol/L Telaprevir 1,44 mg/dL 21,2 μmol/L
Doxiciclina (HCI) 3,24 mg/dL 67,4 μmol/L Telbivudine 1,48 mg/dL 61,1 μmol/L
Tenofovir disoproxilo
2,30 μg/dL 0,083 μmol/L 0,12 mg/dL 1,89 μmol/L
Entecavir fumarato
Etamsilato 3,14 mg/dL 119,3 μmol/L Teofilina 4 mg/dL 222 μmol/L
Etanol 400 mg/dL 86,8 mmol/L Proteínas totales 12 g/dL 120 g/L
Furosemida 6 mg/dL 181 μmol/L Triglicéridos 800 mg/dL 9,12 mmol/L
Hidrato de sodio de
1,8 mg/dL 102 μmol/L 10,25 mg/dL 69 μmol/L
ácido gentísico Vancomicina (HCI)
Glutatión 91 mg/dL 3 mmol/L Warfarina (sal sódica) 1,072 mg/dL 32,5 μmol/L
Hipaque (diatrizoato de
20,035 mg/dL 315 μmol/L
sodio)
Bibliografía
1. Aminotransferases in Diseases, Robert Rej, Clinics in Laboratory Medicine. Vol 9, No 4, December 1989.
2. Evaluation of abnormal liver-enzyme results in asymptomatic patients, Daniel S. Pratt and Marshall M. Kaplan, N Engl J
Med 2000; 342:1266-1271, April 27, 2000.
3. CLSI. Protection of Laboratory Workers From Occupationally Acquired Infections; Approved Guideline—Fourth Edition.
CLSI document M29-A4. Wayne, PA: Clinical and Laboratory Standards Institute; 2014.
4. Calam RR. Specimen Processing Separator Gels: An Update. J Clin Immunoassay. 11:86–90; 1988.
Versión 4.0 N.º de pub. J65397_ES 9 de 13
ALTV INSTRUCCIONES DE USO
Alanina aminotransferasa Bibliografía
5. CLSI. Collection of Diagnostic Venous Blood Specimens. 7th ed. CLSI standard GP41. Wayne, PA: Clinical and
Laboratory Standards Institute; 2017.
6. CLSI. Procedures and Devices for the Collection of Diagnostic Capillary Blood Specimens; Approved Standard – Sixth
Edition. CLSI document GP42-A6. Wayne, PA: Clinical and Laboratory Standard Institute; 2008.
7. Clinical Laboratory Handbook for Patient Preparation and Specimen Handling. Fascicle VI: Chemistry/Clinical
Microscopy. Northfield, IL: College of American Pathologists; 1992.
8. Schumann et al. IFCC Primary Reference Procedures for the Measurement of Catalytic Activity Concentrations of
Enzymes at 37°C. Part 4. Reference Procedure for the Measurement of Catalytic Concentration of Alanine
Aminotransferase. Clin. Chem. Lab. Med. 40(7):718–724; 2002.
9. CLSI. Statistical Quality Control for Quantitative Measurements Procedures: Principles and Definitions. Fourth Edition.
CLSI guideline C24, Wayne, PA: Clinical and Laboratory Standards Institute; 2016.
10. Interference Testing in Clinical Chemistry; Approved Guideline – Second Edition, CLSI document EP07-A2. Wayne,
PA; Clinical Laboratory Standards Institute, 2005.
11. Young DS. Effects of Drugs on Clinical Laboratory Tests. ed. 4. Washington D.C.: AACC Press; 1995.
12. Friedman RB, Young DS. Effects of Disease on Clinical Laboratory Tests. Washington, D.C.: AACC Press; 1990.
13. Thomas, L., Muller, M., Schumann, G., Klein, G., Lunau, S., Pick, K.-H., & Oswald, S. (2005). Consensus of DGKL and
VDGH for interim reference intervals on enzymes in serum. Journal of Laboratory Medicine, 29(5), 301-308.
14. CLSI.Measurement Procedure Comparison and Bias Estimation Using Patient Samples; Approved Guideline – Third
Edition. CLSI Document EP09 – A3. Wayne, PA: Clinical and Laboratory Standards Institute; 2013
15. CLSI. Evaluation of Precision of Quantitative Measurement Procedures- Third Edition. EP05-A3 Wayne PA, Clinical
Laboratory Standards Institute; 2014.
10 de 13 N.º de pub. J65397_ES Versión 4.0
INSTRUCCIONES DE USO ALTV
Glosario de símbolos Alanina aminotransferasa
Glosario de símbolos
Versión 4.0 N.º de pub. J65397_ES 11 de 13
ALTV INSTRUCCIONES DE USO
Alanina aminotransferasa Historial de revisiones
Historial de revisiones
Fecha de revisión Versión Descripción de cambios técnicos*
2019-09-06 3.0 • Se ha añadido información correspondiente al analizador VITROS XT 3400 de
Bioquímica
• Glosario de símbolos: actualizado
• Se actualizó la dirección del representante en la CE
• Muestras no recomendadas: se ha eliminado el punto relativo a muestras
hemolizadas
• Otras limitaciones:
– Aclaración del indicador DP
– Se ha eliminado el punto relativo a muestras hemolizadas
• Esquema de la reacción: se ha añadido CO2
• Diagrama del slide: se ha añadido fosfato de sodio a la capa reactiva
• Tabla de especificidad: se ha corregido la ortografía de propranolol (HCl)
• Referencias: se ha eliminado la referencia de documentación relativa a
muestras hemolizadas
* Las barras de cambio indican la posición de las modificaciones técnicas efectuadas en el texto con respecto a la versión anterior del
documento.
Al sustituir estas Instrucciones de uso, firme y ponga la fecha en el espacio que hay a continuación y consérvelas según lo
especifiquen los reglamentos locales o las políticas de laboratorio, si procede.
Firma Fecha de caducidad
12 de 13 N.º de pub. J65397_ES Versión 4.0
INSTRUCCIONES DE USO ALTV
Historial de revisiones Alanina aminotransferasa
Ortho-Clinical Diagnostics
1500 Boulevard Sébastien Brant
B.P. 30335
67411 Illkirch
CEDEX, France
Ortho-Clinical Diagnostics, Inc.
100 Indigo Creek Drive
Rochester, NY 14626
USA
VITROS es una marca comercial registrada de Ortho Clinical
Diagnostics.
© Ortho Clinical Diagnostics, 2017–2019
Versión 4.0 N.º de pub. J65397_ES 13 de 13
También podría gustarte
- UF1668 - Análisis de agua potable y residualDe EverandUF1668 - Análisis de agua potable y residualAún no hay calificaciones
- Altv J65397 Es I 4Documento12 páginasAltv J65397 Es I 4laboratorio clinicacedanoAún no hay calificaciones
- Ast MP2-113 Es I 13Documento11 páginasAst MP2-113 Es I 13laboratorio clinicacedanoAún no hay calificaciones
- Alt MP2-36 Es IDocumento11 páginasAlt MP2-36 Es IDaniela TroncosoAún no hay calificaciones
- Alpkp2-17 Es I 10Documento10 páginasAlpkp2-17 Es I 10jtovarunigarroAún no hay calificaciones
- Uric MP2-11 Es I 15Documento13 páginasUric MP2-11 Es I 15Alejandro PerezAún no hay calificaciones
- Inserto - VITROS Chemistry Products URIC SlidesDocumento13 páginasInserto - VITROS Chemistry Products URIC SlidesLapis LázuliAún no hay calificaciones
- BSOSR6X0708Documento8 páginasBSOSR6X0708xuanhungyteAún no hay calificaciones
- Inserto - VITROS Chemistry Products GLUC SlidesDocumento18 páginasInserto - VITROS Chemistry Products GLUC SlidessalvadorAún no hay calificaciones
- Insert ALTL 0020764957322COIN V8 EsDocumento5 páginasInsert ALTL 0020764957322COIN V8 EsLuis Ivan MoralesAún no hay calificaciones
- Trig J40115 Es I 6Documento14 páginasTrig J40115 Es I 6Alejandro PerezAún no hay calificaciones
- Instrucciones de Uso Fe: VITROS Chemistry Products Fe SlidesDocumento10 páginasInstrucciones de Uso Fe: VITROS Chemistry Products Fe SlidesPapeleria Diseño y ArteAún no hay calificaciones
- Glu MP2-8 Es IDocumento16 páginasGlu MP2-8 Es IDaniela TroncosoAún no hay calificaciones
- Colesterol VitrosDocumento11 páginasColesterol VitrosNoelia LopezAún no hay calificaciones
- Insert ALTL 04773284001 V8 EsDocumento4 páginasInsert ALTL 04773284001 V8 EsDAVIDAún no hay calificaciones
- Altl TGPDocumento4 páginasAltl TGPTallulahAún no hay calificaciones
- Incerto Determinacion de PotasioDocumento1 páginaIncerto Determinacion de PotasioJosué Quishpe CoelloAún no hay calificaciones
- Calcio VitrosDocumento13 páginasCalcio VitrosNoelia LopezAún no hay calificaciones
- CRP VitrosDocumento12 páginasCRP VitrosAngel CamacaroAún no hay calificaciones
- Ref 1008 EdicAbril2012 Ref140214 EspDocumento6 páginasRef 1008 EdicAbril2012 Ref140214 Espdaniel muñozAún no hay calificaciones
- Manual TecnicasDocumento34 páginasManual TecnicasDj Melon con vino Carlos BustaAún no hay calificaciones
- Centro de Bachillerato O Tecnológico Industrial Y de Servicios No. 32° Cbtis 32 "Ricardo Flores Magón"Documento5 páginasCentro de Bachillerato O Tecnológico Industrial Y de Servicios No. 32° Cbtis 32 "Ricardo Flores Magón"Broca Santos José HarveyAún no hay calificaciones
- Ast Baosr6x0909Documento9 páginasAst Baosr6x0909AdrianaManouAún no hay calificaciones
- TGO, Labtest, Inter.Documento6 páginasTGO, Labtest, Inter.Jose Carlo Sedamano YAún no hay calificaciones
- Upro J04089 Es I 11Documento12 páginasUpro J04089 Es I 11Alejandro PerezAún no hay calificaciones
- Aspartate Aminotransferase - ADVIA Chemistry - Rev G DXDCM 09017fe9804209ab-1586844889019Documento10 páginasAspartate Aminotransferase - ADVIA Chemistry - Rev G DXDCM 09017fe9804209ab-1586844889019WendyPimentelSalasAún no hay calificaciones
- TGP BiosystemsDocumento2 páginasTGP BiosystemsGustavo Jeanpool Quispe Garrido100% (1)
- 2 - Manual de Practicas Bioqui Clinica 2Documento40 páginas2 - Manual de Practicas Bioqui Clinica 2LUISA BERTHA ADUVIRI CORDOVAAún no hay calificaciones
- Informe Lab N°4Documento15 páginasInforme Lab N°4Mariana ChavezAún no hay calificaciones
- Creatinina VitrosDocumento14 páginasCreatinina VitrosNoelia LopezAún no hay calificaciones
- CKMB MP2-48 Es I 12 1Documento12 páginasCKMB MP2-48 Es I 12 1jtovarunigarroAún no hay calificaciones
- IFU - R920 S ALT 4 PDFDocumento3 páginasIFU - R920 S ALT 4 PDFNoel MamaniAún no hay calificaciones
- Bun Baosr6x4110Documento10 páginasBun Baosr6x4110AdrianaManouAún no hay calificaciones
- Insert oDocumento2 páginasInsert oMerly Del Rocio AndradeAún no hay calificaciones
- Practica Soluciones AmortiguadorasDocumento7 páginasPractica Soluciones AmortiguadorasRosa Angelica Guillen GarcésAún no hay calificaciones
- UPRODocumento12 páginasUPROAngelAún no hay calificaciones
- Consulta ApolipoproteínasDocumento12 páginasConsulta ApolipoproteínasAdrián Cumbal JimenezAún no hay calificaciones
- T-15. Fosfatasa Alcalina. Cinético.Documento1 páginaT-15. Fosfatasa Alcalina. Cinético.Francisco Lozano GómezAún no hay calificaciones
- B27 WebDocumento28 páginasB27 WebBio SearchAún no hay calificaciones
- IFU - R920 S AST 1Documento3 páginasIFU - R920 S AST 1Norma RuedaAún no hay calificaciones
- Asat Tgo Ifcc PDFDocumento2 páginasAsat Tgo Ifcc PDFYUNIORAún no hay calificaciones
- UREA-STAT BAOSR6x41 ESDocumento3 páginasUREA-STAT BAOSR6x41 ESAdrianaManouAún no hay calificaciones
- El Aspartato Aminotransferasa (AST o GOT)Documento2 páginasEl Aspartato Aminotransferasa (AST o GOT)Kira GomezAún no hay calificaciones
- TRFRN J21395 Es I 8 1Documento10 páginasTRFRN J21395 Es I 8 1insabi poliforumAún no hay calificaciones
- Guia Laboratorio Inmovilizacion Alfa-AmilasaDocumento4 páginasGuia Laboratorio Inmovilizacion Alfa-AmilasaFAUSTO GABRIEL YEPEZ CALDERONAún no hay calificaciones
- LDHDocumento2 páginasLDHmnilcoAún no hay calificaciones
- PI S ALT 2Documento3 páginasPI S ALT 2Nathaly GuevaraAún no hay calificaciones
- Insert AMYL2 0003183742122COIN V7 EsDocumento6 páginasInsert AMYL2 0003183742122COIN V7 EsLuis Ivan MoralesAún no hay calificaciones
- T-16 AST. Cinetico. UV PDFDocumento1 páginaT-16 AST. Cinetico. UV PDFFrancisco Lozano GómezAún no hay calificaciones
- Inserto Lactato Deshidrogenasa PDFDocumento1 páginaInserto Lactato Deshidrogenasa PDFCarolinaMendozaAún no hay calificaciones
- GPT Uv Aa Liquida SPDocumento8 páginasGPT Uv Aa Liquida SPYola Prisiliana Pozo HuaychaAún no hay calificaciones
- Práctica BioquímicaDocumento10 páginasPráctica BioquímicaErick Tsuji0% (1)
- Kit 1 Calibrador - 1882206Documento6 páginasKit 1 Calibrador - 1882206LABORATORIO ANGELESAún no hay calificaciones
- Bsis32 Urea-Uv 2013Documento2 páginasBsis32 Urea-Uv 2013Hupal Rafael100% (1)
- Aspartate Aminotransferase (Ast/Got) : Biosystems S.ADocumento1 páginaAspartate Aminotransferase (Ast/Got) : Biosystems S.AEunii Cuevas100% (1)
- Urea 37Documento1 páginaUrea 37DanielLociaAún no hay calificaciones
- Alanine Aminotransferase - ADVIA Chemistry - Rev J DXDCM 09017fe98042084e-1586844088677Documento12 páginasAlanine Aminotransferase - ADVIA Chemistry - Rev J DXDCM 09017fe98042084e-1586844088677WendyPimentelSalasAún no hay calificaciones
- T-18. Deshidrogenasa Láctica. LDH. Cinetico. UV PDFDocumento1 páginaT-18. Deshidrogenasa Láctica. LDH. Cinetico. UV PDFFrancisco Lozano Gómez100% (1)
- Arthrobacter Protophormiae) 83.4 Kat/l (25 °C) PeroxidasaDocumento6 páginasArthrobacter Protophormiae) 83.4 Kat/l (25 °C) Peroxidasacalidadsedecorpas lab vejaranoAún no hay calificaciones
- Kit 3 Calibrador - 1290709Documento6 páginasKit 3 Calibrador - 1290709LABORATORIO ANGELESAún no hay calificaciones
- POSTERDocumento1 páginaPOSTERPapeleria Diseño y ArteAún no hay calificaciones
- GimnasiaDocumento1 páginaGimnasiaPapeleria Diseño y ArteAún no hay calificaciones
- Ruta Navideña Sonia Medina PDFDocumento1 páginaRuta Navideña Sonia Medina PDFPapeleria Diseño y ArteAún no hay calificaciones
- Poster 2Documento1 páginaPoster 2Papeleria Diseño y ArteAún no hay calificaciones
- Indicadores de GestionDocumento9 páginasIndicadores de GestionWilton PeñaAún no hay calificaciones
- Cartilla Aspectos AmbientalesDocumento10 páginasCartilla Aspectos Ambientalesmarcela reina osorioAún no hay calificaciones
- FC J12329 Es PDFDocumento4 páginasFC J12329 Es PDFOmar LoezaAún no hay calificaciones
- Alt MP2-36 Es I 11Documento10 páginasAlt MP2-36 Es I 11Papeleria Diseño y ArteAún no hay calificaciones
- Matriz Aspectos Ambientales cll100Documento2 páginasMatriz Aspectos Ambientales cll100Papeleria Diseño y ArteAún no hay calificaciones
- Alt MP2-36 Es I 11Documento10 páginasAlt MP2-36 Es I 11Papeleria Diseño y ArteAún no hay calificaciones
- Phyt MP2-120 Es I 12Documento11 páginasPhyt MP2-120 Es I 12Papeleria Diseño y ArteAún no hay calificaciones
- Instrucciones de Uso Fe: VITROS Chemistry Products Fe SlidesDocumento10 páginasInstrucciones de Uso Fe: VITROS Chemistry Products Fe SlidesPapeleria Diseño y ArteAún no hay calificaciones
- Altv J65397 Es I 3Documento13 páginasAltv J65397 Es I 3Papeleria Diseño y ArteAún no hay calificaciones
- Altv J65397 Es I 3Documento13 páginasAltv J65397 Es I 3Papeleria Diseño y ArteAún no hay calificaciones
- FC J12329 Es PDFDocumento4 páginasFC J12329 Es PDFOmar LoezaAún no hay calificaciones
- Phyt MP2-120 Es I 12Documento11 páginasPhyt MP2-120 Es I 12Papeleria Diseño y ArteAún no hay calificaciones
- Instrucciones de Uso Fe: VITROS Chemistry Products Fe SlidesDocumento10 páginasInstrucciones de Uso Fe: VITROS Chemistry Products Fe SlidesPapeleria Diseño y ArteAún no hay calificaciones
- Da Proceso 20-13-10804389 225489011 74725848Documento5 páginasDa Proceso 20-13-10804389 225489011 74725848Papeleria Diseño y ArteAún no hay calificaciones
- Implementar Iso 9001 CuadernoDocumento9 páginasImplementar Iso 9001 CuadernoPapeleria Diseño y ArteAún no hay calificaciones
- Instrucciones de Uso Fe: VITROS Chemistry Products Fe SlidesDocumento10 páginasInstrucciones de Uso Fe: VITROS Chemistry Products Fe SlidesPapeleria Diseño y ArteAún no hay calificaciones
- FC J12329 Es PDFDocumento4 páginasFC J12329 Es PDFOmar LoezaAún no hay calificaciones
- Ebook Gratuito Documentos y Registros para ISO 9001 1581607131 PDFDocumento20 páginasEbook Gratuito Documentos y Registros para ISO 9001 1581607131 PDFBilbainaAún no hay calificaciones
- Alt MP2-36 Es I 11Documento10 páginasAlt MP2-36 Es I 11Papeleria Diseño y ArteAún no hay calificaciones
- Propuesta EconomicaDocumento3 páginasPropuesta EconomicaPapeleria Diseño y ArteAún no hay calificaciones
- Comparación de Nivel de Cumplimiento de Normas de Bioseguridad Del Personal DelDocumento81 páginasComparación de Nivel de Cumplimiento de Normas de Bioseguridad Del Personal DelPapeleria Diseño y Arte100% (2)
- Phyt MP2-120 Es I 12Documento11 páginasPhyt MP2-120 Es I 12Papeleria Diseño y ArteAún no hay calificaciones
- Propuesta EconomicaDocumento3 páginasPropuesta EconomicaPapeleria Diseño y ArteAún no hay calificaciones
- Informe Corregido de Puerperio JJDocumento42 páginasInforme Corregido de Puerperio JJConsuelo Zavaleta100% (2)
- Línea de TiempoDocumento2 páginasLínea de TiempoNatalia SáenzAún no hay calificaciones
- Modelo Rúbrica Abp Ecoe Medicina IDocumento4 páginasModelo Rúbrica Abp Ecoe Medicina IChristian AndresAún no hay calificaciones
- La Santería en Cuba y El Proceso Salud-Enfermedad Autor Teresa L. González ValdésDocumento12 páginasLa Santería en Cuba y El Proceso Salud-Enfermedad Autor Teresa L. González ValdésNestor P.RAún no hay calificaciones
- Laboratorio #3Documento11 páginasLaboratorio #3Camila Condori100% (1)
- INVENTARIOSDocumento16 páginasINVENTARIOSriopsicologoAún no hay calificaciones
- Morillo Linet Rehabilitacion de Los Trastornos CognitivosDocumento2 páginasMorillo Linet Rehabilitacion de Los Trastornos Cognitivoslinet morilloAún no hay calificaciones
- Fármacos Derivados de Pirazina y QuinoxalinaDocumento23 páginasFármacos Derivados de Pirazina y QuinoxalinaDAVID EMMANUEL PEREZ CRUZ100% (1)
- Ensayo de LenguajeDocumento7 páginasEnsayo de LenguajeALLPAJA ABANTO DAIANA MARJORIE FILOMENAAún no hay calificaciones
- Actividad 2 Fase 1 InformeDocumento11 páginasActividad 2 Fase 1 Informevalentina ramosAún no hay calificaciones
- Trombosis Venosa ProfundaDocumento6 páginasTrombosis Venosa ProfundaSofia Giraldo AraujoAún no hay calificaciones
- Manejo Del Carro Rojo 2023Documento34 páginasManejo Del Carro Rojo 2023Supervision Enfermeria100% (1)
- Mapa Conceptual Generalidades Semiológicas Sofia MontesDocumento3 páginasMapa Conceptual Generalidades Semiológicas Sofia MontesANDREA VALENTINA RAMIREZ GARCIAAún no hay calificaciones
- 05.02 Eu SpaDocumento10 páginas05.02 Eu SpaJuan CarlosAún no hay calificaciones
- Productos y Servicios GeoaseoDocumento8 páginasProductos y Servicios GeoaseoLuis Enrique Uribe RomeroAún no hay calificaciones
- Estructura Del HospitalDocumento20 páginasEstructura Del HospitalJulia Ceron CarranzaAún no hay calificaciones
- Canva - Infografía - Herbolaria y Medicina TradicionalDocumento1 páginaCanva - Infografía - Herbolaria y Medicina TradicionalMonserrat GonzalezAún no hay calificaciones
- Entrevista Con Doctor WeissDocumento5 páginasEntrevista Con Doctor WeissjoyasorientalesAún no hay calificaciones
- Procedimiento Seleccion Compra Entrega Reposicion y Mantencion Del EpaDocumento14 páginasProcedimiento Seleccion Compra Entrega Reposicion y Mantencion Del EpaGabriela Steffany Carrasco FernándezAún no hay calificaciones
- Estudio (Tesis) de San Pedro de Los BañosDocumento245 páginasEstudio (Tesis) de San Pedro de Los Bañosjr2t2 jr2t2Aún no hay calificaciones
- Taller TextualDocumento5 páginasTaller TextualshandiraAún no hay calificaciones
- Objetivos y Metas Del Programa de Seguridad - Bbti SacDocumento3 páginasObjetivos y Metas Del Programa de Seguridad - Bbti SacGuille LRAún no hay calificaciones
- Actividad 1 - Proyecto de Inversión (Entrega 1) V01Documento13 páginasActividad 1 - Proyecto de Inversión (Entrega 1) V01Dayana TimanaAún no hay calificaciones
- Curriculum-Vitae Teo Matamoros2021Documento21 páginasCurriculum-Vitae Teo Matamoros2021Jeyner Martel BravoAún no hay calificaciones
- FT Espirulina TabletDocumento1 páginaFT Espirulina TabletmatiasAún no hay calificaciones
- Incidente CuadroDocumento2 páginasIncidente CuadroMAYERLYAún no hay calificaciones
- 9 8 PBDocumento59 páginas9 8 PBAdriana KummAún no hay calificaciones
- Características Del Nervio CiáticoDocumento12 páginasCaracterísticas Del Nervio CiáticoLuz Liz CLAún no hay calificaciones
- Apuntes Psicoterapia CognitivaDocumento77 páginasApuntes Psicoterapia CognitivaTanyaAndreaVidelaAspe100% (1)
- HIPERPARATIROIDISMODocumento6 páginasHIPERPARATIROIDISMOPaul WalkerAún no hay calificaciones