Documentos de Académico
Documentos de Profesional
Documentos de Cultura
LOpU1 Pre1 GascónCastilloAsafJoshua
Cargado por
Asaf Joshua Gascón Castillo0 calificaciones0% encontró este documento útil (0 votos)
2 vistas4 páginasTítulo original
LOpU1_Pre1_GascónCastilloAsafJoshua
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
2 vistas4 páginasLOpU1 Pre1 GascónCastilloAsafJoshua
Cargado por
Asaf Joshua Gascón CastilloCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 4
#1
DESTILACIÓN DIFERENCIAL
Gascón Castillo Asaf Joshua
Miércoles 11-13 OpUn1 1241-03
Objetivos
1. Relacionar al estudiante con la destilación diferencial, la cual es un caso típico en la
operación de un sistema intermitente o por lotes.
2. Reafirmar los conceptos básicos de equilibrio entre fases vapor-líquido, así como las
leyes que lo rigen para comprender mejor los fundamentos de la destilación.
Guía de estudios
1. ¿A qué se le llama destilación?
A un tipo de operación unitaria utilizada para separar los componentes de una solución líquida
que depende de la distribución de estos componentes entre una fase vapor y una líquida. Su
requerimiento básico es que la composición del vapor sea diferente de la composición del
líquido con el cual está en equilibrio al punto de ebullición.
2. ¿Qué factores influyen en la destilación?
La diferencia en puntos de saturación de las especies a separar, de la presión, la temperatura,
de la composición de alimentación, del equilibrio que hay entre la fase líquida y la de vapor, de
la miscibilidad entre los componentes, de la idealidad de la solución y de la homogeneidad de
la fase líquida.
3. ¿Cuántos tipos de destilación hay?
- La destilación sin retorno/reflujo o mejor conocida como la destilación flash (una etapa)
- La destilación con retorno/reflujo o conocida como destilación fraccionada.
4. ¿En qué consiste la destilación simple y de cuántas maneras se puede llevar a cabo?
Consiste en la alimentación de una mezcla líquida homogénea la cuál mediante por cambios
en la presión o temperatura es llevada a un punto en el cual se hallan en equilibrio la fase
líquida y la fase vapor, dicha fase vapor estará enriquecida del componente más volátil. El
vapor formado se pasa a un condensador y se obtiene un destilado rico en el componente
volátil y residuos ricos en el componente menos volátil. Se puede llevar a cabo por lotes.
5. Enunciar y explicar la regla de las fases.
Regla de las fases de Gibbs (define el número de grados de libertad en un sistema cerrado en
equilibrio)
F= 2-π+N
F -> grados de libertad
Π -> número de fases
N -> número de especies químicas
Las variables de la regla de las fases son propiedades intensivas de forma que proporcionan
en la mims información tanto para sistemas grandes como para pequeños. Únicamente las
composiciones de las fases individuales son variables de la regla de las fases así como las
composiciones globales no son variables de la regla de las fases cuándo esta presenta más de
una fase.
6. Enunciar y explicar las leyes de Raoult y Henry.
Ley de Raoult
La relación entre la presión de vapor de cada componente en una solución ideal es
dependiente de la presión de vapor de cada componente individual y de la fracción molar de
cada componente en la solución. Se aplica para temperaturas subcríticas, se ajusta
correctamente a mezclas de especies químicas semejantes y aplica cuando la fracción es
cercana a la unidad.
𝜸𝒊 ∗ 𝑷 = 𝒙𝒊 ∗ 𝑷𝒊𝒔𝒂𝒕
Ley de Henry
Es la relación que describe el efecto de la presión sobre la solubilidad de los gases. Esta ley
establece que la solubilidad de un gas en contacto con la superficie de un líquido a una
temperatura determinada es directamente proporcional a la presión parcial de dicho gas sobre
el líquido.
𝜸𝒊 ∗ 𝑷 = 𝑿𝒊 ∗ 𝑯𝒊
Hi es la constante específica para el gas, el solvente y la temperatura. Se utiliza cuando uno de
los componentes está por encima del punto crítico
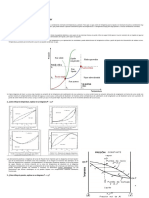
7. ¿Cómo se calculan los datos para construir un diagrama de punto de ebullición y una
curva de equilibrio?
Conociendo la presión total del sistema y las presiones de vapor de los componentes (se utiliza
en la ecuación de Antoine) es posible hacer uso de las siguientes ecuaciones:
ln(𝑃°) = 𝐴 − 𝐵/(𝑇 + 𝐶)
𝑃𝑇 − 𝑃𝐵
𝑋𝐴 =
𝑃𝐴 − 𝑃𝐵
𝑃𝐴 𝑃𝐴 𝑋𝐴
𝑌𝐴 = =
𝑃𝑇 𝑃𝑇
Graficando Ya vs Xa se obtendrá una curva de equilibrio y será T vs Composición, el cuál será
un diagrama de punto de ebullición.
8. ¿Por qué hay desviaciones de la idealidad y cuándo se llama desviación positiva y
cuándo negativa?
Porque las soluciones ya sean en fase líquida o gaseosa no forman una solución ideal, lo que
genera es un azeótropo.
La desviación positiva: es cuando el azeótropo formado tiene un punto mínimo de temperatura
y la desviación negativa cuando forma un punto máximo en la temperatura o un punto mínimo
de presión.
9. ¿Qué es una mezcla azeotrópica?
Es cuando la composición de un componente es la fase líquida tiene la misma composición en
la fase vapor.
10. ¿A qué le llama volatilidad relativa?
Es la medida numérica de la posibilidad de separación por destilación de los componentes de
la mezcla binaria.
11. Deducir la ecuación de Rayleigh.
Partiendo de un balance de materia en dónde dL es la cantidad de vapor que se forma en un
tiempo muy pequeño y x-dx es la concentración del líquido residual que sería L-dL.
𝐿𝑥 = (𝐿 − 𝐷𝐼) ∗ (𝑋 − 𝑑𝑥) + 𝑌𝑑
𝐿𝑋 = 𝐿𝑋 − 𝐿𝑑𝑋 − 𝑋𝑑𝐿 + 𝑑𝐿𝑑𝑋 + 𝑌d
Despreciando 𝑋𝐷 ∗ 𝐷𝐼
Despejando 𝑋𝑑L
𝑋𝑑𝐿 = 𝑌𝑑𝐿 − 𝐿𝑑𝑋
𝐿𝑑 = 𝑌𝑑𝐿 − 𝐿𝑑𝑋
𝐿𝑑𝑋 = (𝑌 − 𝑋)𝑑𝐿
Agrupando e integrando
𝑋𝑙𝑜
𝐿𝑜 𝑑𝑋
ln = ∫
𝐿 𝑋𝐿 (𝑌 − 𝑋)
12. ¿Cómo se obtiene teóricamente la composición promedio del destilado?
Si la presión del sistema es constante se utilizaría un diagrama de Temperatura vs
Composición.
13. ¿Cómo se podría conocer experimentalmente la composición del destilado y del
residuo?
En esta práctica se podrá conocer la composición del destilado y de los residuos pesándolos
en su fase líquida.
También podría gustarte
- Pre1 OperacionesDocumento6 páginasPre1 OperacionesIngeniera Pau JerezAún no hay calificaciones
- Guia de Estudios 1Documento7 páginasGuia de Estudios 1Alfredo AlfaroAún no hay calificaciones
- Pre1.TM Miguel Eduardo FloresDocumento5 páginasPre1.TM Miguel Eduardo FloresMiguel FloresAún no hay calificaciones
- PreLab Transferencia de MasaDocumento5 páginasPreLab Transferencia de MasaCristo Xavier Muñoz Mtz.Aún no hay calificaciones
- Op1 Pre1Documento5 páginasOp1 Pre1FernandoAún no hay calificaciones
- Pre1.OUl Alviso - Camacho.AlejandroDocumento4 páginasPre1.OUl Alviso - Camacho.AlejandroMiguel FloresAún no hay calificaciones
- Diferencia Entre Gas y VaporDocumento8 páginasDiferencia Entre Gas y VaporJosé TorrezAún no hay calificaciones
- Unidad I DestilaciónDocumento32 páginasUnidad I DestilaciónKAREN ESTEFANíA HERNáNDEZ OCAMPOAún no hay calificaciones
- Practica 4 Lab Int 2Documento14 páginasPractica 4 Lab Int 2YulissaAún no hay calificaciones
- Marco Teorico TxyDocumento4 páginasMarco Teorico TxyCraven HorrorsAún no hay calificaciones
- Practica 1 Lab Opiii (Equilibrio Líquido-Vapor y Diagramas de Equilibrio)Documento18 páginasPractica 1 Lab Opiii (Equilibrio Líquido-Vapor y Diagramas de Equilibrio)vidaurre_89Aún no hay calificaciones
- Equilibrio Liquido-VaporDocumento10 páginasEquilibrio Liquido-VaporMiguelAún no hay calificaciones
- Tema 3 DestilacionDocumento17 páginasTema 3 DestilacionCuan TAún no hay calificaciones
- Equilibrio Líquido Vapor en Un Sistema No IdealDocumento3 páginasEquilibrio Líquido Vapor en Un Sistema No IdealDeyaniraAún no hay calificaciones
- p4. Lab Termo 1Documento15 páginasp4. Lab Termo 1Castillo Pérez PaulinaAún no hay calificaciones
- 03 DestilacionDocumento14 páginas03 DestilacionLuis MolloAún no hay calificaciones
- Termo Practica 4Documento24 páginasTermo Practica 4Odin Noe DoroteoAún no hay calificaciones
- Pre1 Ou1 MuñizreynaDocumento8 páginasPre1 Ou1 MuñizreynaAngel ReynaAún no hay calificaciones
- Regla de FasesDocumento7 páginasRegla de Fasesrompecaminos02Aún no hay calificaciones
- Unidad 3 Problemario EquipoDocumento20 páginasUnidad 3 Problemario EquipoFTopnite 08Aún no hay calificaciones
- Copia de Práctica 3 y 4 - EH 2015Documento26 páginasCopia de Práctica 3 y 4 - EH 2015angelriosvazquez08Aún no hay calificaciones
- Destilacion BinariaDocumento23 páginasDestilacion BinariaJacson Rios OjanamaAún no hay calificaciones
- Termodinámica de procesos IIDocumento24 páginasTermodinámica de procesos IIPaul Ruiz BaldeonAún no hay calificaciones
- Pre Examen TermodinamicaDocumento4 páginasPre Examen TermodinamicaJean Pierre Cirilo SosaAún no hay calificaciones
- Lab Op3 Parte 1Documento16 páginasLab Op3 Parte 1Jorge EliasAún no hay calificaciones
- Resumen - Procesos de Separación Vapor LíquidoDocumento11 páginasResumen - Procesos de Separación Vapor LíquidoNICOLAS CASTELLANOS TAMAYOAún no hay calificaciones
- DestilaciónDocumento14 páginasDestilaciónJuan Marcos JaraAún no hay calificaciones
- 2PM32 Practica 5 E5 RecuperacionDocumento32 páginas2PM32 Practica 5 E5 RecuperacionDaniel Quevedo GonzálezAún no hay calificaciones
- Destilacion de Destintos PlatosDocumento4 páginasDestilacion de Destintos PlatosadrianaAún no hay calificaciones
- Elv Etanol AguaDocumento18 páginasElv Etanol AguaJuan Montalvo CerronAún no hay calificaciones
- Práctica 4. LTEL-Equilibrio-liquido Vapor de Una Mezcla BinariaDocumento37 páginasPráctica 4. LTEL-Equilibrio-liquido Vapor de Una Mezcla BinariaGODLOVEAún no hay calificaciones
- MC CABE THIELE Y DESTILACIÓN BINARIADocumento29 páginasMC CABE THIELE Y DESTILACIÓN BINARIAJOSE SILLOCA100% (1)
- Informe T BurbujaDocumento14 páginasInforme T BurbujaRicardo Felipe Cortes CruzAún no hay calificaciones
- Practica 4Documento22 páginasPractica 4adrielAún no hay calificaciones
- Volatilidad RelativaDocumento6 páginasVolatilidad RelativaAna Milena Castañeda Villamarin100% (1)
- Hoja de Ejercicios No 8 UNI 2014 I Sistemas Multifasicos Parte II PDFDocumento7 páginasHoja de Ejercicios No 8 UNI 2014 I Sistemas Multifasicos Parte II PDFfranz_esc20Aún no hay calificaciones
- Informe de Termodinámica Liquido VaporDocumento13 páginasInforme de Termodinámica Liquido VaporStiven K. Rosales CasasAún no hay calificaciones
- Informe Punto BurbujaDocumento9 páginasInforme Punto Burbujalau2631Aún no hay calificaciones
- Construcción del diagrama temperatura-composición para el sistema azeotrópico etanol-aguaDocumento10 páginasConstrucción del diagrama temperatura-composición para el sistema azeotrópico etanol-aguaJuan Sosa San GermanAún no hay calificaciones
- Punto de burbuja propanol-aguaDocumento7 páginasPunto de burbuja propanol-aguaMagaly PinzónAún no hay calificaciones
- Pre Informe 13Documento5 páginasPre Informe 13Laura Vanessa Ramirez ArbelaezAún no hay calificaciones
- Trabajo de Columna de Destilacion 1Documento29 páginasTrabajo de Columna de Destilacion 1Anonymous wP6wa0ZmAún no hay calificaciones
- p5 Reposicion ReDocumento41 páginasp5 Reposicion ReAreli AltamiranoAún no hay calificaciones
- Equilibrio de Fase Líquido - VaporDocumento28 páginasEquilibrio de Fase Líquido - VaporIvan TorresAún no hay calificaciones
- Equilibrio Líquido-Vapor en Sistemas Liquidos BinariosDocumento7 páginasEquilibrio Líquido-Vapor en Sistemas Liquidos BinarioslupitaAún no hay calificaciones
- MARCO TEORICO, Regla de FasesDocumento8 páginasMARCO TEORICO, Regla de FasesAlejandro OrtizAún no hay calificaciones
- EQUILIBRIO DE MEZCLAS MULTICOMPONENTE Y SIMULACIÓNDocumento28 páginasEQUILIBRIO DE MEZCLAS MULTICOMPONENTE Y SIMULACIÓNDylan Gonzales MuñozAún no hay calificaciones
- Informe N°9 - Equilibrio Líquido - VaporDocumento13 páginasInforme N°9 - Equilibrio Líquido - VaporDevra GomezAún no hay calificaciones
- Informe N°13 DestilacionDocumento32 páginasInforme N°13 DestilacionRosa Mariia Quezada ArteagaAún no hay calificaciones
- Unidad 5 FisicoquimicaDocumento25 páginasUnidad 5 FisicoquimicaLuis LiraAún no hay calificaciones
- Preguntas para La Unidad 5 Rault A PropDocumento6 páginasPreguntas para La Unidad 5 Rault A PropEzequiel RiverosAún no hay calificaciones
- Ley de Raoult ModificadaDocumento8 páginasLey de Raoult ModificadaMilagrosCabanillasInfantesAún no hay calificaciones
- Diagramas de equilibrio y destilaciónDocumento9 páginasDiagramas de equilibrio y destilaciónCes CrAún no hay calificaciones
- Diagrama de Fases UmssDocumento7 páginasDiagrama de Fases UmssHelio Tank EbansAún no hay calificaciones
- Practica 5Documento8 páginasPractica 5Alejandra MezaAún no hay calificaciones
- Termodinamica II.Documento14 páginasTermodinamica II.María AlejandraAún no hay calificaciones
- Ingeneria Quimica ComputacionalDocumento18 páginasIngeneria Quimica ComputacionalMirellea AndurayAún no hay calificaciones
- Psicometría. Principios básicos y protocolos experimentales diversosDe EverandPsicometría. Principios básicos y protocolos experimentales diversosAún no hay calificaciones
- Modelamiento y casos especiales de la cinética química heterogéneaDe EverandModelamiento y casos especiales de la cinética química heterogéneaCalificación: 3 de 5 estrellas3/5 (1)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Tema 9 - Enzimas. Estructura y FunciónDocumento6 páginasTema 9 - Enzimas. Estructura y FunciónLara MaríaAún no hay calificaciones
- D-HSEQ-S-005 Estándar de Seguridad Elementos de Protección PersonalDocumento11 páginasD-HSEQ-S-005 Estándar de Seguridad Elementos de Protección PersonaljuanAún no hay calificaciones
- SILABARIODocumento36 páginasSILABARIOMarbelyAnyelineParraSosaAún no hay calificaciones
- Capitulo Ii Higiene en La Industria de LecheDocumento27 páginasCapitulo Ii Higiene en La Industria de LecheDiana VentAún no hay calificaciones
- Ficha de SeguridadDocumento1 páginaFicha de SeguridadstefannyAún no hay calificaciones
- Componente Práctico Virtual - Angela - RamírezDocumento34 páginasComponente Práctico Virtual - Angela - Ramírezangela ramirezAún no hay calificaciones
- Alcohol etílico 70% ficha técnicaDocumento1 páginaAlcohol etílico 70% ficha técnicaYulian12 CardonaAún no hay calificaciones
- Separación de Fosfolípidos Por Cromatografía en Capa Fina y Determinación de Colesterol en La Yema de Huevo Colesterol en La Yema de HuevoDocumento2 páginasSeparación de Fosfolípidos Por Cromatografía en Capa Fina y Determinación de Colesterol en La Yema de Huevo Colesterol en La Yema de HuevoLuis RojasAún no hay calificaciones
- LactosaDocumento3 páginasLactosaBrenda MichelAún no hay calificaciones
- Calcinación de La Cal en Nuestra ZonaDocumento5 páginasCalcinación de La Cal en Nuestra ZonasaulAún no hay calificaciones
- FITORREMEDIACIONDocumento11 páginasFITORREMEDIACIONGris GarcíaAún no hay calificaciones
- Farmacos Presentacion Tabletas, Comprimidos y GrageasDocumento30 páginasFarmacos Presentacion Tabletas, Comprimidos y GrageasYOSELIN MARTINEZ SANCHEZ100% (1)
- Docsity Cinetica Quimica UamDocumento3 páginasDocsity Cinetica Quimica UamTheJerexD JAún no hay calificaciones
- Cinética QuímicaDocumento35 páginasCinética QuímicaAlejandro QuilcaAún no hay calificaciones
- Semana Del 7 Al 11 de Febrero Del 2022Documento6 páginasSemana Del 7 Al 11 de Febrero Del 2022AINNAYDA ARCE100% (1)
- SEG-NOR-007 Colores de Seguridad ABDocumento7 páginasSEG-NOR-007 Colores de Seguridad ABFRANKLIN TENECELAAún no hay calificaciones
- Cristalización Tipos y FallasDocumento2 páginasCristalización Tipos y FallasEric SuarezAún no hay calificaciones
- Criterios de evaluación y contenidos de Biología 2do añoDocumento103 páginasCriterios de evaluación y contenidos de Biología 2do añoErika MartinezAún no hay calificaciones
- Eva Bio PaletaDocumento4 páginasEva Bio PaletaDiego ParadaAún no hay calificaciones
- Podología farmacologíaDocumento4 páginasPodología farmacologíamariapilarAún no hay calificaciones
- Articulo de Calamar Gigante (Pota) Taller3Documento14 páginasArticulo de Calamar Gigante (Pota) Taller3Adix Adelia BernillaAún no hay calificaciones
- Radiaciones Apuntes Parte 1Documento49 páginasRadiaciones Apuntes Parte 1rauldiazsjAún no hay calificaciones
- Introducción A La Operación Del Sistema de Bombeo de Crudo Estabilizad1 44 PREGUNTASDocumento4 páginasIntroducción A La Operación Del Sistema de Bombeo de Crudo Estabilizad1 44 PREGUNTASJoahan Anderson Estela NuñezAún no hay calificaciones
- HIDROMETALURGIADocumento19 páginasHIDROMETALURGIAelizardo macias condoriAún no hay calificaciones
- Tabla Insumos Con Referencia 1Documento6 páginasTabla Insumos Con Referencia 1Gloria Resp. CalidadAún no hay calificaciones
- Difracción de Rayos XDocumento5 páginasDifracción de Rayos XMiguelina MarcaniAún no hay calificaciones
- Javier Ponce Formación Técnica - Valores Óptimos CombustiónDocumento6 páginasJavier Ponce Formación Técnica - Valores Óptimos CombustiónJunior Juanazo BravoAún no hay calificaciones
- Quimica TallerDocumento3 páginasQuimica TallerJose NarvaezAún no hay calificaciones
- Química 10°: Quiz sobre sales, distribución electrónica, gases efecto invernadero y disolventesDocumento2 páginasQuímica 10°: Quiz sobre sales, distribución electrónica, gases efecto invernadero y disolventesSanti LionAún no hay calificaciones
- Fase 4 Analisis de La Transferencia de Masa Equilibrio de Fases IIDocumento28 páginasFase 4 Analisis de La Transferencia de Masa Equilibrio de Fases IIjhon buriticaAún no hay calificaciones