Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cáncer de Tiroides
Cargado por
Ana Itzel Carlon Chavez0 calificaciones0% encontró este documento útil (0 votos)
7 vistas7 páginasCáncer de tiroides
Título original
Cáncer de tiroides
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCáncer de tiroides
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
7 vistas7 páginasCáncer de Tiroides
Cargado por
Ana Itzel Carlon ChavezCáncer de tiroides
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 7
CÁNCER DIFERENCIADO DE TIROIDES
El cáncer de tiroides es el tumor endocrino más frecuente (90%)
Y representa 1% de todas las neoplasias malignas.
Se encuentra entre los 10 primeros cánceres que afectan al sexo femenino y contribuye con
menos de 1% del total de muertes por neoplasias malignas.
● En EUA, la incidencia es de 7.1 a 8.8 casos por cada 100 000 habitantes.
● En México existe poca información sobre la epidemiología del cáncer tiroideo.
El Registro Histopatológico de Neoplasias Malignas (RHNM) reportó en 2001 y 2002 una
prevalencia de 1.9 casos por cada 100.000 habitantes.
Su incidencia parece aumentar un 4% cada año.
Clasificación
1. Diferenciado.
a) Papilar.
b) Folicular.
2. Medular.
3. Indiferenciado.
4. Misceláneo.
CÁNCER DIFERENCIADO
El cáncer diferenciado de tiroides proviene de las células epiteliales foliculares y es el
subtipo más frecuente, de 85 a 90% de los casos; de estos, 85% corresponden a cáncer
papilar, 5% a cáncer folicular.
El cáncer diferenciado comprende varias entidades que suelen tener un comportamiento
indolente, pero podría manifestarse como una neoplasia letal.
Su incidencia incrementa y la mortalidad decrece gracias al aumento del uso del ultrasonido
(US) para diagnosticar tumores pequeños, con mejor pronóstico y probablemente
sobretratados.
La relación mujer:hombre es de 4.4:1, pero en la experiencia de los autores el 85.6% de los
casos ocurrió en mujeres, con una relación 5.9:1.
La máxima frecuencia tiene lugar entre los 41 y los 50 años, y el 60% de los casos
acontecen entre los 31 y los 60 años.
Como dije la mayoría de los pacientes tienen buen pronóstico, la sobrevida a 10 años del
cáncer papilar es de 98% y del folicular de 92%.
Los principales factores etiológicos son exposición a
● radiación ionizante: La exposición accidental o terapéutica a dosis bajas de radiación
ionizante es el factor de riesgo mejor conocido para el cáncer diferenciado, aunque
solo el 1.8-10% de los expuestos lo desarrollan.
● expresión de diversas mutaciones puntuales o rearreglos en receptores tirosina
cinasa y cinasas serina-treonina:
○ El cáncer es producto de un desequilibrio entre los factores de crecimiento,
los receptores de superficie celular, las vías de señalización intracelular y los
factores de transcripción que desencadenan una proliferación desordenada,
la destrucción de tejidos adyacentes y la diseminación a distancia. El gen
RET normalmente codifica para un receptor transmembrana con actividad
tirocino-cinasa que está inactivo en la vida adulta, mientras que activado
induce vías de señalización intracelular con potencial carcinogénico.
○ En el cáncer diferencial de tiroides destacan las translocaciones e
inversiones del gen RET con genes heterólogos que originan un gen
quimérico llamado RET/PTC activado; esto ocurre en el 3-60% de los casos
de tipo papilar y destacan los pacientes jóvenes y los expuestos a
radiaciones.
● deleciones en supresores tumorales
Manifestaciones clínicas y diagnóstico
Por lo general, el cáncer diferenciado de tiroides se manifiesta como un nódulo tiroideo,
aunque también, en forma menos frecuente; como enfermedad metastásica ganglionar o a
distancia.
En el pasado, la mayoría de los pacientes se presentaban con una masa tiroidea
descubierta de forma incidental por él mismo o el médico en la exploración física.
Sin embargo, cada vez es más frecuente encontrar un nódulo tiroideo en un estudio de
imagen de cuello, indicado por un motivo diferente a una enfermedad tiroidea y que
finalmente se diagnostica como cáncer de tiroides. Por lo anterior, es común que los
pacientes estén asintomáticos y eutiroideos.
El cáncer diferenciado de tiroides involucra ganglios linfáticos regionales en el momento del
diagnóstico entre 20 y 50% de los pacientes.
UltrasonidoEl ultrasonido preoperatorio detecta linfadenopatía sospechosa en 20 a 31% de
los casos; no obstante, identifica sólo la mitad de las adenopatías encontradas en la cirugía
debido a que la imagen tiroidea se superpone a los ganglios del compartimento VI, que son
los más afectados en cáncer papilar de tiroides.
Las características ultrasonográficas más relacionadas con metástasis en ganglios linfáticos
son: tamaño mayor a 7.5 mm (en niveles II al VI), contenido quístico y microcalcificaciones
intraganglionares, forma redonda, relación < 2 entre el eje longitudinal y el transversal,
compresión de estructuras vasculares y aumento de la vascularidad periférica identificada
con Doppler.
Histopatología
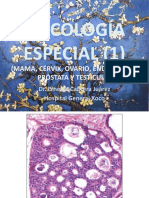
El carcinoma papilar convencional se caracteriza por presentar papilas y cambios nucleares
típicos, como aumento de tamaño, aspecto claro o «vacío» (80%), contorno irregular con
pliegues profundos en la membrana nuclear y seudoinclusiones (80-85%).
Las papilas están conformadas por un tallo fibrovascular, de longitud y espesor variables,
cubierto por células neoplásicas.
Usualmente es un tumor infiltrante, de bordes mal delimitados y consistencia firme (Figura
1). Al corte, su superficie suele ser blanca o amarillenta, de aspecto granular debido a la
presencia de papilas y pueden observarse calcificaciones y lesiones multifocales.
Las variedades histológicas de peor pronóstico son: esclerosante difusa, folicular difusa,
células altas, trabecular, células columnares y desdiferenciado (también llamado carcinoma
poco diferenciado/ indiferenciado con componente de carcinoma papilar).
Las variedades con mejor pronóstico son: encapsulada y microcarcinoma papilar.
Finalmente, las variedades de pronóstico similar son: folicular, sólida, de células oxífilas
(células de Hurtle), estroma similar a fascitis nodular, macrofolicular, similar a tumor de
Warthin, cribiforme-morular y la variedad con estroma lipomatoso.
CÁNCER FOLICULAR
En el cáncer folicular se debe buscar la invasión capsular y vascular. Se considera que hay
invasión capsular cuando el tumor penetra el espesor total de la misma
● , en tanto que la invasión vascular se define como el crecimiento intravascular de
una masa tumoral polipoide cubierta por el endotelio.
Los vasos afectados deben encontrarse en el interior o fuera de la cápsula.
Se clasifica en dos tipos, con importantes implicaciones pronósticas según el grado de
invasividad: mínimamente invasor (encapsulado) y ampliamente invasor.
1) Mínimamente invasor (encapsulado)
- Solo invasión capsular
- Con invasión vascular limitada (<4 vasos)
- Con invasión vascular extensa (> 4 vasos)
● El carcinoma folicular mínimamente invasor macroscópicamente es similar al
adenoma folicular, se encuentra rodeado por una cápsula fibrosa bien definida,
aunque ligeramente irregular y de mayor grosor que en el adenoma, su tamaño varia
entre 1 y 10 cm, generalmente es sólido, de color café o amarillento y puede
presentar zonas de degeneración quística o hemorragia.
● El carcinoma folicular ampliamente invasor muestra infiltración extensa de vasos
sanguíneos y / o del tejido tiroideo adyacente y frecuentemente carece de una
cápsula completa
Diapo 11 Sistemas de estadificación y grupos de riesgo
Los sistemas de estadificación permiten conocer el riesgo de mortalidad a mediano y largo
plazo en los pacientes con cáncer diferenciado de tiroides.
El sistema más utilizado es el TNM, que describe tres piezas clave de información:
● T, indica el tamaño y extensión del tumor
● N, describe la presencia y ubicación de metástasis ganglionares
● M, señala si hay o no metástasis a distancia.
En las guías de la Sociedad Mexicana de Nutrición y Endocrinología se mencionan los
siguientes grupos:
● Muy bajo riesgo. Paciente de cualquier edad con neoplastia unifocal < 1 cm,
intratiroideo y sin extensión vascular o capsular; con resección quirúrgica completa,
sin metástasis, de extirpe histológica no agresiva y sin historia familiar de cáncer
papilar ni personal de radiación ionizante.
● Bajo riesgo. Tumor > 1 y < 4 cm, con el resto de características mencionadas en
muy bajo riesgo.
● Alto riesgo. Enfermos de cualquier edad con una o más de las características
siguientes: tumor > 4 cm, invasión extratiroidea o vascular, extirpe histológica
agresiva, metástasis ganglionares o a distancia, resección quirúrgica incompleta.
American Joint Committee on Cancer (AJCC) y la Unión Internacional Contra el Cáncer
(UICC).
De acuerdo al sistema TNM los pacientes se clasifican en grupos de riesgo de recurrencia o
persistencia.
Según este sistema, la supervivencia observada a los cinco años para el carcinoma
diferenciado en etapa I es del 96.4-97.9%; en la etapa II, del 86.9-93.8; en la etapa III, del
49.8-83.6, y en la etapa IV, del 32.7-48.74
Tratamientos
● Quirúrgico
El tratamiento inicial del cáncer diferenciado de tiroides es quirúrgico y se debe realizar
tiroidectomía.
Para nódulos con PAAF de malignidad
LA PAAF de tiroides es un procedimiento sencillo que consiste en puncionar un nódulo
tiroideo para valorar el riesgo de que sea maligno.,
El procedimiento quirúrgico que se debe efectuar es tiroidectomía total o casi total (dejando
menos de 1 g de tejido adyacente a la inserción del nervio laríngeo recurrente al músculo
cricotiroideo).
● Para tumores mayores de 1 cm, la tirodectomía total disminuye la incidencia de
recurrencias y mejora la sobrevida a largo plazo.
● En pacientes con cáncer diferenciado de tiroides con tumor menor de 1 cm, unifocal,
de muy bajo riesgo, sin evidencia de adenopatías y sin historia de radiación
ionizante, puede ser suficiente una hemitiroidectomía (extirpación de la mitad de la
tiroides).
Se encuentran metástasis ganglionares regionales entre 20 y 90% de los pacientes en el
momento del diagnóstico de cáncer papilar de tiroides. En caso de ser cervicales disminuye
la sobrevida; por ello, si los tumores son primarios avanzados se recomienda la realización
de disección profiláctica del compartimento central del cuello (nivel VI).
● Yodo radiactivo
El objetivo del tratamiento posoperatorio con Yodo-131es la ablación del tejido tiroideo
remanente para destruir el carcinoma residual microscópico.
Facilita la detección temprana de recurrencias con la medición de tiroglobulina sérica y el
rastreo con yodo radiactivo. También disminuye el riesgo de recurrencias reduce 69% las
recurrencias locorregionales y 50% la enfermedad metastásica.
y la mortalidad asociada a cáncer tiroideo en el seguimiento prospectivo en pacientes con
riesgo alto.
En general, en pacientes de riesgo muy bajo no se recomienda el tratamiento con yodo
radiactivo y, en el resto, la dosis dependerá de las características histopatológicas del tumor
y del tipo de paciente.
Puede variar desde 30 mCi milicurio (aunque la tendencia es a utilizar como dosis mínima
70 a 100 mCi) hasta 200 mCi.
● Tratamiento supresivo inicial
Después del tratamiento quirúrgico, ya sea que se haya utilizado yodo radiactivo o no, a los
pacientes se les trata con hormonas tiroideas, con el objetivo de lograr concentraciones de
TSH menores a lo normal; esto se relaciona con 50% menos de mortalidad y 25% de
disminución de las recurrencias, en especial, en pacientes de alto riesgo.
Al inicio se recomienda una meta de TSH menor a 0.1 mU/L en pacientes de riesgo bajo-
alto y de 0.1 a 0.5 mU/L en pacientes de riesgo muy bajo.
TSH NORMAL: .4-4.5
● Seguimiento a largo plazo
Después del tratamiento inicial, 85% de los casos con enfermedad localizada se curan.
● De 10 a 15% tendrán enfermedad recurrente,
○ que en 75% de ellos se localizará en el cuello, siendo más frecuente en los
ganglios linfáticos.
● El 5% de los pacientes tienen enfermedad metastásica desde el principio y sólo una
parte logrará superarla.
La detección temprana de recurrencias ofrece la mejor oportunidad para brindar un
tratamiento eficaz.
El seguimiento se basa en la realización de los estudios siguientes:
• Tiroglobulina sérica.
Como guía, 1 g de tejido tiroideo normal libera 1 ng/mL de tiroglobulina cuando la La
hormona estimulante de la tiroides es normal o 0.5 ng/mL cuando la TSH es menor a 0.1
mU/L.
● Igual pueden puede existir variación de los valores detectados.
Además, los anticuerpos antitiroglobulina pueden interferir en la medición de la tiroglobulina,
por lo que es indispensable que sean negativos para utilizar esta como marcador.
La prevalencia de anticuerpos antitiroglobulina es mayor en pacientes con cáncer
diferenciado de tiroides que en la población general (25 a 30 vs. 10%).
En ausencia de anticuerpos antitiroglobulina, la tiroglobulina tiene una alta sensibilidad y
especificidad para la detección de cáncer tiroideo, sobre todo después de tiroidectomía total
y tratamiento con yodo radiactivo.
• Ultrasonido de cuello.
Ya que el sitio de recurrencias es el cuello, el ultrasonido es una herramienta primordial
para la vigilancia de los pacientes con cáncer tiroideo (sensibilidad de 70 a 100%).
Además, en ganglios sospechosos de metástasis puede realizarse punción guiada por
ultrasonido y medición de tiroglobulina en la muestra obtenida, además del análisis
citológico.
Un valor de tiroglobulina mayor a 10 ng/ mL en el aspirado de un ganglio linfático tiene >
90% de sensibilidad y especificidad en el diagnóstico de metástasis por carcinoma
diferenciado de tiroides.
El ultrasonido tiroideo debe realizarse cada 6 a 12 meses, dependiendo del grupo de riesgo
del paciente y el valor de tiroglobulina sérica.
CARCINOMA MEDULAR DE TIROIDES
El cáncer medular de tiroides es un tumor neuroendocrino de las células parafoliculares o
células C de la glándula tiroides, que representa alrededor de 4% del total de los casos de
cáncer de tiroides.
En cerca de 80% de los casos es esporádico, la edad de presentación es entre la 5a y 6a
décadas de la vida, y es un poco más frecuente en mujeres.
● Por lo regular se manifiesta como un nódulo tiroideo solitario en la porción superior
de un lóbulo tiroideo y, en la mayoría de los pacientes, ya existe enfermedad
metastásica al momento del diagnóstico.
● El 50% tiene adenopatías regionales, 15% síntomas por compresión del tracto
digestivo o aéreo y 5%, enfermedad metastásica a distancia.
● El 20% es de tipo hereditario e incluye carcinoma medular tiroideo familiar (CMTF) y
carcinoma medular como parte de la neoplasia endocrina múltiple (NEM) 2A y 2B.
○ Aparece a edad más temprana (tercera década de la vida) y afecta a ambos
géneros por igual. Lo causa diferentes mutaciones germinales en el
protooncogen RET (proteína codificadora de tirosina quinasa) , que se transmite
de forma autosómica dominante.
A. El NEM 2A corresponde a 75% de las neoplasia endocrina múltiple y se define por
la presencia de carcinoma medular tiroideo (CMT), feocromocitoma e hiperplasia
paratiroidea primaria.
B. La NEM 2B, en cambio, se caracteriza por carcinoma medular tiroideo,
feocromocitoma, ganglioneuromatosis intestinal, neuromas mucosos e intestinales y
rasgos marfanoides; el carcinoma medular tiroideo es más agresivo y se manifiesta
a edades más tempranas.
C. El carcinoma medular tiroideo familiar es una variante de NEM 2A en la que existe
predisposición para CMT, pero no para las demás manifestaciones de NEM 2A.
El diagnóstico puede hacerse sólo cuando hay 10 o más miembros de la familia que son
portadores y varios portadores o afectados tienen más de 50 años de edad.
● Una característica del carcinoma medular es que produce calcitonina y es el
principal marcador sérico.
Algunos tumores también producen antígeno carcinoembrionario que se utiliza, junto con la
calcitonina, como marcador tumoral.
La biopsia por aspiración con aguja fina (PAAF) tiene sensibilidad diagnóstica de 50%.
En todo paciente con diagnóstico preoperatorio de carcinoma medular debe realizarse
ultrasonido de cuello; además, en quienes tienen calcitonina basal mayor a 400 pg/mL debe
realizarse de forma adicional tomografía contrastada de tórax, cuello e hígado porque existe
alta posibilidad de metástasis.
● Los pacientes con cáncer medular de tiroides sólo se pueden curar si se realiza
resección completa del tumor tiroideo y de cualquier metástasis local y regional, por
eso la primera cirugía representa la mejor oportunidad para un tratamiento
adecuado.
El seguimiento se realiza al principio cada 3 a 6 meses con calcitonina y antígeno
carcinoembrionario.
En tanto que los estudios de imagen se realizarán dependiendo de esos marcadores
● utrasonido para búsqueda de enfermedad regional
● tomografía para rastreo de metástasis en tórax y abdomen
● resonancia magnética para metástasis hepáticas.
El tratamiento de la enfermedad metastásica es todo un reto, ya que tiene pobre respuesta
a la radioterapia y a los esquemas de quimioterapia convencionales.
● El yodo radiactivo no tiene ninguna utilidad en este tipo de cáncer.
Los inhibidores de la tirosina cinasa son una opción para estos pacientes; el vandetanib ha
mostrado respuesta parcial entre 20 y 50% de los pacientes, aunque no se ha observado
mejoría en la sobrevida.
Otros inhibidores de tirosina cinasa utilizados en cáncer medular son cabozantinib,
sorafenib y sunitinib.
CARCINOMA ANAPLÁSICO
El cáncer anaplásico es el tumor indiferenciado de las células epiteliales tiroideas.
● Comparado con el cáncer diferenciado de tiroides el anaplásico es muy agresivo,
con una mortalidad que se aproxima a 100% y una sobrevida de 4 a 5 meses.
Corresponde entre 2 y 5% de todos los cánceres tiroideos, la edad promedio de diagnóstico
es de 65 años y 70% son mujeres.
En 20% de los pacientes hay historia de cáncer diferenciado de tiroides y 20 a 30% lo tienen
de forma coexistente. Estos hallazgos llevan a la hipótesis de que el cáncer anaplásico
deriva del cáncer diferenciado de tiroides que ha sufrido diversos eventos de diferenciación.
La mayoría de los pacientes se presentan a consulta con una masa anterior en el cuello y
90% tienen metástasis regionales o a distancia en el momento del diagnóstico, mismo que
se realiza con análisis citopatológico obtenido por PAAF o, de ser necesario, por biopsia
quirúrgica.
También deben considerarse estudios de imagen para delimitar la extensión de la
neoplasia.
Para tumores resecables (casos excepcionales) se debe realizar el tratamiento quirúrgico
asociado a quimio-radioterapia; sin embargo, en los pacientes con enfermedad metastásica
no tiene utilidad la tiroidectomía.
El tratamiento se centra en fines paliativos.
También podría gustarte
- Lección - 2 - Sistema Financiero MexicanoDocumento16 páginasLección - 2 - Sistema Financiero MexicanoJosé De Jesús Ruiz Silva0% (1)
- Gómez E, Cordero J. Traumatología y Ortopedia (SECOT) Generalidades. 1° (2020)Documento571 páginasGómez E, Cordero J. Traumatología y Ortopedia (SECOT) Generalidades. 1° (2020)Micaela Belen100% (5)
- Fundamentos del diagnóstico y tratamiento del cáncer en adultos: Una aproximación inicial para el médico no especialista en cáncerDe EverandFundamentos del diagnóstico y tratamiento del cáncer en adultos: Una aproximación inicial para el médico no especialista en cáncerAún no hay calificaciones
- La importancia de la nutrición en el paciente oncológicoDe EverandLa importancia de la nutrición en el paciente oncológicoAún no hay calificaciones
- Cancer de EndometrioDocumento26 páginasCancer de EndometrioMaha Stephania HafezAún no hay calificaciones
- Cáncer de tiroides: guía completaDocumento31 páginasCáncer de tiroides: guía completaRoque Novillo MendezAún no hay calificaciones
- Patologías de Cabeza y CuelloDocumento50 páginasPatologías de Cabeza y CuelloArturo Martínez González100% (2)
- Cancer TiroidesDocumento41 páginasCancer TiroidesmonchiballsAún no hay calificaciones
- Cáncer de TiroidesDocumento26 páginasCáncer de TiroidesCamilo Fabián Rojas LefeverAún no hay calificaciones
- Patologías Benignas y Malignas de TiroidesDocumento8 páginasPatologías Benignas y Malignas de TiroidesJoséDaniel PerdomoAún no hay calificaciones
- Cáncer de TiroidesDocumento27 páginasCáncer de TiroidesClaudia Raquel Ramírez Pretelín100% (1)
- Cáncer de TiroidesDocumento62 páginasCáncer de TiroidesÁngel Gabriel Velasco GómezAún no hay calificaciones
- Cáncer RenalDocumento12 páginasCáncer RenallollipopAún no hay calificaciones
- CancerDocumento20 páginasCancerAnonymous SxQLvCAún no hay calificaciones
- S36. Neoplasia RenalDocumento17 páginasS36. Neoplasia RenalMary Tineo BautistaAún no hay calificaciones
- CA de Tiroides Guia ColombianaDocumento8 páginasCA de Tiroides Guia ColombianaLuis Andres Dulcey SarmientoAún no hay calificaciones
- Ca TiroidesDocumento11 páginasCa TiroidesTrashAún no hay calificaciones
- Tiroides Cancer PDFDocumento10 páginasTiroides Cancer PDFpedromejiaquevedoAún no hay calificaciones
- Cáncer y Nodulo de Tiroides.Documento8 páginasCáncer y Nodulo de Tiroides.Carlos DíazAún no hay calificaciones
- Anaplastic Thyroid Cancer - UpToDateDocumento30 páginasAnaplastic Thyroid Cancer - UpToDateFrancisco HernandezAún no hay calificaciones
- Ensayo 7 - Cancer de PulmónDocumento11 páginasEnsayo 7 - Cancer de PulmónJoel Macedonio PuertosAún no hay calificaciones
- Patologia Tumoral de TieoidesDocumento9 páginasPatologia Tumoral de TieoidesFelix SaavedraAún no hay calificaciones
- Cancer Anaplasico de TiroidesDocumento9 páginasCancer Anaplasico de TiroidesMEDICKSITOAún no hay calificaciones
- Cáncer de TiroidesDocumento34 páginasCáncer de TiroidesCaminhonete na VeiaAún no hay calificaciones
- Cancer de TiroidesDocumento10 páginasCancer de TiroidesKitzia Daritzy Merino BenítezAún no hay calificaciones
- TiroidesDocumento40 páginasTiroidesJuan David LopezAún no hay calificaciones
- 04 Oncología Especial 1 2020 Genital Masculino y Femenino FinalDocumento113 páginas04 Oncología Especial 1 2020 Genital Masculino y Femenino FinalErnesto CabreraAún no hay calificaciones
- Casos Tiroides 1-8Documento11 páginasCasos Tiroides 1-8CINDY ADILIA FLORES HERNÁNDEZAún no hay calificaciones
- Cáncer de Tiroides: RET MET Trk1 TSH-R Ras p53 p16 PtenDocumento3 páginasCáncer de Tiroides: RET MET Trk1 TSH-R Ras p53 p16 PtenOscar BogadoAún no hay calificaciones
- CANCER-PULMONARDocumento4 páginasCANCER-PULMONARBarbara galvezAún no hay calificaciones
- Nodulos TiroideosDocumento7 páginasNodulos TiroideosCamilo VidalAún no hay calificaciones
- Libro HematologiaDocumento251 páginasLibro HematologiaSilvana VelazquezAún no hay calificaciones
- CÁNCER DE ENDOMETRIO ResumenDocumento6 páginasCÁNCER DE ENDOMETRIO ResumenSol RaspoAún no hay calificaciones
- M.13 - Radioterapia Del Cáncer de MamaDocumento22 páginasM.13 - Radioterapia Del Cáncer de MamaPaco PéreAún no hay calificaciones
- Estudio y Tratamiento de Los Tumores de La Glándula TiroidesDocumento12 páginasEstudio y Tratamiento de Los Tumores de La Glándula TiroidesJuan LandaetaAún no hay calificaciones
- Patología Quirúrgica de La Glándula TiroidesDocumento6 páginasPatología Quirúrgica de La Glándula TiroidesBañuelos NormaAún no hay calificaciones
- Cancer de TesticuloDocumento7 páginasCancer de TesticuloDany Guzman SainzAún no hay calificaciones
- Mod 09 DocumentoDocumento9 páginasMod 09 DocumentoMaria Guadalupe Hernández LópezAún no hay calificaciones
- Cancer TesticularDocumento3 páginasCancer TesticularKaty Marlen GongoraAún no hay calificaciones
- Tumor de WillisDocumento9 páginasTumor de Willisramosurzua37284Aún no hay calificaciones
- Sem. 13 Cancer de TiroidesDocumento42 páginasSem. 13 Cancer de Tiroidesfiorella alexandra vasquez perezAún no hay calificaciones
- Cáncer tiroides: tipos y característicasDocumento7 páginasCáncer tiroides: tipos y característicasCamiladiazAún no hay calificaciones
- Tumores Urologicos MalignosDocumento10 páginasTumores Urologicos MalignosMoises FlowAún no hay calificaciones
- 851-Presentación Electrónica Educativa-988-1-10-20190210Documento12 páginas851-Presentación Electrónica Educativa-988-1-10-20190210Horacio AmadorAún no hay calificaciones
- Tumores-Genitales - 1Documento44 páginasTumores-Genitales - 1Escanor CanAún no hay calificaciones
- Tumores de La Pleura.Documento5 páginasTumores de La Pleura.ismeriAún no hay calificaciones
- Tumor Testicular Expo Dr. Figueredo IiDocumento63 páginasTumor Testicular Expo Dr. Figueredo IiJuanMaraviQuispe0% (1)
- Cancer de TiriodesDocumento35 páginasCancer de TiriodesAna Julia CoelhoAún no hay calificaciones
- Cancer de TiroidesDocumento26 páginasCancer de TiroidesIris GuevaraAún no hay calificaciones
- Patologías Malignas de TiroidesDocumento3 páginasPatologías Malignas de TiroidesJoséDaniel PerdomoAún no hay calificaciones
- Cáncer Papilar TiroideoDocumento2 páginasCáncer Papilar TiroideoRicardo Torres MonteroAún no hay calificaciones
- Cáncer de Tiroides: Epidemiología, Factores de Riesgo, Tipos y TratamientoDocumento10 páginasCáncer de Tiroides: Epidemiología, Factores de Riesgo, Tipos y TratamientoDelia Alejandra FigueroaAún no hay calificaciones
- Cáncer glándulas salivales: causas, tipos, diagnóstico y tratamientoDocumento22 páginasCáncer glándulas salivales: causas, tipos, diagnóstico y tratamientoMaryRuizAún no hay calificaciones
- Cancer PulmonarDocumento7 páginasCancer PulmonarFelipe HermosillaAún no hay calificaciones
- Tumores de ParotidaDocumento21 páginasTumores de ParotidaCynthia BarriaAún no hay calificaciones
- Tumores Cabeza y CuelloDocumento9 páginasTumores Cabeza y CuelloVictor Julio50% (2)
- Tumores Sólidos Más Frecuentes en La InfanciaDocumento14 páginasTumores Sólidos Más Frecuentes en La InfanciajorgeaznarAún no hay calificaciones
- Benemerita Universidad Autonoma de Puebla Endocrinología Cancer de Tiroides Alumno: Porras Flores ErickDocumento13 páginasBenemerita Universidad Autonoma de Puebla Endocrinología Cancer de Tiroides Alumno: Porras Flores ErickErickPorrasFloresAún no hay calificaciones
- DC ResDocumento8 páginasDC ResHENRY GUARACHI HUAMPUAún no hay calificaciones
- Tumores Testiculares RESUMENDocumento3 páginasTumores Testiculares RESUMENMaferRushAún no hay calificaciones
- Cáncer papilar tiroideo: Etiología, factores de riesgo y tratamientoDocumento6 páginasCáncer papilar tiroideo: Etiología, factores de riesgo y tratamientoLiz Estrella UDAún no hay calificaciones
- Cancer de Glandula Tiroides y Glandulas SalivalesDocumento24 páginasCancer de Glandula Tiroides y Glandulas SalivalesdrahernandezckAún no hay calificaciones
- Alergo. Caso Clinico 1Documento9 páginasAlergo. Caso Clinico 1Ana Itzel Carlon ChavezAún no hay calificaciones
- Alergo - E1Documento4 páginasAlergo - E1Ana Itzel Carlon ChavezAún no hay calificaciones
- T2 - Applications and Mechanisms of Immunotherapy in Allergic Rhinitis and AsthmaDocumento4 páginasT2 - Applications and Mechanisms of Immunotherapy in Allergic Rhinitis and AsthmaAna Itzel Carlon ChavezAún no hay calificaciones
- Alergo. Expo Tema 1Documento8 páginasAlergo. Expo Tema 1Ana Itzel Carlon ChavezAún no hay calificaciones
- Alergo 3Documento69 páginasAlergo 3Ana Itzel Carlon ChavezAún no hay calificaciones
- Alergo 2Documento8 páginasAlergo 2Ana Itzel Carlon ChavezAún no hay calificaciones
- Alergología Final-Factores Ambientales y GenéticosDocumento7 páginasAlergología Final-Factores Ambientales y GenéticosAna Itzel Carlon ChavezAún no hay calificaciones
- Alergo 3Documento69 páginasAlergo 3Ana Itzel Carlon ChavezAún no hay calificaciones
- GM 093 FDocumento8 páginasGM 093 FMichael MendozaAún no hay calificaciones
- Artículo 5Documento8 páginasArtículo 5Ana Itzel Carlon ChavezAún no hay calificaciones
- Historia ClinicaDocumento58 páginasHistoria Clinicakarla hernandez bautistaAún no hay calificaciones
- Control prenatal: guía completaDocumento21 páginasControl prenatal: guía completaDanna L. S. Barrios100% (2)
- Los Instrumentos de CuerdaDocumento1 páginaLos Instrumentos de Cuerdaelizabeth aliende garciaAún no hay calificaciones
- Pantomima de ColaseDocumento1 páginaPantomima de ColaseEdwin Adelmo Eugenio MejiaAún no hay calificaciones
- La Música PopDocumento11 páginasLa Música PopSamuel Tomás Ramirez MorenoAún no hay calificaciones
- CTS y Obreros MunicipalesDocumento5 páginasCTS y Obreros MunicipalesMarco AntonioAún no hay calificaciones
- Coleccion de InsectosDocumento8 páginasColeccion de InsectosAlex SantosAún no hay calificaciones
- Sendero de Guerra Gato y Ratón Trabajo Sucio: Cable & DominoDocumento1 páginaSendero de Guerra Gato y Ratón Trabajo Sucio: Cable & DominoJavier MoralesAún no hay calificaciones
- Planificación estratégica de COLQUISIRI SAC para mejorar su proceso productivoDocumento35 páginasPlanificación estratégica de COLQUISIRI SAC para mejorar su proceso productivoCirculo de estudios INMETAMINAMAún no hay calificaciones
- Gestión Calidad COPEMIDocumento24 páginasGestión Calidad COPEMISistemas - Dionicio MelendezAún no hay calificaciones
- Sistema Calidad ISO Almacén RepuestosDocumento51 páginasSistema Calidad ISO Almacén RepuestosAlexis Marcano PradaAún no hay calificaciones
- Notificación y Reporte de Incidentes de TrabajoDocumento1 páginaNotificación y Reporte de Incidentes de Trabajodiana giraldoAún no hay calificaciones
- Argumentacion OralDocumento9 páginasArgumentacion OralArath JerezAún no hay calificaciones
- El Kamasutra Gallego-CSP Proof-08!11!13Documento38 páginasEl Kamasutra Gallego-CSP Proof-08!11!13Alfonso Cordal RodriguezAún no hay calificaciones
- Tipos de acoplamientos mecánicos y sus aplicacionesDocumento8 páginasTipos de acoplamientos mecánicos y sus aplicacionesA.Aún no hay calificaciones
- Caddy 2017 (Abs)Documento7 páginasCaddy 2017 (Abs)Rbrt CruzAún no hay calificaciones
- AndamiosDocumento12 páginasAndamiosPerozo LinaAún no hay calificaciones
- Estructura de La Materia y Estructura AtomicaDocumento9 páginasEstructura de La Materia y Estructura AtomicaAbel V. SolanoAún no hay calificaciones
- Cartas ComercialesDocumento7 páginasCartas ComercialesAngel InterianoAún no hay calificaciones
- T1. La Célula, Organelas y Niveles de Organización Del Cuerpo Humano.Documento25 páginasT1. La Célula, Organelas y Niveles de Organización Del Cuerpo Humano.José Luis Lazo QuispeAún no hay calificaciones
- Electricidad Ley de Ohm y Circuitos Eléctricos Semana 8Documento5 páginasElectricidad Ley de Ohm y Circuitos Eléctricos Semana 8pedro santander lopezAún no hay calificaciones
- Introducción al marketingDocumento262 páginasIntroducción al marketingpityadami100% (1)
- Informe de Avance de EjecuciónDocumento13 páginasInforme de Avance de EjecuciónManuel ObandoAún no hay calificaciones
- Biografía Del Dr. Abel Pacheco de La Espriella-Presidente de Costa Rica-May-2002Documento3 páginasBiografía Del Dr. Abel Pacheco de La Espriella-Presidente de Costa Rica-May-2002Naty PeñaAún no hay calificaciones
- Gtc61 Empaque FruhortalDocumento6 páginasGtc61 Empaque FruhortalAndres GuerreroAún no hay calificaciones
- Contribuyente y ResponsableDocumento4 páginasContribuyente y ResponsableYolanda Coa NoaAún no hay calificaciones
- La Era Del Vacío. Ensayos Sobre El IndividualismoDocumento2 páginasLa Era Del Vacío. Ensayos Sobre El IndividualismoIngrid Rocio de ZapataAún no hay calificaciones
- La Conquista Del Peru. Pizarro y Almagro PDFDocumento24 páginasLa Conquista Del Peru. Pizarro y Almagro PDFZaydi Calla100% (1)
- Costos en hoteles y restaurantesDocumento5 páginasCostos en hoteles y restaurantesGonzAguirre0% (1)
- 2341Documento38 páginas2341daniel mamaniAún no hay calificaciones