Documentos de Académico
Documentos de Profesional
Documentos de Cultura
c17 Ciclo Celular y Mitosis 220421 Downloable 2268276
Cargado por
Mariana Hernández MoralesTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
c17 Ciclo Celular y Mitosis 220421 Downloable 2268276
Cargado por
Mariana Hernández MoralesCopyright:
Formatos disponibles
Accede a apuntes, guías, libros y más de tu carrera
c17-ciclo-celular-y-mitosis
8 pag.
Descargado por Mariana Hernandez (mh3801827@gmail.com)
Encuentra más documentos en www.udocz.com
Kiara Kanackowicz
Una célula se reproduce mediante una secuencia ordenada de acontecimientos en los que duplica su contenido y, luego, se
divide en dos. Esto se conoce como ciclo celular, es el mecanismo esencial de reproducción de todos los seres vivos. Los
detalles del ciclo varían en los distintos organismos y en diferentes momentos de la vida de un organismo dado.
Organismos unicelulares, como bacterias y levaduras, producen un organismo nuevo completo en cada división. Por el
contrario, se requieren muchas rondas de división celular para crear un organismo pluricelular nuevo a partir de un oocito
fecundado.
El ciclo celular de las células eucariontes se divide en cuatro
fases, los dos acontecimientos más notables del ciclo son la
división celular (mitosis) y la división de la célula en dos
(citocinesis). Estos dos procesos constituyen la fase M del ciclo
celular.
El periodo entre una fase M y la siguiente se denomina interfase,
se trata de un período muy activo que comprende las tres fases
restantes del ciclo celular:
la célula replica su ADN nuclear.
se trata del tiempo que media entre el final de la fase M
y el comienzo de la fase S.
es el periodo entre el final de la fase S y el comienzo de
la fase M.
Durante G1 y G2, la célula controla los ambientes intracelular y
extracelular asegurándose que las condiciones sean adecuadas y de que se hayan completado los preparativos antes de
encarar las complejas tareas de la fase S y la mitosis. En determinados puntos de G 1 y G2, la célula decide si pasa a la fase
siguiente o hace una pausa que le permita tener más tiempo para prepararse. Por lo tanto ambas fases permiten ganar
tiempo para que la célula crezca y duplique los orgánulos citoplasmáticos.
El sistema de control del ciclo celular garantiza que los acontecimientos tengan lugar en una secuencia establecida y que cada
proceso se haya completado antes de que comience el siguiente. Este control es regulado en determinados puntos críticos del
ciclo mediante retroalimentación del proceso que se está llevando a cabo.
Este sistema logra detener posibles errores mediante frenos moleculares que pueden
tener el ciclo en diversos puntos de control. Así, el sistema de control no desencadena
el siguiente paso, a menos que la célula esté correctamente preparada. Además, si el
sistema funciona mal y permite que la división celular sea excesiva, puede aparecer
cáncer.
permite que la célula corrobore que el medio es favorable
para su proliferación antes de dedicarse a la fase S. En los animales, se requieren
nutrientes y moléculas de señalización específicas del medio extracelular; si las
condiciones extracelulares son desfavorables, las células pueden retardar el proceso a
través de G1 e, incluso, puede ingresar a un estado de reposo
denominado G0.
garantiza que las células no ingresen
en la fase de mitosis hasta que no se haya reparado el ADN
dañado y se haya completado la reparación del ADN.
garantiza que los
cromosomas replicados estén unidos apropiadamente al huso
mitótico, antes de que este separe los cromosomas y los
distribuya en las dos células hijas.
El sistema de control utiliza la fosforilación seguida de
desfosforilación para estimular o inhibir la actividad de proteínas y
Descargado por Mariana Hernandez (mh3801827@gmail.com) Kiara Kanackowicz
Encuentra más documentos en www.udocz.com
Kiara Kanackowicz
complejos proteicos clave que inician o regulan la replicación del ADN, la mitosis y la citocinesis.
La fosforilación la realiza un conjunto específico de proteincinasas, mientras que la desfoforilación, un grupo de
proteinfosfatasas. Las primeras se encuentran presentes durante todo el ciclo celular en las células en proliferación, pero solo
son activadas en momentos oportunos del ciclo, después de lo cual vuelven a ser desactivadas con rapidez.
Las cinasas dependen de otro grupo de proteínas del sistema de control, las ciclinas, que deben unirse a estas proteínas para
que adquieran actividad enzimática. Las cinasas del sistema de control del ciclo celular se conocen como proteincinasas
dependientes de ciclinas (Cdk).
Para que una ciclina-Cdk sea activada, debe estar fosforilada en un sitio y desfosforilada en otros dos. Cuando se forma
inicialmente, el complejo ciclina-Cdk no está fosforilado y es inactivo. Después, la Cdk es fosforilada en un sitio, lo que es
necesario para su actividad y en otros dos sitios que inhiben su actividad. Este
complejo fosforilado sigue siendo inactivo hasta que, por último, es activado
por una fosfatasa que elimina los dos grupos fosfatos inhibitorios.
Distintos complejos ciclina-Cdk desencadenan diferentes pasos del ciclo
celular.
-La ciclina que actúa en G2 desencadenando el ingreso en la fase M se
denomina ciclina M, y el complejo activa forma con su Cdk, Cdk de M.
-Las ciclinas S y ciclinas G1/s se unen a una proteína Cdk diferente en un
estadio tardío de G1 formando Cdk de S y Cdk de G1/S
-Las ciclinas G1 actúan en un momento más temprano de la fase G1 y se unen a otras proteínas Cdk formando Cdk de G1, que
ayudan a impulsar el pasaje de la célula de la fase G1 a la fase S. La formación de estos complejos suele depender de
moléculas de señalización extracelular que estimulan la división celular.
A su vez, cada uno de estos complejos ciclina-Cdk activados fosforila un grupo distinto de proteínas diana de la célula. En
consecuencia, cada tipo de complejo desencadena un paso de transición diferente del ciclo celular.
La concentración de cada tipo de ciclina aumenta de manera gradual, pero después cae bruscamente en un momento
específico del ciclo celular. Esto se debe a la degradación de la proteína ciclina. Complejos enzimáticos específicos añaden
cadenas de ubicuitina a la ciclina apropiada, que después es dirigida hacia el proteasoma donde se destruye. Esta rápida
eliminación de la ciclina restablece el estado inactivo de las Cdk.
Hay ciertas proteínas que inhiben las Cdk, estas son capaces de detener el ciclo celular en puntos de control específicos, lo
que permite que la célula revise su estado interno y su medio antes de progresar a lo largo del ciclo. Ciertas proteínas
inhibidoras de las Cdk ayudan a mantener las Cdk en estado inactivo durante la fase G1 del ciclo, lo que demora la progresión
a la fase S. La pausa en este punto de control le da más tiempo a la célula para que crezca o le permite aguardar a que las
condiciones extracelulares sean favorables para la división.
Una vez superado el punto de control de G1, una célula suele cumplir con rapidez todo el resto del ciclo celular. Por lo tanto, el
punto de control G1 se denomina start, porque atravesarlo representa un compromiso para completar un ciclo de división
completo, aunque stop podría ser una mejor denominación.
La decisión más radical que puede tomar el sistema de control del ciclo celular es que la célula abandone en forma
permanente el ciclo celular, esto tiene una importancia especial en los organismos pluricelulares. Por ejemplo, las células
nerviosas y las células del musculo esquelético dejan de dividirse en forma permanente cuando se diferencian. Ingresan en un
estado G0 irreversible, en el que el sistema de control del ciclo está, en gran medida, desmantelado.
La replicación del ADN comienza en los orígenes de replicación, secuencias de nucleótidos dispersas a lo largo de cada
cromosoma. Estas reclutan proteínas específicas que controlan el proceso de replicación del ADN. El complejo de
reconocimiento de origen (ORC), permanece unido a los origines de replicación durante todo el ciclo celular y actúa como
una ‘’pista’’ para otras proteínas reguladores que se
unen antes del comienzo de la fase S.
Una de estas proteínas se denomina Cdc6. Está
presente en bajos niveles durante la mayor parte del
ciclo celular, pero su concentración aumenta
transitoriamente en los primeros momentos de G1.
Cuando se une a los ORC en G1, promueve la unión de
otras proteínas y forma un complejo prerreplicación.
Descargado por Mariana Hernandez (mh3801827@gmail.com) Kiara Kanackowicz
Encuentra más documentos en www.udocz.com
Kiara Kanackowicz
Una vez ensamblado este complejo, el origen de replicación se encuentra listo para ‘’disparar’’. Después, la activación de Cdk
de S a fines de G1, ‘’aprieta el gatillo’’, lo que inicia la replicación del ADN.
Cdk de S contribuye a la fosforilación de Cdc6, lo que determina que esta y otras proteínas del complejo prerreplicación se
disocien del ORC después de que un origen se ha activado. Este desensamblaje impide que la replicación se produzca de
nuevo en el mismo origen. Además, la fosforilación es una marca que permite su degradación, lo que asegura que no se
reinicie la replicación del ADN en una fase más avanzada del mismo ciclo celular.
Después de que los cromosomas se duplicaron en la fase S, las dos copias de cada
cromosoma replicado permanecen unidas estrechamente por complejos proteicos
denominados cohesinas como cromátidas hermanas. Las cohesinas se ensamblan a
lo largo de toda la extensión de cada cromática hermana medida que se replica el
ADN, formando anillos proteicos que rodean a ambas cromátidas hermanas y las
mantienen juntas.
Los puntos de control de daño del ADN de las fases G1 y S impiden que la célula
comience o complete la fase S y replique el ADN dañado.
El daño de ADN causa un aumento de la concentración y la actividad de la proteína p53, que es un regulador que activa la
transcripción de un gen que codifica una proteína inhibidora de las Cdk llamada p21. Esta última se une a Cdk de G1/S y a Cdk
de S, y les impide impulsar la célula a la fase S, generando tiempo para reparar el ADN dañado. Si el daño es demasiado
grande para ser reparado, p53 puede inducirá la célula a la autodestrucción por apoptosis. Si no hay p53, surgen mutaciones a
raíz de la replicación del ADN dañado.
Una vez iniciada la replicación del ADN, la fosforilación en
determinados sitios inhibe la actividad de los complejos ciclina-
Cdk. Para que la célula progrese a la mitosis se debe activar la
Cdk de M por eliminación de estos fosfatos inhibitorios por una
proteinfosfatasa específica. Cuando el ADN está dañado, la
proteinfosfatasa activadora está inhibida, de manera que no se
eliminan los fosfatos inhibitorios de la Cdk de M. En
consecuencia, esta permanece inactiva y no se puede iniciar la
fase M hasta que la replicación del ADN sea completa y se haya
reparado cualquier daño del ADN.
Una vez que la célula ha superado estos puntos de control y ha replicado con éxito su ADN en la fase S y avanzado a G2, está
preparada para ingresar a la fase M.
Durante este corto periodo, la célula reconoce casi todos sus componentes y los distribuye por igual en las dos células hijas.
Un solo complejo proteico, Cdk de M, desencadena la condensación de los cromosomas replicados en estructuras compactas,
lo que los separa para la segregación. También induce el ensamblaje del huso mitótico.
Cuando se forman por primera vez estos complejos, son inactivos. La súbita activación
de la reserva de Cdk de M al final de G2 es desencadenada por la activación de una
proteinfosfatasa (Cdc25) que elimina los fosfatos inhibitorios que mantienen frenada a
Cdk de M. Una vez activado, hay un aumento explosivo de la actividad de Cdk de M que
impulsa a la célula bruscamente de la fase G2 a la fase M.
Cuando la célula está por ingresar en la fase M, complejos proteicos denominados
condensinas ayudan a llevar a cabo la condensación cromosómica. Esta condensación
reduce la probabilidad de que los cromosomas se entrelacen, lo que facilita su
segregación en las dos células hijas durante la mitosis.
La Cdk de M que inicia el ingreso en la fase M desencadena el ensamblaje de
complejos de condensina en el ADN al fosforilar algunas de las subunidades de
condensina. Las condensinas se ensamblan en cada cromátida individual al
comienzo de la fase M y enrollan el ADN ayudando a que se condense cada
cromátida.
Después de la condensación de los cromosomas replicados, se forman
secuencialmente dos maquinarias citoesqueléticas complejas que llevan a cabo
los dos procesos mecánicos que se producen en la fase M:
Descargado por Mariana Hernandez (mh3801827@gmail.com) Kiara Kanackowicz
Encuentra más documentos en www.udocz.com
Kiara Kanackowicz
El huso mitótico, compuesto por microtúbulos y las diferentes proteínas que interactúan con ellos, incluidas las proteínas
motoras asociadas con los microtúbulos.
El anillo contráctil, consiste en filamentos de actina y miosina distribuidos de manera anular alrededor del ecuador de la
célula. Comienza a formarse justo por debajo de la membrana plasmática al final de la mitosis.
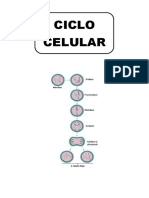
La fase M se divide en seis etapas; las cinco primeras –profase, prometafase, metafase, anafase y telofase- constituyen la
mitosis, período donde los cromosomas son visibles. La citocinesis es la sexta etapa, que se superpone con el final de la
mitosis.
Antes de que comience la fase M, el centrosoma debe replicarse completamente. Este es el principal
centro organizador de microtúbulos en las células animales. Su duplicación contribuye a la formación de los
dos polos del huso mitótico y a que cada célula hija pueda recibir su propio centrosoma.
Al principio, ambas copias permanecen juntas como un complejo único al lado del núcleo. Sin embargo,
cuando comienza la mitosis, los dos centrosomas se separan, y cada uno nuclea una estructura radial de
microtubulos denominada áster. Estos dos se desplazan a lados opuestos del núcleo formando los dos
polos del huso mitótico. El proceso de duplicación y separación del centrosoma se conoce como ciclo del
centrosoma.
El huso mitótico comienza a formarse en esta fase. El ensamblaje depende de las propiedades de los
microtúbulos: aumenta la inestabilidad dinámica de los microtúbulos, ya que
la Cdk de M fosforila proteínas asociadas con los microtúbulos que influyen
en la estabilidad de los filamentos de los mismos. Por lo tanto, se extienden
en todas las direcciones microtúbulos a partir de los dos centrosomas.
Algunos interactúan entre sí, estabilizando la unión y formando el marco
básico del huso mitótico, con su forma bipolar característica. Los dos
centrosomas que dan origen a estos microtúbulos se denominan polos del
huso, y los microtúbulos que interactúan, microtúbulos interpolares.
Los cromosomas comienzan a condensarse
El huso mitótico comienza a formarse.
El nucléolo desaparece.
Se inicia en forma repentina con la desorganización de la
envoltura nuclear, que se rompe en pequeñas
vesículas de membrana. Este proceso se
desencadena por la fosforilación y el
consiguiente desensamblaje de las proteínas del
poro nuclear y las proteínas de los filamentos
intermedios de la lámina nuclear.
Inmediatamente antes de la prometafase, las proteínas del cinetocoro forman un
complejo de gran tamaño en cada centrómero. Por consiguiente, cada cromosoma
duplicado tiene dos cinetocoros orientados en
direcciones opuestas
Los microtúbulos del huso, que estaban fuera del núcleo,
ahora acceden a los cromosomas replicados y los capturan. Estos terminan unidos a los
microtúbulos por medio de cinetocoros, que se ensamblan en los cromosomas condensados
durante la profase tardía y este microtúbulo de cinetocoro une al cromosoma a un polo del huso.
La unión a polos opuestos llamada biorientación, genera tensión en los cinetocoros hermanos
que están correctamente unidos y preparados para ser separados. El sistema de control del ciclo
celular monitoriza esta tensión garantizando la correcta unión de los cromosomas.
Los cromosomas se condensan aún más, por lo que están muy compactos.
La envoltura nuclear se descompone y los cromosomas se liberan.
El huso mitótico crece más y algunos de los microtúbulos empiezan a “capturar” cromosomas.
Descargado por Mariana Hernandez (mh3801827@gmail.com) Kiara Kanackowicz
Encuentra más documentos en www.udocz.com
Kiara Kanackowicz
Los cromosomas, unidos ahora al huso mitótico, comienzan a
moverse de un lado al otro. Finalmente se alinean a mitad de camino entre
ambos polos del huso, lo que forma la placa metafásica. También se requiere un
equilibrio continuo entre el agregado y la perdida de subunidades de tubulina
para mantener el huso metafásico.
Los cromosomas (que se mantienen allí sometidos a tensión) ajustan
continuamente sus posiciones, lo que indica que el tira y afloje entre los
microtúbulos unidos a cada polo del huso persiste aun después de que todos los
cromosomas se encuentran alineados.
Antes de proceder a la anafase, la célula comprobará que todos los cromosomas
estén en la placa metafásica con sus cinetocoros unidos correctamente a los microtúbulos. Esto se llama punto de control del
huso y ayuda a asegurar que las cromátidas hermanas se dividan uniformemente entre las dos células hijas cuando se separan
en el paso siguiente.
Todos los cromosomas se alinean en la placa metafásica
Los dos cinetocoros de cada cromosoma deben unirse a los microtúbulos de los polos opuestos del huso.
Comienza de manera brusca con la liberación de la unión de
cohesinas, que es destruida por una proteasa (separasa) que hasta el
comienzo del anafase se mantiene en estado inactivo por unión a una
proteína inhibitoria (securina). Esta última es marcada para la destrucción
por un complejo proteico conocido como complejo promotor del anafase
(APC). Una vez eliminada la securina, la separasa puede romper las uniones
de cohesina.
La APC también marca la ciclina M que de esta manera se destruye, lo que
desactiva el complejo Cdk de M. Esta rápida desactivación de Cdk de M
ayuda a iniciar la salida de la mitosis.
Una vez que las cromátidas hermanas se separan, son arrastradas al polo
del huso al que están unidas. El desplazamiento es consecuencia de dos procesos independientes mediados por partes
diferentes del huso mitótico.
los microtúbulos del cinetocoro se acortan por despolimerización, y los cromosomas unidos a ellos se desplazan
en dirección al polo. La pérdida de subunidades de tubulina depende de una proteína de tipo motora que utiliza la energía de
la hidrolisis del ATP para eliminar subunidades de tubulina del microtúbulo.
. Los propios polos del uso se separan uno del otro, lo que
contribuye todavía más a la segregación de los dos grupos de cromosomas.
Las fuerzas impulsoras de este movimiento dependen de dos grupos de
proteínas: cinesina y dineínas, que actúan en diferentes tipos de
microtúbulos del huso
El control de salida de la mitosis es el punto de control de ensamblaje del
huso, que supervisa si todos los cromosomas están unidos en forma correcta
al huso antes de terminar el proceso. Sin APC activo, las cromátidas hermanas
continúan adheridas y no es posible separar ninguno de los cromosomas duplicados hasta que se hayan ubicado
correctamente en el huso mitótico.
El “pegamento” proteico que mantiene juntas a las cromátidas hermanas se degrada, lo que permite que se separen. Cada
una ahora es su propio cromosoma. Los cromosomas de cada par son jalados hacia extremos opuestos de la célula.
Los microtúbulos no unidos a los cromosomas se elongan y empujan para separar los polos y hacer más larga a la célula.
Se desensambla el huso mitótico y se reensambla la envoltura nuclear alrededor de cada grupo de
cromosomas formando los dos núcleos hijos.
Se agrupan vesículas de membrana alrededor de cada cromosoma y, después, se fusionan reconstruyendo la envoltura
nuclear. Durante este proceso, se desfosforilan las proteínas del poro nuclear y las láminas nucleares que fueron fosforiladas
durante la prometafase, lo que permite que se vuelvan a ensamblar y formen la envoltura nuclear y la lámina nuclear.
Descargado por Mariana Hernandez (mh3801827@gmail.com) Kiara Kanackowicz
Encuentra más documentos en www.udocz.com
Kiara Kanackowicz
Una vez que sucedió esto, los poros bombean proteínas al interior del núcleo y los
cromosomas mitóticos condensados se descondensan hasta recuperar su estado de
interfase.
El huso mitótico se descompone en sus componentes básicos.
Se forman dos nuevos núcleos, uno para cada conjunto de cromosomas. Las
membranas nucleares y los nucléolos reaparecen.
Los cromosomas comienzan a descondensarse y vuelven a su forma "fibrosa".
Se trata del proceso por el cual el citoplasma se escinde en dos. Comienza en el anafase pero no finaliza hasta que se han
formado los dos núcleos hijos en la telofase. Depende del anillo contráctil.
El anillo contráctil está compuesto por una serie de filamentos de actina y de miosina superpuestos, está unido a proteínas
asociadas con la membrana en la cara citoplasmática de la membrana plasmática. Esta
estructura es transitoria: se forma cuando se lleva a cabo la citocinesis, disminuye
paulatinamente de tamaño a medida que esta progresa y se desensambla por completo una
vez que la célula se divide en dos.
El primer signo visible de citocinesis en las células animales es la aparición de un pliegue y un
surco en la membrana plasmática, que se observa durante la anafase. Siempre se forma en un
plano perpendicular al eje mayor celular entre los dos grupos de cromosomas segregados, de
modo que cada célula hija reciba una dotación idéntica y completa de cromosomas.
Durante la anafase, tanto los microtúbulos del áster como los interpolares, envían señales a la
corteza celular que inician el ensamblaje del anillo contráctil en una posición intermedia entre
los polos del huso.
Cuando el huso mitótico se localiza en la región central de la célula, las dos células hijas producidas serán del mismo tamaño.
La división de muchas células animales se acompaña de grandes modificaciones de la forma de la célula y de una disminución
de su adherencia a sus vecinas o a la matriz extracelular. Esto se debe a que algunas de las integrinas de la membrana
plasmática (responsables de la adherencia) se fosforilan y, en consecuencia, su adherencia se
debilita. Una vez completada la citocinesis, las células hijas restablecen sus firmes contactos
con el sustrato y vuelven a aplanarse.
Este ciclo les permite reorganizar sus contactos con las células vecinas y con la matriz
extracelular, de manera que las nuevas células producidas durante la división celular puedan
ser alojadas dentro del tejido.
Las dos células hijas se separan por la formación de una pared nueva dentro de la célula en
división. La posición de esta nueva pared determina con precisión la localización de las dos
células hijas respecto de las células vecinas.
La pared celular nueva comienza a ensamblarse en el citoplasma entre los dos grupos de
cromosomas segregados al comienzo de la telofase. El proceso es guiado por una estructura denominada fragmoplasto, que
está formada por los restos de los microtúbulos interpolares en el ecuador del antiguo huso mitótico.
Pequeñas vesículas rodeadas de membrana, llenas de polisacáridos y glucoproteinas requeridos para la matriz de la pared
celular, son transportadas a lo largo de los microtúbulos hasta el fragmoplasto. Una vez allí, se fusionan formando una
estructura similar a un disco, delimitada por una membrana, que se expande hacia afuera con nuevas fusiones de vesículas
hasta que alcanza la membrana plasmática y la pared celular original, y divide a la célula en dos. Luego, se depositan dentro
de la matriz microfibrillas de celulosa que completan la construcción de la nueva pared celular.
Por lo general, los orgánulos como las mitocondrias y los cloroplastos están presentes en gran cantidad y se heredarán de
manera segura solo con que, en promedio, se duplique su número con cada ciclo celular. Al ingresar en la fase M, en la
mayoría de las células, el RE liberado permanece intacto durante la mitosis y es seccionado en dos durante la citocinesis. El
Descargado por Mariana Hernandez (mh3801827@gmail.com) Kiara Kanackowicz
Encuentra más documentos en www.udocz.com
Kiara Kanackowicz
complejo de Golgi se fragmenta durante la mitosis; los fragmentos se asocian con los microtúbulos del huso mediante
proteínas motoras, lo que los lleva hacia las células hijas cuando el huso se elonga en la anafase.
Todas las proteínas solubles se heredan en forma aleatoria cuando la célula se divide.
El tamaño de los órganos y el cuerpo está determinado por tres procesos esenciales: crecimiento, división y muerte celular.
Cada uno depende de programas intrínsecos de cada célula y es regulado por
señales provenientes de otras células del organismo.
La cantidad de células de un organismo pluricelular está estrictamente regulada.
Las células que ya no son necesarias pueden suicidarse mediante la activación de
un programa de muerte intracelular, un proceso denominado muerte celular
programada. En los animales, la forma más común se conoce como apoptosis.
¿Cuál es la finalidad de este suicidio celular masivo? En los tejidos adultos, la
muerte celular suele equilibrar exactamente la división celular, a menos que el
tejido esté creciendo o contrayéndose.
En algunos casos, las respuestas son claras. Las patas del ratón –y las manos y los
pies del ser humano- son modelados por apoptosis durante el desarrollo
embrionario: comienzan como estructuras en forma de pala, y los dedos de las manos y los pies se separan a medida que
mueren las células situadas entre ellos.
En otros casos, las células mueren cuando la estructura que han formado deja de ser necesaria.
Una célula que presenta un proceso de apoptosis muere de manera limpia, sin dañar las células adyacentes (sin generar
necrosis). Una célula en vía de apoptosis se retrae y se condensa, el citoesqueleto se colapsa, la envoltura nuclear se
desensambla, y el ADN nuclear se fragmenta. Además, la superficie celular se altera de manera que atrae de inmediato células
fagociticas (macrófagos). Estas engloban la célula apoptótica antes de que esta derrame su contenido. La eliminación rápida
de la célula moribunda evita las consecuencias lesivas de la necrosis celular y permite que el fagocito recicle los componentes
de la célula apoptótica.
En la apoptosis interviene la familia de proteasas caspasa, que escinden y activan a
otros miembros de la familia de procaspasas, lo que determina la amplificación de la
cascada proteolítica. Estas enzimas también degradan otras proteinas clave de la
célula.
La activación del programa de apoptosis se suele desencadenar en una forma todo o
nada. No solo es destructiva y se autoamplifica, sino que también es irreversible: una
vez que la célula llega a un punto crítico de la vía hacia la destrucción, no puede
volver atrás. Por lo tanto, es importante el control estricto de la decisión de morir.
Los organismos unicelulares (bacterias y levaduras), tienden a crecer y a dividirse
con la mayor rapidez posible y su velocidad de proliferación depende, en gran
medida, de la disponibilidad de nutrientes en el medio.
Las células de un organismo pluricelular son controladas de manera que una célula
individual sobrevive solo cuando es necesaria y se divide solo cuando se requiere otra célula, lo que permite el crecimiento
tisular o el reemplazo de células perdidas. Así, una célula animal sobrevive crece o se divide no solo por la presencia de
nutrientes sino también al recibir señales químicas provenientes de otras células, en general sus vecinas.
Las proteínas de señalización que ejercen una acción positiva se pueden dividir de acuerdo con su función, en tres clases
principales:
promueven la supervivencia celular.
Por lo general, se unen a receptores de la superficie celular, que activan vías de señalización intracelular, lo que mantiene
inhibido el programa de muerte celular. Esto se da mediante la regulación de miembros de la familia de proteínas Bcl2, por lo
tanto, realiza una supresión de la apoptosis.
estimulan la división celular, fundamentalmente al contrarrestar los mecanismos intracelulares de freno que
tienden a bloquear la progresión a lo largo del ciclo celular.
Descargado por Mariana Hernandez (mh3801827@gmail.com) Kiara Kanackowicz
Encuentra más documentos en www.udocz.com
Kiara Kanackowicz
La mayoría de los mitógenos son proteínas de señalización secretadas que se unen a receptores de la superficie celular.
Cuando son activados por la unión del mitógenos, estos receptores inician diversas vías de señalización intracelular que
estimulan la división celular. Esas vías de señalización actúan, principalmente, mediante la eliminación de los frenos
moleculares intracelulares que bloquean la transición de la fase G1 del ciclo celular a la fase S y si la deprivación persiste el
tiempo suficiente, la célula abandonara el ciclo celular e ingresara en un estado no proliferativo G0.
La mayor parte de la diversidad en las velocidades de división celular del organismo adulto reside en la variación del tiempo
que las células pasan en G0 o en G1. El escape de este punto de control exige la acumulación de ciclinas G1 y los mitógenos
actúan estimulando esta acumulación.
estimulan el crecimiento celular (aumento del tamaño y de la masa celular) mediante la
promoción de la síntesis y la inhibición de la degradación de proteínas y otras macromoléculas.
El crecimiento de un organismo o de un órgano depende tanto del crecimiento como de la división celular. Si las células se
dividieran sin crecer, se tornarían cada vez más pequeñas y no habría un aumento de la masa celular total.
Los factores de crecimiento se unen a receptores de superficie celular que activan diversas vías de señalización intracelular.
Estas vías inducen la acumulación de proteínas y otras macromoléculas mediante el aumento de su velocidad de síntesis y la
disminución de su velocidad de degradación. Algunas proteínas de señalización extracelular pueden actuar como factores de
crecimiento y como mitógenos, y de esa manera estimulan tanto el crecimiento celular como la progresión a través del ciclo
celular. Estas proteínas ayudan a asegurar que las células conserven su tamaño apropiado a medida que proliferan.
Todas estas proteínas no se excluyen mutuamente, muchas cumplen más de una de las funciones mencionadas. Sin embargo,
algunas proteínas de señalización extracelular ejercen una acción que se opone a la de estos reguladores positivos y, por lo
tanto, inhiben el crecimiento tisular, como por ejemplo la miostatina. Se trata de una proteína de señalización que en
condiciones normales inhibe el crecimiento y la proliferación de los mioblastos que se fusionan formando células del musculo
esquelético durante el desarrollo de los mamíferos.
El cáncer también es consecuencia de mutaciones que liberan a las células de los
controles normales que actúan sobre su supervivencia, crecimiento y proliferación.
Como las células cancerosas suelen ser menos dependientes que las normales de las
señales de otras células, pueden sobrevivir, crecer y dividirse más que sus vecinas
normales, lo que da origen a tumores potencialmente fatales.
Las células de mamíferos solo se multiplicarán si son estimuladas a hacerlo por señales
extracelulares denominadas mitógenos, producidas por otras células
Descargado por Mariana Hernandez (mh3801827@gmail.com) Kiara Kanackowicz
Encuentra más documentos en www.udocz.com
También podría gustarte
- Rejuvenecer Con El Plasma Sanguíneo De Los JóvenesDe EverandRejuvenecer Con El Plasma Sanguíneo De Los JóvenesCalificación: 5 de 5 estrellas5/5 (1)
- C17 - Ciclo Celular y MitosisDocumento8 páginasC17 - Ciclo Celular y MitosisFrank FerreiraAún no hay calificaciones
- Tarea de Reprodución CelularDocumento8 páginasTarea de Reprodución CelularazlacvdAún no hay calificaciones
- Paper de Ciclo Celular.Documento16 páginasPaper de Ciclo Celular.Jean Carlos Hernandez BeltranAún no hay calificaciones
- Proliferacion CelularDocumento9 páginasProliferacion CelularruizAún no hay calificaciones
- 12.ciclo CelularDocumento26 páginas12.ciclo CelularAgostina de MaríaAún no hay calificaciones
- Ensayo Ciclo Celular (29.01)Documento8 páginasEnsayo Ciclo Celular (29.01)Diana VélezAún no hay calificaciones
- Ciclo CelularDocumento11 páginasCiclo CelularEdward Balvin SincheAún no hay calificaciones
- Qué Es El Ciclo CelularDocumento5 páginasQué Es El Ciclo CelularSu SaucedoAún no hay calificaciones
- Resumen 2Documento4 páginasResumen 2xochitl palma naranjoAún no hay calificaciones
- Resumen de Bio Uba Xxi 2ºpDocumento26 páginasResumen de Bio Uba Xxi 2ºpFiorella GurziAún no hay calificaciones
- Biologia Molecular Ciclo CelularDocumento35 páginasBiologia Molecular Ciclo CelularvladymirAún no hay calificaciones
- Ciclo Celular Guia 1Documento9 páginasCiclo Celular Guia 1Belen MercadoAún no hay calificaciones
- Resumen de Bio Uba Xxi 2PDocumento26 páginasResumen de Bio Uba Xxi 2PTere TupperwareAún no hay calificaciones
- Ciclo CelularDocumento161 páginasCiclo CelularAlfonso MoxicaAún no hay calificaciones
- Ciclo Celulary ReplicacionDocumento14 páginasCiclo Celulary ReplicacionVero CvAún no hay calificaciones
- Ciclo CelularDocumento38 páginasCiclo CelularNatália LarsenAún no hay calificaciones
- Ploriferacion CelularDocumento6 páginasPloriferacion CelularRoxana ErazoAún no hay calificaciones
- BC 2 NecroticaenfmedDocumento6 páginasBC 2 NecroticaenfmedCamilaAún no hay calificaciones
- Apunte 7Documento7 páginasApunte 7Lara ReevesAún no hay calificaciones
- Ciclo CelularDocumento24 páginasCiclo CelularEmily MorenoAún no hay calificaciones
- BC 2 Ciclo Celular NecroticaenfmedDocumento6 páginasBC 2 Ciclo Celular NecroticaenfmedCasa LimpiezaAún no hay calificaciones
- ExposiciónDocumento14 páginasExposiciónCarvajal MarlonAún no hay calificaciones
- ACTIVIDADDocumento3 páginasACTIVIDADAlejandra100% (1)
- Bloc de Notas Sin Ti Tulo 2 240705 Downloable 1039797Documento30 páginasBloc de Notas Sin Ti Tulo 2 240705 Downloable 1039797berta riquelmeAún no hay calificaciones
- Ciclo CelularDocumento37 páginasCiclo CelularAurelia Gonzales Calle100% (2)
- Ciclo Celular.Documento4 páginasCiclo Celular.gigi mininaAún no hay calificaciones
- Tema 1 Ciclo CelularDocumento36 páginasTema 1 Ciclo CelularKevin Gustavo Zapata SilvaAún no hay calificaciones
- Control Del Ciclo CelularDocumento2 páginasControl Del Ciclo Celularsofia lopezAún no hay calificaciones
- Ciclo Celular ResumenDocumento15 páginasCiclo Celular ResumenDaniela Rios ArenasAún no hay calificaciones
- Clase 19 Ciclo CelularDocumento38 páginasClase 19 Ciclo CelularEssentia KegAún no hay calificaciones
- Unidad 7Documento9 páginasUnidad 7MelAún no hay calificaciones
- AFPD7 Preguntas GuíaDocumento19 páginasAFPD7 Preguntas GuíaARIANA VALERIA HUALLPA GUTIERREZAún no hay calificaciones
- Control Del Ciclo Celular y MeiosisDocumento4 páginasControl Del Ciclo Celular y MeiosisLaura Mariana Beltran MoralesAún no hay calificaciones
- Semana 12 Ciclo Celular y MitosisDocumento18 páginasSemana 12 Ciclo Celular y MitosisShantal Ponce JáureguiAún no hay calificaciones
- Biología ExposiciónDocumento11 páginasBiología ExposiciónVero GuañunaAún no hay calificaciones
- BIOLOGIADocumento20 páginasBIOLOGIAArturo Alejandro TorresAún no hay calificaciones
- Instituto Tecnologico Del Valle de OaxacaDocumento14 páginasInstituto Tecnologico Del Valle de Oaxacal22920063Aún no hay calificaciones
- Unidad 05 Ciclo Ii GeneticaDocumento18 páginasUnidad 05 Ciclo Ii GeneticaJesus Albertho CuriAún no hay calificaciones
- Ciclo Celular y Duplicación Del AdnDocumento60 páginasCiclo Celular y Duplicación Del AdnDonald MartinAún no hay calificaciones
- Partes de La CélulaDocumento8 páginasPartes de La CélulaMonica Alejandra Favela HuizarAún no hay calificaciones
- Ciclo CelularDocumento26 páginasCiclo CelularMicaela GutiérrezAún no hay calificaciones
- Taller Ciclo Celular NuevoDocumento6 páginasTaller Ciclo Celular NuevoDaniela Galvis HernandezAún no hay calificaciones
- Ciclo CelularDocumento23 páginasCiclo CelularDiego Girón100% (2)
- Resumen de Puntos de ControlDocumento2 páginasResumen de Puntos de ControlMariam GómezAún no hay calificaciones
- Ciclo CelularDocumento23 páginasCiclo CelularOrtiz Alba AndreaAún no hay calificaciones
- Apuntes Tema 9 10Documento12 páginasApuntes Tema 9 10RosaAún no hay calificaciones
- Tema 10 - Ciclo Celular.Documento6 páginasTema 10 - Ciclo Celular.Saul TamayoAún no hay calificaciones
- Bio 13Documento31 páginasBio 13Natalie BorjaAún no hay calificaciones
- Resumen Del Ciclo CelularDocumento4 páginasResumen Del Ciclo CelularAnonymous A2DQ4aKWAún no hay calificaciones
- Ciclo CelularDocumento16 páginasCiclo CelulartripicksAún no hay calificaciones
- Ciclo CelularDocumento9 páginasCiclo CelularKent Junior Limas AyalaAún no hay calificaciones
- Ciclo Celular InterfaseDocumento3 páginasCiclo Celular InterfaseMaria Paz ValenciaAún no hay calificaciones
- SocializacionDocumento15 páginasSocializacioncelia rubioAún no hay calificaciones
- Clases 15-16 Ciclo Celular y MitosisDocumento93 páginasClases 15-16 Ciclo Celular y MitosisKAREN MONSERRAT FRANCO ACHARAún no hay calificaciones
- 4 A VideoDocumento12 páginas4 A VideomairaAún no hay calificaciones
- Tema 1 Ciclo CelularDocumento15 páginasTema 1 Ciclo CelularLuis SanchezAún no hay calificaciones
- Ciclo CelularDocumento3 páginasCiclo CelularROSALINO RUIZ MARTINEZAún no hay calificaciones
- Tarea Histología 15 de Dic.Documento45 páginasTarea Histología 15 de Dic.Andros CansecoAún no hay calificaciones
- Genética Del Cáncer - Grupo 4Documento18 páginasGenética Del Cáncer - Grupo 4Emely RoussAún no hay calificaciones
- Biología Molecular y Cáncer de PulmónDocumento4 páginasBiología Molecular y Cáncer de Pulmónissel morenoAún no hay calificaciones
- Reparación de Los TejidosDocumento63 páginasReparación de Los Tejidoskarlos0407Aún no hay calificaciones
- Ciclo Vital de La CélulaDocumento43 páginasCiclo Vital de La CélulaBRANS ARNOL GARCIA CABANILLASAún no hay calificaciones
- Biología Molecular Del CáncerDocumento72 páginasBiología Molecular Del CáncerCesar Arturo Sanchez LoaizaAún no hay calificaciones
- Protocolo VPHDocumento26 páginasProtocolo VPHClaudiaRojasAún no hay calificaciones
- Genes Del Cancer PDFDocumento26 páginasGenes Del Cancer PDFgabrielAún no hay calificaciones
- EnvejecimientoDocumento33 páginasEnvejecimientoAmelia GibajaAún no hay calificaciones
- HIPERACTINADocumento8 páginasHIPERACTINAAntonio Muñoz RomeroAún no hay calificaciones
- Resumen Biologia: Dimensiones de La CelulaDocumento71 páginasResumen Biologia: Dimensiones de La CelulaCamilaAún no hay calificaciones
- TESISDocumento37 páginasTESISJohn Cuyubamba Nuñez100% (1)
- Trabajo Citología PDFDocumento29 páginasTrabajo Citología PDFMiguel Angel Rodriguez VillaAún no hay calificaciones
- Evasión de Las Defensas Del AnfitriónDocumento4 páginasEvasión de Las Defensas Del AnfitriónNadiuska MolinaresAún no hay calificaciones
- Ciclo CelularDocumento14 páginasCiclo CelularMateo PazmiñoAún no hay calificaciones
- Caso Clinico Patologia Bucal PapilomaDocumento4 páginasCaso Clinico Patologia Bucal PapilomaDiana PalmaAún no hay calificaciones
- Apoptosis CelularDocumento48 páginasApoptosis CelularClara AlegríaAún no hay calificaciones
- E Tesis PDFDocumento316 páginasE Tesis PDFMARIA CAMILA VELASCO CASTAÑEDAAún no hay calificaciones
- Tema 19Documento4 páginasTema 19Marina CerezoAún no hay calificaciones
- 4 - Leucemia de Celulas PlasmaticasDocumento67 páginas4 - Leucemia de Celulas PlasmaticasMATIAS NICOLAS ALVAREZ CASTILLO0% (1)
- 2020 The Cell Cycle and Its Regulation ADocumento26 páginas2020 The Cell Cycle and Its Regulation ATOMAS DAVID CHICA LLAMASAún no hay calificaciones
- Poster Ciclo Celular Del Cancer Cervico UterinoDocumento1 páginaPoster Ciclo Celular Del Cancer Cervico UterinoAdriana Ramos TitoAún no hay calificaciones
- La Radiacion UltravioletaDocumento13 páginasLa Radiacion UltravioletaViviana RiveraAún no hay calificaciones
- Sesion 1 Modulo 5Documento10 páginasSesion 1 Modulo 5Valeria QuinteroAún no hay calificaciones
- Capitulo 51Documento59 páginasCapitulo 51apuntesmedicos2Aún no hay calificaciones
- Marcadores Del Cancer de MamaDocumento15 páginasMarcadores Del Cancer de MamaAlexis AlbánAún no hay calificaciones
- CUESTIONARIO II Patologia NEOPLASIADocumento2 páginasCUESTIONARIO II Patologia NEOPLASIAFerdinan erikson Gomez lipeAún no hay calificaciones
- Genes Supresores de TumoresDocumento4 páginasGenes Supresores de TumoresJesus Yampier Diaz ZeladaAún no hay calificaciones
- GenDocumento2 páginasGenKeyla Torrico SuarezAún no hay calificaciones
- Sulfato de Zinc EndovenosoDocumento26 páginasSulfato de Zinc EndovenosoVinicio Revelant100% (1)
- Examen Seminario CancerDocumento6 páginasExamen Seminario CancerMarbel Maydana MendietaAún no hay calificaciones