Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Eteres, Epòxidos y Sulfuros
Eteres, Epòxidos y Sulfuros
Cargado por
Pedro HernandezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Eteres, Epòxidos y Sulfuros
Eteres, Epòxidos y Sulfuros
Cargado por
Pedro HernandezCopyright:
Formatos disponibles
1
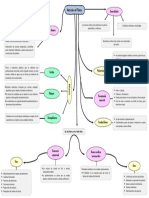
TEMA 17.- Eteres, epxidos y sulfuros. Propiedades generales.
Reacti vidad
R-O-R ter
epxido
R-S-R sulfuro
O
ETERES
R-O-R
Los teres son compuestos de frmula R-O-R en la que R y R pueden ser grupos alquilo o
arilo (fenilo). Los teres podran considerarse derivados del agua, por simple sustitucin
de los tomos de hidrgeno por grupos alquilo. En la siguiente figura se indican, a modo
de comparacin, las estructuras del agua, el metanol y el dimetil ter.
Alifticos ROR (los dos radicales alqulicos).
Aromticos ArOAr (los dos radicales arlicos).
Mixtos ROAr (un radical alqulico y otro arlico).
2
Compuestos incoloros
Puntos de ebullicin bajos (no forman enlace de H)
Solubilidad similar a la de los alcoholes
Muy poco reactivos
Propiedades fsicas
P.ebullicin Solubilidad
(g/100 ml, 25C)
OH
butanol
118C 7,9
O
dietilter
35C 7,5
pentano
36C 0,03
R O
R
H O
H
Densidad menor que el agua
Compuestos muy inertes: disolventes
Pueden ser explosivos
O
+ O
2 O
OOH
hidroxiperoxiter
Son muy usados en la preparacin de reacti vos de Grignard
R-X + Mg > R-MgX
Et
2
O
R Mg X
R
O
R
R
O
R
3
Tratamiento cido de alcoholes
A partir de alcoholes y alquenos
Sntesis de Williamson
Obtencin
La sntesis industrial del dimetil ter (CH
3
-O-CH
3
) y del dietil ter (CH
3
CH
2
-O-CH
2
CH
3
)
se efecta de este modo mediante calentamiento de los correspondientes alcoholes
en presencia de H
2
SO
4
. VISTO EN TEMA ANTERIOR
Sntesis de teres por deshidratacin de alcoholes
Uno de los mtodos ms empleados en la preparacin de teres implica el ataque SN2 de un
in alcxido sobre un halogenuro primario, este mtodo se le conoce como sntesis de
Williamson.
Sntesis de Williamson de teres
4
NaH
Na K
Reacciones de los teres con hidrcidos
Ruptura de teres
Reactividad
Los teres no se emplean como intermedios de sntesis debido a su inercia qumica.
Una de las pocas reacciones que sufren los teres es la ruptura del enlace C-O
cuando se calientan presencia de HBr o HI. Los productos de la reaccin son
bromuros o yoduros de alquilo. Por ejemplo, el dietil ter forma bromuro de etilo
cuando se trata con HBr.
5
EPOXIDOS
OEpxido (oxirano)
O
H
3
C
CH
3
H H
O
H
3
C
H
H CH
3
O
Oxido de etileno
Oxido de cis-2-buteno
Oxido de trans-2-buteno
6
Obtencin
Los epxidos, teres cclicos de tres eslabones, se pueden obtener por reaccin
de alquenos con peroxicidos (RCO
3
H).
O
CH
2
=CH
2
Ag
aire/
- Mediante la reaccin de alquenos con percidos
- Oxidacin del etileno con aire
Oxido de etileno
Como la reaccin de epoxidacin tiene lugar en un solo paso la
estereoqumica presente en el alqueno se retiene en el epxido. El cido
m-cloroperbenzoico, MCPBA) es el reactivo ms empleado en reacciones
de epoxidacin.
7
Reacti vidad
Reacciones de apertura
Los epxidos reaccionan con H
2
O en medio cido para formar glicoles con
estereoqumica anti. El mecanismo del proceso supone la protonacin del oxgeno del
anillo epoxdico seguida de un ataque nucleoflico de la molcula de agua.
Apertura de epxidos por tratamiento con agua
O
+ Nu
-
H
+
HO
Nu
Orientacin en la apertura de epxidos
Los epxidos simtricamente sustitutidos dan el mismo producto, tanto en la
apertura catalizada por cidos como en la apertura catalizada por bases. Sin
embargo,
un epxido asimtricamente sustituido da productos distintos si las condiciones de
apertura son diferentes. Por ejemplo, el 2-metil-1,2-epoxipropano reacciona con
etanol en medio cido para dar el 2-etoxi-2-metil-1-propanol. Sin embargo, cuando
la reaccion se efecta con etxido sdico en etanol se obtiene el 1-etoxi-2-metil-2-
propanol:
8
.
Apertura de epxidos con reacti vos organometlicos
Los reacti vos de Grignard y los reacti vos organolticos, atacan a los epxidos dando
lugar, despus de la hidrlisis de la mezcla de reaccin, a alcoholes.
SULFUROS (TIOETERES)
R-S-R
Obtencin
Se preparan por reacciones de desplazamiento (S
N
2), entre un deri vado halogenado
y un ion tiolato (RS
-
)
R-S
-
Na
+
+ R'-X
SN2
R-S-R'
También podría gustarte
- Resonancia QuimicaDocumento4 páginasResonancia QuimicaAifred RoblesAún no hay calificaciones
- SINTESIS de Williamson (Obtencion de Acido FenoxiaceticoDocumento16 páginasSINTESIS de Williamson (Obtencion de Acido Fenoxiacetico.:("*"BLacK BuLLeT"*"):.93% (29)
- Formulario NomenclaturaDocumento1 páginaFormulario NomenclaturaElia Uri100% (4)
- Cuestionario Repaso FarmacognosiaDocumento10 páginasCuestionario Repaso FarmacognosiaMishell Karolina Machado ValleAún no hay calificaciones
- Ensayo Sobre Las Mypes en El PeruDocumento4 páginasEnsayo Sobre Las Mypes en El Perulenioxx50% (2)
- Éter EtílicoDocumento5 páginasÉter EtílicoMaria Fernanda Tellez JaldinAún no hay calificaciones
- Clase - I - Alcoholes 1Documento35 páginasClase - I - Alcoholes 1joseAún no hay calificaciones
- Introducción a la química de los metales de transiciónDe EverandIntroducción a la química de los metales de transiciónAún no hay calificaciones
- Obtencion de Nitrato de AmonioDocumento3 páginasObtencion de Nitrato de AmonioLaimeOviedo67% (3)
- Hidrolisis Enzimatica de Los LipidosDocumento1 páginaHidrolisis Enzimatica de Los LipidoslisaddAún no hay calificaciones
- ÉTERESDocumento6 páginasÉTERESiviAún no hay calificaciones
- Informe N°1-Propiedades Fisicas y Quimicas de Alcoholes y FenolesDocumento20 páginasInforme N°1-Propiedades Fisicas y Quimicas de Alcoholes y FenolesJesus100% (3)
- 9 ArqueobacteriasDocumento36 páginas9 ArqueobacteriasKARINA SONIA PACHECO SOLISAún no hay calificaciones
- Eteres Epoxidos y Sulfuros - ByQDocumento28 páginasEteres Epoxidos y Sulfuros - ByQptreonito matinexAún no hay calificaciones
- Teoria 1 EteresDocumento8 páginasTeoria 1 EteresMary helen Molina siancasAún no hay calificaciones
- Clase - II - EteresDocumento38 páginasClase - II - EteresjoseAún no hay calificaciones
- Obtención Industrial de ÉteresDocumento13 páginasObtención Industrial de ÉteresLuis Angel100% (2)
- Clase - Ii - Eteres 1Documento25 páginasClase - Ii - Eteres 1Yuber DiazAún no hay calificaciones
- Practica de NerolinaDocumento12 páginasPractica de NerolinaIngrid100% (1)
- B NerolinaDocumento10 páginasB NerolinaDulce Goytia100% (1)
- Practica de Laboratorio 8Documento17 páginasPractica de Laboratorio 8ALDO CLEOCEL CURASMA LUCASAún no hay calificaciones
- Unidad 4. Compuestos Oxigenados 1Documento42 páginasUnidad 4. Compuestos Oxigenados 1Blanca Mariela Ccari CuentaAún no hay calificaciones
- Eteres, Sulfuros y EpóxidosDocumento21 páginasEteres, Sulfuros y EpóxidosVianyeli Dipre De La RosaAún no hay calificaciones
- Practica N°1 de Sintesis de EteresDocumento15 páginasPractica N°1 de Sintesis de EteresArturo OB67% (3)
- EteresDocumento30 páginasEteresmiino san100% (1)
- Alcoholes - y - Eteres 20-21Documento18 páginasAlcoholes - y - Eteres 20-21Manuel GordilloAún no hay calificaciones
- PRESENTACION DE Reacciones de Eteres y eDocumento40 páginasPRESENTACION DE Reacciones de Eteres y eJuan SevillanoAún no hay calificaciones
- AlcoholesDocumento22 páginasAlcoholesJunior Perez CorisAún no hay calificaciones
- Quimica Que Es El EterDocumento3 páginasQuimica Que Es El EterRolando RiosAún no hay calificaciones
- Tema 4Documento12 páginasTema 4liliAún no hay calificaciones
- ETERESDocumento8 páginasETERESLaura MontielAún no hay calificaciones
- Preparación de Los ÉteresDocumento3 páginasPreparación de Los Éteresfernanda100% (1)
- AlcoholesDocumento12 páginasAlcoholesAndy LezametaAún no hay calificaciones
- Química Orgánica Unidad 2Documento24 páginasQuímica Orgánica Unidad 2Amalfy Lised Cubillos Huaca100% (1)
- En Primera Instancia Es para Hacer Llegar Mis Saludos Cordiales Hacia SuDocumento10 páginasEn Primera Instancia Es para Hacer Llegar Mis Saludos Cordiales Hacia Susoloidx5758Aún no hay calificaciones
- AlcoholesDocumento13 páginasAlcoholesStefanni Marisol Irrazábal LeguizamónAún no hay calificaciones
- Alcoholes y Fenoles Acidos Carboxilicos y DerivadosDocumento51 páginasAlcoholes y Fenoles Acidos Carboxilicos y DerivadoskevinAún no hay calificaciones
- Exposición Química IDocumento6 páginasExposición Química Isebastian lunaAún no hay calificaciones
- AlcholesDocumento16 páginasAlcholesEduardo TafurAún no hay calificaciones
- Compuestos Orgánicos OxigenadosDocumento26 páginasCompuestos Orgánicos Oxigenadosmgza0203Aún no hay calificaciones
- Éteres y EpóxidosDocumento22 páginasÉteres y EpóxidosandreamargaritavillagAún no hay calificaciones
- Alcoholes, Expo de QuimicaDocumento30 páginasAlcoholes, Expo de QuimicaVIERHITG HOSHUA ACEVEDO LAVALLEAún no hay calificaciones
- Alcoholes, Fenoles PDFDocumento31 páginasAlcoholes, Fenoles PDFAnderson AntonAún no hay calificaciones
- AlcoholesDocumento8 páginasAlcoholesLiesel Gonzalez PerezAún no hay calificaciones
- ETERESDocumento5 páginasETERESVivianaPerdomo0% (1)
- Alcoholes y FenolesDocumento5 páginasAlcoholes y FenolesDavis MeraAún no hay calificaciones
- EteresDocumento17 páginasEteresKarla ZamoranoAún no hay calificaciones
- Éteres y EpóxidosDocumento19 páginasÉteres y EpóxidosPablo BarriosAún no hay calificaciones
- Alcoholes Fenoles y TiolesDocumento48 páginasAlcoholes Fenoles y TiolesLaura Mercado100% (2)
- Alcoholes 120621001144 Phpapp01Documento31 páginasAlcoholes 120621001144 Phpapp01Saby ChuanAún no hay calificaciones
- E Teres 2010Documento15 páginasE Teres 2010Eduardo SalinasAún no hay calificaciones
- Seminario Eteres y EpoxidosDocumento14 páginasSeminario Eteres y EpoxidosAxel MartinezAún no hay calificaciones
- Tema4 Eteres y EpoxidosDocumento16 páginasTema4 Eteres y EpoxidosGioSntoAún no hay calificaciones
- Alcohol EsDocumento5 páginasAlcohol EsPeluffoLuisAún no hay calificaciones
- 7 Éteres y Compuestos AzufradosDocumento43 páginas7 Éteres y Compuestos AzufradosAlejandra zamoraAún no hay calificaciones
- Capítulo 10-ÉteresDocumento22 páginasCapítulo 10-ÉteresOscarAún no hay calificaciones
- Quimica Organica Esteres y EteresDocumento24 páginasQuimica Organica Esteres y EteresTavo Racho100% (1)
- Teoria 3 EteresDocumento13 páginasTeoria 3 EteresMary helen Molina siancasAún no hay calificaciones
- ÉTERESDocumento3 páginasÉTERESGIAMPIERRE ANDRE FLORES FERNANDEZAún no hay calificaciones
- Eteres TeoriaDocumento12 páginasEteres TeoriaBrian WilliamsAún no hay calificaciones
- ETERESDocumento11 páginasETEREScatherine garcia mirandaAún no hay calificaciones
- Chapter 18 Mcmurry 2023Documento68 páginasChapter 18 Mcmurry 2023Luis LópezAún no hay calificaciones
- Clase FactorizaciónDocumento15 páginasClase FactorizaciónlenioxxAún no hay calificaciones
- Normas para La DiagramaciónDocumento3 páginasNormas para La DiagramaciónlenioxxAún no hay calificaciones
- Cultura TributariaDocumento33 páginasCultura TributarialenioxxAún no hay calificaciones
- Aplicaciones Del Momento de Inercia en La Ingenieria CivilDocumento4 páginasAplicaciones Del Momento de Inercia en La Ingenieria CivillenioxxAún no hay calificaciones
- Texto Expositivo Marca PaisDocumento5 páginasTexto Expositivo Marca PaislenioxxAún no hay calificaciones
- Informe de OndasDocumento25 páginasInforme de OndaslenioxxAún no hay calificaciones
- ALQUINOSDocumento2 páginasALQUINOSlenioxxAún no hay calificaciones
- La Revolucion AgricolaDocumento2 páginasLa Revolucion AgricolalenioxxAún no hay calificaciones
- ALQUINOSDocumento2 páginasALQUINOSlenioxxAún no hay calificaciones
- Introducción - Funciones TrigonométricasDocumento4 páginasIntroducción - Funciones TrigonométricaslenioxxAún no hay calificaciones
- Introducción - Factorización y Ecuaciones de Primer GradoDocumento3 páginasIntroducción - Factorización y Ecuaciones de Primer GradolenioxxAún no hay calificaciones
- Analisis Elemental Cualitativo de HalogenosDocumento13 páginasAnalisis Elemental Cualitativo de HalogenosEDWIN_JUGADOR80% (5)
- Lola Cuadernillo de TecnologiaDocumento2 páginasLola Cuadernillo de TecnologiaJavier Pérez FloresAún no hay calificaciones
- Síntesis de Hidróxido de CuDocumento3 páginasSíntesis de Hidróxido de CuAndrés Aurelijus JuradoAún no hay calificaciones
- Algoritmo Taquicardia Hipoperfusión Pediatria 2010Documento1 páginaAlgoritmo Taquicardia Hipoperfusión Pediatria 2010César AmanzoAún no hay calificaciones
- Familias de HerbicidasDocumento8 páginasFamilias de HerbicidasJuan Manuel Magdaleno TorresAún no hay calificaciones
- TIOLESDocumento8 páginasTIOLESAnahí Velín0% (1)
- Modelo de Diapositivas de Sustentacion UapDocumento22 páginasModelo de Diapositivas de Sustentacion UapPercy Diaz ChuquizutaAún no hay calificaciones
- AmikacinaDocumento9 páginasAmikacinaWalter Paucar Condori100% (1)
- Mecanismo de Toxicidad en Humanos EtanolDocumento6 páginasMecanismo de Toxicidad en Humanos EtanolPeña GutierrezAún no hay calificaciones
- Laboratorio 7 Deteccion de Intermediarios en Fermentacion Alcoholica Por LevadurasDocumento4 páginasLaboratorio 7 Deteccion de Intermediarios en Fermentacion Alcoholica Por LevadurasJonsito Alexander Caicedo Lopez100% (1)
- Estructura y Propiedades de La LecheDocumento26 páginasEstructura y Propiedades de La LecheRUBEN EDWIN OLAYA RUIZAún no hay calificaciones
- OPERONDocumento15 páginasOPERONGineth MaderaAún no hay calificaciones
- Instituto de Ciencias Naturales: Facultad de Medicina Veterinaria Y AgronomiaDocumento5 páginasInstituto de Ciencias Naturales: Facultad de Medicina Veterinaria Y AgronomiaAndrea Araya PachecoAún no hay calificaciones
- Nutricion Mineral en EquinosDocumento5 páginasNutricion Mineral en EquinosWilson Nieto Delgado0% (1)
- La Teoría de La Fuerza VitalDocumento2 páginasLa Teoría de La Fuerza VitalKarin Johanna Colombo100% (1)
- NR - 26 - 45-52 - 2 - 3 ES-desbloqueadoDocumento12 páginasNR - 26 - 45-52 - 2 - 3 ES-desbloqueadoDaniela Orellana ArnezAún no hay calificaciones
- Estructura DNADocumento8 páginasEstructura DNAsonia.alehdezAún no hay calificaciones
- La Química de La Vida PDFDocumento37 páginasLa Química de La Vida PDFoutonnet100% (5)
- Compuestos Bioactivos Con Potencial Uso en El Desarrollo de Alimentos Funcionales o Nutracéuticos (PDFDrive)Documento66 páginasCompuestos Bioactivos Con Potencial Uso en El Desarrollo de Alimentos Funcionales o Nutracéuticos (PDFDrive)alberto bragaAún no hay calificaciones
- Materiales PlasticosDocumento1 páginaMateriales PlasticosMAYARA RODRIGUES OLIVERAAún no hay calificaciones
- PRACTICA N7 Determinacion de Acidez en AceitesDocumento3 páginasPRACTICA N7 Determinacion de Acidez en AceitesRoxana Canaza100% (1)
- Los Hidrocarburos y Su UtilidadDocumento15 páginasLos Hidrocarburos y Su Utilidadmarielis nava100% (1)
- Informe Laboratorio Virtual.Documento4 páginasInforme Laboratorio Virtual.Isa Little BirdAún no hay calificaciones
- 7 Solucio N SteinerDocumento31 páginas7 Solucio N Steinermariela gonzalezAún no hay calificaciones