Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Leucopenia y Linfocitopenia
Cargado por
api-3737581Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Leucopenia y Linfocitopenia
Cargado por
api-3737581Copyright:
Formatos disponibles
MSD, Publicaciones, Manual Merck
Póximamente
RENAAL.msd.es
Últimas Noticias
Salud y Bienestar Home
Enfermedades Home
Si usted es un profesional de los medios de comunicación, pulse aquí para ver las últimas informaciones sobre
MSD, sus actividades y sus productos.
Home
Manual 12 de Octubre 4ª edición
Medicina Basada en la Evidencia
Manual Merck
10ª edición
Manual Merck Hogar
Vademécum
Home
Alopecia
Artrosis
Asma
Enfermedades del Corazón
Glaucoma
Hiperplasia Benigna de Próstata
Hipertensión
Migraña
Osteoporosis
SIDA
Home
Generalidades
Cardiología
Neumología
Alergología
Reumatología
Enfermedades Infecciosas
Gastroenterología
Nefrología
Trastornos Metabólicos
Endocrinología y Nutrición
Hematología y Oncología
Neurología
Psiquiatría
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (1 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
Apéndices
135 / LEUCOPENIA Y LINFOCITOPENIA
LEUCOPENIA
Reducción del número de leucocitos circulantes por debajo de
4.000/ml.
La leucopenia suele caracterizarse por una disminución del número
de neutrófilos sanguíneos, aunque el descenso del número de
linfocitos, monocitos, eosinófilos o basófilos también puede
contribuir a la disminución del recuento celular total. La neutropenia
que se acompaña de monocitopenia y linfocitopenia constituye, a
menudo, un trastorno más grave que la neutropenia aislada.
NEUTROPENIA
(Granulocitopenia, agranulocitosis)
Reducción del recuento de neutrófilos (granulocitos) sanguíneos,
que conlleva, con frecuencia, una mayor susceptibilidad a las
infecciones bacterianas y fúngicas.
Los individuos de raza negra presentan recuentos de neutrófilos
algo inferiores (valor inferior de la normalidad, alrededor de
1.200/ml), cuando se comparan con la población blanca
(>1.500/ml). La neutropenia puede clasificarse según el recuento de
neutrófilos (leucocitos totales 3 % neutrófilos y células en banda) y
el riesgo relativo de infección: leve (1.000-1.500/ml), moderada
(500-1.000/ml) o grave (<500/ml). La neutropenia aguda grave
causada por una alteración en la producción de neutrófilos
representa a menudo una situación de riesgo vital en los pacientes
inmunocomprometidos (v. cap. 151).
Etiología
La neutropenia aguda (presente durante unos pocos días) suele
desarrollarse cuando la utilización de neutrófilos es rápida y su
producción está alterada. La neutropenia crónica (perdura meses o
años) es consecuencia, generalmente, de una disminución de la
síntesis o de un secuestro esplénico excesivo de neutrófilos. La
neutropenia puede clasificarse dependiendo de si es secundaria a
factores extrínsecos a las células mieloides medulares o de si
existe un defecto intrínseco en los progenitores mieloides (v. tabla
135-1).
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (2 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
Neutropenia secundaria. Los fármacos son una de las causas
más habituales de neutropenia. La incidencia de neutropenia
inducida por fármacos se incrementa de manera notable con la
edad; sólo el 10% de los casos aparecen en niños y adultos
jóvenes, observándose más del 50% en adultos.
La neutropenia inducida por fármacos responde a varios
mecanismos subyacentes (reacciones inmunitarias, tóxicas,
idiosincrásicas o de hipersensibilidad) y debe distinguirse de la
neutropenia grave que ocurre de forma previsible tras dosis
elevadas de fármacos antineoplásicos citorreductores o radioterapia
(v. más adelante) y de la producida por infecciones víricas (v. más
adelante). La quimioterapia citotóxica induce neutropenia como
consecuencia de la alta tasa proliferativa de los precursores
neutrofílicos y del rápido recambio de los neutrófilos sanguíneos.
Se cree que la neutropenia mediada por mecanismos inmunitarios,
que generalmente persiste durante una semana, se debe a
fármacos que actúan como haptenos y estimulan la formación de
anticuerpos. Puede surgir cuando se emplea aminopirina,
propiltiouracilo y penicilina. Otros fármacos (p. ej., fenotiacinas)
pueden provocar neutropenia cuando se administran en cantidades
tóxicas. Por su parte, las reacciones idiosincrásicas son
impredecibles en cuanto a la dosis o la duración del empleo y
tienen lugar con fármacos como el cloranfenicol. Las reacciones de
hipersensibilidad aguda (p. ej., las producidas por fenitoína o
fenobarbital) pueden durar unos pocos días, pero las de
hipersensibilidad crónica pueden alargarse durante meses o años.
Las reacciones de hipersensibilidad son raras y, en ocasiones, se
relacionan con metabolitos (generados en el hígado) de los
anticonvulsivantes aromáticos, es decir, fenitoína o fenobarbital. La
neutropenia inducida por hipersensibilidad se asocia a menudo a
fiebre, exantema, adenopatías, hepatitis, nefritis, neumonitis o
anemia aplásica. Algunas veces, esta neutropenia inducida por
fármacos puede ser asintomática a pesar de la neutropenia, sobre
todo en los pacientes en que se controlan regularmente los
recuentos leucocitarios durante el tratamiento farmacológico.
La disminución de la producción de neutrófilos es una característica
frecuente y generalmente precoz de la anemia megaloblástica
provocada por déficit de vitamina B12 o folato, si bien suele
acompañarse de anemia macrocítica y, en ocasiones, de
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (3 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
trombocitopenia leve. El alcohol puede inhibir la respuesta de la
médula ósea a la infección cuando los pacientes desarrollan
enfermedades como la neumonía neumocócica.
La infiltración y la sustitución de la médula ósea por células
malignas de leucemias, mielomas, linfomas o tumores sólidos
metastásicos (p. ej., mama, próstata) pueden deteriorar la
producción de neutrófilos. La mielofibrosis inducida por tumores
puede intensificar aún más la neutropenia. La mielofibrosis también
puede ser secundaria a infecciones granulomatosas, enfermedad
de Gaucher y radioterapia. La neutropenia puede deberse a la
insuficiencia de la médula ósea, como se observa en determinadas
enfermedades raras (p. ej., síndrome de Schwachman-Diamond,
hipoplasia cartílago-pelo, disqueratosis congénita, glucogenosis tipo
IB). Asimismo, la neutropenia es una característica destacada de la
mielodisplasia y se acompaña de rasgos megaloblastoides en la
médula ósea (v. cap. 130). La esplenomegalia de cualquier
etiología (v. cap. 141) puede originar una neutropenia moderada,
trombocitopenia y anemia.
Las infecciones víricas suelen acompañarse de neutropenia
transitoria (p. ej., fases iniciales de la mononucleosis infecciosa) y la
sepsis es una causa particularmente grave de neutropenia. La
neutropenia que se asocia a enfermedades víricas habituales de la
infancia ocurre durante los primeros 2 d de la enfermedad y puede
persistir durante 3-8 d. Suele corresponder con un período de
viremia aguda y se relaciona con la redistribución de los neutrófilos
inducida por el virus desde el compartimiento circulante al marginal.
El secuestro de neutrófilos puede producirse tras lesiones tisulares
por virus. Una neutropenia moderada a intensa también puede ser
consecuencia de una amplia variedad de infecciones (v. tabla
135-2).
La infección por el VIH se acompaña a menudo de neutropenia
crónica, resultado de un deterioro en la producción de neutrófilos y
de una destrucción acelerada de éstos por anticuerpos (v. cap.
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (4 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
145). Las neutropenias autoinmunitarias pueden deberse a la
presencia de anticuerpos antineutrofílicos circulantes y pueden
aparecer aisladas o asociadas a otras enfermedades.
Neutropenia producida por defectos intrínsecos en las células
mieloides o en sus precursores. Este tipo de neutropenia es
infrecuente. La neutropenia cíclica es un raro trastorno
granulocitopoyético congénito que puede heredarse de forma
autosómica dominante y que se caracteriza por oscilaciones
irregulares y periódicas en el número de neutrófilos periféricos. El
período oscilatorio medio es de 21 ± 3 d.
La neutropenia congénita grave (síndrome de Kostmann) es una
enfermedad rara que aparece esporádicamente en Estados Unidos
y que se caracteriza por una detención de la maduración mieloide
en el estado promielocítico de la médula ósea, provocando un
recuento absoluto de neutrófilos inferior a 200/ml.
La neutropenia idiopática crónica representa un grupo de trastornos
infrecuentes, escasamente comprendidos, que afectan a las células
progenitoras condicionadas de las series mieloides y que cursan
con cifras normales de precursores eritrocitarios y plaquetarios sin
esplenomegalia. El grado de susceptibilidad a la infección es
prácticamente proporcional al recuento de neutrófilos sanguíneos
en los pacientes con recuentos absolutos de neutrófilos menores de
500/ml.
Síntomas y signos
Algunos pacientes con neutropenia crónica y recuentos de
neutrófilos inferiores a 200/ml no experimentan infecciones graves,
debido probablemente a que el resto del sistema inmunitario
permanece intacto. No obstante, es habitual que los pacientes con
neutropenia cíclica o neutropenia congénita grave presenten
úlceras orales, estomatitis y faringitis asociadas a adenopatías
durante los estados neutropénicos crónicos graves. A menudo
aparecen neumonías y periodontitis crónica.
Los pacientes con neutropenia secundaria a trastornos adquiridos
de la producción originados por neoplasias o quimioterapia tienen
más probabilidades de desarrollar infecciones bacterianas
importantes, ya que presentan un compromiso global de su sistema
inmunitario. La integridad de la piel y las mucosas, el aporte
vascular a los tejidos y el estado nutricional del paciente también
influyen en el riesgo de padecer infecciones en caso de neutropenia
aguda. Los pacientes con infecciones piógenas tienden a tener
fiebre superior a 38,3 ºC. Las infecciones piógenas que aparecen
con mayor frecuencia en los pacientes con neutropenia intensa son
celulitis cutáneas, abscesos hepáticos, forunculosis, neumonías y
septicemias. También surgen con frecuencia estomatitis, gingivitis,
inflamaciones perirrectales, colitis, sinusitis y otitis medias.
Diagnóstico
El diagnóstico de neutropenia suele sospecharse en un paciente
con infecciones frecuentes o graves y se confirma al comprobar
recuentos sanguíneos bajos. Posteriormente debe buscarse la
etiología y evaluar el riesgo de infección. La neutropenia absoluta
aislada presenta un número limitado de causas.
Durante la exploración física debe prestarse atención especial a los
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (5 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
lugares más frecuentes e importantes de infección: las superficies
mucosas, como el tracto alimentario (encías, faringe), donde las
lesiones inducidas por quimioterapia pueden permitir la invasión por
microorganismos colonizantes, y la piel, donde los catéteres
vasculares pueden actuar como puerta de entrada de la infección.
Otros sitios habituales de infección son los pulmones, el peritoneo,
los puntos de venipunción y de aspirado de la médula ósea y las
uñas de los dedos de las manos.
La duración y la intensidad de la neutropenia influyen en gran
medida en la extensión de la evaluación de laboratorio.
Neutropenia aguda. La evaluación de una sospecha de infección
en caso de neutropenia aguda resulta especialmente difícil porque
los signos típicos de inflamación pueden estar notablemente
disminuidos o ausentes. Deben obtenerse, al menos, dos tandas de
hemocultivos para bacterias y hongos en todos los pacientes
febriles. Si existe un catéter i.v. permanente, deben obtenerse
cultivos de la luz y de una vena periférica. Debe evaluarse la
secreción persistente o crónica en busca de micobacterias atípicas
y deben aspirarse o biopsiarse las lesiones cutáneas sospechosas
para citología y cultivo. Los urocultivos están indicados si están
presentes síntomas o signos de ITU. Si existe diarrea, deben
examinarse las heces en busca de patógenos bacterianos entéricos
y toxinas de Clostridium difficile.
Las radiografías de senos faciales pueden ser útiles si hay
síntomas o signos de sinusitis (p. ej., cefalea, tumefacción facial o
rinorrea).
Neutropenia crónica. Deben realizarse recuentos leucocitarios con
fórmula diferencial tres veces a la semana durante 6 sem en los
pacientes con neutropenia crónica desde la infancia y antecedentes
de fiebre recidivante y gingivitis crónica para evaluar la periodicidad
sugestiva de neutropenia cíclica. El aspirado y la biopsia de la
médula ósea pueden ayudar en el diagnóstico y la valoración de la
celularidad. Los estudios medulares adicionales (p. ej., análisis
citogenéticos, tinciones especiales para detectar leucemias y otras
enfermedades malignas) deben efectuarse en los pacientes con
sospecha de defectos intrínsecos en las células mieloides o sus
precursores y en los pacientes con sospecha de neoplasias. La
selección de otras pruebas de laboratorio está determinada por la
duración y la gravedad de la neutropenia y por los hallazgos de la
exploración física.
Los anticuerpos antineutrofílicos se asocian a la neutropenia
inmunitaria. Se han empleado diversos análisis de anticuerpos
frente a neutrófilos para estudiar a los pacientes con sospecha de
neutropenia autoinmunitaria. Estos análisis miden los anticuerpos
directamente en los neutrófilos o indirectamente en el suero de los
pacientes. Su especificidad y sensibilidad no están bien definidas.
Tratamiento
Neutropenia aguda. El tratamiento de la neutropenia transitoria
adquirida que se asocia de forma característica a neoplasias,
quimioterapia mielodepresora (v. cap. 144) o tratamiento
inmunodepresor es diferente del de las formas crónicas o
congénitas de neutropenia. Los pacientes que padecen una
infección suelen debutar únicamente con fiebre. Las infecciones
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (6 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
son la principal causa de fallecimiento en estos pacientes, cuyo
abordaje requiere, por tanto, un elevado índice de sospecha. La
identificación y el tratamiento precoz de las infecciones puede
salvar la vida del paciente. En caso de sospechar que la
neutropenia aguda está inducida por fármacos, debe detenerse la
administración de todos los medicamentos potencialmente nocivos
de forma inmediata.
El empleo empírico de antibióticos de amplio espectro sigue siendo
el pilar fundamental del tratamiento inicial en los pacientes
neutropénicos con fiebre aguda. Se debe suponer que estos
pacientes presentan infecciones bacterianas graves y se les debe
administrar con prontitud antibióticos de amplio espectro,
generalmente por vía i.v. y en dosis máximas, mientras se realizan
los estudios diagnósticos oportunos. En la mayoría de las
ocasiones, los catéteres vasculares permanentes pueden
mantenerse en su lugar, incluso si se sospecha o se confirma una
bacteriemia, pero deben retirarse tan pronto como sea posible. Los
estafilococos coagulasa negativos y el Staphylococcus aureus son
las bacterias que provocan infecciones relacionadas con los
catéteres con mayor frecuencia. En tanto que las infecciones
producidas por estafilococos coagulasa negativos suelen responder
bien al tratamiento antimicrobiano, las infecciones asociadas a S.
aureus, Bacillus sp., Corynebacterium sp. o Candida sp. requieren
generalmente la retirada del catéter y tratamiento antibiótico.
La selección de una pauta para un determinado paciente debe
basarse en el conocimiento de la susceptibilidad antimicrobiana de
los microorganismos patógenos que predominan en cada
institución. La toxicidad potencial de la pauta también debe tenerse
en cuenta cuando se inicia el tratamiento. La tabla 135-3 muestra
tres protocolos disponibles.
Dado el riesgo de colonización y posible infección posterior con
microorganismos resistentes, debe desaconsejarse la inclusión
rutinaria e indiscriminada de vancomicina como tratamiento
antimicrobiano empírico inicial de la fiebre en los pacientes
neutropénicos. Si los cultivos son positivos, debe ajustarse el
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (7 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
tratamiento antibiótico según la sensibilidad de los microorganismos
y suele mantenerse durante, al menos, 7-10 d. Si el paciente queda
afebril con rapidez en las primeras 72 h, debe continuarse con los
antibióticos durante, al menos, 7 d y hasta que desaparezcan los
síntomas y signos significativos de infección. Aunque el tratamiento
antibiótico suele mantenerse hasta que el recuento de neutrófilos es
superior a 500/ml, puede plantearse la suspensión de la cobertura
antimicrobiana en pacientes seleccionados, sobre todo en aquellos
que presentan una neutropenia prolongada y en quienes han
desaparecido los signos y síntomas de inflamación.
La fiebre que no se resuelve en las primeras 72 h a pesar del
tratamiento antibiótico de amplio espectro sugiere un origen no
bacteriano, una infección con bacterias resistentes a la pauta
empírica elegida, una sobreinfección con una segunda especie
bacteriana, niveles plasmáticos o tisulares inadecuados de los
antibióticos o una infección localizada en un área vascular (p. ej., un
absceso). Los pacientes neutropénicos con fiebre deben
reevaluarse de manera rigurosa al cuarto o quinto día. Si el
paciente va bien desde el punto de vista clínico, puede mantenerse
el régimen antibiótico inicial; en caso de deterioro de la situación
clínica, debe modificarse. En numerosas situaciones está justificada
la adición empírica de vancomicina. Las infecciones fúngicas son
una causa significativa de fiebre persistente en los pacientes
neutropénicos, por lo que debe añadirse tratamiento empírico con
anfotericina B en el caso de que la fiebre no responda en 7 d al
tratamiento antibiótico de amplio espectro. Si no se consigue que el
paciente quede afebril tras 3 sem de tratamiento antibiótico
empírico, incluidas 2 sem con anfotericina B, debe plantearse la
suspensión de todos los fármacos antimicrobianos y reevaluarse el
origen de la fiebre.
El papel de la profilaxis antibiótica en los pacientes
neutropénicos no febriles sigue siendo motivo de controversia. La
trimetoprima-sulfametoxazol (TMP-SMX) es eficaz en la prevención
de la neumonía por Pneumocystis carinii en los pacientes
neutropénicos y no neutropénicos con deterioro de la inmunidad
celular. Además, el TMP-SMX puede reducir la frecuencia de
infecciones bacterianas en los pacientes que van a estar
intensamente neutropénicos durante más de una semana. Las
desventajas de la profilaxis con TMP-SMX incluyen sus efectos
secundarios adversos, la potencial mielodepresión y la aparición de
bacterias resistentes y de candidiasis oral. La profilaxis antifúngica
con anfotericina B o fluconazol también se ha evaluado en
pacientes neutropénicos con riesgo elevado de desarrollar
infecciones por hongos (p. ej., tras trasplante de médula ósea). No
obstante, la profilaxis antifúngica sistémica no se recomienda como
componente rutinario del tratamiento de los pacientes
neutropénicos.
La estimulación de la médula ósea con corticoides, andrógenos y
vitaminas para que produzca más neutrófilos no se ha demostrado
útil. Dos factores de crecimiento (citoquinas), el factor estimulante
de colonias de granulocitos (G-CSF) y el factor estimulante de
colonias de granulocitos y macrófagos (GM-CSF), se han utilizado
ampliamente para prevenir la fiebre y las infecciones en los
pacientes con neutropenia grave (p. ej., tras trasplante de médula
ósea y quimioterapia antineoplásica intensiva). La terapia con
citoquinas es cara; sin embargo, si el riesgo de neutropenia febril
es, como mínimo, del 30%, está justificado el coste del G-CSF. En
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (8 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
general, la mayor parte de los beneficios clínicos se producen
cuando se administra el G-CSF alrededor de 24 h después de
concluir la quimioterapia. Dosis de 5 mg/kg/d por vía s.c. suelen
resultar eficaces. El G-CSF y el GM-CSF aceleran la recuperación
del recuento de neutrófilos a más de 500/ml en los pacientes que
van a someterse a un trasplante autólogo de médula ósea o a
quimioterapia intensiva.
Los enjuagues con suero salino o peróxido de hidrógeno cada
pocas horas, los comprimidos anestésicos (benzocaína, 15 mg
cada 3-4 h) o los colutorios con clorhexidina (solución al 1%)
pueden aliviar las molestias que conllevan las úlceras orofaríngeas.
La candidiasis oral se trata con lavados bucales con nistatina
(400.000-600.000 U 4/d). Puede requerirse una dieta semisólida o
líquida durante las mucositis agudas.
Neutropenia crónica. La producción de neutrófilos en la
neutropenia congénita, cíclica e idiopática puede mejorarse
mediante la administración de G-CSF, 3-10 mg/kg/d por vía s.c.
Esta terapia está indicada en los pacientes sin úlceras bucales ni
otros tipos de inflamación orofaríngea, fiebre, celulitis u otras
infecciones bacterianas documentadas. Los beneficios son
sostenidos y los pacientes pueden mantenerse con G-CSF a diario
o a días alternos durante meses o años sin perder eficacia. El
tratamiento prolongado con G-CSF también se ha utilizado para
prevenir la neutropenia en otras situaciones, como mielodisplasia,
VIH y SIDA y enfermedades autoinmunitarias. En general, se
incrementa el recuento de neutrófilos, si bien los beneficios clínicos
de este tratamiento están menos claros, sobre todo en los
pacientes que no presentan una neutropenia grave. Los pacientes
con neutropenia provocada por una reacción farmacológica
idiosincrásica también pueden beneficiarse del G-CSF,
especialmente si se prevé una recuperación lenta. No obstante,
hasta ahora sólo se han comunicado ensayos no controlados en
esta última circunstancia.
En algunos pacientes con recambio acelerado de neutrófilos
originado por enfermedades autoinmunitarias, los corticoides
(generalmente prednisona, 0,5-1,0 mg/kg/d v.o.) mejoran el
recuento de neutrófilos sanguíneos. Esta mejoría puede
mantenerse con terapia en días alternos.
La esplenectomía eleva el recuento de neutrófilos en determinados
pacientes con esplenomegalia y secuestro esplénico de neutrófilos
(p. ej., síndrome de Felty, leucemia de células peludas). Sin
embargo, debe reservarse para los pacientes con neutropenia
grave (es decir, <500/ml) y problemas infecciosos de consideración,
ya que predispone al paciente a padecer infecciones por
microorganismos encapsulados (v. cap. 141).
LINFOCITOPENIA
Recuento total de linfocitos inferior a 1.000/ml en adultos o a
3.000/ml en niños menores de 2 años.
El recuento normal de linfocitos en adultos es de 1.000-4.800/ml y
en niños menores de 2 años de 3.000-9.500/ml. A la edad de 6
años, el límite inferior de la normalidad es 1.500/ml. Prácticamente
el 65% de las células T sanguíneas son células T CD4+
(cooperadoras). La mayoría de los pacientes con linfocitopenia
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (9 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
muestran una reducción en el número absoluto de células T, sobre
todo en el número de células T CD4+. La cantidad media de células
T CD4+ en la sangre de un adulto es de 1.100/ml (intervalo normal,
300-1.300/ml) y el promedio de células del otro subgrupo
importante de células T, las células T CD8+ (supresoras), es de
600/ml (intervalo normal, 100-900/ml).
Etiología
La linfocitopenia hereditaria puede asociarse a
inmunodeficiencias hereditarias (v. tabla 135-4 y también cap. 147),
que pueden presentar una alteración cuantitativa o cualitativa en las
células progenitoras, la cual provoca una linfocitopoyesis ineficaz.
La linfocitopenia que se relaciona con otras causas, como el
síndrome de Wiskott-Aldrich, puede ser resultado de una
destrucción acelerada de células T. Un mecanismo similar está
presente en los pacientes con deficiencia de adenosina deaminasa
y de purina-nucleósido-fosforilasa.
La linfocitopenia adquirida hace referencia a los síndromes que
se asocian a reducción de los linfocitos sanguíneos sin ser
secundarios a enfermedades hereditarias. El SIDA es la
enfermedad infecciosa que se asocia con mayor frecuencia a
linfocitopenia, la cual se origina por la destrucción de las células T
CD4+ infectadas con el VIH (v. también cap. 145). La linfocitopenia
también puede reflejar un deterioro en la síntesis y la proliferación
de linfocitos como consecuencia de la destrucción de la arquitectura
tímica o linfoide normal. Otras enfermedades bacterianas y víricas
pueden cursar con linfocitopenia. En algunas situaciones de viremia
aguda, los linfocitos pueden estar sometidos a una destrucción
acelerada por infección activa con el virus, pueden estar atrapados
en el bazo o los ganglios linfáticos o pueden migrar al tracto
respiratorio.
La linfocitopenia yatrógena se debe a quimioterapia citotóxica,
radioterapia y administración de globulina antilinfocítica. El
tratamiento prolongado de los pacientes psoriásicos con psoraleno
y radiación ultravioleta puede destruir las células T. Los corticoides
pueden provocar linfopenia al inducir destrucción celular.
Las enfermedades sistémicas que se asocian a autoinmunidad (p.
ej., LES, AR, miastenia grave) pueden desencadenar linfocitopenia.
Trastornos como la enteropatía pierdeproteínas también pueden
provocar un agotamiento de los linfocitos.
Síntomas, signos y diagnóstico
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (10 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
La linfocitopenia, por sí misma, generalmente no produce síntomas
y suele detectarse durante el diagnóstico de otras enfermedades,
sobre todo de infecciones víricas, fúngicas o parasitarias
recidivantes. Los recuentos de linfocitos confirman la presencia de
linfocitopenia. Las subpoblaciones de linfocitos pueden
determinarse mediante citometría de flujo con multiparámetros, que
utiliza el patrón de expresión antigénica para clasificar y
caracterizar estas células.
Los pacientes linfocitopénicos padecen infecciones recidivantes,
muestran a menudo respuestas inusuales frente a agentes
infecciosos habitualmente benignos o desarrollan infecciones por
microorganismos infrecuentes. Las neumonías por Pneumocystis
carinii, citomegalovirus, sarampión o varicela sugieren la existencia
de una posible inmunodeficiencia; no es raro que la neumonitis
producida por cualquiera de estas infecciones sea mortal. Estos
pacientes también presentan una mayor incidencia de neoplasias y
enfermedades autoinmunitarias y pueden tener ausencia o
disminución de las amígdalas o los ganglios linfáticos, lo que indica
inmunodeficiencia celular; alteraciones cutáneas, como alopecia,
eccema, pioderma o telangiectasias; datos sugestivos de
enfermedad hematológica, como palidez, petequias, ictericia o
úlceras orales, así como adenopatías generalizadas y
esplenomegalia, lo que puede indicar enfermedad por el VIH.
El 80% de los pacientes con inmunodeficiencia primaria también
tienen deficiencia de anticuerpos, por lo que las pruebas de función
de anticuerpos y la determinación de los niveles de
inmunoglobulinas son apropiadas. Los pacientes con antecedentes
de infecciones recidivantes deben someterse a otras pruebas para
detectar inmunodeficiencias, incluso aunque las pruebas de cribado
iniciales hayan sido normales. Estas pruebas se describen con
detalle en el capítulo 147. Los recuentos de neutrófilos muy
disminuidos pueden indicar neutropenia congénita grave,
neutropenia cíclica, neutropenia crónica grave, insuficiencia
medular y sustitución de la médula por una neoplasia o por otras
células hematopoyéticas. El conocimiento de las características
clínicas de las inmunodeficiencias permite una interpretación más
racional de los hallazgos que se obtienen en las diferentes pruebas
diagnósticas.
Tratamiento
La linfocitopenia asociada a estrés, administración de corticoides,
quimioterapia o radiación suele remitir tras la eliminación del agente
o el factor etiológico. El tratamiento eficaz de la enfermedad
subyacente que cursa con linfocitopenia (p. ej., enfermedades
infecciosas, inflamatorias o neoplásicas) suele conducir al
incremento del recuento leucocitario. La prevención y el tratamiento
de las inmunodeficiencias primarias se describen en el capítulo 147.
El tratamiento óptimo de los pacientes con enfermedad por el VIH
requiere la identificación y el tratamiento de las infecciones activas
en los individuos que presentan una inmunodeficiencia grave, la
profilaxis primaria y secundaria para prevenir infecciones
oportunistas nuevas o recidivantes y el tratamiento de la infección
primaria por el VIH con el fin de enlentecer el deterioro
inmunológico. El tratamiento farmacológico tiene como objetivo
maximizar los beneficios clínicos, evitar o reducir al mínimo la
toxicidad y mantener la comodidad y la función.
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (11 of 12) [18/11/2001 07:29:30 a.m.]
MSD, Publicaciones, Manual Merck
Copyright ©2001 Merck Sharp & Dohme de España, S.A.
Madrid, España. Todos los derechos reservados.
http://www.msd.es/publicaciones/mmerck/MM_11_135.htm (12 of 12) [18/11/2001 07:29:30 a.m.]
También podría gustarte
- Trastornos Hemorrágicos y de Coagulación en OdontologíaDocumento16 páginasTrastornos Hemorrágicos y de Coagulación en OdontologíaLuisa Salinas AAún no hay calificaciones
- Osteomielitis Aguda y CronicaDocumento93 páginasOsteomielitis Aguda y CronicaJavier Vilar GonzalezAún no hay calificaciones
- Agranulocitosis Por DipironaDocumento6 páginasAgranulocitosis Por DipironaPaula SousaAún no hay calificaciones
- Alteraciones de Color de La Cavidad BucalDocumento71 páginasAlteraciones de Color de La Cavidad BucalAlejandra GomezAún no hay calificaciones
- Caso Clinico Patologia Bucal PapilomaDocumento4 páginasCaso Clinico Patologia Bucal PapilomaDiana PalmaAún no hay calificaciones
- Inmunología - Defectos de La Inmunidad - DiapositivasDocumento49 páginasInmunología - Defectos de La Inmunidad - DiapositivasYesenia VivianaAún no hay calificaciones
- Infeccion Del Tracto UrinarioDocumento35 páginasInfeccion Del Tracto UrinarioRuben Apaza ApazaAún no hay calificaciones
- Microbiologia Pulpar y PeriapicalDocumento52 páginasMicrobiologia Pulpar y PeriapicalDaniel Jonas Abreu Robles100% (1)
- Infecciones FungicasDocumento35 páginasInfecciones FungicasMitchell HoodAún no hay calificaciones
- Prolactinoma 150915005818 Lva1 App6892Documento43 páginasProlactinoma 150915005818 Lva1 App6892Rafa Rodriguez100% (1)
- INFLUENZADocumento42 páginasINFLUENZANadia NavaAún no hay calificaciones
- Mononucleosis InfecciosaDocumento34 páginasMononucleosis InfecciosaCristhianEsequielQuispelayoRamosAún no hay calificaciones
- BlastomicosisDocumento37 páginasBlastomicosisapi-3697227100% (3)
- Resistencia BacterianaDocumento10 páginasResistencia BacterianaRoderick MirandaAún no hay calificaciones
- Torus Palatino y MandibularDocumento6 páginasTorus Palatino y MandibularMarielisa KhouryAún no hay calificaciones
- PielonefritisDocumento4 páginasPielonefritiscateterdoblejotaAún no hay calificaciones
- Micro AlbuminuriaDocumento3 páginasMicro AlbuminuriaJorge OntanedaAún no hay calificaciones
- Roseola InfantilDocumento13 páginasRoseola InfantilCris RamirezAún no hay calificaciones
- Diagnóstico y Diagnóstico Diferencial de Lupus Eritematoso Sistémico en AdultosDocumento17 páginasDiagnóstico y Diagnóstico Diferencial de Lupus Eritematoso Sistémico en AdultosMoni CTAún no hay calificaciones
- Laboratorio Básico en Odontología.Documento10 páginasLaboratorio Básico en Odontología.Doris AbadAún no hay calificaciones
- GLOMERULOPATÍAS ResumenDocumento9 páginasGLOMERULOPATÍAS ResumenSole Lozano RodriguezAún no hay calificaciones
- Adenoma Pleomorfo..Documento4 páginasAdenoma Pleomorfo..Diana Grijalva VasquezAún no hay calificaciones
- Neutropenia Febril en WordDocumento11 páginasNeutropenia Febril en WordBrenda GoyanarteAún no hay calificaciones
- Mecanismos de HipersensibilidadDocumento79 páginasMecanismos de HipersensibilidadYoselyn Castillo BlancoAún no hay calificaciones
- Caso Clinico Sindrome de SjogrenDocumento6 páginasCaso Clinico Sindrome de SjogrenRicardo RodriguezAún no hay calificaciones
- Miopatias InflamatoriasDocumento4 páginasMiopatias InflamatoriasFrancisco Riquelme UrzuaAún no hay calificaciones
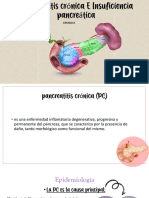
- Cirugia 2: Pancreatitis Crónica E Insuficiencia PancreáticaDocumento31 páginasCirugia 2: Pancreatitis Crónica E Insuficiencia PancreáticaDanniie LopezAún no hay calificaciones
- Tsa3 MicrobiologiaDocumento17 páginasTsa3 MicrobiologiaEddu Medina50% (4)
- OsteomielitisDocumento22 páginasOsteomielitisEyndra MendozaAún no hay calificaciones
- Neutropenia FebrilDocumento13 páginasNeutropenia FebrilFrancisco PuacAún no hay calificaciones
- Fisiopatologia UmsaDocumento10 páginasFisiopatologia UmsaReynaldo GonzalesAún no hay calificaciones
- Xerostomía PosterDocumento1 páginaXerostomía PosterLenin Vlad Qsp LpcAún no hay calificaciones
- Covid Fisiopatologia - En.esDocumento21 páginasCovid Fisiopatologia - En.eswiwiAún no hay calificaciones
- Antibióticos Beta LactamicosDocumento31 páginasAntibióticos Beta LactamicosYader RamosAún no hay calificaciones
- Lupus EritematosoDocumento36 páginasLupus EritematosoFrancelia Quiñonez RuvalcabaAún no hay calificaciones
- Lupus EritematosoDocumento6 páginasLupus EritematosoLucia Lucero Paz OliveraAún no hay calificaciones
- Tumores Benignos de La Mucosa OralDocumento8 páginasTumores Benignos de La Mucosa OralShlomit ZuñigaAún no hay calificaciones
- Anemia FerropénicaDocumento47 páginasAnemia FerropénicaAaron Gomez0% (1)
- Resumen ChagasDocumento5 páginasResumen ChagasPaola GuerraAún no hay calificaciones
- Estructura BacterianaDocumento6 páginasEstructura Bacterianaaimar avilaAún no hay calificaciones
- Familia HerpesviridaeDocumento27 páginasFamilia HerpesviridaeJenyfer Laurel VelasquezAún no hay calificaciones
- Lupus Eritematoso Generalizado: Características Generales, Inmunopatogenia y Antígenos de RelevanciaDocumento7 páginasLupus Eritematoso Generalizado: Características Generales, Inmunopatogenia y Antígenos de RelevanciaInternational Medical PublisherAún no hay calificaciones
- Alergia A MedicamentosDocumento38 páginasAlergia A MedicamentosAntonella Castro CabreraAún no hay calificaciones
- Cancer de ProstataDocumento49 páginasCancer de ProstataMarcelo Guzman MalpartidaAún no hay calificaciones
- SD MielodisplasicosDocumento25 páginasSD MielodisplasicosRaul AmbrosioAún no hay calificaciones
- Lesiones Blancas y Desórdenes Potencialmente MalignosDocumento18 páginasLesiones Blancas y Desórdenes Potencialmente MalignosSalvador HernandezAún no hay calificaciones
- Patologia - Candidiasis OralDocumento8 páginasPatologia - Candidiasis OralEl Kaiser0% (1)
- Patologia Medica 1Documento12 páginasPatologia Medica 1JohnyBarbosaAún no hay calificaciones
- Enfermedad de CrohnDocumento10 páginasEnfermedad de CrohnNadia MartínezAún no hay calificaciones
- Sindrome de Infeccion de Vias UrinariasDocumento21 páginasSindrome de Infeccion de Vias UrinariasAvelar Rios Brenda EscarletteAún no hay calificaciones
- Qué Son Las Miopatías InflamatoriasDocumento16 páginasQué Son Las Miopatías InflamatoriasMarcia Silvana MuñozAún no hay calificaciones
- Enfermedades EstomatologicasDocumento16 páginasEnfermedades EstomatologicasKnarf Gomez Llactahuamani100% (1)
- Diagnóstico de La Patología de Las ArticulacionesDocumento15 páginasDiagnóstico de La Patología de Las Articulacionessilvana_ciardulloAún no hay calificaciones
- Causas de Leucopenia y LeucocitosisDocumento4 páginasCausas de Leucopenia y LeucocitosisSofy EscobedoAún no hay calificaciones
- Simposio: La Interpretación Del Hemograma.Documento54 páginasSimposio: La Interpretación Del Hemograma.Ivette RosarioAún no hay calificaciones
- Examenes de LaboratorioDocumento25 páginasExamenes de LaboratorioLeshly Kenia Campos SilvaAún no hay calificaciones
- Leucemias Aguda y CronicaDocumento35 páginasLeucemias Aguda y CronicaJulio Cesar Pretel LinaresAún no hay calificaciones
- Enfermedades DentalesDocumento33 páginasEnfermedades DentalesMary Cruz Silva del AguilaAún no hay calificaciones
- Anemia PerniciosaDocumento9 páginasAnemia PerniciosaNadiaDanielaDelgadoSuárezAún no hay calificaciones
- Ensayo 3. Moreno CastillejaDocumento8 páginasEnsayo 3. Moreno CastillejaMartín CastillejaAún no hay calificaciones
- 6b9ac59d 4b8b 4e2a Adfc 9bdeb2c8dcb8Documento42 páginas6b9ac59d 4b8b 4e2a Adfc 9bdeb2c8dcb8api-3737581Aún no hay calificaciones
- TrombocitemiaDocumento29 páginasTrombocitemiaapi-3737581100% (1)
- 6b9ac59d 4b8b 4e2a Adfc 9bdeb2c8dcb8Documento42 páginas6b9ac59d 4b8b 4e2a Adfc 9bdeb2c8dcb8api-3737581Aún no hay calificaciones
- Leucemia Linfoblastica Aguda InfantilDocumento51 páginasLeucemia Linfoblastica Aguda Infantilapi-3737581100% (3)
- HiperlipidemiaDocumento39 páginasHiperlipidemiaAli-SanJuan100% (7)
- Manual Sobre El - Uso Clinico de La Sangre OMSDocumento239 páginasManual Sobre El - Uso Clinico de La Sangre OMSQUIMICO CLINICO WILLIANS SANCHEZ100% (5)
- Anemia Falciforme - Polimorfismo - ECI 260511Documento6 páginasAnemia Falciforme - Polimorfismo - ECI 260511Rafael Arturo Vergara TámaraAún no hay calificaciones
- Trastorno de La HemostasiaDocumento22 páginasTrastorno de La Hemostasiaapi-3737581100% (2)
- SangreallDocumento12 páginasSangreallapi-3737581Aún no hay calificaciones
- Casos Clinicos LibroDocumento306 páginasCasos Clinicos Libroapi-3711182100% (8)
- Tamizaje ACFDocumento5 páginasTamizaje ACFapi-3737581100% (1)
- Transfusiones Indicaciones para El Uso de Sangre y Componentes SanguineosDocumento7 páginasTransfusiones Indicaciones para El Uso de Sangre y Componentes SanguineosQUIMICO CLINICO WILLIANS SANCHEZ100% (6)
- Sangre AutologaDocumento15 páginasSangre Autologaapi-3737581100% (2)
- SangreDocumento11 páginasSangreapi-3737581100% (2)
- Medicina TransfucionalDocumento49 páginasMedicina Transfucionalapi-3737581100% (1)
- Int 171 Art 1Documento13 páginasInt 171 Art 1api-3737581100% (1)
- Normativa de HemoterapiaDocumento64 páginasNormativa de Hemoterapiaapi-373758150% (2)
- ProtodrepanocitosisDocumento40 páginasProtodrepanocitosisapi-3737581100% (3)
- Prevalencia de Hemoglinopatias en GestantesDocumento7 páginasPrevalencia de Hemoglinopatias en Gestantesapi-3737581100% (3)
- Leucemia AgudaDocumento58 páginasLeucemia Agudaapi-3737581Aún no hay calificaciones
- Hemoglobinopatias. Capitulo Iii. Primera Parte.Documento53 páginasHemoglobinopatias. Capitulo Iii. Primera Parte.api-3737581100% (4)
- Importancia de La Genealogia AplicadaDocumento28 páginasImportancia de La Genealogia Aplicadaapi-3737581100% (1)
- I434 1Documento18 páginasI434 1api-3737581100% (3)
- HEMATOLOGIADocumento5 páginasHEMATOLOGIAapi-3737581100% (3)
- Anemia Falciforme - Polimorfismo - ECI 260511Documento6 páginasAnemia Falciforme - Polimorfismo - ECI 260511Rafael Arturo Vergara TámaraAún no hay calificaciones
- HemoglobinaDocumento11 páginasHemoglobinaapi-3737581100% (4)
- Haplotipos AnemiaDocumento8 páginasHaplotipos AnemiajaniellegbAún no hay calificaciones
- Frotis de Sangre PerifericaDocumento9 páginasFrotis de Sangre Perifericaapi-3737581100% (8)
- Fisiopatologi de La CIDDocumento6 páginasFisiopatologi de La CIDapi-3737581Aún no hay calificaciones
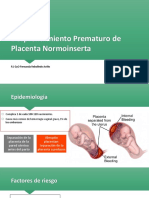
- Desprendimiento Prematuro de Placenta NormoinsertaDocumento31 páginasDesprendimiento Prematuro de Placenta NormoinsertaFer Rebolledo AvilésAún no hay calificaciones
- Historia Clínica VihDocumento6 páginasHistoria Clínica VihSegundo PicoAún no hay calificaciones
- Procedimientos Complementarios de Diagnostico Del Sistema RespiratorioDocumento14 páginasProcedimientos Complementarios de Diagnostico Del Sistema RespiratorioDessire Cruz LauraAún no hay calificaciones
- ENFERMEDAD ULCEROPEPTICA UnefmDocumento22 páginasENFERMEDAD ULCEROPEPTICA Unefmmaria elena ramirez linarezAún no hay calificaciones
- Fibrosis QuisticaDocumento32 páginasFibrosis Quisticacarola rojasAún no hay calificaciones
- Tema 4 MetatarsalgiasDocumento8 páginasTema 4 Metatarsalgias1311jiAún no hay calificaciones
- Trauma ResumenDocumento26 páginasTrauma ResumenARTURO ROMEROAún no hay calificaciones
- DEMENCIAS REVERSIBLES - En.esDocumento20 páginasDEMENCIAS REVERSIBLES - En.esjuliana lópez MAún no hay calificaciones
- Adenoma Hipofisiario (Resumen)Documento9 páginasAdenoma Hipofisiario (Resumen)Diego Gutierrez HernandezAún no hay calificaciones
- Clase 4 PATRONESDocumento28 páginasClase 4 PATRONESIvan AlavaAún no hay calificaciones
- Carcinoma EpidermoideDocumento11 páginasCarcinoma EpidermoideErick TorresAún no hay calificaciones
- Abordaje Del PruritoDocumento8 páginasAbordaje Del Pruritosebastian ochoaAún no hay calificaciones
- Aparato de GolgiDocumento2 páginasAparato de Golgijuan david castillo bernalAún no hay calificaciones
- Banque de Reumato 2023Documento4 páginasBanque de Reumato 2023Wendy Lucero Jurado LenguaAún no hay calificaciones
- Pae - OligohidramniosDocumento30 páginasPae - OligohidramniosEzequiel Cocom100% (1)
- Preguntas-Urología 230721 055928Documento5 páginasPreguntas-Urología 230721 055928Carmen MontesAún no hay calificaciones
- Neurologia @juntosalenarmDocumento52 páginasNeurologia @juntosalenarmGloria VallesAún no hay calificaciones
- Practica 17. Perfil LipidicoDocumento3 páginasPractica 17. Perfil Lipidicojuan rsAún no hay calificaciones
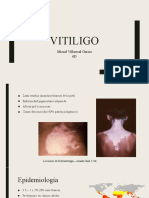
- VitiligoDocumento12 páginasVitiligoJoaoBCCAún no hay calificaciones
- Formacion Reticular y Sistema LimbicoDocumento84 páginasFormacion Reticular y Sistema LimbicoUSMP FN ARCHIVOS100% (1)
- Sistema Límbico y La ConductaDocumento3 páginasSistema Límbico y La ConductaLisbeth Cueva67% (3)
- FR-12-12.5-029 Inspeccion de Equipos TSADocumento3 páginasFR-12-12.5-029 Inspeccion de Equipos TSAJohn JairoAún no hay calificaciones
- Faringitis: RevisiónDocumento4 páginasFaringitis: RevisiónVeronica Perez AguilarAún no hay calificaciones
- Laminas de HipotiroidismoDocumento18 páginasLaminas de HipotiroidismoSigfredo MirandaAún no hay calificaciones
- ALZHEIMERDocumento26 páginasALZHEIMERMarcia Yucra ChinoAún no hay calificaciones
- Caso Clinico Ana Por FinalizarDocumento15 páginasCaso Clinico Ana Por FinalizardanielaAún no hay calificaciones
- Caso Clinico Grupo 3Documento2 páginasCaso Clinico Grupo 3Medalyt Huashuayo CusiAún no hay calificaciones
- Resumen de La Enfermedad Del ParkinsonDocumento2 páginasResumen de La Enfermedad Del ParkinsonNehemias Torres100% (1)
- Glandulas EcrinasDocumento60 páginasGlandulas EcrinasYanet CamposAún no hay calificaciones
- Contaminacion de Metales Pesados en Los AlimentosDocumento9 páginasContaminacion de Metales Pesados en Los AlimentosYancarla BalderramaAún no hay calificaciones