Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Bit 29 Num2 Reacciones Hipersensibilidad AINE 2018 Castella
Cargado por
Fa biDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Bit 29 Num2 Reacciones Hipersensibilidad AINE 2018 Castella
Cargado por
Fa biCopyright:
Formatos disponibles
Departament de Salut Butlletí
d’informació
terapèutica
BIT. Vol. 29, núm. 2, 2018
MANEJO DE LAS REACCIONES DE HIPERSENSIBILIDAD
A LOS ANTIINFLAMATORIOS NO ESTEROIDEOS (AINE)
R Lleonart1, E Santacana2, MD de la Peña2, M Corominas1
Unidad de Alergología, Servicio de Medicina Interna
1
Servicio de Farmacia. Hospital Universitari de Bellvitge, IDIBELL
2
Resumen
Los pacientes con reacciones adversas por hipersensibilidad inducidas por AINE representan un colectivo hetero-
géneo con una expresión clínica muy diversa. Los AINE son la primera causa de hipersensibilidad a fármacos. Las
reacciones de hipersensibilidad a AINE son reacciones adversas tipo B (impredecibles que ocurren en individuos
susceptibles) según la clasificación de la OMS.
Se ha clasificado la hipersensibilidad a AINE de acuerdo a los síntomas que producen (respiratorios, cutáneos,
anafilaxia), la latencia de estos síntomas, (inmediatas o retardadas), las enfermedades concomitantes que pre-
sentan los pacientes (asma, urticaria crónica espontánea) y el posible mecanismo de la reacción (inmunitario
con participación de IgE o predominantemente de células T y no inmunitario por inhibición de COX-1).
No existe ninguna batería de pruebas que permita saber si un paciente, sin haber tenido nunca ninguna reac-
ción, tiene alergia a uno o varios medicamentos. El estudio de las reacciones de alergia a AINE es complejo y se ha
de individualizar tanto por paciente como por medicamento. Ante una posible reacción, los alergólogos realizan,
en primer lugar, una anamnesis dirigida que puede aportar mucha información sobre la probabilidad de que un
paciente tenga una alergia a un medicamento. Las pruebas cutáneas o de laboratorio ayudan al diagnóstico,
pero sólo la prueba de exposición controlada al medicamento permite establecer el diagnóstico definitivo.
Se debe recordar que no existen pruebas de cribado para saber si una persona es alérgica o no. El estudio de
alergia a fármacos puede confirmar el diagnóstico, así mismo si el estudio es negativo no se descarta una sensi-
bilización futura.
Palabras clave: hipersensibilidad a fármacos, alergia a fármacos, antiinflamatorios no esteroideos, AINE
Introducción Los AINE se pueden clasificar según la estructura química (tabla
1) y según la potencia inhibitoria de los enzimas ciclooxigena-
Los AINE son un grupo extenso de fármacos con estructuras sa-1 (COX-1) y ciclooxigenasa-2 (COX-2) (tabla 2). Los AINE se
químicas muy diversas y no necesariamente relacionadas entre asocian con una serie de reacciones adversas, que pueden ir
sí que presentan propiedades analgésicas, antipiréticas y anti- desde gastritis leve a reacciones alérgicas potencialmente mor-
inflamatorias1. Debido a la elevada prevalencia de cuadros clí- tales5. Una duda que se presenta cuando hay una reacción sos-
nicos susceptibles de ser tratados con estos medicamentos, los pechosa de ser alérgica es si en aquel paciente se ha de evitar
AINE son uno de los grupos farmacológicos más utilizados en sólo la administración del AINE que le ha producido la reacción
terapéutica2,3, y de los cuales se registra mayor consumo4. o si debe evitar todos los AINE. De aquí que sea tan importante
llegar a un diagnóstico concreto, ya que de ello dependerá que
se pueda tratar al paciente con determinados AINE o se tengan
que buscar fármacos alternativos.
BIT. Vol. 29 / núm. 2 / 2018 8
Aunque el consumo de AINE en España aumentó un 26,5% en- cadenamiento y la gravedad pueden estar condicionados por
tre el año 2000 y el 20126, se ha observado posteriormente una la potencia inhibitoria que tiene el AINE sobre la enzima COX, y
disminución del 12,13% durante el periodo de 2013 a 20167. también por la dosis de fármaco administrada.
Durante este último periodo, el subgrupo de AINE derivados del
ácido propiónico ha sido el de mayor consumo (aunque tam- En las reacciones mediadas por mecanismos inmunitarios, la
bién ha ido disminuyendo), y representa el 70,72% del consu- respuesta alérgica suele ser contra un solo fármaco o fármacos
mo total de AINE en el 20167. De este subgrupo destaca el ibu- químicamente relacionados (reacciones selectivas), al cual el
profeno, que aunque disminuye su consumo durante el periodo paciente ha de haber estado expuesto como mínimo una vez.
2013-2016, continua siendo el principio activo más utilizado. En En estos casos, los pacientes toleran otros fármacos química-
segundo y tercer lugar se encuentran el naproxeno y el dexke- mente no relacionados. Por otro lado, las reacciones no media-
toprofeno, los cuales han aumentado su uso durante el periodo das inmunitariamente están relacionadas con la inhibición de
2013-20167. Durante el mismo periodo, en Cataluña también se la enzima COX-1 y la liberación de histamina y leucotrienos9. En
ha registrado una ligera disminución del de AINE. Coincidien- estos casos, los pacientes presentan reacciones a diversos AINE
do con los datos anteriores, pese a la disminución observada no relacionados químicamente10. Estas reacciones de hipersen-
en el uso de ibuprofeno durante los últimos años, este también sibilidad no inmunitaria, en que se presenta una intolerancia
destaca como el AINE más consumido en Cataluña; seguido de cruzada, son las más frecuentes (75% de los casos).
naproxeno y diclofenaco.
Los AINE son la primera causa de reacciones de hipersensibili-
dad a fármacos, y los antibióticos beta-lactámicos son la segun-
da8. De acuerdo con el grupo European Network of Drug Allergy,
Reacciones adversas a AINE las reacciones de hipersensibilidad a AINE se pueden clasificar
en 5 subtipos (tabla 3) en función del mecanismo que las pro-
Las reacciones adversas provocadas por AINE se clasifican en duce y los síntomas clínicos que presenta el paciente11,12.
las de tipo A y las de tipo B. Las de tipo A están relacionadas
con los efectos del fármaco; suelen ser predecibles, tienen re-
lación con la dosis, son relativamente frecuentes y raramente
fatales. En cambio, las de tipo B están relacionadas con la res- Manifestaciones clínicas
puesta de cada individuo, no de los efectos del medicamento;
son reacciones imprevisibles y menos frecuentes, representan Los síntomas que pueden presentar los pacientes son muy va-
un 6-10%8, pero pueden poner en riesgo la vida del paciente. riados, principalmente en las reacciones de hipersensibilidad
Las reacciones de hipersensibilidad se incluyen dentro de las de no inmunitaria (no alérgica) y en algunos de estos casos depen-
tipo B, y se pueden clasificar según si el mecanismo es inmuni- derán de la enfermedad de base que estos pacientes sufran. En
tario (son propiamente las reacciones alérgicas, mediadas por las reacciones de hipersensibilidad inmunitaria (alérgica), las
IgE o por células T) o un mecanismo no inmunitario (no alérgi- manifestaciones clínicas se presentan en forma de anafilaxia,
cas, por inhibición de la COX-1)8. Estas reacciones no alérgicas síntomas cutáneos o reacciones retardadas que pueden afectar
anteriormente eran conocidas como reacciones de idiosincrasia a diferentes órganos. De todas formas, a veces, en la práctica
o de intolerancia a los AINE. Son reacciones en las que el desen- clínica es difícil diferenciar entre un tipo u otro de reacción.
Tabla 1. Clasificación del AINE según la estructura química
Salicilatos Ácido acetilsalicílico, acetilsalicilato de lisina
Derivados indolacéticos Indometacina
Derivados arilacéticos Aceclofenaco, diclofenaco, nabumetona, ketorolaco
Derivados arilpropiónicos Dexibuprofeno, dexketoprofeno, flurbiprofeno, ibuprofeno, ketoprofeno, naproxeno
Oxicams Lornoxicam, meloxicam, piroxicam, tenoxicam
Fenamatos Ácido mefenámico, ácido niflúmico
Coxibs Celecoxib, etoricoxib, parecoxib
Anilidas Paracetamol (acetaminofeno)
Pirazolonas Metamizol (dipirona), propifenazona
Otros Isonixina, clonixina (clonixinato de lisina)
Tabla 2. Clasificación del AINE según la potencia inhibitoria de COX-1 y COX-2
Ácido acetilsalicílico, diclofenaco, dexketoprofeno, flurbiprofeno, ibuprofeno, in-
AINE que inhiben preferentemente la COX-1
dometacina, ketoprofeno, ketorolaco, ácid mefenámico, naproxeno, piroxicam.
AINE que inhiben preferentemente la COX-2, pero también inhiben la COX-1 Meloxicam, nabumetona
AINE inhibidores selectivos de la COX-2 Celecoxib, etoricoxib, parecoxib
BIT. Vol. 29 / núm. 2 / 2018 9
Reacciones de hipersensibilidad no in- Reacciones de hipersensibilidad inmu-
munitaria nitaria
Reacciones con AINE generalmente debidas a la inhibición Reacciones alérgicas generalmente a un solo fármaco o po-
de COX-1. cos fármacos de la misma estructura.
• Enfermedad respiratoria exacerbada por AINE (EREA): exa- • Urticaria/angioedema o anafilaxia a un solo antiinflamatorio
cerbación de enfermedades respiratorias (asma y rinitis). (o a otros del mismo grupo) al cabo de unos pocos minutos
En pacientes que ya presentan asma o rinosinusitis crónica o unas horas de tomarlo. Son reacciones mediadas por IgE.
concomitante (también poliposis nasal). Los pacientes pre- • Reacción retardada inducida por AINE selectivo (RTA-S). Las
sentan asma no atópica, poliposis nasal y aumento de sus reacciones retardadas se inician pasadas las 24h de la ex-
síntomas al tomar un AINE. La EREA se conocía anteriormen- posición al fármaco y se pueden manifestar de forma local
te como enfermedad de Widal o tríada ASA (asma, poliposis (exantema fijo pigmentario) o ser multisistémicas: erupción
nasal e intolerancia al ácido acetilsalicílico). maculopapular, DRESS (Drug Rash Eosinophilia and Systemic
• Enfermedad cutánea exacerbada por AINE (ECEA): en pa- Symptoms), síndrome de Steven-Johnson, etc. Son reaccio-
cientes con urticaria crónica se exacerban los síntomas nes mediadas por células T.
cutáneos tanto de urticaria como de angioedema después A veces pacientes alérgicos a alimentos como crustáceos, frutos
de la administración de AINE. La mayoría de las reacciones secos o algunas frutas pueden presentar una urticaria, angioe-
cutáneas inducidas por AINE son debidas a exacerbaciones dema o hasta anafilaxia si a la vez han tomado un AINE. Estos pa-
de una urticaria crónica. Una vez resuelta la urticaria, el pa- cientes toleran el AINE si se toma sin los alimentos nombrados14.
ciente vuelve a tolerar los AINE.
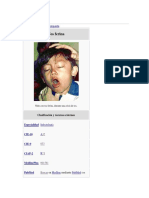
• Urticaria y/o angioedema inducido por AINE (UAIA): el AINE
induce una urticaria y/o angioedema en individuos que no
presentan la enfermedad respiratoria o cutánea de base.
Desmontando mitos
Suele afectar a la cara: párpados y labios. La complejidad y el desconocimiento del diagnóstico correc-
Estas reacciones se presentan de forma aguda, inmediatamen- to en la alergia a AINE han alimentado una serie de mitos con
te o al cabo de unas horas después de la exposición sistémica poca evidencia científica o sin ella, que han sido asumidos sin
(oral, parenteral) al AINE y, generalmente, están en función de cuestionarse por una parte de la población y hasta por algunos
la potencia del AINE para inhibir la COX-1 y de la dosis adminis- profesionales de la salud. A continuación exponemos algunos
trada. Los AINE tópicos pueden causar dermatitis de contacto de estos mitos a vencer15:
alérgicas o fotoalérgicas (p. ej. ketoprofeno). Los pacientes con • Tartrazina (E-102), este aditivo no tiene capacidad inhibi-
este tipo de reacciones suelen tolerar la administración sistémi- dora de la COX ni reacción cruzada con los AINE, por tanto
ca del mismo fármaco, aunque se debe realizar una prueba de los pacientes con hipersensibilidad a AINE no tiene porque
exposición previa para confirmar esta tolerancia. evitarlo.
Hay una forma infantojuvenil de angioedema parpebral aisla- • Hidrocortisona. Si bien se había apuntado la posibilidad que
do sin urticaria con patrón de reacción a múltiples AINE y que en algunos pacientes con EREA el tratamiento con hidrocor-
afecta pacientes atópicos (sensibilización a ácaros) con rinitis tisona intravenosa pudiera inducir broncoespasmo, se ha
y/o asma bronquial13,14. El angioedema suele ser localizado con demostrado que este corticoide no muestra reactividad cru-
afectación periorbital y bilateral. El ácido acetilsalicílico (AAS) es zada con AAS ni con otros AINE.
el AINE más frecuentemente implicado, seguido por el ibupro- • Alimentos ricos en salicilatos. Se había dicho que los pacien-
feno y el metamizol. En ocasiones, pacientes con este tipo de tes alérgicos a los AINE tenían que evitar alimentos ricos en
angioedema pueden presentar reacción por la ingesta de ali- salicilatos (orégano, canela, mostaza, pimienta, albaricoque,
mentos contaminados por ácaros. fresa, ciruela, piña en almíbar, almendra, castaña, alcachofa,
Tabla 3. Clasificación de las reacciones de hipersensibilidad a AINE según el grupo European Network of Drug Allergy
Manifestaciones Tiempo de aparición Enfermedad Reactividad
Tipo de reacción Mecanismo de acción
clínicas de la reacción subyacente cruzada
Obstrucción bronquial,
Enfermedad respiratoria
disnea y/o congestión Asma/rinosinusitis Inhibición COX-1
exacerbada por AINE (EREA)
nasal/rinorrea
Agudo (inmediato o No
Enfermedad cutánea Sí
Ronchas y/o angioedema pocas horas después Urticaria crónica inmunitario Inhibición COX-1
exacerbada por AINE (ECEA)
de la exposición al
Urticaria/angioedema fármaco) Sin enfermedad Desconocido, probable-
Ronchas y/o angioedema
inducido por AINE (UAIA) subyacente mente inhibición COX-1
Urticaria/angioedema o anafilaxia Ronchas y/o angioedema/ Sin enfermedad
Mediado por IgE
inducida por un único AINE (UAIA-S) anafilaxia subyacente
De inicio tardío No Inmunitario
Reacciones tardías inducidas Diversos síntomas y Sin enfermedad
(>24h después de la Mediado por células T
por un único AINE (RTA-S) órganos involucrados subyacente
exposición
BIT. Vol. 29 / núm. 2 / 2018 10
pepino, etc.). Por tanto, los pacientes con hipersensibilidad que permita saber si un paciente tiene o no una hipersensibili-
a AINE no han de restringir ningún alimento. dad a AINE.
• Asma y AAS. Algunos profesionales prohíben la administra- La historia clínica tal como se ha comentado anteriormente es
ción de AINE a todos los pacientes con asma bronquial. Si fundamental para hacer un diagnóstico correcto. Se debe cono-
bien hay una entidad clínica, la EREA, en que el AAS y otros cer si se han presentado reacciones con un único fármaco o si se
AINE pueden desencadenar crisis de broncoespasmo grave, han visto implicados AINE de grupos farmacológicos diferentes,
la mayoría de pacientes con asma bronquial toleran el AAS. el tipo de reacción y su latencia. Se debe saber si ha tolerado
• TTL. Algunas pruebas in vitro, como el test de transforma- posteriormente algún AINE, también qué alimentos se han in-
ción linfoblástica (TTL), que se había utilizado ampliamente gerido en las horas previas e inmediatamente posteriores a la
para el diagnóstico de alergia a AINE no está validado y, por toma del fármaco, ya que en algunas ocasiones el AINE puede
tanto, sus resultados no tienen relevancia clínica. actuar como cofactor de una alergia a algún medicamento16.
Las pruebas in vivo no están libres de riesgo y se deben hacer
en un medio hospitalario por parte de alergólogos expertos en
¿Qué hacer ante un paciente con su interpretación y valoración, y en el tratamiento de una posi-
sospecha de reacción de hiper- ble reacción. Las pruebas cutáneas (prueba del pinchazo [prick
test] e intradermorreacción) son útiles en caso de que se sospe-
sensibilidad a AINE? che una reacción de hipersensibilidad de tipo inmunitario, por
ejemplo, en las UAIA-S por pirazolonas. En las RTA-S las pruebas
La historia clínica es fundamental. Algunas veces ya nos permi- epicutáneas pueden contribuir al diagnóstico17. En las reaccio-
tirá conocer si el paciente presenta hipersensibilidad a un grupo nes de hipersensibilidad no inmunitaria las pruebas cutáneas
concreto de AINE o grupos de AINE no relacionados, en función no son útiles.
de los AINE tolerados después de haber presentado la reacción.
En caso de no poder dilucidar estos aspectos, se deberá derivar No se han validado las pruebas de detección de IgE específica
al paciente para estudio. para AINE. El test de activación de basófilos puede ser una alter-
nativa en las reacciones graves donde se sospecha que existe
Nos podemos encontrar en tres supuestos: IgE específica a pirazolonas18.
1. El paciente ha presentado reacción a un AINE y, posterior- La prueba de exposición controlada constituye el estándar de
mente, ha tolerado AINE de grupos químicos diferentes. En referencia (gold standard), tanto para llegar al diagnóstico de
estos casos se debe evitar el grupo de AINE al que supues- hipersensibilidad a un AINE como para comprobar la tolerancia
tamente ha hecho reacción y administrar los AINE de otros a un AINE alternativo14. Esta prueba no está exenta de riesgos y
grupos que ya ha tolerado. su beneficio se debe valorar ante los riesgos de cada paciente
2. Si el paciente ha presentado reacciones sugestivas de hiper- y fármaco.
sensibilidad a dos o más AINE de estructura química dife-
La guía de la EAACI 2013 (European Academy of Allergy and Clini-
rente, nos encontraremos ante una probable hipersensibi-
cal Immunology) recomienda hacer la prueba de exposición con
lidad no inmunitaria a AINE. Se debe evitar todos los AINE
el AINE implicado si la historia clínica no es concluyente y con
hasta que se haga el estudio por parte de los alergólogos.
AAS para confirmar o excluir una reactividad cruzada13.
Muchos de estos pacientes toleran paracetamol, inhibidores
de la COX-1 de baja potencia (tipo meloxicam) e inhibido-
res de la COX-2, pero se debe hacer la prueba de exposición
controlada para demostrar esta tolerancia. Una vez obtenido el diagnóstico
3. El paciente ha presentado reacción a un solo AINE, pero des-
conoce si tolera otros. Conviene que sea evaluado por aler- En las reacciones de hipersensibilidad selectiva, se recomienda
gólogos con tal de obtener un diagnóstico detallado. evitar el AINE causante de la reacción así como otros AINE con
estructura química similar.
En las reacciones de hipersensibilidad múltiple, la tolerancia
Diágnostico al AINE suele ser inversamente proporcional a su potencia in-
hibitoria de la COX-1. El paracetamol, los inhibidores predomi-
Para el estudio diagnóstico de las reacciones alérgicas se cuen-
nantemente selectivos de la COX-2 (meloxicam) y los coxibs se
ta, a parte de la historia clínica, con una serie de pruebas tan- podrán indicar si se ha demostrado tolerancia espontánea o
to in vivo como in vitro que permiten, en la mayoría de casos, después de una prueba de exposición controlada15.
llegar a un diagnóstico detallado. En el caso de las reacciones
alérgicas a fármacos el estudio es más complejo, porque para la Una vez realizado el diagnóstico de hipersensibilidad a AINE, se
mayoría de ellos no se dispone de pruebas diagnósticas in vitro han de ofrecer fármacos alternativos al paciente. Se entregará a
validadas y en el caso concreto de los AINE, además, se ha de todos los pacientes un informe escrito que especifique los fárma-
diferenciar si el paciente ha presentado una reacción alérgica cos a evitar, los alternativos (tabla 4) y la dosis tolerada de AINE.
o no alérgica, es decir, una reacción con participación o no del
sistema inmunitario. En pacientes con hipersensibilidad a AAS se pueden realizar téc-
nicas de desensibilización consistentes en la administración de
El estudio de las reacciones de hipersensibilidad a AINE, por dosis crecientes de este fármaco hasta llegar a la dosis deseada,
tanto, es complejo y se debe individualizar tanto por paciente que se deberá administrar diariamente. La desensibilización
como por medicamento. No existe ninguna batería de pruebas está indicada:
BIT. Vol. 29 / núm. 2 / 2018 11
- Cuando el fármaco es necesario y no hay alternativas válidas,
como puede ser el caso del AAS como antiagregante plaque-
Bibliografía
tario19. 1. Harirforoosh S, Asghar W, Jamali F. Adverse effects of nonsteroidal antiinflamatory drugs: an upd ate
of gastrointestinal, cardiovascular and renal complications. J Pharm Sci. 2013;16:821-47.
- Cuando se busca un efecto terapéutico en el tratamiento de 2. Brune K, Patrignani P. New insights into the use of currently available non-steroidal anti-inflammatory
drugs. J Pain Res. 2015;8:105-18.
la EREA20. Después de la desensibilización a AAS, en algunos 3. McGettigan P, Henry D. Use of Non-Steroidal Anti-Inflammatory Drugs That Elevate Cardiovascular
casos se ha comunicado una mejoría de los síntomas nasales Risk: An Examination of Sales and Essential Medicines Lists in Low-, Middle-, and High-Income Coun-
y de asma, recuperación del olfato, disminución del número de tries. PLoS Med. 2013; 10 (2): e1001388.
4. Ministerio de Sanidad, Servicios Sociales e Igualdad. La salud y el sistema sanitario en 100 tablas.
polipectomías y de visitas a urgencias o de los ingresos hospi- Datos y Cifras España. Juliol 2016. Disponible en: https://www.msssi.gob.es/estadEstudios/estadis-
talarios por asma. ticas/sisInfSanSNS/tablasEstadisticas/SaludSistemaSanitario_100_Tablas1.pdf [Consulta: 24 de julio
de 2017]
5. NSAIDs (including aspirin): Allergic and pseudoallergic reactions. UpToDate. Last updated: Aug
Puntos clave 01, 2017. Disponible en: https://www.uptodate.com/contents/nsaids-including-aspirin-aller-
gic-and-pseudoallergic-reactions [Consulta: 21 de noviembre de 2017]
6. Utilización de medicamentos antiinflamatorios no esteroideos (AINE) en España durante el periodo
• La hipersensibilidad a AINE puede ser debida a diferen- 2000-2012. Fecha de publicación: 27 de enero de 2014. Disponible en: https://www.aemps.gob.es/
medicamentosUsoHumano/observatorio/docs/AINE.pdf [Consulta: 21 de noviembre de 2017]
tes mecanismos (participación del sistema inmunitario
7. Utilización de medicamentos antiinflamatorios no esteroideos (AINE) en España durante el periodo
o por inhibición de la enzima COX) y presenta manifes- 2013-2016. Fecha de publicación: 22 de septiembre de 2017. Disponible en: https://www.aemps.
taciones clínicas muy variadas. gob.es/medicamentosUsoHumano/observatorio/docs/antiinflamatorios-AINEs-periodo-2013-2016.
pdf [Consulta: 21 de noviembre de 2017]
• Se deben restringir las reacciones de hipersensibilidad 8. Doña I, Barrionuevo E, Blanca-Lopez N, Torres MJ, Fernández TD, Mayorga C, et al. Trends in Hypersen-
de las reacciones adversas predecibles (gastrointestina- sitivity Drug Reactions: More drugs, More Response Patterns, More Heterogeneity. J Investig Allergol
Clin Immunol 2014;24:143-53.
les, renales, etc.)
9. Szczeklik A, Stevenson DD. Aspirin-induced asthma: advances in pathogenesis, diagnosis and man-
• Conviene evitar algunas afirmaciones ampliamente agement. J Allergy Clin Immunol. 2003;111:913-21.
difundidas sin evidencia científica como que todos los 10. Doña I, Blanca-López N, Cornejo-García JA, Torres MJ, Laguna JJ, Fernández J, et al. Characteristics
of subjects experiencing hypersensitivity to non-steroidal anti-in ammatory drugs: patterns of re-
asmáticos deben evitar el AAS. sponse. Clin Exp Allergy. 2011;41:86-95.
11. Kowalski ML, Asero R, Bavbek S, Blanca M, Blanca-López N, Bochenek G, et al. Classification and prac-
• El diagnóstico correcto de hipersensibilidad a AINE es tical approach to the diagnosis and management of hypersensitivity to nonsteroidal anti-iflammato-
necesario tanto para confirmar como para descartar ry drugs. Allergy.2013;68:1219-32.
una sospecha. Una vez diagnosticada una hipersensibi- 12. Ortega N, Doña I, Moreno E, Audicana M, Barasona M, Berges-Gimeno M. Practical guidelines for di-
agnosing hypersensitivity reactions to nonsteroidal anti-inflammatory drugs. J Investig Allergol Clin
lidad a un AINE, se debe saber si lo es a un solo AINE, a Immunol. 2014;24:308-23.
AINE del mismo grupo químico o si es cruzada con AINE 13. Quiralte J, Blanco C, Delgado J, Ortega N, Alcántara M, Castillo R et al. Challenge-based clinical pat-
de grupos químicos no relacionados. terns of 223 Spanish patients with nonsteroidal anti-inflammatory-drug-induced-reactions. J Inves-
tig Allergol Clin Immunol. 2007;17:182-8.
• La historia clínica es fundamental para el diagnóstico 14. Quiralte J, Ávila-Castellano R, Cimbollek S. A phenotype-based classification of NSAIDs hypersensitiv-
correcto, si bien en muchos casos será necesario reali- ity: New patients, new challenges. Allergy. 2014;69:814-5.
15. Gaig P, Corominas M, Guspi R, Garcia-Ortega, Cerdà MT, Giner MT, et al. Protocol d’estudi d’al·lèrgia a
zar pruebas diagnósticas in vivo de las que la prueba de fàrmacs de l’SCAIC: antiinflamatoris no esteroidals. Capítulo 18. Octubre 2011.
exposición controlada nos permitirá llegar al diagnós- 16. Cardona V, Luengo O, Garriga T, Labrador-Horrillo M, Sala-Cunill A, Izquierdo A, et al. Co-factor-en-
tico concreto. hanced food allergy. Allergy 2012; 67:1316–8.
17. Demoly P, Adkinson NF, Brockow K, Castells M, Chiriac AM, Greenberger PA, et al. International Con-
• En caso de que se confirme la hipersensibilidad a un sensus on drug allergy. Allergy. 2014;69:420-37.
AINE, debe registrarse en la historia clínica con tal de 18. Ortega Rodríguez NR, Quiralte Enriquez J, Fraj Lázaro J, Palacios Colom L. Reacciones adversas a los
evitar nuevas exposiciones que podrían producir reac- AINE: alergia, intolerancia. A: Peláez Dávila A, González IJ(Ed.) Tratado de alergología (tom II), Madrid:
2007, 1461–1473.
ciones graves, hasta el punto de comprometer la vida
19. Cortellini G, Romano A, Santucci A, Barbaud A, Bavbek S, Bignardi D, et al. Clinical approach on chal-
del paciente. También es necesario proporcionar posi- lenge and desensitization procedures with aspirin in patients with ischemic heart disease and non-
bles alternativas terapéuticas. steroidal anti-inflammatory drug hypersensitivity. Allergy. 2017;72:498-506.
20. White AA1, Stevenson DD. Aspirin desensitization in aspirin-exacerbated respiratory disease. Immu-
nol Allergy Clin North Am. 2013;33:211-22.
Tabla 4. Fármacos alternativos en pacientes con reacción de hipersensibilidad no inmunitaria a AINE
ANALGÉSICOS
Paracetamol, dosis menores a 1.000 mg, si los tolera
Opiáceos menores:
Codeína
Tramadol
Opiáceos mayores:
Buprenorfina
Fentanil
Meperidina, petidina
Morfina
Oxicodona
ANTIINFLAMATORIOS
Meloxicam, si lo tolera
Coxibs: celecoxib, etoricoxib, parecoxib si los tolera
Corticoides
BIT. Vol. 29 / núm. 2 / 2018 12
En un clic...
Harmonización farmacoterapéutica
Informes y acuerdos del Programa d’harmonització farmacoterapéutica del Servei Català de la Salut:
• Estiripentol (Diacomit®) para el tratamiento del síndrome de Dravet.
• Opicapona (Ongentys®) para el tratamiento de la enfermedad de Parkinson.
• Bortezomib (Velcade®) en combinación con melfalan y prednisona, para el tratamiento de pacientes adultos con mielo-
ma múltiple que no han recibido tratamiento previo y que no son candidatos a un trasplante.
• Lenalidomida (Revlimid®) en combinación con melfalán y prednisona, para el tratamiento de pacientes adultos con
mieloma múltiple que no han recibido tratamiento previo y que no son candidatos a trasplante.
• Adalimumab, infliximab, ustekinumab y vedolizumab para el tratamiento de la enfermedad de Crohn en pacientes
adultos.
Prestación farmacéutica
• Butlletí GeCoFarma. Generando conocimiento sobre la prestación farmacéutica (marzo de 2018). CatSalut.
Recomendaciones, informes, evaluaciones y guías
• Nuevas consultas farmacoterapéuticas publicadas en el CIM Virtual del CedimCat, servicio en línea de consultas de
medicamentos para profesionales
- Artritis reumatoide, tratamiento con etanercept y contracepción oral.
- Ranitidina y test del aliento en infección por Helicobacter pylori.
- Metformina en insuficiencia renal crónica.
Seguridad en el uso de medicamentos
• Prevención de errores de medicación en centros sociosanitarios. Butlletí de Prevenció d’Errors de Medicació de Cata-
lunya.
• Alertas de seguridad de fármacos. Newsletter 44 (marzo de 2018). Centre d’Informació de Medicaments de Catalunya.
• Información relacionada con alertas de seguridad de medicamentos: aácido valproico. Àrea del Medicament. Direc-
ció General d’Ordenació Professional i Regulació Sanitària. Servei Català de la Salut. Departament de Salut.
Información para vuestros pacientes
• Información sobre la alerta de seguridad relativa en la utilización de ácido valproico en mujeres en edad fértil.
Àrea del Medicament. Direcció General d’Ordenació Professional i Regulació Sanitària. Servei Català de la Salut. Departa-
ment de Salut.
Fecha de redacción: Marzo 2018
En el próximo número: Prescripción del ejercicio físico desde los centros de salud
Butlletí d’Informació Terapèutica del Departament de Salut de la Generalitat de Catalunya
Direcció: Josep Maria Argimon
Subdirecció: Joaquín Delgadillo
Coordinació editorial: Xavier Bonafont i Pujol
Coordinació de la Comissió d’Informació Terapèutica: Pilar López Calahorra
Comitè científic: Xavier Bonafont, Jordi Camarasa, Xavier Carné, Joan Costa, Laura Diego, Núria Escoda, Anna Feliu, Francesc de B. Ferrer, Pilar López, Roser Llop,
Josep Manuel Llop, Rosa Madridejos, Eduardo L. Mariño, Carlos Martín, Diego Mena, M. Àngels Parada, Alba Prat, Manel Rabanal, Laia Robert, Emília Sánchez,
Mónica Sanmartín, Amelia Troncoso, Noemí Villén
Secretaria Tècnica: Ester Saperas
Suport tècnic: CedimCat
ISSN: 1579-9441
Per a la reproducció total o parcial d’aquesta publicació, cal fer-ne la sol·licitud
a la Secretaria Tècnica de la Comissió d’Informació Terapèutica,
Gerència de Prestacions Farmacèutiques i Accés al Medicament, Travessera de les Corts, 131-159, 08007 Barcelona
Es poden consultar tots els números publicats des de l’any 1999 a:
http://medicaments.gencat.cat/ca/professionals/butlletins/butlleti-d-informacio-terapeutica-bit/
http://medicaments.gencat.cat/ca
BIT. Vol. 29 / núm. 2 / 2018 13
También podría gustarte
- Uso del Cannabis en la epilepsia refractaria infantilDe EverandUso del Cannabis en la epilepsia refractaria infantilAún no hay calificaciones
- Hipersensibilidadad AINESDocumento8 páginasHipersensibilidadad AINESJorge RodriguezAún no hay calificaciones
- Reacciones Adversas MedicamentosasDocumento4 páginasReacciones Adversas MedicamentosasLuis AntonioAún no hay calificaciones
- La Alergia A Los Medicamentos y Protocolos de Tratamiento PDFDocumento28 páginasLa Alergia A Los Medicamentos y Protocolos de Tratamiento PDFMiraldaperezAún no hay calificaciones
- El Libro de la Dieta Antiinflamatoria: Plan de 14 días para Sanar el Sistema inmunológico y Sentirte Mejor que NuncaDe EverandEl Libro de la Dieta Antiinflamatoria: Plan de 14 días para Sanar el Sistema inmunológico y Sentirte Mejor que NuncaCalificación: 4.5 de 5 estrellas4.5/5 (14)
- Clase 11 Relación Riesgo BeneficioDocumento4 páginasClase 11 Relación Riesgo BeneficioZabrinaletAún no hay calificaciones
- Proyecto de HipersensibilidadDocumento26 páginasProyecto de HipersensibilidadFriorela Miriam ALVARADO MELGAREJOAún no hay calificaciones
- Reacciones Adversas A MedicamentosDocumento10 páginasReacciones Adversas A MedicamentosAnyle MendozaAún no hay calificaciones
- Aines RamDocumento24 páginasAines RamAdri Aleja HerreraAún no hay calificaciones
- Alergia A AlimentosDocumento24 páginasAlergia A AlimentosjasonmAún no hay calificaciones
- Consensos - Reacciones Alergicas A Betalactamicos en Pediatria Recomendaciones para Su Diagnostico y Tratamiento 83Documento13 páginasConsensos - Reacciones Alergicas A Betalactamicos en Pediatria Recomendaciones para Su Diagnostico y Tratamiento 83maripaubravoAún no hay calificaciones
- Tema 2.3 FarmacologiaDocumento4 páginasTema 2.3 FarmacologiavalericsamAún no hay calificaciones
- Reacción Adversa A Fmrs 1 PDFDocumento8 páginasReacción Adversa A Fmrs 1 PDFluisillo007Aún no hay calificaciones
- Alergia A FármacosDocumento27 páginasAlergia A FármacosJoseergioAún no hay calificaciones
- Shock AnafilacticoDocumento13 páginasShock AnafilacticoWilliam Yesid Rodriguez MuñozAún no hay calificaciones
- Modulo 7 Alergias MedicamentosasDocumento13 páginasModulo 7 Alergias MedicamentosasAndrea PersiaAún no hay calificaciones
- Tema 21 TEORIA ALERGIA MEDICAMENTOSA 2020Documento25 páginasTema 21 TEORIA ALERGIA MEDICAMENTOSA 2020DRAKE LGAún no hay calificaciones
- 20 Ra Medicamentos GeneralidadesDocumento11 páginas20 Ra Medicamentos GeneralidadesErik TorresAún no hay calificaciones
- Capítulo 4. Toxicidad de Fármacos y EnvenenamientoDocumento6 páginasCapítulo 4. Toxicidad de Fármacos y EnvenenamientoGABRIEL MOCTEZUMAAún no hay calificaciones
- LECTURA 3B FarmacotoxiaDocumento12 páginasLECTURA 3B FarmacotoxiaAlondra Cortez LlaczaAún no hay calificaciones
- Reacciones Adversas A MedicamentosDocumento9 páginasReacciones Adversas A MedicamentosDavid BarreraAún no hay calificaciones
- Reacc Adversas de AnalgésicosDocumento7 páginasReacc Adversas de AnalgésicosDuniesky CancioAún no hay calificaciones
- Alergia A DrogasDocumento24 páginasAlergia A DrogasMstza MpAún no hay calificaciones
- AlergiasDocumento7 páginasAlergiasMU�OZ SEGURA LEONARDO SASHENKAAún no hay calificaciones
- Hi Per Sensibilidad EsDocumento37 páginasHi Per Sensibilidad EsBryan SandovalAún no hay calificaciones
- Reacciones Adversas A FarmacosDocumento38 páginasReacciones Adversas A FarmacosVíctor Ignacio Carrasco IriarteAún no hay calificaciones
- Alergia A MedicamentosDocumento53 páginasAlergia A MedicamentosSamanthavonDüsterchAún no hay calificaciones
- Manual de Alergia y Reacciones Adversas en La Práctica de La Salud BucalDocumento9 páginasManual de Alergia y Reacciones Adversas en La Práctica de La Salud BucalFernando Colli CastanedaAún no hay calificaciones
- Reacciones Adversas A Anestésicos LocalesDocumento8 páginasReacciones Adversas A Anestésicos Localescoolboy17Aún no hay calificaciones
- Lectura 2Documento30 páginasLectura 2JuanCarlosSoteloAún no hay calificaciones
- Alergia A MedicamentosDocumento21 páginasAlergia A MedicamentosivanAún no hay calificaciones
- Tipos de Efectos IndeseablesDocumento2 páginasTipos de Efectos IndeseablesPatricia Aranguren OspinaAún no hay calificaciones
- ESPrur06342 01Documento9 páginasESPrur06342 01Paola CastilloAún no hay calificaciones
- Ensayo de Alergia A Los MedicamentosDocumento8 páginasEnsayo de Alergia A Los MedicamentosDILSON DAVID OROZCO GOMEZAún no hay calificaciones
- REACCIONES ADVE-WPS OfficeDocumento2 páginasREACCIONES ADVE-WPS OfficeFabián PatrizAún no hay calificaciones
- Alergia A MedicamentosDocumento22 páginasAlergia A Medicamentosapi-3698281100% (3)
- Lectura Critica Farmaco IIDocumento5 páginasLectura Critica Farmaco IIthreysiAún no hay calificaciones
- Alergia y AnestesiaDocumento4 páginasAlergia y AnestesiaIngrid Pisfil Quiroz100% (1)
- Ram e Interacciones FarmacologicasDocumento48 páginasRam e Interacciones FarmacologicasDudley PadillaAún no hay calificaciones
- Toxicidad de Los FármacosDocumento37 páginasToxicidad de Los FármacosMendoza Rodríguez Danna MichelleAún no hay calificaciones
- Als 221 MDocumento4 páginasAls 221 MRosa ItzelAún no hay calificaciones
- Aines y Morbobilidades PDFDocumento7 páginasAines y Morbobilidades PDFPablo RojasAún no hay calificaciones
- TEMA 2. Reacciones Adversas e Interacciones Medicamentosas. FarmacovigilanciaDocumento9 páginasTEMA 2. Reacciones Adversas e Interacciones Medicamentosas. Farmacovigilancialesyani barrosoAún no hay calificaciones
- DINAMICA 5 (Resumen)Documento5 páginasDINAMICA 5 (Resumen)Juan FernándezAún no hay calificaciones
- 5 Reaccion Adversa A MedicamentosDocumento54 páginas5 Reaccion Adversa A MedicamentosYuly Hoyos HidalgoAún no hay calificaciones
- 2-Interacciones y Reacciones AdversasDocumento26 páginas2-Interacciones y Reacciones Adversasnelsolis7Aún no hay calificaciones
- REACCIONES ADVERSAS A MEDICAMENTOs.Documento5 páginasREACCIONES ADVERSAS A MEDICAMENTOs.carl.737.boAún no hay calificaciones
- Intoxicaciones Por Medicamento 3Documento5 páginasIntoxicaciones Por Medicamento 3Enfermera Adriana VelezAún no hay calificaciones
- Guia Practica Clinica-HISTAMINOSISDocumento5 páginasGuia Practica Clinica-HISTAMINOSISMarlenin FernandezAún no hay calificaciones
- Alergia AinesDocumento7 páginasAlergia AinesFlip VillaAún no hay calificaciones
- Guía Del Estudiantes 710.99Documento4 páginasGuía Del Estudiantes 710.99Maredi LaredoAún no hay calificaciones
- Farmacología en Enfermería 2012 PDFDocumento18 páginasFarmacología en Enfermería 2012 PDFRainyDevilAún no hay calificaciones
- Lesiones Por Fármacos Terapéuticos y Drogas de Abuso (Unidad I Tema 7)Documento6 páginasLesiones Por Fármacos Terapéuticos y Drogas de Abuso (Unidad I Tema 7)leonardo flores100% (1)
- Alergia A Los AINESDocumento7 páginasAlergia A Los AINESDILSON DAVID OROZCO GOMEZAún no hay calificaciones
- Aines Recomendaciones de Expo 1Documento9 páginasAines Recomendaciones de Expo 1EH LeynaAún no hay calificaciones
- Intolerancias e Intoxicaciones AlimentariasDocumento7 páginasIntolerancias e Intoxicaciones AlimentariasKAREN TATIANA RICO CARABALIAún no hay calificaciones
- SEAIC Guia MEDICAMENTOS PDFDocumento42 páginasSEAIC Guia MEDICAMENTOS PDFJesus Eduardo Ruiz DiazAún no hay calificaciones
- Virus y Bacterias en Banano y PlátanoDocumento8 páginasVirus y Bacterias en Banano y PlátanoYAz Lizette100% (1)
- Manejo Cerda ReemplazoDocumento26 páginasManejo Cerda ReemplazoEdi CastellanosAún no hay calificaciones
- Soapie - LeddyDocumento4 páginasSoapie - LeddyLeddy Rebaza89% (9)
- presentación/ULCERAS POR PRESIÓNDocumento29 páginaspresentación/ULCERAS POR PRESIÓNPatricia de la o100% (2)
- Los Mecanismos Hemodinámicos Del Síndrome Cardiorrenal Se Refieren A Las Alteraciones en El Flujo Sanguíneo y La Presión Que Se Producen Por La Disfunción Cardiaca o RenalDocumento1 páginaLos Mecanismos Hemodinámicos Del Síndrome Cardiorrenal Se Refieren A Las Alteraciones en El Flujo Sanguíneo y La Presión Que Se Producen Por La Disfunción Cardiaca o RenalMaCa ParedesAún no hay calificaciones
- Dilutores Equino AdicionalDocumento8 páginasDilutores Equino AdicionalLuis Esplana IzarraAún no hay calificaciones
- Molusco ContagiosoDocumento10 páginasMolusco ContagiosoChristian MartínezAún no hay calificaciones
- Examen Sistemas de Produccion Horticolas y Fruticolas 7Documento1 páginaExamen Sistemas de Produccion Horticolas y Fruticolas 7NNNAún no hay calificaciones
- Conducción Defensiva Vehículos Livianos - MFDocumento43 páginasConducción Defensiva Vehículos Livianos - MFPablo Donoso0% (1)
- Enfermeria 2023Documento1 páginaEnfermeria 2023Eigna GafaAún no hay calificaciones
- Movimientos Ritmico1Documento15 páginasMovimientos Ritmico1Mª ÁngelesAún no hay calificaciones
- 3 Pasos Claves para Tomar y Leer EkgDocumento14 páginas3 Pasos Claves para Tomar y Leer EkgCristian VillanuevaAún no hay calificaciones
- Nom 031 STPS 2011Documento48 páginasNom 031 STPS 2011DanielTrujillo100% (1)
- Ficha AmpicilinaDocumento4 páginasFicha AmpicilinaAida TeneAún no hay calificaciones
- Cirugia General Manual Residente 2011Documento74 páginasCirugia General Manual Residente 2011Traw OnAún no hay calificaciones
- Enlace de Turno en EnfermeriaDocumento13 páginasEnlace de Turno en EnfermeriaGeeder Noh100% (1)
- Maribel Formato v2Documento44 páginasMaribel Formato v2Fredy DextreAún no hay calificaciones
- Informe 2019Documento31 páginasInforme 2019Héctor JiménezAún no hay calificaciones
- Programa Neuroanatomia FuncionalDocumento6 páginasPrograma Neuroanatomia FuncionalSara MarquezAún no hay calificaciones
- Exposicion de La Lactancia MaternaDocumento162 páginasExposicion de La Lactancia MaternaGabriela Garcia Ordoñez100% (1)
- Administración de Recursos Humanos en Una Clínica IiDocumento8 páginasAdministración de Recursos Humanos en Una Clínica IiMeghan CruzAún no hay calificaciones
- TTO CASO HipocondriacoDocumento21 páginasTTO CASO HipocondriacodiapositivasAún no hay calificaciones
- Quehacer FinalDocumento29 páginasQuehacer FinalConstanza Valentina Toledo VillegasAún no hay calificaciones
- Anatomía Del CorazónDocumento6 páginasAnatomía Del CorazónSebastian BrandAún no hay calificaciones
- CeliacosDocumento4 páginasCeliacostzecretoAún no hay calificaciones
- Los Reales Beneficios Del Sauna Baño Turco y JacuzziDocumento3 páginasLos Reales Beneficios Del Sauna Baño Turco y JacuzziPriscilaDiBartoloAún no hay calificaciones
- Sin Título-1 PDFDocumento1 páginaSin Título-1 PDFJhojan Mejia FernandezAún no hay calificaciones
- Tos FerinaDocumento20 páginasTos Ferinacrysmari hernandezAún no hay calificaciones
- Respuestas Guia de Ejercicios N9Documento3 páginasRespuestas Guia de Ejercicios N9Alejandro Rendic50% (2)
- Pruebas de Miembro InferiorDocumento24 páginasPruebas de Miembro InferiorJose Alan Rivera ViverosAún no hay calificaciones
- Más vida con hábitos saludablesDe EverandMás vida con hábitos saludablesCalificación: 4.5 de 5 estrellas4.5/5 (8)
- Cuerpo Tóxico: Como Liberar Tu Cuerpo De Las Toxinas Externas E Internas, Y Evitar Asi Los Efectos De Los Radicales LibresDe EverandCuerpo Tóxico: Como Liberar Tu Cuerpo De Las Toxinas Externas E Internas, Y Evitar Asi Los Efectos De Los Radicales LibresCalificación: 5 de 5 estrellas5/5 (2)
- En sintonía con tu ciclo femenino: FLO. Aprende a sincronizarte con tu bioquímica para dar rienda suelta a tu creatividad, mejorar tu vida y hacer más con menos estrésDe EverandEn sintonía con tu ciclo femenino: FLO. Aprende a sincronizarte con tu bioquímica para dar rienda suelta a tu creatividad, mejorar tu vida y hacer más con menos estrésCalificación: 4.5 de 5 estrellas4.5/5 (11)
- Los 12 chakras: Desbloquea tus dones espiritualesDe EverandLos 12 chakras: Desbloquea tus dones espiritualesCalificación: 4 de 5 estrellas4/5 (14)
- Tu cerebro tiene hambre: 5 grandes cambios que te ayudarán a perder grasa y ganar saludDe EverandTu cerebro tiene hambre: 5 grandes cambios que te ayudarán a perder grasa y ganar saludCalificación: 5 de 5 estrellas5/5 (8)
- Un intestino feliz. Cómo la microbiota mejora tu salud mental y te ayuda a manejar las emocionesDe EverandUn intestino feliz. Cómo la microbiota mejora tu salud mental y te ayuda a manejar las emocionesCalificación: 5 de 5 estrellas5/5 (4)
- El concepto Mulligan de terapia manual (Color)De EverandEl concepto Mulligan de terapia manual (Color)Calificación: 5 de 5 estrellas5/5 (3)
- Muchas Vidas, Muchos Sabios (Many Lives, Many Masters): (Many Lives, Many Masters)De EverandMuchas Vidas, Muchos Sabios (Many Lives, Many Masters): (Many Lives, Many Masters)Calificación: 4 de 5 estrellas4/5 (475)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- Por qué dormimos: La nueva ciencia del sueñoDe EverandPor qué dormimos: La nueva ciencia del sueñoCalificación: 4.5 de 5 estrellas4.5/5 (23)
- Flores de Bach Recursos y estrategias terapéuticasDe EverandFlores de Bach Recursos y estrategias terapéuticasCalificación: 3.5 de 5 estrellas3.5/5 (3)
- Entrenamiento Científico con pesas: Fitness InteligenteDe EverandEntrenamiento Científico con pesas: Fitness InteligenteCalificación: 5 de 5 estrellas5/5 (3)
- CAMBIA TU CEREBRO CAMBIA TU VIDA: CAMBIA TU CEREBRO CAMBIA TU VIDADe EverandCAMBIA TU CEREBRO CAMBIA TU VIDA: CAMBIA TU CEREBRO CAMBIA TU VIDACalificación: 3.5 de 5 estrellas3.5/5 (38)
- Ondas de choque extracorpóreas radiales: Aplicación en patologías músculo esqueléticasDe EverandOndas de choque extracorpóreas radiales: Aplicación en patologías músculo esqueléticasCalificación: 5 de 5 estrellas5/5 (3)
- GuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisDe EverandGuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisCalificación: 4 de 5 estrellas4/5 (9)
- Un plan de vida con calidad para después de los 50: Nunca es tarde para planear el resto de su vidaDe EverandUn plan de vida con calidad para después de los 50: Nunca es tarde para planear el resto de su vidaCalificación: 4.5 de 5 estrellas4.5/5 (119)
- Sana tu Cuerpo, Calma tu Mente: Desintoxicar Hígado, Intestino Permeable, Salud Hormonal, Curación Emocional, Relajación, Ansiedad y Sanidad mental, Atención Plena, Psicoterapia y NutriciónDe EverandSana tu Cuerpo, Calma tu Mente: Desintoxicar Hígado, Intestino Permeable, Salud Hormonal, Curación Emocional, Relajación, Ansiedad y Sanidad mental, Atención Plena, Psicoterapia y NutriciónCalificación: 5 de 5 estrellas5/5 (4)
- Manual de ortopedia maxilar: Modelo diagnóstico de maloclusiones para pacientes en crecimientoDe EverandManual de ortopedia maxilar: Modelo diagnóstico de maloclusiones para pacientes en crecimientoCalificación: 4.5 de 5 estrellas4.5/5 (14)
- El Tesoro Escondido (Hidden Treasure): La vida interior de niños y adolescentes. Terapia infanto-juvenilDe EverandEl Tesoro Escondido (Hidden Treasure): La vida interior de niños y adolescentes. Terapia infanto-juvenilCalificación: 5 de 5 estrellas5/5 (4)
- Despierta a las diosas que hay en ti: Nueve arquetipos para sanar y transformar tu vida con lo sagrado femeninoDe EverandDespierta a las diosas que hay en ti: Nueve arquetipos para sanar y transformar tu vida con lo sagrado femeninoCalificación: 5 de 5 estrellas5/5 (1)
- La medicina biorreguladora: Un enfoque holístico e innovador de la autocuraciónDe EverandLa medicina biorreguladora: Un enfoque holístico e innovador de la autocuraciónCalificación: 3.5 de 5 estrellas3.5/5 (2)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- Puntos gatillo y cadenas musculares funcionales en osteopatía y terapia manual (Bicolor)De EverandPuntos gatillo y cadenas musculares funcionales en osteopatía y terapia manual (Bicolor)Calificación: 4.5 de 5 estrellas4.5/5 (23)
- Las Enfermedades comienzan y terminan en tu mente: Una guía para la autosanaciónDe EverandLas Enfermedades comienzan y terminan en tu mente: Una guía para la autosanaciónCalificación: 4 de 5 estrellas4/5 (4)
- Fundamentos de medicina tradicional chinaDe EverandFundamentos de medicina tradicional chinaCalificación: 4.5 de 5 estrellas4.5/5 (5)