Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Informe 2 - Enlace Químico
Cargado por
Naomi Blas Julca0 calificaciones0% encontró este documento útil (0 votos)
26 vistas4 páginasTítulo original
INFORME 2 - ENLACE QUÍMICO
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
26 vistas4 páginasInforme 2 - Enlace Químico
Cargado por
Naomi Blas JulcaCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 4
UNIVERSIDAD CIENTÍFICA DEL SUR
FACULTAD DE: MEDICINA VETERINARIA Y ZOOTECNIA
LABORATORIO DE QUÍMICA
CURSO: QUÍMICA
PROFESORAS: GLADYS GASPAR LA CRUZ
INFORME DE PRÁCTICAS
PRÁCTICA N°: 2
TÍTULO: ENLACE QUÍMICO
ESTUDIANTE:
• NAOMI EMILIA BLAS JULCA
LIMA – PERÚ 2022
INFORME 2
ENLACE QUIMICO
IV. Datos y resultados
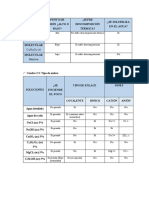
✓ Cuadro 4.2: Propiedades de los compuestos moleculares y iónicos.
Punto de fusión Descomposición térmica Solubilidad enagua ¿Se Tipo de
Sustancia
¿Alto o bajo? ¿Se descompone? disuelve en agua? compuesto
Cloruro de sodio NaCl (s) Alto No Si Iónico
Sacarosa
Bajo Si Si Covalente
C(12)H22O11 (s)
Manteca
Bajo Si No Iónico
Mezcla de triglicéridos (s)
✓ Cuadrado 4.3: Tipo de enlace
¿SE ENCIENDE EL TIPO DE ENLACE IONES
SOLUCIONES
FOCO? COVALENTE IÓNICO CATIÓN ANIÓN
Agua destilada No ✓ - X X
Mg +1
Agua de caño Si - ✓ Na+1 OH
Ca+
NaCl (ac) 5% Si - ✓ Na+1 Cl+-1
NaOH (ac) 5% Si - ✓ Na+1 OH-1
CuSO4 (ac) 5% Si - ✓ Cu+2 SO4 -2
C12H 22O11 (ac) 5% No - - - -
MgCl2 (ac) 5% Si ✓ - Mg+2 Cl2-1
C2H 5OH (ac) 5% No ✓ - - -
CH 3COOH concentrado No ✓ - - -
CH 3 COOH (ac) 5% Si ✓ - H+1 CH3COO-1
CH 3 – CO – CH 3 (ac) 5% No ✓ - - -
✓ Cuadrado 4.4: Polaridad molecular
MISCIBLE EN: TIPO DE MOLÉCULA
COMPUESTO MOLECULAR
Agua n - hexano Polar Apolar
CH 3 OH (p.a.) ✓ - ✓ -
C2H 5OH (p.a.) ✓ - ✓ -
CH 3 – CO – CH 3 (p.a.) ✓ - ✓ -
CHCl3 (p.a.) ✓ ✓ ✓ ✓
CH 3COOH (p.a.) ✓ - ✓ -
C3H 7OH (p.a.) ✓ - ✓ -
C12H 22O11 (p.a.) ✓ - ✓ -
(NH 2 )2CO (p.a.) ✓ - ✓ -
Triglicérido (aceite vegetal) - ✓ - ✓
CUESTIONARIO
1. Representar mediante la simbología de Lewis y la regla del octeto, 4 sustancias
iónicas que determinó en la práctica.
2. Representar mediante la simbología de Lewis y la regla del octeto, 4 sustancias
moleculares que determinó en la práctica.
3. ¿Por qué el NaOH acuoso conduce la corriente eléctrica y el CH 3 OH acuoso no
conduce la corriente eléctrica sin en ambos se observa el grupo OH?
Ambos compuestos tienen propiedades distintas.
El hidróxido de sodio (NaOH) se disocia en iones: Na+ y OH- presentando enlace
iónico fuerte, y por ello excelente conductividad eléctrica. El CH3OH presenta
enlace covalente porque se separan en iones, por lo tanto, no conduce electricidad.
4. Describa el funcionamiento de los hornos de microondas.
El horno de microondas funciona a través de ondas electromagnéticas en la
frecuencia de las microondas. Las sustancias presentes en los alimentos absorben
la energía del microondas en un proceso llamado calentamiento dieléctrico. En el
mencionado proceso, hay moléculas girando en su entorno intentando alinearse
con el campo eléctrico de las microondas, donde estas chocan con otras,
dispersando así la energía en forma de calor.
5. Explica la naturaleza de la dinamita, el inverso de Alfred Nobel.
En 1867 Nobel consiguió fabricar la dinamita, mezclando la nitroglicerina con un
material absorbente (la tierra de diatomeas), así obtuvo un polvo que se podía
percutir e, incluso, quemar el aire libre sin que explotara.
También podría gustarte
- Quim 03 ENLACE QUIMICODocumento5 páginasQuim 03 ENLACE QUIMICOHady Quispe LeónAún no hay calificaciones
- Cuadro de Datos y ResultadosDocumento3 páginasCuadro de Datos y ResultadosValentina Roman SantivañezAún no hay calificaciones
- Informe de Práctica N°2Documento6 páginasInforme de Práctica N°2MarjiAún no hay calificaciones
- Química - Informe 3Documento6 páginasQuímica - Informe 3ruben usquianoAún no hay calificaciones
- Informe de Laboratorio 2Documento13 páginasInforme de Laboratorio 2valeriaAún no hay calificaciones
- PRÁCTICA NO 6, 7 y 8Documento3 páginasPRÁCTICA NO 6, 7 y 8Rony O. MartinezAún no hay calificaciones
- Practica 05Documento5 páginasPractica 05Ana Lucia Vasquez JesusAún no hay calificaciones
- Informe Qumica Practica 4Documento2 páginasInforme Qumica Practica 4Xiomara RiveraAún no hay calificaciones
- Falta CuadroDocumento10 páginasFalta CuadroWalter Obregón SánchezAún no hay calificaciones
- Informe N°2 Química Laboratorio Enlaces Químicos Grupo 2Documento10 páginasInforme N°2 Química Laboratorio Enlaces Químicos Grupo 2Himiko TogaAún no hay calificaciones
- Informe Enlace Químico. TDocumento6 páginasInforme Enlace Químico. THyperWillAún no hay calificaciones
- Informe 4 - Química General - PrácticaDocumento6 páginasInforme 4 - Química General - PrácticaMelania Ghisel Sanchez HerasAún no hay calificaciones
- Tema 7Documento25 páginasTema 7Gloria Quetzaly Zavala VazquezAún no hay calificaciones
- Solubilidad KpsDocumento15 páginasSolubilidad KpsRonaldo BrionesAún no hay calificaciones
- Informe 2 de QuimicaDocumento5 páginasInforme 2 de Quimicaguayando041Aún no hay calificaciones
- Presentacion Webinar PresentadoDocumento26 páginasPresentacion Webinar Presentadocalamaroo10Aún no hay calificaciones
- Compuesto QuimicoDocumento6 páginasCompuesto QuimicoLucas LancharesAún no hay calificaciones
- PRL8 - 2B - IQ-444 - Transferencia de Masa I (R) - Ing - Quimica - KEscalanteDocumento19 páginasPRL8 - 2B - IQ-444 - Transferencia de Masa I (R) - Ing - Quimica - KEscalanteJean Pierre Cirilo SosaAún no hay calificaciones
- Informe de Laboratorio 3 IMPRIMIRDocumento9 páginasInforme de Laboratorio 3 IMPRIMIRDaisuke BasadoAún no hay calificaciones
- Trabajo Práctico 8 - InorgánicaDocumento5 páginasTrabajo Práctico 8 - InorgánicaZoe SpamerAún no hay calificaciones
- Constante ÁcidaDocumento5 páginasConstante ÁcidaJuanse ParoliAún no hay calificaciones
- Informe 11Documento10 páginasInforme 11Gabriela Cardenas GuzmanAún no hay calificaciones
- Quimica ConchatumadreDocumento8 páginasQuimica ConchatumadreAndres Lozano Apaza100% (2)
- Resultados Practica 6Documento25 páginasResultados Practica 6Juan Carlos Portillo VillarruelAún no hay calificaciones
- Unidad 4-Parte A-Estequiometrà A Tpos de Reacciones Qumicas Balanceo de Ecuaciones ACTUALIZADA JUNIO 2020Documento13 páginasUnidad 4-Parte A-Estequiometrà A Tpos de Reacciones Qumicas Balanceo de Ecuaciones ACTUALIZADA JUNIO 2020Camila RogerAún no hay calificaciones
- Informe Quimica 2Documento10 páginasInforme Quimica 2Dayana NaranjoAún no hay calificaciones
- Informe 3 Quimica AnalíticaDocumento4 páginasInforme 3 Quimica AnalíticaJaroll RodríguezAún no hay calificaciones
- Lab 2 Ok. REACCIONES QUIMICAS y PROPIEDADES PERIODICASDocumento18 páginasLab 2 Ok. REACCIONES QUIMICAS y PROPIEDADES PERIODICASadan schneider julian sotoAún no hay calificaciones
- Quimica Virtual 6 - Reacciones QuimicasDocumento16 páginasQuimica Virtual 6 - Reacciones QuimicasLeoAún no hay calificaciones
- 2022.2S LAB-QO1 Guía para La Elaboración de ProtocolosDocumento14 páginas2022.2S LAB-QO1 Guía para La Elaboración de ProtocolosJosue OlivaAún no hay calificaciones
- Hernández Troncozo Logan David Act2Documento3 páginasHernández Troncozo Logan David Act2liz100% (1)
- Tema v. 1 Alcohóles (Teoría)Documento5 páginasTema v. 1 Alcohóles (Teoría)Yefrain J. ArzolayAún no hay calificaciones
- CUESTIONARIOLABANALITICADocumento13 páginasCUESTIONARIOLABANALITICAValeria LeónAún no hay calificaciones
- CUESTIONARIOLABANALITICADocumento13 páginasCUESTIONARIOLABANALITICAValeria LeónAún no hay calificaciones
- QAI Segunda Fase Segunda UnidadDocumento21 páginasQAI Segunda Fase Segunda UnidadAraceli MayeliAún no hay calificaciones
- Informe de Laboratorio 3 IMPRIMIRDocumento8 páginasInforme de Laboratorio 3 IMPRIMIRCarolAlvarado0% (1)
- Filemd8544-2023-11-18 20-03-55Documento35 páginasFilemd8544-2023-11-18 20-03-55Blancanelly ruiz peraltaAún no hay calificaciones
- Reacciones Químicas Primera Parte 2023Documento33 páginasReacciones Químicas Primera Parte 2023laboratoriodecienciasbiologiaAún no hay calificaciones
- Tema 6. Equilibrios en Disolución Acuosa. Ácido-BaseDocumento32 páginasTema 6. Equilibrios en Disolución Acuosa. Ácido-BaseCésarAún no hay calificaciones
- Cuaderno de Info 2Documento9 páginasCuaderno de Info 2Wily GarciaAún no hay calificaciones
- 29 y 30 Estados de La Materia. Sólidos. Diagramas de Fase (12y13.07.2021) (T)Documento14 páginas29 y 30 Estados de La Materia. Sólidos. Diagramas de Fase (12y13.07.2021) (T)Alessandro Cabezas MedinaAún no hay calificaciones
- Informe FQ 1Documento4 páginasInforme FQ 1juan pabloAún no hay calificaciones
- Disolucion de SalesDocumento9 páginasDisolucion de SalesStefany XiomAra B SAún no hay calificaciones
- Guía de Práctica Laboratorio - Quimica General 2022-2Documento10 páginasGuía de Práctica Laboratorio - Quimica General 2022-2Jossue MolinaAún no hay calificaciones
- Informe 2Documento2 páginasInforme 2Mathias Fabrizio Oliveros TamayoAún no hay calificaciones
- Informe 2 Reaciones Quimica 2020Documento12 páginasInforme 2 Reaciones Quimica 2020Sergio SusaraAún no hay calificaciones
- 1586 - Reporte 8 de Laboratorio VirtualDocumento7 páginas1586 - Reporte 8 de Laboratorio VirtualFiorela VargasAún no hay calificaciones
- Complementario NaturalesDocumento19 páginasComplementario NaturalesJulián David Narváez SepúlvedaAún no hay calificaciones
- Química Orgánica - Sem-13 - Sesión-37 - 2022-2Documento32 páginasQuímica Orgánica - Sem-13 - Sesión-37 - 2022-2CCAún no hay calificaciones
- Química Orgánica - Sem-13 - Sesión-13 - 2021-2Documento34 páginasQuímica Orgánica - Sem-13 - Sesión-13 - 2021-2LisbethAún no hay calificaciones
- Informe Tabla PeriodicaDocumento18 páginasInforme Tabla PeriodicaJhonatan Santa Cruz CamposAún no hay calificaciones
- Reacciones QuímicasDocumento48 páginasReacciones QuímicasWilly frey Idrogo diazAún no hay calificaciones
- Pract. # 7 Fo-Doc-112Documento6 páginasPract. # 7 Fo-Doc-112daniel camilo florez santanaAún no hay calificaciones
- CristalizacionDocumento36 páginasCristalizacionAnonymous FYhiqo7uPAún no hay calificaciones
- CuestionarioDocumento5 páginasCuestionarioEva CaballeroAún no hay calificaciones
- Clase SolucionesDocumento70 páginasClase Solucionesdavid zambranoAún no hay calificaciones
- Trabajo Enlace QuimicoDocumento10 páginasTrabajo Enlace QuimicobuenaventuuraAún no hay calificaciones
- 2 Fundamentos TermodinamicosDocumento74 páginas2 Fundamentos TermodinamicosCristian Gonzalo Urbina UrbinaAún no hay calificaciones
- Informe Reacciones Químicas Grupo 12Documento9 páginasInforme Reacciones Químicas Grupo 12DaniiAún no hay calificaciones
- Contrato PDFDocumento1 páginaContrato PDFNaomi Blas JulcaAún no hay calificaciones
- Actividad 01 - Semana 1 - BiologiaDocumento3 páginasActividad 01 - Semana 1 - BiologiaNaomi Blas JulcaAún no hay calificaciones
- Informe 12 - Propiedades Químicas Aminoácidos y ProteínasDocumento6 páginasInforme 12 - Propiedades Químicas Aminoácidos y ProteínasNaomi Blas JulcaAún no hay calificaciones
- Informe 9 - Propiedades Generales de Los Alcoholes y FenolesDocumento5 páginasInforme 9 - Propiedades Generales de Los Alcoholes y FenolesNaomi Blas JulcaAún no hay calificaciones
- Informe 3 - Reacciones Químicas en Disolución AcuosaDocumento10 páginasInforme 3 - Reacciones Químicas en Disolución AcuosaNaomi Blas JulcaAún no hay calificaciones
- Informe 1 - Identificación Manejo de Equipos y Materiales de Laboratorio PDFDocumento13 páginasInforme 1 - Identificación Manejo de Equipos y Materiales de Laboratorio PDFNaomi Blas JulcaAún no hay calificaciones
- DIAGRAMA de POURBAIX Y Procesos Unitarios de Oxidación y ReducciónDocumento3 páginasDIAGRAMA de POURBAIX Y Procesos Unitarios de Oxidación y Reducciónhug martinez leccaAún no hay calificaciones
- Formato de Mantenimiento de Servicios Generales 2Documento3 páginasFormato de Mantenimiento de Servicios Generales 2josue bravoAún no hay calificaciones
- Guia Ejercicios Analisis Instrumental N°4-2022Documento3 páginasGuia Ejercicios Analisis Instrumental N°4-2022ChasconaAún no hay calificaciones
- Taller de Nomenclatura Quimica 2020-2Documento3 páginasTaller de Nomenclatura Quimica 2020-2juanes cortesAún no hay calificaciones
- ACIDEZ Y BASICIDAD. II Corte.Documento15 páginasACIDEZ Y BASICIDAD. II Corte.SeliannyAún no hay calificaciones
- Thermolift EsDocumento26 páginasThermolift EsIssamAún no hay calificaciones
- Datos de Data Bank YausDocumento3 páginasDatos de Data Bank YausJared PérezAún no hay calificaciones
- VALVULAS DE SEGURIDAD Y DISPOSITIVOS DE ALIVIO Final 1Documento351 páginasVALVULAS DE SEGURIDAD Y DISPOSITIVOS DE ALIVIO Final 1Daniel VazquezAún no hay calificaciones
- Historia de La RefrigeracionDocumento9 páginasHistoria de La Refrigeracionmuricio tapias llerenaAún no hay calificaciones
- Practico N°4 - Gravimetria - 2023Documento2 páginasPractico N°4 - Gravimetria - 2023ivan RicaldezAún no hay calificaciones
- SISTEMA "DRYWALL" ¿Ventaja o Desventaja Ingenieril - UNPRGDocumento23 páginasSISTEMA "DRYWALL" ¿Ventaja o Desventaja Ingenieril - UNPRGAnonymous F9t6qljCF75% (4)
- Ejercicios 8. Espectrofotometría Emisión y Absorción AtómicaDocumento3 páginasEjercicios 8. Espectrofotometría Emisión y Absorción AtómicaMeliza López100% (1)
- EmulsionDocumento44 páginasEmulsionKarina CastroAún no hay calificaciones
- Tugas Kimia AlipDocumento3 páginasTugas Kimia Alipgamersakti024Aún no hay calificaciones
- Leyes de Los GasesDocumento42 páginasLeyes de Los GasesNicoleAún no hay calificaciones
- 02-Billete 005milDocumento2 páginas02-Billete 005milDiana AyalaAún no hay calificaciones
- Biofisica Reacciones AcopladasDocumento2 páginasBiofisica Reacciones AcopladasKEVINAún no hay calificaciones
- EVAPORADORESDocumento22 páginasEVAPORADORESJairo TiconaAún no hay calificaciones
- 2018 ASHRAE Handbook - Refrigeration SI PDF 51-75Documento25 páginas2018 ASHRAE Handbook - Refrigeration SI PDF 51-75Adrian Rentfleich100% (1)
- Balance Metalurgico Grupo 3 Procesamiento de MineralesDocumento4 páginasBalance Metalurgico Grupo 3 Procesamiento de MineralesNando SalaverryAún no hay calificaciones
- Aislamiento de CloroplastosDocumento8 páginasAislamiento de CloroplastosAngelica RestrepoAún no hay calificaciones
- Barniz Rojo 3m 1602Documento19 páginasBarniz Rojo 3m 1602princesa762Aún no hay calificaciones
- Acid FoamDocumento6 páginasAcid FoamLolita Jiménez AlvaradoAún no hay calificaciones
- Guia8 Grado11°2021Documento5 páginasGuia8 Grado11°2021Sergio MásterAún no hay calificaciones
- Cuestionario 1 Industria PetroquimicaDocumento4 páginasCuestionario 1 Industria PetroquimicaIván Helmerd SalasAún no hay calificaciones
- Determinación Del Contenido de Calcio y Magnesio Por Volumetría ComplexometricaDocumento4 páginasDeterminación Del Contenido de Calcio y Magnesio Por Volumetría ComplexometricaDamaris Pantoja LaraAún no hay calificaciones
- Bme Psicrometria Humedad y SaturacionDocumento11 páginasBme Psicrometria Humedad y SaturacionLuis EnriqueAún no hay calificaciones
- Preparacion Del ElectrodoDocumento4 páginasPreparacion Del ElectrodoTere Torres PAún no hay calificaciones
- Desinfectante de Ambientes Aerosol Campos de LavandaDocumento1 páginaDesinfectante de Ambientes Aerosol Campos de LavandaFely UruñaAún no hay calificaciones
- Analisis Estadistico Metalurgico (1) AvanceDocumento18 páginasAnalisis Estadistico Metalurgico (1) AvanceJP VSAún no hay calificaciones