Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Tubulopatías (Soneivi)
Cargado por
Victor MonsalveTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Tubulopatías (Soneivi)
Cargado por
Victor MonsalveCopyright:
Formatos disponibles
TUBULOPATÍAS
GENERALIDADES
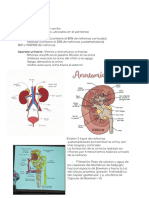
El aparato urinario está constituido por los dos riñones, los uréteres, la vejiga y la
uretra. A los riñones se les compete la mayor parte de la actividad del aparato urinario, el
resto son vías de paso. Una vez que los riñones filtran el plasma sanguíneo, devuelven la
mayor parte del agua y los solutos al torrente sanguíneo, los restantes constituyen la
orina, que pasa por los uréteres y se almacena en la vejiga hasta que es evacuada a través
de la uretra.
Entonces, los riñones son órganos pares, rojizos, en forma de “frijol”, situados en
los flancos, retroperitoneales, ubicados entre T12 y L3, protegidos parcialmente por la
11º-12º costillas, estando el derecho un poco más descendido que el izquierdo.
Las funciones de los riñones son:
- Regulación de la composición iónica de la sangre (Na+, K+, Ca++, Cl-,
HPO42-).
- Regulación del pH sanguíneo (excreción de H+, conservación de HCO3-).
- Regulación del volumen plasmático (H2O).
- Regulación de la Presión Arterial (H2O, Renina).
- Mantenimiento de la osmolaridad sanguínea (entendida como una
medida del número total de partículas disueltas por litro de solución).
VN: 300 mOsm/L.
- Producción de hormonas (Calcitriol, eritropoyetina).
- Regulación de la concentración de glucosa sanguínea (Como el hígado,
los riñones pueden usar glutamina para la gluconeogénesis).
- Excreción de desechos y sustancias extrañas (amoníaco, urea,
creatinina, bilirrubina, ácido úrico, fármacos, toxinas ambientales).
Son estructuras muy vascularizadas (reciben 20-25% del gasto cardiaco por las Arterias
renales, el flujo sanguíneo renal –FSR- en un adulto sano es de alrededor de 1200
mL/minuto). Las arterias renales se dividen en: Segmentarias, interlobulares, arcuatas,
interlobulillares y finalmente arteriolas eferentes dentro de la corteza renal, cada una de
las cuales va a una nefrona dividiéndose en una red capilar en forma de ovillo: el
glomérulo. Los capilares glomerulares se reúnen formando la arteriola eferente, que se
ramifican para formar los capilares peritubulares y los vasos rectos. Pasan a formarse las
vénulas peritubulares, venas interlobulillares, venas arcuatas, venas interlobulares y se
Tubulopatías (Soneivi Henríquez) Página 1
unen para abandonar el riñón en la vena renal. La inervación se da a través del ganglio
celíaco, a través del plexo renal (parte del Sistema Nervioso Autónomo Simpático).
Tiene en su estructura 3 capas: Capsula fibrosa (t. conectivo denso irregular), cápsula
adiposa y fascia renal (t. conectivo denso irregular). Un corte frontal del riñón nos muestra
dos regiones que juntas constituyen el parénquima renal (PORCIÓN FUNCIONAL DEL
RIÑÓN):
- Corteza renal: Se ubica entre el borde y las bases de las pirámides y
entre ellas (como columnas renales).
- Médula renal: Presenta entre 8 y 18 pirámides renales cónicas, cada una
de las cuales posee una base dirigida a la corteza y un vértice o papila
que se orienta al hilio renal.
Dentro del parénquima se encuentran las UNIDADES FUNCIONALES DEL RIÑÓN: 1
MILLÓN DE NEFRONAS (80-85% corticales, 15-20% yuxtamedulares), las cuales drenan a
través de las papilas hacia los cálices menores (8 a 18), luego los mayores (2 a 3), pelvis
renal para ir al uréter y la vejiga. Cada nefrona consta de dos partes:
- Corpúsculo renal: Donde se filtra el plasma sanguíneo. Incluye el
glomérulo y la cápsula glomerular de Bowman.
- Túbulos renales: Hacia el cual pasa el líquido filtrado en la cápsula de
Bowman, divididos en:
1. Túbulo contorneado proximal (TCP): Parte del túbulo unida a la cápsula
glomerular.
2. Asa de Henle: Se extiende hacia la médula renal (rama descendente) y regresa
(rama ascendente fina y gruesa).
3. Túbulo contorneado distal (TCD): Parte del túbulo alejada de la cápsula
glomerular. Vacía en túbulos colectores, que se unen y convergen en los
conductos papilares.
Para producir la orina las nefronas y sus túbulos desarrollan tres procesos básicos:
a. Filtración glomerular: El agua y la mayor parte de los solutos en el plasma se
movilizan a través de la pared de los capilares glomerulares hacia la cápsula de
Bowman y luego hacia el túbulo renal. El líquido que entra en el espacio capsular
se llama filtrado glomerular (Fracción de filtración normal=16-20%). Éste proceso
ocurre a través de una membrana de filtración formada por células endoteliales
del capilar glomerular, la lámina basal (colágeno y proteoglicanos, matriz de
glicoproteínas) y una hendidura formada por podocitos. Se sigue el principio de
Starling sobre diferencia de presiones para el proceso de filtración, pero el
Tubulopatías (Soneivi Henríquez) Página 2
volumen de líquido filtrado es mayor que en otros capilares del organismo porque
son altamente permeables y existe una gran superficie (regulada por células
mesangiales), la cual es muy delgada y porosa (<1 micra), además la presión del
capilar glomerular es muy alta. La presión que favorece la filtración es la Presión
hidrostática sanguínea glomerular (55mmHg) y las presiones que se oponen son la
Presión Hidrostática capsular (15mmHg) y Presión coloidosmótica sanguínea
(30mmHg), dando una Presión Neta de Filtración (PNF) de 10mmHg. La Tasa de
Filtración Glomerular normal es de 125ml/minuto en hombres y 105ml/minuto en
mujeres, éste valor es importante para el mantenimiento de la homeóstasis de
líquidos corporales, la misma depende del ajuste del flujo sanguíneo dentro y fuera
del glomérulo y de la superficie disponible adaptada para el proceso, así como la
autorregulación por inhibición de la liberación de Óxido Nítrico (NO) que en
condiciones normales dilata los capilares. Otros mecanismos de regulación son el
neural (a través de noradrenalina que disminuye la TFG) y el hormonal
(Angiotensina II disminuye la TFG y el Péptido Natriurético Auricular aumenta la
TFG).
b. Reabsorción tubular: Comprende el retorno de la mayor parte del agua filtrada y
muchos de los solutos al torrente sanguíneo (cerca del 99% del agua filtrada). Ésta
función es llevada a cabo por las células epiteliales de los túbulos, pero las que
tienen mayor contribución son las del TCP (60%), seguido del Asa de Henle con un
20 a 30% de solutos, 35% de Cl- y 15% de agua, TCD (10%). Puede ocurrir por vía
paracelular o transcelular. Los solutos reabsorbidos por procesos activos (primarios
o secundarios, cotransportadores, intercambiadores o antiportes) o pasivos son
glucosa, urea e iones como Na+, K+, Ca++, Cl-, HPO42-, con la finalidad de mantener
sus valores en equilibrio homeostático. La mayor parte de pequeñas proteínas que
pasan el filtro también se reabsorben por pinocitosis. En el TCD y el TC existen dos
tipos de células: Principales que reabsorben Na+ y secretan K+ y las intercalares
que reabsorben K+ y HCO3- y secretan H+.
c. Secreción tubular: Es la transferencia de sustancias desde la sangre y las células
tubulares hacia el líquido tubular. Las sustancias secretadas son H+, K+ y NH 4-,
creatinina y ciertos fármacos como la penicilina. (Para eliminación y control del
pH).
Los reguladores hormonales más importantes de la reabsorción y secreción de electrolitos
y agua son:
- Angiotensina II: Disminuye la TFG por vasoconstricción de arteriolas
aferentes, aumenta la reabsorción de Na+, Cl- y H2O en el TCP
Tubulopatías (Soneivi Henríquez) Página 3
estimulando los intercambiadores Na+/H+ y estimula la corteza
suprarrenal para que libere aldosterona.
- Aldosterona: Estimula las células principales en TC para reabsorber Na+
y Cl- y secretar K+. Incrementando la volemia.
- Hormona antidiurética (ADH) o vasopresina: Se libera en el Lóbulo
posterior de la Hipófisis. Aumenta la permeabilidad al agua de las
células principales del TCD y TC, incluyendo por exocitosis las vesículas
que contienen acuaporinas a la membrana apical.
- PNA: Liberado en el corazón, puede inhibir la reabsorción de Na+ y agua
en el TCP y TC, suprime la secreción de Aldosterona y ADH, produciendo
aumento de la natriuresis y diuresis, disminuyendo la volemia y la PA.
Otra de las importantes funciones de los túbulos renales se basa en la producción
de orina diluida y concentrada, el control lo tiene la ADH, la cual en niveles bajos produce
orina muy diluida y en niveles altos produce orina muy concentrada. El filtrado glomerular
tiene la misma proporción de agua y solutos que el plasma sanguíneo (300 mOsm/L), el
líquido que abandona el TCP aún es isotónico con respecto al plasma. A medida que
avanza a través de la rama descendente del asa de Henle, la osmolaridad tubular va
aumentando por el incremento de la reabsorción de agua por ósmosis al líquido
intersticial (el cual es muy concentrado) pudiendo alcanzar valores de 1200 mOsm/L (ya
que ésta porción es impermeable a los solutos). Al avanzar a la porción gruesa de la rama
ascendente, las células que la tapizan tienen un gran número de cotransportadores que
reabsorben Na+, Cl- y K+ desde el líquido tubular, pero la reabsorción de agua es bastante
baja en ésta porción, lo que permite la dilución del líquido tubular, alcanzando valores de
osmolaridad de hasta 150 mOsm/L. Mientras fluye por el TCD se reabsorben más solutos y
poca cantidad de agua. Finalmente, al llegar a las células principales del TC el líquido
tubular se diluye en mayor proporción porque las mismas son poco permeables al agua en
ausencia de ADH. En el momento en que drena a la pelvis renal, la concentración puede
estar entre 60 y 70 mOsm/L (4 veces más diluido que el plasma o la TFG).
CONCEPTO
Las tubulopatías o enfermedades del túbulo renal son un grupo heterogéneo de
entidades o alteraciones clínicas definidas por anomalías de la función tubular renal, con
afectación escasa o nula de la función glomerular. Esta afirmación es válida únicamente en
estadios precoces, ya que en el curso evolutivo de una tubulopatía puede también
producirse una patología glomerular secundaria. Dependiendo de la función tubular que
se encuentre afectada, cada entidad tiene una edad de aparición, manifestaciones clínicas
y analíticas, gravedad y pronóstico propios.
Tubulopatías (Soneivi Henríquez) Página 4
CLASIFICACIÓN
Según su origen:
a. Primarias, que tienen por lo general un carácter congénito, se les reconoce
como hereditarias y suelen manifestarse en la infancia.
b. Secundarias, aparecen en cualquier grupo etario y son la consecuencia de
procesos generales que afectan el riñón o se producen tras la administración
de fármacos o tóxicos.
Según la zona tubular alterada:
a. Nefrona proximal
- Síndrome de Fanconi
- Acidosis tubular renal proximal o tipo II
- Raquitismo hipofosfatémico ligado al cromosoma X
- Raquitismos dependientes de la vitamina D
- Glucosuria renal
- Aminoacidurias
- Hipouricemia renal congénita
- Cistinosis
- Nefrolitiasis hipercalciúrica ligada al cromosoma X
b. Asa de Henle
- Síndrome de Bartter
- Síndrome de Gitelman
- Hipomagnesemia familiar con hipercalciuria y nefrocalcinosis
c. Nefrona distal
- Acidosis tubular renal distal o tipo I
- Acidosis tubular renal hipercalcémica o tipo IV o
pseudohipoaldosteronismo
- Pseudohiperaldosteronismo
- Diabetes insípida nefrogénica hereditaria
Según el número de sustancias afectadas:
a. Simples: 1 sustancia.
b. Complejas: 2 o más sustancias.
•Según el tipo de transporte alterado:
a. Transporte de proteínas
Tubulopatías (Soneivi Henríquez) Página 5
- Proteinuria tubular
b. Transporte de glucosa
- Glucosuria renal hereditaria
c. Transporte de aminoácidos
- Cistinuria
- Hipercistinuria aislada
- Hiperaminoaciduria dibásica (tipo I, tipo II o lisinuria)
- Enfermedad de Hartnup
- Hipoabsorción de metionina
- Iminoglicinuria familiar y otras glicinurias
- Aminoaciduria dicarboxílica
- Aminoacidurias renales no específicas
d. Transporte de fosfatos
- Hipofosfatemia familiar
- Pseudohipoparatiroidismo
e. Transporte de ácido úrico
- Hipouricemia de origen renal
f. Transporte múltiple del túbulo proximal
- Síndrome de Fanconi
g. Trastornos de la función reguladora del equilibrio ácido-base
- Acidosis tubular renal
h. Transporte de calcio
- Hipercalciuria de origen renal
i. Transporte de sodio, potasio y magnesio
- Pseudoaldosteronismo tipo I
- Pseudoaldosteronismo tipo II o Síndrome de Gordon
- Síndrome de Bartter
- Síndrome de Gitelman
- Síndrome de Liddle
- Déficit de la 11-beta-hidrosteroide deshidrogenasa
- Hipomagnesemia-hipercalciuria familiar
j. Transporte de agua
- Diabetes insípida nefrogénica
ACIDOSIS TUBULAR RENAL
Es un grupo de alteraciones tubulares que producen una pérdida renal excesiva de
HCO3- o una disminución en la secreción de ácido, impidiendo la adecuada acidificación de
la orina. En todas ellas existe una incapacidad para excretar Cl- en proporción al Na+.
Tubulopatías (Soneivi Henríquez) Página 6
Existen varios tipos, los tipo I y II pueden ser adquiridos o primarios, en tanto que la tipo
IV suele adquirirse junto con alguna disfunción renal moderada y se caracteriza por
hiperpotasemia.
Tipo I (Distal): Existe una disminución de la secreción de hidrogeniones en el TCD, por lo
que el Na+ se intercambia con el K+: Se reabsorbe Na+ y se secreta K+. El pH en estos
segmentos, que normalmente llega al nivel mínimo de 4,5 se queda por encima de 5,3. Se
retienen los hidrogeniones y el bicarbonato desciende progresivamente hasta por debajo
de 10 mEq/L. Se debe a causas autoinmunes (Síndrome de Sjogren y Artritis Reumatoide)
y a intoxicaciones. En ocasiones solo se manifiesta si existe una sobrecarga exógena de
ácidos. Suele responder a la administración de bicarbonato sódico (50-100 mEq/día). Se
acompaña de hipopotasemia, aunque existe una variante hiperpotasémica por un defecto
en el transporte de Na+ en el TC que disminuye la excreción de K+. Se asocia con
frecuencia a nefrocalcinosis, osteomalacia y nefrolitiasis con cálculos de fosfato cálcico o
de estruvita, resultado de cuatro factores: hipercalciuria, hiperfosfaturia, pH urinario
persistentemente elevado e hipocitraturia. Terapia de elección: Citrato de Potasio.
Tipo II (proximal): Presenta un déficit de la reabsorción proximal de Na+, K+ y HCO3-, el
cual no se reabsorbe en el TCP, por lo que llega en exceso a los TC, lo que induce una
secreción de K+. Puede ser un defecto aislado o formar parte de un Síndrome de Fanconi.
Las causas más frecuentes en los niños son la idiopática y la cistinosis, y en los adultos los
inhibidores de la anhidrasa carbónica y el mieloma. No responde al tratamiento con
bicarbonato sódico y se prefiere el citrato como fuente de álcali. La respuesta a las tiazidas
es variable. Se complica con raquitismo (niños) u osteomalacia (adultos).
Tipo IV: Se caracteriza por la disminución de la secreción distal de H+ por déficit de
aldosterona o resistencia tubular a la misma. En éste tipo existe hiperpotasemia. La causa
puede ser fármacos (AINES, heparina, diuréticos ahorradores de K+) e hipoaldosteronismo
de diversa etiología. La acidosis suele ser leve (Bicarbonato plasmático alrededor de 15
mEq/L) y el pH urinario muy bajo <5,3.
Lo que antes se conocía como tipo III, hoy se sabe que es la misma tipo I en una
variante presentada en lactantes.
SINDROME DE TONI-DEBRÉ-FANCONI
Con este término se designa a cualquier disfunción tubular proximal compleja y
completa, causada por la alteración de algún proceso metabólico esencial que afecta a
múltiples transportadores simultáneamente. Se caracteriza por una pérdida renal, en
grado variable, de fosfato, bicarbonato, sodio, potasio, cloro, ácido úrico, aminoácidos,
glucosa, proteínas de bajo peso molecular, carnitina y otros solutos manejados en este
Tubulopatías (Soneivi Henríquez) Página 7
segmento. El TCP es reemplazado por una delgada estructura tubular constituyendo la
deformidad en “cuello de cisne” y es acortado en su longitud.
Puede ser primario (autosómico dominante [AD], autosómico recesivo [AR] o
recesivo ligado al cromosoma X) o secundario a otras enfermedades (fructosemia,
galactosemia, tirosinemia, síndrome de Lowe, glucogenosis, cistinosis, déficit citocromo C
oxidasa, citopatías mitocondriales, enfermedad de Wilson). Puede ser también adquirido
en relación con fármacos (antibióticos, citostáticos), tóxicos (metales pesados),
enfermedades de carácter inmunitario (nefropatías inmunológicas) u otros (hierbas
chinas, proteinurias, tumores). La evolución es variable, dependiendo del agente
etiológico. Así, algunos cuadros desaparecen al suprimir el agente causal o tratar la
enfermedad subyacente.
Los síntomas principales son poliuria, polidipsia, episodios de deshidratación y
fiebre, retraso de crecimiento, raquitismo y osteomalacia, debilidad muscular y
manifestaciones extrarrenales que dependen de la enfermedad a la que se asocie.
En sangre, existe acidosis metabólica hiperclorémica, hipofosfatemia, normo o
hiponatremia, hipopotasemia, hipouricemia. La PTH puede estar normal o alta y el 1-
25(OH)2vitD3 normal o disminuido. En orina se comprueba hiperfosfaturia, aumento de la
eliminación de sodio y potasio, hiperaminoaciduria, glucosuria, proteinuria de bajo peso
molecular, hiperuricosuria, y de forma no constante hipercalciuria. En ecografía, puede
haber nefrocalcinosis.
Existen varios Síndrome asociados al Síndrome de Fanconi, por ser hoy en día un
término amplio que designa múltiples patologías complejas que cursan con disfunción
variada en la reabsorción del túbulo proximal renal, entre ellos:
- Síndrome de Bickel-Fanconi: Que representa un error congénito del
metabolismo que incluye la asociación de una glucogenosis
hepatorrenal, con hipergalactosemia, hipoglucemia de ayuno e
hiperglucemia postprandial, y una nefropatía tipo Fanconi, con
glucosuria de intensidad desproporcionada. Hoy día está establecido
que se debe a mutaciones del gen GLUT2 que codifica un transportador
específico de glucosa2. Este gen se expresa en hepatocitos, células
pancreáticas β y membranas basolaterales de células epiteliales de
intestino y riñón. La pérdida de actividad funcional de este
transportador explicaría la presencia de galactosuria y la gran
intensidad de la glucosuria.
Tubulopatías (Soneivi Henríquez) Página 8
- Síndrome óculo-cerebro-renal de Lowe: Asocia una tubulopatía
proximal compleja con un retraso mental grave y anomalías congénitas
oculares y neurológicas. Se hereda con un carácter recesivo ligado al
sexo, por lo que se manifiesta clínicamente en varones. El locus causal
(OCRL1) ha sido localizado en la región q26 del cromosoma X. Utilizando
el punto de rotura de una traslocación como marcador genético ha sido
posible el aislamiento del gen implicado, que codifica el fosfatidil -
inositol 4,5-bifosfato -5-fosfatasa6, 7. Esta proteína parece ser necesaria
para un correcto tráfico intracelular por lo que su disfunción da origen a
una alteración lisosomial compleja.
- NEFROLITIASIS HIPERCALCIÚRICA LIGADA AL CROMOSOMA X O
SÍNDROME DE DENT: Está presente únicamente en varones, se asocia
durante la infancia nefrolitiasis y una tubulopatía proximal compleja
tipo Fanconi con proteinuria tubular e hipercalciuria, mientras que
durante la edad adulta se manifiesta mediante litiasis e insuficiencia
renal crónica, generalmente éstos pacientes presentan normocalcemia.
La enfermedad descrita en 1964 por Dent y Friedman es la misma
entidad que las reportadas bajo los nombres de urolitiasis familiar con
herencia ligada al sexo, raquitismo hipofosfatémico recesivo ligado al
sexo y proteinuria idiopática de bajo peso molecular. El gen responsable
se encuentra ligado al cromosoma X (CLC-5).
RAQUITISMO HIPOFOSFATÉMICO LIGADO AL CROMOSOMA X
Esta entidad, también llamada raquitismo vitamino-D resistente hipofosfatémico o
hipofosfatemia familiar ligada al sexo, se caracteriza por retraso de crecimiento y lesiones
radiológicas de raquitismo con deformidades de las extremidades inferiores. La calcemia
es normal pero existe siempre hipofosfatemia y elevación en sangre de la fosfatasa
alcalina. La enfermedad se transmite a través de una herencia dominante ligada al sexo,
aunque pueden existir también formas aparentemente esporádicas. Existen mutaciones
espontáneas que dan un síndrome similar en ratones (la llamada mutación HYP) y que
también han sido localizada en el cromosoma X. Esta enfermedad dependería, por lo
tanto de un fallo de degradación de una hormona polipeptídica, la llamada fosfotonina,
secretada en el osteoblasto y que intervendría en la regulación de metabolismo calcio-
fosfórico inhibiendo la reabsorción tubular proximal de fosfato inorgánico a través del
transportador apical Na-dependiente (NPT2). La función del gen PHEX es esencial para
limitar esta inhibición del transporte de fosfato. Alteraciones funcionales de dicho gen
conllevan un exceso de fosfotonia circulante y una mayor inhibición de dicha reabsorción
con la consiguiente hiperfosfaturia.
Tubulopatías (Soneivi Henríquez) Página 9
RAQUITISMOS DEPENDIENTES DE LA VITAMINA D
Aparece en dos modalidades que se manifiestan por hipocalcemia, hipofosfatemia,
mayores concentraciones de PTH y las anomalías esqueléticas del raquitismo y la
osteomalacia. En casos graves, puede surgir tetania. Es un trastorno autosómico recesivo
consecuencia de mutaciones en CYP27B1, el gen que codifica 25(OH)D 3-1 alfa- hidroxilasa,
enzima del TCP que cataliza la hidroxilación y activación de 25(OH)D 3 en 1,25(OH)2D3.
GLUCOSURIA RENAL
Es una enfermedad benigna causada por mutaciones en el gen SLC5A2, que
codifica el transportador SGLT2 de sodio-glucosa, de baja afinidad y alta capacidad, que
causa un trastorno en el transporte tubular activo de la glucosa. Se excretan en la orina
cantidades variables de glucosa, siendo la concentración plasmática de glucosa normal. En
el diagnóstico se deben excluir glucosurias asociadas a otros defectos tubulares. Aunque
algunos pacientes presentan poliuria importante por diuresis osmótica, habitualmente no
tiene síntomas o consecuencias físicas, excepto durante el embarazo o la inanición
prolongada, cuando puede aparecer deshidratación y cetosis. La alteración existe desde la
infancia hasta la edad adulta y el diagnóstico se hace habitualmente de forma casual.
Según la intensidad de la anomalía, puede disminuir el máximo de reabsorción tubular de
glucosa con concentraciones normales de glucosa y originar glucosuria >50 g/día.
AMINOACIDURIAS
Causadas por una falla proximal en la reabsorción de aminoácidos, a veces uno en
particular como la cistinuria que puede determinar la formación de cálculos de cistina. En
otros casos, la falla comprende varios aminoácidos y con frecuencia de suma glucosuria y
fosfaturia. Se ha hallado una lesión orgánica consistente en el afinamiento de la porción
yuxtaglomerular de los TCP.
HIPOURICEMIA RENAL CONGÉNITA
La hipouricemia aislada de origen renal se hereda con carácter AR. La variedad más
frecuente está causada por mutaciones en el gen SLC22A12, que codifica el transportador
de urato URAT1, que interviene en la reabsorción tubular proximal de ácido úrico. Suele
ser asintomática o expresarse tardíamente en la edad adulta en forma de litiasis o
episodios de insuficiencia renal aguda en situaciones de ejercicio y estrés oxidativo. Se
diagnostica por niveles de ácido úrico sérico menores de 2 mg/dl con una excreción
fraccional superior elevada (alrededor del 40-90%). En algunos casos se puede asociar con
hipercalciuria. El tratamiento consiste en una ingesta abundante de líquidos, dieta rica en
cítricos y evitar la práctica de ejercicio anaeróbico, por lo que el ejercicio físico se debe
Tubulopatías (Soneivi Henríquez) Página 10
realizar acompañado de abundante hidratación. Se debe mantener el pH urinario entre 6-
7, mediante la administración de citrato potásico. La salida del ácido úrico hacia el espacio
peritubular se realiza mediante el transportador basolateral GLUT9 que es codificado por
el gen SLC2A9.
CISTINOSIS
Patología autosómica recesiva, con afección del gen 17p13, que genera
manifestaciones clínicas similares al Síndrome de Fanconi, eliminación de NaCl y agua, que
avanza rápidamente a Insuficiencia renal progresiva, retraso del creimiento, raquitismo,
vómitos, estreñimiento y fiebre inexplicable, fotofobia, ceguera, debilidad muscular por
deficiencia de carnitina, hepatomegalia, hipotiroidismo, pubertad tardía y anomalías
neurológicas tardías. Es una enfermedad infrecuente de aparatos y sistemas múltiples
causada por mutaciones de la cistinosina, transportador de hidrógeno impulsado por
iones, encargado de exportar cistina desde los lisosomas. La acumulación de cistina
insoluble provoca formación de cristales de las células tubulares proximales y otros
órganos. Hay tres variedades: Infantil (nefropática), de adolescentes y de adultos. El
diagnóstico se hace por encuentro de cistina elevada en los leucocitos periféricos.
SÍNDROME DE BARTTER
El síndrome de Bartter define una enfermedad hereditaria, autosómica recesiva,
que puede ser consecuencia de mutaciones que afectan cualquiera de las cuatro proteínas
de transporte iónico en el asa de Henle. Las proteínas afectadas comprenden la NKCC2
(tipo 1), cotransportadorsa de sodio-potasio-cloruro susceptible a diuréticos en el asa
apical y ROMK de conducto de potasio apical (tipo 2) y el conducto basolateral de cloruro
C1C-Kb (tipo 3). La variante tipo 4 es consecuencia de mutaciones en la barttina,
subunidad esencial de la C1C-Ka y C1C-Kb que permiten el transporte de los conductos de
cloruro hacia la superficie celular. Es caracterizada por alcalosis metabólica,
hipopotasemia, hiperaldosteronismo con presión arterial normal, hipomagnesemia,
hiperprostaglandinismo e hiperplasia del aparato yuxtaglomerular. Hallazgos recientes
han establecido la heterogeneidad genética del síndrome de Bartter permitiendo
distinguir entre una forma muy grave de presentación ante- o neonatal (síndrome de
Bartter neonatal) y una forma de aparición algo más tardía, durante los primeros años de
la vida (síndrome de Bartter típico). Las manifestaciones clínicas del síndrome de Bartter
neonatal suelen ya aparecer durante la vida intrauterina o inmediatamente después del
nacimiento e incluyen polihidramnios, prematuridad, poliuria masiva, hipercalciuria y
nefrocalcinosis. Suele presentar retraso en el crecimiento. En la tipo 4 se ha observado
sordera neurosensorial. Los individuos con una modalidad grave que viven después de la
Tubulopatías (Soneivi Henríquez) Página 11
infancia temprana pueden presentar insuficiencia renal crónica por nefrocalcinosis o por
atrofia tubular y fibrosis intersticial, por hipopotasemia persistente intensa.
SÍNDROME DE GITELMAN
El síndrome de hipokaliemia-hipomagnesemia familiar (síndrome de Gitelman) es
más frecuente, con una evolución clínica menos intensa, fue descrito en 1966 por
Gitelman, Graham y Welt. Hasta hace poco tiempo no se distinguía en la literatura entre
este síndrome y el síndrome de Bartter en general. En realidad, la mayoría de los
pacientes adultos descritos bajo el epónimo de síndrome de Bartter corresponden a casos
de síndrome de Gitelman.
Los pacientes están con frecuencia asintomáticos, con la excepción de episodios
recurrentes de debilidad muscular y tetania, que se pueden acompañar de dolor
abdominal, vómitos y fiebre. Los intervalos de aparente salud pueden ser muy
prolongados y el diagnóstico no establecerse hasta la edad adulta. Sin embargo, casi la
mitad de los pacientes presentan síntomas menores tales como apetito por la sal, fatiga,
debilidad muscular, calambres, mareos, nicturia y polidipsia. El retraso de crecimiento
están ausentes o son de grado leve. La condrocalcinosis, debida a depósitos de cristales de
pirofosfato cálcico deshidratado, es una complicación relevante en adultos. Los hallazgos
bioquímicos más relevantes son hipopotasemia, hipomagnesemia, alcalosis metabólica e
hipocalciuria.
HIPOMAGNESEMIA FAMILIAR CON HIPERCALCIURIA Y NEFROCALCINOSIS
Es el primer ejemplo de un trastorno atribuible a una proteína con anomalías y
deficiencias, que interviene en el transporte de iones paracelulares. La CLDCN16 codifica
la Claudina 16, miembro de la familia de proteínas de Claudina que intervienen en la
formación de las uniones herméticas. Se piensa que es componente esencial de la vía
paracelular de magnesio y calcio. Las manifestaciones clínicas comienzan en la lactancia y
comprenden hipomagnesemia resistente a los complementos ingeribles, hipercalciuria y
nefrocalcinosis. Se observan también infecciones recurrentes de vías urinarias y
nefrolitiasis y algunos enfermos presentan defectos oculares como calcificaciones de
córnea y coriorretinitis, así como hipertensión arterial. La hipomagnesemia crónica puede
dar origen a tetania, convulsiones y, ocasionalmente, a hipocalcemia y raquitismo
vitamino-D resistente. Se transmite por herencia autosómica recesiva. Individuos
heterocigotos pueden manifestar únicamente hipercalciuria, sin evidencia de
hipomagnesemia.
PSEUDOHIPERALDOSTERONISMO TIPO I
Tubulopatías (Soneivi Henríquez) Página 12
Se trata de una enfermedad hereditaria caracterizada por pérdida salina con
hipovolemia, hiponatremia, hiperpotasemia y acidosis metabólica (acidosis tubular renal
tipo IV) con niveles elevados de renina y aldosterona. La variante renal es la más
frecuente, se hereda con carácter AD y está causada por mutaciones en el gen NR3C2, que
codifica la síntesis del receptor mineralocorticoide humano (4q31.1). Se manifiesta en la
primera infancia por polihidramnios, fallo de crecimiento, pérdida de peso, vómitos,
deshidratación, pérdida salina renal, hiperpotasemia, hiponatremia y acidosis metabólica
con gran aumento de renina y aldosterona en plasma. En las familias afectadas pueden
existir individuos aparentemente asintomáticos. El tratamiento se basa en suplementos de
cloruro sódico, pudiendo existir una mejoría espontanea a partir de uno a tres años de
vida. La variante sistémica se hereda con carácter AR y está causada por mutaciones con
pérdida de función de uno de los genes codificadores SNCC1A, SNCC1B y SNCC1G de las
subunidades α, β y γ del canal epitelial de sodio ENaC que se expresa en las células
principales del túbulo colector. Existe una resistencia periférica a la acción de los
mineralocorticoides en riñón, colon, glándulas sudoríparas y glándulas salivares. La
sintomatología aparece al nacimiento con pérdida salina masiva, poliuria, deshidratación y
posible muerte. Se comprueba un aumento de la concentración de electrolitos en sudor y
saliva. El tratamiento consiste en la administración de suplementos de cloruro sódico y, si
es necesario, resinas de intercambio para controlar la hiperpotasemia.
PSEUDOHIPERALDOSTERONISMO TIPO II O SÍNDROME DE GORDON O HIPERTENSIÓN
HIPERPOTASÉMICA FAMILIAR
Se transmite de forma AD y es debido a mutaciones de ganancia de función de los
genes WKN1 y WKN4, que codifican las kinasas WKN1 y WKN4, respectivamente, que
regulan el transporte tubular de Na+ y Cl- en el túbulo distal. Puede haber mutaciones
también en el gen KLHL3 y CUL3. Los individuos afectados presentan hipertensión, talla
baja, hiperpotasemia, acidosis metabólica (acidosis tubular distal tipo IV) y un descenso de
los niveles plasmáticos de renina y aldosterona. Característicamente, algunos pacientes
presentan hipercalciuria. Se manifiesta en adolescentes o adultos jóvenes, es infrecuente.
DIABETES INSÍPIDA NEFROGÉNICA HEREDITARIA (DIN)
Es una enfermedad monogénica rara que suele aparecer en la lactancia con
poliuria grave resistente a vasopresina, deshidratación, retraso del crecimiento. Es un
trastorno de la reabsorción de agua en el túbulo colector. Puede ser de origen genético o
secundario. Se manifiesta por la excreción de grandes cantidades de orina muy diluida,
dada la incapacidad de concentrar la orina debido al fallo de respuesta tubular a la
hormona antidiurética (ADH) o vasopresina. La forma de herencia más frecuente de la DIN
primaria (90% de los casos) es la recesiva ligada al cromosoma X y está causada por
Tubulopatías (Soneivi Henríquez) Página 13
mutaciones del gen que codifica el AVPR2, en la región Xq28. En un 10% de los pacientes
la DIN es AR por mutaciones del gen que codifica la aquaporina 2 (AQP2), localizado en el
cromosoma 12q13, y afecta indistintamente a niños de ambos sexos. La DIN adquirida se
debe a la pérdida del gradiente osmótico y a la lesión tubular que cursa con una reducción
en la expresión de AQP2 en la médula renal. Se observa en nefropatías tubulointersticiales
crónicas (poliquistosis, uropatía obstructiva, displasia renal, nefronoptisis, insuficiencia
renal, depleción de potasio o hipercalcemia crónicas) o puede ser secundaria a fármacos
(litio, colchicina, anfotericina B, vincristina). En la DIN de origen genético, los síntomas
aparecen en las primeras semanas de vida. Las manifestaciones iniciales en los niños
pequeños son irritabilidad, rechazo de las tomas, avidez por el agua, anorexia, vómitos,
fallo de medro, fiebre y estreñimiento. En niños mayores, es frecuente la nicturia y la
eneuresis. La poliuria puede derivar en alteraciones urológicas como megavejiga,
megauréter e hidronefrosis no obstructiva. El retraso psicomotor podría estar relacionado
con los desequilibrios hidroelectrolíticos, ya que su incidencia es baja en niños
adecuadamente tratados. La clínica es sugestiva. Consiste en poliuria y polidipsia
marcadas. La conservación de electrolitos es normal y la hipernatremia depende
netamente de la pérdida de agua.
El diagnóstico en lactantes y niños con la modalidad hereditaria se sustenta en los
antecedentes familiares y las manifestaciones clínicas iniciales, asimismo, se confirma por
la presencia de una concentración plasmática alta de vasopresina en una situación de
poliuria y orina hipotónica. Los estudios genéticos de identificación de mutaciones en
AVPR2 y AQP2 se realizan en centros de investigación y son útiles en la determinación
hereditaria.
SÍNDROME DE LIDDLE
Es una tubulopatía AD causada por mutaciones de ganancia de función en los
genes SNCC1B y SNCC1G, que codifican las subunidades β y γ del canal epitelial de sodio
ENaC, con lo que se evita su unión a Nedd4-2 y aumenta la densidad apical de ENaC. En
situación normal, la unión de Nedd4-2 a ENaC favorece la endocitosis y su degradación. La
enfermedad se manifiesta con signos clínicos y bioquímicos que son consecuencia de una
reabsorción tubular renal excesiva de Cloruro de sodio. El resultado es una expansión del
espacio extracelular con hipertensión arterial grave, alcalosis metabólica e hipopotasemia.
Los niveles de renina y aldosterona se encuentran muy reducidos. El tratamiento se basa
en diuréticos. Simula un estado de exceso de aldosterona.
ENFERMEDAD DE HARTNUP
Tubulopatías (Soneivi Henríquez) Página 14
Es un trastorno AR causado por un defecto en el transporte de aminoácidos
neutros en el aparato digestivo y renal. Las manifestaciones clínicas principales son ataxia
cerebelosa y lesiones cutáneas pelagriformes. Salvo la aminoaciduria, no hay más afección
renal. El gen alterado, SLC6A19, codifica un transportador de aminoácidos neutro que
depende de sodio y es independiente del cloruro y que se expresa de forma predominante
en el intestino y los túbulos renales.
DIAGNÓSTICO
1) Anamnesis: Considerando inicialmente las manifestaciones clínicas por las cuales
el paciente asiste a la consulta, en caso de existir. En caso contrario, ante la
sospecha, iniciar con la consideración de antecedentes que pueden relacionarse
con enfermedades renales, alteraciones de la diúresis, presencia de edema,
modificaciones en el color o aspecto de la orina y eliminación de sustancias
anormales. También considerar cualquier otro antecedente patológico del
paciente, tomando en cuenta posibles manifestaciones extrarrenales de las
patologías, así como antecedentes de infecciones urinarias o de cualquier tipo. Es
importante hábitos como polidipsia (si está asociada o no a poliuria y su inicio),
nicturia, eneuresis. Traumatismos en el área renal, patologías endocrinas,
especialmente DM y gota, circunstancias asociadas a hipercalcemia e hipercalciuria
(hipertiroidismo, exceso de vitamina D, sarcoidosis, MT óseas). Antecedentes
familiares de cualquiera de los aspectos anteriores también importan.
2) Examen físico: Depende de la inspección del abdomen, de la región lumbar y de
los órganos genitales. Incluye palpación de todas las zonas, puñopercusión lumbar
y auscultación de zona lumbar. Incluye la valoración de signos vitales y examen
físico completo del paciente.
3) Examen de orina simple: Como método extremadamente útil y poco invasivo.
- Macroscópicamente se observa la cantidad o volumen de orina (que
varía considerablemente, pero se consideran 1 o 2 litros diarios como
normal), el color, dependiente de urocromos y urobilina (el cual puede
ir desde incoloro hasta amarillo oscuro, lo cual en éste sentido nos
habla de concentración de la orina, aunque puede representar muchas
otras cosas, incluso la dieta), el aspecto (que en condiciones normales
debe ser límpido, volviéndose turbio con el estancamiento), la densidad
urinaria (cuyo valor normal oscila entre 1.000 y 1.035 y depende de la
conentración de solutos), el olor (poco aromático, aunque con el
estancamiento adquiere un olor a amoníaco) y el pH (importante en las
tubulopatías asociadas a equilibrio ácido-base, su valor normal es
aproximadamente 4,6-8, con promedio de 6,0, el mismo varía
Tubulopatías (Soneivi Henríquez) Página 15
considerablemente con la dieta: Proteínas aumentan la acidez,
vegetales aumentan la alcalinidad).
- Química: Incluye la presencia de proteínas (especialmente albúmina),
glucosa, cuerpos cetónicos, hemoglobina, bilirrubina, nitritos,
urobilinógeno. Los cuales deben ser NEGATIVOS en la normalidad.
- Microscópicamente se observa la presencia de células planas (con valor
normal de 0-5 xCPO), leucocitos (valor normal de 0-2 xCPO), hematíes
(valor normal de 0-2 xCPO), bacterias (que deben ser negativas).
4) Orina en 24 horas:
- Potasio (VN: 1,5-3,5 g)
- Fosforo (VN: 0,5-3 g)
- Calcio (VN: 0.5-2,2 g)
- Ácido úrico (VN: 2,5-7,5 g)
- Proteínas (VN: Hasta 1 g)
- Aminoácidos (VN: 1-3 g)
- Glucosa (Negativa)
5) Química sanguínea:
- Glicemia (VN: 70-110 mg/dL)
- Urea (VN: 10-50 mg/dL).
- Creatinina (VN: 0,6-1,4 mg/dL)
- Ácido úrico (VN: 2-5 mg/dL)
- Proteínas Totales y Fraccionadas (VN: Total 6,4-8,3 g/dL, Albúmina 3,5-
4,8 g/dL, Globulinas 2,3-3,5 g/dL, relación A/G 1,2-2,2).
- Fosfatasa alcalina (VN: 21-85 UI)
6) Electrolitos séricos:
- Cloro (VN: 95-100 mEq/L)
- Sodio (VN: 135-145 mEq/L)
- Potasio (VN: 3,5-5,1 mEq/L)
- Calcio (VN: 8,5-10,5 mg/dL o 4,5-5,3 mEq/L)
- Fosfato (VN: 1,8-2,9 mEq/L)
- Magnesio (VN: 1,5-3 mEq/L)
7) Equilibrio ácido-base (Gases arteriales):
- pH (VN: 7,35-7,45)
- HCO3- (VN: 22-26 mEq/L)
- pCO2 (VN: 35-45 mmHg)
8) Hormonas séricas:
- Paratohormona o PTH (VN: 0,66 +- 0,33 ng/ml)
9) Hematología Completa:
Tubulopatías (Soneivi Henríquez) Página 16
- Hematocrito (VN: 37-47%)
10) Ultrasonido abdominal-renal (sobre todo busca nefrocalcinosis, con lo que cursan
muchas de las patologías).
11) Estudios radiolígicos (Para raquitismos, donde el hallazgo más característico es la
presencia de pseudofracturas o líneas de Looser-Milkman, que son bandas
radiotransparentes perpendiculares a la cortical, generalmente bilaterales y
simétricas, siendo sus localizaciones más frecuentes: costillas, ramas púbicas,
fémur proximal, escápula y metatarsianos).
12) Estudios genéticos (para las causas hereditarias, según genes específicos)
Tubulopatías (Soneivi Henríquez) Página 17
REFERENCIAS BIBLIOGRÁFICAS
Aguirre, M. y Luis, I. (2014). Tubulopatías. Protocolos diagnósticos en pediatría, Asociación
Española de Pediatría. 1, 135 – 153.
Andreoli, T., Carpenter, C., Plum, F. y Smith, L. (1991). Cecil: Compendio de Medicina
Interna. (2da. Edición). Ciudad de México: Interamericana – McGraw- Hill.
Balcells, A. (1992). La clínica y el laboratorio. (15ta. Edición). Ciudad de México: Salvat.
Cossio, P., Fustinoni, O., Rospide, P., Martínez, F. y Miatello, V. (1987). Medicina Interna.
(6ta. Edición). Buenos Aires, Argentina: CTM Servicios Bibliográficos.
García, A. y Espinosa, L. (2008). Tubulopatías. Anales de pediatría continuada. 6 (5), 247 –
257.
Krupp, M. y Chatton, M. (1982). Diagnóstico clínico y tratamiento. (17ma. Edición). Ciudad
de México: Editorial El Manual Moderno.
Longo, D., Kasper, D., Jameson, J., Fauci, A., Hauser. y Loscalzo, J. (2012). Harrison:
principios de medicina interna. (18va. Edición). New York, USA: Mc Graw hill.
Rodríguez, J. et al. (2012). Diagnóstico y tratamiento médico. Madrid, España: Marbán.
Rodríguez, J. (2003). Tubulopatías renales hereditarias: de la clínica a la biología
molecular. Nefrología. 23 (1), 71 – 83.
Tortora, G. y Derrickson, B. (2007). Principios de anatomía y fisiología. (11va. Edición).
Madrid, España: Editorial médica panamericana.
Tubulopatías (Soneivi Henríquez) Página 18
También podría gustarte
- Coagulación Para Todos: Medicina Para TodosDe EverandCoagulación Para Todos: Medicina Para TodosCalificación: 4.5 de 5 estrellas4.5/5 (3)
- Fisiología Del Aparato UrinarioDocumento15 páginasFisiología Del Aparato Urinariokarenmmo16Aún no hay calificaciones
- Reporte DiuresisDocumento21 páginasReporte DiuresisElízabeth VanegasAún no hay calificaciones
- El Aparato UrinarioDocumento8 páginasEl Aparato UrinarionikocjsAún no hay calificaciones
- Farmacologia Del Riñon JeidyDocumento14 páginasFarmacologia Del Riñon JeidySandra Patricia Peña VelezAún no hay calificaciones
- Aparato Urinario ADocumento8 páginasAparato Urinario ADimar yahir Ramírez EstevaAún no hay calificaciones
- Fisiologia Del RiñonDocumento6 páginasFisiologia Del RiñonShirly RodriguezAún no hay calificaciones
- Seminario 11 Funcion Glomerular y TubularDocumento5 páginasSeminario 11 Funcion Glomerular y TubularJulio Borja100% (1)
- Generalidades de riñón: Filtración glomerular y procesos de formación de orinaDocumento7 páginasGeneralidades de riñón: Filtración glomerular y procesos de formación de orinaOri SbocciaAún no hay calificaciones
- Nefrofisiologia (Guyton and Hall) RESUMENDocumento46 páginasNefrofisiologia (Guyton and Hall) RESUMENCarlos Urrutia Ramos100% (1)
- Fisiología Renal y OsmorregulaciónDocumento5 páginasFisiología Renal y OsmorregulaciónAngely MartinezAún no hay calificaciones
- Uri FinalDocumento4 páginasUri FinalAlexaMoraAún no hay calificaciones
- Fisiología GenitourinariaDocumento7 páginasFisiología GenitourinariajonathanAún no hay calificaciones
- fisiología renalDocumento8 páginasfisiología renalc.auditorbravocarlosAún no hay calificaciones
- Sistema UrinarioDocumento4 páginasSistema UrinarioRocio AndiaAún no hay calificaciones
- Aula 2 Fisiologia Renal I 12010Documento31 páginasAula 2 Fisiologia Renal I 12010Yessica UrionaAún no hay calificaciones
- Lab 08 Manejo de Sales - OrINA Horario 9y30 Mesa3Documento20 páginasLab 08 Manejo de Sales - OrINA Horario 9y30 Mesa3Rosita Senmache CarranzaAún no hay calificaciones
- Histologia Del Sistema Urinario ActualDocumento32 páginasHistologia Del Sistema Urinario ActualAshley MaradiagaAún no hay calificaciones
- Monografia Sistema UrinarioDocumento14 páginasMonografia Sistema UrinarioAlexander Herrera67% (6)
- Fisiología y semiología renal: procesos de filtración, reabsorción y secreción en la nefronaDocumento7 páginasFisiología y semiología renal: procesos de filtración, reabsorción y secreción en la nefronaWendy Victoria Castillo BenitezAún no hay calificaciones
- Anatomia y Fisiologia RenalDocumento48 páginasAnatomia y Fisiologia RenalAhuitzolt BravoAún no hay calificaciones
- Fisiología renalDocumento5 páginasFisiología renalLaury GuerreroAún no hay calificaciones
- Resumen Fisio RenalDocumento11 páginasResumen Fisio RenalNayla celmary González cunemoAún no hay calificaciones
- Anatomía y Función RenalDocumento36 páginasAnatomía y Función RenalJuan Jose Marin Roman100% (1)
- RiñónDocumento8 páginasRiñóniansaucedo06Aún no hay calificaciones
- Bioqui ReneDocumento6 páginasBioqui ReneANA MARIA BETZABE BRITO RAYMUNDOAún no hay calificaciones
- Fisiologia RenalDocumento40 páginasFisiologia RenalNoryeski LopezAún no hay calificaciones
- FISIOLOGÍA Unidad 5Documento16 páginasFISIOLOGÍA Unidad 5Santi PalomequeAún no hay calificaciones
- Mecanismos de La Formación de OrinaDocumento2 páginasMecanismos de La Formación de OrinaDiego PatiñoAún no hay calificaciones
- Fisiología Renal y AnatomiaDocumento41 páginasFisiología Renal y AnatomiaAbraxas72Aún no hay calificaciones
- Aparato UrinarioDocumento5 páginasAparato UrinarioRosalínda Mamani VelardeAún no hay calificaciones
- Sistema UrinarioDocumento5 páginasSistema UrinarioalexiaguzzmanAún no hay calificaciones
- NEFRO-3Documento40 páginasNEFRO-3galiartpavelAún no hay calificaciones
- NefronaDocumento5 páginasNefronaDiego RiosAún no hay calificaciones
- Fisiología Del Sistema RenalDocumento43 páginasFisiología Del Sistema RenalipqcueramaroAún no hay calificaciones
- 8 DiureticosDocumento104 páginas8 DiureticosHasse HasseAún no hay calificaciones
- Cuestionario Fisiologia RenalDocumento5 páginasCuestionario Fisiologia RenalKoky De la CruzAún no hay calificaciones
- Anatomía y Fisiología RenalDocumento12 páginasAnatomía y Fisiología RenalGrecia HibarraAún no hay calificaciones
- Fisiología renal enDocumento5 páginasFisiología renal enSaul Olmeda FregosoAún no hay calificaciones
- Biología III HOMEOSTASIS (II)Documento5 páginasBiología III HOMEOSTASIS (II)Ignacio Madrid CanalesAún no hay calificaciones
- Tema 13 FHDocumento9 páginasTema 13 FHMaria MingAún no hay calificaciones
- Manual de EgoDocumento47 páginasManual de EgoRosenda DLAún no hay calificaciones
- Apuntes NefrologiaDocumento12 páginasApuntes NefrologiaVale ReynosoAún no hay calificaciones
- M1 T1 Actualización Sobre Enfermedad Renal PDFDocumento10 páginasM1 T1 Actualización Sobre Enfermedad Renal PDFFernando SantaellaAún no hay calificaciones
- Trastornos hidroelectrolíticos: Hiponatremia, Hipernatremia, Hipokalemia y másDocumento5 páginasTrastornos hidroelectrolíticos: Hiponatremia, Hipernatremia, Hipokalemia y másIngris PalmarAún no hay calificaciones
- RESUMEN APARATO URINARIO - TortoraDocumento5 páginasRESUMEN APARATO URINARIO - TortoraFerminAún no hay calificaciones
- Informe de Laboratorio de Fisiología Humana Practica N 8Documento16 páginasInforme de Laboratorio de Fisiología Humana Practica N 8Valeria Fuentes RiojaAún no hay calificaciones
- Taller Sistema Excretor Maryoris PDFDocumento20 páginasTaller Sistema Excretor Maryoris PDFMaryoris Del C. Osorio DE LA OssaAún no hay calificaciones
- Fisiología Resumen Medicina Segundo Año. Sistema Renal y Digestivo Universidad de SantiagoDocumento40 páginasFisiología Resumen Medicina Segundo Año. Sistema Renal y Digestivo Universidad de SantiagoClaudio Alexis CifuentesAún no hay calificaciones
- Fisiología renal: Filtración glomerular y formación de orinaDocumento31 páginasFisiología renal: Filtración glomerular y formación de orinachirly roque da silvaAún no hay calificaciones
- Fisiologia RenalDocumento15 páginasFisiologia RenalkennedyAún no hay calificaciones
- Fisiología Renal GeneralidadesDocumento29 páginasFisiología Renal GeneralidadesHenrySalazarLazoMD100% (22)
- P1 Fisio2Documento42 páginasP1 Fisio2Yarianny GuanteAún no hay calificaciones
- Fármacos que regulan la función renal y el equilibrio hidricoDocumento28 páginasFármacos que regulan la función renal y el equilibrio hidricoyanettAún no hay calificaciones
- Guia Sistema RenalDocumento5 páginasGuia Sistema RenalDavid FloresAún no hay calificaciones
- Aparato UrinarioDocumento27 páginasAparato UrinarioAntonio RodriguezAún no hay calificaciones
- Renal - Tarea 1-5Documento31 páginasRenal - Tarea 1-5barrioslissette87Aún no hay calificaciones
- SistexcretorDocumento5 páginasSistexcretorCandela Rodriguez BarrientosAún no hay calificaciones
- MicroDocumento3 páginasMicroLauraAún no hay calificaciones
- Manual de E.G.O.Documento50 páginasManual de E.G.O.Nino Flores100% (1)
- Trastornos por sustancias.Documento23 páginasTrastornos por sustancias.Victor MonsalveAún no hay calificaciones
- Trastorno BipolarDocumento13 páginasTrastorno BipolarVictor MonsalveAún no hay calificaciones
- Micobacterias No TuberculosasDocumento5 páginasMicobacterias No TuberculosasVictor MonsalveAún no hay calificaciones
- Enfermedades Tumorales Del SNCDocumento12 páginasEnfermedades Tumorales Del SNCRichard TorrealbaAún no hay calificaciones
- Traumatismos ToraìcicosDocumento13 páginasTraumatismos ToraìcicosVictor MonsalveAún no hay calificaciones
- Infecciones Urinarias (Víctor Belly)Documento9 páginasInfecciones Urinarias (Víctor Belly)Victor MonsalveAún no hay calificaciones
- MiopatíasDocumento15 páginasMiopatíasVictor MonsalveAún no hay calificaciones
- TB Extrapulmonar-2Documento12 páginasTB Extrapulmonar-2Victor Monsalve100% (1)
- Semiología de Estomago y Duodeno. Dr. PereriroDocumento4 páginasSemiología de Estomago y Duodeno. Dr. PereriroVictor MonsalveAún no hay calificaciones
- Enfermedades Infecciosas Del SNCDocumento16 páginasEnfermedades Infecciosas Del SNCStephany LopezAún no hay calificaciones
- Semiología de Pancreas. Dr. HerreraDocumento6 páginasSemiología de Pancreas. Dr. HerreraVictor MonsalveAún no hay calificaciones
- CA Arritmias CardiacasDocumento4 páginasCA Arritmias CardiacasStephany LopezAún no hay calificaciones
- Semiología de Estomago y Duodeno. Dr. PereriroDocumento4 páginasSemiología de Estomago y Duodeno. Dr. PereriroVictor MonsalveAún no hay calificaciones
- Glomerulopatías (Víctor)Documento9 páginasGlomerulopatías (Víctor)Victor MonsalveAún no hay calificaciones
- CA Trastornos de Conducción IntraventricularDocumento4 páginasCA Trastornos de Conducción IntraventricularVictor MonsalveAún no hay calificaciones
- CA Síndrome Coronario AgudoDocumento5 páginasCA Síndrome Coronario AgudoVictor MonsalveAún no hay calificaciones
- CA Hipertension ArterialDocumento4 páginasCA Hipertension ArterialVictor MonsalveAún no hay calificaciones
- Crisis de AnsiedadDocumento9 páginasCrisis de AnsiedadVictor MonsalveAún no hay calificaciones
- CA Bloqueos de Conducción AVDocumento3 páginasCA Bloqueos de Conducción AVVictor MonsalveAún no hay calificaciones
- CA Arritmias SupraventricularesDocumento4 páginasCA Arritmias SupraventricularesVictor MonsalveAún no hay calificaciones
- LEPTOSPIROSISDocumento9 páginasLEPTOSPIROSISVictor MonsalveAún no hay calificaciones
- Elvac - ReguladoresDocumento3 páginasElvac - ReguladoresemepbasAún no hay calificaciones
- Defensoria Penal MapucheDocumento15 páginasDefensoria Penal MapucheJulia IzabelleAún no hay calificaciones
- Tema 4 Material ComplementarioDocumento16 páginasTema 4 Material ComplementarioJan Carlos LeónAún no hay calificaciones
- Deloitte. Liderando Equipos VirtualesDocumento13 páginasDeloitte. Liderando Equipos VirtualesPaulo Contreras CastroAún no hay calificaciones
- Problema 2.35: Derivación de la fórmula del volumen de una berenjena en función del tiempoDocumento3 páginasProblema 2.35: Derivación de la fórmula del volumen de una berenjena en función del tiempoKaren RodriguezAún no hay calificaciones
- Oración Por ConflictosDocumento3 páginasOración Por ConflictosLoengrith RosalesAún no hay calificaciones
- Tema 3 Investigacion ADCGDocumento16 páginasTema 3 Investigacion ADCGAmayrani De la CruzAún no hay calificaciones
- Datos Bivariado en EstadisticaDocumento3 páginasDatos Bivariado en EstadisticavalentinaAún no hay calificaciones
- La Importancia de La Orientación Familiar en La Orientacion Familiar en La Educacion Infantil PDFDocumento41 páginasLa Importancia de La Orientación Familiar en La Orientacion Familiar en La Educacion Infantil PDFNatalia AtlanxochitlAún no hay calificaciones
- Unidad 1Documento11 páginasUnidad 1Jose Maria Duran YaselliAún no hay calificaciones
- CorresponsalDocumento5 páginasCorresponsalHeidy PinedaAún no hay calificaciones
- Ejercicios EstadisticaDocumento6 páginasEjercicios EstadisticaLuarSoft20% (1)
- Participación Social y ComunitariaDocumento12 páginasParticipación Social y ComunitariaNicole Lobos VillatoroAún no hay calificaciones
- 5 Lenguaje Clase 74Documento10 páginas5 Lenguaje Clase 74roxanaAún no hay calificaciones
- Segunda Semana de Clases Con La Animadora Pedagógica Betty OsorioDocumento7 páginasSegunda Semana de Clases Con La Animadora Pedagógica Betty OsorioANA YOLEIDA PACHECO ZAMBRANOAún no hay calificaciones
- Tabla Nutricional MemanDocumento315 páginasTabla Nutricional MemanGuillermo Ariel Mardones VergaraAún no hay calificaciones
- Acero Estructural Jimenez Romero JonathanDocumento29 páginasAcero Estructural Jimenez Romero JonathanJonathan JimenezAún no hay calificaciones
- Tight GasDocumento22 páginasTight GasElvis AguilarAún no hay calificaciones
- 7.-Direccion Administrativa de La C.E.P.P.Documento102 páginas7.-Direccion Administrativa de La C.E.P.P.GUADALUPE CALDERON CONCEPCIONAún no hay calificaciones
- Durand Segura Mirko AndréDocumento6 páginasDurand Segura Mirko AndréBrayam GomezAún no hay calificaciones
- O - T - Minlab - Laboratorio Metalurgico - 2014 CorregidoDocumento1 páginaO - T - Minlab - Laboratorio Metalurgico - 2014 CorregidoElvis Jhoan Herrera MelchorAún no hay calificaciones
- AUDIO-ENTREVISTA - Maria SalazarDocumento4 páginasAUDIO-ENTREVISTA - Maria SalazarSantiago ManchenoAún no hay calificaciones
- Camper (Empresa) : Ir A La Navegación Ir A La BúsquedaDocumento6 páginasCamper (Empresa) : Ir A La Navegación Ir A La BúsquedaPiboAún no hay calificaciones
- Tarea de Dibujo TecnicoDocumento18 páginasTarea de Dibujo TecnicoJesus Alejandro MontejoAún no hay calificaciones
- PSA NAMA CAFE COSTA RICA EdMDocumento23 páginasPSA NAMA CAFE COSTA RICA EdMJuan MarinAún no hay calificaciones
- EXPLICACIÓN SOBRE Las Ruinas CircularesDocumento4 páginasEXPLICACIÓN SOBRE Las Ruinas CircularesEmiliaGabrielaAún no hay calificaciones
- Unidad 4Documento25 páginasUnidad 4jennifer guzmanAún no hay calificaciones
- Monografia Fluidos FinalDocumento8 páginasMonografia Fluidos FinalNilcer Vargas TorresAún no hay calificaciones
- Pautas de Apoyo Inspeccion de ECF V1Documento11 páginasPautas de Apoyo Inspeccion de ECF V1Marcia PozoAún no hay calificaciones
- Cómo prepararse para el futuro: la lección del caminante del desiertoDocumento2 páginasCómo prepararse para el futuro: la lección del caminante del desiertoSheilin VillanuevaAún no hay calificaciones