Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cardiopatia Isquémica.-2
Cargado por
bryanjhoan320 calificaciones0% encontró este documento útil (0 votos)
7 vistas4 páginasTítulo original
CARDIOPATIA ISQUÉMICA.-2
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
7 vistas4 páginasCardiopatia Isquémica.-2
Cargado por
bryanjhoan32Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 4
A B C D
UNIVERSIDAD AUTONOMA DE LOS ANDES. UNIANDES.
ACTIVIDAD DOCENTE: CONFERENCIA
DURACION: 2 HORAS.
DOCENTE: DR. ENRIQUE RAMON RODRIGUEZ REYES.
UNIDAD 1. ENFERMEDAD HIPERTENSIVA.
TEMA. CARDIOPATIA ISQUÉMICA (SÍNDROMES CORONARIOS)
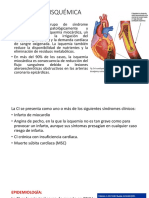
Cardiopatía isquémica. Conjunto de síndromes, estrechamente
relacionados con la isquemia miocárdica provocados por un
desequilibrio entre las demandas metabólicas (Necesidades de O2)
y el aporte que pueden brindar los vasos coronarios. Dado que el
corazón genera energía mediante fosforilación oxidativa, por lo
que la función cardiaca depende casi exclusivamente del aporte de
sangre oxigenada.
En mas del 90 por ciento de los pacientes, la CI es consecuencia
de una reducción del flujo coronario debido a una aterosclerosis
obstructiva, que se va instalando deforma progresiva a lo largo
de toda la vida. Entonces cuando hablamos de CI esto se considera
sinónimo de enfermedad arterial coronaria.
En el resto de los casos, la isquemia puede ser provocada por
algunas de las siguientes situaciones. EJ.
1. Aumento de la demanda de O2 (Aumento de la frecuencia
cardiaca, HTA).
2. Una reducción del volumen de sangre. (Hipotensión o shock)
3. Por una disminución de la oxigenación (Neumonías o
insuficiencia cardiaca)
4. Una disminución de la capacidad de transportación de
O2(Anemia o intoxicación por monóxido de carbono)
En resumen, la CI es la consecuencia de un aporte insuficiente de
oxigeno al corazón y su presentación clínica puede corresponder a
uno de los siguientes sindromes.
1. Angina de pecho. (Dolor)En este caso la isquemia induce la
aparición del dolor, pero no es suficiente para causar
necrosis de los mioicardiocitos. (Estable, Inestable,
Prinzmetal) Al referirnos a la angina de pecho estable, vamos
a observar que se trata de un cuadro de dolor que aparece
con un esfuerzo determinado y este es predecible, ya que el
paciente generalmente conoce su afección, siendo la
intensidad más o menos la misma en todas las ocasiones. Este
cuadro isquémico está relacionado con una oclusión Fija de
la luz vascular, por una placa de ateroma, cuando esta ha
alcanzado a obstruir el 70 por ciento o mas de la luz del
vaso. Para la angina inestable, Es necesario señalar, que
una placa inestable es la responsable de este cuadro, no
obstante cuando una placa estable alcanza el 90 por ciento
de obstrucción de la luz también puede desencadenar un dolor
anginoso de estas características, pues en esta situación
los signos de isquemia pueden aparecer incluso sin que haya
un aumento de la demanda de O2 por parte del corazón además
se han descrito la formación de trombos en la zona de la
Enrique Ramón Rodriguez Reyes
placa, quizás en relación con las alteraciones hemodinámicas
que la misma genera, a esto debemos añadir otros factores
extrínsecos como el estrés parietal, y las descargas
adrenérgicas, que actuando en conjunto sobre un endotelio
disfuncional colocan en una situación precaria la irrigación
del miocardio. La angina inestable no provoca necrosis, no
obstante, se debe tener muy en cuenta pues si el cuadro se
prolonga, si puede evolucionar hacia un IMA. La angina de
Prinzmetal, está relacionada con una oclusión “dinámica”
generalmente se debe a espasmos de la s arterias coronarias,
estos fenómenos se producen en la zona, o sobre la placa de
ateroma, pero no necesariamente por modificación de la
misma, se cree que una de las causas puede ser las descargas
adrenérgicas sobre un endotelio disfuncional, que genera una
respuesta exagerada, provocando la aparición de episodios
isquémicos. Se ha señalado que Prinzmetal, puede aparecer
también sobre un vaso aparentemente sano.
2. IMA. La intensidad de la isquemia es tal que produce necrosis
celular. En este caso el área de muerte celular está
relacionado con el calibre del vaso ocluido. Debemos
recordar que la isquemia miocárdica comienza a instalarse
desde el endocardio hasta el epicardio pues es el primero la
zona que se encuentra mas alejada, por lo tanto, la menos
vascularizada, al ponerse en crisis la circulación, este
sector es de los primeros en sufrir los efectos de la falta
de O2
3. CI Crónica con Insuficiencia cardiaca. Es una afección
progresiva, que ocurre tras un IM, o secundaria a pequeñas
lesiones isquémicas, que acaban precipitando un fracaso
mecánico del corazón como bomba.
4. Muerte súbita cardiaca. Como consecuencia a una lesión
tisular, secundaria a un IM, pero generalmente ocurre por
una arritmia severa, sin necrosis de los mioicardiocitos.
Debemos destacar que, si una lesión aterosclerótica ocluye la luz
de un vaso, de forma progresiva pero lenta a lo largo de los años,
habrá un proceso de remodelación vascular y aparecerán vasos de
neoformación para aportar un flujo compensador en la zona del
tejido que se encuentra en riesgo. Esto se denomina Perfusión
colateral y tiene gran importancia, pues puede comportarse como
una protección en caso de que el vaso llegara a ocluirse en su
totalidad. Esto no sucede cuando el bloqueo coronario tiene lugar
de forma aguda, llegando a producirse entonces un infarto. Es
necesario destacar que esto solo ocurre en pacientes c que
presentan placas estables, que han ocluido de forma lenta pero
progresiva la luz de un vaso.
Ya sabemos que dependiendo del tipo de placa y de los factores ya
sean intrínsecos o extrínsecos, que la hagan vulnerables, serán
las manifestaciones que provocaran en un paciente determinado.
RESPUESTA DEL MIOCARDIO A LA ISQUÉMIA. (Esta respuesta comienza a
suceder a los pocos segundos de la oclusión vascular)
1. Se interrumpe el metabolismo aeróbico. Al no existir
oxígeno, se detiene la fosforilación oxidativa en el
Enrique Ramón Rodriguez Reyes
mioicardiocito, en consecuencia, se reduce el nivel de ATP
en el sarcoplasma del mioicardiocito.
2. Se acumulan sustancias nocivas producto del metabolismo
anaerobio. (ácido láctico)
3. Perdida de la contractilidad, que se instala rápidamente.
4. Cambio en la ultraestructura celular, incluidas las
miofibrillas. Agotamiento del glucógeno, tumefacción
celular y mitocondrial.
5. La presencia de estos cambios puede traer consigo una grave
disfunción del corazón que provoca una insuficiencia
cardiaca transitoria (Miocardio aturdido) aunque
reversible, pero solo cuando se hayan eliminado del
sarcoplasma todas estas sustancias metabólicas “toxicas”
6. Inestabilidad eléctrica del corazón en las regiones
isquémicas, que puede traer consigo la aparición de
arritmias graves.
7. Estos cambios precoces son reversibles, después de 20 – 40
minutos de iniciada la isquemia comienza a instalarse
cambios irreversibles por la necrosis celular luego
aparece3n zonas de trombosis que agravan mas aun el estado
circulatorio del miocardio.
Recordando lo anteriormente dicho con respecto al diámetro del
vaso afectado, los infartos del miocardio pueden seguir uno de
los siguientes patrones.
1. IM transmurales afectan todo el espesor de la pared
ventricular. Provocan elevación del segmento ST, ondas Q
negativas, con perdida de la amplitud de R.
2. IM subendocárdicos, Se limitan al tercio interno del
miocardio y no suelen asociarse a elevación del segmento ST
u ondas Q.
3. IM microscópicos, que no suelen asociarse a ninguna
alteración del electrocardiograma.
CAMBIOS MORFOLÓGICOS.
1. Casi todos los IM transmurales, afectan una parte importante
del ventrículo izquierdo y el tabique interventricular.
2. IM con afectación de la pared posterior o postero septal,
también afectan al ventrículo derecho.
3. En casi todos los infartos incluidos los transmurales, se
conserva un pequeño ribete de miocardio subendocárdico (0,1
mm) viable, esto se debe a la difusión de O2 y nutrientes
desde la luz ventricular.
Aspecto macroscópico. Evolucionan dependiendo de la antigüedad de
la lesión, a través de una secuencia muy característica de cambios
morfológicos, desde la necrosis de coagulación hasta la
inflamación aguda. Puede ser muy difícil reconocer cambios macro
y microscópicos cuando es muy reciente, con menos de 12 horas es
difícil reconocerlos desde el punto de vista macro. En general
entre 12 a 24 horas es posible reconocer el infarto por el color
rojo azulado, secundario a la extravasación y atrapamiento de
sangre, posteriormente se van delimitando como áreas blandas
pardo-amarillentas, que posteriormente es sustituido por tejido
fibroso cicatricial.
Enrique Ramón Rodriguez Reyes
Aspecto microscópico. Son las características típicas de la
necrosis de coagulación (Revisar en el capítulo 2 del Robbins
“Necrosis de coagulación)
Enrique Ramón Rodriguez Reyes
También podría gustarte
- ACV Accidente Cerebrovascular: Guía de actividades con ejercicios y desafíos mentalesDe EverandACV Accidente Cerebrovascular: Guía de actividades con ejercicios y desafíos mentalesAún no hay calificaciones
- Síndrome Coronario Agudo CHM 2020Documento15 páginasSíndrome Coronario Agudo CHM 2020Thomas Schweitzer SaavedraAún no hay calificaciones
- Cardiopatia IsquemicaDocumento11 páginasCardiopatia Isquemicashadi mAún no hay calificaciones
- 4-CARDIOPATÍA ISQUÉMICA ESTABLEDocumento34 páginas4-CARDIOPATÍA ISQUÉMICA ESTABLEflorian debergueAún no hay calificaciones
- Cardiopatia2 IsquemicaDocumento15 páginasCardiopatia2 IsquemicadvdprcyAún no hay calificaciones
- Nota de Voz SCADocumento23 páginasNota de Voz SCAEstefany Rivera MorenoAún no hay calificaciones
- Practica 9Documento22 páginasPractica 9Claudia SalasAún no hay calificaciones
- T3 Fisiopatología Cardiopatía Isquémica I 2023 FINAL PDFDocumento32 páginasT3 Fisiopatología Cardiopatía Isquémica I 2023 FINAL PDFAngye KarenAún no hay calificaciones
- INFARTODocumento8 páginasINFARTOmaluRubielasAún no hay calificaciones
- Subtema 3-5. Infarto Al MiocardioDocumento29 páginasSubtema 3-5. Infarto Al MiocardioJosé LuisAún no hay calificaciones
- Clase Cardiologia - Cardiopatia IsquemicaDocumento42 páginasClase Cardiologia - Cardiopatia IsquemicaLarissa SeabraAún no hay calificaciones
- Word - Infarto Agudo de MiocardioDocumento10 páginasWord - Infarto Agudo de MiocardioVenuziita Garcia100% (1)
- Cardiopatía isquémicaDocumento3 páginasCardiopatía isquémicaDubhé PeredaAún no hay calificaciones
- Trastornos Circulatorios y CardiacosDocumento33 páginasTrastornos Circulatorios y CardiacosMaríaAún no hay calificaciones
- Sindrome CoronarioDocumento13 páginasSindrome CoronarioEli TobarAún no hay calificaciones
- Resumen Cardiopatía IsquémicaDocumento4 páginasResumen Cardiopatía IsquémicaDonovan Noe Gamez VegaAún no hay calificaciones
- Clinica de La AterosclerosisDocumento4 páginasClinica de La Aterosclerosisbryanjhoan32Aún no hay calificaciones
- Insuficiencia CoronariaDocumento12 páginasInsuficiencia Coronariabolgan2603Aún no hay calificaciones
- Enfermedad de Las Arterias Coronarias PDFDocumento24 páginasEnfermedad de Las Arterias Coronarias PDFGesselle GalarragaAún no hay calificaciones
- Insuficiencia CoronariaDocumento15 páginasInsuficiencia CoronariaAndrea PeñaAún no hay calificaciones
- Guión de PatologiasDocumento11 páginasGuión de PatologiasBritney ErazoAún no hay calificaciones
- Cap 03 PDFDocumento36 páginasCap 03 PDFCarolina A. AlmendraAún no hay calificaciones
- Cardiopatia IsquemicaDocumento36 páginasCardiopatia IsquemicaWilfredo AmayaAún no hay calificaciones
- Caso Clínico #5 - IamDocumento13 páginasCaso Clínico #5 - IamGenaro Colina YesquénAún no hay calificaciones
- Infarto Al Miocardio - PPTMDocumento6 páginasInfarto Al Miocardio - PPTMJhon OcandoAún no hay calificaciones
- Arterioesclerosis y sus factores de riesgoDocumento14 páginasArterioesclerosis y sus factores de riesgoIsabella ValentinaAún no hay calificaciones
- Cap 50-62 Pág 433-542 Circ Renal y EndocrinoDocumento99 páginasCap 50-62 Pág 433-542 Circ Renal y EndocrinoVïctor RiquelmeAún no hay calificaciones
- Insuficiencia Cardíaca Con Fracción de Eyección ReducidaDocumento2 páginasInsuficiencia Cardíaca Con Fracción de Eyección ReducidaMannie O. Carhuaricra FloresAún no hay calificaciones
- Marco TeoricoDocumento3 páginasMarco TeoricoPedro Quiroga0% (1)
- Sindrome Coronario Agudo Expo MillanDocumento15 páginasSindrome Coronario Agudo Expo MillanAndresOsorioGomezAún no hay calificaciones
- Fisiopatología de la isquemia miocárdica: causas, consecuencias y mecanismosDocumento8 páginasFisiopatología de la isquemia miocárdica: causas, consecuencias y mecanismostomas sererAún no hay calificaciones
- Sindrome Coronaria AgudoDocumento16 páginasSindrome Coronaria AgudoSamanta MozAún no hay calificaciones
- AcvDocumento26 páginasAcvCamila SantisAún no hay calificaciones
- Infarto MiocardioDocumento10 páginasInfarto MiocardioNathaliPerezAún no hay calificaciones
- IAM-InfartoAgudoMiocardioDocumento81 páginasIAM-InfartoAgudoMiocardiomariocperaltaAún no hay calificaciones
- Cardiologia Apuntes Completos Ano 20142015Documento269 páginasCardiologia Apuntes Completos Ano 20142015Adrian Garcia MAún no hay calificaciones
- Enfermedad Cerebrovascular APDocumento4 páginasEnfermedad Cerebrovascular APastrid carolina gamboa castellanosAún no hay calificaciones
- CardiopatiasDocumento4 páginasCardiopatiasBernard HubbardAún no hay calificaciones
- Cardiopatía IsquémicaDocumento4 páginasCardiopatía IsquémicaVialy SantanaAún no hay calificaciones
- Cardiopatia IsquemicaDocumento40 páginasCardiopatia IsquemicaCamila Andrea De La Hoz Polonia100% (1)
- Evc Isquémico - jesWPS OfficeDocumento19 páginasEvc Isquémico - jesWPS OfficeJessy QuezadaAún no hay calificaciones
- Cardiopatia IsquemicaDocumento40 páginasCardiopatia IsquemicaAna Mirian LagoAún no hay calificaciones
- Cardiopatía isquémica: causas, síntomas y diagnósticoDocumento33 páginasCardiopatía isquémica: causas, síntomas y diagnósticoMaricarmen De La Cruz100% (3)
- Sindrome CoronarioDocumento16 páginasSindrome Coronariodaiana pachecoAún no hay calificaciones
- Acv IsquémicoDocumento13 páginasAcv IsquémicoThamara SandovalAún no hay calificaciones
- Síndrome coronario agudo.pptxDocumento45 páginasSíndrome coronario agudo.pptxIsabelle CzwAún no hay calificaciones
- Apunte45 Infarto Agudo Al MiocardioDocumento7 páginasApunte45 Infarto Agudo Al MiocardioDANIEL ALEJANDROAún no hay calificaciones
- Infarto agudo de miocardio con elevación del segmento ST. SCACESTDocumento8 páginasInfarto agudo de miocardio con elevación del segmento ST. SCACESTHermus Espiritu MaturranoAún no hay calificaciones
- Infarto Agudo Del MiocardioDocumento15 páginasInfarto Agudo Del MiocardioGaby MedinaAún no hay calificaciones
- Fisio 12Documento12 páginasFisio 12jenry chapoñanAún no hay calificaciones
- Enfermedades Cerebrovasculares Dra RaimondiDocumento12 páginasEnfermedades Cerebrovasculares Dra RaimondiMaria ElinaAún no hay calificaciones
- ICC: Insuficiencia Cardíaca CongestivaDocumento12 páginasICC: Insuficiencia Cardíaca CongestivaPaola GarciaAún no hay calificaciones
- Acv IsquemicoDocumento7 páginasAcv IsquemicoPatricia Aragon BeltranAún no hay calificaciones
- Etiologia Del Infarto Agudo de MiocardioDocumento3 páginasEtiologia Del Infarto Agudo de MiocardioGrizsel PatonAún no hay calificaciones
- Cardiopatia IsquemicaDocumento26 páginasCardiopatia IsquemicaJuan Antonio CordónAún no hay calificaciones
- Cardiopatía Isquémica (Síndrome Coronario Agudo)Documento24 páginasCardiopatía Isquémica (Síndrome Coronario Agudo)Mariangélica Álvarez SuárezAún no hay calificaciones
- GPC 7 Sica 2014Documento20 páginasGPC 7 Sica 2014MeliSsa DanielaAún no hay calificaciones
- Cardiopatía IsquémicaDocumento17 páginasCardiopatía IsquémicaOsmar MirellaAún no hay calificaciones
- Infarto de MiocardioDocumento10 páginasInfarto de MiocardioJose HernandezAún no hay calificaciones
- Infarto CerebralDocumento10 páginasInfarto Cerebraljennifer enriquezAún no hay calificaciones
- Clase 8 Tejido Muscular 1Documento52 páginasClase 8 Tejido Muscular 1bryanjhoan32Aún no hay calificaciones
- Clase 8-Membrana Celular-Dr LesterDocumento22 páginasClase 8-Membrana Celular-Dr Lesterbryanjhoan32Aún no hay calificaciones
- Huesos Del NeurocraneoDocumento45 páginasHuesos Del Neurocraneobryanjhoan32Aún no hay calificaciones
- Artritis ReumatoideDocumento6 páginasArtritis Reumatoidebryanjhoan32Aún no hay calificaciones
- Cardiopatia Isquémica.-2Documento4 páginasCardiopatia Isquémica.-2bryanjhoan32Aún no hay calificaciones
- 2023 JunioDocumento456 páginas2023 JunioPaulina CuevaAún no hay calificaciones
- Discapacidad IntelectualDocumento17 páginasDiscapacidad IntelectualCarmen CarrilloAún no hay calificaciones
- ANEMIASDocumento37 páginasANEMIASMatías Fernández Müllendorff100% (1)
- Entamoeba MicrobiologíaDocumento11 páginasEntamoeba MicrobiologíaCristhian V. PasquelAún no hay calificaciones
- EsquistocitosDocumento4 páginasEsquistocitosJuanAún no hay calificaciones
- Sind Vertiginosos PerifericoDocumento9 páginasSind Vertiginosos PerifericoSaic MhunAún no hay calificaciones
- Trombofilia y SAF DR Rosa Nov 2022Documento74 páginasTrombofilia y SAF DR Rosa Nov 2022yandros666Aún no hay calificaciones
- Guia #5 Fracturas Por Caidas, Armas de Fuego y Minas en El Campo de OperacionesDocumento6 páginasGuia #5 Fracturas Por Caidas, Armas de Fuego y Minas en El Campo de OperacionesValenn AldanaAún no hay calificaciones
- Uncinariasis y EstrongiloidiasisDocumento27 páginasUncinariasis y EstrongiloidiasisileanaAún no hay calificaciones
- Plan de Sesiones Educativas para La Prevención de Anemia Dirigido A Madres Con Niños Menores de 5 Años Del Centro de Salud La Unión, 2023Documento15 páginasPlan de Sesiones Educativas para La Prevención de Anemia Dirigido A Madres Con Niños Menores de 5 Años Del Centro de Salud La Unión, 2023Franklin Florentino Herrera SanchezAún no hay calificaciones
- EXAMEN PSICO 3ER ParcialDocumento4 páginasEXAMEN PSICO 3ER ParcialDrisdale Nuñez FondeurAún no hay calificaciones
- 2 Era de Microbiología Tanto 2020como 2021Documento24 páginas2 Era de Microbiología Tanto 2020como 2021Leonardo PereiraAún no hay calificaciones
- Criterios Diagnosticos de Demencia A Las Puertas DDocumento8 páginasCriterios Diagnosticos de Demencia A Las Puertas DÁngeles Guerrero RodríguezAún no hay calificaciones
- Unidad 3 - Tarea - 4 - Evaluación de Los Aspectos Neuropsicológicos Del ComportamientoDocumento13 páginasUnidad 3 - Tarea - 4 - Evaluación de Los Aspectos Neuropsicológicos Del ComportamientoDanissPuerto0% (2)
- Casoclinico ICTERICIADocumento4 páginasCasoclinico ICTERICIAhumberto100% (2)
- Botox - ProspectoDocumento15 páginasBotox - ProspectoFernando TochoAún no hay calificaciones
- Adherencia Al Tratamiento FARMACOLOGICODocumento8 páginasAdherencia Al Tratamiento FARMACOLOGICOmartaAún no hay calificaciones
- Medici 2Documento49 páginasMedici 2api-3715153Aún no hay calificaciones
- FisuraDocumento18 páginasFisuraIsraael JuuareezAún no hay calificaciones
- Exposición Riesgo Biomecanico C1Documento25 páginasExposición Riesgo Biomecanico C1Damaris Valdes Lopez100% (2)
- Presion Alta y Baja, Infeccion UrinariaDocumento10 páginasPresion Alta y Baja, Infeccion UrinariaMiguel JocolAún no hay calificaciones
- Glosario MedicoDocumento13 páginasGlosario MedicoLuis BenitezAún no hay calificaciones
- Consentimiento Informado (Radiofrecuencia)Documento3 páginasConsentimiento Informado (Radiofrecuencia)Prema SpaAún no hay calificaciones
- Abordaje de TO en Un Hospital de Agudos Desde Una Mirada ClinicaDocumento25 páginasAbordaje de TO en Un Hospital de Agudos Desde Una Mirada Clinicaaimaraangeles98Aún no hay calificaciones
- DISLIPIDEMIADocumento4 páginasDISLIPIDEMIAandre gilAún no hay calificaciones
- Caso de Dever Sin RespuestasDocumento7 páginasCaso de Dever Sin RespuestasXiomara Melo machadoAún no hay calificaciones
- Cea CérvixDocumento13 páginasCea CérvixArantza Tapia QuispeAún no hay calificaciones
- BIOFÍSICADocumento2 páginasBIOFÍSICAAle UCAún no hay calificaciones
- Aparato RespiratorioDocumento5 páginasAparato RespiratorioDinny GaruzAún no hay calificaciones
- 8 Promociones Consolidado GLORIA MOREIRA TOLEDODocumento31 páginas8 Promociones Consolidado GLORIA MOREIRA TOLEDOgloryrockzAún no hay calificaciones
- Periodontitis and GingivitisDocumento60 páginasPeriodontitis and GingivitisSt@r golden100% (3)