Documentos de Académico
Documentos de Profesional
Documentos de Cultura
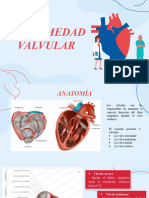
Insuficiencia Aórtica
Cargado por
trofincrisDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Insuficiencia Aórtica
Cargado por
trofincrisCopyright:
Formatos disponibles
Fisterra
Fecha de revisión: 19/04/2019
Inicio > Guías > Insuficiencia aórtica
Relaciones
Insuficiencia aórtica
Técnicas relacionadas
Índice de contenidos ¿De qué hablamos? • Exploración cardiológica
• ¿De qué hablamos?
Son muy numerosas y diversas las enfermedades que pueden causar Trabajos recientes relacionados
• ¿Cuál es la clínica y la insuficiencia aórtica (IAo) como se enumeran en la tabla 1. Es muy importante
historia natural? diferenciar entre ellas las que causan IAo aguda de las que producen IAo • 22/11/2021 - Enfermedad valvular
• ¿Cómo diagnosticarla? crónica por su distinta fisiopatología, clínica, manejo diagnóstico y cardiaca en adultos: investigación
terapéutico. No son compartimentos rígidos, puede haber causas agudas que y manejo (Guía NICE)
• ¿Cuál es su tratamiento
en ocasiones se comportan como crónicas (Vahanian A, 2009).
médico?
Codificación
• ¿Cuáles son las
indicaciones del Tabla 1. Causas de IAo.
CIAP-2K83 CIE10I08.0
tratamiento IAo aguda IAo crónica
quirúrgico? CIE10I08.2 CIE10I35.1
Dilatación idiopática de la aorta o ectasia anulo-
• Seguimiento y pruebas Endocarditis infecciosa*
aórtica* CIE9396.2 CIE9396.3
seriadas
Infarto agudo de CIE9424.1
• Bibliografía Congénitas-bicúspides*
miocardio*
• Más en la red
Disfunción válvula Síndrome de Marfan, Ehlers-Danlos, Hurler,
• Autores
protésica* Reiter
Aneurisma de aorta* Reumática*
Disección aórtica* HTA*
Traumatismo de tórax Sífilis
Espondilitis anquilopoyética, artritis
reumatoide, arteritis de células gigantes
(*) Causas más frecuentes.
La característica fisiopatológica fundamental de la IAo aguda es la falta de
adaptación del ventrículo izquierdo (VI) al aumento repentino de volumen y
presión procedente de la válvula aórtica incompetente y de la contracción
auricular izquierda (AI). Esta rapidez de instauración hace que el VI no pueda
aumentar su distensibilidad con la consiguiente elevación brusca de la
presión diastólica que se transmite hacia la AI produciéndose finalmente una
rápida congestión pulmonar e insuficiencia cardiaca (IC).
En la IAo crónica el VI se adapta con dilatación y aumento de la distensibilidad
(hipertrofia excéntrica) sin gran aumento del volumen diastólico durante
muchos años produciéndose, sólo al final, la situación de fracaso del mismo e
IC. Las necesidades de oxígeno miocárdico están aumentadas por este
mecanismo de hipertrofia y por la disminución de flujo coronario.
¿Cuál es la clínica y la historia natural?
En la IAo aguda lo más frecuente es que nos encontremos al paciente en
situación de shock cardiogénico y edema agudo pulmonar (EAP). Los
pacientes con IA aguda grave, cuyas causas más frecuentes son la endocarditis
infecciosa y la disección aórtica, tienen mal pronóstico sin intervención,
debido a su inestabilidad hemodinámica.
En la IAo crónica se mantienen asintomáticos durante muchos años. Al
principio son muy frecuentes las palpitaciones con el ejercicio produciéndose
finalmente angor, síncope y arritmias ventriculares. La muerte súbita sucede
en <0,2% de los pacientes asintomáticos. Al final se produce IC con disnea y
edemas en miembros inferiores.
Los pacientes con IA crónica grave y síntomas también tienen mal pronóstico
a largo plazo. Una vez se presentan los síntomas, la mortalidad entre los
pacientes no intervenidos puede alcanzar un 10-20% anual (Bonow RO, 1991).
En pacientes asintomáticos con IA grave crónica y función del VI normal, la
posibilidad de complicaciones graves es baja. Sin embargo, cuando el
diámetro telesistólico del ventrículo izquierdo (DTSVI) es >50 mm, la
probabilidad de muerte, síntomas o disfunción del VI es del 19% anual.
La historia natural de la aorta ascendente y aneurismas de la raíz ha sido
mejor definida en el síndrome de Marfan.
Los predictores más potentes de muerte o complicaciones de aorta son el
diámetro de la raíz aórtica y la historia familiar de eventos cardiovasculares
(disección de aorta y muerte súbita).
Por lo general, se creía que los pacientes con válvulas aórticas bicúspides
tenían mayor riesgo de disección. La evidencia científica más reciente indica
que este riesgo puede estar relacionado con la alta prevalencia de dilatación
de la aorta ascendente.
¿Cómo diagnosticarla?
La historia clínica y la exploración física son, como siempre, de suma
importancia.
En la IAo aguda no habrá signos en la exploración física salvo los signos
típicos del shock cardiogénico y EAP. Puede existir un soplo diastólico débil.
En el ECG veremos más frecuentemente taquicardia sinusal y en la
radiografía de tórax no existirá cardiomegalia y sí datos de edema intersticial.
La ecocardiografía es la exploración básica para determinar la IAo y
determinar la causa. En el caso de que la causa sea una disección aórtica o
una endocarditis infecciosa está indicado el ecocardiograma transesofágico e
incluso el TAC y/o la RNM del tórax en el primer caso. En la mayoría de los
casos no es preciso una coronariografía por la situación de inestabilidad del
paciente.
En la IAo crónica es típico encontrar en la auscultación un soplo
protodiastólico en el segundo y tercer espacio intercostal izquierdo, de alta
frecuencia que puede irradiarse a lo largo del borde esternal, hueco
supraesternal hasta raíz del cuello, aumentando con la incorporación del
paciente hacia delante. Además existe un tercer ruido S3 por sobrecarga de
volumen. El latido apical y la presión diferencial de pulso son amplios e
implican gravedad de la IAo. En el ECG es frecuente el ritmo sinusal excepto
en los casos donde se asocia valvulopatía mitral que puede existir fibrilación
auricular (FA). En las etapas avanzadas hay signos de sobrecarga diastólica del
VI con Q profunda, R alta y T picuda y en estadios avanzados depresión del
segmento ST y arritmias ventriculares. La radiografía de tórax puede mostrar
cardiomegalia, elongación del cayado aórtico y datos de IC en estadios
avanzados. La prueba cumbre en la IAo es la ecocardiografía. En la tabla 2 se
enumeran las indicaciones de la ecocardiografía y en la tabla 3 la clasificación
de la gravedad de la IAo.
Tabla 2. Indicaciones de ecocardiografía.
Recomendado
Confirmar la presencia y severidad de la IAo aguda y crónica.
Mecanismo causal de la IAo crónica (incluyendo morfología valvular y de
raíz aórtica):
• Tipo 1: cúspides normales pero coaptación insuficiente debido a la
dilatación de la raíz aórtica con chorro central.
• Tipo 2: prolapso de cúspides con chorro excéntrico.
• Tipo 3: retracción con una calidad deficiente del tejido valvular y chorro
central o excéntrico grande.
Para valoración de la hipertrofia ventricular, dimensión (o volumen), y
función sistólica.
Medición de la raíz aórtica y aorta ascendente bidimensional (2D) en 4
niveles*: anillo, senos de Valsalva, unión sinotubular y porción tubular de
aorta ascendente.
Fenotipos de aorta ascendente:
• Aneurisma de la raíz aórtica (senos de Valsalva >45 mm).
• Aneurisma tubular de la aorta ascendente (senos de Valsalva <40-45
mm).
• Insuficiencia aórtica aislada (todos los diámetros <40 mm).
Reevaluación periódica del tamaño del VI y función del mismo en pacientes
asintomáticos con IAo severa.
Reevaluación de IAo leve-moderada o severa cuando existen nuevos
síntomas.
(*) Medición en plano paraesternal longitudinal del borde anterior al borde
anterior de la pared de la aorta en telediástole, (excepto anillo aórtico,
medido en sístole media).
Tabla 3. Clasificación de la severidad de la IAo.
Ligera Moderada Severa
Grado
1+ 2+ 3-4+
angiográfico
Flujo
Mayor que
central, Flujo central,
Ancho del la IAo ligera
ancho ancho mayor
flujo por pero sin
menor del al 65% del
Cualitativo Doppler signos de
25% del flujo del VI
IAo severa
flujo del VI
Ancho de
vena Menor de Mayor o igual
0,30-0,69
contracta por 0,30 a 0,70
Doppler (cm)
Volumen de
Menor de Mayor o igual
regurgitación 30-59
30 a 60
(ml/impulso)
Fracción de
Cuantitativo Menor de Mayor o igual
regurgitación 30-49
(cateterismo o 30 a 50
(%)
ecocardiografía)
Área del
orificio de Menor de Mayor o igual
0,10-0,29
regurgitación 0,10 a 0,30
(cm2)
Criterio
Tamaño del
adicional Incrementado
VI
esencial
En los casos de IAo asintomáticos con vida activa, una ecocardiografía de
buena calidad es suficiente para valorar el grado de IAo. En los casos de IAo
severa y vida sedentaria o con síntomas de difícil interpretación, la prueba de
esfuerzo o ergometría ayuda a definir la capacidad funcional, los síntomas y
los efectos hemodinámicos con el ejercicio.
Las principales indicaciones de la ergometría en IAo crónica son: a) valoración
de la capacidad funcional y respuesta sintomática en pacientes con historia
clínica equívoca; b) valoración de la capacidad funcional y respuesta
sintomática antes de la participación en actividades atléticas (American
College of Cardiology, 2006).
La resonancia magnética nuclear (RNM) nos sirve para cuantificar la fracción
regurgitante cuando las mediciones ecocardiográficas sean equívocas.
Para pacientes con dilatación aórtica, se recomienda la tomografía
computarizada sincronizada (TC) para determinar el diámetro máximo.
La RNM puede emplearse durante el seguimiento, pero la indicación de
cirugía debe basarse preferiblemente en las mediciones de la TC. Para
mejorar la reproducibilidad, se recomienda medir los diámetros usando la
técnica de borde interior a borde interior al final de la diástole en el plano
estrictamente transversal, con reconstrucción doble oblicua perpendicular al
eje del flujo sanguíneo del segmento correspondiente.
Deben registrarse los diámetros a nivel del anillo, senos de Valsalva, unión
sinotubular, aorta ascendente tubular y arco aórtico. El diámetro máximo de
la raíz debe tomarse de seno a seno.
¿Cuál es su tratamiento médico?
En la IAo aguda habrá que realizar un tratamiento intensivo del shock
cardiogénico y del EAP con vasodilatadores arteriales como el nitroprusiato
sódico e inotrópicos positivos (dopamina/dobutamina), previa a la
intervención quirúrgica urgente. El balón de contrapulsación aórtica está
contraindicado.
La IAo crónica ligera o moderada con buena función ventricular no precisa
tratamiento farmacológico.
El tratamiento médico puede mejorar los síntomas de los individuos con
insuficiencia aórtica grave crónica que no son candidatos a cirugía. Para los
pacientes que después de la cirugía siguen sufriendo insuficiencia cardiaca o
hipertensión, son útiles los inhibidores de la enzima de conversión de la
angiotensina (IECA), los antagonistas del receptor de la angiotensina II (ARA-
II) y los bloqueadores beta.
En pacientes con síndrome de Marfan, los bloqueadores beta y el losartán
pueden reducir la dilatación de la raíz aórtica y el riesgo de complicaciones
aórticas, por lo que se debe considerarlos antes y después de la cirugía.
En la práctica clínica se recomienda frecuentemente el tratamiento con
bloqueadores beta o losartán para pacientes con válvula aórtica bicúspide si la
raíz aórtica o la aorta ascendente están dilatadas.
Gestación: para las mujeres con síndrome de Marfan y un diámetro aórtico
>45 mm, se desaconseja la gestación antes de la reparación de la válvula
debido al alto riesgo de disección. Aunque un diámetro aórtico <40 mm se
asocia raramente con la disección aórtica, no existe un diámetro
completamente seguro. Si el diámetro de la aorta es de 40-45 mm, el
crecimiento aórtico previo y la historia familiar son aspectos importantes para
aconsejar a las pacientes sobre la gestación con o sin reparación aórtica
previa.
Aunque el riesgo real de disección no está bien documentado en los casos de
válvulas bicúspides, se recomienda desaconsejar la gestación a las pacientes
con diámetros aórticos >50 mm.
Actividad deportiva: se debe desaconsejar la práctica de ejercicio físico
extenuante o deportes de contacto físico, competitivos e isométricos a los
pacientes con síndrome de Marfan o con diámetros de la raíz aórtica cercanos
al límite del umbral de intervención.
Screening: dado el riesgo familiar de aneurisma de aorta torácica, está
indicado el cribado y remitir para pruebas genéticas y de imagen a los
familiares de primer grado de los pacientes con enfermedad del tejido
conectivo.
Para pacientes con válvulas bicúspides, es apropiado realizar un cribado
ecocardiográfico de los familiares de primer grado.
¿Cuáles son las indicaciones del
tratamiento quirúrgico?
La insuficiencia aórtica aguda puede requerir cirugía urgente. Sus causas
principales son la endocarditis infecciosa y la disección aórtica.
Las indicaciones de intervención en la insuficiencia aórtica crónica se
resumen en la siguiente tabla según las recomendaciones de la guía europea
(Baumgartner H, 2017) (tabla 4).
Para los pacientes sintomáticos, la cirugía está recomendada
independientemente de la FEVI, excepto en casos extremos, siempre que la
insuficiencia aórtica sea grave y el riesgo operatorio no excesivamente alto.
En los pacientes asintomáticos con insuficiencia aórtica grave, la función del
VI disminuida (FEVI ≤50%) y la dilatación del VI con un diámetro
telediastólico >70 mm o un diámetro telesistólico (DTSVI) >50 mm se debe
intentar la cirugía cuando se alcancen estos valores.
Los aneurismas de raíz requieren el reemplazo de la raíz con reimplante
coronario.
Los aneurismas de la aorta ascendente tubular, con o sin conservación de la
válvula aórtica nativa, requieren el reemplazo con injerto tubular
supracomisural, sin reimplante coronario.
Ante pacientes con diámetros aórticos en valores límite para la cirugía, hay
que tener en cuenta la historia familiar, la edad y el riesgo estimado del
procedimiento.
Para los individuos con válvula aórtica bicúspide sin insuficiencia significativa,
debe considerarse la cirugía profiláctica si los diámetros aórticos son ≥55 o
≥50 mm en presencia de factores adicionales de riesgo o coartación.
La cirugía está indicada para todo paciente con síndrome de Marfan y un
diámetro aórtico máximo ≥50 mm. Para los pacientes con síndrome de
Marfan y factores de riesgo adicionales y los pacientes con mutación de
TGFBR1 o TGFBR2 (incluido el síndrome de Loeys-Dietz), debe considerarse
la cirugía si el diámetro aórtico máximo es ≥45 mm. En este último grupo, las
mujeres con ASC baja, los pacientes con mutación en TGFBR2 o los pacientes
con enfermedad grave no relacionada con la aorta tienen un riesgo
especialmente elevado y puede considerarse la cirugía en umbrales <40 mm.
Para los pacientes con raíz aórtica ≥55 mm, debe considerarse la cirugía
independientemente del grado de insuficiencia aórtica o el tipo de
enfermedad valvular.
En los pacientes que tienen una indicación para cirugía de válvula aórtica, un
diámetro aórtico ≥45 mm se considera indicación para cirugía concomitante
de la raíz aórtica o de la aorta ascendente tubular.
Deben considerarse la estatura del paciente y la etiología de la valvulopatía
(válvula bicúspide), además de la forma y el grosor de la pared de la aorta
ascendente determinados durante el procedimiento, para tomar decisiones
individualizadas.
Aunque el reemplazo valvular es el procedimiento estándar para la mayoría de
los pacientes con insuficiencia aórtica, debe considerarse el reemplazo
valvular o la cirugía con conservación de la válvula para los pacientes con
válvula tricúspide o bicúspide flexible y no calcificada, con mecanismo
subyacente de tipo I (dilatación de la raíz aórtica con movilidad normal de las
cúspides) o de tipo II (prolapso de cúspides).
En centros con experiencia, con el reemplazo de la raíz y conservación de la
válvula y la reparación valvular, si es factible, se han demostrado buenos
resultados a largo plazo, con tasas bajas de complicaciones relacionadas con la
válvula y mejor calidad de vida.
La elección del procedimiento quirúrgico debe adaptarse a la experiencia del
equipo, la presencia de aneurisma de raíz aórtica, las características de las
cúspides, la esperanza de vida y al estado de anticoagulación deseado. Se debe
remitir a equipos quirúrgicos con experiencia en el procedimiento a todo
paciente para el que el equipo cardiológico interdisciplinario considere viable
la reparación de la válvula aórtica.
Tabla 4. Indicaciones de recambio o reparación valvular en la insuficiencia aórtica.
A) Indicación para cirugía en IAo severa
IAo severa sintomática sin tener en cuenta la FEVI. Recomendado
IAo crónica severa asintomática con disfunción del VI (FEVI ≤50%)
Recomendado
en reposo.
IAo crónica severa que van a ser sometidos a cirugía coronaria, de
Recomendado
aorta o de otras válvulas.
IAo severa asintomáticos con función del VI normal (FEVI >50%),
con dilatación severa del VI (DTD >70 mm o DTS >50 mm, o DTS Razonable
>25 mm/m2 IMC ).a
B) Indicación para cirugía en enfermedad de raíz aórtica (sea cual sea la severidad
de la IAo)
Paciente con enfermedad de raíz aórtica con un diámetro máximo
de aorta ascendenteb ≥50 mm en pacientes con síndrome de Recomendado
Marfan.
Pacientes con enfermedad en raíz aórtica con diámetro máximo
aórtico (sea cual sea la severidad de la IAo):
1. ≥45 mm para pacientes con síndrome de Marfan con factores
de riesgo.c Razonable
2. ≥50 mm para pacientes con válvula bicúspide con factores de
riesgo.d
3. ≥55 mm para otros pacientes.
a Se deben tener en cuenta los cambios en el seguimiento.
b En la decisión hay que tener en cuenta también la forma de las distintas partes
de la aorta. Se puede utilizar umbrales más bajos para la cirugía combinada de la
aorta ascendente en pacientes que tienen una indicación de cirugía valvular
aórtica.
c Pacientes con historia familiar de disección aórtica y/o un aumento de la aorta >2
mm/año (en el seguimiento con la misma técnica de imagen, medidas en el
mismo nivel de la aorta con comparación «lado a lado» y confirmadas por otra
técnica), insuficiencia aórtica o mitral grave, deseo de gestar.
d Coartación de la aorta, hipertensión sistémica, historia familiar de disección
aórtica o un aumento de la aorta >2 mm/año (en el seguimiento con la misma
técnica de imagen, medidas en el mismo nivel de la aorta con comparación «lado
a lado» y confirmadas por otra técnica).
Seguimiento y pruebas seriadas
Los pacientes con IAo leve-moderada pueden ser revisados clínicamente cada
año, y mediante ecocardiografía cada 2 años.
Todos los pacientes con IAo severa y función VI normal deben ser seguidos a
los 6 meses después de su examen inicial, si el diámetro del VI y/o la FE
muestra cambios significativos, o se acerca al umbral de intervención, el
seguimiento debe de continuarse a intervalos de 6 meses. En los casos no
concluyentes, puede ser útil determinar las concentraciones de BNP, ya que
su elevación durante el seguimiento se ha asociado con deterioro de la
función del VI.
Los pacientes asintomáticos con insuficiencia aórtica grave y función del VI
normal y parámetros estables pueden ser seguidos anualmente.
En pacientes con dilatación de aorta, y especialmente en síndrome de Marfan
o con válvula bicúspide, un ecocardiograma debe ser realizado de rutina una
vez al año.
En los casos de dilatación de la aorta ascendente (>40 mm), la TC o RMC
están recomendadas. La evaluación de seguimiento de las dimensiones de la
aorta debe realizarse mediante ecocardiografía o RMC. Cualquier aumento >3
mm debe validarse mediante angio-TC/RMC y compararse con los datos
basales.
Bibliografía
• American College of Cardiology; American Heart Association Task Force
on Practice Guidelines (Writing Committee to revise the 1998 guidelines
for the management of patients with valvular heart disease); Society of
Cardiovascular Anesthesiologists, Bonow RO, Carabello BA, Chatterjee K,
de Leon AC Jr, Faxon DP, Freed MD, et al. ACC/AHA 2006 guidelines for
the management of patients with valvular heart disease: a report of the
American College of Cardiology/American Heart Association Task Force
on Practice Guidelines (writing Committee to Revise the 1998 guidelines
for the management of patients with valvular heart disease) developed in
collaboration with the Society of Cardiovascular Anesthesiologists
endorsed by the Society for Cardiovascular Angiography and
Interventions and the Society of Thoracic Surgeons. J Am Coll Cardiol.
2006;48(3):e1-148. PubMed PMID: 16875962. Texto completo
• Azpitarte J, Alonso AM, García GF, González Santos JM, Paré C, Tello A.
Guías de práctica clínica de la Sociedad Española de Cardiología en
valvulopatías. Rev Esp Cardiol. 2000;53(9):1209-78. PubMed PMID: 10978
237
• Baumgartner H, Falk V, Bax JJ, De Bonis M, Hamm C, Holm PJ, et al; ESC
Scientific Document Group. 2017 ESC/EACTS Guidelines for the
management of valvular heart disease. Eur Heart J. 2017;38(36):2739-91.
PubMed PMID: 28886619. Texto completo
• Baumgartner H. Aortic stenosis: medical and surgical management.
Heart. 2005;91(11):1483-8. PubMed PMID: 16230456. Texto completo
• Bekeredjian R, Grayburn PA. Valvular heart diseases. Aortic regurgitation.
Circulation. 2005;112(1):125-34. PubMed PMID: 15998697. Texto completo
• Bonow RO, Lakatos E, Maron BJ, Epstein SE. Serial long-term assessment
of the natural history of asymptomatic patients with chronic aortic
regurgitation and normal left ventricular systolic function. Circulation.
1991;84:1625-35. PubMed PMID: 1914102
• Borer JS, Bonow RO. Contemporary approach to aortic and mitral
regurgitation. Circulation. 2003;108(20):2432-8. PubMed PMID:
14623790. Texto completo
• Botkin NF, Aurigemma GP. Aortic valve disease: current
recommendations. Curr Cardiol Rep. 2004;6(2):89-95. PubMed PMID: 147
59350
• Carabello BA, Crawford FA. Valvular herat disease. N Engl J Med.
1997;337(1):32-41. PubMed PMID: 9203430
• Chirillo F, Salvador L, Cavallini C. Medical and surgical treatment of
chronic mitral regurgitation. J Cardiovasc Med (Hagerstown).
2006;7(2):96-107. PubMed PMID: 16645368
• Davies RR, Kaple RK, Mandapati D, Gallo A, Botta DM, Elefteriades JA, et
al. Natural history of ascending aortic aneurysms in the setting of an
unreplaced bicuspid aortic valve. Ann Thorac Surg. 2007;83(4):1338-44.
PubMed PMID: 17383337. Texto completo
• Evangelista A, Tornos P, Sambola A, Permanyer-Miralda G, Soler-Soler J.
Longterm vasodilator therapy in patients with severe aortic regurgitation.
N Engl J Med. 2005;353(13):1342-9. PubMed PMID: 16192479. Texto comp
leto
• Keeffe BG, Otto CM. Mitral regurgitation. Minerva Cardioangiol.
2003;51(1):29-39. PubMed PMID: 12652258
• Otto CM. Timing of surgery in mitral regurgitation. Heart.
2003;89(1):100-5. PubMed PMID: 12482807. Texto completo
• Vahanian A, Alfieri O, Andreotti F, Antunes MJ, Barón-Esquivias G,
Baumgartner H, et al. Guidelines on the management of valvular heart
disease (version 2012): the Joint Task Force on the Management of
Valvular Heart Disease of the European Society of Cardiology (ESC) and
the European Association for Cardio-Thoracic Surgery (EACTS). Eur J
Cardiothorac Surg. 2012 Oct;42(4):S1-44. PubMed PMID: 22922698. Texto
completo
• Vahanian A, Iung B, Pierard L, Dion R, Pepper J. Valvular heart disease.
En: Camm AJ, Luscher TF, Serruys PW, editors. The ESC Textbook of
Cardiovascular Medicine. 2.ª ed. Malden/Oxford/Victoria: Blackwell
Publishing Ltd.; 2009. p. 625-70.
• Zoghbi WA, Enriquez-Sarano M, Foster E, Grayburn PA, Kraft CD, Levine
RA, et al; American Society of Echocardiography. Recommendations for
evaluation of the severity of native valvular regurgitation with two-
dimensional and Doppler echocardiography. J Am Soc Echocardiogr.
2003;16(7):777-802. PubMed PMID: 12835667. Texto completo
Más en la red
• Akinseye OA, Pathak A, Ibebuogu UN. Aortic Valve Regurgitation: A
Comprehensive Review. Curr Probl Cardiol. 2018 Aug;43(8):315-334.
PubMed PMID: 29174586
• Baumgartner H, Falk V, Bax JJ, De Bonis M, Hamm C, Holm PJ, et al; ESC
Scientific Document Group. 2017 ESC/EACTS Guidelines for the
management of valvular heart disease. Eur Heart J. 2017;38(36):2739-91.
PubMed PMID: 28886619. Texto completo
• Nishimura RA, Otto CM, Bonow RO, Carabello BA, Erwin JP 3rd, Guyton
RA, et al. American College of Cardiology; American College of
Cardiology/American Heart Association; American Heart Association.
2014 AHA/ACC guideline for the management of patients with valvular
heart disease: a report of the American College of Cardiology/American
Heart Association Task Force on Practice Guidelines. J Thorac Cardiovasc
Surg. 2014 Jul;148(1):e1-e132. PubMed PMID: 24939033. Texto completo
Autores
José María Cubero
Médico Especialista en Cardiología (1)
Gómez
Mª Asunción Navarro
Médico Especialista en Medicina Interna (2)
Puerto
Rocío Gómez
Médico Especialista en Medicina Interna (2)
Herreros
Isabel Melguizo
Médico Especialista en Medicina Interna (2)
Moya
(1) UGC Cardiología. Hospital Universitario Virgen del Rocío. Sevilla.
(2) UGC Medicina Interna. Hospital Universitario de Valme. Sevilla.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Acerca de Suscríbase Destacados Ayuda Siga a Fisterra
Fisterra Instituciones Guías clínicas FAQ's
Metodología Prueba gratis Dietas Atención al cliente
Comité Boletines Medicamentos Salir
Términos y condiciones Política de privacidad
Elsevier España S.L.U. © 2023. Todos los derechos reservados. .
Este sitio utiliza cookies. Impostazioni cookie
También podría gustarte
- Urgencias médicas en el consultorio odontológico: Conocimientos básicos odontológicos, #2De EverandUrgencias médicas en el consultorio odontológico: Conocimientos básicos odontológicos, #2Calificación: 5 de 5 estrellas5/5 (1)
- Apuntes Insuficiencia Cardiaca 2019 PDFDocumento16 páginasApuntes Insuficiencia Cardiaca 2019 PDFGuillermo Castro ContardoAún no hay calificaciones
- Hipertensión en Adulto MayorDocumento31 páginasHipertensión en Adulto MayorvalentinoAún no hay calificaciones
- SICA - BiomarcadoresDocumento36 páginasSICA - BiomarcadoresJULIO CÉSAR FLORES TRUJILLOAún no hay calificaciones
- Resumen - Fisiologia CardiovascularDocumento28 páginasResumen - Fisiologia CardiovascularVicky Salazar100% (3)
- Iamcest IamsestDocumento68 páginasIamcest Iamsestmaria calderon quinteroAún no hay calificaciones
- Prolapso de La Válvula MitralDocumento1 páginaProlapso de La Válvula MitraltrofincrisAún no hay calificaciones
- Insuficiencia Arterial CronicaDocumento45 páginasInsuficiencia Arterial CronicaLoquisloroquis100% (1)
- ValvulopatíasDocumento63 páginasValvulopatíasKiara GuzmanAún no hay calificaciones
- Resumen Acad. Cardiología - Parte IiDocumento16 páginasResumen Acad. Cardiología - Parte IiHarold Aliaga BlancoAún no hay calificaciones
- Cardiopatías Congénitas (CC)Documento10 páginasCardiopatías Congénitas (CC)RosselyRamosAún no hay calificaciones
- Cardiopatias CongenitasDocumento48 páginasCardiopatias CongenitasVerónica Ñacato Pincay0% (1)
- 6º CN - Refuerzo - 3 PDFDocumento4 páginas6º CN - Refuerzo - 3 PDFAnonymous 0O7DJrntAAún no hay calificaciones
- Manual para la prevención de la enfermedad coronaria: Consejos para mejorar la calidad de vidaDe EverandManual para la prevención de la enfermedad coronaria: Consejos para mejorar la calidad de vidaAún no hay calificaciones
- Apunte Sindrome Coronario Agudo 2019 (Oficial)Documento12 páginasApunte Sindrome Coronario Agudo 2019 (Oficial)Jotam Muñoz M100% (1)
- Fisiopatología CardiovascularDocumento95 páginasFisiopatología Cardiovasculartrompito333Aún no hay calificaciones
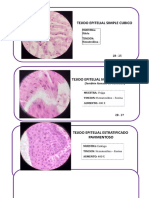
- TEJIDOSDocumento19 páginasTEJIDOSLaura Torres ArteagaAún no hay calificaciones
- ValvulopatíasDocumento25 páginasValvulopatíasKarla HernandezAún no hay calificaciones
- Medicina Interna Tomo 2Documento214 páginasMedicina Interna Tomo 2Lucas OrlandoAún no hay calificaciones
- Heart FailureDocumento70 páginasHeart FailureOscar ChavezAún no hay calificaciones
- Insuficiencia CardiacaDocumento13 páginasInsuficiencia Cardiacaalexandra rangelAún no hay calificaciones
- Insuficiencia Cardiaca Derecha e IzquierdDocumento23 páginasInsuficiencia Cardiaca Derecha e IzquierdJuan C. Sánchez-VicenteAún no hay calificaciones
- VALVULOPATIA AORTICA y PUMONAR 2023-IDocumento71 páginasVALVULOPATIA AORTICA y PUMONAR 2023-IBooksmedicsAún no hay calificaciones
- Manejo Actual ICADocumento15 páginasManejo Actual ICAsol valeria mejia garciaAún no hay calificaciones
- Insuficiencia Cardíaca Crónica: ResumenDocumento13 páginasInsuficiencia Cardíaca Crónica: ResumenMelanny Perez GonzalesAún no hay calificaciones
- VALVULOPATIAS FisiopatologiaDocumento57 páginasVALVULOPATIAS Fisiopatologiaapi-3699557100% (7)
- Cardiopatías Congénitas ClaseDocumento49 páginasCardiopatías Congénitas ClaseEdward AlfonsoAún no hay calificaciones
- 3 MI-ValvulopatíasDocumento106 páginas3 MI-ValvulopatíasJuan C BarrónAún no hay calificaciones
- Expo Lesiones ValvularesDocumento16 páginasExpo Lesiones ValvularesTennessee Ayala MendozaAún no hay calificaciones
- Valvulopatías SemDocumento50 páginasValvulopatías SemDaniela MoraAún no hay calificaciones
- 02.07. Shock CardiogenicoDocumento3 páginas02.07. Shock Cardiogenicofidelurtecho4881Aún no hay calificaciones
- Pae 1Documento18 páginasPae 1marichelitorres.48Aún no hay calificaciones
- Valvulopatias 180206032155Documento90 páginasValvulopatias 180206032155Daniela Reyes HardyAún no hay calificaciones
- PAE IMPRIMIR UTI MejoradoDocumento29 páginasPAE IMPRIMIR UTI MejoradoSara Daniela MamaniAún no hay calificaciones
- Insuficiencia Cardíaca: Docente: Natalia Rebolledo CordonesDocumento25 páginasInsuficiencia Cardíaca: Docente: Natalia Rebolledo Cordonesdaniksa152003Aún no hay calificaciones
- Fisiopatologia Estenosis AorticaDocumento15 páginasFisiopatologia Estenosis AorticaJaviera SolisAún no hay calificaciones
- Insuficiencia Cardíaca para Odontología Medicina EstomatologicaDocumento19 páginasInsuficiencia Cardíaca para Odontología Medicina EstomatologicaIsrael Pineda CastroAún no hay calificaciones
- Insuficiencia CardiacaDocumento14 páginasInsuficiencia CardiacaCARLOS MANUEL CAIRO CAMARENAAún no hay calificaciones
- Infarto Agudo de MiocardioDocumento7 páginasInfarto Agudo de MiocardioGisel MonzalvoAún no hay calificaciones
- Valvulopatias PMDocumento43 páginasValvulopatias PMalejandracorderoAún no hay calificaciones
- Medicina Interna 5toDocumento16 páginasMedicina Interna 5toAnabela GataniAún no hay calificaciones
- Corazón (Anatomia Patologica)Documento12 páginasCorazón (Anatomia Patologica)Gretel RochaAún no hay calificaciones
- 5ta Semana CardiologiaDocumento383 páginas5ta Semana Cardiologiadpb7122Aún no hay calificaciones
- PDFDocumento6 páginasPDFMontserrat ÁlvarezAún no hay calificaciones
- VALVULOPATÍASDocumento4 páginasVALVULOPATÍASClauMcClauAún no hay calificaciones
- Cardiomiopatia Hipertrofica y RestrictivaDocumento33 páginasCardiomiopatia Hipertrofica y RestrictivaLeddy Blas NavarroAún no hay calificaciones
- Cardiopatias Congeni 72218 Downloadable 762038Documento12 páginasCardiopatias Congeni 72218 Downloadable 762038BianAún no hay calificaciones
- Patología Del CorazónDocumento12 páginasPatología Del CorazónByron SolórzanoAún no hay calificaciones
- Cardiologia ClinicaDocumento76 páginasCardiologia Clinicaeddcito100% (1)
- Pato CardiólogoDocumento4 páginasPato CardiólogoJavier SernaAún no hay calificaciones
- MQ2 - Tema 1.2Documento4 páginasMQ2 - Tema 1.2Maria Escarabajal FernándezAún no hay calificaciones
- S35-05 30 - IiiDocumento11 páginasS35-05 30 - IiiLehcim InamamAún no hay calificaciones
- S35-05 30 - IiiDocumento11 páginasS35-05 30 - IiiMarisolCamposAún no hay calificaciones
- 1 Generalidades CardiologíaDocumento2 páginas1 Generalidades CardiologíaCARLOS FRANCISCO JAVIER PEREZ TORRESAún no hay calificaciones
- Temp ppt-198995019Documento97 páginasTemp ppt-198995019CarlosYovadSaldamandoCruzAún no hay calificaciones
- ValvulopatiasDocumento34 páginasValvulopatiasAzul 99Aún no hay calificaciones
- Insuficiencia Arterial CronicaDocumento45 páginasInsuficiencia Arterial CronicaAdriana LaraAún no hay calificaciones
- Seminario FisiopatologiaDocumento19 páginasSeminario FisiopatologiakeiverAún no hay calificaciones
- 18 - ANGINAS e IMADocumento10 páginas18 - ANGINAS e IMAvicentehueteme983Aún no hay calificaciones
- Expo de Insuficienccia Cardiaca.Documento15 páginasExpo de Insuficienccia Cardiaca.Guadalupe H.TAún no hay calificaciones
- Cardiopatias CongénitasDocumento17 páginasCardiopatias CongénitasVitor FloreAún no hay calificaciones
- Cardiologia 3° ParcialDocumento31 páginasCardiologia 3° ParcialjesicaAún no hay calificaciones
- Cardiopatias Congenicas AcianoticasDocumento66 páginasCardiopatias Congenicas AcianoticasJUDITH INGAAún no hay calificaciones
- VALVULOPATIA MITRAL y TRICUSPIDEA 2023-IDocumento88 páginasVALVULOPATIA MITRAL y TRICUSPIDEA 2023-IBooksmedicsAún no hay calificaciones
- Tema 2 SCADocumento44 páginasTema 2 SCAjernsssAún no hay calificaciones
- Insuficiencia CardiacaDocumento10 páginasInsuficiencia Cardiacajose chavez ramirezAún no hay calificaciones
- Guía Clínica de Medicación de Urgencia en Los Centros de Salud - FisterraDocumento1 páginaGuía Clínica de Medicación de Urgencia en Los Centros de Salud - FisterratrofincrisAún no hay calificaciones
- Nitroglicerina - FisterraDocumento1 páginaNitroglicerina - FisterratrofincrisAún no hay calificaciones
- Furosemida - FisterraDocumento1 páginaFurosemida - FisterratrofincrisAún no hay calificaciones
- Digoxina - FisterraDocumento1 páginaDigoxina - FisterratrofincrisAún no hay calificaciones
- Soporte Vital Básico Del Adulto - FisterraDocumento1 páginaSoporte Vital Básico Del Adulto - FisterratrofincrisAún no hay calificaciones
- Shock: Valoración y Manejo en Atención Primaria - FisterraDocumento2 páginasShock: Valoración y Manejo en Atención Primaria - FisterratrofincrisAún no hay calificaciones
- Soporte Vital Avanzado Del Adulto - FisterraDocumento1 páginaSoporte Vital Avanzado Del Adulto - FisterratrofincrisAún no hay calificaciones
- Manejo Específico de Las Taquiarritmias de QRS AnchoDocumento2 páginasManejo Específico de Las Taquiarritmias de QRS AnchotrofincrisAún no hay calificaciones
- Lupus Eritematoso SistémicoDocumento2 páginasLupus Eritematoso SistémicotrofincrisAún no hay calificaciones
- Enfermedad Por Depósito de Cristales de Pirofosfato CálcicoDocumento2 páginasEnfermedad Por Depósito de Cristales de Pirofosfato CálcicotrofincrisAún no hay calificaciones
- Monitorización Ambulatoria de La Presión Arterial (MAPA)Documento2 páginasMonitorización Ambulatoria de La Presión Arterial (MAPA)trofincrisAún no hay calificaciones
- Morfofisiología II Monografía #2: Universidad Norbert Wiener Facultad de Ciencias de La SaludDocumento20 páginasMorfofisiología II Monografía #2: Universidad Norbert Wiener Facultad de Ciencias de La SaludCielo Perez MendozaAún no hay calificaciones
- Principios Del Corazón y Modelo MatemáticoDocumento6 páginasPrincipios Del Corazón y Modelo MatemáticoDelta ShooterAún no hay calificaciones
- Dialnet AnginaInestable 8294238Documento13 páginasDialnet AnginaInestable 8294238jhoan castroAún no hay calificaciones
- Angina de PechoDocumento3 páginasAngina de PechoZulma NeyraAún no hay calificaciones
- Ciclo CardiacoDocumento50 páginasCiclo CardiacoClaudia Araujo GuitierresAún no hay calificaciones
- Fármacos HipertensivosDocumento1 páginaFármacos Hipertensivosedu.choqueAún no hay calificaciones
- Circulación Pulmonar y Relación Ventilación PerfusiónDocumento39 páginasCirculación Pulmonar y Relación Ventilación PerfusiónRicky G. Velesville0% (1)
- SD Coronario Diagnóstico y Tratamiento - Dr. Carlos LópezDocumento47 páginasSD Coronario Diagnóstico y Tratamiento - Dr. Carlos LópezJuan JaramilloAún no hay calificaciones
- Isquemia MesentericaDocumento11 páginasIsquemia MesentericaChuyin VcAún no hay calificaciones
- 1 CorsDocumento19 páginas1 Corskevin diazAún no hay calificaciones
- PREACONDICIONAMIENTODocumento34 páginasPREACONDICIONAMIENTOJIMENA BOTERO ARBELAEZAún no hay calificaciones
- Informe 26Documento5 páginasInforme 26Anbru GamesAún no hay calificaciones
- Hipertension Pulmonar CorregidoDocumento8 páginasHipertension Pulmonar CorregidoMonica BenavidesAún no hay calificaciones
- Sistema Circulatorio: Victor Raúl Cano FuentesDocumento22 páginasSistema Circulatorio: Victor Raúl Cano FuentesfranklinAún no hay calificaciones
- Vasos SanguineosDocumento16 páginasVasos SanguineosGuillermo LaraAún no hay calificaciones
- Sistema Circulatorio. SeminarioDocumento10 páginasSistema Circulatorio. SeminarioStefAún no hay calificaciones
- Tabaco y Enfermedad CardiovascularDocumento2 páginasTabaco y Enfermedad CardiovascularMaria HidalgoAún no hay calificaciones
- Banco de Preguntas AnatomiaDocumento8 páginasBanco de Preguntas AnatomiaDaniela GutierrezAún no hay calificaciones
- Estructura Del DienteDocumento9 páginasEstructura Del DienteDanna BurgosAún no hay calificaciones
- Anatomia Del CorazonDocumento8 páginasAnatomia Del CorazonArturoJimenezMeroAún no hay calificaciones
- Anatomía Del Corazón DiapositivasDocumento19 páginasAnatomía Del Corazón DiapositivasCitlaliAún no hay calificaciones
- Enfermedad Vascular Cerebral en Un Hospital de Tercer Nivel: Estudio DescriptivoDocumento6 páginasEnfermedad Vascular Cerebral en Un Hospital de Tercer Nivel: Estudio DescriptivoVictor Euclides Briones MoralesAún no hay calificaciones
- Emergencia HipertensivaDocumento6 páginasEmergencia HipertensivaRafael E. RodriguezAún no hay calificaciones
- Patología CardiovascularDocumento19 páginasPatología CardiovascularAngela Alvarado DelgadoAún no hay calificaciones
- Linfáticos EsplacnologíaDocumento5 páginasLinfáticos EsplacnologíaRamiro EspositoAún no hay calificaciones