Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Trastornos de Metales
Cargado por
Jordan Irán López GarcíaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Trastornos de Metales
Cargado por
Jordan Irán López GarcíaCopyright:
Formatos disponibles
ACTUALIZACIÓN
Trastornos del metabolismo del hierro
y del cobre. Hemocromatosis y enfermedad
de Wilson
J.M. Mesa Latorrea,b,*, J.D. García Díaza,b, D. Corps Fernándeza y A.R. Valbuena Parraa
a
Servicio de Medicina Interna. bUnidad de Genética Clínica y Lípidos. Hospital Universitario Príncipe de Asturias. Universidad de Alcalá. Alcalá de Henares. Madrid.
España.
Palabras Clave: Resumen
- Metabolismo del hierro Introducción. El hierro y el cobre son nutrientes esenciales para la síntesis de numerosas proteínas, in-
- Metabolismo del cobre terviniendo en diversas reacciones enzimáticas. Estas funciones derivan esencialmente de su capacidad
de participar en reacciones de reducción-oxidación intercambiando electrones. Sin embargo, esta mis-
- Hemocromatosis ma capacidad es responsable de que puedan generar radicales libres lesivos para la célula.
- Enfermedad de Wilson
Etiopatogenia. Tanto el déficit como el exceso de estos metales es causa de deterioro de las funciones
celulares y enfermedad, existiendo una serie de mecanismos fisiológicos que proporcionan un estrecho
control de la homeostasis de ambos elementos.
Manifestaciones clínicas. La hemocromatosis y la enfermedad de Wilson son trastornos del metabolis-
mo de estos metales, que ocasionan la acumulación de hierro y cobre, y la lesión de diversos órganos,
fundamentalmente del hígado. Ambas enfermedades tienen un origen genético, muestran un patrón au-
tosómico recesivo y un espectro fenotípico variable.
Diagnóstico. El conocimiento de su patogenia permite la correcta interpretación de las pruebas bioquí-
micas para su diagnóstico.
Tratamiento. La depleción de estos metales, en el primer caso mediante sangrías y en el segundo con el
uso de quelantes, previene la aparición de complicaciones orgánicas.
Keywords: Abstract
- Iron metabolism Disorders of iron and copper metabolism. Hemochromatosis and Wilson’s disease
- Copper metabolism Introduction. The iron and copper are essential nutrients for the synthesis of numerous proteins
- Hemochromatosis interfering in various enzymatic reactions. These functions derive essentially from their ability to
participate in redox reactions exchanging electrons. However, this same ability is responsible for that
- Wilson’s disease
generate harmful free radicals for the cell.
Etiopathogeny. Both the deficit and excess of these metals causes deterioration of cell functions and
disease, and there are a number of physiological mechanisms that provide tight control of the
homeostasis of both.
Clinical manifestations. Hemochromatosis and Wilson’s disease are disorders of the metabolism of
these metals, causing the accumulation of iron and copper, and the injury of various organs, primarily the
liver. Both diseases are genetic, show an autosomal recessive pattern and a variable phenotypic
spectrum.
Diagnosis. Understanding its pathogenesis allows the correct interpretation of biochemical tests for
diagnosis.
Treatment. Depletion of these metals, in the first case by the second indents and with the use of
chelators, prevents the development of organ complications.
*Correspondencia
Correo electrónico: jmesa@salud.madrid.org
1094 Medicine. 2016;12(19):1094-106
TRASTORNOS DEL METABOLISMO DEL HIERRO Y DEL COBRE. HEMOCROMATOSIS Y ENFERMEDAD DE WILSON
Trastornos del metabolismo del hierro. fundamental en la regulación de la concentración plasmática
de hierro5,6.
Hemocromatosis Una vez en el plasma el hierro se une a la transferrina
(Tf) para ser transportado a los diversos tejidos para su utili-
Metabolismo del hierro zación o almacenamiento. Para poder unirse a la Tf el Fe2+
debe ser oxidado a Fe3+ por la hefaestina, en la superficie
La cantidad total de hierro del organismo es el resultado del basolateral de las células intestinales, o por la ceruloplasmina
balance entre las pérdidas, producidas fundamentalmente a (Cp) presente en el plasma. La Tf se encuentra en el plasma
través de la descamación de células cutáneas e intestinales, el en tres formas: como proteína no ligada al Fe2+ (apotransfe-
sudor, las pequeñas pérdidas sanguíneas o la menstruación, y rrina) unida a un átomo de hierro, o como Tf diférrica (ho-
la absorción de aproximadamente un 10% de los 10-20 mg/ lotransferrina). La coexistencia en el plasma de estas tres
día que contiene la dieta normal. Los requerimientos diarios formas de la Tf permite una capacidad de amortiguación
de hierro son de aproximadamente 20 mg, de los que solo ante aumentos agudos de la absorción de hierro, evitando los
entre 1 y 2 mg proceden de la absorción intestinal, la mayo- efectos tóxicos del hierro no unido a la Tf (NTBI, non-trans-
ría restante procede del reciclado de los hematíes senescen- ferrin bound iron) sobre el organismo4.
tes por los macrófagos del sistema reticuloendotelial1. Aun- Para poder ser utilizado por las células, el Fe3+ unido a la
que el porcentaje de hierro procedente de la dieta es pequeño, Tf (TBI, transferrin bound iron) es captado por el receptor 1
su absorción está altamente controlada, porque no hay me- de la Tf, (TfR1, transferrin receptor 1). El complejo TBI-TfR1
canismos reguladores de su excreción y, en consecuencia, el es internalizado por la célula formando un endosoma, donde
aumento de la absorción intestinal conduce a la sobrecarga el Fe3+ es liberado de la Tf y transformado en Fe2+ por una
de hierro en el organismo2,3. reductasa de la membrana del endosoma, y liberado al cito-
La regulación del metabolismo del hierro implica funda- plasma por el DMT1; la Tf se devuelve a la circulación y el
mentalmente el control de su absorción, almacenamiento y TfR1 es reciclado volviendo a la membrana citoplasmática4.
reciclaje, en el que intervienen diversas proteínas y cuatro El hierro liberado de los endosomas es cedido a las organelas
grupos de células: enterocitos duodenales, precursores eri- donde será empleado en la síntesis de proteínas, principal-
troides, macrófagos y hepatocitos (fig. 1). mente de hemoglobina4.
El hierro está presente en la dieta en dos formas: hierro- El almacenamiento del hierro previene la existencia de
heme (10%) y hierro-no heme (90%) este último se encuentra hierro libre, y sirve como compartimento de rápida libera-
en forma férrica (Fe3+) difícilmente absorbible, una vez redu- ción en situaciones de déficit. La ferritina es la principal pro-
cido a forma ferrosa (Fe2+) por el pH gástrico, ácido ascórbico teína relacionada con el almacenamiento de hierro; es un
y la acción del citocromo b duodenal (reductasa expresada en heteropolímero de 24 subunidades con estructura de cápsula
el borde en cepillo duodenal) puede pasar al interior del ente- esférica formado por cadenas H (heavy) y L (light) codificadas
rocito a través del transportador de
metales divalentes-1 (DMT1, diva-
lent metal transporter-1). El hierro
heme es absorbido más fácilmente, Fe Hem 2+
probablemente por una proteína Fe 3+
Citicromo b
DMT-1
transportadora específica; ya en el
e 3+
aF
rrin
enterocito una oxigenasa libera
sfe
3+
n
2+
Enterocito
Tra
DMT
TfR
el Fe2+ ligado al heme4. Dentro del
Fe 3+
-1
1
2+
Fe
Transferrina
2+
enterocito el Fe puede ser almace- Ferritina
Hem
nado como ferritina, permanecien- Hipoxia
Anemia
do así hasta la descamación de la 3+ 3+
Fe Transferrina Fe
célula intestinal, o ser exportado al Precursor
FPN eritroide
plasma por una proteína transporta- Hefaestina
Fe Transferrina 3+
dora, la ferroportina (FPN). Esta STOP
Ceruloplasimina
ina
3+
Fe 2+ Fe Transferrina
sim
proteína es el único exportador ce-
pla
Hepcidina STOP
ulo
Cer
Aumento de Fe circulante
lular de hierro identificado, codifi- BMP 6 Fe 2+
Matriptasa-2
cada por el gen SLC40A1, se expre- Fe Transferrina Fe 3+
Fe Transferrina Fe 3+ 3+ 3+
FPN
DMT-1
sa en las células de la mucosa
TfR1
TfR2
HFE BMP-R
FPN
duodenal, macrófagos, hepatocitos HJV
Fe 2+
y células del sincitiotrofoblasto de la Hepatocito
o
fag
placenta. La FPN transfiere el hie-
cró
Aumento de Fe
IL 6 Ferritina
Ma
intracelular
rro procedente de la luz intestinal, o Aumento de la
Ferritina
de los lugares de almacenamiento síntesis de hepcidina
Inflamación
interno y reciclado (hepatocitos y IL 6-R
macrófagos del sistema reticuloen-
dotelial) al torrente sanguíneo; de
Fig. 1. Principales vías del metabolismo del hierro y su control sistémico. La explicación en el texto.
esta forma, la FPN tiene un papel
Medicine. 2016;12(19):1094-106 1095
ENFERMEDADES ENDOCRINOLÓGICAS Y METABÓLICAS (VII)
por genes distintos. La mayoría de la ferritina es intracelular,
los hepatocitos y los macrófagos contienen cantidades eleva-
Aumento de los
das de ferritina, siendo el hígado y el sistema reticuloendote- requerimientos
Aumento del hierro
lial los principales órganos de almacenamiento del hierro, circulante y en los eritopoyéticos de hierro
Inflamación
cantidades menores se encuentran en los precursores eritroi- depósitos
des, fibras miocárdicas y otras células. En las células el hierro
Hepcidina
se almacena en dos formas: en el citoplasma, como ferritina,
o en los lisosomas como hemosiderina. La hemosiderina re- Ferroportina Macrófagos
Enterocitos Ferroportina esplénicos
presenta una pequeña fracción de los depósitos normales del duodenales
organismo, localizada fundamentalmente en los macrófagos.
Ferroportina
Este hierro acumulado en los macrófagos no produce daño
Hepatocitos y
tisular oxidativo. La hemosiderina es un agregado de ferriti- células de Kupffer
na parcialmente degradada, junto con otros materiales7. Una
pequeña proporción de ferritina es secretada al plasma pro-
porcionando una herramienta diagnóstica, al reflejar la pro-
ducción total de ferritina y los depósitos de hierro del orga- Hierro plasmático
nismo.
La mayor parte del hierro circulante, superando en mu- Fig. 2. Papel de la hepcidina en la homeostasis del hierro. La hepcidina actúa
cho al procedente de la absorción intestinal, proviene del produciendo la internalización y degradación de la ferroportina y, en conse-
reciclado realizado en los macrófagos esplénicos y hepáticos cuencia, inhibiendo el paso del hierro desde los enterocitos, macrófagos y
hepatocitos a la sangre. Su síntesis se ve aumentada en respuesta a la so-
al destruir los hematíes senescentes, liberándose el hierro de brecarga de hierro y a la inflamación, y disminuida en respuesta a la eritro-
la hemoglobina para su almacenamiento o liberación al plas- poyesis ineficaz y aumentos de los requerimientos eritropoyéticos de hierro.
ma, como en los enterocitos, también a través de la FPN4,8.
El organismo dispone de diversos mecanismos para la ho-
meostasis del hierro, que afectan al control de su absorción, BMP 6. La interacción entre la BMP 6 y el receptor BMP
almacenamiento y reciclado (fig. 1). Esta homeostasis del hie- inicia la señalización, a través de la cadena de proteínas SMAD,
rro está regulada tanto a nivel sistémico como intracelular. aumentando la síntesis de hepcidina8,9. La HJV es una proteí-
El regulador más importante de la homeostasis del hierro na que actúa como cofactor esencial del receptor BMP, nece-
a nivel sistémico es la hepcidina, codificada por el gen HAMP. saria para el inicio de la señalización que ocasiona el aumento
La hepcidina se sintetiza en el hígado, como un propéptido de la expresión del gen HAMP.
biológicamente inactivo de 84 aminoácidos que es procesado Existen también reguladores negativos de la hepcidina, a
a la forma activa circulante con 25 aminoácidos. Actúa pro- través de la vía de señalización BMP-SMAD, como la ma-
duciendo la internalización y degradación de la FPN y, en triptasa-2, codificada por el gen TMPRSS6, que ejerce su
consecuencia, inhibiendo el paso del hierro desde los entero- función a través de la inhibición de la HJV5. Mutaciones
citos, macrófagos y hepatocitos a la sangre5. Su síntesis se ve bialélicas en el gen TMPRSS6 son responsables de la anemia
aumentada en respuesta a la sobrecarga de hierro y a la infla- ferropénica refractaria al hierro (IRIDA, iron-refractory iron-
mación, y disminuida en respuesta a las situaciones de defi- deficiency anemia) caracterizada por la presencia de anemia
ciencia de hierro, hipoxia o eritropoyesis ineficaz4 (fig. 2). ferropénica congénita, refractaria al hierro, debida a un estí-
Como otras hormonas, la hepcidina es regulada mediante mulo excesivo de la síntesis de hepcidina que se traduce en el
un mecanismo de retroalimentación por la sustancia cuya con- secuestro del hierro en los macrófagos y descenso de la ab-
centración controla, el hierro, que controla la expresión de la sorción del hierro de la dieta.
hepcidina por dos mecanismos: mediante los niveles de hierro Además de la elevación del hierro circulante y de sus de-
circulante, y a través de los depósitos hepáticos de hierro. La pósitos, las situaciones de inflamación aumentan los niveles
regulación de la hepcidina por el hierro circulante se produce de hepcidina, a través de señales mediadas por la interleucina
mediante la interacción del TBI con un complejo multiprotei- 6, disminuyendo la absorción intestinal y ocasionando el se-
co, situado en la membrana del hepatocito, formado por el cuestro de los depósitos de hierro, contribuyendo así a la
receptor de la cascada de señalización de la proteína morfogé- anemia asociada a los procesos crónicos. En situaciones de
nica del hueso (BMP, bone morphogenic protein), el correptor aumento de la eritropoyesis o hipoxia, disminuye la síntesis
hemojuvelina (HJV) y una serie de proteínas auxiliares que de hepcidina favoreciendo la absorción intestinal de hierro y
incluyen al TfR1, al receptor 2 de la Tf (TfR2, transferrin re- su liberación desde los lugares de almacenamiento8.
ceptor 2) y a la proteína HFE, que interactúa con ambos recep- La mayoría de los casos de sobrecarga de hierro son de-
tores de la Tf. Al aumentar la saturación de Tf se produce un bidos a la alteración de los mecanismos de sensado de los
desplazamiento de HFE desde TfR1 a TfR2 que estimularía niveles de hierro, o de la señalización eritropoyética, que
la producción de hepcidina a través de la interacción con el ocasionan una producción inadecuadamente baja de hepcidi-
complejo receptor-BMP/HJV, que desencadena la modifica- na, responsable del paso excesivo del hierro a la sangre desde
ción en proteínas que trasladan la señal al núcleo (proteínas enterocitos y macrófagos, y a que se exceda la capacidad de
SMAD) y activan la expresión del gen HAMP, que codifica la almacenamiento en las células; además, al saturarse la Tf au-
hepcidina2,4,5,8,9. Por otro lado, el aumento de los depósitos he- menta el NTBI que es captado por las células susceptibles
páticos de hierro ocasiona un aumento de la producción de la (incluidos hepatocitos, cardiomiocitos y células de los islotes
1096 Medicine. 2016;12(19):1094-106
TRASTORNOS DEL METABOLISMO DEL HIERRO Y DEL COBRE. HEMOCROMATOSIS Y ENFERMEDAD DE WILSON
pancreáticos) con el subsiguiente daño oxidativo10. TABLA 1
Clasificación de los síndromes de sobrecarga de hierro
Junto a la regulación sistémica de la homeostasis del hie-
rro proporcionada por la hepcidina, las células poseen meca- Hemocromatosis hereditarias
nismos propios para regular la expresión de los genes rela- Tipo I, o clásica, debida a mutaciones en el gen HFE
cionados con el metabolismo del hierro a través las proteínas Tipo II (hemocromatosis juvenil)
reguladoras del hierro (IRP, iron regulatory protein) y los ele- 2A, debida a mutaciones en el gen HJV
mentos respondedores al hierro (IRE, iron responsive element). 2B, por mutaciones en el gen HAMP
Los IRE son secuencias situadas en las regiones 3’UTR y Tipo III, por mutaciones en el gen TFR2
5’UTR de los ARNm maduros que codifican las proteínas Tipo IV, debida a mutaciones en el gen SLC40A1
responsables de la incorporación del hierro a la célula Mutaciones con pérdida de función (enfermedad de la ferroportina)
(DMT1 y TfR1) almacenamiento (unidades H y L de la fe- Mutaciones con ganancia de función (sobrecarga de hierro verdadera)
rritina) y exportación (FPN). Las IRP actúan como sensores Sobrecargas de hierro secundarias
del nivel de hierro intracelular, su acción sobre el ARNm Anemias con sobrecarga de hierro (con o sin transfusiones múltiples)
(estabilización o inhibición) depende del lugar de unión con Talasemia mayor y talasemia intermedia
el IRE, 3’UTR o 5’UTR4,6. Anemia sideroblástica
Anemias hemolíticas crónicas
Síndromes mielodisplásicos
Hemocromatosis. Síndromes de sobrecarga Enfermedades hepáticas crónicas
de hierro Hepatitis C y B
Hepatopatía alcohólica
A pesar de la existencia de mecanismos para mantener la ho- Esteatohepatitis no alcohólica
meostasis del hierro, numerosos factores, tanto genéticos Porfiria cutánea tarda
como ambientales, pueden alterar el equilibrio; en concreto Otras
la disregulación del eje hepcidina-FPN es responsable de si- Síndrome metabólico
tuaciones tanto de sobrecarga como de déficit de hierro. Sobrecargas de hierro parenterales
Los síndromes de sobrecarga de hierro son etiológicamente Aceruloplasminemia
heterogéneos y pueden tener un origen tanto hereditario Atransferrinemia/hipotransferrinemia
como adquirido. Actualmente se acepta reservar el término Deficiencia de DMT1
hemocromatosis para aquellas situaciones en las que la so- Hemocromatosis neonatal
Sobrecarga de hierro africana
brecarga de hierro, y su efecto tóxico sobre las células paren-
quimatosas de diversos órganos, está causada por mutaciones
en alguno de los genes que limitan la entrada de hierro a la
sangre disminuyendo los niveles o actividad de la hepcidina, co recesivo, es debida a mutaciones en el gen HFE (6p22.2).
en ausencia de unas necesidades eritropoyéticas aumenta- Hemocromatosis tipo 2 o juvenil, con patrón hereditario au-
das5,11. Esta reducción en la síntesis o actividad de la hepcidi- tosómico recesivo y subdividida en otras dos formas; 2A
na puede ser debida a mutaciones con pérdida de función en (OMIM 602390) causada por mutaciones en el gen HJV
el gen HAMP que la codifica, a mutaciones en el gen (1q21.1); y 2B (OMIM 613313) causada por mutaciones en
SLC40A1 que codifica la FPN y alteran la interacción entre el gen HAMP (19q13.12). Hemocromatosis tipo 3 (OMIM
esta y la hepcidina, o a mutaciones en genes que regulan la 604250) con herencia autosómica recesiva, es debida a muta-
síntesis de hepcidina, como HFE (responsable de más del ciones en el gen TFR2 (7q22.1). Hemocromatosis tipo 4
90% de los casos de hemocromatosis) TFR2 y HJV. El resto (OMIM 606069) con patrón autosómico dominante, causada
de situaciones de sobrecarga de hierro se recogen dentro de por mutaciones en el gen SLC40A1 (2q32.2). Hemocroma-
los llamados síndromes de sobrecarga secundaria de hierro, tosis tipo 5 (OMIM 615517) una sola familia comunicada
ya tengan estos un origen genético o adquirido. En la tabla 1 con patrón autosómico dominante, causada por mutaciones
se recoge la clasificación de las causas de sobrecarga de hierro. en el gen FTH1 (11q12.3) que codifica las cadenas H de la
Frecuentemente es difícil, o puede ser artificial, la sepa- ferritina.
ración entre causas genéticas o ambientales de la reducción La hemocromatosis asociada con HFE (HC-HFE), tam-
de los niveles de hepcidina, y de los síndromes de sobrecarga bién denominada clásica o tipo 1, es la forma más frecuente
de hierro; así, solo una minoría de los portadores homocigo- de la enfermedad. Debida a mutaciones homocigotas o hete-
tos de la mutación C282Y en el gen HFE desarrolla comple- rocigotas compuestas en el gen HFE, muestra un patrón he-
tamente la enfermedad, probablemente por la coexistencia reditario autosómico recesivo con penetrancia incompleta.
en ellos de otros factores genéticos o ambientales, habiéndo- Los síntomas relacionados con la sobrecarga de hierro apa-
se considerado la hemocromatosis-HFE como un trastorno recen entre los 40 y 60 años en hombres y más tardíamente,
multifactorial5,12. después de la menopausia, en las mujeres.
Aunque se han descrito numerosas mutaciones en el gen,
Clasificación y bases genéticas de la hemocromatosis la mayoría de los casos de HC-HFE debida a un cambio de
La base de datos Online Mendelian Inherance in Man (OMIM) base, guanina por adenina, en la posición 485 (c.485G>A)
describe 5 tipos de hemocromatosis: hemocromatosis tipo 1, que provoca la sustitución de una cisteína por tirosina en la
o clásica (OMIM 235200) con patrón hereditario autosómi- posición 282 en el producto del gen (p.Cys282Tyr, o C282Y).
Medicine. 2016;12(19):1094-106 1097
ENFERMEDADES ENDOCRINOLÓGICAS Y METABÓLICAS (VII)
Se trata de un polimorfismo altamente prevalente en pobla- Los depósitos de hierro en las células parenquimatosas tam-
ción con origen en el norte de Europa, la prevalencia de la bién están aumentados, pero en menor medida caracterizán-
mutación en homocigosis en caucásicos es de 1/200-300. dose el trastorno por una afectación visceral leve. A pesar de
Aproximadamente un 85-90% de los pacientes con fenotipo la elevación de la ferritina, los niveles de sideremia y satura-
típico de hemocromatosis son homocigotos para la mutación ción de Tf son normales y la realización de flebotomías con-
C282Y. Sin embargo, muchos de los portadores homocigo- duce a la anemia ferropénica con relativa rapidez. El marca-
tos C282Y no llegan a presentar manifestaciones clínicas; dor de la enfermedad, y llave para su diagnóstico, es la
solo un 38-50% desarrollan datos bioquímicos de sobrecarga sobrecarga férrica en el sistema retículo endotelial, que pue-
de hierro y un10-33% presentan morbilidad asociada, sugi- de ser puesta de manifiesto en la resonancia magnética, que
riendo una penetrancia incompleta y la posibilidad de que muestra típicamente acumulación del hierro en bazo y mé-
otros factores genéticos o ambientales actúen como modula- dula ósea5,11,14.
dores del fenotipo. El 3-5% de los pacientes con hemocro-
matosis son heterocigotos compuestos para las mutaciones Manifestaciones clínicas de la hemocromatosis
C282Y y H63D; esta última mutación es más frecuente que En la hemocromatosis el hierro se deposita inicialmente en
la C282Y, con una frecuencia del 10-20% en población des- las células parenquimatosas, ocurriendo la acumulación
cendiente de europeos y menor variación geográfica. La mu- en las células del sistema retículo endotelial de forma más
tación H63D muestra una menor penetrancia que la C282Y. tardía. El daño celular parenquimatoso es responsable de las
Los sujetos heterocigotos compuestos C282Y/H63D y los manifestaciones clásicas de la enfermedad: cirrosis, diabetes,
homocigotos H63D presentan parámetros bioquímicos del artropatía, hipogonadismo, miocardiopatía y pigmentación
metabolismo del hierro alterados e incluso, en ocasiones, au- cutánea.
mento de los depósitos de hierro hepático, pero en este caso Las manifestaciones hepáticas incluyen: alteración de las
habitualmente tienen otros factores asociados causantes de la transaminasas, hepatomegalia, fibrosis progresiva y cirrosis.
sobrecarga de hierro, como consumo de alcohol o hepatitis Numerosos estudios han demostrado el aumento del riesgo
víricas5,6,13. de sufrir hepatocarcinoma en pacientes con hemocromatosis,
Las hemocromatosis no relacionadas con HFE son raras su frecuencia aumenta con la edad, en varones, y se da casi
en comparación con la HC-HFE pero, al contrario que esta, exclusivamente en pacientes cirróticos.
no se restringen a población descendiente europea. La diabetes mellitus es debida al depósito del hierro en el
La forma de hemocromatosis caracterizada por un inicio páncreas, está presente en aproximadamente la mitad de los
temprano y fenotipo severo, clásicamente denominada hemo- pacientes con hemocromatosis sintomáticos.
cromatosis juvenil, es debida a mutaciones con pérdida de fun- El 25-50% de los pacientes sintomáticos padecen una ar-
ción del gen HAMP que codifica la hepcidina o, con más fre- tropatía similar a la condrocalcinosis después de los 50 años,
cuencia, a mutaciones en el gen HJV que codifica la aunque puede aparecer antes y ser la manifestación inicial;
hemojuvelina. El espectro etiológico de las hemocromatosis frecuentemente las primeras articulaciones afectas son la se-
juveniles se ha visto extendido por la identificación de pacien- gunda y tercera articulación metacarpofalángica.
tes con mutaciones combinadas en los genes HFE y TFR2 En la hemocromatosis es característico el depósito de
que presentan un síndrome similar a las formas juveniles12. hierro en las células de la adenohipófisis, evidenciable en la
La mayoría de los casos comunicados de hemocromatosis resonancia magnética, que puede conducir al hipogonadismo
no relacionada con HFE son debidos a mutaciones en el gen hipogonadotrófico; por el contrario el depósito en la neuro-
del TFR2, e incluyen familias de distintas etnias que mues- hipófisis es raro. Otros trastornos hipofisarios también pue-
tran un fenotipo similar a la HC-HFE o intermedio (entre den ocurrir, pero son mucho menos frecuentes, al igual que
las formas juveniles y la HC-HFE) respecto de la edad de el hipogonadismo primario.
inicio y severidad de las manifestaciones clínicas11,12,14. La hemocromatosis puede conducir a la miocardiopatía
Algunas mutaciones missense heterocigotas en el gen dilatada, insuficiencia cardiaca y aparición de trastornos del
SLC40A1, que codifica la FPN, dan lugar a la única forma de ritmo, como la enfermedad del nodo sinusal; la ausencia de
hemocromatosis con patrón hereditario autosómico domi- otros hallazgos clínicos característicos de la hemocromatosis
nante y manifestaciones clínicas similares a la HC-HFE. De- no debe hacer excluir esta posibilidad diagnóstica.
bido a mutaciones que producen una resistencia de la FPN a En los pacientes con enfermedad avanzada se observa hi-
su inhibición por la hepcidina (mutaciones con ganancia de perpigmentación cutánea (color gris metálico o pizarra) des-
función) facilitando el paso del hierro desde los enterocitos y crito clásicamente como «bronceado».
macrófagos a la sangre11,14. Sin embargo, la mayoría de las La tríada clásica de cirrosis, diabetes e hiperpigmenta-
mutaciones en el gen que codifica la FPN dan lugar a la lla- ción cutánea aparece de forma tardía en la evolución de la
mada enfermedad de la FPN, patológicamente distinta de la enfermedad. En la actualidad, los pacientes habitualmente
hemocromatosis14. son diagnosticados tras hallazgos bioquímicos casuales, o en
La enfermedad de la FPN es debida a mutaciones hete- el cribado de familiares de pacientes, de forma que una ma-
rocigotas en el gen SLC40A1 que causan la pérdida de fun- yoría se encuentran asintomáticos.
ción en la FPN, e impiden su papel como exportador de La hemocromatosis es un trastorno genéticamente hete-
hierro, fundamentalmente en los macrófagos del sistema re- rogéneo resultante de la interacción compleja entre factores
tículo endotelial; lo que ocasiona el secuestro del hierro en genéticos y ambientales. Su fenotipo es variable dependien-
estas células, reflejado por la elevación de la ferritina sérica. do de la magnitud y la velocidad con que se produce el de-
1098 Medicine. 2016;12(19):1094-106
TRASTORNOS DEL METABOLISMO DEL HIERRO Y DEL COBRE. HEMOCROMATOSIS Y ENFERMEDAD DE WILSON
pósito de hierro y estas varían dependiendo de la proteína tabolismo del hierro es necesario recordar que estos marca-
cuya función se ve alterada11. Si el gen alterado tiene un efec- dores pueden estar elevados en situaciones en las que no
to dominante en la síntesis o actividad de la hepcidina (como existe sobrecarga de este metal y que, en distintos síndromes
HAMP o HJV) la sobrecarga de hierro ocurre de forma rá- de sobrecarga, la saturación de Tf y la ferritina sérica pueden
pida, los factores ambientales no tienen un papel importante comportarse de forma diferente según el mecanismo subya-
y el desarrollo de la enfermedad es rápido y más dramático, cente.
con manifestaciones cardiacas y endocrinológicas en la se- La medición del hierro sérico no tiene valor en sí misma
gunda década, dando lugar a las llamadas formas juveniles. en el diagnóstico de sobrecarga de hierro, pero es necesaria
En contraste, los genes cuyas mutaciones causan una sobre- para medir la saturación de Tf. El índice, o porcentaje, de
carga más lenta, como HFE, TFR2 o SLC40A1 conducen a saturación de Tf (IST) es el cociente entre el hierro sérico y
un fenotipo más leve, que frecuentemente necesitan de la la capacidad total de transportar hierro del plasma (TIBC,
concurrencia de otros factores genéticos o ambientales para total iron binding capacity). Para considerar que existe un au-
producir enfermedad. Se han descrito también fenotipos in- mento del IST habitualmente se elige un punto de corte del
termedios en los que; por ejemplo, mutaciones homocigotas 45%, escogido por su alta sensibilidad para detectar homoci-
en HFE muestran un fenotipo más grave al combinarse con gotos C282Y, aunque muestra una menor especificidad, y
mutaciones heterocigotas en genes asociados a las formas ju- valor predictivo positivo, comparado con valores más altos;
veniles como HAMP; estas últimas mutaciones combinadas este valor permite además detectar sobrecargas secundarias
con mutaciones heterocigotas en HFE, habitualmente silen- leves y heterocigotos C282Y, que pueden precisar otras valo-
tes, pueden conducir a un fenotipo no esperado5,12. raciones posteriores15.
En las hemocromatosis debidas a mutaciones en los ge-
Valoración diagnóstica en pacientes con sospecha nes HFE, TFR2, HJV, HAMP y mutaciones con ganancia de
de hemocromatosis función en el gen de la FPN, el IST se eleva antes de produ-
El diagnóstico de hemocromatosis puede plantearse en di- cirse la elevación de los valores de ferritina. En la práctica se
versos escenarios clínicos como: pacientes con signos y sín- puede asumir que la presencia de un IST normal excluye el
tomas clínicos sugestivos de hemocromatosis; tras la detec- diagnóstico de hemocromatosis. El IST puede mostrarse
ción de valores elevados de ferritina y/o de la saturación de elevado en situaciones sin sobrecarga de hierro, como en las
Tf, en el diagnóstico diferencial de una sobrecarga de hierro; situaciones de citolisis (que aumentan la sideremia) o fallo
como parte de la valoración de pacientes que han recibido hepático (que disminuyen los niveles de Tf).
transfusiones múltiples, o con un trastorno conocido con La elevación de la ferritina sérica (300 Pg/l en varones o
predisposición a ocasionar sobrecarga de hierro y en el estu- más de 200 Pg/l en mujeres) es un hallazgo altamente sensi-
dio de familiares de pacientes con hemocromatosis. ble para la detección de sobrecarga de hierro, pero presenta
Los signos y síntomas iniciales de la hemocromatosis son falsos positivos dada su condición de reactante de fase aguda,
inespecíficos, por lo que es necesario considerar este diag- elevándose en situaciones de inflamación, enfermedades au-
nóstico al valorar pacientes con fatiga crónica, artralgias, im- toinmunes o neoplasias; en estas situaciones el IST general-
potencia, diabetes, miocardiopatía o hepatopatía. Los pa- mente es normal o bajo. En la población general la hemocro-
cientes con hemocromatosis sintomática inevitablemente matosis no es la causa más frecuente de elevación de la
tienen sobrecarga de hierro tisular, reflejada por un aumento ferritina. Se estima que aproximadamente en un 90% de los
de los niveles de ferritina sérica; por lo tanto, en pacientes de pacientes con hiperferritinemia se puede identificar alguna
cualquier raza con signos y/o síntomas sospechosos de he- de las siguientes causas: ingesta crónica de alcohol, inflama-
mocromatosis, el hallazgo de unos valores normales de ferri- ción, esteatosis hepática no alcohólica, síndrome metabólico,
tina excluye la hemocromatosis como causa responsable de necrosis celular o tumores13,15.
los síntomas11,13, mientras que la presencia de hiperferritine- En la hemocromatosis el aumento de los niveles de ferri-
mia debe llevar al estudio de sus posibles causas, incluida la tina se acompaña de aumento del IST. La presencia de eleva-
hemocromatosis. ción de los niveles de ferritina con IST normal, descartadas
Los procedimientos diagnósticos a realizar en pacientes situaciones de inflamación o neoplasias, en las que la eleva-
con sospecha de sobrecarga de hierro pueden ir dirigidos a: ción de la ferritina se debe a su carácter de reactante de fase
a) establecer el diagnóstico de sobrecarga de hierro; b) deter- aguda, obliga a excluir otras causas de hiperferritinemia
minar la gravedad y c) aclarar la causa o causas de la sobre- como el síndrome metabólico, el consumo excesivo de bebi-
carga, hemocromatosis o sobrecarga secundaria. das alcohólicas, las hepatitis víricas, la enfermedad de la
Los métodos empleados para establecer la presencia de FPN, el síndrome hereditario hiperferritinemia-cataratas o
sobrecarga de hierro incluyen la determinación de marcado- la aceruloplasminemia16.
res bioquímicos del metabolismo del hierro (sideremia, satu-
ración de Tf y ferritina sérica) biopsia hepática, técnicas de Biopsia hepática. La biopsia hepática y la determinación de
resonancia magnética y la valoración de la respuesta a las la concentración hepática de hierro (CHH) ha sido histórica-
flebotomías. mente la prueba de referencia para el diagnóstico de hemo-
cromatosis. Actualmente la presencia de la mutación C282Y
Marcadores bioquímicos del metabolismo del hierro. En en homocigosis, junto con la existencia de aumento de los
la aproximación en el diagnóstico de sobrecarga de hierro depósitos de hierro, con o sin síntomas, es suficiente para es-
mediante el estudio de los marcadores bioquímicos del me- tablecer el diagnóstico de HC-HFE13. La biopsia hepática
Medicine. 2016;12(19):1094-106 1099
ENFERMEDADES ENDOCRINOLÓGICAS Y METABÓLICAS (VII)
puede ser necesaria en el caso de la existencia de hiperferriti- Una vez diagnosticada la sobrecarga de hierro es nece-
nemia junto con otras enfermedades concomitantes que pue- sario establecer la gravedad del proceso y si existe daño de
dan ser factores de confusión, o como medida pronóstica para órganos; para ello se pueden emplear una combinación
establecer la presencia de fibrosis o cirrosis hepática. La exis- de pruebas de laboratorio junto con la RM y, en ciertas oca-
tencia de cirrosis ocasiona modificaciones en el seguimiento siones, la biopsia hepática. Valores del IST superiores a
de los pacientes, como la necesidad de realizar cribado de 70-75% suponen un mayor riesgo de la existencia de daño
hepatocarcinoma o varices esofágicas. Los niveles de ferritina en los órganos, por el aumento del NTIB. La sobrecarga de
sérica pueden ayudar a identificar pacientes que se puedan hierro se considera presente cuando los niveles de ferritina
beneficiar de la biopsia hepática, los pacientes homocigotos sérica son mayores de 300 ng/ml en varones o mayores de
C282Y con ferritina sérica superior a 1.000 Pg/l tienen una 200 ng/ml en mujeres; debe sospecharse la presencia de
prevalencia de cirrosis del 20-45%, por el contrario menos de daño hepático cuando los valores superan los 1.000 Pg/l.
2% de los homocigotos C282Y con ferritina sérica inferior a Los pacientes con CHH mayor de 15 mg/g muestran un
1.000 Pg/l tienen cirrosis en ausencia de otros factores de mayor riesgo de desarrollar complicaciones cardiacas y
riesgo como ingesta etílica excesiva o hepatitis víricas15. La muerte precoz.
posibilidad de utilizar técnicas no invasivas para medir la Un listado de las causas de sobrecarga de hierro se reco-
CHH, mediante la resonancia magnética, o para valorar la ge en la tabla 1. Muchas de estas causas serán sospechadas o
presencia de fibrosis, mediante la elastografía de transición, diagnosticadas tras la recogida de la historia clínica, explora-
ha disminuido la necesidad de realizar biopsias hepáticas en ción física y estudios de laboratorio iniciales. La hemocro-
pacientes estudiados por sospecha de hemocromatosis. matosis es la única condición desencadenante de sobrecarga
de hierro con una historia negativa y exploración, estudios
Resonancia magnética. La resonancia magnética (RM) hematológicos y hepáticos normales.
permite detectar la sobrecarga de hierro tanto en el hígado Dado el papel central de la hepcidina en la homeostasis
como en el miocardio. La RM hepática proporciona además del hierro, la medición de sus niveles probablemente será
información sobre el mecanismo fisiopatológico subyacente incorporada a los protocolos diagnósticos de los síndromes
a la sobrecarga de hierro al mostrar el balance entre la sobre- de sobrecarga de hierro.
carga hepática (células parenquimatosas) y esplénica (macró- El 85-90% de los pacientes con hemocromatosis son ho-
fagos). La existencia de sobrecarga hepática con nula o esca- mocigotos para la mutación C282Y en HFE, el estudio de
sa sobrecarga esplénica es el patrón típico de las sobrecargas los polimorfismos del gen (C282Y y H63D) permite el diag-
debidas a situaciones de deficiencia de hepcidina (hemocro- nóstico etiológico de la gran mayoría de los casos de hemo-
matosis y sobrecargas secundarias a diseritripoyesis), la pre- cromatosis. Otras mutaciones en el gen HFE o en genes
sencia de sobrecarga tanto hepática como esplénica es suges- responsables de hemocromatosis no-HFE son muy raras,
tiva de la existencia de sobrecarga de hierro transfusional; pudiéndose plantear su estudio si las exploraciones comple-
por otro lado, la presencia de un patrón de sobrecarga fun- mentarias soportan el diagnóstico de hemocromatosis sin
damentalmente esplénica con un hígado respetado es típica haberse logrado aclarar su causa. En esta unidad temática se
de la enfermedad de la FPN17. presenta un protocolo para el diagnóstico de pacientes con
Los valores T2* de la RM hepática muestran una buena hiperferritinemia y sobrecarga de hierro en el que se propo-
correlación con la CHH y con la ferritina sérica, además per- ne un escalonamiento de las pruebas diagnósticas.
mite detectar la existencia de lesiones neoplásicas. Habitual- Dada la alta frecuencia en la población de los polimorfir-
mente se prefiere la RM, frente a la biopsia hepática, en la mos del gen HFE, muchos pacientes con sobrecargas secun-
valoración de casos de sobrecarga de hierro con ferritina darias de hierro pueden tener factores genéticos que contri-
inferior a 1.000 Pg/l, si no hay sospecha de otras enfermeda- buyan a esta situación, en consecuencia, todos los pacientes
des hepáticas. La existencia de sobrecarga hepática supone con sobrecarga de hierro deben ser testados para los poli-
un factor de riesgo de sobrecarga cardiaca. Sin embargo, no morfismos del gen HFE.
existe un valor de sobrecarga hepática que determine si exis- De acuerdo con las recomendaciones de la European As-
te o no sobrecarga cardiaca, por lo que cada órgano necesi- sociation for the Study of the Liver se aconseja el estudio de los
taría ser evaluado de forma específica e independiente. La hermanos de los pacientes diagnosticados de HC-HFE, dado
RM cardiaca permite evaluar la sobrecarga cardiaca antes de el patrón hereditario autosómico recesivo de la enfermedad,
que se produzca disfunción sistólica18. mediante el genotipado del gen HFE y la determinación de
ferritina sérica e IST. Una vez testados, el seguimiento
Respuesta a las flebotomías. En pacientes no anémicos de estos familiares dependerá del resultado de los estudios,
puede emplearse la respuesta a las flebotomías para confir- edad y existencia de otras enfermedades. Frecuentemente los
mar la sobrecarga de hierro. Los depósitos normales de hie- pacientes con HC-HFE solicitan valoración sobre el riesgo
rro son aproximadamente 10 mg/kg de peso, cada flebotomía de sufrir la enfermedad de sus hijos, frecuentemente meno-
de 500 ml remueve de 200 a 250 mg de hierro. Los indivi- res de edad para otorgar el consentimiento para la realiza-
duos con depósitos normales alcanzarán una situación de ción de estudios genéticos; en esta situación, dado que la
ferropenia caracterizada por un descenso de la hemoglobina HC-HFE presenta una penetrancia reducida con manifesta-
menor de 12 g/dl y volumen corpuscular medio menor de 80 ciones clínicas durante la edad adulta, el genotipado del cón-
fl, después de 3 o 4 flebotomías realizadas en un plazo de 4 a yuge puede ser de ayuda para establecer el riesgo y la nece-
8 semanas. sidad de realizar estudios posteriormente13.
1100 Medicine. 2016;12(19):1094-106
TRASTORNOS DEL METABOLISMO DEL HIERRO Y DEL COBRE. HEMOCROMATOSIS Y ENFERMEDAD DE WILSON
Tratamiento intestino delgado. La entrada del cobre al enterocito se rea-
Las flebotomías son el pilar básico del tratamiento en pa- liza a través del transportador CTR1 (copper transporter 1)
cientes con hemocromatosis debidas a un descenso de los este proceso es facilitado por la acción de reductasas de la
niveles de hepcidina (tipos 1, 2, 3 y 4B) con evidencia de membrana apical del enterocito21,22. En el citoplasma del en-
sobrecarga de hierro, con o sin síntomas. Los pacientes con terocito el cobre se une a pequeñas proteínas, para proteger
hemocromatosis tratados con flebotomías, antes de haber a la célula, o a chaperonas que lo conducen hasta su unión a
desarrollado cirrosis o diabetes, tienen una supervivencia distintas enzimas. La chaperona ATOX1 cede el cobre a la
equivalente a la población general. ATP7A, un transportador de la clase ATPasa de tipo P, para
El tratamiento con flebotomías puede mejorar la fatiga, su incorporación al aparato de Golgi y participación en la
la hiperpigmentación, la elevación de las transaminasas e in- síntesis de proteínas. Al aumentar los niveles de cobre en
cluso de la fibrosis hepática; en pacientes cirróticos se ha la célula, la ATP7A cambia su localización a la membrana
informado de la mejoría de las varices esofágicas, incluida su basolateral del enterocito, para facilitar la secreción al siste-
resolución. En los pacientes diabéticos puede lograrse una ma venoso portal (fig. 3). La ATP7A se expresa de forma
reducción de las necesidades de insulina. La mejoría de las ubicua, las mutaciones en el gen ATP7A (Xq21.1) que la co-
manifestaciones cardiológicas es variable dependiendo del difica, causantes de la pérdida de la función ATPasa, son res-
grado del daño tisular al iniciar el tratamiento. ponsables de la enfermedad de Menkes (OMIM 309400)
Las flebotomías deben iniciarse al alcanzar niveles de fe- cuyas manifestaciones son explicadas por el déficit de incor-
rritina superiores a los normales y en la práctica se acepta poración del cobre intestinal al sistema circulatorio y el défi-
como objetivo el obtener valores de ferritina inferiores a cit de la incorporación del cobre al aparato de Golgi, de las
50 ng/ml. Una vez alcanzado este objetivo, las flebotomías células periféricas, para la síntesis de proteínas dependientes
cada 3-6 meses permiten mantener valores de ferritina de del cobre21.
50-100 ng/ml13. Unido a la albúmina, a la D2-macroglobulina y al ami-
No hay estudios que prueben que las medidas dietéticas noácido histidina, el cobre circula en el sistema venoso portal
tengan beneficios adicionales a los obtenidos con el trata- alcanzando el hígado, donde el transportador de membrana
miento habitual. El tratamiento con inhibidores de la bomba CTR1 permite su paso al interior del hepatocito. En el inte-
de protones (IBP) se ha comunicado que reduce la absorción rior de la célula el cobre puede ser almacenado, unido a las
de Fe y los requerimientos de sangrías13. metalotioneínas (proteínas ricas en cisteína de bajo peso mo-
El tratamiento con quelantes se emplea en pacientes con lecular), o ser fijado por una serie de chaperonas encargadas
intolerancia a las flebotomías y, fundamentalmente, en los de su distribución para la incorporación a enzimas como la
síndromes de sobrecarga de hierro secundarios ocurridos en superóxido dismutasa o la citocromo C-oxidasa. En el hepa-
el contexto de anemias crónicas. Existen actualmente tres tocito la chaperona ATOX1 cede el cobre a la ATP7B, otro
compuestos disponibles: desferrioxamina, que necesita ser transportador ATPasa de tipo P, que la transfiere al aparato
empleado parenteralmente y muestra una vida media corta; de Golgi para ser incorporado a la Cp y su posterior libera-
deferiprona, empleado por vía oral y con eliminación esen- ción al plasma. Cuando se elevan los niveles de cobre intra-
cialmente urinaria y deferasirox con una vida media larga y celular, la ATP7B es transferida desde el aparato de Golgi a
eliminación fundamentalmente biliar. los lisosomas posibilitando su transporte a la luz lisosomal y
la eliminación del exceso de cobre a la bilis vía exocito-
sis21,23-25 (fig. 3). Las mutaciones del gen ATP7B (13q14.3)
Trastornos del metabolismo del cobre. producen un defecto de la excreción de cobre (hacia al plas-
Enfermedad de Wilson ma unido a la Cp, y hacia la vía biliar para su eliminación)
conduciendo a su anormal acumulación en los tejidos, dando
lugar a la enfermedad de Wilson (EW) (OMIM 277900). El
Metabolismo del cobre cobre excretado hacia la bilis es unido a las sales biliares, que
lo inmovilizan previniendo su reabsorción.
El cobre es un elemento esencial en reacciones enzimáticas La Cp es una D2-glicoproteína que transporta el 95% del
importantes, en la biosíntesis de neurotransmisores y en la cobre existente en el plasma. Sintetizada en el hígado, duran-
formación del tejido conjuntivo. Su deficiencia o exceso tie- te su biosíntesis incorpora 6 átomos de cobre, dando lugar a
ne consecuencias patológicas en diversos órganos, especial- la holoceruloplasmina. Su principal función es la de ferroxi-
mente en cerebro e hígado. dasa, facilitando el paso de Fe2+ a Fe3+ para su incorporación
La cantidad de cobre ingerido y absorbido diariamente a la Tf. La disminución de los niveles de cobre intracelular
excede a las necesidades metabólicas del organismo, el equi- no afecta a la cantidad de apoceruloplasmina (Cp no unida al
librio en el balance de este elemento es mantenido por la cobre) sintetizada o excretada, pero el fallo de la incorpora-
secreción biliar, que es el mecanismo fundamental por el co- ción del cobre durante su biosíntesis da como resultado la
bre que es eliminado del organismo. En condiciones fisioló- secreción de una apoceruloplasmina carente de actividad fe-
gicas la cantidad de cobre eliminada por la orina es despre- rroxidasa que se degrada rápidamente26.
ciable19-21. La mayoría del cobre liberado desde el hepatocito a la
El cobre de la dieta es absorbido principalmente en el sangre lo hace unido a la holoceruloplasmina; sin embargo,
duodeno, aunque se considera que parte de la absorción pue- la función de la Cp como proteína transportadora de cobre
de tener lugar también en el estómago y regiones distales del es discutida. Aunque la mayoría del cobre circulante en san-
Medicine. 2016;12(19):1094-106 1101
ENFERMEDADES ENDOCRINOLÓGICAS Y METABÓLICAS (VII)
Cobre Cobre
Aporte de cobre Circulación
con la dieta portal
Enterocito Hepatocito
CTR1 CTR1
COX COX
ATOX1
SOD
MT ATOX1 SOD
Aparato de
Golgi MT CP
ATOX1 CP
ATP
7A
AT
OX1
AT Aparato de
Núcleo P7B Golgi Circulación
sanguínea
ATO
X1
ATP
Eliminación
7B
biliar de cobre Núcleo
ATOX1
ATP
7A
Fig. 3. Esquema general del metabolismo del cobre. El cobre de la dieta es incorporado a los enterocitos a través del transportador CTR1, para proteger a la célula, en
el citoplasma el cobre se une a pequeñas proteínas ricas en cisteína de bajo peso molecular, metalotioneínas (MT) o es fijado por una serie de chaperonas encarga-
das de su distribución para la incorporación a enzimas como la superóxido dismutasa (SOD) o a la citocromo C-oxidasa (COX). En el enterocito la chaperona ATOX1
cede el cobre a la ATP7A para su incorporación al aparato de Golgi y participación en la síntesis de diversas proteínas. Al aumentar los niveles de cobre en la célula,
la ATP7A cambia su localización a la membrana basolateral, para facilitar la secreción al sistema venoso portal. Tras alcanzar el hígado, el transportador CTR1 per-
mite su paso al interior de la célula. En el hepatocito la chaperona ATOX1 cede el cobre a la ATP7B que la transfiere al aparato de Golgi para ser incorporado a la
ceruloplasmina (Cp) y otras proteínas, para su posterior liberación al plasma. Cuando se elevan los niveles de cobre intracelular, la ATP7B es transferida a los lisoso-
mas posibilitando su transporte a la luz lisosomal y eliminación del exceso de cobre a la bilis vía exocitosis.
gre lo hace unido a esta proteína, en la aceruloplasminemia ferencia del cobre a la Cp, para su liberación a la sangre, y de
(resultante de mutaciones en el gen que codifica la Cp) se su excreción hacia la vía biliar. Como consecuencia se produ-
produce una sobrecarga de hierro en distintos órganos, como ce una acumulación de cobre en el hígado, desde el que es
consecuencia de la pérdida de la actividad ferroxidasa, pero liberado a la sangre, este cobre libre es responsable de las
el metabolismo del cobre aparentemente no se encuentra in- manifestaciones extrahepáticas de la enfermedad, particular-
fluenciado26. Por otro lado, en la EW hay una disminución mente de las neurológicas. La enfermedad tiene una inciden-
de los niveles de Cp circulante, pero no se observan signos cia de 1/30.000-100.000 estimándose una frecuencia de por-
de sobrecarga de hierro; probablemente por el manteni- tadores de 1/9028.
miento de una producción de holoceruloplasmina, en lugares
extrahepáticos, suficiente para mantener la actividad ferroxi- Manifestaciones clínicas
dasa20,26. El espectro de las manifestaciones clínicas de la EW es am-
Al igual que la síntesis, la degradación de la holocerulo- plio, en términos generales los pacientes pueden presentarse:
plasmina se produce fundamentalmente en el hígado, reci- a) con un cuadro agudo de insuficiencia hepática, hemolisis
clándose el cobre liberado21,27. o ambas y b) con un cuadro de instauración más crónica con
El cobre liberado desde el hepatocito al plasma, y no uni- manifestaciones neurológicas, hepáticas, o ambas. Los pa-
do a la holoceruloplasmina, circula unido a la D2-macroglo- cientes que presentan sintomatología neurológica o psiquiá-
bulina, albúmina, pequeños péptidos y aminoácidos, forman- trica como primera manifestación de la enfermedad tienden
do probablemente un sistema tampón, que protege el a ser mayores que aquellos solo con manifestaciones hepáti-
organismo de los efectos tóxicos del cobre libre, y asegura la cas. La mayoría de los pacientes con afectación del sistema
disponibilidad constituyendo la fracción intercambiable con nervioso tienen ya enfermedad hepática, aunque no hayan
las células de los distintos tejidos22,28. mostrado síntomas de esta28.
En los pacientes con EW la acumulación de cobre se ini-
cia al nacimiento, y continúa gradualmente durante toda la
Enfermedad de Wilson (OMIM 277900) vida, dando lugar al desarrollo de la enfermedad. La mayoría
de los pacientes con EW son diagnosticados entre los 5 y 35
Es un trastorno de origen genético del metabolismo del co- años. La variabilidad en la edad de presentación de la EW
bre, con patrón hereditario autosómico recesivo, debido a probablemente refleja diferencias en la penetrancia de las
mutaciones en las dos copias del gen ATP7B, que se expresa distintas mutaciones y la existencia de cofactores genéticos y
en el hígado y que codifica la ATPasa responsable de la trans- ambientales.
1102 Medicine. 2016;12(19):1094-106
TRASTORNOS DEL METABOLISMO DEL HIERRO Y DEL COBRE. HEMOCROMATOSIS Y ENFERMEDAD DE WILSON
necesario para confirmar los casos dudosos. Lesiones indis-
tinguibles del anillo de K-F pueden verse en otras enferme-
dades hepáticas crónicas especialmente en colestasis prolon-
gadas o cirrosis criptogenéticas. Las cataratas en girasol se
producen por depósito del cobre en el cristalino, habitual-
mente son visibles solo con la lámpara de hendidura28,29.
Otras manifestaciones de la EW, menos frecuentes, in-
cluyen: anomalías renales como aminoaciduria, hipercalciu-
ria o nefrocalcinosis; miocardiopatía y arritmias; osteoporo-
sis, fracturas espontáneas, condrocalcinosis y osteoartritis.
Diagnóstico
El diagnóstico de EW debe considerarse en cualquier pa-
ciente con anomalías hepáticas, neurológicas o psiquiátricas
inexplicadas. En pacientes con manifestaciones clínicas su-
gestivas de EW la realización de hemograma completo, bio-
química hepática, niveles de Cp, cobre en plasma, examen
con lámpara de hendidura y determinación de excreción de
cobre en orina de 24 horas, puede ser suficiente para estable-
cer el diagnóstico, o excluirlo; en pacientes con resultados
indeterminados serán necesarias otras pruebas como el estu-
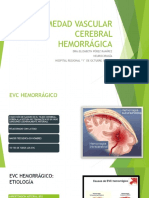
Fig. 4. Anillo corneal de Kayser-Fleischer en la enfermedad de Wilson. dio molecular del gen ATP7B o la biopsia hepática.
Aproximadamente el 95% de los pacientes con EW
muestran niveles bajos de Cp sérica (menos de 200 mg/l). La
Las manifestaciones hepáticas de la EW suelen ser la for- presencia de anillos de K-F y el descenso de los valores de
ma de presentación de la enfermedad en niños y adultos jó- Cp se considera diagnóstica de EW. Sin embargo, niveles
venes. La afectación hepática puede manifestarse como ele- bajos de Cp pueden verse también en pacientes sin EW,
vación asintomática de transaminasas y esteatosis, episodios como en enfermos con síndromes malabsortivos, pérdidas de
de hepatitis aguda autolimitados, insuficiencia hepática agu- proteínas renales o entéricas, insuficiencia hepática, acerulo-
da grave (con anemia hemolítica Coombs negativa) hepatitis plasminemia, enfermedad de Menkes, situaciones de déficit
crónicas o cirrosis. Aproximadamente el 5% de los pacientes adquirido de cobre, o en el 10-20% de los portadores hete-
se presentan con un fallo hepático fulminante. La liberación rocigotos de EW. Por otro lado, la Cp es un reactante de fase
del cobre a la sangre, tras los episodios de hepatonecrosis, es aguda y puede elevarse en situaciones de inflamación, ade-
responsable de la anemia hemolítica28,29. más de en estados de hiperestrogenismo como el embarazo
Las manifestaciones neurológicas y neuropsiquiátricas de o tratamientos con estrógenos. Los niveles de Cp aparecen
la EW son el síntoma de presentación en EL 40-50% de los típicamente descendidos en pacientes con afectación neuro-
pacientes. Pueden ser categorizadas como: lógica por la EW, pero hasta el 50% de los pacientes con
1. Síndrome rígido-acinético, similar a la enfermedad de enfermedad hepática activa presentan Cp en valores dentro
Parkinson. del rango normal, probablemente por la presencia de necro-
2. Cuadro de pseudoesclerosis, dominado por el temblor. sis hepática. Además hay que recordar que los valores norma-
3. Ataxia. les de Cp varían con la edad, siendo especialmente bajos en
4. Síndrome distónico. los primeros seis meses de vida19,28,30.
Cambios neuropsiquiátricos sutiles pueden preceder a las La concentración sérica de cobre se encuentra disminuida
manifestaciones neurológicas, como cambios en el compor- de forma proporcional a la reducción de la Cp sérica, a
tamiento, trastornos del aprendizaje o incapacidad para rea- pesar de la existencia de sobrecarga de cobre. La medición del
lizar actividades que requieren una buena coordinación ojo- cobre sérico incluye tanto el cobre unido, como el no unido a Cp.
mano. Junto con estos desórdenes también pueden aparecer La determinación de los niveles de cobre no unido a la Cp se
trastornos psiquiátricos como depresión o psicosis franca. ha propuesto como una prueba diagnóstica en la EW. Aunque el
Las manifestaciones oftalmológicas incluyen el anillo de cobre no unido a Cp puede medirse directamente mediante
Kayser-Fleischer (K-F) y las cataratas en girasol. Ambos ha- absorción atómica, habitualmente se determina de forma indi-
llazgos son reversibles con el tratamiento y su reaparición recta empleando la ecuación: cobre no unido a Cp Pg/l = co-
debe hacer sospechar el incumplimiento terapéutico. El ani- bre sérico Pg/l – (3,15 x Cp sérica mg/l). En los pacientes con
llo de K-F (fig. 4) puede observarse en una mayoría de pa- EW, los valores de cobre no unido a Cp típicamente son
cientes con manifestaciones neurológicas y en la mitad de los superiores a 200-250 Pg/l (valores normales inferiores a
pacientes con manifestaciones hepáticas. Está causado por el 150 Pg/l). Los valores de cobre no unido a CP se encuentran
depósito de cobre en la membrana de Descemet, en la super- elevados en situaciones de fallo hepático de cualquier etiolo-
ficie interior de la córnea, tienen coloración dorado-verdoso gía, en colestasis crónicas y casos de intoxicación por cobre.
y afectan primero al polo superior; aunque pueden ser obser- Esta determinación puede ser de más valor en la monitoriza-
vados a simple vista, el examen con lámpara de hendidura es ción del tratamiento que en el diagnóstico de EW19,30..
Medicine. 2016;12(19):1094-106 1103
ENFERMEDADES ENDOCRINOLÓGICAS Y METABÓLICAS (VII)
La excreción urinaria de cobre, en la orina de 24 horas, descartar el diagnóstico de la enfermedad, fundamentalmen-
puede ser de ayuda en el diagnóstico de la EW y para moni- te por la existencia de más de 500 mutaciones descritas y la
torizar su tratamiento. Refleja la cantidad de cobre en plasma dificultad de realizar los estudios. Con la incorporación de
no unido a Cp. El valor tomado convencionalmente para las técnicas de secuenciación masiva y la creciente disponibi-
realizar el diagnóstico de EW en pacientes sintomáticos es lidad de los estudios moleculares, es de esperar un nuevo
superior a 100 Pg/24 horas, aunque valores menores se han posicionamiento de estos en los protocolos diagnósticos de
descrito en pacientes asintomáticos con enfermedad confir- la EW, evitando la realización de pruebas invasivas. Además
mada; valores superiores a 40 Pg/24 horas se consideran su- permiten, en caso de ser diagnósticos, la realización del ade-
gestivos de EW y deben implicar estudios adicionales. En cuado cribado familiar, dado que los individuos afectados
caso de insuficiencia renal, el test no es aplicable. Para la presintomáticos suelen presentar valores descendidos de Cp,
interpretación de los resultados es fundamental asegurar y leves aumentos basales de la excreción urinaria de cobre,
la correcta recogida de la orina de 24 horas y su procesamien- que no permiten diferenciarlos de los portadores heterocigo-
to; para asegurar una correcta recogida debe medirse simul- tos. No se ha descrito la EW en portadores heterocigotos,
táneamente la excreción urinaria de creatinina (valores nor- aunque esta posibilidad no se ha excluido adecuadamente a
males de 15-20 mg/kg de peso). La excreción urinaria de edades avanzadas. Los estudios moleculares informativos po-
cobre puede estar también elevada en pacientes con otros ti- sibilitan la realización del diagnóstico prenatal o preinplan-
pos de enfermedades hepáticas crónicas y, especialmente, en tacional.
el fallo hepático agudo de cualquier origen; además de en En el 8th International Meeting on Wilson disease and Menkes
portadores heterocigotos, aunque estos habitualmente mues- disease celebrado en Leipzig en 2001 se propuso un sistema de
tran valores inferiores a 100 Pg/24 horas. La excreción urina- puntuación para establecer el diagnóstico de EW31. Este siste-
ria de cobre tras la administración de D-penicilamina puede ma ha sido incorporado a las guías para el diagnóstico y trata-
emplearse como una prueba diagnóstica complementaria. miento de la EW de la European Association for the Study of the
Esta prueba ha sido estandarizada solo en población pediátri- Liver19. El sistema de puntuación asigna valores numéricos
ca; se administran 500 mg de D-penicilamina por vía oral para una serie de hallazgos clínicos (presencia de anillos de
(independientemente del peso) al inicio de la prueba y 12 ho- K-F, síntomas neurológicos o anemia hemolítica), pruebas
ras más tarde. Comparado con otras enfermedades hepáticas bioquímicas (Cp sérica, cobre hepático y cobre en orina) y
se puede establecer una diferenciación, una eliminación ma- estudio de mutaciones en el gen ATP7B. Una puntuación total
yor de 1.600 Pg/24 horas es sugestiva de EW; sin embargo, el igual o superior a 4 establece el diagnóstico, una puntuación
estudio tras D-penicilamina es de poca ayuda cuando la ex- de 3 cataloga el diagnóstico como posible, siendo necesarias
creción de cobre en 24 horas es menor de 40 Pg/24 horas. El pruebas adicionales, y una puntuación igual o menor a 2 hace
estudio tras D-penicilamina es de utilidad para confirmar el el diagnóstico improbable (tabla 2).
diagnóstico en pacientes pediátricos con EW y enfermedad
hepática activa; en los adultos y portadores heterocigotos el Tratamiento
valor predictivo de la prueba es desconocido19,28,30. En el tratamiento de la EW pueden considerarse dos fases:
La biopsia hepática permite la cuantificación de la con- la eliminación de la sobrecarga de cobre, y la prevención
centración de cobre hepático y el estudio de los cambios his- de la reacumulación. Todos los pacientes presintomáticos de-
tológicos. ben recibir tratamiento profiláctico, puesto que la enferme-
La cuantificación de la concentración hepática de cobre dad tiene una penetrancia prácticamente del 100%.
se ha considerado clásicamente como la prueba de referencia Para la eliminación de la sobrecarga de cobre se emplean
para el diagnóstico de la EW. Los pacientes presentan habi- quelantes (D-penicilamina, trientina o tetratiomolibdato
tualmente más de 250 Pg (más de 4 Pmol)/g de peso seco, amónico). En la prevención de la reacumulación pueden em-
este punto de corte tiene una sensibilidad y especificidad de plearse sales de zinc o quelantes (estos empleados en dosis
83,3 y 98,6% respectivamente; reduciendo el punto de corte menores a las usadas durante la fase inicial), además de man-
a 75 Pg (1,2 Pmol)/g de peso seco se aumenta la sensibilidad tener una dieta baja en cobre. El tratamiento debe mantener-
con un pequeño descenso de la especificidad (96,5 y 95,4%, se durante toda la vida, incluso durante el embarazo. Es ne-
respectivamente)19. Se han comunicado casos de pacientes cesaria la monitorización del tratamiento para detectar la
con EW y concentraciones de cobre hepáticas normales en falta de adherencia o fallos terapéuticos.
la biopsia hepática, probablemente por la irregular distribu- La D-penicilamina actúa aumentando la eliminación uri-
ción del cobre en pacientes con cirrosis hepática20,31. Los ha- naria de cobre y puede también inducir la producción de
llazgos histológicos en pacientes con EW son similares a metalotioneínas. Numerosos estudios han demostrado la efi-
aquellos con esteatohepatitis no alcohólica y hepatitis au- cacia de la D-penicilamina en el tratamiento de la EW; en
toinmune. Con fines diagnósticos, la biopsia hepática solo es pacientes con enfermedad hepática avanzada puede obser-
necesaria cuando los hallazgos clínicos y el resultado de las varse una mejoría en 2 a 6 meses, incluso pacientes con cirro-
pruebas no invasivas no permiten establecer un diagnóstico sis o fibrosis avanzadas pueden experimentar mejoría. En
final, o si hay sospecha de otras patologías hepáticas adicio- pacientes con manifestaciones neurológicas la mejoría es más
nales. lenta y se ha comunicado el empeoramiento de la sintomato-
El estudio molecular del gen ATP7B tradicionalmente ha logía en un 10-50% de los pacientes en la fase inicial; este
sido recomendado para el diagnóstico en pacientes en los deterioro neurológico se ha comunicado también en pacien-
que los estudios anteriores no habían permitido establecer o tes tratados con trientina o zinc, pero fundamentalmente con
1104 Medicine. 2016;12(19):1094-106
TRASTORNOS DEL METABOLISMO DEL HIERRO Y DEL COBRE. HEMOCROMATOSIS Y ENFERMEDAD DE WILSON
TABLA 2 La administración de zinc oral interfiere con la absorción
Sistema de puntuación para el diagnóstico de la enfermedad de Wilson
intestinal de cobre, e induce la formación de metalotioneínas
Signos y síntomas típicos Puntuación que actúan como quelantes en el enterocito, este cobre liga-
Anillos de Kayser-Fleischer do es eliminado por las heces con la descamación de las cé-
Presentes 2 lulas de la mucosa duodenal. Actualmente se emplea en el
Ausentes 0 tratamiento de la fase de mantenimiento de pacientes, trata-
Síntomas neurológicos** dos previamente con quelantes, o en el tratamiento de pa-
Severos 2 cientes presintomáticos. También se ha usado como trata-
Leves 1 miento primario en pacientes que presentan deterioro
Ausentes 0 neurológico tras tratamiento con D-penicilamina, o durante
Ceruloplasmina sérica el embarazo.
Normal (>0,2 g/l) 0 Debe restringirse la ingesta de alimentos ricos en cobre
0,1-0,2 g/l 1 como los frutos secos, chocolate, setas, mariscos o carne de
< 0,1 g/l 2 vísceras19.
Anemia hemolítica negativa en la prueba de Coombs El trasplante hepático puede ser la única solución para
Presente 1 pacientes con fallo hepático agudo o con cirrosis hepática
Ausente 0 descompensada. El trasplante hepático corrige el defecto en-
Otras pruebas zimático subyacente.
Cobre hepático (en ausencia de colestasis)
> 5x LSN (> 4 μmol/g) 2
0,8-4 μmol/ 1 Conflicto de intereses
Normal (< 0,8 μmol/g) –1
Gránulos rodamina-positivos* 1 Los autores declaran no tener ningún conflicto de intereses.
Cobre en orina (en ausencia de hepatitis)
Normal 0
1-2x LSN 1 Responsabilidades éticas
> 2X LSN 2
Normal, pero > 5x LSN tras D-penicilamina 2
Protección de personas y animales. Los autores declaran
Análisis de mutaciones
que para esta investigación no se han realizado experimentos
Detectada en ambos alelos 4
en seres humanos ni en animales.
Detectada e un alelo 1
No detectadas 0
Confidencialidad de los datos. Los autores declaran que en
4 o más: diagnóstico establecido; 3: diagnóstico posible, se precisan más pruebas;
2 o menos: diagnóstico muy improbable. este artículo no aparecen datos de pacientes.
LSN: límite superior a la normalidad. *Si cobre hepático cuantitativo no disponible;
**o anomalías características en la resonancia magnética.
Derecho a la privacidad y consentimiento informado. Los
autores declaran que en este artículo no aparecen datos de
pacientes.
D-penicilamina. El uso de D-penicilamina se asocia a múlti-
ples efectos adversos, que en el 30% de los casos obligan a su
suspensión. Debido a la existencia de reacciones cruzadas Bibliografía
debe usarse con cautela en pacientes con alergia conocida a
la penicilina. La D-penicilamina inactiva la piridoxina, por lo t Importante tt Muy importante
que deben asociarse pequeñas dosis de piridoxina en pacien-
tes tratados con este fármaco. ✔ Metaanálisis ✔ Artículo de revisión
La trientina es otro quelante del cobre, empleado en el ✔ Ensayo clínico controlado ✔ Guía de práctica clínica
tratamiento de pacientes con intolerancia a la D-penicilami- ✔ Epidemiología
na, o como primer tratamiento. Los datos existentes sugieren
que es tan eficaz como la D-penicilamina en el tratamiento ✔
1. Finberg KE. Regulation of systemic iron homeostasis. Curr Opin Hema-
tol. 2013;20(3):208-14.
de la EW y muestra menor frecuencia de efectos adversos; el
deterioro neurológico también se observa con este fármaco, ✔
2. Camaschella C. Iron and hepcidin: a story of recycling and balance. He-
matology Am Soc Hematol Educ Program. 2013;2013:1-8.
pero es menos frecuente que con D-penicilamina. Debe evi- ✔
3. Wang J, Pantopoulos K. Regulation of cellular iron metabolism. Biochem J.
2011;434(3):365-81.
tarse su administración conjunta con hierro por formar un
complejo nefrotóxico.
✔
4. tt Silva B, Faustino P. An overview of molecular basis of iron me-
tabolism regulation and the associated pathologies. Biochim Bio-
phys Acta. 2015;1852(7):1347-59.
El tetramolibdato amónico interfiere la absorción intes-
tinal de cobre y liga el cobre plasmático reduciendo la incor-
✔
5. tt Pietrangelo A. Genetics, genetic testing, and management of
hemochromatosis: 15 years since hepcidin. Gastroenterology.
2015;149(5):1240-51.
poración a las células. Se ha propuesto como tratamiento en
pacientes con afectación neurológica dado que el riesgo de
✔
6. t Siddique A, Kowdley KV. Review article: the iron overload syn-
dromes. Aliment Pharmacol Ther. 2012;35(8):876-93.
deterioro neurológico es menor que con la trientina. No está ✔
7. Munñoz M, García-Erce JA, Remacha AF. Disorders of iron metabolism.
Part 1: molecular basis of iron homoeostasis. J Clin Pathol. 2011;64(4):
disponible comercialmente. 281-6.
Medicine. 2016;12(19):1094-106 1105
ENFERMEDADES ENDOCRINOLÓGICAS Y METABÓLICAS (VII)
✔8. tt Fleming RE, Ponka P. Iron overload in human disease. N Engl
J Med. 2012;366(4):348-59.
20. tt EASL Clinical Practice Guidelines: Wilson’s disease. J Hepa-
tol. 2012;56(3):671-85.
✔9. t Ganz T, Nemeth E. Hepcidin and iron homeostasis. Biochim
Biophys Acta. 2012;1823(9):1434-43.
✔
21. tt Trocello JM, Chappuis P, El BS et al. [Abnormal copper me-
tabolism in adult]. Rev Med Interne. 2010;31(11):750-6.
✔
10. Gujja P, Rosing DR, Tripodi DJ, Shizukuda Y. Iron overload cardiomyo-
pathy: better understanding of an increasing disorder. J Am Coll Cardiol.
✔
22. van den Berghe PV, Klomp LW. New developments in the regulation of
intestinal copper absorption. Nutr Rev. 2009;67(11):658-72.
2010;56(13):1001-12. ✔
23 Hordyjewska A, Popiolek L, Kocot J. The many “faces” of copper in me-
✔
11. t Pietrangelo A. Hereditary hemochromatosis: pathogenesis, dicine and treatment. Biometals. 2014;27(4):611-21.
diagnosis, and treatment. Gastroenterology. 2010;139(2):393-408. ✔
24. Aggarwal A, Bhatt M. Update on Wilson disease. Int Rev Neurobiol.
✔
12. tt Pietrangelo A. Hereditary hemochromatosis--a new look at an
old disease. N Engl J Med. 2004;350(23):2383-97.
2013;110:313-48.
25. Kaler SG. ATP7A-related copper transport diseases-emerging concepts
✔
13. tt EASL clinical practice guidelines for HFE hemochromatosis. and future trends. Nat Rev Neurol. 2011;7(1):15-29.
J Hepatol. 2010;53(1):3-22. ✔
26. Wu F, Wang J, Pu C, Qiao L, Jiang C. Wilson’s disease: a comprehensive
✔
14. tt Pietrangelo A, Caleffi A, Corradini E. Non-HFE hepatic iron review of the molecular mechanisms. Int J Mol Sci. 2015;16(3):6419-31.
overload. Semin Liver Dis. 2011;31(3):302-18. ✔
27. Harris ZL, Klomp LW, Gitlin JD. Aceruloplasminemia: an inherited neu-
✔
15. tt Bacon BR, Adams PC, Kowdley KV, Powell LW, Tavill AS.
Diagnosis and management of hemochromatosis: 2011 practice gui-
rodegenerative disease with impairment of iron homeostasis. Am J Clin
Nutr. 1998;67(5)Suppl:972S-7.
deline by the American Association for the Study of Liver Diseases.
Hepatology. 2011;54(1):328-43.
✔
28. Tumer Z, Moller LB. Menkes disease. Eur J Hum Genet. 2010;18(5):511-
8.
✔
16. Adams PC, Barton JC. A diagnostic approach to hyperferritinemia with a
non-elevated transferrin saturation. J Hepatol. 2011;55(2):453-8.
✔ tt
29. Ala A, Walker AP, Ashkan K, Dooley JS, Schilsky ML. Wilson’s
disease. Lancet. 2007;369(9559):397-408.
✔
17. Brissot P. Optimizing the diagnosis and the treatment of iron overload
diseases. Expert Rev Gastroenterol Hepatol. 2015;1-12.
✔t
30. Rodríguez-Castro KI, Hevia-Urrutia FJ, Sturniolo GC. Wilson’s
disease: A review of what we have learned. World J Hepatol. 2015;
✔
18. Barrera Portillo MC, Uranga UM, Sánchez GJ, Ustiza Echeverria JM, 7(29):2859-70.
Gervas WC, Guisasola IA. [Liver and heart T2* measurement in secon-
dary haemochromatosis]. Radiologia. 2013;55(4):331-9.
✔
31. Roberts EA, Schilsky ML. Diagnosis and treatment of Wilson disease: an
update. Hepatology. 2008;47(6):2089-111.
✔t
19. Muñoz M, García-Erce JA, Remacha AF. Disorders of iron me-
tabolism. Part II: iron deficiency and iron overload. J Clin Pathol.
✔
32. Ferenci P, Caca K, Loudianos G, Mieli-Vergani G, Tanner S, Sternlieb I,
et al. Diagnosis and phenotypic classification of Wilson disease. Liver Int.
2011;64(4):287-96. 2003;23(3):139-42.
1106 Medicine. 2016;12(19):1094-106
También podría gustarte
- Causas De Mala Circulación - Basado En Las Enseñanzas De Frank Suarez: Factores Y Desencadenantes De Problemas CirculatoriosDe EverandCausas De Mala Circulación - Basado En Las Enseñanzas De Frank Suarez: Factores Y Desencadenantes De Problemas CirculatoriosAún no hay calificaciones
- Latorre (2016) - WilsonDocumento13 páginasLatorre (2016) - WilsonMARIA MONTSERRAT SOMOZA MONCADAAún no hay calificaciones
- Trastornos Del Metabolismo Del Hierro y PDFDocumento10 páginasTrastornos Del Metabolismo Del Hierro y PDFBetzabe TtiraAún no hay calificaciones
- Metabolismo Del Hierro: Desde El Laboratorio A La ClínicaDocumento5 páginasMetabolismo Del Hierro: Desde El Laboratorio A La ClínicaLaura Alvarado BrophyAún no hay calificaciones
- El HierroDocumento6 páginasEl Hierroblancagaona.2001Aún no hay calificaciones
- Alteraciones Del Metabolismo Del HierroDocumento11 páginasAlteraciones Del Metabolismo Del HierroOmar CarrizoAún no hay calificaciones
- Anemia FerropenicaDocumento22 páginasAnemia FerropenicaRomina Reyes LoorAún no hay calificaciones
- Metabolismo Del HierroDocumento10 páginasMetabolismo Del HierroGabriel Henrique OliveiraAún no hay calificaciones
- Metabolismo Del Hierro y Anemia Del EmbarazoDocumento25 páginasMetabolismo Del Hierro y Anemia Del EmbarazoJose Wildo Oblitas ZeaAún no hay calificaciones
- Efectos Toxicos de Los MetalesDocumento18 páginasEfectos Toxicos de Los MetalesMariafernanda Coronado FernándezAún no hay calificaciones
- 03.003 Anemias CarencialesDocumento10 páginas03.003 Anemias CarencialesSabrina BronfenAún no hay calificaciones
- Seminario Del HierroDocumento8 páginasSeminario Del HierroJuan Carlos Tenecora QuitoAún no hay calificaciones
- Bioquimica Del FeDocumento5 páginasBioquimica Del FeMiriam SanchezAún no hay calificaciones
- Monografia Anemia FerropenicaDocumento42 páginasMonografia Anemia FerropenicaDiego PacherresAún no hay calificaciones
- n5-297-307 - Luis BlesaDocumento12 páginasn5-297-307 - Luis BlesaGisela Anampa MonzonAún no hay calificaciones
- Clase 36 - Hematología - Anemia Ferropriva y de Enfermedad CrónicaDocumento8 páginasClase 36 - Hematología - Anemia Ferropriva y de Enfermedad CrónicaMatameloca YaaAún no hay calificaciones
- Metabolismo de Hierro, Cobalamina y Acido FolicoDocumento12 páginasMetabolismo de Hierro, Cobalamina y Acido FolicoangelaAún no hay calificaciones
- Pregunta 1Documento2 páginasPregunta 1Seydy Briggetty Tenazoa LopezAún no hay calificaciones
- Anemia y Su ClasificacionDocumento7 páginasAnemia y Su ClasificacionAngela CVAún no hay calificaciones
- Anemia Por Deficiencia de HierroDocumento4 páginasAnemia Por Deficiencia de HierroDanielaAún no hay calificaciones
- 7.7 HemocromatosisDocumento18 páginas7.7 HemocromatosisNicöle AndradeAún no hay calificaciones
- Seminario 2 Farma 2Documento13 páginasSeminario 2 Farma 2Joselyn Esmeralda Cruz SantamariaAún no hay calificaciones
- Iron Metabolism in Pancreatic Beta-Cell Function and Dysfunction-2021.en - EsDocumento17 páginasIron Metabolism in Pancreatic Beta-Cell Function and Dysfunction-2021.en - EsKammiloPAún no hay calificaciones
- Anemia de Los Procesos CrónicosDocumento44 páginasAnemia de Los Procesos Crónicosmaria aguirreAún no hay calificaciones
- Interpretacion Parametros Hematimetricos Bioquimicos PDFDocumento15 páginasInterpretacion Parametros Hematimetricos Bioquimicos PDFmilleralselmoAún no hay calificaciones
- V. Anemia Ferropenica y Sobrecarga de HierroDocumento49 páginasV. Anemia Ferropenica y Sobrecarga de HierroCitlali SanchezAún no hay calificaciones
- Metabolismo Del Hierro PDFDocumento12 páginasMetabolismo Del Hierro PDFVannia Rodriguez MartinezAún no hay calificaciones
- 2017 CHile Biomarcadores de Anemia y NutriciónDocumento9 páginas2017 CHile Biomarcadores de Anemia y NutriciónVictor Arellano NuñezAún no hay calificaciones
- Fisiopatología Metabolismo HierroDocumento14 páginasFisiopatología Metabolismo HierroMacabre Blood BloodAún no hay calificaciones
- LOS ANTIANÉMICOS y ANTIHISTAMINICOSDocumento48 páginasLOS ANTIANÉMICOS y ANTIHISTAMINICOSWalter Jose Valbuena100% (1)
- Enfermedad Metabolica HereditariaDocumento16 páginasEnfermedad Metabolica Hereditariagirolama366Aún no hay calificaciones
- 3) Metabolismo Del HierroDocumento7 páginas3) Metabolismo Del HierroAlfonso PrietoAún no hay calificaciones
- 1 s2.0 S0185106315000918 MainDocumento10 páginas1 s2.0 S0185106315000918 MainRisma SakeAún no hay calificaciones
- Trastornos en El Metabolismo Del HierroDocumento8 páginasTrastornos en El Metabolismo Del HierroVictor CastroAún no hay calificaciones
- Metabolismo de Fe, Anemia FerropénicaDocumento7 páginasMetabolismo de Fe, Anemia FerropénicaCatalina CirausAún no hay calificaciones
- Barragan-Ibanez2016 Iron Deficiency Anaemia PDFDocumento10 páginasBarragan-Ibanez2016 Iron Deficiency Anaemia PDFAna Muñoa DuchateauAún no hay calificaciones
- 14586-Texto Del Artículo-58372-2-10-20160227Documento6 páginas14586-Texto Del Artículo-58372-2-10-20160227xirepew543Aún no hay calificaciones
- LN Cap 1.28Documento46 páginasLN Cap 1.28Eduardo FontAún no hay calificaciones
- Anemia Inflamatoria o Ferropenia FuncionalDocumento9 páginasAnemia Inflamatoria o Ferropenia FuncionalAlfonsina RocciaAún no hay calificaciones
- Anemia, LeucemiaDocumento32 páginasAnemia, LeucemiaAngie CalderónAún no hay calificaciones
- Anemias FinalDocumento9 páginasAnemias FinalRocio sosaAún no hay calificaciones
- Anemia FerropenicaDocumento47 páginasAnemia FerropenicaCassandra TorresAún no hay calificaciones
- Anemia Ferropenica Monsalve CardonaDocumento5 páginasAnemia Ferropenica Monsalve CardonaJuliAún no hay calificaciones
- HierroDocumento5 páginasHierroFernando Cordova PardoAún no hay calificaciones
- Expo HematologiaDocumento3 páginasExpo HematologiaMarlin TavarezAún no hay calificaciones
- Indicaciones de Terapia Quelante de HierroDocumento4 páginasIndicaciones de Terapia Quelante de HierroMatias BossieAún no hay calificaciones
- Práctica Nº3 Anemia FerropenicaDocumento13 páginasPráctica Nº3 Anemia FerropenicaCristian Rodrigo Barrios SotomayorAún no hay calificaciones
- Absorción y Metabolismo Del Hierro - MGVDocumento10 páginasAbsorción y Metabolismo Del Hierro - MGVMica Salas VictoriaAún no hay calificaciones
- 6Documento4 páginas6Carlos NeuroAún no hay calificaciones
- Anemia Carencial PDFDocumento10 páginasAnemia Carencial PDFEbony Mariset Terrones DiazAún no hay calificaciones
- Ferropenia y Otras Anemia Hiporpoliferativas Versión BuenaDocumento11 páginasFerropenia y Otras Anemia Hiporpoliferativas Versión BuenaAmbar ToledoAún no hay calificaciones
- Taller HematologíaDocumento5 páginasTaller Hematologíafernando joseAún no hay calificaciones
- Cap 14 - Libro de CatedraDocumento17 páginasCap 14 - Libro de CatedraBarDFAún no hay calificaciones
- Estudio Del HierroDocumento24 páginasEstudio Del HierroPablo Ignacio Hernández RivasAún no hay calificaciones
- METABOLISMO (Fe, CaDocumento40 páginasMETABOLISMO (Fe, CasayraAún no hay calificaciones
- Fisiopatología Del Metabolismo Del Hierro. Implicaciones Diagnósticas y TerapéuticasDocumento11 páginasFisiopatología Del Metabolismo Del Hierro. Implicaciones Diagnósticas y TerapéuticasdrheayAún no hay calificaciones
- Química de macrocomponentes de alimentosDe EverandQuímica de macrocomponentes de alimentosAún no hay calificaciones
- Enfermedad de WilsonDocumento5 páginasEnfermedad de WilsonJordan Irán López GarcíaAún no hay calificaciones
- HC Ast SPDocumento9 páginasHC Ast SPJordan Irán López GarcíaAún no hay calificaciones
- Enfermedad de Paget Ósea: Manifestaciones Clínicas, Diagnóstico y TratamientoDocumento6 páginasEnfermedad de Paget Ósea: Manifestaciones Clínicas, Diagnóstico y TratamientoVictor Espinoza FuenzalidaAún no hay calificaciones
- Calculo de L y e Desequilibio He - 20240126 - 145958 - 0000Documento39 páginasCalculo de L y e Desequilibio He - 20240126 - 145958 - 0000Jordan Irán López GarcíaAún no hay calificaciones
- Tipos de EnvejecimientoDocumento1 páginaTipos de EnvejecimientoJordan Irán López GarcíaAún no hay calificaciones
- Vejez 2010Documento18 páginasVejez 2010JimmyAún no hay calificaciones
- Teorías Del EnvejecimientoDocumento13 páginasTeorías Del EnvejecimientoJordan Irán López GarcíaAún no hay calificaciones
- Historia Clínica GeriátricaDocumento11 páginasHistoria Clínica GeriátricaJordan Irán López GarcíaAún no hay calificaciones
- Tabla Comparativa Teorias EnvejecimientoDocumento1 páginaTabla Comparativa Teorias EnvejecimientoJordan Irán López GarcíaAún no hay calificaciones
- Directoreditorial Ockham 18-1-8Documento8 páginasDirectoreditorial Ockham 18-1-8Camilo CastilloAún no hay calificaciones
- BIOGRAFÍASDocumento5 páginasBIOGRAFÍASJordan Irán López GarcíaAún no hay calificaciones
- Azucar Hechos y MitosDocumento6 páginasAzucar Hechos y MitosJose RonAún no hay calificaciones
- Tumores CranealesDocumento17 páginasTumores CranealesJordan Irán López GarcíaAún no hay calificaciones
- Fiebre TifoideaDocumento4 páginasFiebre TifoideaJordan Irán López GarcíaAún no hay calificaciones
- Anatomia, Semiologia y Exploracion NeurológicasDocumento19 páginasAnatomia, Semiologia y Exploracion NeurológicasJordan Irán López GarcíaAún no hay calificaciones
- Neuroinfeccion TB y VirusDocumento18 páginasNeuroinfeccion TB y VirusJordan Irán López GarcíaAún no hay calificaciones
- Evc HemorragicoDocumento23 páginasEvc HemorragicoJordan Irán López GarcíaAún no hay calificaciones
- Exploracion Neurológica AbreviadaDocumento5 páginasExploracion Neurológica AbreviadaElizabeth Pérez RamírezAún no hay calificaciones
- Neuroinfeccion BacterianaDocumento14 páginasNeuroinfeccion BacterianaJordan Irán López GarcíaAún no hay calificaciones
- Neuroinfeccion NeurocisticercosisDocumento21 páginasNeuroinfeccion NeurocisticercosisJordan Irán López GarcíaAún no hay calificaciones
- Eq.2 - Práctica 8Documento7 páginasEq.2 - Práctica 8GLADYS ITZEL DOMINGUEZ BERNALAún no hay calificaciones
- Dulet y El GlutationDocumento2 páginasDulet y El GlutationOmar Gtz100% (1)
- Caso Clinico Fisiologia RenalDocumento3 páginasCaso Clinico Fisiologia RenalYamilex Rojas RodríguezAún no hay calificaciones
- SEMINARIO 7 ResueltoDocumento12 páginasSEMINARIO 7 ResueltoLome IfmsaAún no hay calificaciones
- Caloría, Es Una Unidad de Energía Térmica, de Símbolo Cal, Que Equivale A La Cantidad de Calor NecesariaDocumento14 páginasCaloría, Es Una Unidad de Energía Térmica, de Símbolo Cal, Que Equivale A La Cantidad de Calor NecesariaCarlos Perez T.Aún no hay calificaciones
- Biologia Carbohidratos, Lipidos y ProteinasDocumento58 páginasBiologia Carbohidratos, Lipidos y Proteinasjosep josue prado fasanandoAún no hay calificaciones
- Oli Go Elementos UltimoDocumento34 páginasOli Go Elementos Ultimojuan gerardoAún no hay calificaciones
- Los Cuatro Tejidos Basicos: (Universidad Del Perú, DECANA DE AMERICA)Documento28 páginasLos Cuatro Tejidos Basicos: (Universidad Del Perú, DECANA DE AMERICA)VALERIA ALEJANDRA CHINCHON OLIVERAAún no hay calificaciones
- Manual de Prácticas de Laboratorio de Bioquímica MédicaDocumento27 páginasManual de Prácticas de Laboratorio de Bioquímica MédicaDaniela Ruelas CisnerosAún no hay calificaciones
- Osorio Bedoya Maria JohanaDocumento1 páginaOsorio Bedoya Maria JohanaSol Angel Orobio OsorioAún no hay calificaciones
- AntidotosDocumento9 páginasAntidotosYeiny SánchezAún no hay calificaciones
- Clase # 1 Sistema HemáticoDocumento51 páginasClase # 1 Sistema HemáticoMiriam GonzalezAún no hay calificaciones
- Genetica Del CancerDocumento174 páginasGenetica Del CancervbalderalitzyanAún no hay calificaciones
- Tarea5 CuestionarioDocumento3 páginasTarea5 Cuestionarioleidy jaquelin valdez bazanAún no hay calificaciones
- Neurotoxicidad Af EsDocumento12 páginasNeurotoxicidad Af EsjuanAún no hay calificaciones
- Laboratorio 2021061610850Documento3 páginasLaboratorio 2021061610850Santiago OsorioAún no hay calificaciones
- Presentacion MalonatoDocumento21 páginasPresentacion Malonatorguerrerov020Aún no hay calificaciones
- Guía 3 - Reproducción. RespuestasDocumento6 páginasGuía 3 - Reproducción. Respuestasjuan Felipe Vergara uribe 8DAún no hay calificaciones
- Tamiz PlusDocumento13 páginasTamiz Plusjimy salazarAún no hay calificaciones
- Colección König. Anatomía de Los Animales Domésticos: (2 Tomos) Texto y Atlas en ColorDocumento3 páginasColección König. Anatomía de Los Animales Domésticos: (2 Tomos) Texto y Atlas en ColorRolando J. ValleAún no hay calificaciones
- Paper Antocianina ArandanoDocumento121 páginasPaper Antocianina ArandanoKarolyne VegaAún no hay calificaciones
- Elaboración de Yogurt - DiazMoralesDocumento8 páginasElaboración de Yogurt - DiazMoralesChuy MoralesAún no hay calificaciones
- Enfermedades Por Mala Alimentacion ResumenDocumento9 páginasEnfermedades Por Mala Alimentacion ResumenOndina AguiluzAún no hay calificaciones
- Anatomia Del Sistema NefrourologicoDocumento9 páginasAnatomia Del Sistema NefrourologicoCamila A CarmonaAún no hay calificaciones
- Certamen 3 PPF PDFDocumento31 páginasCertamen 3 PPF PDFConi Merino PeiranoAún no hay calificaciones
- Páncreas Exposicion Geovanny CotaDocumento8 páginasPáncreas Exposicion Geovanny Cotaalbertocotaceb82Aún no hay calificaciones
- Cánceres: Intervenciones Dietéticas en El Tratamiento y La Respuesta Al Cáncer: Una Revisión ExhaustivaDocumento30 páginasCánceres: Intervenciones Dietéticas en El Tratamiento y La Respuesta Al Cáncer: Una Revisión ExhaustivaCarla Nava MagriAún no hay calificaciones
- 5 Desgrabe Fármacos Alucinógenos o PsicomotoresDocumento9 páginas5 Desgrabe Fármacos Alucinógenos o Psicomotoresjordi bastidasAún no hay calificaciones
- El Metabolismo Lipídico Bovino y Su Relación Con La DietaDocumento11 páginasEl Metabolismo Lipídico Bovino y Su Relación Con La DietaGary Jheferson Salazar RondonAún no hay calificaciones
- Lesión CelularDocumento7 páginasLesión CelularJasmín VelásquezAún no hay calificaciones