Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Oncofertilidad
Cargado por
Martin GonzalezDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Oncofertilidad
Cargado por
Martin GonzalezCopyright:
Formatos disponibles
Puesta al día
Oncofertilidad
¿qué debemos saber?
Dra. Dana Kimelman*, Dr. Santiago Scasso**
* Ginecóloga, Master in Reproductive Science and
Medicine. Northwestern University, Chicago, Illinois.
Policlínica de Oncofertilidad, Hospital Pereira Rossell.
** Ginecólogo Oncólogo. Presidente de la
Sociedad Uruguaya de Ginecología Oncológica.
Montevideo, Uruguay.
Resumen. La detección temprana del cáncer, junto Abstract. The early detection of cancer, together with
con la disponibilidad de tratamientos oncológicos the availability of effective oncological treatments,
efectivos, determinan una alta sobrevida de las pa- determine a high survival of patients with oncological
cientes con patologías oncológicas. pathologies.
Dado el riesgo gonadotóxico de los tratamientos sisté- Given the gonadotoxic risk of systemic treatments
micos (quimio y radioterapia) y las cirugías oncológicas (chemo and radiotherapy) and sterilizing oncology
esterilizantes, es primordial ocuparnos de la calidad surgeries, it is essential to address the quality of life of
de vida de las sobrevivientes una vez superada la survivors once the disease has been overcome.
enfermedad. Oncofertility is the discipline that seeks to protect and
La oncofertilidad es la disciplina que busca proteger preserve the fertility and hormonal function of children,
y preservar la fertilidad y función hormonal de niños, adolescents and young adults who may see their re-
niñas, adolescentes y adultos jóvenes que pueden ver productive future compromised by certain diseases
su futuro reproductivo comprometido por enfermeda- and/or complex oncological or medical treatments.
des y/o tratamientos oncológicos. Scientific evidence has shown that correct reproduc-
El asesoramiento reproductivo mejora la adherencia tive counseling improves treatment adherence and
al tratamiento y la tolerancia al mismo. tolerance.
Palabras clave: oncofertilidad, gonadotoxicidad, tratamiento oncológico, quimioterapia.
Keywords: oncofertility, gonadotoxicity, cancer treatment, chemotherapy.
Introducción Epidemiología
La oncofertilidad es la disciplina que busca proteger El cáncer afecta 14 millones de personas en el mundo
y preservar la fertilidad y función hormonal de niños, anualmente. Un 10 % de los casos ocurren en edad
niñas, adolescentes y adultos jóvenes, que pueden reproductiva(1).
ver su futuro reproductivo comprometido por cier- En Uruguay, en el período comprendido entre 2012 y
tas enfermedades y/o tratamientos oncológicos o 2016 según el Registro Nacional de Cáncer, se registra-
médico complejos. ron en promedio anualmente (excluyendo al cáncer de
Se trata de una subespecialidad médica que in- piel no melanoma) 465 neoplasias malignas en mujeres
tegra varios pilares como la investigación básica, de 15 a 39 años. Fallecieron en el mismo período en
oncología, hematología, urología, ginecología on- promedio 89 mujeres por año en ese rango de edad.
cológica, medicina reproductiva y endocrinología, Los tumores más frecuentes en esta población son
entre otros. mama, tiroides y cérvix. Los tumores génito-mamarios
representan 48 % de las neoplasias, similar a lo descrito
E mail: danakimelmanf@gmail.com - sscasso@gmail.com a nivel internacional(2).
Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61 1
Oncofertilidad
Riesgo gonadotóxico Por esta razón, importantes sociedades científicas
internacionales como la Sociedad Americana de On-
de los tratamientos oncológicos cología Clínica (ASCO), Sociedad Europea de Oncolo-
El avance, efectividad y disponibilidad de los trata- gía Médica (ESMO), Sociedad Americana de Medicina
mientos oncológicos, sumado a las estrategias de Reproductiva (ASRM) y la Academia Americana de Pe-
detección temprana, determinan una alta sobrevida diatría (AAP), establecen que todo paciente en edad
de este grupo de pacientes. Es por esto que debemos pediátrica, adolescente o adulto joven debe ser ase-
preocuparnos y ocuparnos por la calidad de vida de sorado sobre la potencial pérdida de su capacidad
las sobrevivientes una vez superada la enfermedad. reproductiva, previo al inicio del tratamiento y se
Los tratamientos oncológicos muchas veces asocian debe ofrecer la estrategia más acertada de acuerdo
toxicidad en diferentes órganos y sistemas, dentro de a la patología y tipo de tratamiento que recibirá el
estos se encuentra el potencial daño gonadal. paciente(3-6).
El riesgo gonadotóxico puede estar presente en los
tratamientos sistémicos como la quimioterapia, Estrategias estandarizadas para
radioterapia y en los tratamientos quirúrgicos este- la preservación de la fertilidad
rilizantes. La estrategia de elección para protección de la ferti-
Dentro de los efectos gonadotóxicos de los trata- lidad en mujeres luego de la menarca es la criopre-
mientos se comprenden la afectación en la fertilidad, servación de embriones u ovocitos.
función gonadal y salud sexual. La técnica de criopreservación de embriones fue la
El riesgo gonadotóxico de los tratamientos de qui- primera en ser estandarizada a nivel internacional
mioterapia estará determinado por el fármaco que y durante años fue la única opción que se ofrecía
se utilice, dosis, edad y reserva ovárica de la paciente a mujeres para preservar su fertilidad. Recurrir a
que la recibe. Es importante destacar que existen es- esta técnica implica una fertilidad supeditada a una
calas de riesgo gonadotóxico: alto, moderado, bajo relación de pareja o a la fertilización de óvulos con
o desconocido. espermatozoides donados.
Los agentes alquilantes, junto con la irradiación La técnica de criopreservación de ovocitos es más
pélvica, encefálica y corporal total constituyen los reciente y dejó de ser considerada experimental por la
tratamientos de mayor riesgo gonadotóxico(1). ASRM en el año 2012. Actualmente es la estrategia de
La complejidad del ejercicio de esta subespecialidad, elección para pacientes postmenarca que quieran
se basa en que, en el momento en que se proponen proteger su fertilidad(6).
tratamientos médicos que permitirán a la persona
sobrevivir, también deben discutirse aspectos del Criopreservación de ovocitos
perfil de riesgo del tratamiento que pueden afec- La técnica de criopreservación de ovocitos debe
tar de forma severa y negativa la calidad de vida ser ofrecida a toda paciente que se someterá a un
posterior. tratamiento potencialmente gonadotóxico y previo
Por esta razón, se debe tener una clara discusión sobre al inicio del mismo(6).
las consecuencias endocrinológicas de los tratamien- Las sociedades científicas internacionales ESMO,
tos oncológicos, incluyendo la potencial pérdida de ASCO, ASRM y AAP establecen que toda paciente que
la fertilidad, disfunción hormonal y afectación de se someterá a un tratamiento gonadotóxico debe
órganos que dependen de hormonas esteroideas
recibir asesoramiento adecuado a su edad, oportuno
(hueso, corazón, cerebro) como también las posibles
y previo al inicio del tratamiento onco-específico,
disfunciones en la esfera sexual.
idealmente durante la planificación del mismo, in-
Se deben ofrecer estrategias de preservación de dependiente del tipo de enfermedad, el estadío de
la fertilidad y asesorar en anticoncepción con el la misma y el pronóstico.
objetivo de optimizar la calidad de vida futura de
Se tendrá en cuenta la situación clínica de la paciente
los sobrevivientes(1).
en el momento del asesoramiento y se decidirá en
conjunto con el equipo médico tratante si la paciente
Guías clínicas internacionales podría someterse a un tratamiento de preservación
El asesoramiento reproductivo de pacientes jóvenes en ese momento. En definitiva, será decisión de la
con diagnóstico reciente de cáncer mejora la adhe- paciente si desea recurrir o no a las estrategias
rencia al tratamiento y la tolerancia al mismo(3). planteadas(3,5-8).
2 Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61
Kimelman D, Scasso S Puesta al día
El tratamiento de criopreservación de ovocitos se
inicia luego de un correcto asesoramiento de la
paciente, en el que se le explica el riesgo de los tra-
tamientos oncológicos y las posibles estrategias de
preservación de fertilidad(8).
En caso que la criopreservación de ovocitos sea la
técnica de elección, se debe explicar a la paciente
las características del tratamiento y las tasas de éxito
reportadas hasta el momento.
Debemos ser sumamente claros y cuidadosos en el
asesoramiento para que las pacientes puedan mane-
jar la expectativa basándose en la evidencia científica
disponible(7). También debemos ser claros en cuanto
a la posibilidad de que la paciente no llegue a utilizar
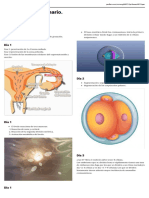
los ovocitos criopreservados, ya sea por no desear una Figura 1 Procedimiento ICSI (Inyección
maternidad biológica o por la posibilidad de lograr intracitoplasmática de espermatozoide).
un embarazo espontáneo(9). Imagen de microscopio de alta resolución
de laboratorio de Reproducción Humana,
Estimulación ovárica Centro Esterilidad Montevideo (CEM).
Gentileza Dra. L. Cantú.
Existen diferentes protocolos de estimulación ová-
rica controlada para la obtención de ovocitos. El
protocolo corto con administración de antagonistas El líquido folicular se envía en forma inmediata al
de la hormona liberadora de gonadotropina (GnRH) laboratorio de embriología que debe estar próximo
es el más utilizado(10). El motivo por el cual se opta a la sala donde se realiza el procedimiento.
por un protocolo corto, es que habitualmente las Una vez finalizado el tratamiento de estimulación y
pacientes tienen urgencia por comenzar el trata- criopreservación de ovocitos la paciente se encuentra
miento oncológico y por otro lado el protocolo corto libre para comenzar el tratamiento oncológico.
permite que la paciente que se somete a un aumento
de los niveles de estrógenos séricos, lo haga por el Random start
menor tiempo posible; especialmente en pacientes
con tumores hormono sensibles. Durante el proceso, Hasta hace pocos años, existía el concepto de que
la paciente se somete a estimulación hormonal con durante el ciclo ovárico, el reclutamiento folicular solo
gonadotrofinas. ocurría los primeros días del ciclo menstrual.
Aproximadamente al día 6 de estimulación, (cuando Hoy sabemos que existen diferentes momentos de
1 o 2 folículos en crecimiento llegan a un diámetro de reclutamiento folicular a lo largo del ciclo femenino.
aproximadamente 13 mm) se indica la administración En este grupo de pacientes en las que el tiempo es
de antagonistas de GnRH para evitar la rotura folicu- un factor limitante, la estimulación ovárica controlada
lar prematura. La estimulación ovárica controlada se comienza en cualquier momento del ciclo (fase
se mantiene durante aproximadamente 9 a 12 días folicular precoz, tardía o fase lútea). Existe evidencia
y cuando la cohorte total de folículos antrales llega científica que ha demostrado que comenzar la es-
a un promedio de diámetro de 16 mm se procede a timulación en diferentes etapas del ciclo no tiene
realizar el “trigger” para lograr la maduración de los un impacto negativo sobre el número de ovocitos
ovocitos. En este grupo de pacientes el trigger se recuperados(11).
realiza con agonistas de GnRH(10).
Inhibidores de la aromatasa
Extracción de ovocitos Las pacientes que presentan tumores hormono
La extracción de ovocitos se realiza 34-36 horas des- sensibles (por ejemplo, cáncer de mama o de endo-
pués del trigger mediante un procedimiento sencillo metrio) pueden verse beneficiadas al recibir inhi-
que se realiza con sedación, guiado por ecografía bidores de la aromatasa durante la estimulación
mediante punción transvaginal a través de los fon- hormonal, con el objetivo de disminuir los niveles
dos de saco vaginales, realizándose la aspiración de séricos de estradiol provocados por la estimulación
líquido folicular. ovárica controlada.
Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61 3
Oncofertilidad
Los trabajos científicos han demostrado que la esti- Tasas de éxito
mulación hormonal acompañada de letrozol no afec-
ta el número de ovocitos recuperados. Por lo tanto, las Debido a que la criopreservación de ovocitos no se
tasas de éxito de los tratamientos de criopreservación considera experimental desde el año 2012, la eviden-
cia científica respecto a las tasas de éxito de la misma
de ovocitos no se ven afectados(10).
es aún limitada.
Oportunidad En 2021, Kawwass y cols. publicaron las tasas de éxito
(embarazo y nacidos vivos) con embriones vitrificados
Los tratamientos de criopreservación de ovocitos entre 2012 y 2018 (en más del 90 % de los centros de
deben realizarse previo al inicio del tratamiento onco- reproducción asistida de Estados Unidos).
lógico. Dolmans y cols. demostraron la afectación del Las tasas de éxito en mujeres menores de 35 años
número de ovocitos recuperados y la calidad embrio- son de aproximadamente 42 % , disminuyendo con
naria por haber recibido poliquimioterapia (PQT; 1 o la edad en el momento de la criopreservación(7).
más ciclos) previo al tratamiento de criopreservación.
Idealmente se recomienda realizar los tratamientos Criopreservación de embriones
de preservación de fertilidad antes del inicio del trata- La paciente puede optar por la criopreservación de
miento oncológico. Si no fuera posible, por el estado embriones. Esta técnica fue estandarizada previo a
de gravedad de la paciente o por no haber recibido la de criopreservación de ovocitos y se realiza desde
asesoramiento en forma oportuna, se podría plantear hace más tiempo.
un tratamiento de criopreservación de ovocitos lue- La vitalidad posterior a la descongelación de los em-
go de 6 meses a 1 año del último ciclo de PQT. Esto briones es mínimamente superior a la de ovocitos.
permitiría otorgar tiempo a la reparación del daño Debemos ser muy cuidadosos a la hora de asesorar
a nivel de ADN celular de las células expuestas(12-13). a las pacientes ya que si bien esta es una técnica
Marco normativo - Legislación en Uruguay
Desde el año 2013, está vigente en Uruguay la Ley de Reproducción Humana Asistida (Ley
19.167) que regula las técnicas de reproducción asistida que se realizan en el país.
En Uruguay se brinda cobertura para los tratamientos de reproducción asistida de alta
complejidad (Fecundación in vitro [FIV], inyección espermática intracitoplasmática [ICSI]) a
pacientes con diagnóstico de esterilidad. La preservación de gametos fue contemplada en la
ley pero en el momento de la reglamentación y la creación de la normativa del Fondo Nacional
de Recursos (FNR) quedó por fuera de la cobertura.
En Julio de 2022 se aprobó un proyecto de ley de artículo único que modifica la Ley 19.167 y
brinda cobertura a través del FNR para la preservación de gametos femeninos y masculinos
previo al inicio del tratamiento oncológico. Este es un paso muy importante, que posiciona a
nuestro país una vez más como pionero en derechos reproductivos.
La ley aprobada aún no ha sido reglamentada pero en corto plazo la preservación de gametos
para preservación de la fertilidad previo al inicio de tratamientos oncológicos será una posibilidad
real para toda persona menor a 40 años que tenga que enfrentar un tratamiento potencialmente
gonadotóxico y desee proteger su fertilidad.
El hecho de que la cobertura económica sea realizada por el FNR, implica que los pacientes
tienen derecho a realizar los tratamientos o solicitar asesoramiento de preservación de fertilidad
con el centro o clínica que ellos deseen.
No son los prestadores los que estarán a cargo de la financiación ni de la realización de dichos
tratamientos. Este es un punto importante a la hora de asesorar los pacientes sobre la libertad
de elección de clínicas y médicos tratantes.
4 Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61
Kimelman D, Scasso S Puesta al día
disponible y estandarizada, cuando los ovocitos se obtención del tejido, el proceso de criopreservación
fertilizan con espermatozoides de la pareja la fertili- y abordaje quirúrgico, en el momento del reimplante
dad futura queda supeditada a la durabilidad de esa de tejido ovárico(14).
relación de pareja. En cuanto a la obtención del tejido, existe la posibi-
En Uruguay no hay cobertura para la fertilización in lidad de realizar una ooforectomía total mediante
vitro como estrategia de preservación de fertilidad. laparoscopía o una ooforectomía parcial intentando
remover un fragmento de corteza ovárica.
Criopreservación de tejido ovárico
El reimplante de tejido ovárico puede realizarse orto-
La criopreservación de tejido ovárico es una estra- tópico (en el sitio anatómico del ovario) o heterotópico
tegia que puede ofrecerse para preservación de la
(en otro sitio). La gran mayoría de nacimientos se han
fertilidad y/o recuperación de la función hormonal
reportado en reimplantes ortotópicos.
de niñas, adolescentes y mujeres jóvenes con diag-
nóstico oncológico(14). Con respecto a la criopreservación de tejido ovárico
Ha dejado de ser una estrategia considerada expe- en niñas, es escasa la evidencia científica en cuanto
rimental para la Sociedad Americana de Medicina al reimplante de un tejido ovárico pediátrico. Hay
Reproductiva desde el año 2019. solamente dos nacimientos reportados en la litera-
El primer nacimiento reportado en la literatura cien- tura científica de niñas de que tenían 9 y 13 años en
tífica luego de un autotrasplante de tejido ovárico el momento de la ooforectomía por una patología
fue en el año 2004, desde entonces el número de hematológica benigna(18).
nacimientos reportados ha aumentado de forma
exponencial(15). Tasas de éxito
En el caso de niñas que no han iniciado la pu- Las tasas de éxito de estos tratamientos se estiman
bertad, la criopreservación de tejido ovárico es entre un 30-40 % y los embarazos y posteriores
la única estrategia de preservación de fertilidad nacimientos se dan por embarazo espontáneo o
disponible. No obstante, también puede ofrecerse fecundación in vitro(19).
a adolescentes y/o adultas jóvenes que no puedan
o quieran retrasar dos semanas el inicio del trata- Se están desarrollando actualmente líneas de inves-
miento oncológico(5). tigación para realizar maduración ovocitaria in vitro
de ovocitos inmaduros obtenidos del tejido ovárico
Criterios de inclusión extraído para evitar la realización de reimplante y así
evitar el riesgo de reintroducción de células tumorales
Las pacientes candidatas a recurrir a esta estrategia
en el momento del autotrasplante, que puede darse
de preservación son:
en hematopatías malignas como leucemia o cáncer
• Niñas, adolescentes
o adultas jóvenes < 35 años de edad. de mama.
• Riesgo alto de gonadotoxicidad En los últimos años se han desarrollado herramientas
por el tratamiento > 50 %. biotecnológicas que permiten identificar la presencia
• Posibilidades razonables de sobrevida(16). de células tumorales en el tejido a reimplantar (cito-
metría de flujo, inmuno histoquímica, xenotrasplante,
Oportunidad entre otras). Se han reportado nacimientos luego de
Como todas las estrategias de preservación de ferti- reimplante de tejido ovárico en mujeres sobrevivien-
lidad, debe plantearse e idealmente llevarse a cabo tes de enfermedades como leucemia, en las cuales
antes del inicio del tratamiento oncológico. hasta hace años estaba contraindicado por el riesgo
A diferencia de la criopreservación de ovocitos, es de metástasis a nivel ovárico(20).
posible realizar la criopreservación de tejido ovárico La técnica de preservación de tejido ovárico tiene
cuando ya se ha iniciado el tratamiento oncoespecí- algunas ventajas respecto a la criopreservación
fico con quimioterapia(17). de ovocitos, ya que permite criopreservar miles
de ovocitos asociados a la propia matriz ovárica.
Proceso Asimismo, permite la posibilidad de embarazo es-
Si bien la Sociedad Americana de Medicina Reproduc- pontáneo una vez reimplantado el tejido y también
tiva no considera experimental la criopreservación hace posible el retorno de la función hormonal por
de tejido ovárico, aún existe evidencia científica un tiempo limitado, el cual puede extenderse a más
controvertida respecto a la estrategia quirúrgica de de 10 años(21).
Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61 5
Oncofertilidad
Experiencia en Uruguay Transposición ovárica
En el año 2004 se creó e implementó en Uruguay previa al tratamiento de radioterapia
un programa denominado “Preservando la función La transposición quirúrgica de los ovarios es una es-
ovárica en pacientes oncológicas”. El mismo utilizaba trategia que tiene como objetivo retirar los ovarios
un protocolo de criopreservación de tejido ovárico del sitio de irradiación para proteger su función y
creado y supervisado por el Dr. Callejo y colaborado-
eventualmente la fertilidad. Es un tratamiento que
res de la Universidad de Barcelona, España.
debería realizarse a toda paciente que tenga que
Entre los años 2004 y 2005, 15 pacientes entre 12 y 35 someterse a radioterapia pélvica.
años fueron incluidas en el protocolo. Se reportaron
2 casos en los que las pacientes presentaron insufi- Se trata de una cirugía sencilla mínimamente in-
ciencia ovárica precoz, con síntomas climatéricos y vasiva y puede aprovecharse otro acto anestésico
solicitaron el trasplante heterotópico. quirúrgico para su realización. En los países en que
El trasplante se realizó y las pacientes presentaron se realiza criopreservación de tejido ovárico, una es-
recuperación de la función endocrinológica. Hasta trategia utilizada es la ooforectomía unilateral para
el momento no se reportaron casos de embarazo en criopreservación de tejido ovárico y la transposición
estas pacientes ni han sido sometidas a tratamientos del ovario contralateral.
de estimulación(22). Las tasas de éxito de estos tratamientos dependerán
Actualmente se está llevando a cabo desde el año de la dosis, tipo y sitio de irradiación, la edad de la
2020 un proyecto de investigación y desarrollo fi- paciente que la recibe y si el tratamiento se acompaña
nanciado por la Agencia Nacional de Investigación de quimioterapia o no.
y Desarrollo (ANII) en el que se busca estandarizar la
En el caso de que la paciente deba recibir también
técnica de vitrificación de tejido ovárico en un modelo
animal (ovinos). un tratamiento de quimioterapia radio sensibilizante,
como es el caso del cáncer de cuello uterino, se debe
Los resultados obtenidos al finalizar esta etapa per-
tener en cuenta que los agentes quimioterápicos
mitirán implementar un programa de vitrificación
de tejido ovárico para preservación de fertilidad en sistémicos pueden tener un impacto en la función
nuestro país. gonadal(1).
Estrategias experimentales Preservación de la fertilidad
de preservación de fertilidad en cánceres ginecológicos
En Uruguay los tumores génito-mamarios represen-
Análogos de GnRH o tan el 48 % de las neoplasias. La frecuencia de estos
supresión ovárica tumores varía dependiendo del tramo de edades
En la literatura científica se ha debatido por más de analizado, después de los 30 años. El cáncer de mama
30 años en cuanto al efecto protector de los agonistas es el más frecuente, seguido del cáncer de cuello
de GnRH para la función gonadal. uterino(2).
Algunas revisiones sistemáticas y metaanálisis han Debemos resaltar la importancia del diagnóstico
demostrado una correlación entre la administración precoz y derivación oportuna de las pacientes con
de agonistas de GnRH previo y durante el tratamiento cánceres ginecológicos a centros o equipos de refe-
oncológico y una menor incidencia de insuficiencia rencia en ginecología oncológica.
ovárica prematura en las sobrevivientes. El mecanis-
Se debe pensar en estrategias de preservación de
mo de acción mediante el cual los análogos de GnRH
protegen la función ovárica aún no está claro. Es por fertilidad hormonal y cirugías oncológicas conserva-
esto que se trata de una estrategia que aún no puede doras siempre que la paciente lo desee y del punto
ser considerada estandarizada. de vista oncológico sea posible. Cuando se da esta
Igualmente, las sociedades científicas incentivan el situación es prioritario tratar la patología de base y
uso de análogos de GnRH durante los tratamientos no generar retrasos en el inicio de los tratamientos. Es
de quimioterapia siempre y cuando los pacientes por esto que la interacción entre el ginecólogo oncó-
tengan claro que se trata de una estrategia experi- logo y el especialista en oncofertilidad es importante
mental y que se hayan ofrecido también estrategias para optimizar tiempos y poder ofrecer estrategias
estandarizadas y esta sea utilizada como un com- de protección y preservación de la fertilidad a este
plemento(23). grupo de pacientes.
6 Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61
Kimelman D, Scasso S Puesta al día
Figura 2 Pasos de la traquelectomía radical vía abdominal.
A) Evaluación linfonodal (ganglio centinela + linfadenectomía pélvica), B) Parametrectomía
C) Tiempo de traquelectomía radical y tallado de la pieza, D) Estrategias de prevención de posibles
complicaciones (cerclaje cervical y cánula de drenaje), E) Anastomosis cuerpo uterino a vagina.
Cáncer de cuello uterino informadas. De esta manera, podemos evitar el
arrepentimiento posterior por haber optado por
Es un cáncer evitable en la mayoría de los casos.
Lamentablemente es el tumor ginecológico más fre- tratamientos radicales.
cuente en mujeres jóvenes. Un 30 % se diagnostican Actualmente, existen protocolos experimentales en
en mujeres menores de 40 años(2). los que se plantea la realización de un tratamiento
Actualmente, en grupos muy selectos de pacientes quimioterápico neoadyuvante para disminuir el ta-
(lesiones < 2 cm, sin invasión de espacios linfovasculares maño tumoral en tumores de cuello menores a 4 cm
y subtipos histológicos favorables) pueden plantear- confinados al cuello uterino. Esta estrategia aún se
se tratamientos quirúrgicos conservadores (cono considera experimental y todos los trabajos realizados
quirúrgico con relevo ganglionar, traquelectomía o hasta la fecha son retrospectivos.
traquelectomía radical).
El objetivo de esta terapéutica es reducir el tamaño
Debemos ser muy claros y cautos en la valoración y tumoral para poder realizar un tratamiento quirúr-
asesoramiento de cada caso y discutirlo en el comité gico conservador posterior y así poder conservar el
de tumores institucional. Se debe informar sobre la
cuerpo uterino.
seguridad oncológica demostrada y la expectativa
de un embarazo posterior. En pacientes no candidatas a cirugías preservadoras
Cuando la enfermedad se presenta en pacientes muy de fertilidad, ya sea por tamaño tumoral, estadío de la
jóvenes y las mismas solicitan tratamientos radicales, enfermedad o por el tipo histológico, podrá evaluarse
debemos tomarnos el tiempo para poder explicarles el beneficio o rol de criopreservación de ovocitos y
las distintas posibilidades y lograr que las pacientes de la transposición ovárica para conservar potencial
dimensionen la conveniencia de tomar decisiones reproductivo y hormonal(24).
Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61 7
Oncofertilidad
Cáncer de endometrio
De los cánceres ginecológicos es el tercero en fre-
cuencia en Uruguay, luego del cáncer de mama y cue-
llo uterino. Es más frecuente en países desarrollados,
con un incremento en su incidencia vinculado a
factores de riesgo como el estilo de vida sedentario,
obesidad y alimentación no saludable.
En Uruguay, su incidencia viene en aumento. Típi-
camente es una enfermedad de la posmenopausia,
pero un 25 % de las mujeres son premenopáusicas
al momento del diagnóstico y de estas un 50-70 %
son nulíparas. Este dato se vincula con la maternidad
postergada y con que muchas veces son pacientes
que tienen una esterilidad previa. Por lo tanto, los Figura 3 Gestación subrogada. Paciente con cáncer
de cuello uterino de tipo neuroendócrino,
aspectos reproductivos deben ser abordados a la
subtipo no recomendado para cirugía
hora de planificar los tratamientos de pacientes con preservadora de fertilidad. Se realizó
esta patología (25). criopreservación ovocitaria previo al
Si bien el tratamiento estándar del cáncer de endo- tratamiento quimio-radioterapéutico.
metrio es quirúrgico, existe la posibilidad de realizar
tratamiento médico con seguridad en casos selec-
cionados y lograr posponer el tratamiento quirúrgico
hasta luego de completar el embarazo. recurrir eventualmente a la subrogación uterina. La
misma está contemplada en la ley de Reproducción
Las pacientes candidatas a tratamiento médico deben
Humana Asistida de Uruguay (Ley 19.167) y actual-
cumplir con los siguientes criterios:
mente está siendo evaluado en el parlamento un
• edad menor de 40 años,
proyecto de ley que permitirá aumentar las posibi-
• mujeres con deseo de conservar la fertilidad,
• adenocarcinoma endometroide grado 1, limitado lidades de acceso a esta estrategia para pacientes
al útero, que la requieran.
• sin invasión miometrial, histológica ni imageno-
lógica, Cáncer de ovario
• ausencia de contraindicaciones para recibir trata- Las estrategias de preservación de fertilidad son un
miento hormonal, desafío cuando la enfermedad está situada en las
• posibilidad y deseo real de buscar un embarazo gónadas.
a corto plazo, En Uruguay, y según el último reporte de la Comisión
• posibilidad de seguimiento estrecho desde el Honoraria de Lucha Contra el Cáncer (CHLCC), se
punto de vista clínico. reportaron en el periodo 2012-2018 aproximada-
El tratamiento médico para estadíos iniciales de esta mente 120 casos de cáncer de ovario con una inci-
patología está dado por gestágenos. Dentro de es- dencia de 8,36/100.000 pacientes y una mortalidad
tos tratamientos, los que han demostrado mejores de 4,64/100.000 mujeres(2).
resultados y perfil de riesgo son acetato de medro- En casos de tumores Borderline, tumores estromales,
xiprogesterona, acetato de megestrol y dispositivo
germinales e incluso epiteliales en estadios iniciales
intrauterino (DIU) liberador de levonorgestrel.
podría ser posible en casos seleccionados realizar
Es muy importante la valoración paraclínica previa a tratamiento quirúrgico conservador junto a una es-
la toma de decisiones terapéuticas y la valoración en tadificación completa de la enfermedad.
conjunto por ginecólogo oncólogo y especialista en
oncofertilidad para evaluar cuáles son las posibles En casos que no sea posible preservar ovocitos y/o
estrategias terapéuticas, el seguimiento exahustivo tejido gonadal alguno, las pacientes deben ser infor-
para evaluar la respuesta al tratamiento y even- madas que si desean un embarazo posterior se puede
tualmente planificar un embarazo una vez lograda recurrir a un tratamiento de reproducción asistida con
la respuesta esperada (25). Cuando el tratamiento óvulos donados.
médico no es una posibilidad y la paciente debe En Uruguay existe cobertura para los tratamientos de
someterse a una histerectomía debemos plantear la reproducción asistida de alta complejidad con óvulos
posibilidad de la criopreservación de ovocitos para propios o donados, a través del FNR.
8 Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61
Kimelman D, Scasso S Puesta al día
Conclusiones reproductiva previo al inicio del tratamiento y se debe
ofrecer la estrategia más acertada, adecuándose a la
Existe evidencia científica contundente que ha de- patología y tipo de tratamiento que recibirá.
mostrado que el correcto asesoramiento reproduc- El trabajo interdisciplinario es clave para el ejercicio
tivo de pacientes jóvenes con reciente diagnóstico de la oncofertilidad.
de cáncer mejora la adherencia al tratamiento y la Aún existen múltiples desafíos por delante, pero sin
tolerancia al mismo. duda seguiremos avanzando para lograr la mejor ca-
Es por esto que las sociedades científicas interna- lidad de vida posible en las pacientes sobrevivientes
cionales establecen que toda paciente en edad de enfermedades oncológicas de nuestro medio.
pediátrica, adolescente o adulto joven debe ser ase-
sorado sobre la potencial pérdida de la capacidad Aprobado para publicación: 21/12/2022
Bibliografía
1. Salama, M. Sandler, V. Woodruff, T. Managing Re- for women with breast cancer: a multicentre 19. Shapira M, Dolmans MM, Silber S, Meirow D.
productive Disorders in Cancer,WilliamsTextbook randomized controlled trial on various ovar- Evaluation of ovarian tissue transplantation:
of Endocrinology, 14th Edition, ELSEVIER, 2019 ian stimulation protocols. Hum Reprod. results from three clinical centers. Fertil Steril.
2022;37(8):1786-94. 2020;114(2):388-97.
2. Registro Nacional del Cáncer CHLCC. Situación
Epidemiológica del Uruguay en relación al 11. Filippi F, Somigliana E, Busnelli A, Guarneri C, 20. Shapira M, Raanani H, Barshack I, Amariglio N,
Cáncer.2019:1-61. Noli S, et al. The presence of dominant follicles Derech-Haim S, et al. First delivery in a leukemia
3. Oktay K, Harvey E, Brittany., Patridge A, H., Quinn and corpora lutea does not perturb response to survivor after transplantation of cryopreserved
G, et al. Fertility Preservation in Patients With controlled ovarian stimulation in random start ovarian tissue, evaluated for leukemia cells
Cancer: ASCO Clinical Practice Guideline Update. protocols. Sci Rep. 2020;10(1):10083. contamination. Fertil Steril. 2018;109(1):48-53.
Journal of Clinical Oncology. 2018;36(19). 12. Dolmans MM, Demylle D, Martinez-Madrid B, 21. Diaz-Garcia C, Domingo J, Garcia-Velasco JA,
4. Meirow D, Ra’anani H, Shapira M, Brenghausen Donnez J. Efficacy of in vitro fertilization after Herraiz S, Mirabet V, et al. Oocyte vitrification
M, Derech Chaim S, et al. Transplantations of chemotherapy. Fertil Steril. 2005;83(4):897-901. versus ovarian cortex transplantation in fertil-
frozen-thawed ovarian tissue demonstrate high 13. Meirow D, Schiff E. Appraisal of chemotherapy ity preservation for adult women undergoing
reproductive performance and the need to revise effects on reproductive outcome according to gonadotoxic treatments: a prospective cohort
restrictive criteria. Fertil Steril. 2016;106(2):467- animal studies and clinical data. J Natl Cancer study. Fertil Steril. 2018;109(3):478-85 e2.
74. Inst Monogr. 2005(34):21-5. 22. Pérez H, Cóppola F, Martínez J, Alfonzo Y, Domín-
5. Klipstein S, Fallat ME, Savelli S. Fertility Pres- 14. Practice Committee of the American Society for guez A, et al. Criopreservación de corteza ovárica
ervation for Pediatric and Adolescent Patients Reproductive Medicine. Electronic address aao. en pacientes jóvenes con cáncer e indicación
With Cancer: Medical and Ethical Considerations. Fertility preservation in patients undergoing go- de tratamiento gonadotóxico. Rev Med Urug.
Pediatrics. 2020;145(3). nadotoxic therapy or gonadectomy: a committee 2007;23:99-108.
6. Practice Committees of the American Society opinion. Fertil Steril. 2019;112(6):1022-33.
23. Munhoz R, Pereira A, Sasse A, Hoff P, Traina T, et
for Reproductive M, the Society for Assisted 15. Donnez J, Dolmans MM. Fertility Preservation in al. Gonadotropin-Releasing Hormone Agonists
Reproductive T. Mature oocyte cryopreservation: Women. N Engl J Med. 2017;377(17):1657-65. for Ovarian Function Preservation in Premeno-
a guideline. Fertil Steril. 2013;99(1):37-43.
16. WallaceW, Smith A, KelseyT, Edgar A, Anderson R. pausal Women Undergoing Chemotherapy for
7. Kawwass JF, Crawford S, Hipp HS. Frozen eggs: Fertility preservation for girls and young women Early-Stage Breast Cancer: A Systematic Review
national autologous oocyte thaw outcomes. with cancer: population-based validation of and Meta-analysis. JAMA Oncol. 2016;2(1):65-
Fertil Steril. 2021;116(4):1077-84. criteria for ovarian tissue cryopreservation. The 73.
8. Lambertini M, Peccatori FA, Demeestere I, Lancet Oncology. 2014;15(10):1129-36. 24. Nezhat C, Roman RA, Rambhatla A, Nezhat F.
Amant F, Wyns C, et al. Fertility preservation and 17. Poirot C, Fortin A, Lacorte JM, Akakpo JP, Genestie Reproductive and oncologic outcomes after
post-treatment pregnancies in post-pubertal C, et al. Impact of cancer chemotherapy before fertility-sparing surgery for early stage cer-
cancer patients: ESMO Clinical Practice Guide- ovarian cortex cryopreservation on ovarian tissue vical cancer: a systematic review. Fertil Steril.
lines(dagger). Ann Oncol. 2020;31(12):1664-78. 2020;113(4):685-703.
transplantation. Hum Reprod. 2019;34(6):1083-
9. Jeruss JS, Woodruff T. Preservation of Fertility 94. 25. Greenwald Z, Huang L, Wissing M, Franco E,
in Patients with Cancer. New England Journal Gotlieb W. Does hormonal therapy for fertility
18. Demeestere I, Simon P, Dedeken L, Moffa F,
of Medicine. 2009. preservation affect the survival of young women
Tsepelidis S, et al. Live birth after autograft of
10. Balkenende EME, Dahhan T, Beerendonk CCM, ovarian tissue cryopreserved during childhood. with early-stage endometrial cancer? Cancer.
Fleischer K, Stoop D, et al. Fertility preservation Hum Reprod. 2015;30(9):2107-9. 2017;123(9):1545-54.
Tendencias en Medicina • Diciembre 2022; Año XXXI Nº 61 9
También podría gustarte
- Nutrición y cancer: Guía para la prevención y tratamiento del cancer (2ª edición)De EverandNutrición y cancer: Guía para la prevención y tratamiento del cancer (2ª edición)Calificación: 3.5 de 5 estrellas3.5/5 (3)
- Propuesta Tratamiento Del CancerDocumento29 páginasPropuesta Tratamiento Del Cancerlaprad1Aún no hay calificaciones
- Cáncer de Próstata y Cáncer de TestículoDocumento14 páginasCáncer de Próstata y Cáncer de TestículoCamilo VidalAún no hay calificaciones
- Tuve Cáncer de mama con invasión a pulmón y ... ¡Estoy Sana!: Experiencia de vida de una guerreraDe EverandTuve Cáncer de mama con invasión a pulmón y ... ¡Estoy Sana!: Experiencia de vida de una guerreraAún no hay calificaciones
- La importancia de la nutrición en el paciente oncológicoDe EverandLa importancia de la nutrición en el paciente oncológicoAún no hay calificaciones
- Fundamentos del diagnóstico y tratamiento del cáncer en adultos: Una aproximación inicial para el médico no especialista en cáncerDe EverandFundamentos del diagnóstico y tratamiento del cáncer en adultos: Una aproximación inicial para el médico no especialista en cáncerAún no hay calificaciones
- Métodos AnticonceptivosDocumento14 páginasMétodos AnticonceptivosmarthaAún no hay calificaciones
- Cuidando a tus seres queridos con cáncer - Como sobrellevar esta enfermedad, tratamientos, terapias, alternativas y ejercicios contra el cáncer - Parte 2: Cuidando a tus seres queridos con cáncer, #2De EverandCuidando a tus seres queridos con cáncer - Como sobrellevar esta enfermedad, tratamientos, terapias, alternativas y ejercicios contra el cáncer - Parte 2: Cuidando a tus seres queridos con cáncer, #2Calificación: 5 de 5 estrellas5/5 (1)
- CaquexiaDocumento6 páginasCaquexiaMartin GonzalezAún no hay calificaciones
- RÚBRICA 1 MT Laura Silva TovarDocumento5 páginasRÚBRICA 1 MT Laura Silva TovarLaura Silva TovarAún no hay calificaciones
- Cardiopatías y SexualidadDocumento4 páginasCardiopatías y SexualidadMartin GonzalezAún no hay calificaciones
- Rubrica MTDocumento3 páginasRubrica MTjuliana blancoAún no hay calificaciones
- JimenezDocumento19 páginasJimenezGREVILLI MARLITT GARCÍA GODOS CASTILLOAún no hay calificaciones
- UntitledDocumento15 páginasUntitledAnahi PoalacinAún no hay calificaciones
- Trabajo Anual Integrador PsicooncologiaDocumento60 páginasTrabajo Anual Integrador Psicooncologiapaula tejadaAún no hay calificaciones
- Diagnóstico Molecular Del Cáncer de Mama: Implicaciones Pronósticas y TerapéuticasDocumento13 páginasDiagnóstico Molecular Del Cáncer de Mama: Implicaciones Pronósticas y TerapéuticasCristóbal Díaz De LeónAún no hay calificaciones
- BASES ONCOLOGICAS QX de La Torre BahenaDocumento5 páginasBASES ONCOLOGICAS QX de La Torre BahenaDavid Atzin Dela Torre BahenaAún no hay calificaciones
- Cancer de MamaDocumento12 páginasCancer de MamaaxeljosefatdesantiagogonzalezAún no hay calificaciones
- Cirugía Oncológica 9ADocumento30 páginasCirugía Oncológica 9AAngel OntiverosAún no hay calificaciones
- Informe 1Documento20 páginasInforme 1libiaaguilar21Aún no hay calificaciones
- Preservación Médica de La FertilidadDocumento19 páginasPreservación Médica de La FertilidadPablo Loste RamosAún no hay calificaciones
- Oncoguía de Cáncer de Ovario 2020Documento17 páginasOncoguía de Cáncer de Ovario 2020Aldair SanchezAún no hay calificaciones
- To en Oncología PediátricaDocumento21 páginasTo en Oncología PediátricaEva ColomoAún no hay calificaciones
- Eficacia de La Musicoterapia 4Documento52 páginasEficacia de La Musicoterapia 4DENISE DARLETH SOSA TOVARAún no hay calificaciones
- Qué Es La Fase Terminal de Un CáncerDocumento21 páginasQué Es La Fase Terminal de Un CáncerErick FslAún no hay calificaciones
- Oncoguía de Cáncer de Endometrio 2023Documento12 páginasOncoguía de Cáncer de Endometrio 2023Aldair SanchezAún no hay calificaciones
- TesisDocumento23 páginasTesisAbdil ChangirAún no hay calificaciones
- Ref. Caracterizacion de Cancer de OvarioDocumento12 páginasRef. Caracterizacion de Cancer de OvarioMericia Guadalupe Sandoval ChavezAún no hay calificaciones
- Cancer MamarioDocumento7 páginasCancer MamarioPablo VidalAún no hay calificaciones
- Oncologia PediatricaDocumento10 páginasOncologia Pediatricaapi-286186921Aún no hay calificaciones
- Introducción Oncológia Pediátrica 2022Documento23 páginasIntroducción Oncológia Pediátrica 2022Talía TalíaAún no hay calificaciones
- Nápoles GonzálezDocumento15 páginasNápoles Gonzálezgatitamich502Aún no hay calificaciones
- Revista Peruana de Oncología Médica - Volumen 7 #02 2008Documento23 páginasRevista Peruana de Oncología Médica - Volumen 7 #02 2008spomedicaAún no hay calificaciones
- El CancerDocumento86 páginasEl CancerBelexx VCAún no hay calificaciones
- Work Cancer TrabajoDocumento28 páginasWork Cancer Trabajojuvenal7271Aún no hay calificaciones
- Resumen Ninoska FernándezDocumento14 páginasResumen Ninoska FernándezNinoska FernandezAún no hay calificaciones
- Fic Manual - Modulo 3 1 5Documento5 páginasFic Manual - Modulo 3 1 5MaríaAún no hay calificaciones
- Actualizacion Consenso FASGO 2018 Preservacion de La FertilidadDocumento40 páginasActualizacion Consenso FASGO 2018 Preservacion de La Fertilidadmaidecuzzi743Aún no hay calificaciones
- LAROTRECTINIBDocumento6 páginasLAROTRECTINIBsergioAún no hay calificaciones
- Introduccion de Factores de La Metastasis...Documento8 páginasIntroduccion de Factores de La Metastasis...Stefano LetelierAún no hay calificaciones
- Oncología GeriátricaDocumento11 páginasOncología GeriátricaFrancisco MartinezAún no hay calificaciones
- Vgi PDFDocumento10 páginasVgi PDFCatalina KAún no hay calificaciones
- Pdfcompilado Vol 5 N2.pdf#page 31Documento52 páginasPdfcompilado Vol 5 N2.pdf#page 31Lola RodríguezAún no hay calificaciones
- Protocolo SarcomasDocumento5 páginasProtocolo SarcomasOmar Rosales TiconaAún no hay calificaciones
- Ec2 26825326Documento10 páginasEc2 26825326Orianna CabelloAún no hay calificaciones
- Prevalencia y Sobrevida en Tumores NeuroendocrinosDocumento10 páginasPrevalencia y Sobrevida en Tumores NeuroendocrinosFreya Esthetic and HealthAún no hay calificaciones
- Tratamiento MiomasDocumento7 páginasTratamiento MiomasDiegoyKattyAún no hay calificaciones
- RF Articulo 141Documento8 páginasRF Articulo 141MSAún no hay calificaciones
- Cancer y Reproducción SEFDocumento21 páginasCancer y Reproducción SEFSalome Adame GuisadoAún no hay calificaciones
- Primer Consenso Nacional de Cáncer Epitelial de Ovario Diagnóstico y Tratamiento - Venezuela 2014Documento58 páginasPrimer Consenso Nacional de Cáncer Epitelial de Ovario Diagnóstico y Tratamiento - Venezuela 2014Yoleisy BruceAún no hay calificaciones
- Diagnostico CitoDocumento5 páginasDiagnostico CitoMarylin Andrea FernándezAún no hay calificaciones
- Unidad - 6 Qué Hay Después de Finalizar El Tratamiento Del Cáncer en La InfanciaDocumento15 páginasUnidad - 6 Qué Hay Después de Finalizar El Tratamiento Del Cáncer en La InfanciaJuan Acevedo VegaAún no hay calificaciones
- 2V2N2 RODRIGUEZ MONTES Cancer ColorrectalDocumento14 páginas2V2N2 RODRIGUEZ MONTES Cancer ColorrectalCesar LlanesAún no hay calificaciones
- Cancer de MamaDocumento16 páginasCancer de MamaWilmer J. Tovar100% (1)
- Cáncer de TiroidesDocumento14 páginasCáncer de TiroidespaulinamargaritahmAún no hay calificaciones
- Plan de Cuidados CancerDocumento46 páginasPlan de Cuidados CancerRosa Villafranca VelasquezAún no hay calificaciones
- 30 Rivera Maria PAE PDFDocumento14 páginas30 Rivera Maria PAE PDFAlejandrina RiveraAún no hay calificaciones
- Manejo Anestesico Del Paciente OncologicoDocumento96 páginasManejo Anestesico Del Paciente OncologicoMiguel Angel Romero GaonaAún no hay calificaciones
- Cáncer de Mama - WORDDocumento3 páginasCáncer de Mama - WORDGabriela RMAún no hay calificaciones
- RESUMEN (Recuperado Automáticamente)Documento21 páginasRESUMEN (Recuperado Automáticamente)chmildreth109Aún no hay calificaciones
- Modulo 7 Proyecto FinalDocumento15 páginasModulo 7 Proyecto FinalYasmary GonzalezAún no hay calificaciones
- 5.C.ANTICONCEPCION EN HTA-DM-DLP-ObesidadDocumento32 páginas5.C.ANTICONCEPCION EN HTA-DM-DLP-ObesidadNayadet MenesesAún no hay calificaciones
- Resistencia A Los AntimicrobianosDocumento6 páginasResistencia A Los AntimicrobianosMartin GonzalezAún no hay calificaciones
- Tratamiento de Metastasis EncefalicasDocumento8 páginasTratamiento de Metastasis EncefalicasMartin GonzalezAún no hay calificaciones
- Infecciones Urinarias FemeninasDocumento10 páginasInfecciones Urinarias FemeninasMartin GonzalezAún no hay calificaciones
- Uso de Cama SolarDocumento4 páginasUso de Cama SolarMartin GonzalezAún no hay calificaciones
- X Jornadas de Novedades TerapéuticasDocumento3 páginasX Jornadas de Novedades TerapéuticasMartin GonzalezAún no hay calificaciones
- MSP Guia Uso Sedoanalgesia OdontologiaDocumento20 páginasMSP Guia Uso Sedoanalgesia OdontologiaMartin GonzalezAún no hay calificaciones
- Diabetes Tipo II y FarmacologíaDocumento7 páginasDiabetes Tipo II y FarmacologíaMartin GonzalezAún no hay calificaciones
- La Importancia Del AguaDocumento6 páginasLa Importancia Del AguaMartin GonzalezAún no hay calificaciones
- ¿Cómo Debe Avanzar El Conocimiento Médico?Documento3 páginas¿Cómo Debe Avanzar El Conocimiento Médico?Martin GonzalezAún no hay calificaciones
- Cannabis Medicinal y EpilepsiaDocumento3 páginasCannabis Medicinal y EpilepsiaMartin GonzalezAún no hay calificaciones
- Muerte Súbita en El DeportistaDocumento5 páginasMuerte Súbita en El DeportistaMartin GonzalezAún no hay calificaciones
- 04 Ciclo Ovarico y TubaricoDocumento39 páginas04 Ciclo Ovarico y TubaricoskarlettAún no hay calificaciones
- Guía Práctica 17 Herencia Ligada Al Sexo y Genealogías. Razas PDFDocumento16 páginasGuía Práctica 17 Herencia Ligada Al Sexo y Genealogías. Razas PDFQuimica TecnologiaAún no hay calificaciones
- Guía Nº3 Repaso Reproducción en Los Seres VivosDocumento2 páginasGuía Nº3 Repaso Reproducción en Los Seres VivosCarlos LuboAún no hay calificaciones
- SexualidadDocumento12 páginasSexualidadDaniela Paniagua CastellonAún no hay calificaciones
- Reproducción SESIONDocumento3 páginasReproducción SESIONNico Ch100% (1)
- Ciclo Menstrual y OvaricoDocumento10 páginasCiclo Menstrual y Ovariconarcisa zambranoAún no hay calificaciones
- 14 PPT Etapas o Edades Del Desarrollo Humano IiiDocumento21 páginas14 PPT Etapas o Edades Del Desarrollo Humano IiipedrodiegocpAún no hay calificaciones
- Embarazo EctopicoDocumento37 páginasEmbarazo EctopicoEduardo OrtizAún no hay calificaciones
- Anatomia 2 PelvicaDocumento48 páginasAnatomia 2 PelvicaanyAún no hay calificaciones
- 2° Cuatrimestrs TP 8 Sistema Reproductor FemeninoDocumento4 páginas2° Cuatrimestrs TP 8 Sistema Reproductor FemeninoOscar MendozaAún no hay calificaciones
- BIENVENIDA A TU CICLICIDAD. Woman RootsDocumento2 páginasBIENVENIDA A TU CICLICIDAD. Woman RootsBeatriz MedinaAún no hay calificaciones
- Padlet 2pr5eeazh912iparDocumento10 páginasPadlet 2pr5eeazh912iparMine RGAún no hay calificaciones
- Aparato ReproductorDocumento7 páginasAparato ReproductorJavier LincopánAún no hay calificaciones
- Ginecologia 1er Parcial.Documento176 páginasGinecologia 1er Parcial.Sergio David Vargas ChoqueticllaAún no hay calificaciones
- Docsity Aparato Reproductor ApuntesDocumento25 páginasDocsity Aparato Reproductor ApuntesNancyAún no hay calificaciones
- EmbriologiaDocumento40 páginasEmbriologiakine 201750% (2)
- Grado 9Documento18 páginasGrado 9Portal 3D El CopeyAún no hay calificaciones
- Manejo y Reproducción de Cuyes 2016-IDocumento57 páginasManejo y Reproducción de Cuyes 2016-Iwilder luisAún no hay calificaciones
- Definitivoformato Programa Sintético-Esm - Enero 2022Documento21 páginasDefinitivoformato Programa Sintético-Esm - Enero 2022Arturo MendozaAún no hay calificaciones
- Dónde Viven Los AnimalesDocumento8 páginasDónde Viven Los AnimalesbrendaAún no hay calificaciones
- Folleto Tríptico Clinica Embarazadas BienestarDocumento2 páginasFolleto Tríptico Clinica Embarazadas Bienestarjoce eliana almanza yucraAún no hay calificaciones
- Laboratorio de Reproducion Asistida PDFDocumento133 páginasLaboratorio de Reproducion Asistida PDFGUIDO ERNESTO VILLOTA CALVACHIAún no hay calificaciones
- Reproduccion CelularDocumento27 páginasReproduccion CelularVicky Jimenez100% (1)
- Establecimiento Upgf - NMX Aa 169 Scfi 2014 - 17 07 14Documento126 páginasEstablecimiento Upgf - NMX Aa 169 Scfi 2014 - 17 07 14EdgarAún no hay calificaciones
- Clase 2 - 27 Agosto - Anatomia HembraDocumento31 páginasClase 2 - 27 Agosto - Anatomia HembraMATIAS ALEJANDRO BECERRA SANTANDERAún no hay calificaciones
- Frutos - 1Documento2 páginasFrutos - 1Henrry Ávila OrtegaAún no hay calificaciones
- Guía 5 - Grado Octavo 2015 - 2015 - Reproducción Sexual y AsexualDocumento5 páginasGuía 5 - Grado Octavo 2015 - 2015 - Reproducción Sexual y Asexualantonia estefania coral yepezAún no hay calificaciones
- INDICADORESDocumento8 páginasINDICADORESMilene Jahayra Galvez SanchezAún no hay calificaciones
- RMC 162 TDocumento7 páginasRMC 162 TCielo Gómez BriceñoAún no hay calificaciones
- Trabajo de PartoDocumento6 páginasTrabajo de PartoAntonio AvellaAún no hay calificaciones