Documentos de Académico
Documentos de Profesional
Documentos de Cultura
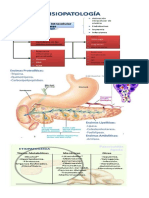
CETOACIDOSIS DIABETICA Acidosis Metabólica
Cargado por
Teresa Dávila EspinosaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
CETOACIDOSIS DIABETICA Acidosis Metabólica
Cargado por
Teresa Dávila EspinosaCopyright:
Formatos disponibles
Acidosis metabólica
Por James L. Lewis, III, MD, Attending Physician, Brookwood Baptist Health and Saint Vincent’s Ascension Health, Birmingham
Regulación y trastornos del equilibrio ácido base
Regulación del equilibrio ácido base
Trastornos del equilibrio ácido base
Acidosis metabólica
Alcalosis metabólica
Acidosis respiratoria
Alcalosis respiratoria
La acidosis metabólica es la reducción primaria de la concentración de bicarbonato (HCO 3−), típicamente con descenso compensador de la presión
parcial de dióxido de carbono (PCO2); el pH puede ser muy bajo o solo algo inferior al valor normal. La acidosis metabólica se clasifica como con
brecha aniónica normal o elevada de acuerdo con la presencia o la ausencia de aniones no medidos en el suero. Sus causas son la acumulación de
cetonas y ácido láctico, la insuficiencia renal y la ingestión de fármacos o toxinas (brecha aniónica elevada) y la pérdida de HCO 3− por el tubo
digestivo o el riñón (brecha aniónica normal). En los casos graves, los signos y los síntomas consisten en náuseas y vómitos, letargo e hiperpnea.
El diagnóstico es clínico y también requiere la medición de los gases en sangre arterial y la concentración sérica de electrolitos. La causa debe
tratarse y puede indicarse la infusión intravenosa de NaHCO3 si el pH es muy bajo.
(Véase también Regulación del equilibrio ácido-base y Trastornos del equilibrio ácido-base).
ACIDOSIS METABOLICA
Introducción a la acidosis metabólica
Etiología
La acidosis metabólica es la acumulación de ácido debido a
Aumento de la producción de ácido o ingestión de ácido
Disminución de la excreción de ácido
Pérdidas gastrointestinales o renales de HCO3−
Se desarrolla acidemia (pH arterial 7,35) cuando la sobrecarga de ácido supera la compensación respiratoria. Las causas se clasifican según su
efecto sobre la brecha aniónica (ver Brecha aniónica y ver Causas de acidosis metabólica).
Calculadora clínica: Brecha aniónica
Acidosis con brecha aniónica elevada
Las causas más frecuentes de acidosis metabólica con brecha aniónica elevada son
Cetoacidosis
Acidosis láctica
Insuficiencia renal
Intoxicaciones
La cetoacidosis es una complicación frecuente de la diabetes mellitus tipo 1 (vease cetoacidosis diabética), pero también puede asociarse con
alcoholismo crónico (véase cetoacidosis alcohólica), con desnutrición y, en menor medida, con ayuno. En estas condiciones, el cuerpo desvía la
glucosa hacia el metabolismo de los ácidos grasos libres, a través del cual estos ácidos grasos se convierten en cetoácidos, ácido acetoacético y
beta-hidroxibutirato en el hígado (todos aniones no medidos). La cetoacidosis también es una manifestación poco frecuente de la acidemia
isovalérica y metilmalónica congénita.
La acidosis láctica es la causa más frecuente de acidosis metabólica en pacientes hospitalizados. La acumulación de lactato es el resultado de una
combinación de formación excesiva y disminución del uso del lactato. Cuando predomina el metabolismo anaeróbico, se produce una cantidad
excesiva de lactato. La forma más grave se identifica durante los diversos tipos de shock. El aumento de la utilización suele identificarse en
pacientes con disfunción hepatocelular causada por hipoperfusión hepática o como parte de un shock generalizado. Las enfermedades y los
fármacos que alteran la función mitocondrial pueden causar acidosis láctica.
La insuficiencia renal causa acidosis con brecha aniónica debido a la reducción de la excreción de ácido y la reabsorción de HCO 3− . La
acumulación de sulfatos, fosfatos, uratos e hipuratos es responsable del aumento de la brecha aniónica.
Las toxinas pueden tener metabolitos ácidos o generar acidosis láctica. La rabdomiólisis es una causa infrecuente de acidosis metabólica que se
considera secundaria a la liberación de protones y aniones del músculo en forma directa.
Causas de acidosis metabólica
Causa Ejemplos
Brecha aniónica elevada
Cetoacidosis Diabetes
Alcoholismo crónico
Desnutrición
Ayuno
Acidosis láctica (secundaria a procesos fisiológicos) Shock
Hipoxia primaria debido a enfermedades pulmonares
Convulsiones
Alcohol (abuso crónico)
Acidosis láctica (secundaria a toxinas exógenas) Monóxido de carbono
Cianuro
Hierro
Isoniacida
Tolueno (en un principio, brecha aniónica elevada; luego, la excreción de los
metabolitos normaliza la brecha)
Inhibidores nucleósidos de la transcriptasa reversa del HIV
Biguanidas (raro salvo con lesión renal aguda)
Propofol
generación de D-lactato Sobrecrecimiento bacteriano/síndrome de intestino corto
Insuficiencia renal —
Toxinas metabolizadas en ácidos Metanol (formato)
Etilenglicol (oxalato)
Paraldehído (acetato, cloracetato)
Salicilatos
Rabdomiólisis —
Brecha aniónica normal (acidosis hiperclorémica)
Pérdida GI de bicarbonato (HCO3−) Colostomía
Diarrea
Fístulas entéricas
Ileostomía
Uso de resinas de intercambio iónico
Cloruro de calcio (CaCl2)
Sulfato de magnesio (MgSO4)
Procedimientos urológicos Ureterosigmoidostomía
Conducto ureteroileal
Pérdida renal de HCO3− Nefropatía tubulointersticial
Acidosis tubular renal tipos 1, 2 y 4
Hiperparatiroidismo
Acetazolamida
Infusión parenteral Arginina
Lisina
Cloruro de amonio (NH4Cl)
Infusión rápida de cloruro de sodio (NaCl)
Otras Hipoaldosteronismo
Hiperpotasemia
Tolueno (tardío)
Acidosis con brecha aniónica normal
Las causas más frecuentes de acidosis con brecha aniónica normal son
Pérdidas gastrointestinales o renales de HCO3−
Compromiso de la excreción renal de ácido
La acidosis metabólica con brecha aniónica normal también se denomina acidosis hiperclorémica, porque los riñones reabsorben cloruro (Cl −) en
lugar de HCO3−.
Muchas secreciones gastrointestinales tienen abundante cantidad de HCO 3− (p. ej., jugos biliar, pancreático e intestinal), y las pérdidas causadas
por diarrea, drenaje a través de sonda o fístulas pueden causar acidosis. En los pacientes sometidos a ureterosigmoidostomía (inserción de los
uréteres en el colon sigmoides después de una obstrucción o una cistectomía), el colon secreta y pierde HCO 3−, que intercambia por el Cl− urinario,
y absorbe el amonio urinario, que se disocia en amoníaco (NH 3+) y ion hidrógeno (H+). Rara vez, las resinas de intercambio iónico aumentan la
pérdida de HCO3− al unirse a este anión HCO3−.
La acidosis tubular renal compromete la secreción de H+ (tipos 1 y 4) o la absorción de HCO3− (tipo 2). El compromiso en la excreción de ácido con
brecha aniónica normal también se observa en la insuficiencia renal temprana, la nefropatía tubulointersticial y en individuos que consumen
inhibidores de la anhidrasa carbónica (p. ej., acetazolamida).
Signos y síntomas
Los signos y los síntomas (ver Consecuencias clínicas de los trastornos del equilibrio ácido base) son, predominantemente, los ocasionados por la
causa. La acidemia leve no produce síntomas por sí misma. La acidemia más grave (pH 7,1) puede provocar náuseas, vómitos y malestar general.
Los síntomas pueden desarrollarse con pH más altos si la acidosis evoluciona rápidamente.
El signo más característico es la hiperpnea (respiraciones profundas y prolongadas con frecuencia normal), que refleja un aumento compensador
de la ventilación alveolar; esta hiperpnea no se acompaña de sensación de disnea.
Perlas Y Errores
•La hiperpnea inducida por la acidosis metabólica no causa una sensación de disnea. La acidemia aguda grave predispone al desarrollo de
disfunción cardíaca con hipotensión arterial y shock, arritmias ventriculares y coma. La acidemia crónica causa desmineralización ósea (p. ej.,
raquitismo, osteomalacia, osteopenia).
Calculadora clínica: Interpretation TreeCalc de gases en sangre arterial
Diagnóstico
Gases en sangre arterial y concentraciones séricas de electrolitos
Brecha aniónica y brecha delta calculada
Fórmula de Winter para identificar los cambios compensadores
Estudios complementarios para investigar la causa
La identificación de la acidosis metabólica y de la compensación respiratoria apropiada se analizan en Trastornos del equilibrio ácido base :
Diagnóstico. La definición de la causa de la acidosis metabólica comienza con la brecha aniónica.
La causa de la brecha aniónica elevada puede evidenciarse en la evaluación clínica (p. ej., shock hipovolémico, necesidad de hemodiálisis), pero, si
no se detecta, las pruebas en sangre deben incluir glucemia, nitrógeno ureico en sangre, creatinina, lactato y búsqueda de posibles toxinas. La
mayoría de los laboratorios pueden medir las concentraciones de salicilato, pero con frecuencia no es posible la medición de las concentraciones de
metanol y etilenglicol, cuya presencia puede sospecharse en caso de observarse una brecha osmolar. Debe calcularse la osmolaridad medida
menos la osmolaridad sérica calculada (2 [sodio] + [glucosa]/18 + BUN/2,8 + alcoholemia/5). Una diferencia > 10 implica la presencia de una
sustancia osmóticamente activa, en cuyo caso la acidosis con brecha aniónica elevada debe ser secundaria a metanol o etilenglicol. Aunque la
ingestión de etanol puede causar una brecha osmolar con acidosis leve, nunca debe considerarse que puede ser la causa de una acidosis
metabólica significativa.
Si la brecha aniónica es normal y no se identifica la causa (p. ej., diarrea intensa), deben medirse las concentraciones urinarias de electrolitos y
calcular la brecha aniónica urinaria con la siguiente fórmula: [sodio] + [potasio] – [cloruro]. La brecha aniónica urinaria normal (incluso en pacientes
con pérdidas a través del tubo digestivo) oscila entre 30 y 50 mEq/L; el aumento por encima de este valor sugiere una pérdida renal de HCO 3− (para
la evaluación de la acidosis tubular renal, ver Acidosis tubular renal : Diagnóstico).
Además, en presencia de acidosis metabólica, debe calcularse la brecha delta (ver Brecha aniónica) con el fin de identificar una alcalosis
metabólica concomitante, y la fórmula de Winter (ver Diagnóstico) se aplica para determinar si la compensación respiratoria es apropiada o refleja
un desequilibrio ácido-base secundario.
Calculadora clínica: Fórmula de Winter para la PCO2 esperada
Calculadora clínica: Brecha aniónica urinaria
Tratamiento
Tratamiento de la causa
Bicarbonato de sodio (NaHCO3) principalmente para la acidemia grave, administrar con precaución
El tratamiento está destinado a la causa subyacente. Los pacientes con insuficiencia renal requieren hemodiálisis, que en ocasiones también se
utiliza para los individuos con intoxicación por etilenglicol, metanol y salicilato.
El tratamiento de la acidemia con NaHCO3 sólo debe indicarse en algunas circunstancias y es probable que sea nocivo en otras. Cuando la acidosis
metabólica es secundaria a la pérdida de HCO 3− o a la acumulación de ácidos inorgánicos (o sea, acidosis con brecha aniónica normal), el
tratamiento con HCO3− suele ser seguro y apropiado. No obstante, cuando la acidosis se debe a la acumulación de ácidos orgánicos (acidosis con
brecha aniónica elevada), el tratamiento con HCO3− es controvertido, dado que no disminuye significativamente la tasa de mortalidad en estas
condiciones y puede asociarse con algunos riesgos.
Una vez tratado el trastorno subyacente, el lactato y los cetoácidos se metabolizan otra vez a HCO 3−, por lo cual la administración de
HCO3− exógeno puede provocar una alcalosis metabólica por “tratamiento excesivo”. En todas las situaciones, el HCO 3− también puede producir
sobrecarga de sodio y volumen, hipopotasemia e hipercapnia, esta última a través de la inhibición del estímulo respiratorio. Asimismo, dado que el
HCO3− no difunde a través de las membranas celulares, la acidosis intracelular no se corrige y puede empeorar paradójicamente porque parte del
HCO3− agregado se convierte en dióxido de carbono (CO2), que no ingresa en la célula y se hidroliza a H+ y HCO3−.
A pesar de estas y otras controversias, la mayoría de los expertos aún recomiendan la administración intravenosa de HCO 3− en la acidosis
metabólica grave (pH 7,1). H .
El tratamiento requiere 2 cálculos. El primero es el nivel hasta el cual debe elevarse la concentración de HCO 3−, que se determina con la ecuación
de Kassirer-Bleich y produce un valor de [H+] de 63 nmol/L, que corresponde a un pH de 7,2 (el objetivo para la acidosis con brecha aniónica
elevada es [H+] de 79 nmol/L, pH ≤ 7,1):
63 = 24 × PCO2/HCO3− o HCO3− deseado = 0,38 × PCO2
La cantidad de HCO3− necesaria para alcanzar este nivel es
NaHCO3 necesario (mEq) = ([HCO3− deseado] − [HCO3−] observado) × 0,4 × peso corporal (kg)
Esta cantidad de NaHCO3 debe administrarse durante varias horas. El pH sanguíneo y las concentraciones de HCO 3− pueden controlarse entre 30
minutos y 1 hora después de la administración, en espera de que se alcance el equilibrio con el HCO 3− extravascular.
Las alternativas al NaHCO3 son
Trometamina, un aminoalcohol que amortigua tanto los ácidos metabólicos (H +) como los respiratorios (ácido carbónico [H2CO3])
Carbicarb, una mezcla equimolar de NaHCO3 y carbonato (el último consume CO2 y genera HCO3−)
Dicloroacetato, que estimula la oxidación del lactato
Ninguna de estas alternativas produjo un beneficio documentado sobre el NAHCO 3 y pueden causar complicaciones.
La depleción de K+ , frecuente en la acidosis metabólica, debe identificarse mediante controles frecuentes de la concentración sérica de K + y debe
tratarse según sea necesario con cloruro de potasio por vía oral o parenteral.
Conceptos clave
La acidosis metabólica puede estar causada por la acumulación de ácido debido al aumento de la producción o la ingestión de ácido, la
disminución de la excreción de ácido o la pérdida de HCO 3− por vía gastrointestinal o renal.
Las acidosis metabólicas se clasifican en función de si la brecha aniónica es alta o normal.
Las brechas aniónicas altas se deben con mayor frecuencia a la cetoacidosis, la acidosis láctica, la insuficiencia renal, o ciertas
ingestiones tóxicas
Las acidosis con brecha aniónica normal se deben más a menudo a pérdidas renales o gastrointestinales de HCO 3− .
Debe calcularse la brecha delta con el fin de identificar una alcalosis metabólica concomitante, y aplicar la fórmula de Winter para
determinar si la compensación respiratoria es apropiada o refleja un desequilibrio ácido base secundario.
Tratar la causa subyacente
Se indica NaHCO3 cuando la acidosis se debe a un cambio en el HCO3− (acidosis con brecha aniónica normal )
La administración ntravenosa de NaHCO3 es objeto de controversia en la acidosis con brecha aniónica elevada (pero puede ser
considerada cuando el pH 7, con un pH objetivo ≤ 7,1).
ACIDOSIS LÁCTICA
La acidosis láctica es una acidosis metabólica con brecha aniónica elevada debido a un aumento del lactato en sangre. La acidosis láctica se
produce como resultado de una hiperproducción de lactato o una disminución del metabolismo del lactato.
(Véase también Regulación del equilibrio ácido-base y Trastornos del equilibrio ácido-base).
El lactato es un subproducto normal del metabolismo de la glucosa y los aminoácidos. Hay 2 tipos principales de acidosis láctica
Acidosis láctica tipo A
Acidosis láctica tipo B
La acidosis láctica tipo RE es un tipo inusual.
Acidosis láctica tipo A
La acidosis láctica tipo A, la forma más grave, aparece cuando se sintetiza una cantidad excesiva de ácido láctico en el tejido isquémico para
generar ATP durante un episodio de deficiencia de O2. La hiperproducción de lactato se identifica típicamente en pacientes con hipoperfusión
asociada con shock hipovolémico, cardíaco o séptico y se agrava a medida que empieza a disminuir el metabolismo del lactato en el hígado poco
perfundido. También puede detectarse en caso de hipoxia primaria generada por una enfermedad pulmonar y asociada con hemoglobinopatías.
Acidosis láctica tipo B
La acidosis láctica tipo B aparece en individuos con perfusión tisular global normal (y, por ende, con producción normal de ATP) y es menos
ominosa. La producción de lactato puede aumentar en presencia de hipoxia local relativa, como durante el esfuerzo muscular intenso (p. ej.,
ejercicio, convulsiones, temblores por hipotermia), en pacientes con cáncer y tras la ingestión de algunos fármacos o toxinas (ver Causas de
acidosis metabólica). Los medicamentos incluyen los inhibidores de la transcriptasa inversa nucleósidos y las biguanidas fenformina y, en menor
medida, metformina; aunque fenformina ha sido retirada del mercado en la mayor parte de los países del mundo, todavía está disponible en China
(como componente de algunos medicamentos con patente china). El metabolismo puede disminuir en presencia de una insuficiencia hepática o una
deficiencia de tiamina.
Acidosis láctica tipo D
La acidosis por ácido D-láctico es una forma inusual de acidosis láctica que se caracteriza por la absorción sistémica del ácido D-láctico, producto
del metabolismo de los hidratos de carbono en las bacterias del colon en pacientes sometidos a derivación yeyunoileal o resección intestinal. Este
compuesto persiste en la circulación porque la lactato deshidrogenasa humana sólo puede metabolizar el L-lactato.
Signos y síntomas
Los signos y los síntomas corresponden a los del trastorno de base (p. ej., shock séptico, ingestión de toxinas).
Diagnóstico
Gases en sangre arterial y concentraciones séricas de electrolitos
Brecha aniónica y brecha delta calculada
Nivel de lactato en sangre
Los hallazgos en la acidosis láctica tipos A y B son los mismos que para otras acidosis metabólicas. El diagnóstico requiere un pH arterial < 7,35 y
lactato > 5 a 6 mmol/L. Los cambios de lactato y pH menos extremos se conocen como hiperlactatemia.
En la acidosis D-láctica, la brecha aniónica es menor que la esperada para la disminución de la concentración de bicarbonato (HCO 3−) y puede
detectarse una brecha osmolar urinaria (diferencia entre la osmolaridad urinaria calculada y la medida). Las pruebas típicas de laboratorio para
medir el lactato no son sensibles al D-lactato. Se pueden evaluar los niveles específicos de Dlactato y a veces son necesarios para aclarar la causa
de la acidosis en pacientes con múltiples causas potenciales, incluyendo problemas intestinales.
Tratamiento
Tratamiento de la causa
El tratamiento de la acidosis láctica tipos A y B es el mismo que para las otras acidosis metabólicas. El tratamiento de la causa es de suma
importancia. El bicarbonato es potencialmente peligroso en la acidosis con brecha aniónica alta, pero puede ser considerado cuando el pH <7, con
un pH objetivo ≤ 7,1.
En la acidosis láctica tipo D, el tratamiento se realiza con líquidos por vía intravenosa, restricción de hidratos de carbono y, en ocasiones,
antibióticos por vía oral (p. ej., metronidazol)
También podría gustarte
- Materias PrimasDocumento8 páginasMaterias Primasmorris mendez89% (19)
- Acidosis metabólica: clasificación y causas principalesDocumento8 páginasAcidosis metabólica: clasificación y causas principalesJuliana CarrilloAún no hay calificaciones
- Acidosis Metabólica - Trastornos Endocrinos y Metabólicos - Manual MSD Versión para ProfesionalesDocumento10 páginasAcidosis Metabólica - Trastornos Endocrinos y Metabólicos - Manual MSD Versión para ProfesionalesMaria Sulbarán QuinteroAún no hay calificaciones
- AcidobaseDocumento63 páginasAcidobaseDavid Vanegas100% (1)
- ACIDOSIS y ALCALOSIS METABOLICADocumento9 páginasACIDOSIS y ALCALOSIS METABOLICAManuel Álvarez GonzálezAún no hay calificaciones
- Acidosis Metabolica BorradorDocumento7 páginasAcidosis Metabolica BorradorEnma GómezAún no hay calificaciones
- Acidosis Metabólica TóxicaDocumento3 páginasAcidosis Metabólica TóxicaGonzalo FernandezAún no hay calificaciones
- Acidosis metabólica: causas y clasificaciónDocumento4 páginasAcidosis metabólica: causas y clasificaciónAndrés Santa Cruz EspinozaAún no hay calificaciones
- Farma Equipo17 DiureticosDocumento80 páginasFarma Equipo17 DiureticosAdairon Luvanor SuárezAún no hay calificaciones
- Acido - BaseDocumento35 páginasAcido - BaseKristel SarmientoAún no hay calificaciones
- Acidosis metabólica: causas y clasificaciónDocumento40 páginasAcidosis metabólica: causas y clasificaciónClaudia AlessandraAún no hay calificaciones
- 4938db77 827a 4220 887c d430bbd74569 Desequilibrio Acido Base Zamná 2021Documento3 páginas4938db77 827a 4220 887c d430bbd74569 Desequilibrio Acido Base Zamná 2021jose Antonio vazquez padillaAún no hay calificaciones
- 7 Acidosis-MetablicaDocumento29 páginas7 Acidosis-MetablicaVictor Cercado VásquezAún no hay calificaciones
- Antiácidos y sucralfatos: comparación de sus propiedades farmacocinéticas y farmacodinámicasDocumento20 páginasAntiácidos y sucralfatos: comparación de sus propiedades farmacocinéticas y farmacodinámicasbrianAún no hay calificaciones
- Acidosis MetabolicaDocumento39 páginasAcidosis MetabolicaJulio AlbinezAún no hay calificaciones
- Trastornos ácido-básicos: clasificación y mecanismosDocumento13 páginasTrastornos ácido-básicos: clasificación y mecanismosMichael PerozoAún no hay calificaciones
- Semiología Médica Clase de Acidosis y Alcalosis MetabólicaDocumento40 páginasSemiología Médica Clase de Acidosis y Alcalosis MetabólicaLuz Ledesma OropezaAún no hay calificaciones
- Acidosis MetabolicaDocumento5 páginasAcidosis MetabolicaRoseli EspinalAún no hay calificaciones
- Acidosis MetabólicaDocumento31 páginasAcidosis MetabólicaLuis Carlos PabónAún no hay calificaciones
- Acidocis y Alcalosis - BiologiaDocumento11 páginasAcidocis y Alcalosis - BiologiamariaAún no hay calificaciones
- Acidosis y AlcalosisDocumento102 páginasAcidosis y AlcalosisArykellAún no hay calificaciones
- Litiasis Renal ExposiciónDocumento39 páginasLitiasis Renal ExposiciónNicole MaldonadoAún no hay calificaciones
- Acidosis MetabolicaDocumento6 páginasAcidosis MetabolicaJulian DiazAún no hay calificaciones
- Acidosis Metabolica 2 puedeserEL MEJORDocumento40 páginasAcidosis Metabolica 2 puedeserEL MEJORkevin hilaquitaAún no hay calificaciones
- Clase de Acidosis y Alcalosis MetabólicaDocumento19 páginasClase de Acidosis y Alcalosis MetabólicaLuz Ledesma OropezaAún no hay calificaciones
- Análisis de electrolitos y equilibrio ácido-baseDocumento15 páginasAnálisis de electrolitos y equilibrio ácido-baseYamispAún no hay calificaciones
- Fundamentos de Trastornos Acido BaseDocumento22 páginasFundamentos de Trastornos Acido BaseENMANUEL JESUS SILVA MERCADOAún no hay calificaciones
- Equilibrio Acido BasicoDocumento34 páginasEquilibrio Acido BasicoEidel CastellanoAún no hay calificaciones
- Agua corporal y equilibrio ácido-baseDocumento26 páginasAgua corporal y equilibrio ácido-baseYendry RamirezAún no hay calificaciones
- Cetoacidosis Diabética CA DR BernalDocumento34 páginasCetoacidosis Diabética CA DR BernalLuis RamirezAún no hay calificaciones
- Acidosis Tubular RenalDocumento7 páginasAcidosis Tubular RenalAngel AyalaAún no hay calificaciones
- TUBULOPATÍASDocumento37 páginasTUBULOPATÍASAndres MottaAún no hay calificaciones
- Equilibrio Acido BaseDocumento38 páginasEquilibrio Acido BaseraulAún no hay calificaciones
- Desequilibrio Acido-BasicoDocumento7 páginasDesequilibrio Acido-BasicoSTEVEN DURÁNAún no hay calificaciones
- ALTERACIONES DEL EQUILIBRIO ACIDOBÁSICO DR David SerranoDocumento8 páginasALTERACIONES DEL EQUILIBRIO ACIDOBÁSICO DR David SerranoDavid SerranoAún no hay calificaciones
- Acidosis y AlcalosisDocumento15 páginasAcidosis y AlcalosisBlackdragon23Aún no hay calificaciones
- AMINOACIDURIASDocumento30 páginasAMINOACIDURIASJose Manuel PedrozaAún no hay calificaciones
- HidroelectroDocumento27 páginasHidroelectroNatalia Sandoval MAún no hay calificaciones
- 2DA PARCIAL Equilibrio Acido Base PDFDocumento19 páginas2DA PARCIAL Equilibrio Acido Base PDFMiguel Angel LlunaAún no hay calificaciones
- Clase 8 - Alteraciones Del Estado Acido-BaseDocumento68 páginasClase 8 - Alteraciones Del Estado Acido-BaseYeysonHDzAún no hay calificaciones
- 9 Nefrologia 2004Documento30 páginas9 Nefrologia 2004renato favioAún no hay calificaciones
- Acidosis Tubular RenalDocumento16 páginasAcidosis Tubular RenalAlma CamachoAún no hay calificaciones
- Luis Alberto Sánchez Cámara 6º Medicina HGUGMDocumento58 páginasLuis Alberto Sánchez Cámara 6º Medicina HGUGMYaizaGariglioAún no hay calificaciones
- Acido Base Apunte Del Goic Dr. RoesslerDocumento8 páginasAcido Base Apunte Del Goic Dr. RoesslerSofia SimpertigueAún no hay calificaciones
- Fisiopato - Tema 3Documento75 páginasFisiopato - Tema 3Zulle Natali Quispe CarbajalAún no hay calificaciones
- Unidad 3Documento21 páginasUnidad 3NoeliaAún no hay calificaciones
- Acidosis MetabolicaDocumento17 páginasAcidosis MetabolicaJuan Pablo BaldiviesoAún no hay calificaciones
- Manejo de Desequilibrio Ácido-BaseDocumento31 páginasManejo de Desequilibrio Ácido-BaseAlan Cubilla PonceAún no hay calificaciones
- Acidosis y Alcalosis MetabólicaDocumento9 páginasAcidosis y Alcalosis Metabólicajesus valentinAún no hay calificaciones
- El Desarrollo de Acidemia (PH Arterial 7,35)Documento7 páginasEl Desarrollo de Acidemia (PH Arterial 7,35)axl345Aún no hay calificaciones
- ACIDOSIS METABOLICA CDocumento14 páginasACIDOSIS METABOLICA CDanIel DiazAún no hay calificaciones
- Manejo y Diagnóstico de Trastornos MetabólicosDocumento26 páginasManejo y Diagnóstico de Trastornos MetabólicosCristhian Temoche100% (1)
- Copia de INTERPRETACION AGA 2012 UNMSM PDFDocumento89 páginasCopia de INTERPRETACION AGA 2012 UNMSM PDFYancarlos Chocce PachasAún no hay calificaciones
- Marcha Reto Mary Priscila: Acidosis y Alcalosis MetabólicaDocumento18 páginasMarcha Reto Mary Priscila: Acidosis y Alcalosis MetabólicaLuz Ledesma OropezaAún no hay calificaciones
- 11exposición Trastornos Ácido BaseDocumento9 páginas11exposición Trastornos Ácido BasePediatria TroncosoAún no hay calificaciones
- Tema 1 TABDocumento7 páginasTema 1 TABChristian Yohan Sierra HurtadoAún no hay calificaciones
- Clase de Acidosis y Alacalosis MetabólicaDocumento42 páginasClase de Acidosis y Alacalosis MetabólicaLuz Ledesma OropezaAún no hay calificaciones
- Tema 30-31. Acidosis y Alcalosis FINALDocumento18 páginasTema 30-31. Acidosis y Alcalosis FINALLuYsLuAún no hay calificaciones
- Electrolitos y Gases ArterialesDocumento38 páginasElectrolitos y Gases ArterialesELIANA BACA CHOQUEHUANCAAún no hay calificaciones
- Dieta Alcalina: Libro de recetas alcalinas: deliciosas recetas alcalinas para poner en marcha tu dietaDe EverandDieta Alcalina: Libro de recetas alcalinas: deliciosas recetas alcalinas para poner en marcha tu dietaAún no hay calificaciones
- Cómo Elaborar Un Plan de Mejora en 7 PasosDocumento3 páginasCómo Elaborar Un Plan de Mejora en 7 PasosTeresa Dávila EspinosaAún no hay calificaciones
- Cómo Elaborar Un Plan de Mejora en 7 PasosDocumento3 páginasCómo Elaborar Un Plan de Mejora en 7 PasosTeresa Dávila EspinosaAún no hay calificaciones
- Cómo Hacer Un Tutú de Colores Sin CoserDocumento4 páginasCómo Hacer Un Tutú de Colores Sin CoserTeresa Dávila EspinosaAún no hay calificaciones
- Cómo Elaborar Un Plan de Mejora en 7 PasosDocumento3 páginasCómo Elaborar Un Plan de Mejora en 7 PasosTeresa Dávila EspinosaAún no hay calificaciones
- Preguntas de Ley y Principios Scout para MaratónDocumento1 páginaPreguntas de Ley y Principios Scout para MaratónTeresa Dávila EspinosaAún no hay calificaciones
- ENDOCRINODocumento15 páginasENDOCRINOTeresa Dávila EspinosaAún no hay calificaciones
- Cómo Hacer Un Tutú de Colores Sin CoserDocumento4 páginasCómo Hacer Un Tutú de Colores Sin CoserTeresa Dávila EspinosaAún no hay calificaciones
- Preguntas de Ley y Principios Scout para MaratónDocumento1 páginaPreguntas de Ley y Principios Scout para MaratónTeresa Dávila EspinosaAún no hay calificaciones
- Enfermedades y Riesgos Asociados A Las Deficiencias en Los Servicios de Agua y SaneamientoDocumento1 páginaEnfermedades y Riesgos Asociados A Las Deficiencias en Los Servicios de Agua y SaneamientoTeresa Dávila EspinosaAún no hay calificaciones
- Champiñones Con Ajo y ChileDocumento1 páginaChampiñones Con Ajo y ChileTeresa Dávila EspinosaAún no hay calificaciones
- DX SituacionalDocumento2 páginasDX SituacionalTeresa Dávila EspinosaAún no hay calificaciones
- DIURESISDocumento9 páginasDIURESISTeresa Dávila EspinosaAún no hay calificaciones
- Cuadro Signos VitalesDocumento2 páginasCuadro Signos VitalesTeresa Dávila EspinosaAún no hay calificaciones
- Cómo Se Forma Un GrupoDocumento4 páginasCómo Se Forma Un GrupoTeresa Dávila EspinosaAún no hay calificaciones
- RESUMEN de Mapa ConceptualDocumento3 páginasRESUMEN de Mapa ConceptualTeresa Dávila EspinosaAún no hay calificaciones
- Tortas de PlátanoDocumento8 páginasTortas de PlátanoTeresa Dávila EspinosaAún no hay calificaciones
- La Enfermería y La InvestigaciónDocumento13 páginasLa Enfermería y La InvestigaciónTeresa Dávila EspinosaAún no hay calificaciones
- La Receta Delas Albóndigas de IkeaDocumento1 páginaLa Receta Delas Albóndigas de IkeaTeresa Dávila EspinosaAún no hay calificaciones
- Desarrollo Organizacional PlaneacionDocumento52 páginasDesarrollo Organizacional PlaneacionTeresa Dávila EspinosaAún no hay calificaciones
- Fisiologia de PancreatitisDocumento1 páginaFisiologia de PancreatitisTeresa Dávila EspinosaAún no hay calificaciones
- Receta de Camarones Al Mojo de Ajo FacilDocumento2 páginasReceta de Camarones Al Mojo de Ajo FacilTeresa Dávila EspinosaAún no hay calificaciones
- Menu para Campamento de Grupo AgostoDocumento1 páginaMenu para Campamento de Grupo AgostoTeresa Dávila EspinosaAún no hay calificaciones
- Gestion Conflictos MAPA CONCEPTUALDocumento2 páginasGestion Conflictos MAPA CONCEPTUALTeresa Dávila EspinosaAún no hay calificaciones
- Herramientas GerencialesDocumento1 páginaHerramientas GerencialesTeresa Dávila EspinosaAún no hay calificaciones
- Enlaces SeminarioDocumento3 páginasEnlaces SeminarioTeresa Dávila EspinosaAún no hay calificaciones
- Caso Clínico 23 Embarazo AdolescenteDocumento3 páginasCaso Clínico 23 Embarazo AdolescenteTeresa Dávila EspinosaAún no hay calificaciones
- Vendajes CONTROL DE LIQUIDOS Y OTRASDocumento16 páginasVendajes CONTROL DE LIQUIDOS Y OTRASTeresa Dávila EspinosaAún no hay calificaciones
- Tipos de MetodosDocumento21 páginasTipos de MetodosTeresa Dávila EspinosaAún no hay calificaciones
- II Microbiologia ParasitologiaDocumento40 páginasII Microbiologia ParasitologiaTeresa Dávila EspinosaAún no hay calificaciones
- Cianofitas y Mal SaborDocumento3 páginasCianofitas y Mal SaborGersan Joel Laines AguilarAún no hay calificaciones
- Taller de Preparacion de Productos de LimpiezaDocumento5 páginasTaller de Preparacion de Productos de LimpiezaEmerson Chourio100% (1)
- Enlaces químicos polaresDocumento4 páginasEnlaces químicos polaresMARIA VALENTINA ARANA VASQUEZAún no hay calificaciones
- Actividad 10 Exp 4Documento12 páginasActividad 10 Exp 4Mari MhAún no hay calificaciones
- Tema 5. Los Materiales Compuestos. 20-21YBVDocumento20 páginasTema 5. Los Materiales Compuestos. 20-21YBVAitor GarciaAún no hay calificaciones
- Adn Egg MsdsDocumento5 páginasAdn Egg MsdsKatiuska AlvarezAún no hay calificaciones
- Lab SQ5Documento10 páginasLab SQ5Anthony SanchezAún no hay calificaciones
- Tipos de PlasticosDocumento1 páginaTipos de PlasticosEduardo CanoAún no hay calificaciones
- Acetaminofen Uv TerminadoDocumento9 páginasAcetaminofen Uv TerminadoJuanka GonzalezAún no hay calificaciones
- Investigación de Proceso de Elaboración de Carmelo de AnísDocumento4 páginasInvestigación de Proceso de Elaboración de Carmelo de AnísPriscila E. Jaramillo M.Aún no hay calificaciones
- Ficha Tecnica Aceite 15W-40Documento1 páginaFicha Tecnica Aceite 15W-40khristian Alexander Chuello QueralesAún no hay calificaciones
- CARACTERÍSTICAS FÍSICOQUÍMICAS DE RESIDUOS TRANSPORTADOSDocumento36 páginasCARACTERÍSTICAS FÍSICOQUÍMICAS DE RESIDUOS TRANSPORTADOScamila100% (1)
- Procesamiento de Gas Natural El Objetivo Del Procesamiento Del Gas Natural Es Eliminar Los ContaminantesDocumento3 páginasProcesamiento de Gas Natural El Objetivo Del Procesamiento Del Gas Natural Es Eliminar Los ContaminanteskaneAún no hay calificaciones
- Ideas InnovadorasDocumento5 páginasIdeas InnovadorasangelAún no hay calificaciones
- Folle To No SpotsDocumento2 páginasFolle To No SpotsVeronica GarciaAún no hay calificaciones
- Ficha Técnica AC-4100 Rev 5 (Oct 22,19)Documento2 páginasFicha Técnica AC-4100 Rev 5 (Oct 22,19)felipe adolfo herrera hidalgoAún no hay calificaciones
- Sesion 6. Anexo de Los Estados de Agregacion y Cambios de Estado 101VDocumento4 páginasSesion 6. Anexo de Los Estados de Agregacion y Cambios de Estado 101VMARIA DE LOS SUAREZAún no hay calificaciones
- HDS Meropa XL 150 220 320 460 680Documento7 páginasHDS Meropa XL 150 220 320 460 680manuel DuranAún no hay calificaciones
- Bioquímica Parcial 1Documento5 páginasBioquímica Parcial 1laura ortizAún no hay calificaciones
- PRE2Documento16 páginasPRE2cuenta socialAún no hay calificaciones
- Tema 9Documento16 páginasTema 9KATHERINEAún no hay calificaciones
- Ecologia Acuatica ESTANQUE Y RIODocumento24 páginasEcologia Acuatica ESTANQUE Y RIOYomira Enamorado LopezAún no hay calificaciones
- Ap 24 Co PipDocumento2 páginasAp 24 Co PipAndersson Fabian MAún no hay calificaciones
- Certificado de conformidad de producto clavijasDocumento16 páginasCertificado de conformidad de producto clavijasDiego Alejandro GonzalezAún no hay calificaciones
- Memoria Práctica 8Documento21 páginasMemoria Práctica 8Sandra MartínAún no hay calificaciones
- Ejercicios de MolaridadDocumento5 páginasEjercicios de Molaridadgral89Aún no hay calificaciones
- Informe Equilibrio Acido-BaseDocumento5 páginasInforme Equilibrio Acido-Baseanon_315528371Aún no hay calificaciones
- Trabajo de QuimicaDocumento5 páginasTrabajo de QuimicaSegunda Sección ConarAún no hay calificaciones
- Zap Ox No Grit Sds EsDocumento7 páginasZap Ox No Grit Sds EsShava AkoztaAún no hay calificaciones