Documentos de Académico
Documentos de Profesional
Documentos de Cultura
SDRA y COVID 19
Cargado por
ANGELA GISELLE RUIZ AVILADescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
SDRA y COVID 19
Cargado por
ANGELA GISELLE RUIZ AVILACopyright:
Formatos disponibles
produce un aumento de su permeabilidad que
provoca la extravasación de plasma rico en
proteínas hacia el intersticio y los alvéolos con
activación del complemento de la coagulación y
de la respuesta inflamatoria. Se lesionan los
El síndrome de dificultad respiratoria aguda
neumocitos tipo II y se altera la síntesis de
(SDRA) o distrés respiratorio agudo es un
surfactante, que produce colapso alveolar y
síndrome que produce disnea, infiltrados
edema intersticial. Pueden formarse membranas
pulmonares difusos e insuficiencia respiratoria
hialinas como resultado del depósito de fibrina y
aguda grave, de rápida evolución, secundaria a
otras sustancias en el alvéolo. Todas estas
un aumento en la permeabilidad de la membrana
alteraciones predominan en zonas declives,
alveolocapilar en respuesta a diferentes
quedando sólo una parte de pulmón sano, que se
estímulos, que pueden ser directos, como la
ve obligado a realizar un trabajo “extra”.
inhalación de gases tóxicos, o indirectos, como la
sepsis. Debido al edema intersticial y al colapso alveolar,
los pulmones se vuelven rígidos (disminución de
la distensibilidad) y aumenta el trabajo
respiratorio. La sobrecarga mecánica produce
fatiga de los músculos respiratorios, con
Las causas más frecuentes de SDRA son: disminución de los volúmenes ventilatorios.
• SRIS: sepsis, politraumatismo, politransfusión, Se producen importantes alteraciones de la
gran quemado, pancreatitis aguda, embolismos ventilación/perfusión y cortocircuito intrapulmonar
grasos, pancreatitis. por los alvéolos colapsados y áreas
atelectasiadas. Estas alteraciones se ven
• Inflamación pulmonar: neumonía grave, embolia agravadas por la oclusión de vasos pulmonares
grasa, aspiración bronquial de contenido finos, lo que disminuye la perfusión en áreas
gástrico, ahogamiento, inhalación de toxinas. ventiladas, con la consecuente aparición de
hipertensión pulmonar, por un lado, y aumento del
• Fármacos que aumentan la permeabilidad
espacio muerto fisiológico, por otro, cuya
(opiáceos) o inducen inflamación pulmonar
consecuencia es la hipercapnia.
(nitrofurantoína).
La fase exudativa transcurre en los primeros 5-7
• Estados de shock, enfermedades
días de la enfermedad, en los que aparece disnea
autoinmunitarias o cirugía extracorpórea.
y taquipnea, e infiltrados alveolares difusos en los
estudios radiológicos. El diagnóstico diferencial
con el edema agudo de pulmón cardiogénico se
hace por ausencia de cardiomegalia y de derrame
pleural bilateral en el distrés.
El SDRA se produce como consecuencia de una •• Fase proliferativa. Tiene lugar entre los días 7
respuesta inflamatoria anormal, desencadenada y 21. Tras la fase exudativa se produce una
por diversos estímulos exógenos, que llegan al mejoría del paciente que puede desconectarse
pulmón por vía inhalada o sistémica. En del ventilador, aunque persisten la disnea y la
consecuencia, se produce una lesión de la taquipnea. Histológicamente en el pulmón
membrana alveolocapilar. En la evolución de esta aparecen signos de reparación pulmonar,
enfermedad se describen tres fases: consistentes en la organización de los exudados
alveolares, la sustitución de neutrófilos por
•• Fase exudativa. La lesión del endotelio capilar linfocitos y la proliferación de neumocitos tipo II,
que reinician la producción de surfactante y, por organizativa criptogenética, hemorragia
su condición pluripotencial, se transforman en alveolar difusa o neumonía eosinófila aguda).
neumocitos tipo I. En esta fase, la elevación del
procolágeno tipo III se asocia con mal pronóstico. 4. Descarte de edema pulmonar cardiogénico
(presión capilar pulmonar o presión de
•• Fase fibrótica. Pasados 21 días, en ocasiones, enclavamiento normal).
las alteraciones previas dan paso a una fibrosis
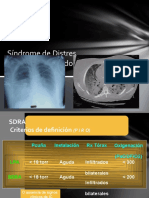
extensa con alteración y desestructuración de la El SDRA se diagnostica con cociente PaO2/FiO2
arquitectura pulmonar. Aparecen zonas de previo a ventilación <200, pero se clasifica según
panalización, disminución de la distensibilidad y el nivel del cociente PaO2/ FiO2 tras iniciar la
alteraciones en el intercambio gaseoso. Si esto ventilación mecánica en: SDRA leve (200 a 299),
ocurre, la mortalidad es mayor. Cuando la moderado (100-199) o grave (<100).
situación se mantiene, puede aparecer fibrosis a
El cuadro conocido como lesión pulmonar aguda
partir de las 2-3 semanas.
(ALI, del inglés Acute Lung Injury) tiene las
3. Y la existencia de infiltrados pulmonares
mismas características, pero menor gravedad, y
bilaterales, después de descartar la presencia
se diferencia del anterior por un cociente
de edema pulmonar cardiogénico y otras
PaO2/FiO2 ≤ 300 mmHg. Si se agrava, se
causas de infiltrados alveolares bilaterales
transforma en distrés.
(como brotes inflamatorios de FPI, neumonitis
ʹ
ʹ
enfermedad, se instaure una hipoxemia refractaria al
tratamiento con oxígeno suplementario (por el efecto
shunt).
Se debe descartar edema agudo de pulmón de
causa cardiogénica; el método más fiable para Estudios complementarios
ello es medir la presión capilar pulmonar o
presión de enclavamiento y constatar que no está • Radiografía de tórax: pueden apreciarse en la
elevada (≤ 15 cmH2O). fase inicial infiltrados intersticiales bilaterales de
predominio basal y, posteriormente, infiltrados
El diagnóstico del SDRA es clínico pero, en alveolares bilaterales y difusos
casos de duda, debe utilizarse un catéter de
Swan-Ganz para medir la presión capilar
pulmonar enclavada, que será normal o estará
disminuida.
Los criterios diagnósticos del SDRA son:
1. Insuficiencia respiratoria grave con
cociente PaO2/FiO2 <200 (en ocasiones lo
han preguntado como PaO2 <55 mmHg con
FiO2 >50%, o bien PaO2 <50 mmHg con FiO2
>60%), con descenso de distensibilidad.
2. Existencia de patología desencadenante.
• Gasometría arterial: en la gasometría
Si no hay desencadenante conocido, no puede
inicialmente sólo se observan hipocapnia y
diagnosticarse SDRA, debiendo valorarse el
aumento del gradiente alveoloarterial de oxígeno,
diagnóstico de neumonitis interstical aguda o
pero en fases más avanzadas hay hipoxemia
pulmón de Hamman-Rich.
grave.
• Estudio hemodinámico: es característico el
aumento de la presión en la arteria pulmonar,
pero con la presión capilar enclavada normal
El cuadro clínico se caracteriza por la aparición de (aspecto que lo diferencia del edema pulmonar
taquipnea, junto con taquicardia, sudoración, cardiogénico).
cianosis, disnea e insuficiencia respiratoria grave. En
un principio, la hipoxemia mejora con la
oxigenoterapia, pero es típico que, según avanza la
de la membrana alveolocapilar obliga a mantener
presiones de llenado auricular izquierdo bajas
para no empeorar el edema pulmonar, siempre
que la situación hemodinámica lo permita
Si no se corrige a tiempo puede aparecer fibrosis (ausencia de hipotensión).
a partir de la segunda o tercera semana de su
instauración. -- Oxigenación con membrana extracorpórea
(ECMO). Para los casos más graves, pasar la
sangre por una membrana extracorpórea que
cumple esa función.
-- Bloqueo neuromuscular. El uso precoz de
agentes bloqueantes neuromusculares mejora la
Se basa en la identificación y el tratamiento de la
supervivencia sin aumentar la debilidad muscular.
causa subyacente, asegurar una adecuada
nutrición, profilaxis de enfermedad Las complicaciones principales del tratamiento
tromboembólica y de la hemorragia pulmonar y el son el barotrauma, la toxicidad por el oxígeno (
tratamiento de la insuficiencia respiratoria. FiO2 > 60% durante más de 3 días; parece
inducida por la formación de radicales libres de
Dada la presencia de shunt generalizado en
oxígeno) y las neumonías nosocomiales. La
estos pacientes, la oxigenoterapia rara vez mortalidad ha mejorado en los últimos años,
es eficaz en revertir la insuficiencia pero se mantiene entre el 25-45%. Los pacientes
respiratoria, y suele ser necesaria la que superan el episodio agudo suelen quedar
ventilación mecánica invasiva. libres de secuelas, pero algunos desarrollan
alteraciones funcionales a largo plazo y unos
La ventilación mecánica debe utilizar presión pocos una enfermedad intersticial de tipo no
teleespiratoria positiva (PEEP) para evitar el específica.
colapso de los alvéolos y volúmenes corrientes
bajos para evitar el volutrauma. El ajuste de la
PEEP a este valor (12-15 mmHg) mejora la COVID 19
oxigenación al mantener más alvéolos abiertos,
pero no ha demostrado reducir la mortalidad. La COVID-19 es la enfermedad infecciosa
causada por SARSCoV-2
∙ La denominada ventilación protectora en el
distrés respiratorio se basa en una serie de EPIDEMIOLOGÍA
recomendaciones que buscan optimizar el
México acumula 2 millones 305,602 contagios
reclutamiento pulmonar sin producir fenómenos
y 212,339 decesos al 18 de abril de 2020.
de sobredistensión del pulmón. Ha demostrado
beneficios en la mortalidad. Sus principios son:
FISIOPATOLOGÍA
• Volumen tidal <10 ml/kg de peso ideal,
presión meseta <30 cmH20, PEEP >10-12 1. Unión del virión a la célula huésped mediante la
cmH2O (ajustada a la mecánica pulmonar y interacción de la proteína S y su receptor ECA II.
respuesta clínica). Después, el virus tiene acceso al citosol de la célula
• Frecuencia respiratoria pautada entre 15-25 huésped que permite la formación y liberación del
rpm. genoma viral al citoplasma.
• FiO2 <0,7 si se logra PaO2 >90 mmHg. 2. Replicación de las proteínas virales (traducción
del ARN genómico del virión).
• Empleo de la mínima sedación para lograr
adecuada sincronía con el ventilador. 3. Las proteínas estructurales virales S, E y M se
traducen y se insertan en el retículo
• Estrategias para disminuir la incidencia de endoplásmico de las células del huésped. Estas
neumonía asociada al ventilador. proteínas se desplazan al aparato de Golgi,
donde se envuelven en la membrana y forman
• Minimizar la posibilidad de desreclutamiento viriones maduros.
durante las aspiraciones. .
•• Otras medidas:
-- Fluidoterapia. El aumento en la permeabilidad
de incubación de 1-14 días, con mayor
CLÍNICA frecuencia de 3-7, con una media de 5.2 días.
PRUEBAS DIAGNÓSTICAS
En los casos de infección autolimitada el
diagnóstico de coronavirus es innecesario, ya que
la enfermedad naturalmente seguirá su curso. El
estudio por RT-PCR se ha convertido en el
método de elección para el diagnóstico de
COVID-19, ya que detecta el ácido nucleico de
SARS-CoV-2 en muestras de esputo, hisopos de
garganta y secreciones del tracto respiratorio
inferior.
PRUEBAS DE IMAGEN
Los resultados y hallazgos que con mayor
frecuencia se han reportado en pruebas de
imagen de pacientes infectados por SARS-CoV-2
son anormalidades en las imágenes por
tomografía computarizada (TC) de tórax,
TRANSMISIÓN
principalmente múltiples opacidades de vidrio
: 1. Por gotas: ocurre cuando una persona esmerilado periférico en regiones subpleurales de
infectada tose o estornuda y las gotas liberadas ambos pulmones con distribución periférica,
son ingeridas o inhaladas por personas cercanas. involucro de los lóbulos inferiores y conforme
progresan las opacidades pulmonares el cuadro
2. Por contacto: cuando un sujeto tiene contacto
clínico de estos pacientes empeora.
con superficies u objetos contaminados con el
virus y posteriormente se toca la boca, la nariz o PRINCIPALES COMPLICACIONES
los ojos.
∙ SDRA
3. Por aerosoles: sucede cuando las gotas ∙ Lesión cardíaca aguda y opacidades de
respiratorias se mezclan en el aire del ambiente de gran tamaño en los pulmones
un lugar relativamente cerrado, formando aerosoles
TRATAMIENTO Y MANEJO HOSPITALARIO
que se inhalan en altas dosis causando infección
Hasta la fecha no existen terapias antivirales que
PERÍODO DE INCUBACIÓN
se dirijan específicamente a COVID-19, por lo que
Se ha reportado que los síntomas de infección los tratamientos son únicamente de apoyo.
por SARSCoV-2 aparecen después de un período
Bibliografia:
● Bravo, A. y Jimenez, M. (2020). SARS-CoV-2 y pandemia de síndrome respiratorio agudo
(COVID 19). Ars Pharmaceutica, 61(2), 63-79. Obtenido de:
https://scielo.isciii.es/pdf/ars/v61n2/2340-9894- ars-61-02-63.pdf
● Fauci, A., Braunwald, E., Kasper, D., Hauser, S. y Longo, D. (2010). Harrison manual de
medicina. McGraw Hill Educación.
● Grupo, C. T. O. (2019). Manual CTO. a. 10th ed.: CTO editorial
● Salazar, J., Hidalgo, F. y Álvarez, P. (2018). Síndrome de Distrés Respiratorio Agudo.
Revista Clínica HSID, 9(1), 56-64. Obtenido de:
https://www.medigraphic.com/pdfs/revcliescmed/ucr 2019/ucr191g.pdf
● Vargas, K., Schreiber, V., Ochoa, E. y Lopez, A. (2020). SARS-CoV-2: una revisión
bibliográfica de los temas más relevantes y evolución del conocimiento médico sobre la
enfermedad. Neumología y Cirugía de Tórax, 79 (3). Obtenido de:
https://www.medigraphic.com/pdfs/neumo/nt-2020/nt203k.pdf
También podría gustarte
- La pandemia del covid-19. Efectos sobre la saludDe EverandLa pandemia del covid-19. Efectos sobre la saludCalificación: 5 de 5 estrellas5/5 (1)
- Síndrome Distrés Respiratorio Agudo CHM 2020Documento7 páginasSíndrome Distrés Respiratorio Agudo CHM 2020Martín A. GaticaAún no hay calificaciones
- Conceptos Y Estrategias En Terapia RespiratoriaDe EverandConceptos Y Estrategias En Terapia RespiratoriaCalificación: 4 de 5 estrellas4/5 (1)
- S D D R D A (ADRS) : ResumenDocumento8 páginasS D D R D A (ADRS) : ResumenLuis Antonio Cifuentes CifuentesAún no hay calificaciones
- Pulmón Húmedo TraumáticoDocumento21 páginasPulmón Húmedo TraumáticoJulio Granado Yance100% (4)
- Presentación Marca Personal Creativa Psicodélica Rosa Crema PDFDocumento24 páginasPresentación Marca Personal Creativa Psicodélica Rosa Crema PDFAidee MorenoAún no hay calificaciones
- Clase 8 A Enfermedades RespiratoriasDocumento26 páginasClase 8 A Enfermedades RespiratoriassofiaAún no hay calificaciones
- Enfermedades Pulmonares RestrictivasDocumento90 páginasEnfermedades Pulmonares Restrictivaskarlos0407Aún no hay calificaciones
- Presentación Marca Personal Creativa Psicodélica Rosa Crema PDFDocumento22 páginasPresentación Marca Personal Creativa Psicodélica Rosa Crema PDFAidee MorenoAún no hay calificaciones
- Anatomia Patologica 8Documento25 páginasAnatomia Patologica 8Micaela Aguero ArecoAún no hay calificaciones
- Lesión Pulmonar Aguda y Síndrome de Dificulta Respiratoria AgudaDocumento8 páginasLesión Pulmonar Aguda y Síndrome de Dificulta Respiratoria AgudaMaria Camila Correa CastiblancoAún no hay calificaciones
- 10) Síndrome de Distress Respiratorio AgudoDocumento10 páginas10) Síndrome de Distress Respiratorio AgudoAlfonso PrietoAún no hay calificaciones
- Tema 2Documento7 páginasTema 2Milton JaroAún no hay calificaciones
- 9 Guia Docente de Patologia PulmonarDocumento12 páginas9 Guia Docente de Patologia PulmonarEddy Romario Vilcanqui JiménezAún no hay calificaciones
- TP9 - Respiratorio-Alfonso-Maita-BarzolaDocumento7 páginasTP9 - Respiratorio-Alfonso-Maita-BarzolaPablo BarzolaAún no hay calificaciones
- Sindrome de Distres Respiratorio AgudoDocumento10 páginasSindrome de Distres Respiratorio AgudoMilguard GavinoAún no hay calificaciones
- EPOCDocumento26 páginasEPOCeduardo cuevaAún no hay calificaciones
- Guía de Insuficiencia RespiratoriaDocumento4 páginasGuía de Insuficiencia RespiratoriaFabiana OrtegaAún no hay calificaciones
- EPIDDocumento16 páginasEPIDFANY ADELA CONDORI CARDOZAAún no hay calificaciones
- Pato RespiDocumento19 páginasPato RespimarianoprofessiAún no hay calificaciones
- Síndrome Del Distrés Respiratorio Del AdultoDocumento11 páginasSíndrome Del Distrés Respiratorio Del AdultoIvan Bravo PozoAún no hay calificaciones
- SiraDocumento7 páginasSiraKarina Itzel Castro EleuterioAún no hay calificaciones
- Pulmón PT1Documento9 páginasPulmón PT1Gianella AvilaAún no hay calificaciones
- Apuntes Sobre Fisiopatología RespiratoriaDocumento7 páginasApuntes Sobre Fisiopatología RespiratoriaGabriel Alejandro Rodríguez GuerreroAún no hay calificaciones
- PulmónDocumento5 páginasPulmónMakarena GonzálezAún no hay calificaciones
- Cuadro Enfermedades Restrictivas y ObstructivasDocumento9 páginasCuadro Enfermedades Restrictivas y ObstructivasEMMANUEL CURREA GOMEZAún no hay calificaciones
- Trabajo 2Documento11 páginasTrabajo 2Andi Monasterios TejerinaAún no hay calificaciones
- Pulmon Resumen Robbins Cotran PatologiaDocumento26 páginasPulmon Resumen Robbins Cotran PatologiaTatiana Bonza100% (1)
- SDRA SemiologiaDocumento26 páginasSDRA SemiologiaFabio Luis Padilla Avila0% (1)
- Enfermedad Pulmonar Restrictiva-Hl SiteDocumento13 páginasEnfermedad Pulmonar Restrictiva-Hl SiteLinea Educativa Health & Life IPSAún no hay calificaciones
- Sindrome de Distres Respiratorio 1Documento18 páginasSindrome de Distres Respiratorio 1Katherine Janeta LazoAún no hay calificaciones
- Sindrome de Dificultad RespiratoriaDocumento1 páginaSindrome de Dificultad RespiratoriaMonserrath CarranzaAún no hay calificaciones
- Pulmón (Patologia)Documento12 páginasPulmón (Patologia)Gretel RochaAún no hay calificaciones
- Síndrome de Distrés RespiratorioDocumento22 páginasSíndrome de Distrés Respiratoriobeatriz narcisoAún no hay calificaciones
- Secuelas y Tratamiento EstelaDocumento8 páginasSecuelas y Tratamiento EstelaESTELA DANIELA CAMPERO ROSALESAún no hay calificaciones
- SdraDocumento4 páginasSdraJazmín AguileraAún no hay calificaciones
- SDRA, Trauma de Torax & CirugiaDocumento99 páginasSDRA, Trauma de Torax & CirugiaMelissa Osorio RomeroAún no hay calificaciones
- Clase 7. Sistema Respiratorio IIDocumento42 páginasClase 7. Sistema Respiratorio IIRocio Stefany Casanova Alegria100% (1)
- Sindrome de Dificultad Respiratoria AgudaDocumento4 páginasSindrome de Dificultad Respiratoria AgudatonyAún no hay calificaciones
- Clase de LouisianaDocumento18 páginasClase de LouisianaCele19Aún no hay calificaciones
- Sindromes ParenquimatososDocumento15 páginasSindromes ParenquimatososALEJANDRA CATHERINE CORDOBA SOLARTEAún no hay calificaciones
- Sindrome de Insuficiencia RespiratoriaDocumento3 páginasSindrome de Insuficiencia RespiratoriacarmenAún no hay calificaciones
- Síndrome de Distrés RespiratorioDocumento2 páginasSíndrome de Distrés RespiratorioRocío SánchezAún no hay calificaciones
- Ira en Paciente Epoc PDFDocumento31 páginasIra en Paciente Epoc PDFAlejandro Aucar PoudesAún no hay calificaciones
- Cuestionario PulmonDocumento28 páginasCuestionario PulmonDarwin RamirezAún no hay calificaciones
- At Elect AsiaDocumento50 páginasAt Elect AsiananyglzAún no hay calificaciones
- Respiratorio - PatologíaDocumento25 páginasRespiratorio - PatologíaCande MedicinaAún no hay calificaciones
- Sindrome Insuficiencia RespiratoriaDocumento9 páginasSindrome Insuficiencia RespiratoriaRodrigo ZuñigaAún no hay calificaciones
- Mapa Conceptual FisiopatologiaDocumento7 páginasMapa Conceptual FisiopatologiaAndrea Gonzalez100% (1)
- Distress RespiratorioDocumento10 páginasDistress RespiratorioDavid OstroskiAún no hay calificaciones
- Sindromes Parenquimatosos 2Documento30 páginasSindromes Parenquimatosos 2dessire reyesAún no hay calificaciones
- Pulmón Cap 15Documento32 páginasPulmón Cap 15Lilu Montedo DelamarreAún no hay calificaciones
- Sndromedeldistrsrespiratorioagudo 150327110516 Conversion Gate01Documento19 páginasSndromedeldistrsrespiratorioagudo 150327110516 Conversion Gate01melisza rueda salazarAún no hay calificaciones
- Lección 8Documento7 páginasLección 8api-3698281Aún no hay calificaciones
- Insuficiencia Respiratoria Aguda, Cronica y Cronica AgudizadaDocumento6 páginasInsuficiencia Respiratoria Aguda, Cronica y Cronica AgudizadaJesús Sánchez Castro.Aún no hay calificaciones
- La Enfermedad Pulmonar Obstructiva y La RestrictivaDocumento8 páginasLa Enfermedad Pulmonar Obstructiva y La RestrictivaAbrahamFoxMartinezAún no hay calificaciones
- SDRA2Documento5 páginasSDRA2João Nuno Duarte OliveiraAún no hay calificaciones
- 9 - SdraDocumento15 páginas9 - SdraPatricia DoldanAún no hay calificaciones
- Pulmon Grupo 6Documento75 páginasPulmon Grupo 675929778Aún no hay calificaciones
- Fisiopato Enf. Respiratorias y Cardiovasculares PDFDocumento62 páginasFisiopato Enf. Respiratorias y Cardiovasculares PDFconsultorio.niwaAún no hay calificaciones
- Resumen RubivirusDocumento5 páginasResumen RubivirusANGELA GISELLE RUIZ AVILAAún no hay calificaciones
- Síndrome de RettDocumento3 páginasSíndrome de RettANGELA GISELLE RUIZ AVILAAún no hay calificaciones
- Síndrome de WilliamsDocumento4 páginasSíndrome de WilliamsANGELA GISELLE RUIZ AVILAAún no hay calificaciones
- Síndrome de Síndrome de EhlersDocumento4 páginasSíndrome de Síndrome de EhlersANGELA GISELLE RUIZ AVILAAún no hay calificaciones
- EpocDocumento5 páginasEpocANGELA GISELLE RUIZ AVILAAún no hay calificaciones
- 10.1.-Síndrome NefróticoDocumento5 páginas10.1.-Síndrome NefróticoANGELA GISELLE RUIZ AVILAAún no hay calificaciones
- 4.-Ferropenia y Anemias HipoproliferativasDocumento3 páginas4.-Ferropenia y Anemias HipoproliferativasANGELA GISELLE RUIZ AVILAAún no hay calificaciones
- 5.-Anemias MegaloblásticasDocumento4 páginas5.-Anemias MegaloblásticasANGELA GISELLE RUIZ AVILAAún no hay calificaciones
- DiscapacidadDocumento27 páginasDiscapacidadAmira GarciaAún no hay calificaciones
- Shock Organizador GraficoDocumento1 páginaShock Organizador GraficoCecy ToaquizaAún no hay calificaciones
- Triptico Primeros Auxilios WordDocumento2 páginasTriptico Primeros Auxilios Word53104220Aún no hay calificaciones
- Fiebre Sin Foco PediatriaDocumento8 páginasFiebre Sin Foco PediatriaNeorlidis Maria Vasquez HernandezAún no hay calificaciones
- Barreras DefensivasDocumento15 páginasBarreras DefensivasNatalia Oviedo UrrutiaAún no hay calificaciones
- 2-Anatomía y Fisiología Del Aparato RespiratorioDocumento16 páginas2-Anatomía y Fisiología Del Aparato RespiratorioAnaAún no hay calificaciones
- Definición de Neuropsicología PDFDocumento3 páginasDefinición de Neuropsicología PDFkael zaiffer100% (2)
- Re144b PDFDocumento7 páginasRe144b PDFV.v. TaguisAún no hay calificaciones
- Enfermeria-Qué Es La BioseguridadDocumento7 páginasEnfermeria-Qué Es La BioseguridadFher Fex NatAún no hay calificaciones
- Práctica 3 Desarrollo y Anomalías Del Ojo 2021FDocumento8 páginasPráctica 3 Desarrollo y Anomalías Del Ojo 2021FWILFREDO LEON NINAAún no hay calificaciones
- HIPERTENSIÓN ARTERIAL PULMONAR EcocardiogramaDocumento13 páginasHIPERTENSIÓN ARTERIAL PULMONAR EcocardiogramaIsabel Mallory Aco BravoAún no hay calificaciones
- RESUMEN SEMINARIO LLA (1) Grupo B 2021-2Documento7 páginasRESUMEN SEMINARIO LLA (1) Grupo B 2021-2Diana AvilaAún no hay calificaciones
- Reuma 200 CONDocumento74 páginasReuma 200 CONanndreaoliveraAún no hay calificaciones
- Result A DosDocumento5 páginasResult A DosStalin EnriquezAún no hay calificaciones
- Circulacion EspláncicaDocumento4 páginasCirculacion Espláncicaaxel ramon susanibarAún no hay calificaciones
- TablasDocumento1 páginaTablasYeit LoboAún no hay calificaciones
- Exéresis de Quiste Tirogloso. Churruca-2020Documento16 páginasExéresis de Quiste Tirogloso. Churruca-2020juanrangoneAún no hay calificaciones
- Les - Caso ClinicoDocumento6 páginasLes - Caso ClinicoBryan A. SaltoAún no hay calificaciones
- 11-MH-MARIA ISABEL DIAZ HUAMAN - Aula Virtual ML CuestionarioDocumento11 páginas11-MH-MARIA ISABEL DIAZ HUAMAN - Aula Virtual ML Cuestionariomaria isabelAún no hay calificaciones
- Agentes Fisicos IDocumento38 páginasAgentes Fisicos IMassiel Torres AriasAún no hay calificaciones
- Flujograma CANCER DE PIELDocumento3 páginasFlujograma CANCER DE PIELPiero Gomez GuadalupeAún no hay calificaciones
- Escolarizacion de Niños Con DisfasiaDocumento2 páginasEscolarizacion de Niños Con DisfasiaAndre AgramontAún no hay calificaciones
- BNM Residual ANESTESIOLOGIADocumento32 páginasBNM Residual ANESTESIOLOGIALucas MagañaAún no hay calificaciones
- Betalactamasas de Espectro ExtendidoDocumento12 páginasBetalactamasas de Espectro ExtendidoRafael PasteurAún no hay calificaciones
- Diseño de Matriz de Politica Pública - Julissa Soto Linares y Soledad Rodriguez ChavezDocumento2 páginasDiseño de Matriz de Politica Pública - Julissa Soto Linares y Soledad Rodriguez ChavezJu SolAún no hay calificaciones
- Examen Tipo Test Resuelto Enero 2015Documento11 páginasExamen Tipo Test Resuelto Enero 2015rndlAún no hay calificaciones
- Plan de Respuesta y Prevención - Citricos Del ElquiDocumento20 páginasPlan de Respuesta y Prevención - Citricos Del Elquivicky ornella guerrero casanovaAún no hay calificaciones
- PEDIATRIA Y NEONATOLOGIA Estudios M y CDocumento133 páginasPEDIATRIA Y NEONATOLOGIA Estudios M y CEisnthen León Suárez0% (1)
- Examen General de Orina PoeDocumento4 páginasExamen General de Orina PoeJulieta Gutierrez83% (12)
- Troncos LinfáticosDocumento4 páginasTroncos LinfáticosBryan CAAún no hay calificaciones
- CAMBIA TU CEREBRO CAMBIA TU VIDA: CAMBIA TU CEREBRO CAMBIA TU VIDADe EverandCAMBIA TU CEREBRO CAMBIA TU VIDA: CAMBIA TU CEREBRO CAMBIA TU VIDACalificación: 3.5 de 5 estrellas3.5/5 (38)
- En sintonía con tu ciclo femenino: FLO. Aprende a sincronizarte con tu bioquímica para dar rienda suelta a tu creatividad, mejorar tu vida y hacer más con menos estrésDe EverandEn sintonía con tu ciclo femenino: FLO. Aprende a sincronizarte con tu bioquímica para dar rienda suelta a tu creatividad, mejorar tu vida y hacer más con menos estrésCalificación: 4.5 de 5 estrellas4.5/5 (11)
- Entrenamiento Científico con pesas: Fitness InteligenteDe EverandEntrenamiento Científico con pesas: Fitness InteligenteCalificación: 5 de 5 estrellas5/5 (3)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- Más vida con hábitos saludablesDe EverandMás vida con hábitos saludablesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Mega Piernas: Entrenamiento Científico de PiernasDe EverandMega Piernas: Entrenamiento Científico de PiernasCalificación: 4 de 5 estrellas4/5 (4)
- Muchas Vidas, Muchos Sabios (Many Lives, Many Masters): (Many Lives, Many Masters)De EverandMuchas Vidas, Muchos Sabios (Many Lives, Many Masters): (Many Lives, Many Masters)Calificación: 4 de 5 estrellas4/5 (475)
- La medicina biorreguladora: Un enfoque holístico e innovador de la autocuraciónDe EverandLa medicina biorreguladora: Un enfoque holístico e innovador de la autocuraciónCalificación: 3.5 de 5 estrellas3.5/5 (2)
- Ondas de choque extracorpóreas radiales: Aplicación en patologías músculo esqueléticasDe EverandOndas de choque extracorpóreas radiales: Aplicación en patologías músculo esqueléticasCalificación: 5 de 5 estrellas5/5 (3)
- Sistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)De EverandSistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)Calificación: 5 de 5 estrellas5/5 (9)
- Cambia tu cerebro cambia tu cuerpoDe EverandCambia tu cerebro cambia tu cuerpoCalificación: 3.5 de 5 estrellas3.5/5 (38)
- Joven a cualquier edad. El método definitivo para una vida larga, saludable y felizDe EverandJoven a cualquier edad. El método definitivo para una vida larga, saludable y felizAún no hay calificaciones
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- Mindfulness: Guía práctica para encontrar la paz en tu vida diariaDe EverandMindfulness: Guía práctica para encontrar la paz en tu vida diariaCalificación: 5 de 5 estrellas5/5 (5)
- Formulación de cosméticos naturales: Guía completa para la formulación de productos naturales para el cuidado de la piel y el cabello, junto con la elaboración de perfumes y cosméticos decorativosDe EverandFormulación de cosméticos naturales: Guía completa para la formulación de productos naturales para el cuidado de la piel y el cabello, junto con la elaboración de perfumes y cosméticos decorativosCalificación: 5 de 5 estrellas5/5 (1)
- Dieta Para El Reflujo Biliar y Gastritis Alcalina - Incluye 20 Deliciosas Recetas Libres de Gluten y de Lácteos Para Tratar y Aliviar el Reflujo Biliar y Sus Molestos SíntomasDe EverandDieta Para El Reflujo Biliar y Gastritis Alcalina - Incluye 20 Deliciosas Recetas Libres de Gluten y de Lácteos Para Tratar y Aliviar el Reflujo Biliar y Sus Molestos SíntomasCalificación: 4 de 5 estrellas4/5 (9)
- Kundalini: La guía definitiva para despertar a tus chakras a través del Kundalini Yoga y la meditación y para experimentar la conciencia superior, la clarividencia y el viaje astralDe EverandKundalini: La guía definitiva para despertar a tus chakras a través del Kundalini Yoga y la meditación y para experimentar la conciencia superior, la clarividencia y el viaje astralCalificación: 4 de 5 estrellas4/5 (11)
- 7 Pasos Para Superar Una Crisis: Cómo atravesar un duelo o una pérdida y salir fortalecidoDe Everand7 Pasos Para Superar Una Crisis: Cómo atravesar un duelo o una pérdida y salir fortalecidoCalificación: 5 de 5 estrellas5/5 (5)
- El código de la obesidad: Descifrando los secretos de la pérdida de pesoDe EverandEl código de la obesidad: Descifrando los secretos de la pérdida de pesoCalificación: 4.5 de 5 estrellas4.5/5 (51)
- Las Enfermedades comienzan y terminan en tu mente: Una guía para la autosanaciónDe EverandLas Enfermedades comienzan y terminan en tu mente: Una guía para la autosanaciónCalificación: 4 de 5 estrellas4/5 (4)
- Sana tu Cuerpo, Calma tu Mente: Desintoxicar Hígado, Intestino Permeable, Salud Hormonal, Curación Emocional, Relajación, Ansiedad y Sanidad mental, Atención Plena, Psicoterapia y NutriciónDe EverandSana tu Cuerpo, Calma tu Mente: Desintoxicar Hígado, Intestino Permeable, Salud Hormonal, Curación Emocional, Relajación, Ansiedad y Sanidad mental, Atención Plena, Psicoterapia y NutriciónCalificación: 5 de 5 estrellas5/5 (4)
- Cuerpo Tóxico: Como Liberar Tu Cuerpo De Las Toxinas Externas E Internas, Y Evitar Asi Los Efectos De Los Radicales LibresDe EverandCuerpo Tóxico: Como Liberar Tu Cuerpo De Las Toxinas Externas E Internas, Y Evitar Asi Los Efectos De Los Radicales LibresCalificación: 5 de 5 estrellas5/5 (2)
- Lactancia humana y fonoaudiología: Guía para madres lactantesDe EverandLactancia humana y fonoaudiología: Guía para madres lactantesCalificación: 5 de 5 estrellas5/5 (4)
- Vivir con endometriosis: Una guía para recuperar el bienestarDe EverandVivir con endometriosis: Una guía para recuperar el bienestarCalificación: 5 de 5 estrellas5/5 (5)
- Código Mujer: Womancode: Optimiza tu ciclo, aumenta tu fertilidad, potencia tu deseo sexual y conviértete en una fuente de energíaDe EverandCódigo Mujer: Womancode: Optimiza tu ciclo, aumenta tu fertilidad, potencia tu deseo sexual y conviértete en una fuente de energíaCalificación: 5 de 5 estrellas5/5 (2)
- Las Causas Psíquicas de la Enfermedades: La Nueva Medicina (Color Edition) SpanishDe EverandLas Causas Psíquicas de la Enfermedades: La Nueva Medicina (Color Edition) SpanishCalificación: 5 de 5 estrellas5/5 (1)