Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Guia Clinica Amiloidosis
Cargado por
Ulises Saldias RoaDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Guia Clinica Amiloidosis
Cargado por
Ulises Saldias RoaCopyright:
Formatos disponibles
Guías Prácticas Clínicas
PARA DIAGNÓSTICO Y
TRATAMIENTO DE LA
AMILOIDOSIS AL
Aprobadas por la Sociedad Chilena de Hematología SOCHIHEM 2020
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Declaración
Este documento es una guía general para el manejo de la enfermedad, que debe ser utilizada con el adecuado juicio
médico para cada individuo.
La Guías se realizaron con el objetivo de proporcionar información para facilitar las decisiones médicas y están basadas
en la mejor información disponible en agosto 2020.
Conflicto de interés
El desarrollo de estas guías de práctica clínica ha sido realizado por trabajo no remunerado de un grupo médico de la
Sociedad Chilena de Hematología.
Actualización periódica
Nueva información científica disponible que se considere importante será actualizada en forma periódica, discutida en la
SOCHIHEM y deberá ser aprobada para su inclusión.
Autores
Versión 2.0
Los siguientes especialistas, han contribuido con la elaboración de esta guía clínica.
Dra. Paola Aravena Rodríguez
Dra. Marcela Espinoza Zelada
Dra. Camila Peña Ojeda
Dra.Mónica Torrens Parraguez
Aprobación de la guía por hematólogos a cargo de revisión de guías clínicas: Dra. Cao Pochintesta, Dra. Patricia
Fardella Bello, Dra. María de los Angeles Rodríguez Siclari.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
ALCANCE DE LA GUÍA
Tipo de pacientes y escenarios clínicos a los que se refiere:
Población de ambos sexos mayores de 15 años con diagnóstico de Amiloidosis AL.
La Amiloidosis AL (previamente llamada Primaria) se clasifica según CIE- 10 E85.9.
Usuarios a los que está dirigida la guía:
Médicos hematólogos y otros que intervienen en el manejo y tratamiento de pacientes hemato-oncológicos
adultos.
Otros profesionales de la salud con responsabilidades en la atención y cuidados de pacientes hemato-
oncológicos: enfermeras, kinesiólogos, químicos farmacéuticos, tecnólogos médicos y psicólogos, entre otros.
Directivos de instituciones de salud.
OBJETIVOS
Esta guía es una referencia para la atención de los pacientes con “Amiloidosis AL”.
Sus objetivos son:
Aportar recomendaciones sobre el manejo de personas con “Amiloidosis AL”, basadas en la mejor evidencia
científica disponible, el consenso de los expertos y adecuadas al contexto nacional.
Contribuir a disminuir la mortalidad ajustada por edad en Chile.
Disminuir la variabilidad de la atención en el manejo preventivo, el tratamiento y seguimiento de los pacientes
con Amiloidosis AL.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
TABLA DE CONTENIDOS
1.- INTRODUCCIÓN
2.- CRITERIOS DIAGNÓSTICOS
3.- ESTRATIFICACIÓN PRONÓSTICA Y EVALUACIÓN DE RIESGOS
5.- TRATAMIENTO
6.- CRITERIOS DE RESPUESTA
7.- LÍNEAS DE TRATAMIENTO
8.- SEGUIMIENTO
9.- ALGORITMO
10.- BIBLIOGRAFÍA
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
1.- INTRODUCCIÓN
Amiloidosis
Las amiloidosis son un grupo heterogéneo de enfermedades raras causadas por el depósito extracelular en tejidos de
fibrillas de amiloide, demostrables mediante la tinción con rojo Congo(1); son enfermedades conformacionales de
proteínas, causadas por el plegamiento incorrecto y la agregación de proteínas autólogas.
En ellas, las proteínas normales se desestabilizan, ya sea por acumulación, mutaciones o inflamación constante, y son
depositadas finalmente como fibras anormales insolubles, produciendo disrupción de tejidos, alterando su estructura y
determinando disfunción del órgano afectado. Se han descrito más de 30 proteínas diferentes capaces de formar
amiloide.(2) (Si bien cada proteína es diferente en cuanto a su estructura y función, el producto final (amiloide) es el
mismo. El hallazgo de amiloide en algún tejido obliga a dilucidar de qué tipo de amiloidosis se trata, ya que el
enfrentamiento clínico y el tratamiento será diferente, dependiendo de las distintas variantes de amiloidosis.(Tabla1)
Tabla 1. Ejemplos de algunas de las amiloidosis más frecuentes y sus proteínas patogénicas.(3)(4)
TIPO de AMILOIDOSIS PROTEINA INVOLUCRADA HEREDITARIA/ADQUIRIDA
Amiloidosis AL Cadenas livianas K o L Adquirida 78 %
Amiloidosis AA Proteína A Adquirida 3%
Amiloidosis ATTRm Transtirretina mutada Hereditaria 7%
Amiloidosis ATTRwt Transtirretina no mutada (“salvaje”) Adquirida 6%
Amiloidosis AB2 B2 microglobulina Adquirida
Amiloidosis ALECT Factor Quimiotáctico 2 de leucocitos Desconocida 3%
Amiloidosis AL
La amiloidosis más frecuente es la amiloidosis de cadenas ligeras (AL), con una incidencia que ha ido en aumento
desde 9,7 a 14 casos por millón de habitantes al año(3), aunque se estima que es subdiagnosticada por su
inespecificidad clínica.(5) En promedio, los pacientes pueden estar más de un año, consultando diversos especialistas
antes del lograr un diagnóstico adecuado.
En Chile no existen datos de incidencia o prevalencia; existe escasa información de este grupo de patologías y creemos
que su diagnóstico en nuestro país es subóptimo.(6) Recientemente se publicó una cohorte de pacientes chilenos del
sistema público de Salud, demostrando resultados subóptimos en términos de supervivencia (SV). (7)
El depósito de amiloide puede ser sistémico o localizado, como en las amiloidosis cerebrales, siendo la enfermedad de
Alzheimer la más frecuente; y en la amiloidosis AL localizada, que afecta principalmente a las vías respiratorias, la piel y
el tracto urinario, y que generalmente no requiere terapia sistémica.(8)
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
En la amiloidosis AL, las proteínas patogénicas son las cadenas livianas monoclonales producidas por un clon
(generalmente pequeño) de células plasmáticas. Puede presentarse como enfermedad primaria, pero también en el
desarrollo de un mieloma múltiple (MM), condición que se denomina “amiloidosis AL asociada a MM”.
Las proteínas comprometidas se configuran diferente a las proteínas normales, formando hojas B-plegadas, las que se
depositan en diferentes órganos y afectan finalmente su función.
Para un diagnóstico inequívoco se requiere de estudios histológicos, con la detección de depósitos de amiloide con
tinción de rojo Congo positivo en algún tejido, y detección de monoclonalidad mediante anticuerpos anti cadenas
livianas de inmunoglobulinas (Kappa o Lambda) por inmunohistoquímica (IHQ) y/o citometría de flujo(9). El “gold
standard” para su tipificación es la espectrometría de masa, examen que no está disponible en nuestro país.
Se ha postulado que la microdisección con laser y espectrometría de masas constituye la mejor técnica para identificar
el tipo de sustancia amiloideDicha técnica estaría especialmente indicada en los casos en que dos proteínas
precursoras amiloides pueden potencialmente estar presentes en el mismo paciente. Una vez se ha establecido el
diagnóstico de AL, debe determinarse la extensión de la afectación orgánica. (10) (11).
Afecta a personas entre los 50 a 80 años, aunque hay algunos casos de personas diagnosticadas jóvenes (20 años).
La relación varón: mujer es 2:1(12)
2.- CRITERIOS DIAGNÓSTICOS
Concepto y manifestaciones clínicas:
Las fibrillas amiloides pueden depositarse en cualquier órgano o tejido, excepto en el sistema nervioso central, dando
lugar a las manifestaciones clínicas y, en último término, producir la muerte del paciente. (13)(14) – (Tabla 2)
Sin tratamiento, la supervivencia mediana de los pacientes con AL es de 12 meses.
La clínica puede ser inespecífica: fatiga, edema, baja de peso y compromiso del estado general.
Los síntomas más específicos dependen del sistema involucrado. Signos que conllevan una alta sospecha son la
macroglosia, el púrpura periorbitario e la infiltración periarticular, aunque estos ocurren sólo en un 15% de los casos.
Los órganos más frecuentemente afectados son: riñón (74%), corazón (60%), hígado (27%) y sistema nervioso
autonómico (17%).
La evolución de la amiloidosis es difícil de objetivar, pues casi nunca se conoce con precisión el comienzo de la misma.
La amiloidosis sistémica tiene una supervivencia, que no es igual en todo el mundo, pero en Chile sí se ha objetivado un
aumento de la misma. La amiloidosis con compromiso cardíaco es la causa principal de muerte, así como también la
insuficiencia renal.
La amiloidosis que debuta con Mieloma o que presenta inicialmente insuficiencia cardíaca tiene una supervivencia
promedio de 7 a 8 meses. La que presenta inicialmente neuropatías o claudicación mandibular es de alrededor de 40
meses.
Las complicaciones más frecuentes: insuficiencia cardíaca, insuficiencia renal e insuficiencia respiratoria; todas ellas
pueden ser mortales. (9)(13)
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Síntomas generales:
Fatiga, Letargia, Disnea
Sequedad bucal
Pérdida de peso
Insuficiencia cardíaca (hipertrofia concéntrica + ECG con bajo voltaje)
Hemorragia digestiva
Diarrea / Constipación
Trastornos visuales
Examen físico:
Edema (retención de líquido)
Hepatomegalia
Signos del síndrome de túnel carpiano
Signos de polineuropatía periférica
Macroglosia
Púrpura (Hemorragias cutáneas)
Sospecha:
Compromiso renal: Síndrome nefrótico (50%) y/o falla renal (18%). (20)
Compromiso cardíaco: Falla cardiaca congestiva (>NYHA class II), con FEVI conservada, arritmias o ambas.
Ecocardiograma concordante con miocardiopatía restrictiva con disfunción diastólica y septum engrosado.
Cabe destacar que el compromiso cardiaco es la principal causa de muerte; se asocia con una sobrevida media
de 6 meses y determina el pronóstico.
Compromiso hepático: Hepatomegalia palpable, fosfatasa alcalina (FA) elevadas.
Compromiso esplénico: Paradoja de esplenomegalia e hipoesplenismo, con Howell-Jolly.
Compromiso neurológico: Axonal y desmielinizante. Comienza por síntomas sensitivos en extremidades
inferiores, luego alteraciones motoras, progresando a extremidades superiores. Es frecuente el síndrome de
túnel carpiano bilateral.
Neuropatía autonómica: Puede afectar al tracto GI con pseudoobstrucción, diarrea, constipación o vómitos.
Hipotensión ortostática, síncope o impotencia.
Macroglosia, púrpura periorbitaria.
Sospecha de laboratorio:
GMSI que comienza con proteinuria o aumento de la razón K/L de cadenas livianas libres (CLL)
Estudios básicos al diagnóstico (15)(16) – (Tabla 3)
Signos vitales ortostáticos
Historia clínica completa con fecha de inicio de síntomas, PS, CF según NYHA,
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Examen físico: Peso , talla, superficie corporal
Neuropatía: evaluar grado
Imágenes radiográficas
Espectrometría de masas (estudio de proteína aislada) (10)
Examen oftalmológico
Tabla 2 (21)(22)(23)
Afectación por órganos: Frecuencia Síntomas y signos
20 % Creatininemia > de 2mg/dL. Proteinuria de 24hs > ó = 0.5 g/d
RIÑÓN predominio de albúmina.
60 % Insuficiencia cardíaca, arritmia, infarto.
CORAZÓN Ecocardiograma: aumento del septum interventricular >12mm
sin otra causa.
ProBNP >332ng/L (en ausencia de falla renal o fibrilación
auricular), o grosor ventricular en diástole >12mm (sin otra
causa)
HÍGADO 25 % Hepatomegalia, >15 cm BRC sin falla cardíaca u otra causa o
Y FAL >1.5 veces el valor normal superior.
VÍA BILIAR Ictericia colestásica, Bilirrubina > 5mg/dL
BAZO 5% Ruptura espontánea, shock hipovolémico
TRACTO GASTRO-INTESTINAL 60 % Por biopsia
TEJIDOS BLANDOS 40 % Macroglosia, lesiones cutáneas,
15 % Hipotensión, diarrea, impotencia. Disautonomía: retardo en el
SISTEMA NERVIOSO AUTÓNOMO vaciamiento gástrico, pseudo-obstrucción.
SISTEMA NERVIOSO PERIFÉRICO 15 % Neuropatía periférica simétrica, sensitivo motora de EEII
Insensibilidad o dolor en manos o pies (neuropatía periférica).
SÍNDROME DE TÚNEL CARPIANO 25 % Dolor, parestesias, debilidad en manos.
SISTEMA ARTICULAR Artropatías. Miopatía (por biopsia)
EXTREMIDADES INFERIORES Claudicación intermitente (amiloide vascular)
50 % Obstrucción de la vía aérea.
PULMÓN Radiología: imagen con patrón intersticial,
Afectación pleural. Biopsia para diagnóstico.
MÉDULA ÓSEA 5% Plasmocitos anómalos en AL, similar a la GMSI ≥ 20%,Dg.dif:
con MM.(25)
SANGRE PERIFÉRICA Trombocitosis.
COAGULACIÓN 15 % Déficit de factor X.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Tabla 3 (22)(23)(24)
Exámenes a realizar en los pacientes con amiloidosis:
1. Historia clínica y exploración física completas, con atención a los síndromes asociados
2. Laboratorio básico: hemograma, VHS, creatinina, calcemia, albúmina, bilirrubina, fosfatasa alcalina, LDH, beta-
2- microglobulina, vitamina B 12 sérica, factor X, TP, TTPK, BUN, colesterol y triglicéridos
3. Estudio proteico en suero: proteínas totales, electroforesis de proteínas, inmunofijación y cuantificación de
inmunoglobulinas
4. Determinación de cadenas livianas libres en suero (free-light chains)(CLL)
5. Estudio proteico en orina: proteinuria de 24 horas y/o IPC, electroforesis en orina e inmunofijación
6. Determinación de troponinas (cTnT y cTnI) y péptido natriurético cerebral NT-ProBNP-
7. Demostración del depósito de sustancia amiloide (tinción de rojo Congo) e inmunohistoquímica (por biopsia
grasa, médula ósea, órgano comprometido, etc.)
8. Tipificación inmunohistoquímica del depósito tisular (cadenas livianas de Igs, transtiretina, proteína A, beta-2-
microglobulina)
Estudio de extensión:
9. Radiografía de tórax (AP y lateral)
10. ECG, ecocardiograma (con técnica de Strain)(17) y Holter (este último sólo si afectación cardiaca)
11. Resonancia nuclear magnética cardíaca
12. Cintigrafía cardíaca de pirofosfato
13. Mielograma / Biopsia de médula ósea (IHQ)
14. Inmunofenotipificación por Citometría de Flujo(18) (CD138,CD38,CD19,CD20,CD5,CD56, cKappa,cLambda)
15. Estudio citogenético
16. Radiografías de huesos (dolores óseos)
17. Electromiografía (sospecha de polineuropatía periférica)
18. Endoscopía digestiva con biopsia (si sospecha de afectación de tubo digestivo)
19. Estudio molecular de la transtiretina (sospecha de amiloidosis familiar) y cardiológico (19)
Otras Localizaciones:
20. Pruebas endocrinológicas: TSH, cortisol; Pruebas Pulmonares: examen funcional respiratorio
Estudios especiales: Biopsia / aspirado de tejido adiposo subcutáneo:
Si es negativo con clínica sugerente: Biopsia de glándula salival menor, recto u órgano afectado
Tinciones: corriente con Hematoxilina/eosina; IHQ con rojo Congo con y sin pretratamiento con permanganato
Tinción con cristal violeta; Tinción con agentes específicos de estructura amiloide (Dg.diferencial)
Biopsia Renal
Biopsia cutánea/cuero cabelludo
Biopsia de nervio sural
Biopsia cardíaca
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Estudios genéticos(23). (Tabla 4)
La amiloidosis presenta las mismas anomalías descritas para otras discrasias de células plasmáticas pero con diferente
distribución. La t(11;14)(q13;q32) es la anomalía más frecuente. La ganancia de 1q21 se asocia significativamente
con progresión de enfermedad. Estudios por técnicas de FISH en amiloidosis AL tienen valor pronóstico, especialmente
cuando aún no hay tratamiento y deben servir para tomar las decisiones terapéuticas correctas.
En la Tabla 4 se detallan las anomalías más frecuentes.
Tabla 4. (23)
Anomalía Frecuencia (%)
t(11;14)(q13;q32) 38-55
del13q 21-42
ganancia 1q21 19-21
hiperdiploidía 4-11
t(4;14)(p16;q32) 3-4
t(14;16)(q32;q23) 2-3
del17p 0-1
Las alteraciones genéticas más frecuentes son: t(11;14) (50%); la monosomía 13/del13q (36%); y las trisomías (26%).
La frecuencia de la del(17p) es del 3%. Más infrecuentes son la t(4;14) y t(14;16). Estas tres alteraciones genéticas que
sí son de alto riesgo en mieloma múltiple, no confieren pronóstico adverso en pacientes tratados con bortezomib.
El bortezomib y otras drogas inmunomoduladoras (IMIDs) se asocian con resultados insatisfactorios indicados en
pacientes que presentan la t(11;14), con tasas de respuesta parcial (RP) o muy buena respuesta parcial (MBRP) y con
una supervivencia global (SG) disminuida. Debe considerarse el TPH autólogo a dosis convencionales en estos
pacientes.(26)
Las trisomías se asocian a menor SG, alcanzando significancia estadística sólo en pacientes tratados con melfalán.
Las ganancias de 1q21 son menos frecuentes en amiloidosis AL y no confieren mal pronóstico a pacientes tratados con
bortezomib.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
3.- ESTRATIFICACIÓN PRONÓSTICA Y EVALUACIÓN DE RIESGOS
La supervivencia depende de dos factores principales: la extensión del daño cardíaco y la carga/biología de las células
plasmáticas.(Tabla 5)
Tabla 5
El pronóstico en función de la afectación de órganos y la carga de células plasmáticas / biología
Daño del órgano Carga de células plasmáticas/biología
NT-proBNP, troponina Inmunoglobulina sérica FLC
PS, clase NYHA, síncope por esfuerzo Carga de células plasmáticas
Presión arterial sistólica<100 mmHg Citogenética
Fosfatasa alcalina, bilirrubina, malabsorción Respuesta hematológica profunda
FLC = cadena ligera libre; NT-proBNP = péptido natriurético cerebral N-terminal; NYHA = Asociación de Corazón de Nueva York; PS =
performance status ó estado de rendimiento
En adición al porcentaje de células plasmáticas y anomalías descriptas en el FISH, una diferencia de concentración
entre la cadena liviana libre involucrada y no involucrada (dFLC) >180 mg/L revela un mal pronóstico.
La combinación de NT-proBNP y los niveles de troponinas cardíacas permiten separar a los pacientes en cuatro grupos
de riesgo. Se procederá a estratificar según riesgo, una vez confirmado el diagnóstico de AL.
Existen 3 scores pronósticos más reconocidos que están actualmente en revisión, pero el más utilizado es la de la
Clínica Mayo del 2012 (27): Cada factor mencionado tiene puntaje de 1.
Diferencia entre CLL afectada y la no afectada: ≥ 18 mg/dL
cTnT ≥ 0.025 mcg/L
NT-ProBNP ≥1,800 ng/L
Esto lo divide en 4 estadíos: I,II,III,IV, siendo el estadío I el de mejor pronóstico, y el IV el de peor pronóstico.(Tabla 6)
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Adicionalmente se suele definir la etapa IIIb en pacientes con NTproBNP >8500.
Tabla 6*
Factores de riesgo Estadío Supervivencia media
0 I 94,1 meses
1 II 40,3 meses
2 III 14 meses
3 IV 5,8 meses
*Mayo Clinic Revisado / Actualizado
I. No hay marcadores por encima del corte
II. Un marcador por encima del corte
III. Dos marcadores por encima del corte
IV. Tres marcadores por encima del corte
Recientemente se ha validado un sistema de estadificación para la afectación renal, basado en la tasa de filtración
glomerular estimado (eGFR) y la proteinuria, que puede predecir el riesgo de diálisis. Estas respuestas de órgano
también están siendo revisadas actualmente. (23)(Tabla 7)
Tabla 7
Sistema de estadificación Marcadores y umbrales Estadíos
I. Tanto eGFR arriba como proteinuria
debajo
de los puntos de corte
II. eGFR por debajo o proteinuria por
eGFR<50ml/min por 1,73/m2
encima
Renal Proteinuria>5 g/24h de los puntos de corte
III. Tanto eGFR por debajo como
proteinuria
por encima de los puntos de corte
eGFR tasa de filtración glomerular estimada
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
5.- TRATAMIENTO
5.1 Trasplante autólogo de precursores hematopoyéticos (TPHau)
Los resultados del tratamiento de la AL han ido evolucionando, es así como actualmente la proporción de pacientes que
sobreviven a los 10 años desde el diagnóstico ha aumentado de 5% a 25%, como lo muestra una serie de pacientes
trasplantados, así como el arsenal terapéutico en investigación. (26)(28)(29)(30)
El tratamiento se divide en pacientes elegibles o no elegibles para trasplante autólogo de progenitores
hematopoyéticos.(TPHau) Este procedimiento ha mostrado supervivencia de más de 20 años en hasta un tercio de los
pacientes, y debe seleccionarse toda vez que un paciente sea candidato, hecho que lamentablemente ocurre en un 20%
de los casos solamente.
El TPHau es una alternativa terapéutica eficaz para la amiloidosis AL, en pacientes seleccionados; sin embargo, su rol
requiere ser evaluado en futuros ensayos prospectivos, ante la aparición de nuevas terapias más eficaces.
Pacientes , que al momento del diagnóstico, presentan una carga tumoral mayor al 10% de células plasmáticas se
benefician de recibir ciclos de inducción previo al procedimiento. Los demás casos podrían ir directo a TPHau.
5.2 Tratamiento farmacológico
El tratamiento de la AL tiene por objetivo eliminar la población clonal de células plasmáticas que produce la proteína
amiloidogénica, precozmente, con respuesta profunda y prolongada, considerándose como óptimo lograr una muy
buena respuesta parcial (MBRP), además de respuesta de órgano, aunque este punto también se está evaluando, ya
que podría ser subóptimo. De no lograrse esta meta, debe considerarse cambiar de tratamiento de forma precoz
(después de 2 ciclos).
La terapia debe ser individualizada y adaptada al riesgo, basada en los marcadores cardíacos y en la respuesta.
5.2.1. Primera línea(31)
El tratamiento se basa fundamentalmente en esquemas de quimioterapia, basadas en bortezomib: con ciclofosfamida,
bortezomib y dexametasona. La combinación de los tres agentes (CyBorD) produce habitualmente una respuesta
profunda, rápida y duradera incluso en los casos con afectación cardíaca o multisistémica. Con éstos se logra una
RC/MBRP entre el 50-60%, y en pacientes con etapa IIIa o IIIb del 20-40%. Recientemente se publicó un estudio que
muestra respuestas igualmente prometedoras con Bortezomib, melfalán y dexametasona (BMDex).
Más recientemente se han publicado los resultados preliminares del estudio Andrómeda, que muestra respuestas sin
precedentes en esta patología con el uso de anticuerpos monoclonales “target” como Daratumumab (antiCD38) s.c. y
CyBorD.(32) Sin embargo, por ser resultados preliminares se debe esperar al término del estudio para cambiar de
estrategia terapéutica.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Adicionar doxicilina vía oral (100mg cada 12 horas) a pacientes con compromiso cardiaco podría ser eficaz según un
estudio reciente de fase II, aunque aún está pendiente realizar el estudio de fase III.(33)
Tener en cuenta que si la amiloidosis AL se ve asociada a Linfoma o presencia de IgM, puede evaluarse utilizar
Rituximab (anticuerpo monoclonal antiCD20) dirigido contra el clon CD20+.(34)
5.2.2. Segunda línea(35)
En segunda línea existen varias opciones, ninguna de ellas aprobadas aún.
Se recomienda repetir la primera línea si hubo respuesta profunda y prolongada objetivándose buenas respuestas.
El uso de Daratumumab también ha demostrado ser muy eficaz en segunda línea.(36)
Otro estudios han sido publicados, basados en inhibidores de proteasoma de segunda generación como: Carfilzomib o
Ixazomib, sin demostrar mejor eficacia, y con eventos adversos cardiacos y renales poco tolerados.(37)
Los inmunomoduladores (IMIDs) también han sido evaluados, sin embargo, se ha visto que estos pueden aumentar el
proBNP, y algunos como la Lenalidomida, requieren ajuste renal de su dosis y tienen potencial nefrotóxico.(38)(39)(40)
Se prefiere en general el uso de Pomalidomida.
Otro fármaco en investigación es el inhibidor de BCL2, Venetoclax (41) La racionalidad de su uso en amiloidosis AL se
basa en que el 50% de las amiloidosis AL tienen la traslocación t(11;14). Este fármaco se perfila con gran potencial en
esta enfermedad.
La Bendamustina también ha mostrado buenas respuestas en amiloidosis refractarias o en recaídas.(42)
Los anticuerpos antifibrillas están generando gran expectación, ya que podrían significar un quiebre en la
morbimortalidad de esta enfermedad. Sin embargo, sólo hay un estudio de estos agentes en desarrollo, CAEL101.
CAEL-101 es un anticuerpo monoclonal (mAb) reactivo a fibrillas que se encuentra actualmente en fase 3 de desarrollo
clínico para el tratamiento de pacientes con amiloidosis de cadena ligera amiloide ("AL"). El programa clínico Cardiac
Amyloid Reaching for Extended Survival (CARES) incluye dos estudios de fase 3 paralelos, uno en pacientes con
enfermedad en estadio IIIa de Mayo y otro en pacientes con enfermedad en estadio IIIb de Mayo, para 370 pacientes en
todo el mundo. El objetivo principal del programa clínico es evaluar la supervivencia general. Se espera pronto el inicio
de un estudio fase 3.(43)
6.- CRITERIOS DE RESPUESTA (14)(15)(23)(44)(45) (Tabla 8)
Es relevante medir la respuesta luego de cada ciclo, para evaluar la efectividad del tratamiento utilizado.
Además es crucial la respuesta de órgano; sin embargo, ésta es más lenta, pudiéndose observar su máxima respuesta
a los 6 a 12 meses de iniciado el tratamiento. A mayor respuesta hematológica, se ve mayor respuesta de órgano.
Estos criterios de respuesta también están siendo evaluados actualmente.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Tabla 8
Respuesta hematológica Criterio
RC = respuesta hematológica completa Inmunofijación en suero y orina negativa y rCLL normal
RC en pacientes con baja dCLL al diagnóstico dCLL 20- dFLC<10mg/L
50 mg/L
MBRP = muy buena respuesta parcial dFLC <40 mg/L
RP = respuesta parcial dFLC disminución >50%
NR = no respuesta Ninguna de las respuestas anteriores
Respuesta de órgano Criterio
Reducción proteinuria ≥50%, sin aumento de crea.
RENAL COMPLETA Reducción a menos de 500mg/24 hrs de proteinuria sin
progresión renal
≥50% de descenso en proteinuria con estabilización de
RENAL PARCIAL creatinina
Reducción proBNP de >30%, o reducción de >300ng/L si
su basal al diagnóstico (si basal fue >650ng/L). Mejoría de
CORAZÓN 2 estadíos en NYHA, si su basal fue 3 ó 4.
HÍGADO Disminución > al 50% valor de fosfatasa alcalina, del
tamaño del hígado mínimo en 2cm medido por imágenes.
PROGRESIÓN DE ÓRGANO
Cardíaca Aumento de 30% o >300ng/L proBNP. Aumento troponina
>33%. FE reducida >10%.
Renal Aumento clearence en >25% (eGFR). Proteinuria >25%
Debido al aumento del arsenal terapéutico con drogas que logran respuestas cada vez más profundas, se han
propuesta nuevos scores de respuestas basadas en cadenas livianas libres (CLL), como CLL involucrada <20mg/L, o
diferencia CLL <10mg/L (46)
También existen estudios para evaluar la importancia de medir la enfermedad mínima residual (EMR) por Citometría d
flujo (18) e incluso en sangre periférica por espectrometría de masa. Todas estas se encuentran actualmente en
revisión.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
7.- LÍNEAS DE TRATAMIENTO
LÍNEAS DE TRATAMIENTO (recomendadas en primera línea)
Bortezomib/ciclofosfamida/dexametasona (47)(48)
Bortezomib/melfalán/dexametasona(49)
Otros
Bortezomib /dexametasona (50)(51)(52)(53)(54)
MelDex en pacientes con neuropatía o fibrosis pulmonar
Rituximab en amiloidosis asociada a Linfoma no Hodgkin o IgM
LINEAS DE TRATAMIENTO (recomendadas en segunda línea)
Repetir la primera línea si hubo respuesta profunda y prolongada
Otro régimen referido en primera línea
Regímenes con Daratumumab
Lendex/ CyLenDex
Pomalidomida /dexametasona
Bendamustina /dexametasona
Venetoclax
8.- SEGUIMIENTO
El seguimiento es posterior a cada ciclo de quimioterapia, para evaluar tanto respuesta hematológica como la
respuesta de órgano.
Posteriormente podría evaluarse cada 3 meses. De encontrarse durante el seguimiento una recaída bioquímica, debe
plantearse el inicio de tratamiento de segunda línea precozmente.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
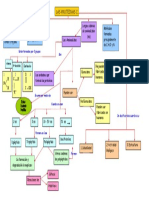
9.- ALGORITMO
AMILOIDOSIS
AL
CANDIDATO A TPH NO CANDIDATO A
TPH
INDUCCIÓN CyBORD
SI LA MÉDULA BMdex
ÓSEA TIENE
MelDex
INFILTRACIÓN >
10% (Dara CyBorD)
TPH < VGPR o
> progresión o
recaída
> ó = VGPR
Daratumumab
IMIDs
IP 2ª generación
SEGUIMIENTO
Venetoclax
Bendamustina
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
10.- BIBLIOGRAFÍA
1. Falk RH, Comenzo RL, Skinner M: The systemic amyloidoses. N Engl J Med. 1997; 337(13): 898–909.).
2. Benson MD, Buxbaum JN, Eisenberg DS, Merlini G, Saraiva MJM, Sekijima Y.Amyloid. 2018 Dec;25(4):215-
219. doi: 10.1080/13506129.2018.1549825. Epub 2019 Jan 7. Amyloid nomenclature 2018: recommendations
by the International Society of Amyloidosis (ISA) nomenclature committee.
3. Quock TP, Yan T, Chang E, Guthrie S, Broder MS. Epidemiology of AL amyloidosis: a real-world study using
US claims data. Blood Adv. 2018;2(10):1046–1053.)
4. Eriksson M, Schönland S, Yumlu S, Hegenbart U, Von Hutten H, Gioeva Z, Lohse P, Büttner J, Schmidt H and
Röcken C. Journal of Molecular Diagnostics, Vol. 11, No. 3, May 2009 Copyright © American Society for
Investigative Pathology and the Association for Molecular Pathology DOI: 10.2353/jmoldx.2009.080161257
5. Lousada et al. Light Chain Amyloidosis: Patient Experience Survey from the Amyloidosis Research Consortium.
Adv Ther (2015) 32:920–928.
6. Palma CL, Grünholz D, Osorio G, et al. Amiloidosis. Comunicación de 11 casos y revisión de la literature. Rev
Méd Chile 2005; 133: 655-66.
7. Peña et al. AL Amyloidosis in the Chilean public system: a pending debt. Multicenter study of the Chilean
cooperative group. Rev Med Chile 2019; 147: 1239-1246
8. Guías de diagnóstico y tratamiento: Gammapatías monoclonales 2019. Sociedad Argentina de Hematología.
9. Bruno Paiva 1, Joaquin Martinez-Lopez 2, Luis A Corchete 3, et al. : Blood. 2016 Jun 16;127(24):3035-9. Epub
2016 Apr 11. Phenotypic, transcriptomic, and genomic features of clonal plasma cells in light-chain amyloidosis
Affiliations expandPMID: 27069257 DOI: 10.1182/blood-2015-10-673095.
10. Vrana JA, Gamez JD, Madden BJ, et al. Classification of amyloidosis by laser microdissection and mass
spectrometry-based proteomic analysis in clinical biopsy specimens. Blood 2009; 114: 4957-9.
11. Cibeira M, Bladé J. Amiloidosis primaria: diagnóstico, pronóstico y tratamiento. Haematologica/edición
española | 2011; 96 Institut de Malalties Hemato-Oncològiques. Servei d’Hematologia. Institut d’Investigacions
Biomèdiques August Pi i Sunyer (IDIBAPS). Hospital Clínic Barcelona
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
12. Dispenzieri A. Amyloid proteins in pathogenesis of AA amyloidosis. Lancet 2001; 358: 24-9.
13. Merlini G, Bellotti V. Molecular mechanisms of amyloidosis. N Engl J Med 2003; 349: 583-96.
14. Gertz M, Merlini G. Definition of organ involvement and response to treatment in AL amyloidosis: an updated
consensus opinion Am. J. Haematol 2005; 79: 319-328.
15. NCCN Guidelines Version 1.2020- Systemic Light Chain Amyloidosis NCCN Guidelines Index.
16. Cibeira M, Bladé J Amiloidosis primaria: diagnóstico, pronóstico y tratamiento SEHH 2020.
17. Strain: Una ventana a la mecánica ventricular.Rev Chil Cardiol 2011; 31: 89-94 y 95-102.
18. Puig N., Paiva B. et al. Leukemia. 2019 May;33(5):1256-1267. Epub 2018 Dec 12.Flow cytometry for fast
screening and automated risk assessment in systemic light-chain amyloidosis.
19. Chacko L,Martone R, Bandera F, et al. Echocardiographic phenotype and prognosis in transthyretin cardiac
amiloidosis. Eur Heart 2020 Jan 17. pii: ehz905.
20. Peña C, Intriago M, Gray A, Cabrera M. Amiloidosis extrema asociada a mieloma múltiple e insuficiencia renal
terminal. Rev Med Chile 2011; 139: 1471-1474.
21. Gertz MA, Kyle RA. Hepatic amyloidosis (primary -AL-, immunoglobulin light chain): the natural history in 80
patients. Am J Med 1988; 85: 73-80.
22. Kyle RA, Gertz MA. Primary systemic amyloidosis: clinical and laboratory features in 474 cases. Semin
Hematol 1995; 32: 45.
23. Guías de Diagnóstico y tratamiento 2019, Sociedad Argentina de Hematología.
24. Institut Ferran de Reumatología, S.L. Última Modificación : 30/12/2013
25. Peña C, Intriago M, Gray A, Cabrera M, Rev Med Chile 2011; 139: 1471-1474.
26. Sanchorawala V, Skinner M, Quillen K, Finn KT, Doros G, Seldin DC. Long-term outcome of patients with
AL amyloidosis treated with high-dose melphalan and stem-cell transplantation. Blood 2007; 110: 3561-3.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
27. Kumar S, Dispenzieri A, Lacy M, Hayman S, Buadi F, Colby C, Laumann K,. Zeldenrust S, Nelson Leung, Dingli
D, Greipp P, Lust J, Russell S, Kyle RA, Rajkumar V, and Gertz MA. J Clin Oncol. 2012 Mar 20; 30(9): 989–995.
Published online 2012 Feb 13. PMC3675680PMID: 22331953 Revised Prognostic Staging System for Light
Chain Amyloidosis Incorporating Cardiac Biomarkers and Serum Free Light Chain Measurements.
28. Gertz MA, Lacy MQ, Dispenzieri A, et al. Autologous stem cell transplant for immunoglobulin light chain
amyloidosis: a status report. Leuk Lymphoma. 2010; 51 (12): 2181- 2187.
29. Dispenzieri A, Lacy MQ, Katzman JA, et al. Absolute value of immunoglobulin light chain are prognostic in
patients with primary systemic amyloidosis undergoing peripheral blood stem cell transplantation. Blood 2006;
107: 3378-83.
30. Muchtar E, Gertz MA, Kumar SK, et al. Improved outcomes for newly diagnosed AL amyloidosis 520 between
2000 and 2014: cracking the glass ceiling of early death. Blood. 2017;129:2111-2119.
31. Mikhael JR, Schuster SR, Jimenez-Zepeda VH, et al. Cyclophosphamide-bortezomib-dexamethasone (CyBorD)
produces rapid and complete hematologic response in patients with AL amyloidosis. Blood. 2012;119(19):4391-
4394.
32. Palladini et al, Daratumumab Plus CyBorD for Patients With Newly Diagnosed AL Amyloidosis: Safety Run-in
Results of ANDROMEDA. Blood 2020.
33. Wechalekar. Encouraging impact of doxycycline on early mortality in cardiac light chain (AL) amyloidosis. Blood
Cancer J. 2017 Mar; 7(3): e546. // María Valero-Muñoz et al, Doxycycline Decreases Amyloidogenic Light
Chain-Induced Autophagy in Isolated Primary Cardiac Myocytes. International Journal of Cardiology 2020,
AnitaD’Souza et al., Adjuvant doxycycline to enhance anti-amyloid effects: Results from the dual phase 2 trial.
EClinicalMedicine 2020.
34. Milani P., Merlini G., Palladini G. Light Chain Amyloidosis. Mediterr J Hematol Infect Dis 2018, 10(1): e2018022,
Published: March 1, 2018.
35. N Tandon, E Muchtar, S Sidana, A Dispenzieri, M Q Lacy, D Dingli, F K Buadi, S R Hayman, R Chakraborty, W
J Hogan, W Gonsalves, R Warsame, T V Kourelis, N Leung, P Kapoor, S K Kumar & M A Gertz . Revisiting
conditioning dose in newly diagnosed light chain amyloidosis undergoing frontline autologous stem cell
transplant: impact on response and survival. Bone Marrow Transplantation 2017: volume 52, pages1126–1132.
36. Giovanni Palladini, Efstathios Kastritis, Mathew S. Maurer, Jeffrey Zonder, Monique C. Minnema, Ashutosh D.
Wechalekar, Arnaud Jaccard, Hans C. Lee, Naresh Bumma, Jonathan L. Kaufman, Eva Medvedova, Tibor
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
Kovacsovics, Michael Rosenzweig, Vaishali Sanchorawala, Xiang Qin, Sandra Y. Vasey, Brendan M. Weiss,
Jessica Vermeulen, Giampaolo Merlini, Raymond L. Comenzo Daratumumab plus CyBorD for patients with
newly diagnosed AL amyloidosis: safety run-in results of ANDROMEDA . Clinical Trials & Observations. Blood
(2020) 136 (1): 71–80.
37. Dispenzieri A, Sanchorawala V, et al. A phase 1/2 study of the oral proteasome inhibitor ixazomib in relapsed or
refractory AL amyloidosis. Blood. 2017;130(5):597-605. Cohen AD, et al. Safety and efficacy of carfilzomib
(CFZ) in previously-treated systemic light-chain (AL) amyloidosis [abstract]. Blood. 2016;128(22):645.)
38. Dispenzieri A, Buadi F, Laumann K, LaPlant B, Hayman S, Kumar S, Dingli D, Zeldenrust S, Mikhael J, Hall R,
Rajkumar V, Reeder C, Fonseca R, Bergsagel PL, Stewart A, Roy V, Witzig T, Lust J, Russell S, Gertz MA,
and Lacy MQ: Activity of pomalidomide in patients with immunoglobulin light-chain amyloidosis Blood. 2012 Jun
7; 119(23): 5397–5404.
39. Sanchorawala V, Shelton AC, Lo S, Varga C, Sloan JM, Seldin DC. Pomalidomide and dexamethasone in the
treatment of AL amyloidosis: results of a phase 1 and 2 trial. Blood 2016;128(8):1059–62.
40. Palladini G, Milani P, Foli A, Basset M, Russo F, Perlini S, et al.: A phase 2 trial of pomalidomide and
dexamethasone rescue treatment in patients with AL amyloidosis. Blood 2017;129(15):2120–2123.
41. Sidiqi M, Al Saleh A, Leung N, Jevremovic D, Aljama M, Gonsalves W, Buadi F, Kourelis T, Warsame R,
Muchtar E, Hobbs M, Lacy M, Dingli D, Go R, Hayman S, Rajkumar V, Dispenzieri A, Gertz MA, Kumar S,
Fonseca R and Kapoor P. : Venetoclax for the treatment of translocation (11;14) AL amyloidosis . Blood Cancer
J. 2020 May; 10(5): 55.
42. Lentzsch S, Lagos G, Comenzo R, Zonder J, Osman K, Pan S. : Bendamustine With Dexamethasone in
Relapsed/Refractory Systemic Light-Chain Amyloidosis: Results of a Phase II Study. Journal of Clinical
Oncology : Volume 38, Issue 13.
43. December 2, 2019: Caelum Biosciences Granted Orphan Medicinal Product Designation from the European
Commission for CAEL-101 for the Treatment of AL Amyloidosis.
44. Palladini G, et al. Validation of the criteria of response to treatment in AL amyloidosis [Abstract]. Blood 2010
116: Abstract 1364.
45. Milani P, Merlini G and Palladini G.: New concepts in the treatment and diagnosis of amyloidosis Expert Rev
Hematol 2018 Feb;11(2):117-127.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
46. Despina Fotiou, Meletios Athanasios Dimopoulos, and Efstathios Kastritis : Systemic AL Amyloidosis: Current
Approaches to Diagnosis and Management. Hemasphere. 2020 Aug; 4(4): e454.
47. Venner CP, Lane T, Foard D, et al. Cyclophosphamide, bortezomib, and dexamethasone therapy in AL
amyloidosis is associated with high clonal response rates and prolonged progression-free survival. Blood
2012;119:4387-4390.
48. Mikhael JR, Schuster SR, Jimenez-Zepeda VH, et al. Cyclophosphamide-bortezomib-dexamethasone (CyBorD)
produces rapid and complete hematologic response in patients with AL amyloidosis. Blood 2012;119:4391-
4394.
49. Gasparetto C, Sanchorawala V, Snyder RM, et al. Use of melphalan (M)/dexamethasone (D)/bortezomib in AL
amyloidosis [abstract]. J Clin Oncol 2010;28:Abstract 8024.
50. Reece DE, Hegenbart U, Sanchorawala V, et al. Efficacy and safety of once-weekly and twice-weekly
bortezomib in patients with relapsed systemic AL amyloidosis: results of a phase ½ study. Blood 2011;118:865-
873.
51. Kastritis E, Wechalekar AD, Dimopoulos MA, et al. Bortezomib with or without dexamethasone in primary
systemic (light chain) amyloidosis. J Clin Oncol 2010;28:1031-1037.
52. Singh V, Saad A, Palmer J, et al. Response to bortezomib based induction therapy in newly diagnosed light
chain (AL) amyloidosis [abstract]. Blood 2009;114:Asbtract 1867
53. Lamm W, Willenbacher W, Lang A, et al. Efficacy of the combination of bortezomib and dexamethasone in
systemic AL amyloidosis. Ann Hematol 2011;90:201-206.
54. Reece DE, Sanchorawala V, Hegenbart U, et al. Weekly and twice-weekly bortezomib in patients with systemic
AL amyloidosis: results of a phase 1 dose-escalation study. Blood 2009;114:1489-1497.
Sociedad Chilena de Hematología
Bernarda Morin 488, segundo piso, Providencia, Santiago, Chile | www.hematologia.org | www.sochihem.cl
Fono (56-2) 2753 5565 | Fax (56-2) 2268 3394 | sochihem@smschile.cl | sochihem@gmail.com
También podría gustarte
- Criterios clínicos de enfermedades genéticasDe EverandCriterios clínicos de enfermedades genéticasCalificación: 1 de 5 estrellas1/5 (1)
- Mmieloma Criterios ChileDocumento50 páginasMmieloma Criterios ChileDebora AssumAún no hay calificaciones
- Absorción con filtro BK como terapia eficaz en el riñón del mieloma múltipleDe EverandAbsorción con filtro BK como terapia eficaz en el riñón del mieloma múltipleAún no hay calificaciones
- Guia Clinica Tratamiento HemoglobinuriaDocumento18 páginasGuia Clinica Tratamiento HemoglobinuriaUlises Saldias RoaAún no hay calificaciones
- Sindrome MielodisplasicoDocumento20 páginasSindrome MielodisplasicoSophie Alvarez C.Aún no hay calificaciones
- Arch 1312Documento25 páginasArch 1312Mario Colville SolarAún no hay calificaciones
- Hemofilia Proceso de EnfermeríaDocumento24 páginasHemofilia Proceso de EnfermeríaMargarita Molina Rodriguez67% (3)
- Enfermedad de Câmbios Mínimos-AnatopatologiaDocumento13 páginasEnfermedad de Câmbios Mínimos-AnatopatologiaDaniele CampanharoAún no hay calificaciones
- Taller Mitocondria 2019 IDocumento8 páginasTaller Mitocondria 2019 IJESUS ALBERTO SÁNCHEZ GARZONAún no hay calificaciones
- 8 Burgos Lorena Amiloidosis Reporte de Un CasoDocumento4 páginas8 Burgos Lorena Amiloidosis Reporte de Un Casofish goldenAún no hay calificaciones
- Protocolo Aplasia Medular Achop 2017Documento28 páginasProtocolo Aplasia Medular Achop 2017JOHN LOPERAAún no hay calificaciones
- Caso Clínico 1Documento8 páginasCaso Clínico 1Alejandro RuizAún no hay calificaciones
- Mieloma. Dra. Ana López de La GuíaDocumento3 páginasMieloma. Dra. Ana López de La GuíaHBakkaliAún no hay calificaciones
- PDF AnemiaDocumento16 páginasPDF AnemiaDeivi Salazar0% (1)
- ENFERMEDADES HEMATOLOGICAS - InasesDocumento129 páginasENFERMEDADES HEMATOLOGICAS - InasesAlison Andrea Bernal100% (1)
- Diagnosticos de Enfermeria DIAGNOSTICOS-DE-ENFERMERIA ONCOLOGIA - OncologiaDocumento8 páginasDiagnosticos de Enfermeria DIAGNOSTICOS-DE-ENFERMERIA ONCOLOGIA - OncologiaMilagros Chafloque CapuñayAún no hay calificaciones
- 215 517 1 PBDocumento13 páginas215 517 1 PBSandy_YsabelAún no hay calificaciones
- Alteraciones Hematologicas en El Adulto Mayor 2022Documento19 páginasAlteraciones Hematologicas en El Adulto Mayor 2022panchoAún no hay calificaciones
- Caso Clinico Emily Villacis PovedaDocumento7 páginasCaso Clinico Emily Villacis PovedaemilyAún no hay calificaciones
- Leucemia - Mieloide - Aguda CorregidoDocumento6 páginasLeucemia - Mieloide - Aguda Corregidocarolinachillo0212Aún no hay calificaciones
- Cuestionario Inmuno S2Documento6 páginasCuestionario Inmuno S2Juan PurizacaAún no hay calificaciones
- Ejercicio OrtografiaDocumento3 páginasEjercicio OrtografiaAbel Henarejos AlmagroAún no hay calificaciones
- Resumen Hematologia GeriatricaDocumento7 páginasResumen Hematologia GeriatricaAgustin Martinez MoraAún no hay calificaciones
- Fernández, Silva, UrraDocumento41 páginasFernández, Silva, UrraPau Fer Mujica CAún no hay calificaciones
- EstoDocumento11 páginasEstokarina janampaAún no hay calificaciones
- Articulo CientificoDocumento19 páginasArticulo CientificoLuis alvaro Mejia tapiaAún no hay calificaciones
- Cuidados de Enfermeria en El Paciente Hemato-Oncologico - Jornadas Upc 17.10.2022Documento53 páginasCuidados de Enfermeria en El Paciente Hemato-Oncologico - Jornadas Upc 17.10.2022Lorena FlandezAún no hay calificaciones
- TRombocitopenia en NiñosDocumento18 páginasTRombocitopenia en NiñosBenjamin ValenzuelaAún no hay calificaciones
- PET y AlzheimerDocumento8 páginasPET y AlzheimerJosé Oscar Tarazona La TorreAún no hay calificaciones
- Monografia Enfermedad de AddisonDocumento10 páginasMonografia Enfermedad de AddisonAngélicaAún no hay calificaciones
- Proceso Onco-HematoDocumento21 páginasProceso Onco-HematoKatia AldanaAún no hay calificaciones
- Cuidados A Pacientes CrónicosDocumento25 páginasCuidados A Pacientes CrónicosOswaldo HernandezAún no hay calificaciones
- Proyecto GaucherDocumento8 páginasProyecto GaucherErnesto Méndez NavarroAún no hay calificaciones
- Guia Sindromes Mieloproliferativos AEALDocumento50 páginasGuia Sindromes Mieloproliferativos AEALMaria CoaboyAún no hay calificaciones
- Clínica Del Sistema Cardiovascular (Interrogatorio)Documento21 páginasClínica Del Sistema Cardiovascular (Interrogatorio)luis edgar gonzalez hernandezAún no hay calificaciones
- Semana 14-HipertiroidismoDocumento4 páginasSemana 14-HipertiroidismoShelley Roque LozadaAún no hay calificaciones
- Periodontitis Como Manifestación de Enfermedades SistémicasDocumento34 páginasPeriodontitis Como Manifestación de Enfermedades SistémicasDaniel GamarraAún no hay calificaciones
- Ensayo Terminado VeranoDocumento17 páginasEnsayo Terminado VeranoKarenina EscajadilloAún no hay calificaciones
- La Pandemia Del Siglo XxiDocumento6 páginasLa Pandemia Del Siglo XximilaqgroAún no hay calificaciones
- LeucemiaDocumento41 páginasLeucemiaCinthia GarciaAún no hay calificaciones
- Tesis Aun No TerminadaDocumento22 páginasTesis Aun No TerminadaYanet AyzanoaAún no hay calificaciones
- GPC Hemofilia - Version CortaDocumento24 páginasGPC Hemofilia - Version CortawaltermalcaAún no hay calificaciones
- Gammapatias Monoclonales Guia 2021 LibroDocumento48 páginasGammapatias Monoclonales Guia 2021 LibroEder paterninamartinezAún no hay calificaciones
- 556-Texto Del Artículo-3570-1-10-20200729Documento14 páginas556-Texto Del Artículo-3570-1-10-20200729Ešmęrąldą ŤôrôAún no hay calificaciones
- SialidosisDocumento3 páginasSialidosisapi-3697492Aún no hay calificaciones
- Monografia TerminadaDocumento19 páginasMonografia TerminadaWaltter EstucoAún no hay calificaciones
- 5 PriapismoDocumento3 páginas5 PriapismoDenise GuevaraAún no hay calificaciones
- Caso Clinico de MielomaDocumento11 páginasCaso Clinico de MielomaBryan CruzAún no hay calificaciones
- Jaime Restrepo Carmona Hemofilia en AntioquiaDocumento106 páginasJaime Restrepo Carmona Hemofilia en AntioquiaJaime Alonso Restrepo CarmonaAún no hay calificaciones
- Neurotransmisión en La Enfermedad de Alzheimer. Efectos en La Comunicación SinápticaDocumento15 páginasNeurotransmisión en La Enfermedad de Alzheimer. Efectos en La Comunicación SinápticaYADIRA HUAMAN ROMEROAún no hay calificaciones
- 120-Texto Del Artículo-906-1-10-20211001Documento17 páginas120-Texto Del Artículo-906-1-10-20211001Sara AspuruAún no hay calificaciones
- Aplasia Medular y Su Diagnc3b3stico en El LaboratorioDocumento47 páginasAplasia Medular y Su Diagnc3b3stico en El LaboratorioGrace CastilloAún no hay calificaciones
- 2 - HematologíaDocumento8 páginas2 - HematologíaAngy Sharon Aguilar LizarmeAún no hay calificaciones
- Formato Desarrollo Caso U1 m1 t8Documento17 páginasFormato Desarrollo Caso U1 m1 t8MARIELLA ESTEFANNY VALENTIN PE�AAún no hay calificaciones
- AlzheimerDocumento48 páginasAlzheimerdrmario311Aún no hay calificaciones
- SX de Marfan VIEDMADocumento13 páginasSX de Marfan VIEDMASabrina Viedma GonzalezAún no hay calificaciones
- Formato Desarrollo Caso U1 m1 t8Documento17 páginasFormato Desarrollo Caso U1 m1 t8MARIELLA ESTEFANNY VALENTIN PE�AAún no hay calificaciones
- Patologia General Fase 4 Grupo 151005 4Documento18 páginasPatologia General Fase 4 Grupo 151005 4MARIA FERNANDA MATAMOROS CARDENASAún no hay calificaciones
- Ficha ClinicaDocumento82 páginasFicha ClinicaCatalina Paz DiazAún no hay calificaciones
- 6 Hipocortisolismo Enfermedad de AddisonDocumento5 páginas6 Hipocortisolismo Enfermedad de AddisonPhoenix GeiaAún no hay calificaciones
- Tbi Bilirrubina Total para BS 1Documento2 páginasTbi Bilirrubina Total para BS 1Ulises Saldias RoaAún no hay calificaciones
- Microalbuminuria (Inmunoturbidimetría)Documento2 páginasMicroalbuminuria (Inmunoturbidimetría)Ulises Saldias RoaAún no hay calificaciones
- Verificación de Métodos Formulas Grupo 2Documento36 páginasVerificación de Métodos Formulas Grupo 2Ulises Saldias RoaAún no hay calificaciones
- Fósforo UV. InsertoDocumento2 páginasFósforo UV. InsertoUlises Saldias RoaAún no hay calificaciones
- MAU Control 1Documento1 páginaMAU Control 1Ulises Saldias RoaAún no hay calificaciones
- CK NAC. InsertoDocumento2 páginasCK NAC. InsertoUlises Saldias RoaAún no hay calificaciones
- MAU Calibrador 1Documento1 páginaMAU Calibrador 1Ulises Saldias RoaAún no hay calificaciones
- TG - Color - Gpo - Pap - Aa - Liquida - SP WinweDocumento9 páginasTG - Color - Gpo - Pap - Aa - Liquida - SP WinweUlises Saldias RoaAún no hay calificaciones
- AlbúminaDocumento2 páginasAlbúminaFernando100% (1)
- Colesterol HDL. InsertoDocumento2 páginasColesterol HDL. InsertoUlises Saldias RoaAún no hay calificaciones
- Amilasa (Cnp-G3) : Reactivo Líquido para La Determinación Fotométrica de La Amilasa en SueroDocumento2 páginasAmilasa (Cnp-G3) : Reactivo Líquido para La Determinación Fotométrica de La Amilasa en SueroUlises Saldias RoaAún no hay calificaciones
- CK MB. InsertoDocumento2 páginasCK MB. InsertoUlises Saldias RoaAún no hay calificaciones
- Thromborel - S Instrucciones de UsoDocumento7 páginasThromborel - S Instrucciones de UsoUlises Saldias Roa100% (2)
- Generalidades de La Terapia Transfusional: Irene Sánchez VadilloDocumento10 páginasGeneralidades de La Terapia Transfusional: Irene Sánchez VadilloUlises Saldias RoaAún no hay calificaciones
- Alteraciones Electrolíticas y Del Equilibrio Ácido-Base en La Enfermedad Renal Crónica AvanzadaDocumento7 páginasAlteraciones Electrolíticas y Del Equilibrio Ácido-Base en La Enfermedad Renal Crónica AvanzadaMiguel Angel Romero GaonaAún no hay calificaciones
- RIQAS - Completo EspañolDocumento38 páginasRIQAS - Completo EspañolUlises Saldias Roa100% (1)
- Trombopatías Congénitas y Adquiridas: Módulo Vi Hemostasia Y TrombosisDocumento6 páginasTrombopatías Congénitas y Adquiridas: Módulo Vi Hemostasia Y TrombosisUlises Saldias RoaAún no hay calificaciones
- Ref 3002 EdiOutubro2018 Rev - Ref270819 EspDocumento6 páginasRef 3002 EdiOutubro2018 Rev - Ref270819 EspUlises Saldias RoaAún no hay calificaciones
- Generalidades Sobre La Hemostasia. Diagnóstico de Los Trastornos de La HemostasiaDocumento8 páginasGeneralidades Sobre La Hemostasia. Diagnóstico de Los Trastornos de La HemostasiaUlises Saldias RoaAún no hay calificaciones
- Pauta Chequeo Lab. Clínico y Sala Toma MuestrasDocumento22 páginasPauta Chequeo Lab. Clínico y Sala Toma MuestrasUlises Saldias RoaAún no hay calificaciones
- Comparación Operadores Cuantitativa H20 E HernandezDocumento54 páginasComparación Operadores Cuantitativa H20 E HernandezUlises Saldias RoaAún no hay calificaciones
- E Hernandez Verificación de Proc de Medida de Serología InfecciosaDocumento55 páginasE Hernandez Verificación de Proc de Medida de Serología InfecciosaUlises Saldias RoaAún no hay calificaciones
- AX-06-IT-231.00-012 v2 MANUAL USUARIO HEMATO INMUN8060297Documento27 páginasAX-06-IT-231.00-012 v2 MANUAL USUARIO HEMATO INMUN8060297Ulises Saldias RoaAún no hay calificaciones
- Inst. Entrevista y Seleccion Del Donante de Sangre (v2)Documento10 páginasInst. Entrevista y Seleccion Del Donante de Sangre (v2)Ulises Saldias RoaAún no hay calificaciones
- Sedimento Urinario - 28022013A PDFDocumento14 páginasSedimento Urinario - 28022013A PDFTaniaRodriguez199509Aún no hay calificaciones
- Quien Descubrió La CélulaDocumento4 páginasQuien Descubrió La CélulaJancito Tlv Eps100% (1)
- 62 Cultivo Bacterias DAVID AGUDDocumento3 páginas62 Cultivo Bacterias DAVID AGUDAnaitz BeHappyAún no hay calificaciones
- Ensayo Sobre El CáncerDocumento2 páginasEnsayo Sobre El CáncerzandyAún no hay calificaciones
- Informe 05 de Biología - FragmentaciónDocumento11 páginasInforme 05 de Biología - FragmentaciónGenny Isabel Geldres PintoAún no hay calificaciones
- Clasificacion de La MicrobiologiaDocumento3 páginasClasificacion de La MicrobiologiaChristo Cruz González83% (6)
- CicloheximidaDocumento4 páginasCicloheximidaJesús IbarraAún no hay calificaciones
- ActinobacillusDocumento18 páginasActinobacillusThelma Cecilia Arce LaurelAún no hay calificaciones
- Salmonella NuevoDocumento9 páginasSalmonella NuevoDaniel Jonatan VelazquezAún no hay calificaciones
- Taller Genética Mendeliana y Reproducción VegetalDocumento9 páginasTaller Genética Mendeliana y Reproducción VegetaldianaAún no hay calificaciones
- Genética de Las Enfermedades MentalesDocumento3 páginasGenética de Las Enfermedades MentalesMoisés Alejandro Campos Díaz100% (1)
- Sistema Linfatico e Inmunologico - Escamilla Pérez AndreaDocumento40 páginasSistema Linfatico e Inmunologico - Escamilla Pérez AndreaAndrea Escamilla PerezAún no hay calificaciones
- Informe 6 de ParasitologíaDocumento8 páginasInforme 6 de ParasitologíaBryan Andres GuevaraAún no hay calificaciones
- ANTIHELMÍNTICOSDocumento13 páginasANTIHELMÍNTICOSValentina GutierrezAún no hay calificaciones
- Clase 1 Introduccion Flujo de Informacion GeneticaDocumento37 páginasClase 1 Introduccion Flujo de Informacion GeneticaKarina Susan D Carlos PerezAún no hay calificaciones
- Plan Profilactico de Aves PonedorasDocumento18 páginasPlan Profilactico de Aves PonedorasKenia Vanessa Hernández RamírezAún no hay calificaciones
- Variante Du.-2018 - PlataformaDocumento13 páginasVariante Du.-2018 - PlataformaDavidGutiérrez100% (1)
- Mapa Conceptual ProteinasDocumento1 páginaMapa Conceptual ProteinasTu NegroAún no hay calificaciones
- Fundamentos Basicos Del Derecho Genetico Enrique Varsi RospigliosiDocumento17 páginasFundamentos Basicos Del Derecho Genetico Enrique Varsi RospigliosiJhon Eddy Ccasani0% (1)
- Tema 5 Complejo Mayor HistocompatibilidadDocumento19 páginasTema 5 Complejo Mayor HistocompatibilidadANGEL BAQUEAún no hay calificaciones
- Actividad 1. Necesitamos Las Plantas para VivirDocumento4 páginasActividad 1. Necesitamos Las Plantas para VivirDavid Rafael Medina Galindo50% (2)
- Clase InmunidadDocumento16 páginasClase InmunidadMaria Alejandra Caicedo EscateAún no hay calificaciones
- Actividad 01 - S8Documento2 páginasActividad 01 - S8Yeshika Barrera TiconaAún no hay calificaciones
- VacunasDocumento14 páginasVacunasMercedez GavidiaAún no hay calificaciones
- Observaciones FenológicasDocumento28 páginasObservaciones Fenológicaswalfer yocAún no hay calificaciones
- 12 SepsisDocumento14 páginas12 Sepsisrichard alarconAún no hay calificaciones
- Crianza de Limnae (Fossaria) Viatrix (Caracol) - Primer Huesped Intermediario de Fasciola Hepática.Documento19 páginasCrianza de Limnae (Fossaria) Viatrix (Caracol) - Primer Huesped Intermediario de Fasciola Hepática.Carlos Manuel Carranza VegaAún no hay calificaciones
- Conceptos Básicos de Ecología y AmbienteDocumento31 páginasConceptos Básicos de Ecología y AmbienteDavid AndrésAún no hay calificaciones
- Universidad de San Carlos de Guatemala Facultad de Ingeniería Escuela de Ingeniería QuímicaDocumento220 páginasUniversidad de San Carlos de Guatemala Facultad de Ingeniería Escuela de Ingeniería QuímicaChristian Alex Barroso OrtizAún no hay calificaciones
- Resumen NutricionDocumento43 páginasResumen NutricionSHIRLEY CASTROAún no hay calificaciones
- Aplicación de Nuevas Tecnologías en La Conservación de PescadoDocumento3 páginasAplicación de Nuevas Tecnologías en La Conservación de PescadomariaAún no hay calificaciones
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- Liberación del trauma: Perdón y temblor es el caminoDe EverandLiberación del trauma: Perdón y temblor es el caminoCalificación: 4 de 5 estrellas4/5 (4)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- Dieta Para El Reflujo Biliar y Gastritis Alcalina - Incluye 20 Deliciosas Recetas Libres de Gluten y de Lácteos Para Tratar y Aliviar el Reflujo Biliar y Sus Molestos SíntomasDe EverandDieta Para El Reflujo Biliar y Gastritis Alcalina - Incluye 20 Deliciosas Recetas Libres de Gluten y de Lácteos Para Tratar y Aliviar el Reflujo Biliar y Sus Molestos SíntomasCalificación: 4 de 5 estrellas4/5 (9)
- Sistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)De EverandSistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)Calificación: 5 de 5 estrellas5/5 (9)
- Guía práctica para la refracción ocularDe EverandGuía práctica para la refracción ocularCalificación: 5 de 5 estrellas5/5 (2)
- Ondas de choque extracorpóreas radiales: Aplicación en patologías músculo esqueléticasDe EverandOndas de choque extracorpóreas radiales: Aplicación en patologías músculo esqueléticasCalificación: 5 de 5 estrellas5/5 (3)
- Cerebro y silencio: Las claves de la creatividad y la serenidadDe EverandCerebro y silencio: Las claves de la creatividad y la serenidadCalificación: 5 de 5 estrellas5/5 (2)
- Sana tu Cuerpo, Calma tu Mente: Desintoxicar Hígado, Intestino Permeable, Salud Hormonal, Curación Emocional, Relajación, Ansiedad y Sanidad mental, Atención Plena, Psicoterapia y NutriciónDe EverandSana tu Cuerpo, Calma tu Mente: Desintoxicar Hígado, Intestino Permeable, Salud Hormonal, Curación Emocional, Relajación, Ansiedad y Sanidad mental, Atención Plena, Psicoterapia y NutriciónCalificación: 5 de 5 estrellas5/5 (4)
- Homo antecessor: El nacimiento de una especieDe EverandHomo antecessor: El nacimiento de una especieCalificación: 5 de 5 estrellas5/5 (1)
- 50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaDe Everand50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaCalificación: 4 de 5 estrellas4/5 (37)
- Muchas Vidas, Muchos Sabios (Many Lives, Many Masters): (Many Lives, Many Masters)De EverandMuchas Vidas, Muchos Sabios (Many Lives, Many Masters): (Many Lives, Many Masters)Calificación: 4 de 5 estrellas4/5 (475)
- Hematología. Casos clínicos: preguntas y respuestasDe EverandHematología. Casos clínicos: preguntas y respuestasCalificación: 4 de 5 estrellas4/5 (4)
- El código de la obesidad: Descifrando los secretos de la pérdida de pesoDe EverandEl código de la obesidad: Descifrando los secretos de la pérdida de pesoCalificación: 4.5 de 5 estrellas4.5/5 (51)
- Cerebros rotos: Pacientes asombrosos que me enseñaron a vivirDe EverandCerebros rotos: Pacientes asombrosos que me enseñaron a vivirCalificación: 5 de 5 estrellas5/5 (3)
- Historia del cuerpo humano: Evolución, salud y enfermedadDe EverandHistoria del cuerpo humano: Evolución, salud y enfermedadAún no hay calificaciones
- La comida y el inconsciente: Psicoanálisis y trastornos alimentariosDe EverandLa comida y el inconsciente: Psicoanálisis y trastornos alimentariosAún no hay calificaciones
- Sesgos Cognitivos: Una Fascinante Mirada dentro de la Psicología Humana y los Métodos para Evitar la Disonancia Cognitiva, Mejorar sus Habilidades para Resolver Problemas y Tomar Mejores DecisionesDe EverandSesgos Cognitivos: Una Fascinante Mirada dentro de la Psicología Humana y los Métodos para Evitar la Disonancia Cognitiva, Mejorar sus Habilidades para Resolver Problemas y Tomar Mejores DecisionesCalificación: 4.5 de 5 estrellas4.5/5 (13)
- 200 tareas en terapia breve: 2ª ediciónDe Everand200 tareas en terapia breve: 2ª ediciónCalificación: 4.5 de 5 estrellas4.5/5 (33)
- Lactancia humana y fonoaudiología: Guía para madres lactantesDe EverandLactancia humana y fonoaudiología: Guía para madres lactantesCalificación: 5 de 5 estrellas5/5 (4)
- El concepto Mulligan de terapia manual (Color)De EverandEl concepto Mulligan de terapia manual (Color)Calificación: 5 de 5 estrellas5/5 (3)
- GuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisDe EverandGuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisCalificación: 4 de 5 estrellas4/5 (9)
- El Libro de la Dieta Antiinflamatoria: Plan de 14 días para Sanar el Sistema inmunológico y Sentirte Mejor que NuncaDe EverandEl Libro de la Dieta Antiinflamatoria: Plan de 14 días para Sanar el Sistema inmunológico y Sentirte Mejor que NuncaCalificación: 4.5 de 5 estrellas4.5/5 (14)
- La medicina biorreguladora: Un enfoque holístico e innovador de la autocuraciónDe EverandLa medicina biorreguladora: Un enfoque holístico e innovador de la autocuraciónCalificación: 3.5 de 5 estrellas3.5/5 (2)
- La increíble conexión intestino cerebro: Descubre la relación entre las emociones y el equilibrio intestinalDe EverandLa increíble conexión intestino cerebro: Descubre la relación entre las emociones y el equilibrio intestinalCalificación: 4.5 de 5 estrellas4.5/5 (103)