Documentos de Académico
Documentos de Profesional
Documentos de Cultura
TPCU3.en ESPAÑOL
Cargado por
Waiola VaitiareDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
TPCU3.en ESPAÑOL
Cargado por
Waiola VaitiareCopyright:
Formatos disponibles
Traducido del inglés al español - www.onlinedoctranslator.
com
PAG 3
t
12.0
C
010333
Ud.
382519 0c501V
Proteína Total Orina/LCR Gen. 3
Información de pedido
Analizador(es) en el quecobas cse pueden utilizar paquetes
03333825190 Proteína Total Orina/LCR Gen.3 150 pruebas ID del sistema 07 6763 8 Roche-Hitachicobas c311,cobasco501/502
03121305122 Cfas PUC (5 x 1 ml) Código 489
03121313122 Precinorm PUC (4 x 3 ml) Código 240
03121291122 Precipath PUC (4 x 3 ml) Código 241
04489357190 Diluyente NaCl 9 % (50 mL) ID del sistema 07 6869 3
Inglés Este kit contiene componentes clasificados de la siguiente manera de acuerdo con el
Reglamento (CE) nº 1272/2008:
Información del sistema
Paracobas cAnalizadores 311/501:
TPU3:ACN 708
TPC3:ACN 402
Paracobas cAnalizador 502:
TPU3:ACN 8708 Peligro
TPC3:ACN 8402
H290 Puede ser corrosivo para los metales.
Uso previsto
Prueba in vitro para la determinación cuantitativa de proteínas en orina y líquido H314 Provoca quemaduras graves en la piel y daños oculares.
cefalorraquídeo humanos en Roche/Hitachicobas csistemas.
H412 Nocivo para la vida acuática con efectos duraderos.
Resumen
Las mediciones de proteínas en la orina se utilizan en el diagnóstico y tratamiento de Prevención:
enfermedades como enfermedades renales o cardíacas, o trastornos de la tiroides,
que se caracterizan por proteinuria o albuminuria. Las mediciones de proteínas del
P234 Mantener solo en el envase original.
líquido cefalorraquídeo (LCR) se utilizan en el diagnóstico y tratamiento de afecciones
como meningitis, tumores cerebrales e infecciones del sistema nervioso central.1 P264 Lave bien la piel después de la manipulación.
P273 Evitar su liberación al medio ambiente.
La orina se forma por ultrafiltración de plasma a través de la pared capilar glomerular. Las proteínas con
una masa molecular relativa > 40 000 se retienen casi por completo, mientras que las sustancias más
pequeñas ingresan fácilmente al filtrado glomerular. La mayor parte de las proteínas del LCR se originan
P280 Utilice guantes/ropa protectora/protección para los ojos/
por difusión desde el plasma a través de la barrera hematoencefálica. Los niveles elevados se producen protección facial.
como resultado de una mayor permeabilidad de la barrera hematoencefálica o del aumento de la síntesis
Respuesta:
local de inmunoglobulinas.
Los métodos turbidimétricos que utilizan ácido tricloroacético (TCA) o ácido sulfosalicílico (SSA) P301 + P330 EN CASO DE INGESTIÓN: Enjuagar la boca. No induzca el vomito.
precipitan las proteínas en la muestra según su tamaño; la turbidez resultante puede ser + P331
inestable y flocular. Los reactivos de los métodos de unión de colorantes, como el azul de
Coomassie y el rojo de pirogalol y molibdato, reaccionan con las proteínas dependiendo de su P303 + P361 EN CASO DE CONTACTO CON LA PIEL (o el cabello): Quitar/quitar inmediatamente
composición de aminoácidos, pero pueden manchar vidrio y artículos de plástico. Debido a sus
+ P353 toda la ropa contaminada. Enjuague la piel con agua/ducha.
mecanismos de reacción, todos los métodos, turbidimétricos y colorimétricos, presentan
diferentes sensibilidades a diversas proteínas, especialmente a fragmentos de proteínas como
P304 + P340 EN CASO DE INHALACIÓN: Lleve a la persona al aire libre y
las proteínas de Bence Jones.2y proteínas pequeñas como la α1-microglobulina.
manténgala cómoda para respirar.
El ensayo de proteína en orina/LCR de Roche Diagnostics se basa en el método descrito
P305 + P351 EN CASO DE CONTACTO CON LOS OJOS: Enjuague cuidadosamente con agua durante varios
por Iwata y Nishikaze,3posteriormente modificado por Luxton, Patel, Keir y Thompson.
4En este método, el cloruro de bencetonio reacciona con la proteína en un medio
+ P338 minutos. Quítese los lentes de contacto, si están presentes y son fáciles de hacer. Continúe
básico para producir una turbidez más estable y distribuida uniformemente que la enjuagando.
observada con las metodologías SSA o TCA. Este ensayo muestra una recuperación
insuficiente de γ‑globulina en comparación con la albúmina de alrededor del 30 %,5y P310 Llame inmediatamente a un CENTRO DE TOXICOLOGÍA o a un médico.
sin interferencia de iones de magnesio debido a la adición de EDTA.
P337 + P313 Si la irritación de los ojos persiste: busque atención o asesoramiento médico.
Principio de prueba
P363 Lave la ropa contaminada antes de volver a usarla.
Método turbidimétrico.
La muestra se preincuba en una solución alcalina que contiene EDTA, que P390 Absorber los derrames para evitar daños materiales.
desnaturaliza la proteína y elimina la interferencia de los iones de magnesio.
Luego se añade cloruro de bencetonio, lo que produce turbidez. Almacenamiento:
Reactivos - soluciones de trabajo P405 Tienda cerrada.
R1 Hidróxido de sodio: 677 mmol/L; EDTA‑Na: 74 mmol/L
P406 Almacenar en un recipiente de acero inoxidable resistente a la corrosión con un
R2 Cloruro de bencetonio: 32 mmol/L revestimiento interior resistente.
R1 está en la posición B y R2 está en la posición C. Desecho:
Precauciones y advertencias
P501 Eliminar el contenido/el recipiente en una planta de eliminación de
Para uso diagnóstico in vitro.
residuos aprobada.
Tome las precauciones normales necesarias para manipular todos los reactivos de
laboratorio. El etiquetado de seguridad del producto sigue principalmente las directrices del SGA de la
La eliminación de todo el material de desecho debe realizarse de acuerdo con las pautas locales. Ficha de UE. Teléfono de contacto: todos los países: +49-621-7590
datos de seguridad disponible para el usuario profesional que la solicite.
2015-05, V 12.0 Inglés 1/4
PAG 3
t
12.0
C
010333
Ud.
382519 0c501V
Proteína Total Orina/LCR Gen. 3
Manejo de reactivos Pipeteo de reactivos Diluyente (H2Oh)
Listo para usar R1 100 µL –
Almacenamiento y estabilidad
R2 40 µL –
TPUC3 Volúmenes de muestra Muestra Muestra
Periodo de validez a 15‑25 °C: Ver fecha de caducidad dilución
encobas cembalar Muestra Diluyente
etiqueta. (NaCl)
A bordo en uso y refrigerado en el analizador: Diluyente 6 semanas Normal 6 µL – –
NaCl 9 % Periodo de validez a 2‑8 °C: Disminuido 2 µL – –
Ver fecha de caducidad Aumentó 6 µL – –
encobas cembalar
etiqueta. cobas c501definición de prueba
A bordo en uso y refrigerado en el analizador: 12 semanas Tipo de ensayo Extremo de 2 puntos
Tiempo de reacción / 10 / 10‑30
Recolección y preparación de muestras.
Puntos de ensayo
Para la recogida y preparación de muestras utilice únicamente tubos o recipientes
de recogida adecuados. Longitud de onda 700/505 nanómetro
Sólo los especímenes enumerados a continuación fueron probados y considerados (sub principal)
aceptables. Orina Dirección de reacción Aumentar
Utilice muestras de orina aleatorias o de 24 horas. No utilice conservantes. Refrigere la muestra
unidades mg/L (mg/dL, g/L)
durante la recolección.
LCR Pipeteo de reactivos Diluyente (H2Oh)
No se requieren aditivos especiales. La sangre en una muestra de LCR invalida el valor R1 100 µL –
de proteínas.1
R2 40 µL –
Se deben recolectar muestras de proteína en orina/LCR antes de administrar
Volúmenes de muestra Muestra Dilución de muestra
fluoresceína o al menos 24 horas después.6
Nota:Las muestras de orina, LCR y control con una concentración de proteínas superior a Muestra Diluyente (NaCl)
7000 mg/l no deben medirse con TPUC3, ya que esto puede obstruir las líneas del
Normal 6 µL – –
instrumento.
Disminuido 2 µL – –
Estabilidad:7
Aumentó 6 µL – –
Orina: 1 día a 15‑25 °C
cobas c502definición de prueba
7 días a 2‑8 °C
Tipo de ensayo
1 mes a (-15)‑(-25) °C 1 Extremo de 2 puntos
10 / 10‑30
LCR: día a 15‑25 °C
Tiempo de reacción /
Puntos de ensayo
6 días a 2‑8 °C
Longitud de onda 700/505 nanómetro
> 1 año a (-15)‑(-25) °C (sub principal)
Centrifugar las muestras que contengan precipitados antes de realizar el ensayo. Las Dirección de reacción Aumentar
muestras no centrifugadas pueden producir resultados elevados.
unidades mg/L (mg/dL, g/L)
Materiales proporcionados
Pipeteo de reactivos Diluyente (H 2 Oh)
Consulte la sección "Reactivos: soluciones de trabajo" para conocer los reactivos.
R1 100 µL –
Materiales necesarios (pero no proporcionados)
R2 40 µL –
▪ Ver apartado “Información del pedido”
Volúmenes de muestra Muestra Dilución de muestra
▪ Equipo general de laboratorio
Muestra Diluyente (NaCl)
Ensayo
Para un rendimiento óptimo del ensayo, siga las instrucciones proporcionadas en este documento Normal 6 µL – –
para el analizador en cuestión. Consulte el manual del operador correspondiente para obtener
Disminuido 2 µL – –
instrucciones de ensayo específicas del analizador.
El rendimiento de las aplicaciones no validadas por Roche no está garantizado y Aumentó 12 µL – –
debe ser definido por el usuario.
Calibración
Solicitud de orina y LCR
Calibradores T1: H2oh
cobas c311definición de prueba
T2‑S6: Cfas PUC
Tipo de ensayo Extremo de 2 puntos
Multiplique los valores del calibrador Cfas PUC específicos del
Tiempo de reacción/puntos de ensayo 10 / 6‑14 lote por los factores que se indican a continuación para
Longitud de onda (sub/principal) 700/505 nanómetro determinar las concentraciones estándar para la curva de
calibración de 6 puntos.
Dirección de reacción Aumentar
Unidades mg/L (mg/dL, g/L)
2/4 2015-05, V 12.0 Inglés
PAG 3
t
12.0
C
010333
Ud.
382519 0c501V
Proteína Total Orina/LCR Gen. 3
S2: 0,025 S5: 0,250 Cuando sea necesario, se debe implementar una programación especial de evasión de
lavado/transferencia antes de informar los resultados de esta prueba.
S3: 0,050 S6: 1,0
Límites y rangos
S4: 0,125
Rango de medición
Modo de calibración RCM 40‑2000 mg/L (4‑200 mg/dL; 0,04‑2 g/L)
Frecuencia de calibración Calibración completa Determine muestras que tengan concentraciones más altas mediante la función de repetición. La
dilución de muestras mediante la función de repetición es una dilución 1:3. Los resultados de las
- después del cambio de lote de reactivos
muestras diluidas con la función de repetición se multiplican automáticamente por un factor de 3.
- según sea necesario siguiendo los procedimientos de
control de calidad
Límites inferiores de medición
Trazabilidad:8Este método se ha estandarizado con respecto a un estándar Límite inferior de detección de la
primario rastreable hasta NIST.
prueba. 40 mg/L (4 mg/dL; 0,04 g/L)
Control de calidad El límite de detección inferior representa el nivel de analito medible más bajo que
Para el control de calidad, utilice los materiales de control que se enumeran en la sección "Información del pedido". se puede distinguir de cero. Se calcula como el valor que se encuentra
3 desviaciones estándar por encima del estándar más bajo (estándar 1 + 3 DE,
Además, se pueden utilizar otros materiales de control adecuados. repetibilidad, n = 21).
Los intervalos y límites de control deben adaptarse a los requisitos individuales de Valores esperados
cada laboratorio. Los valores obtenidos deben estar dentro de los límites definidos.
Cada laboratorio debe establecer medidas correctivas a tomar si los valores caen Orina:12 24h: < 140 mg/24 h*
fuera de los límites definidos. aleatorio: < 150 mg/L*
Siga las regulaciones gubernamentales aplicables y las pautas locales para el
*Valores obtenidos de muestras centrifugadas
control de calidad.
LCR: rango de referencia según a Tietz:
Cálculo
150‑450 mg/L (15‑45 mg/dL)13
Roche-Hitachicobas cLos sistemas calculan automáticamente la
concentración de analito de cada muestra. rango de referencia según a Thomas:
200-400 mg/L (20-40 mg/dL)14
Factores de conversión: mg/L x 0,1 = mg/dL
Cada laboratorio debe investigar la transferibilidad de los valores esperados a su propia
mg/L x 0,001 = g/L población de pacientes y, si es necesario, determinar sus propios rangos de referencia.
Para calcular la excreción de proteínas en orina de 24 horas:
mg/L x volumen total (litros por 24 horas) = mg/día. Datos de rendimiento específicos
A continuación se proporcionan datos de rendimiento representativos de los analizadores. Los
Limitaciones - interferencia
resultados obtenidos en laboratorios individuales pueden diferir.
Criterio: Recuperación dentro de ± 10 % del valor inicial con una concentración de
proteína total de 120 mg/L (12 mg/dL; 0,12 g/L). Precisión
Efecto gancho de dosis alta: los resultados de las muestras con altas concentraciones de La precisión se determinó utilizando muestras y controles humanos en un protocolo
proteína total por encima del rango de medición de hasta 100000 mg/L serán marcados por el interno con repetibilidad (n = 21) y precisión intermedia (3 alícuotas por ejecución, 1
instrumento con > TEST o > ABS. ejecución por día, 21 días). Los siguientes resultados fueron obtenidos:
Orina
Orina
Ictericia: No hay interferencia significativa hasta una concentración de 342
µmol/L (20 mg/dL) para la bilirrubina conjugada.
Repetibilidad Significar Dakota del Sur CV
Hemólisis: interfiere la hemoglobina.9 mg/L (mg/dL) mg/L (mg/dL) %
Fármacos: No se encontraron interferencias en concentraciones terapéuticas utilizando paneles PUC precinorm 159 (15,9) 1 (0,1) 0,7
de fármacos comunes.10
Precipato PUC 1576 (158) 8 (0,8) 0,5
Excepción: Levodopa, metildopa y Na2La cefoxitina provoca resultados de proteínas totales
artificialmente elevados y el dobesilato de calcio provoca resultados de proteínas artificialmente bajos. Orina humana 1 101 (10,1) 1 (0,1) 1.0
Orina humana 2 191 (19,1) 4 (0,4) 2.2
Otros: Las muestras de pacientes que contienen > 8 g/l de yodo unido orgánicamente de
medios radiopacos (p. ej., Hexabrix) pueden tener resultados falsamente elevados.
Precisión intermedia Significar Dakota del Sur CV
Se pueden encontrar altos niveles de ácido homogentísico en la orina de pacientes con el raro
trastorno genético alcaptonuria.11El ácido homogentísico en muestras de orina en
mg/L (mg/dL) mg/L (mg/dL) %
concentraciones > 0,6 mmol/L puede provocar resultados falsos. PUC precinorm 156 (15,6) 2 (0,2) 1.5
La administración de sustitutos plasmáticos a base de gelatina puede provocar un aumento de
Precipato PUC 1482 (148) 8 (0,8) 0,5
los valores de proteínas en la orina.
LCR Orina humana 3 106 (10,6) 2 (0,2) 1.6
Hemólisis: interfiere la hemoglobina.9 Orina humana 4 154 (15,4) 1 (0,1) 0,9
Para fines de diagnóstico, los resultados siempre deben evaluarse junto
con el historial médico del paciente, el examen clínico y otros hallazgos.
LCR
ACCIÓN REQUERIDA Repetibilidad Significar Dakota del Sur CV
Programación de Lavado Especial:El uso de pasos de lavado especiales es obligatorio cuando
ciertas combinaciones de pruebas se ejecutan juntas en Roche/Hitachi. cobas csistemas. La mg/L (mg/dL) mg/l (mg/dl) %
última versión de la lista de evasión de transferencia se puede encontrar en las hojas de
Nivel de control 1 281 (28,1) 4 (0,4) 1.5
métodos NaOHD-SMS-SmpCln1+2-SCCS. Para obtener más instrucciones, consulte el manual
del operador.cobas cAnalizador 502: toda la programación de lavado especial necesaria para Nivel de control 2 691 (69,1) 4 (0,4) 0,6
evitar el arrastre está disponible a través delcobasenlace, no se requiere entrada manual.
LCR humano 1 355 (35,5) 4 (0,4) 1.1
2015-05, V 12.0 Inglés 3/4
PAG 3
t
12.0
C
010333
Ud.
382519 0c501V
Proteína Total Orina/LCR Gen. 3
LCR humano 2 517 (51,7) 5 (0,5) 1.0 14 Thomas L. Labor und Diagnose, 6. Auflage, TH-Books
Verlagsgesellschaft mbH, Frankfurt/Main 2005;930-934.
Precisión intermedia Significar Dakota del Sur CV 15 Bablok W, Passing H, Bender R, et al. Un procedimiento de regresión general para la
mg/L (mg/dL) mg/L (mg/dL) % transformación de métodos. Aplicación de procedimientos de regresión lineal para
estudios de comparación de métodos en química clínica, Parte III. J Clin Chem Clin
Nivel de control 1 272 (27,2) 4 (0,4) 1.6 Biochem 1988 noviembre;26(11):783-790.
Nivel de control 2 660 (66,0) 6 (0,6) 0,9 En esta Hoja de Método siempre se utiliza un punto (punto/parada) como
separador decimal para marcar el límite entre las partes integral y fraccionaria de
LCR humano 3 349 (34,9) 4 (0,4) 1.2 un número decimal. No se utilizan separadores de miles.
LCR humano 4 501 (50,1) 7 (0,7) 1.5 Símbolos
Comparación de métodos Roche Diagnostics utiliza los siguientes símbolos y signos además de los
Valores de proteínas totales para muestras de orina y LCR humanas enumerados en la norma ISO 15223‑1.
obtenidas en un Roche/Hitachicobas c501 (y) se compararon con los
Contenido del kit
determinados con el reactivo correspondiente en un analizador Roche/
Hitachi 917 (x). Volumen después de la reconstitución o mezcla
Orina
GTIN Número de artículo comercial global
Tamaño de la muestra (n) = 70
COBAS, COBAS C, PRECINORM y PRECIPATH son marcas comerciales de Roche. Todos los demás nombres de
Pasando/Bablok15 Regresión lineal
productos y marcas comerciales son propiedad de sus respectivos dueños. Las adiciones, eliminaciones o
y = 0,985x + 6,23 mg/L τ y = 0,988x + 5,35 mg/L r cambios se indican mediante una barra de cambios en el margen.
© 2015, Diagnóstico Roche
= 0,970 = 1,000
Las concentraciones de la muestra estuvieron entre 47,0 y 1887 mg/L (4,70 y
189 mg/dL).
LCR Roche Diagnostics GmbH, Sandhofer Strasse 116, D-68305 Mannheim
www.roche.com
Tamaño de la muestra (n) = 86
Pasando/Bablok15 Regresión lineal
y = 1,015x - 7,51 mg/L τ y = 1,010x - 5,23 mg/l r
= 0,975 = 0,999
Las concentraciones de la muestra estuvieron entre 53,0 y 1087 mg/L (5,30 y
109 mg/dL).
Referencias
1 Tietz NO. Fundamentos de Química Clínica, 3ª ed. Pensilvania: WB
Saunders Co 1987:336.
2 Boege F. Bence Jones-Proteína. J Lab Med 1999;23(9):477-482.
3 Iwata J, Nishikaze O. Nuevo método microturbidimétrico para la determinación de
proteínas en el líquido cefalorraquídeo y la orina. Clínica Química
1979;25(7):1317-1319.
4 Luxton RW, Patel P, Keir G, et al. Un micrométodo para medir la proteína total en el
líquido cefalorraquídeo mediante el uso de cloruro de bencetonio en pocillos de placas
de microtitulación. Clin Chem 1989;35(8):1731-1734.
5 Hohnadel DC, Koller A. Proteína total en orina. En: Pesce AJ, Kaplan LA,
editores. Métodos en química clínica, St. Louis, Mosby 1987.
6 Koumantakis G. Interferencia de la fluoresceína con las mediciones de proteínas
y creatinina en orina. Clin Chem 1991;37/10:1799.
7 Publicación de la OMS: Uso de anticoagulantes en investigaciones de laboratorio
de diagnóstico, WHO/DIL/LAB/99.1 Rev.2: enero de 2002.
8 Materiales de referencia estándar de NERL, rastreables hasta NIST
(Instituto Nacional de Estándares y Tecnología).
9 Yilmaz FM, Yücel D. Efecto de la adición de hemolizado en ensayos de
proteínas en orina y líquido cefalorraquídeo. Clin Chem 2006;52:152-153.
10 Sonntag O, Scholer A. Interferencia de fármacos en química clínica:
recomendación de fármacos y sus concentraciones para su uso en estudios de
interferencia de fármacos. Ann Clin Biochem 2001;38:376-385.
11 Phornphutkul C, Introne WJ, Perry MB y col. Historia natural de la
alcaptonuria. N Engl J Med 2002;347(26):2111-2121.
12 Junge W, Wilke B, Halabi A, et al. Intervalos de referencia para proteína total
en orina recolectada y aleatoria u canta el cloruro de bencetonio
Método [Resumen]. Clin Chem 2006;52:157.
13 Tietz NW, ed. ClínicoGRAMO Guía de pruebas de laboratorio, 3ª ed.
Filadelfia, PA: WB Saunders Company 1995;518-523.
4/4 2015-05, V 12.0 Inglés
También podría gustarte
- Calificación CAQDocumento13 páginasCalificación CAQStéfano Durán Solórzano67% (9)
- Insert CHOL2 0008057443190c503 V2 EsDocumento4 páginasInsert CHOL2 0008057443190c503 V2 EsJuan José Damian Salazar50% (2)
- Universidad Estatal Del Sur de Manabí: Informacion General EstudiantesDocumento19 páginasUniversidad Estatal Del Sur de Manabí: Informacion General EstudiantesElvia León100% (1)
- Higiene y Manipulación de AlimentosDocumento80 páginasHigiene y Manipulación de AlimentosLiceth Lubo ArgumedoAún no hay calificaciones
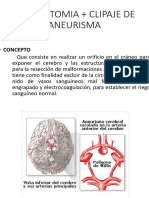
- Craneotomia + Clipaje de AneurismaDocumento14 páginasCraneotomia + Clipaje de AneurismaJuan Carlos Cordova100% (1)
- Show Document Prot TOrinaDocumento4 páginasShow Document Prot TOrinaDra. Lisy BarçaAún no hay calificaciones
- Proteinas OrinaDocumento4 páginasProteinas Orinayuya_sol100% (1)
- Proteinas TotDocumento3 páginasProteinas Totyuya_solAún no hay calificaciones
- Seminario Western BlotDocumento71 páginasSeminario Western BlotLilian Zoraida ACAún no hay calificaciones
- Transferrinac501u V2 EsDocumento4 páginasTransferrinac501u V2 EsAle ZevallosAún no hay calificaciones
- A Determinacion de ColinesterasaDocumento4 páginasA Determinacion de ColinesterasaMarielaAún no hay calificaciones
- Transferrin ADocumento4 páginasTransferrin ARoberto AriasAún no hay calificaciones
- Proteinas TotalesDocumento4 páginasProteinas Totalesoctavio omar villegasAún no hay calificaciones
- Insert - Fibrinogen.ms 07153473190.v3.esDocumento3 páginasInsert - Fibrinogen.ms 07153473190.v3.esGerardo SoteloAún no hay calificaciones
- Insert - Elecsys FT3 III.09005811500.V2.es-1Documento4 páginasInsert - Elecsys FT3 III.09005811500.V2.es-1ronald lopezAún no hay calificaciones
- Insert - Elecsys FT3 III.09005811500.V3.es-6Documento4 páginasInsert - Elecsys FT3 III.09005811500.V3.es-6ronald lopezAún no hay calificaciones
- Anteced Proteínas Plasmáticas 2401Documento20 páginasAnteced Proteínas Plasmáticas 2401luis enrique islas garciaAún no hay calificaciones
- Western Blot PIADocumento27 páginasWestern Blot PIAJavier LealAún no hay calificaciones
- TPDocumento3 páginasTPjuan solos100% (1)
- Nefrología Básica 2Documento20 páginasNefrología Básica 2Lopez Alvarado JheisonAún no hay calificaciones
- Informe 2-Bioquimica LabDocumento8 páginasInforme 2-Bioquimica LabIvett Dayana Pérez CastilloAún no hay calificaciones
- Insert - Elecsys Prolactin II.03203093500.V11.esDocumento5 páginasInsert - Elecsys Prolactin II.03203093500.V11.esLab San SebastianAún no hay calificaciones
- TP Baosr6x3211Documento10 páginasTP Baosr6x3211AdrianaManouAún no hay calificaciones
- Práctica 3 - DiagramaDocumento1 páginaPráctica 3 - Diagramaisrragame7Aún no hay calificaciones
- MicroalbuminaDocumento7 páginasMicroalbuminaoctavio omar villegasAún no hay calificaciones
- ProteinasDocumento4 páginasProteinasDulce Daniela Amador CastilloAún no hay calificaciones
- Informe 2 - Determinación de La Concentración Sérica de Proteínas Totales y FraccionadasDocumento10 páginasInforme 2 - Determinación de La Concentración Sérica de Proteínas Totales y FraccionadasAlex MendivilAún no hay calificaciones
- Analisis de Proteinas: Electroforesis, Transferencia e InmunoprecipitaciónDocumento24 páginasAnalisis de Proteinas: Electroforesis, Transferencia e InmunoprecipitaciónMaría McSharryAún no hay calificaciones
- Western BlotDocumento5 páginasWestern BlotOrlando SevillanoAún no hay calificaciones
- ProteinasDocumento4 páginasProteinasDulce Daniela Amador CastilloAún no hay calificaciones
- Determinación de Proteínas Totales y Albúmina en SueroDocumento9 páginasDeterminación de Proteínas Totales y Albúmina en SueroRocio Reyes Cueva100% (1)
- Extracción y Cuantificación de ProteínasDocumento5 páginasExtracción y Cuantificación de ProteínasFiore MotesAún no hay calificaciones
- Practica No 3 Extraccion de ArnDocumento10 páginasPractica No 3 Extraccion de ArnBianca Buck67% (3)
- Nº 6 Proteinas Totales y Sus Fracciones23Documento7 páginasNº 6 Proteinas Totales y Sus Fracciones23Monica Peredo OrtizAún no hay calificaciones
- Astl - TgoDocumento4 páginasAstl - TgoChristian MartinoniAún no hay calificaciones
- Proteinuria Rojo de PirogalolDocumento3 páginasProteinuria Rojo de PirogalolJuly QBAún no hay calificaciones
- Polyclonal Rabbit Anti-Human Synaptophysin #De Catálogo A 0010Documento2 páginasPolyclonal Rabbit Anti-Human Synaptophysin #De Catálogo A 0010Neiz Valverde PorrasAún no hay calificaciones
- Lab. Clinica Proteinas Totales PDocumento3 páginasLab. Clinica Proteinas Totales Pjvasquezl3Aún no hay calificaciones
- Resumen IHQ y ELISADocumento9 páginasResumen IHQ y ELISAMari MendozaAún no hay calificaciones
- Westen Blot yDocumento34 páginasWesten Blot yJulio Laurel AriasAún no hay calificaciones
- Western Blot PresentaciónDocumento33 páginasWestern Blot PresentaciónAndres MoralesAún no hay calificaciones
- Guà - A 025 EXTRACCIà - N Y CUANTIFICACIà - N DE PROTEà - NAS DE SUERO SANGUà - NEO PARA ELECTROFORESISDocumento3 páginasGuà - A 025 EXTRACCIà - N Y CUANTIFICACIà - N DE PROTEà - NAS DE SUERO SANGUà - NEO PARA ELECTROFORESISYuli Alejandra Torres RequinivaAún no hay calificaciones
- Inmunodeteccion Directa e IndirectaDocumento2 páginasInmunodeteccion Directa e IndirectaVeronica MejiaAún no hay calificaciones
- Informe PR 13Documento7 páginasInforme PR 13Janella RodríguezAún no hay calificaciones
- Practica 10Documento6 páginasPractica 10Gacha MaxAún no hay calificaciones
- ASTL 0020764949322c501 V16 EsDocumento4 páginasASTL 0020764949322c501 V16 Escalidadsedecorpas lab vejaranoAún no hay calificaciones
- Guia PracticaDocumento33 páginasGuia PracticaNIL CHARLIE MARAÑON PINTOAún no hay calificaciones
- Practico Bioquímica bcc5 - 2018 PDFDocumento16 páginasPractico Bioquímica bcc5 - 2018 PDFRomina DuréAún no hay calificaciones
- Insert ASTL 0020764949322c501 V14 EsDocumento4 páginasInsert ASTL 0020764949322c501 V14 EsDAVIDAún no hay calificaciones
- Western Blot PDFDocumento14 páginasWestern Blot PDFJosé Álvarez del HoyoAún no hay calificaciones
- Tecnicas, Pruebas de Funcionamiento Renal: Quimica Clinica IDocumento18 páginasTecnicas, Pruebas de Funcionamiento Renal: Quimica Clinica IEvelyn SalomónAún no hay calificaciones
- Proteínas Totales Wiener LabDocumento3 páginasProteínas Totales Wiener LabCesar Emmanuel Miss Salgado100% (1)
- AAT2 EsDocumento3 páginasAAT2 EsJose Carlos Parras CasasAún no hay calificaciones
- Extracción de ADN de Cultivo BacterianoDocumento6 páginasExtracción de ADN de Cultivo BacterianoLuz AngelaAún no hay calificaciones
- Western BlotDocumento4 páginasWestern BlotPam Pam Díaz de LeónAún no hay calificaciones
- Informe 5Documento6 páginasInforme 5Alexa FloresAún no hay calificaciones
- 5 Electroforesis de Proteínas en Acetato de Celulosa Proteínas SéricasDocumento9 páginas5 Electroforesis de Proteínas en Acetato de Celulosa Proteínas SéricasKath RodríguezAún no hay calificaciones
- Western BlotDocumento7 páginasWestern BlotRicardo SotalìnAún no hay calificaciones
- Proti U LCR SPDocumento3 páginasProti U LCR SPEmi Gómez RediAún no hay calificaciones
- PresentaciónDeterminación de Proteínas Totales y Albúmina en SueroDocumento19 páginasPresentaciónDeterminación de Proteínas Totales y Albúmina en SueroEmily VidalAún no hay calificaciones
- Crea Baosr6x7815Documento11 páginasCrea Baosr6x7815AdrianaManouAún no hay calificaciones
- APTT Cas Rev03 PDFDocumento2 páginasAPTT Cas Rev03 PDFDariforiAún no hay calificaciones
- Dominando las Tinciones: Manual para el Laboratorio MicrobiológicoDe EverandDominando las Tinciones: Manual para el Laboratorio MicrobiológicoAún no hay calificaciones
- Anemia HipoplasicaDocumento19 páginasAnemia HipoplasicaMelisa FlorianAún no hay calificaciones
- GalactoreaDocumento23 páginasGalactoreaNeglest ArciszAún no hay calificaciones
- Pielonefritis 160630020909Documento37 páginasPielonefritis 160630020909Galia Torrez100% (2)
- Manual de Metodos CapturaDocumento45 páginasManual de Metodos CapturaMaria JaraAún no hay calificaciones
- Achs-Curso Prevencion de RiesgosDocumento37 páginasAchs-Curso Prevencion de RiesgosJuankillo100% (2)
- Proyecto de APS - GRUPO DDocumento23 páginasProyecto de APS - GRUPO DSheila helens Solange Murillo LazaroAún no hay calificaciones
- Alteraciones en El Metabolismo de Metionina y CisteinaDocumento8 páginasAlteraciones en El Metabolismo de Metionina y CisteinaElzy MariteAún no hay calificaciones
- Radiobiologia ...Documento11 páginasRadiobiologia ...Scream Gabriela100% (1)
- Guia de Aprendizaje Fase Ejecución - 1Documento5 páginasGuia de Aprendizaje Fase Ejecución - 1ZURIDAY VALENCIA MORENO100% (1)
- Auxiliar de Farmacia: Modulo - 1 Tema 3Documento18 páginasAuxiliar de Farmacia: Modulo - 1 Tema 3Galo ArturoAún no hay calificaciones
- Signo de GodetDocumento4 páginasSigno de Godetangela135100% (1)
- 16 - Toma de Muestras y Cultivos Microbiológicos NuevaDocumento36 páginas16 - Toma de Muestras y Cultivos Microbiológicos NuevaRodriguez EdisonAún no hay calificaciones
- Crianza SaludDocumento40 páginasCrianza SaludTATIANAAún no hay calificaciones
- Hoja MembretadaDocumento24 páginasHoja MembretadaJESSENIA CLARA VIGIL CAMACHOAún no hay calificaciones
- Valoracion Neurologica EnfermeriaDocumento1 páginaValoracion Neurologica EnfermeriaVane Alaniz HernandezAún no hay calificaciones
- Farmacologia Peptidos Vasoactivos Clase 17Documento8 páginasFarmacologia Peptidos Vasoactivos Clase 17MARCOS ENZER UZIEDA DÁVALOSAún no hay calificaciones
- Actividad Física: ImportanciaDocumento2 páginasActividad Física: ImportanciaSalomé Violeta LeónAún no hay calificaciones
- TendinitisDocumento6 páginasTendinitisAmanda RodriguezAún no hay calificaciones
- Atipia de Células EscamosasDocumento2 páginasAtipia de Células Escamosasatole29Aún no hay calificaciones
- EF NeonatalDocumento18 páginasEF NeonatalGaston Gabriel GonzalezAún no hay calificaciones
- Epidemiologia y PrevalenciaDocumento15 páginasEpidemiologia y PrevalenciaJulio C NnssAún no hay calificaciones
- Tamiz MetabolicoooDocumento3 páginasTamiz MetabolicoooLuzdaly VillaAún no hay calificaciones
- Prestaciones Centro Veterinario MunicipalDocumento3 páginasPrestaciones Centro Veterinario MunicipalCarla ElguetaAún no hay calificaciones
- Drenaje PosturalDocumento17 páginasDrenaje PosturalLaurix Silva FonsecaAún no hay calificaciones
- Estrategia de Intervencion Tda Aprendizaje SocialDocumento7 páginasEstrategia de Intervencion Tda Aprendizaje SocialDavid MAún no hay calificaciones
- Triptico de Las Hueso HumanoDocumento3 páginasTriptico de Las Hueso HumanoMalenaAún no hay calificaciones
- Formulario 008Documento2 páginasFormulario 008fernanflo ESPOCH-LIZARZABURUAún no hay calificaciones