Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Higado
Cargado por
Flor Franchetto0 calificaciones0% encontró este documento útil (0 votos)
9 vistas59 páginasTítulo original
Untitled
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
9 vistas59 páginasHigado
Cargado por
Flor FranchettoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 59
Higado
Situación y dimensiones del hígado
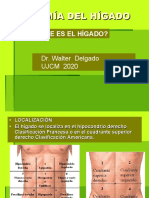
• El hígado es la mayor glándula del organismo.
Pesa alrededor de 1,5 kg,
• se sitúa justo debajo del diafragma y ocupa la
mayor parte del hipocondrio derecho y parte
del epigastrio
Lóbulos hepáticos
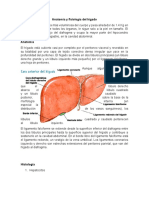
• El hígado está formado por dos lóbulos separados
por el ligamento falciforme.
• El lóbulo izquierdo ocupa alrededor de un sexto
del hígado, mientras que el lóbulo derecho ocupa
el resto.
• El lóbulo derecho tiene tres partes que se
designan como lóbulo derecho propiamente
dicho, lóbulo caudado (una pequeña superficie
oblonga en la cara posterior) y lóbulo cuadrado
(una sección de cuatro lados en la superficie
inferior).
Lóbulos hepáticos
• Cada lóbulo está dividido en numerosos
lobulillos mediante pequeños vasos
sanguíneos y tractos fibrosos que forman un
armazón de soporte para ellos (la cápsula de
Glisson).
• La cápsula de Glisson es una extensión de la
dura cápsula de tejido conjuntivo que
envuelve todo el hígado.
Los lobulillos hepáticos
• Unidades anatómicas estructurales del hígado,
son diminutos cilindros con forma hexagonal o
pentagonal que miden 2 mm de alto por 1 mm de
diámetro.
• A través del centro de cada lobulillo se extiende
una pequeña rama de la vena hepática.
Alrededor de esta vena central (intralobulillar),
las células hepáticas se disponen en láminas de
paredes irregulares que se irradian hacia fuera.
Los lobulillos hepáticos
• En las esquinas exteriores de cada lobulillo se disponen
varios grupos de diminutos tubos, ramas de la arteria
hepática, de la vena porta (venas interlobulillares) y del
conducto hepático (conductos biliares interlobulillares).
• Desde éstos, se extienden ramas irregulares
(sinusoidales) de las venas interlobulillares entre las
láminas radiantes de las células hepáticas para unirse a
la vena central.
• Se forman pequeños canalículos biliares en los espacios
alrededor de cada célula que almacena la bilis secretada
por las células hepáticas.
función de los lobulillos hepáticos
• La sangre penetra en el lobulillo por
ramas de la arteria hepática y de la vena
porta.
• La sangre arterial oxigena las células
hepáticas, mientras que la sangre del
sistema porta atraviesa el hígado para
sufrir una «inspección».
función de los lobulillos hepáticos
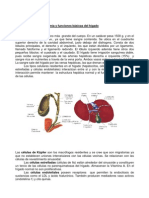
• Los sinusoides del lobulillo poseen muchas
células reticuloendoteliales (sobre todo células
de Kupffer) a lo largo de su trayectoria. Estas
células fagocíticas pueden eliminar las bacterias,
los hematíes viejos y otras partículas del torrente
sanguíneo.
• Las vitaminas que ingerimos y otros nutrientes
que deben ser almacenados o metabolizados por
las células hepáticas entran en las que forman las
paredes radiantes del lobulillo.
función de los lobulillos hepáticos
• Las toxinas disueltas en la sangre también son absorbidas
en las células hepáticas, donde son destoxificadas
(convertidas en inofensivas).
• La sangre continúa a lo largo de los sinusoides hasta una
vena en el centro del lobulillo.
• Estas venas centrales, intralobulillares, desembocan
finalmente en las venas hepáticas principales que drenan
en la vena cava inferior.
• La bilis formada por las células hepáticas pasa a través de
los canalículos hasta la periferia del lobulillo para unirse a
los pequeños conductos biliares.
Conductos biliares
• Los pequeños conductos biliares dentro del hígado se
unen para formar dos conductos mayores que emergen
de la superficie inferior del órgano; se trata de los
conductos hepáticos derecho e izquierdo.
• Éstos se unen inmediatamente para formar el conducto
hepático.
• El conducto hepático se une con el conducto cístico de
la vesícula biliar, formando el conducto colédoco, que
se abre en el duodeno en una pequeña área elevada
denominada papila duodenal mayor. Esta papila se
localiza 7 a 10 cm por debajo de la abertura pilórica del
estómago.
Funciones del hígado
El hígado es uno de los órganos más vitales del organismo, y
éstas son, en resumen, sus principales funciones:
• Las células hepáticas detoxifican ciertas sustancias.
• Las células hepáticas secretan alrededor de medio litro de
bilis al día.
• Las células hepáticas llevan a cabo muchos pasos
importantes en el metabolismo de las tres clases de alimento,
proteínas, grasas y carbohidratos.
• Las células hepáticas almacenan diferentes sustancias, por
ejemplo, hierro y vitaminas A, B12 y D.
• El hígado sintetiza importantes proteínas plasmáticas y sirve
como lugar de hematopoyesis (producción de células
sanguíneas) durante el desarrollo fetal.
Detoxificación por las células hepáticas
• Numerosas sustancias tóxicas entran en la sangre
procedentes del intestino.
• Circulan hasta el hígado, donde, a través de una
serie de reacciones químicas, pueden
transformarse en compuestos atóxicos.
• Las sustancias que se ingieren, alcohol,
paracetamol y otros tipos de fármacos, así como
las sustancias tóxicas formadas en el intestino,
pueden ser detoxificadas en el hígado.
Secreción biliar por el hígado
• Los principales componentes de la bilis son las
sales biliares, los pigmentos biliares y el
colesterol.
• Las sales biliares (formadas en el hígado a partir
de colesterol) son la parte más importante de la
bilis.
• Colaboran en la absorción de las grasas y luego
son absorbidas en el íleon.
• El ochenta por ciento de las sales biliares se
recicla en el hígado para convertirse de nuevo en
parte de bilis.
Secreción biliar por el hígado
• La bilis también sirve como pasadizo para eliminar
algunos productos defectuosos de las células rojas
sanguíneas.
• Cuando los eritrocitos viejos y frágiles son destruidos
en el bazo, la porción hemo de la molécula de
hemoglobina liberada es convertida en bilirrubina y
transportada por la sangre hacia el hígado.
• Las células hepáticas extraen la bilirrubina y la excretan
en la bilis.
• Dado que el hígado secreta bilis en los conductos, se
clasifica como una glándula exocrina.
Metabolismo hepático
Aunque todas las funciones hepáticas
son importantes para la salud del
organismo, algunos de sus procesos
metabólicos son cruciales para la
supervivencia.
FISIOLOGÍA
El hígado tiene un papel vital para el
organismo humano, presentando
multiplicidad funcional metabólica,
digestiva, hemostática, inmunológica y de
reservorio,
con flujo de alrededor de 1500 ml de
sangre por minuto.
Hepatocitos
• El citoesqueleto tiene papel funcional en el
transporte de sustancias y en la dinámica de
los canalículos biliares.
• Las mitocondrias participan en la fosforilación
oxidativa y la oxidación de ácidos grasos.
• El retículo endoplasmático rugoso se encarga
de la síntesis de albúmina, fibrinógeno y
diversas proteínas mediadoras de reacciones
inflamatorias y de la coagulación sanguínea.
Hepatocitos
En el retículo endoplasmático liso se da el
depósito de glicógeno, conjugación de
bilirrubina, esterificación de ácidos grasos,
glicogenolisis, des-iodación de tiroxina,
síntesis de colesterol y de ácidos biliares,
metabolismo de lípidos y de sustancias
liposolubles, de esteroides y de fármacos
como fenobarbitúricos, alcohol y tabaco.
Hepatocitos
• El aparato de Golgi realiza el transporte de lípidos hacia
el plasma, tiene actividad fosfatásica ácida catabólica,
produce glicoproteína y promueve la adición de
carbohidrato a las lipoproteínas.
• Los lisosomas presentan actividad fosfatásica ácida
además de poseer 30 enzimas hidrolíticas responsables
del catabolismo de cuerpos extraños, elementos
sanguíneos envejecidos y depositar hierro.
• Los peroxisomas metabolizan las purinas, los lípidos, el
alcohol y el peróxido de hidrogeno, participan en la
gluconeogénesis, en la beta-oxidación de los ácidos
grasos de cadena larga.
Sinusoides
• Realizan endocitosis, intervienen en la síntesis de
la matriz extracelular, con producción de colágeno
y fibronectina.
• Producen mediadores de reacciones inflamatorias
tales como interleucinas, prostaciclinas y
prostaglandinas y vasorreguladores como el
monóxido de nitrogeno, que representa un papel
fundamental en el desarrollo de fibrosis e
hipertensión portal.
Células de Kupffer
• Las células de Kupffer son células
macrofágicas, móviles, ligadas a las células
endoteliales, pueden representar 80 a 90 % de
la población macrofágica fija del organismo,
con funciones inmunitarias de fagocitosis de
agentes infecciosos y de células tumorales.
• Sintetizan citosinas, eicosanoides y derivados
reactivos de oxigeno.
Células Estrelladas o Células de Ito
• Son células peri sinusoidales, tienen papel de
depósito de grasa y, principalmente de vitamina A,
siendo el principal almacenador de esta vitamina.
• Sintetizan y modulan la degradación de la matriz
extracelular, produciendo colágeno, glicoproteínas
y proteoglicanos.
• Regulan el flujo sanguíneo sinusoidal por su
capacidad contráctil en respuesta a diversos
agentes como tromboxano, prostaglandinas,
sustancia P y endotelinas .
Matriz Extracelular
• Situada en el espacio porta, en continuidad con el
tejido conjuntivo de la cápsula de Glisson y en las
venas centrolobulillares.
• Está compuesta de colágeno, proteoglicanos y
glicoproteínas.
• La interacción entre las células y la matriz
extracelular es esencial para el mantenimiento de
la homeostasia.
• Esta interacción es extremamente compleja y
frágil y representa un papel fundamental en la
fibrosis y en la oncogénesis hepática.
Células Tronco
• En el hígado normal o patológico estas células
surgen de células hijas provenientes de la propia
división celular de hepatocitos o de células
biliares.
• Se pueden originar también de las células del
tronco de origen medular que colonizan el
hígado por vía sanguínea dando origen a nuevos
hepatocitos o nuevas células biliares.
Metabolismo
• El hígado es un órgano complejo y de múltiples e
intensas funciones metabólicas, energéticas,
hemostáticas y de defensa.
• El metabolismo hepático resulta de interacciones
complejas, las cuales contribuyen a las relaciones
entre los hepatocitos y
las células extra-parenquimatosas,
las variaciones de substratos y de mediadores
humorales, su inervación y presión de oxígeno.
Metabolismo de los Carbohidratos
El hígado es el principal responsable de la
homeostasia de los carbohidratos,
consumiendo, almacenando y produciendo
glucosa. Gracias a su situación anatómica,
absorbe glucosa y hormonas intestinales y
pancreáticas.
Metabolismo de los Carbohidratos
• Los carbohidratos ingeridos en la dieta en
forma de polisacáridos (almidón) o como
disacáridos (sacarosa, lactosa), se transforman
bajo la acción de enzimas en monosacáridos
(glucosa, fructosa, galactosa, ribosa), llegan al
hígado por la vena porta, siendo rápidamente
absorbidos por los hepatocitos, cerca de 50%
de la ingesta, para ser metabolizados.
Metabolismo de los Carbohidratos
• La penetración de la glucosa en los hepatocitos se da
por difusión facilitada por transportador de
membrana, lográndose rápidamente un equilibrio
con la extracelular.
• En el hepatocito la glucosa es rápidamente
transformada en glucosa-6-fosfato y de ahí a glucosa-
1-fosfato, siendo incorporada al glucógeno, reacción
catalizada por la glucógeno sintetasa, proceso
llamado de glucogénesis, principal forma de
almacenamiento de carbohidratos.
• Este proceso se da en los hepatocitos periportales.
Metabolismo de los Carbohidratos
• En la glucólisis, que generalmente ocurre en hepatocitos
perivenosos, la fosforilación de glucosa en glucosa-6-fosfato
constituye la primera etapa, asegurada por una glucoquinasa,
degradando la glucosa en ácido pirúvico. La desfosforilación
de la glucosa-6-fosfato, catalizada por la glucosa 6-fosfatasa,
mantiene el ciclo glucosa/glucosa-6-fosfato.
• El ácido pirúvico es precursor del radical acetilo y del ion
acetato, que forman el Acetil-Coenzima A, involucrado en el
ciclo de Krebs, etapa aeróbica de la oxidación de los
carbohidratos y fase final común al metabolismo de lípidos y
proteínas.
Metabolismo de los Carbohidratos
• La glucemia se controla indirectamente por intermedio de la
glucoregulación hecha por la insulina y el glucagón.
• La hiperglucemia estimula la insulina favoreciendo la
formación de glucógeno y bloqueando la producción de
glucosa.
• La hipoglucemia se acompaña de elevación de glucagón, con
disminución de la relación insulina/glucagón, lo que activa la
glucogenólisis y la neoglucogénesis, transformando el hígado
en gran productor de glucosa.
Metabolismo de los Carbohidratos
• En la fase interprandial y en reposo, e hígado
produce 4,5 g/h de glucosa por la
glucogenólisis, degradación de glucógeno en
glucosa-6-fosfato, que será convertido en
glucosa en el hígado y en el riñón y en lactato
en el músculo.
• La neoglucogénesis promueve la conversión
de sustancias no glucídicas en glucógeno,
principalmente ácidos grasos, amino-ácidos y
ácido pirúvico.
Metabolismo de los Carbohidratos
La glucosa-6-fosfato puede además formar
el ácido 6 fosfoglucónico, dando lugar a
una pentosa, que es metabolizada y
produce nucleótidos, ácidos nucleicos y
adenosina tri-fosfato, representa 5% del
metabolismo de los carbohidratos y es
importante para la síntesis de ácidos grasos
y esteroides.
Metabolismo de los Carbohidratos
• La fructosa participa del metabolismo de los glúcidos por
intermedio de la conversión de metabolitos integrables en la
glucólisis. Controlada por la actividad de una
fosfofructoquinasa, produciendo acetilcoenzima A y
gliceraldehído-3-fosfato, participa en la glucólisis. Su
transformación en fructosa 1-6-difosfato podrá transformarla
en glucosa o glucógeno.
• La galactosa es fosforilada por una galactoquinasa
transformándose en uridil-difosfo-galactosa, que es utilizada
en la síntesis de diversas glicoproteínas y de
glucosaminglicanos. La transformación en uridil-difosfo-
glucosa también es posible.
Metabolismo de las Proteínas
• Tras la alimentación, el hígado capta aminoácidos de
la circulación portal y a través de transaminación los
recompone en proteínas estructurales y plasmáticas
(albúmina, haptoglobinas, transferrina,
ceruloplasminas, alfa, beta y gama globulinas y
lipoproteínas), enzimas, nucleótidos y el radical
heme.
• En la desaminación, con formación de ácidos grasos
y carbohidratos, hay producción energética a través
del ciclo de Krebs o por neoglucogénesis.
Metabolismo de las Proteínas
• La actividad de síntesis es intensa y representa cerca
del 25% del consumo energético, es continua y no
presenta posibilidad de almacenamiento local,
produce enzimas implicadas en la depuración de
toxinas y de xenobióticos.
• Las células extraparenquimatosas participan de la
síntesis del factor VIII y las células de Ito de la
proteína “retino-band” y de alfa-1-antitripsina.
• También se sintetizan el factor I de crecimiento y
proteínas de ligación.
Metabolismo de las Proteínas
• Los principales factores de estimulación son la
disponibilidad de aminoácidos, el aumento de la relación
insulina/glucagón y el aumento de volumen hepático.
• La variación de estos factores tiene efecto inhibidor, lo
mismo que el cortisol.
• El hígado es capaz de sintetizar aminoácidos no esenciales
por seis vías, que utilizan alfa-cetoácidos, para los cuales
se transfiere un radical aminado durante la
transaminación: oxaloacetato y alfa-cetoglutarato (ciclo
de Krebs); piruvato, 3-fosfoglicerato y fosfoenolpiruvato
(glucólisis) y ribosa 5 fosfato (pentosa fosfato).
Metabolismo de las Proteínas
Los amino-ácidos son degradados por diversas vías que
convergen hacia el ciclo de Krebs: alanina, glicina,
cisteína, serina, treonina y triptófano por el piruvato;
isoleucina, leucina y triptófano por el Acetil-Coenzima
A; leucina, lisina, fenil-alanina, tirosina y triptófano por
el Acetoacetil-Coenzima A; glutamato, glutamina,
histidina, prolina y arginina por el alfa-ceto-glutarato;
isoleucina, metionina y valina por el Succinil-Coenzima
A; tirosina, fenil-alanina y aspartato por el fumarato;
aspartato por el oxaloacetato.
Metabolismo de las Proteínas
• La leucina y la isoleucina no sirven de sustrato
para la neoglucogénesis, mas son cetogénicos.
• Los aminoácidos de cadena ramificada no son
degradados en el hígado.
• La hidroxiprolina y la metil-histidina no son
utilizadas para la síntesis proteica por sufrir
modificaciones durante su incorporación en
cadenas peptídicas.
Metabolismo de las Proteínas
• La ureogénesis ocurre estrictamente en el hígado,
pues la arginasa, que cataliza la última reacción, es
exclusiva del hígado, transforma la casi totalidad del
amonio producido en los riñones y por bacterias
intestinales en urea. En este ciclo, la producción de
fumarato hace la relación con el ciclo de Krebs
produciendo piruvato.
• En presencia de acidosis se observa diminución de la
producción de urea e inversamente en presencia de
alcalosis.
• En este ciclo, los principales surtidores de radicales
aminados son la glutamina, arginina y alanina.
Metabolismo de las Proteínas
• La tasa de producción de urea depende de la concentración de
substratos y de la regulación alostérica a nivel de enzimas.
• El acúmulo de aminoácidos activa la ureogénesis, en el
período posprandial, 50% del nitrógeno absorbido es
transformado en urea.
• En períodos interprandiales, ayuno o agresión (trauma o
sepsis), la liberación de aminoácidos por el tejido muscular,
necesaria para la producción de energía, conlleva el
funcionamiento continuo de la ureogénesis.
• La arginina es el principal estimulador, su efecto está limitado
por la conversión en citrulina, que es poco captada por el
hígado, cuya enzima está inhibida por régimen hiperproteico.
Metabolismo de los Lípidos
• En el hígado ocurre lipolisis: degradación de
triglicéridos en glicerol y ácidos grasos, que son
degradados en acetilcoenzima A y no son
reconvertidos en glucosa.
• En la fase posprandial, la liberación de ácidos grasos
por el tejido adiposo llega a 5g/h, siendo utilizada
con fines energéticos tras conversción en
acetilcoenzima A por betaoxidación mitocondrial.
• El hígado participa del metabolismo de la mayoría de
los ácidos grasos, excepto de los ácidos linoleico, que
debe ser suministrados por la alimentación.
Metabolismo de los Lípidos
• Los ácidos grasos originados en la lipólisis contribuyen a la
síntesis de triglicéridos en el hígado, excretados en forma de
lipoproteínas de bajo peso molecular.
• La lipogénesis, síntesis de ácidos grasos a partir de
acetilcoenzima A y de triglicéridos a partir de ácidos grasos y
glicerolfosfato, es una vía alimentada exclusivamente por la
glucólisis.
• El acetilcoenzima A resulta de la acción de una piruvato
deshidrogenasa en el interior de la mitocondria;
posteriormente, en presencia de biotina en el citoplasma el
acetilcoenzima A se convierte en malonil-coenzima A, que es
el primer intermediario de la síntesis de ácidos grasos.
Metabolismo de los Lípidos
• La introducción de una unión al ácido palmítico o al
ácido esteárico, forman respectivamente los ácidos
palmitoleico y oleico, que son el origen de ácidos
grasos mono o polisaturados.
• La síntesis de triglicéridos se hace por esterificación
de ácidos grasos libres en el hígado.
• Hay además producción de fosfolípidos y
lipoproteínas, que se ligan a los triglicéridos y pasan
a la circulación, reacción estimulada por la insulina.
Metabolismo de los Lípidos
• En la luz intestinal, los triglicéridos sufren
hidrólisis parcial por la acción de la lipasa,
produciendo glicerol que es hidrosoluble y es
transportado hacia el hígado, donde formará
complejos con las sales biliares, los ácidos
grasos promueven nueva síntesis de
triglicéridos en el intestino, a través de nueva
conjugación con glicerol.
Metabolismo de los Lípidos
• La síntesis hepática de colesterol depende de la cantidad
absorbida por el intestino de este esterol, además de otros
factores como catecolaminas y estrógenos.
• Se hace a partir de moléculas de acetilcoenzima A.
• El colesterol se excreta en la bilis, siendo convertido en ácidos
biliares, pero cerca de 70% del colesterol plasmático es
esterificado a ácido graso.
• La cetogénesis, síntesis de compuestos en C4, como
acetoacetato e hidroxibutirato, cuerpos cetónicos que
constituyen unidades acetil-exportables y son una manera de
solubilizar los lípidos.
Metabolismo de los Lípidos
• En la circulación, los cuerpos cetónicos se comportan
como substratos energéticos alternativos de glucosa,
pudiendo penetrar en las células e incorporarse al ciclo
de Krebs, tras reactivación en acetoacetilcoenzima A.
• La regulación de la cetogénesis es hormonal, siendo el
glucagón el principal estimulador de la oxidación de
ácidos grasos.
• La elevación de la relación insulina/glucagón e ingesta
elevada de carbohidratos bloquean la entrada de
ácidos grasos de cadena larga en la mitocondria y
favorecen su integración en triglicéridos.
Hemostasia
• El hígado es el responsable de la síntesis,
activación y aclaramiento de los diversos
factores de coagulación, de sus inhibidores y
de fibrinolisis.
• La hemostasia primaria depende del número y
de la función plaquetaria, en cuanto que la
coagulación depende de la activación de
factores y de la presencia de plaquetas
activadas.
Hemostasia
• La fibrinolisis se inicia por el hígado con la
producción y liberación por las células
endoteliales del activador tisular de
plasminógeno, que convierte el plasminógeno
en plasmina activada, causando la degradación
de la fibrina.
• El plasminógeno y los factores antifibrinolíticos
también son sintetizados por el hígado.
Hemostasia
• El hígado sintetiza la mayoría de los
factores de coagulación, con producción
exclusiva del fibrinógeno (factor I),
protrombina (factor II) y factores V, VII, IX
y X.
• En la insuficiencia hepática la
disminución de estos factores acarrea
coagulopatía.
Hemostasia
• El hígado también sintetiza una pequeña
fracción del factor VIII.
• Los factores II, VII, IX y X son
glicoproteínas cuya síntesis es
dependiente de la absorción de vitamina
K, encontrándose disminuidos en
presencia de colestasis.
Hemostasia
El factor VII ha sido utilizado como
excelente marcador de función hepática y
el factor V ha sido empleado para indicar
trasplante hepático en presencia de
hepatitis fulminante o subfulminante.
También podría gustarte
- Higado, Vesicula Biliar y PancreasDocumento52 páginasHigado, Vesicula Biliar y PancreasShasmery AbreuAún no hay calificaciones
- 1.2 HigadoDocumento53 páginas1.2 HigadoLuigui esnaider Chipeno pinoAún no hay calificaciones
- Higado, Pancreas y Vesicula BiliarDocumento69 páginasHigado, Pancreas y Vesicula BiliarEvelina CidAún no hay calificaciones
- 5 - Metabolismo de La BilirrubinaDocumento82 páginas5 - Metabolismo de La BilirrubinaFanni Stefany Salazar PenadoAún no hay calificaciones
- fUNCIONES DEL HIGADODocumento22 páginasfUNCIONES DEL HIGADOPaula Alejandra Montoya PiñerosAún no hay calificaciones
- Histologà A de Hà Gado y PáncreasDocumento30 páginasHistologà A de Hà Gado y Páncreascandida almanzarAún no hay calificaciones
- Digestivo IIIDocumento12 páginasDigestivo IIIBryan Fernando MurilloAún no hay calificaciones
- Capítulo 71 Guyton - SEEMDocumento6 páginasCapítulo 71 Guyton - SEEM3021773100101Aún no hay calificaciones
- 09-Higado y PancreasDocumento25 páginas09-Higado y PancreasAzul AmiamaAún no hay calificaciones
- Histologia Higado Vesicula Biliar y Pancreas 200720 Downloable 1290849Documento11 páginasHistologia Higado Vesicula Biliar y Pancreas 200720 Downloable 1290849Clarisse MarinoAún no hay calificaciones
- Higado y PancreasDocumento33 páginasHigado y PancreasJoan Montero100% (1)
- Fisiologia Hepatica y PancreaticaDocumento19 páginasFisiologia Hepatica y PancreaticaAyelén SanchezAún no hay calificaciones
- Glándulas AnexasDocumento5 páginasGlándulas AnexasGrecia AparicioAún no hay calificaciones
- FISIOLOGIA - HEPATICA Oct. 2019Documento60 páginasFISIOLOGIA - HEPATICA Oct. 2019Nico EVAún no hay calificaciones
- Clase 4.2 Unidad 4 Anatomia - UpsDocumento32 páginasClase 4.2 Unidad 4 Anatomia - UpsMario 78776Aún no hay calificaciones
- Hígado, Páncreas y Sist. EndocrinoDocumento12 páginasHígado, Páncreas y Sist. EndocrinoLAURA ISABELLA CÁRDENAS GUARNIZOAún no hay calificaciones
- Sistema Digestivo III ResumenDocumento6 páginasSistema Digestivo III ResumenKenneth Leon Garcia CastellónAún no hay calificaciones
- Unidad 7. Pruebas de Función HepáticaDocumento14 páginasUnidad 7. Pruebas de Función HepáticaCristiana Auxiliadora Fonseca MayorgaAún no hay calificaciones
- Estómago, Páncreas, Hígado y VesículaDocumento41 páginasEstómago, Páncreas, Hígado y VesículaIván TepalAún no hay calificaciones
- HIGADO , VESICULA BILIAR y PANCREASDocumento36 páginasHIGADO , VESICULA BILIAR y PANCREASLizbeth Zuñiga CisnerosAún no hay calificaciones
- A Sistema Digestivo 2Documento6 páginasA Sistema Digestivo 2Joyce ZambranoAún no hay calificaciones
- 309eba8b PDFDocumento69 páginas309eba8b PDFAdriana Nappa FernándezAún no hay calificaciones
- DIGESTIVO IIIDocumento4 páginasDIGESTIVO IIIÁvila Simenoff MailénAún no hay calificaciones
- Glandulas Anexas Del Aparato Digestivo IVDocumento32 páginasGlandulas Anexas Del Aparato Digestivo IVCarlos J. Farías LindaoAún no hay calificaciones
- Sistema Digestivo 3Documento43 páginasSistema Digestivo 3Valmir AntunesAún no hay calificaciones
- Capitulo 71 Fisiolog 305063 Downloadable 3896834Documento5 páginasCapitulo 71 Fisiolog 305063 Downloadable 3896834OmarysAlvarezAún no hay calificaciones
- El HígadoDocumento12 páginasEl HígadoItzel palacios100% (1)
- Tema 18 y 19 Histologia Del Higado Vesicula Biliar y PancreasDocumento14 páginasTema 18 y 19 Histologia Del Higado Vesicula Biliar y PancreasKarla JuárezAún no hay calificaciones
- Anatomía funcional 16° ClaseDocumento37 páginasAnatomía funcional 16° ClaseDANITZA RUBIELI GALA QUINTOAún no hay calificaciones
- Tubo Digestivo, Hígado, Vías ViliaresDocumento32 páginasTubo Digestivo, Hígado, Vías ViliaresBrigith ArmasAún no hay calificaciones
- Anatomía hígadoDocumento57 páginasAnatomía hígadoGiuliana Manzano camposAún no hay calificaciones
- HIGADODocumento16 páginasHIGADOBetlejuice srvnAún no hay calificaciones
- Anatomia Del HigadoDocumento6 páginasAnatomia Del HigadocristosegAún no hay calificaciones
- Capitulo 71 Fisiologia Hepatica 305063 Downloable 2219085Documento5 páginasCapitulo 71 Fisiologia Hepatica 305063 Downloable 2219085Jissell FergusonAún no hay calificaciones
- Glándulas salivalesDocumento8 páginasGlándulas salivalesJorgelis CuevasAún no hay calificaciones
- Explicacion Proyecto FinalDocumento8 páginasExplicacion Proyecto FinalKimberly BaqueroAún no hay calificaciones
- Glándulas Anexas PDFDocumento55 páginasGlándulas Anexas PDFFiama BonomiAún no hay calificaciones
- Hígado y vesícula biliarDocumento34 páginasHígado y vesícula biliarTitulación IFICEDAún no hay calificaciones
- Tejidos HematopoyeticosDocumento40 páginasTejidos HematopoyeticosÁngel CoronadoAún no hay calificaciones
- Hígado, Vesícula Biliar Y PáncreasDocumento118 páginasHígado, Vesícula Biliar Y PáncreasYohn LópezAún no hay calificaciones
- Exposición HígadoDocumento54 páginasExposición HígadoMaycol Baeza TéllezAún no hay calificaciones
- Aparato Digestivo IIIDocumento39 páginasAparato Digestivo IIIRuiz FerAún no hay calificaciones
- Hígado, Vesícula Biliar y PancreasDocumento8 páginasHígado, Vesícula Biliar y Pancreasjuan.asAún no hay calificaciones
- HÍGADODocumento8 páginasHÍGADOVirginia GaliassoAún no hay calificaciones
- Higado y Vias BiliaresDocumento90 páginasHigado y Vias BiliaresTalita IstefaneAún no hay calificaciones
- Higado Anato y FisioDocumento6 páginasHigado Anato y FisioYareli VázquezAún no hay calificaciones
- HígadoDocumento13 páginasHígadoLisdee BelloAún no hay calificaciones
- Unidad 6 - HígadoDocumento11 páginasUnidad 6 - HígadoMaría Prieto MarchalAún no hay calificaciones
- El HígadoDocumento6 páginasEl HígadoArianna SalazarAún no hay calificaciones
- PancreasDocumento22 páginasPancreasjohariver100% (1)
- Digest IvoDocumento2 páginasDigest IvoRayza RodriguesAún no hay calificaciones
- TemaDocumento4 páginasTemaw1t3rtkmAún no hay calificaciones
- Hígado Cap 13Documento18 páginasHígado Cap 13dylangarzon033Aún no hay calificaciones
- Anatomía y fisiología del hígado y vías biliaresDocumento34 páginasAnatomía y fisiología del hígado y vías biliaresRafael Torres Katia100% (2)
- Hígado y Vesicula PDFDocumento10 páginasHígado y Vesicula PDFMichelle ZambranoAún no hay calificaciones
- Cirrosis Hepática - PPTX 1Documento31 páginasCirrosis Hepática - PPTX 1Aly HerreraAún no hay calificaciones
- Perfil HepaticoDocumento3 páginasPerfil HepaticoReynaldo CallisayaAún no hay calificaciones
- Encefalopatia HepaticaDocumento37 páginasEncefalopatia HepaticamsakaAún no hay calificaciones
- Sistema Digestivo-Glandulas AnexasDocumento35 páginasSistema Digestivo-Glandulas AnexasMaria OntanedaAún no hay calificaciones
- Coagulación Para Todos: Medicina Para TodosDe EverandCoagulación Para Todos: Medicina Para TodosCalificación: 4.5 de 5 estrellas4.5/5 (3)
- Organos de Los SentidosDocumento35 páginasOrganos de Los SentidosFlor FranchettoAún no hay calificaciones
- Sistema urinario: riñones, nefronas y procesos de filtración, reabsorción y secreciónDocumento23 páginasSistema urinario: riñones, nefronas y procesos de filtración, reabsorción y secreciónFlor FranchettoAún no hay calificaciones
- EndocrinoDocumento183 páginasEndocrinoFlor FranchettoAún no hay calificaciones
- Sentido Del GustoDocumento22 páginasSentido Del GustoFlor FranchettoAún no hay calificaciones
- Intestino Delgado, Colon, Recto y AnoDocumento30 páginasIntestino Delgado, Colon, Recto y AnoFlor FranchettoAún no hay calificaciones
- DuodenoDocumento12 páginasDuodenoFlor FranchettoAún no hay calificaciones
- PancreasDocumento31 páginasPancreasFlor FranchettoAún no hay calificaciones
- EndocrinoDocumento183 páginasEndocrinoFlor FranchettoAún no hay calificaciones
- Anatomía de la pelvisDocumento52 páginasAnatomía de la pelvisFlor FranchettoAún no hay calificaciones
- HigadoDocumento59 páginasHigadoFlor FranchettoAún no hay calificaciones
- PancreasDocumento31 páginasPancreasFlor FranchettoAún no hay calificaciones
- Biotina y GlutationDocumento3 páginasBiotina y Glutationalejandro zamora100% (1)
- Guía de nomenclatura en Química OrgánicaDocumento16 páginasGuía de nomenclatura en Química OrgánicaDinacely EspinalAún no hay calificaciones
- Guia de Cetonas y AldehidosDocumento4 páginasGuia de Cetonas y Aldehidoskote_martinAún no hay calificaciones
- Control Crónico EU y NTA Final 2017Documento3 páginasControl Crónico EU y NTA Final 2017AuriculoterapiaADomicilioAún no hay calificaciones
- Sesión 1. Parte 2. Psicobiología y Genética Humana. PsicologíaDocumento4 páginasSesión 1. Parte 2. Psicobiología y Genética Humana. PsicologíaPablito ClavóAún no hay calificaciones
- Producción etanol fermentación glucosa 40cDocumento10 páginasProducción etanol fermentación glucosa 40cJesús Miguel Jacinto NavaAún no hay calificaciones
- 8 - AlquinosDocumento26 páginas8 - AlquinosSoledad Taipe VallejosAún no hay calificaciones
- Informe Practica 1-Omar Quintero CastroDocumento14 páginasInforme Practica 1-Omar Quintero CastroOmar Jhusset Quintero CastroAún no hay calificaciones
- Lourdes Tesis Bachiller 2015Documento98 páginasLourdes Tesis Bachiller 2015marieAún no hay calificaciones
- Semana N°-04 (Finalizado)Documento13 páginasSemana N°-04 (Finalizado)Manuel BocanegraAún no hay calificaciones
- Requerimientos ClostridiumDocumento18 páginasRequerimientos ClostridiumJavier Ramirez Carbajal0% (1)
- Estructura y función de las biomoléculasDocumento16 páginasEstructura y función de las biomoléculasStivens MurilloAún no hay calificaciones
- Dieta cetogénica para el tratamiento de la epilepsiaDocumento4 páginasDieta cetogénica para el tratamiento de la epilepsiaEstefanía AGAún no hay calificaciones
- Consumo FARMACIA PRIVADA MOV - EXIS - CERODocumento3 páginasConsumo FARMACIA PRIVADA MOV - EXIS - CEROAtlantis AvendanaAún no hay calificaciones
- Informe 1 Aldehidos y CetonasDocumento18 páginasInforme 1 Aldehidos y CetonasMiguel TorresAún no hay calificaciones
- Catalogo Abasmed Light 11-09-23Documento20 páginasCatalogo Abasmed Light 11-09-23Antonio OffAún no hay calificaciones
- Unidad 4 Catabolismo Esqueleto de Carbonos y Compuestos EspecializadosDocumento43 páginasUnidad 4 Catabolismo Esqueleto de Carbonos y Compuestos EspecializadosKris WuAún no hay calificaciones
- Biositesis de ProstaglandinasDocumento5 páginasBiositesis de ProstaglandinasValeria Lagos Carvajal0% (1)
- 0915 Nutrinews LIPTOSA Alternativas A Aminoacidos SinteticosDocumento5 páginas0915 Nutrinews LIPTOSA Alternativas A Aminoacidos SinteticosPierina MoralesAún no hay calificaciones
- Eteres y EpoxidosDocumento13 páginasEteres y EpoxidosJosé Luis PacoAún no hay calificaciones
- Adn ConservativoDocumento7 páginasAdn ConservativoYassir EspinozaAún no hay calificaciones
- Hidrocarburos AromáticosDocumento5 páginasHidrocarburos AromáticosDANIEL BRANDO OBESO HUAMANAún no hay calificaciones
- Proteinas. Hemoglobina y MioglobinaDocumento3 páginasProteinas. Hemoglobina y MioglobinaSara FleitasAún no hay calificaciones
- Tabla de Composicon en 100 Gr. HojuelasDocumento7 páginasTabla de Composicon en 100 Gr. HojuelasBuscando Nuestro Real SerAún no hay calificaciones
- Tabla Cofactores Enzimas PDFDocumento2 páginasTabla Cofactores Enzimas PDFAngie Morales100% (1)
- Preguntas para El Examen Bioquimica - de Todos Los TemasDocumento62 páginasPreguntas para El Examen Bioquimica - de Todos Los TemasLuis AngelAún no hay calificaciones
- Catalogo A Costo Directo CEAS PUEBLA 2do. Semestre 2014Documento31 páginasCatalogo A Costo Directo CEAS PUEBLA 2do. Semestre 2014cofamyAún no hay calificaciones
- UntitledjkjhDocumento4 páginasUntitledjkjhPablo DomínguezAún no hay calificaciones
- Pac V2Documento19 páginasPac V2Daniel Romero CalderonAún no hay calificaciones
- Drogueria Por Tu Salud Lista de MedicamentosDocumento92 páginasDrogueria Por Tu Salud Lista de MedicamentosPaola Andrea Caballero FeriaAún no hay calificaciones