Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Mapa Mental - Grupo 05
Cargado por
Maria Julia PinedaDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Mapa Mental - Grupo 05
Cargado por
Maria Julia PinedaCopyright:
Formatos disponibles
UNIVERSIDAD NACIONAL DE TRUJILLO
FACULTAD DE CIENCIAS AGROPECUARIAS
ESCUELA DE AGRONOMIA
DOCENTE: Marino Olivares de La Cruz
INTEGRANTES:
• Marín Bautista Walter Alexis
• Quiroz Sánchez Segundo Tomas
• García Bautista Robert Francisco
• Pineda Vilca Maria Julia
• Romero Huayán Rosa Maide
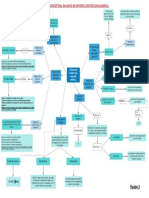
TAREA: Mapa conceptua - Cinética enzimática I: Velocidad
de reacción. Energía de activación. Km, Vmáx, Kcat.
• Factores físico-químicos que influyen en la actividad de
las enzimas.
GRUPO: 05
CURSO: Bioquímica Agrícola
CICLO: IV
Estudia la velocidad de una RX
Cinética enzimática I Es la quimica, los factores que permiten
su control y sus mecanismos de
acción.
a
Energía de activación
Velocidad de reacción
Es la reacción de los
reactivos o productor
respecto del tiempo km Vmáx Kcat
es es
Teoría de las colisiones Una medida de S Velocidad límite a la que
tiende una Rx cuando [S]
N° de procesos de Rx
(recambios) catalizados
requerida para que ocurra por un sitio catalítico por
es muy elevada y E se
catálisis significativa unidad de tiempo
encuentra saturada
Se divide en:
es decir tiene
N° de moles de S
Es una medida de la convertidos a P por
afinidad de la E por el S unidades de velocidad segundo y por mol de E
Frecuencia de los Orientación
Eficacia de los
choques por favorable de los es
choques choques
se define en el estado
unidad de volumen [S] a la cual la velocidad estacionario
de la Rx es la mitad de la Igual a la constante cinética
donde k2 y tiene unidades de
Vmáx tiempo-1
[E]T = [ES] si depende de la [E]
Se [E]T : [Enzima total]
su
A > frecuencia > velocidad de Rx • Es una medida útil para
Debe tener suficiente No todos los choques Magnitud varía comparar las actividades de ≠ E.
energía para que den de suficiente energía ampliamente de acuerdo a Vmáx = k2 [E]T
dan lugar a Rx la naturaleza de la E y del
lugar a la Rx.
S. •Este valor solo puede obtenerse
Al aumentar la T°, aumentar cuando se tiene a la E pura y por lo
y tanto se conoce su [ ]
la agitación térmica de las
moléculas, aumenta su
Hay choques con
velocidad, y por lo tanto su También es una función
energía cinética orientación más
favorables y otras con de la T° y del pH • A mayor valor de Kcat la
catálisis ocurre en un tiempo
menos favorables menor.
Habrá más moléculas que
alcancen la energía de al No depende de la [E].
activación, con ellos
aumento de la velocidad de
Rx. Tener menor superficie Tener mayor superficie
de contacto, hay menor de contacto, dan como
frecuencia de choques y resultado una mayor
con ello menor frecuencia de choques,
velocidad de reacción es decir mayor velocidad
de reacción
Estudio cuantitativo de la catálisis enzimática.
es el
CINÉTICA ENZIMÁTICA Estudia la velocidad de las Rx químicas que son
catalizadas por las enzimas.
TEORÍA DEL ESTADO DE
TRANSICIÓN O DEL COMPLEJO ENERGÍA DE Efecto de las enzimas Factores que influyen en
ACTIVADO ACTIVACIÓN sobre ∆G≠ la actividad enzimática
si
Las enzimas funcionan mejor dentro de
es rangos de temperatura y de pH específicos, y
Perfecciona la teoría de las Disminuyen ∆G≠, aumenta la bajo condiciones que no son las óptimas una
colisiones al indicar un modo enzima puede perder su capacidad de unirse
velocidad de la Rx (las Rx. se a un sustrato
de calcular la constante de La energía que necesita
un sistema antes de
realizan más rápido)
velocidad
poder iniciar un
determinado proceso La energía de
a activación suele
utilizarse para
esta Químicos
pesar de las exigencias
denominar la energía
mínima necesaria para Sin E, ∆G≠ es mayor >═
estéricas sean significativas que se produzca una pocos R poseen suficiente Físicos
Representa el proceso energía para alcanzar “T”
reacción química dada.
de activación pH
es
y
Al combinarse E y S, ∆G≠ es
Un intento de identificar los Diferencia entre la menor que en ausencia de E. Temperatura Concentración
aspectos principales que energía de R y la de
gobiernan el valor de una “T”.
de sustrato:
constante de velocidad [S]
es Si aumenta la T°, aumenta
el movimiento molecular y
La energía necesaria con ello la interacción E-S
en para llevar todas las Concentración
moléculas de 1 mol de R
hacia “T”.
de enzima: [E].
Términos de un modelo de
Por lo general aumenta de
eventos que ocurren durante la
2 a 4 veces la velocidad
reacción
de Rx
. Presencia de
inhibidores (Inh). •
Presión
Concentración de
sales: [Sales]
También podría gustarte
- Informe Puertas y Ventanas de FierroDocumento22 páginasInforme Puertas y Ventanas de Fierroac1050% (2)
- Modelamiento y casos especiales de la cinética química heterogéneaDe EverandModelamiento y casos especiales de la cinética química heterogéneaCalificación: 3 de 5 estrellas3/5 (1)
- Recibo DiciembreDocumento2 páginasRecibo DiciembreRosa RuizAún no hay calificaciones
- Calculos Justificativos Linea y Red PrimariaDocumento30 páginasCalculos Justificativos Linea y Red PrimariaCJ CotrinaAún no hay calificaciones
- Diseño de FermentadorDocumento58 páginasDiseño de Fermentadorlisnayda100% (3)
- Molino de MartillosDocumento4 páginasMolino de MartillosLi Ming0% (1)
- Formulario FísicaDocumento2 páginasFormulario FísicaCarlos100% (1)
- Diagrama Sin TítuloDocumento2 páginasDiagrama Sin TítuloBell RoseAún no hay calificaciones
- BACH2 FÍSICA MAS y Ondas - FormularioDocumento4 páginasBACH2 FÍSICA MAS y Ondas - FormularioAlex LanciuAún no hay calificaciones
- Quimica 1Documento8 páginasQuimica 1Luis Ángel Pérez XicotencatlAún no hay calificaciones
- Cinética QuímicaDocumento1 páginaCinética QuímicaDennys GarciaAún no hay calificaciones
- Mapas ConceptualesDocumento3 páginasMapas Conceptualesliliana martinezAún no hay calificaciones
- 2023 - 09 - 21 8 - 57 P. M. Office LensDocumento4 páginas2023 - 09 - 21 8 - 57 P. M. Office LensJess TellezAún no hay calificaciones
- Los Factores Que Modifican e Intervienen La Rapidez de Una ReacciónDocumento2 páginasLos Factores Que Modifican e Intervienen La Rapidez de Una ReacciónCarlos DanielAún no hay calificaciones
- Mapa Conceptual-Balance de Mteria Con Reaccion QuimicaDocumento1 páginaMapa Conceptual-Balance de Mteria Con Reaccion QuimicaIvaan Romaan100% (1)
- Reactores QuimicosDocumento5 páginasReactores QuimicosDiana María TrujilloAún no hay calificaciones
- 04 - Quimica ElectivoDocumento24 páginas04 - Quimica ElectivoLuis Armando PandoAún no hay calificaciones
- F I Unidad3 Semana10Documento33 páginasF I Unidad3 Semana10Hans LeguiaAún no hay calificaciones
- DinámicaDocumento131 páginasDinámicaWendy PulidoAún no hay calificaciones
- Cinética QuímicaDocumento1 páginaCinética Químicaambarmendoza2003Aún no hay calificaciones
- Mapa Conceptual Practica 1Documento1 páginaMapa Conceptual Practica 1Saul GarciaAún no hay calificaciones
- Presupuesto AsdrubalDocumento136 páginasPresupuesto AsdrubalDaivid Sebastian Muñoz RoballoAún no hay calificaciones
- Introducción Al Diseño de ReactoresDocumento18 páginasIntroducción Al Diseño de ReactoresanaAún no hay calificaciones
- Unidad I IRQ I ParteDocumento14 páginasUnidad I IRQ I Partecarlosp7682Aún no hay calificaciones
- Química - Ciclo Uni 2022 - Semana-08Documento23 páginasQuímica - Ciclo Uni 2022 - Semana-08Ronald FgAún no hay calificaciones
- Tema 1 CINEMATICA DE LA PARTICULADocumento6 páginasTema 1 CINEMATICA DE LA PARTICULAMicaela PereiraAún no hay calificaciones
- GARCIAMCyDB (QI) P4EQ3Documento2 páginasGARCIAMCyDB (QI) P4EQ3Saul GarciaAún no hay calificaciones
- Ingeniería Bioquímica - 202134 - 916Documento2 páginasIngeniería Bioquímica - 202134 - 916Kelly Johana Caicedo ZamoraAún no hay calificaciones
- Tarea9 MCMDocumento3 páginasTarea9 MCMMauricio De la CruzAún no hay calificaciones
- Informe 5 LabDocumento8 páginasInforme 5 LabLeonel Libio Banque ZangaAún no hay calificaciones
- MapaConceptual TransductoresDocumento4 páginasMapaConceptual Transductoresmarieth ruiz lopezAún no hay calificaciones
- Mapa Conceptual Quimica #14Documento3 páginasMapa Conceptual Quimica #14Isaì GalloAún no hay calificaciones
- Semana VIIIDocumento3 páginasSemana VIIIfrawilken cisneroAún no hay calificaciones
- GUÍA 1. Ingenieria de Las Reacciones Quimicas. Resumen-1Documento27 páginasGUÍA 1. Ingenieria de Las Reacciones Quimicas. Resumen-1Rodriguez GomezAún no hay calificaciones
- Cinética de Las Reacciones HomogéneasDocumento54 páginasCinética de Las Reacciones HomogéneasDiego VillanuevaAún no hay calificaciones
- Cadena de Marcov Cuadro SinopticoDocumento2 páginasCadena de Marcov Cuadro SinopticoGaby JimenezAún no hay calificaciones
- 3.0 Cinematica Teoria y ProblemasDocumento59 páginas3.0 Cinematica Teoria y ProblemasJean Bazan100% (1)
- Mapa Mental de Cinética Química 1Documento2 páginasMapa Mental de Cinética Química 1Fabrizzio HernandezAún no hay calificaciones
- Wuolah Free Resum ParcialDocumento10 páginasWuolah Free Resum ParcialJuud VivesAún no hay calificaciones
- Guia 1. Fundamentos Basicos-CineticaDocumento26 páginasGuia 1. Fundamentos Basicos-CineticaBerjimery RojasAún no hay calificaciones
- Regimenes Transitorios en Acc EléctricosDocumento26 páginasRegimenes Transitorios en Acc EléctricosPaulaAún no hay calificaciones
- Tema Iv - Cantidad de Movimiento y Momento CineticoDocumento12 páginasTema Iv - Cantidad de Movimiento y Momento CineticoHector VidalAún no hay calificaciones
- 0402 Unidad 4 - SintesisDocumento1 página0402 Unidad 4 - SintesisTomas BurgosAún no hay calificaciones
- FundamentDocumento49 páginasFundamentReyes GonzálezAún no hay calificaciones
- Taller 10Documento1 páginaTaller 10Devora Miluska AlfaroAún no hay calificaciones
- Aplicaciones La Transformada Delaplace en Otros CamposDocumento1 páginaAplicaciones La Transformada Delaplace en Otros CamposEl Jerry 7u7Aún no hay calificaciones
- Algunos Ejemplos Clásicos de EDP y Sus Principales AspectosDocumento31 páginasAlgunos Ejemplos Clásicos de EDP y Sus Principales AspectosCaro Villa MoraAún no hay calificaciones
- ValoracionesDocumento1 páginaValoracionesGARCIA GAMEZ JORGE ABRAHAMAún no hay calificaciones
- Tema 1.1 - 2022Documento13 páginasTema 1.1 - 2022Emerson SivinchaAún no hay calificaciones
- Mapa Relaciones Constante EquilibrioDocumento3 páginasMapa Relaciones Constante EquilibrioDaniel FalconAún no hay calificaciones
- Teoría de CircuitosDocumento33 páginasTeoría de CircuitosVioletaAún no hay calificaciones
- Wuolah Free Tema 1Documento21 páginasWuolah Free Tema 1JORGE DANIEL CASARES REFOLIOAún no hay calificaciones
- Lección 03 - Movimiento Con Aceleración ConstanteDocumento9 páginasLección 03 - Movimiento Con Aceleración Constante勝勝利Aún no hay calificaciones
- Xt-Ed-sts-smrxx-Er-smi-sni-onjvnn - TT: CinemáticaDocumento29 páginasXt-Ed-sts-smrxx-Er-smi-sni-onjvnn - TT: CinemáticaJair CervantesAún no hay calificaciones
- Lab10. - Cinética de La Mutarrotación de La GlucosaDocumento7 páginasLab10. - Cinética de La Mutarrotación de La GlucosaBrayan Huanca0% (1)
- Free Principi Fonamentals de La MecanicaDocumento4 páginasFree Principi Fonamentals de La Mecanicaalberto.martinezAún no hay calificaciones
- Factor de PotenciaDocumento3 páginasFactor de PotenciaSusana AmuraAún no hay calificaciones
- B2.1 Mapa MentalDocumento2 páginasB2.1 Mapa MentalAlberto JimenezAún no hay calificaciones
- 2.cinetica de Reacciones Octubre 2021-Marzo 2022Documento46 páginas2.cinetica de Reacciones Octubre 2021-Marzo 2022Alexandra RodriguezAún no hay calificaciones
- M C3 B3dulos - 5y 6Documento29 páginasM C3 B3dulos - 5y 6Estefany Fuentes ElíasAún no hay calificaciones
- Analogías de SistemasDocumento3 páginasAnalogías de SistemasMarck Jafer GonzalezAún no hay calificaciones
- Mcu McuvDocumento4 páginasMcu McuvDafne Lázaro AquinoAún no hay calificaciones
- Actividad 2, Unidad 1, Grupo 4EDocumento2 páginasActividad 2, Unidad 1, Grupo 4ENorma Mendoza LuceroAún no hay calificaciones
- Conceptos Básicos: ProcesosDocumento7 páginasConceptos Básicos: ProcesosAngelAún no hay calificaciones
- Correlación cruzada: Desbloqueo de patrones en visión por computadoraDe EverandCorrelación cruzada: Desbloqueo de patrones en visión por computadoraAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Valle Jequetepeque Escuela de Ingeniería AgronómicaDocumento11 páginasUniversidad Nacional de Trujillo Sede Valle Jequetepeque Escuela de Ingeniería AgronómicaMaria Julia PinedaAún no hay calificaciones
- MIPEDocumento4 páginasMIPEMaria Julia PinedaAún no hay calificaciones
- Rúbrica Calificación Infome Final de TifDocumento1 páginaRúbrica Calificación Infome Final de TifMaria Julia PinedaAún no hay calificaciones
- 1.fertilidad Química Forestal 2021-6-1Documento60 páginas1.fertilidad Química Forestal 2021-6-1Maria Julia PinedaAún no hay calificaciones
- Practica 2.mezcla de FertilizantesDocumento24 páginasPractica 2.mezcla de FertilizantesMaria Julia PinedaAún no hay calificaciones
- AgroecologiaDocumento16 páginasAgroecologiaMaria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento21 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento42 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- Control de Malezas 4º SemanaDocumento11 páginasControl de Malezas 4º SemanaMaria Julia PinedaAún no hay calificaciones
- Control de Malezas 6º SemanaDocumento13 páginasControl de Malezas 6º SemanaMaria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento31 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento43 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento47 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento18 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- Guía Práctica-1Documento33 páginasGuía Práctica-1Maria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento25 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento26 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- S AADocumento5 páginasS AAMaria Julia PinedaAún no hay calificaciones
- Universidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaDocumento25 páginasUniversidad Nacional de Trujillo Sede Guadalupe Escuela de Agronomía Experiencia Curricular: Bioquímica AgrícolaMaria Julia PinedaAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa ConceptualMaria Julia PinedaAún no hay calificaciones
- Guía de La Práctica 7Documento8 páginasGuía de La Práctica 7Maria Julia PinedaAún no hay calificaciones
- Seminarios y Teorias de Suelos, Asfalto, CBR OtrosDocumento67 páginasSeminarios y Teorias de Suelos, Asfalto, CBR OtrosCamacaroBelkisAún no hay calificaciones
- Batería de NiquelDocumento12 páginasBatería de NiquelDaniel BuitronAún no hay calificaciones
- EXAMEN DEL TEMA I (Teoria Del Fuego)Documento4 páginasEXAMEN DEL TEMA I (Teoria Del Fuego)Ernesto cruz calderonAún no hay calificaciones
- Tabelas ÁguaDocumento50 páginasTabelas ÁguaBDCFAún no hay calificaciones
- El Campo CobraDocumento6 páginasEl Campo CobraCruz Colque MarceloAún no hay calificaciones
- Chofer Vendedor Industria CerveceraDocumento116 páginasChofer Vendedor Industria CerveceraArturo AndradeAún no hay calificaciones
- Circuito ParaleloDocumento6 páginasCircuito ParaleloAnonymous hQ6z6OBw100% (1)
- 200216335-Prelab NoDocumento18 páginas200216335-Prelab Noapi-576334472Aún no hay calificaciones
- Desintegracion Mecanica de SolidosDocumento20 páginasDesintegracion Mecanica de SolidosAndrea Sánchez100% (1)
- CotDocumento4 páginasCotAlberto JavierAún no hay calificaciones
- Inductores y CapacitoresDocumento13 páginasInductores y CapacitoresDaniel Sanchez Martinez100% (1)
- Arteaga Chapa. Flores Fernández.Documento22 páginasArteaga Chapa. Flores Fernández.Raul Montante SalazarAún no hay calificaciones
- Yaluk Draw PDFDocumento8 páginasYaluk Draw PDFFelipe OchoaAún no hay calificaciones
- Especificaciones Pdvsa TeaDocumento5 páginasEspecificaciones Pdvsa TeaDIEGO ANDRES NINOAún no hay calificaciones
- Cajetin GtzaDocumento2 páginasCajetin Gtzasimon aguayoAún no hay calificaciones
- Sala Calderas UNE 60601Documento54 páginasSala Calderas UNE 60601Robertobes BesAún no hay calificaciones
- Descripción Del Proceso de La Elaboracion Del CafeDocumento3 páginasDescripción Del Proceso de La Elaboracion Del CafeCINDY ALBANIS TACOURDEEN FRIAS100% (1)
- Cuaderno Virtual de AutomatismoDocumento36 páginasCuaderno Virtual de AutomatismoJunior Javier Hilario RománAún no hay calificaciones
- Frozen® (2023)Documento2 páginasFrozen® (2023)Mada FakaAún no hay calificaciones
- Memoria Anual ASJ 2020Documento28 páginasMemoria Anual ASJ 2020Ruben Nolasco MamaniAún no hay calificaciones
- Apuntes de Construcción IV (30-09-2019)Documento111 páginasApuntes de Construcción IV (30-09-2019)agen.enrAún no hay calificaciones
- 3o. Secundaria Fase 3 SolucionarioDocumento2 páginas3o. Secundaria Fase 3 SolucionarioTtezilOkAún no hay calificaciones
- Alutermic 731 PDFDocumento1 páginaAlutermic 731 PDFCarlos Prado100% (1)
- TripticoDocumento2 páginasTripticodk100% (1)
- Estudio Del Rendimiento Y Eficiencia Del Proceso de Electrólisis en La Producción de Cloro-Alcalí Y Escalar El Proceso A Nivel LaboratorioDocumento9 páginasEstudio Del Rendimiento Y Eficiencia Del Proceso de Electrólisis en La Producción de Cloro-Alcalí Y Escalar El Proceso A Nivel LaboratorioomarAún no hay calificaciones