Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Benzoato
Cargado por
GustavoCalderinTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Benzoato
Cargado por
GustavoCalderinCopyright:
Formatos disponibles
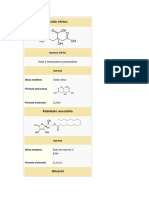
Benzoato de sodio
El benzoato de sodio, también conocido Benzoato sódico
como benzoato de sosa o (E211), es una sal
del ácido benzoico, blanca, cristalina y
gelatinosa o granulada, de fórmula
C6H5COONa. Es soluble en agua y
ligeramente soluble en alcohol. La sal es
antiséptica y se usa generalmente para
conservar los alimentos.
C6H5-COOH + NaOH <-> NaC6H5CO2 +
H2O Nomenclatura IUPAC Benzoato Sódico
Otros nombres E211, benzoato de sosa
Fórmula semidesarrollada NaC6H5CO2
Índice Masa molecular 144,1053 g mol−1
Número CAS [532-32-1]
Usos
Densidad 1,44 g cm−3
Mecanismo de conservación de los
alimentos Punto de fusión 410 °C (770 °F; 683 K)
Seguridad y salud Punto de ebullición N/A
Referencias SMILES O=C([O-])C1=CC=CC=C1.[Na+]
Usos
Como aditivo alimentario es usado como conservante, matando eficientemente a la mayoría de levaduras, bacterias y hongos . El
benzoato sódico sólo es efectivo en condiciones ácidas (pH,-6) lo que hace que su uso más frecuente sea en conservas, en aliño de
ensaladas (vinagre), en bebidas carbonatadas (ácido carbónico), en mermeladas (ácido cítrico), en zumo de frutas (ácido cítrico) y
en salsas de comida china (soja, mostaza y pato). También se encuentra en enjuagues de base alcohólica y en el pulido de la plata.
Más recientemente, el benzoato sódico viene estando presente en muchos refrescos como Sprite, Fanta, Coke Zero. El sabor del
benzoato sódico no puede ser detectado por alrededor de un 35% de la población, pero para los que han probado el producto
químico, tienden a percibirlo como dulce, salado o a veces amargo.
También se utiliza en pirotecnia, como combustible en la mezcla del polvo que produce un silbido cuando es comprimida y
encendida en un tubo.
En la naturaleza lo podemos encontrar en arándanos, pasas, ciruelas pasas, canela, clavos de olor maduros y manzanas.
Los gatos tienen una tolerancia perceptiblemente más baja contra el ácido benzoico y sus sales que las ratas y ratones.1 Sin
embargo, está permitido como aditivo del pienso (alimento) hasta en un 0,1%.2
Mecanismo de conservación de los alimentos
El mecanismo comienza con la absorción del ácido benzoico por la célula. Si el pH intracelular cambia a 5 o más bajo, la
fermentación anaerobia de la glucosa con fosfofructocinasa es disminuida un 100%.3
Seguridad y salud
La FDA (Administración de Alimentos y Medicamentos), de los Estados Unidos designa al benzoato de sodio como
«generalmente considerado seguro».4 El Programa Internacional sobre la Seguridad Química no encontró ningún efecto nocivo
en seres humanos para dosis de 647-825 mg/kg de masa corporal por día.5 6
El Comité Mixto FAO / OMS de Expertos en Aditivos Alimentarios (JECFA) ha evaluado el ácido benzoico y sus sales varias
veces y encontraron que son aceptables para su uso en los alimentos. La última revisión se llevó a cabo en 1997.[cita requerida]
Cerca de 50 países en cinco regiones del Codex permiten el uso de ácido benzoico y sus sales en los niveles de 1.000 ppm o
mayores. Estos países incluyen los Estados Unidos, Canadá y México.
Referencias
1. Bedford PG, Clarke EG (1972). «Experimental benzoic acid poisoning in the cat». Vet Rec (90): 53-58. PMID
2. AFCO (2004). OFFICIAL PUBLICATION.
3. Krebs HA, Wiggins D, Stubbs M (1983). «Studies on the mechanism of the antifungal action of benzoate».
Biochem J (214): 657-663.
4. CFR - Code of Federal Regulations Title 21 (http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.
cfm?CFRPart=184)
5. Concise International Chemical Assessment Document 26: BENZOIC ACID AND SODIUM BENZOATE (http://ww
w.inchem.org/documents/cicads/cicads/cicad26.htm)
6. Cosmetic Ingredient Review Expert Panel Bindu Nair (2001). «Final Report on the Safety Assessment of Benzyl
Alcohol, Benzoic Acid, and Sodium Benzoate». Int J Tox (20 (Suppl. 3)): 23-50.
Obtenido de «https://es.wikipedia.org/w/index.php?title=Benzoato_de_sodio&oldid=117109500»
Esta página se editó por última vez el 2 jul 2019 a las 13:44.
El texto está disponible bajo la Licencia Creative Commons Atribución Compartir Igual 3.0; pueden aplicarse
cláusulas adicionales. Al usar este sitio, usted acepta nuestros términos de uso y nuestra política de privacidad.
Wikipedia® es una marca registrada de la Fundación Wikimedia, Inc., una organización sin ánimo de lucro.
También podría gustarte
- Libro de cocina de dieta renal, La guía para principiantes de una dieta baja en proteínas, sodio, potasio y fósforo para el riñónDe EverandLibro de cocina de dieta renal, La guía para principiantes de una dieta baja en proteínas, sodio, potasio y fósforo para el riñónCalificación: 4.5 de 5 estrellas4.5/5 (2)
- Bicarbonato de Sodio PDFDocumento3 páginasBicarbonato de Sodio PDFSteven Jacobo Gonzalez100% (1)
- Vitamina B15 - Ácido Pangámico: ¿Un poderoso medicamento suprimido?: Cura al Cáncer - Desintoxicación del Cuerpo - Ayuda para el Dolor de Nervios y Enfermedad de Corazón?De EverandVitamina B15 - Ácido Pangámico: ¿Un poderoso medicamento suprimido?: Cura al Cáncer - Desintoxicación del Cuerpo - Ayuda para el Dolor de Nervios y Enfermedad de Corazón?Aún no hay calificaciones
- Benzoato de SodioDocumento3 páginasBenzoato de Sodiomb4000Aún no hay calificaciones
- Benzoato de SodioDocumento13 páginasBenzoato de SodioAlexander Tenorio EscalanteAún no hay calificaciones
- Benzoato de SodioDocumento3 páginasBenzoato de SodiomegadethymetAún no hay calificaciones
- PreservantesDocumento2 páginasPreservantesEvelin Johana Bernal IbañezAún no hay calificaciones
- Ácido BenzoicoDocumento4 páginasÁcido BenzoicoJohaAlvarezAún no hay calificaciones
- Benzoato de SodioDocumento12 páginasBenzoato de SodioBeatriz Lopez LopezAún no hay calificaciones
- Ácido SórbicoDocumento4 páginasÁcido SórbicoBryan LópezAún no hay calificaciones
- Ácido BenzoicoDocumento4 páginasÁcido BenzoicoJosé YalibatAún no hay calificaciones
- Informe Ejecutivo Bebida Artificial No Carbonatada FinalDocumento6 páginasInforme Ejecutivo Bebida Artificial No Carbonatada FinalFlorent TobarAún no hay calificaciones
- Aditivos en Los Alimentos (Caro)Documento35 páginasAditivos en Los Alimentos (Caro)JeddysBarrios100% (1)
- Tecno Agro 3Documento41 páginasTecno Agro 3José Daniel Romero ChávezAún no hay calificaciones
- Remedios Con BicarbonatoDocumento5 páginasRemedios Con BicarbonatoherareAún no hay calificaciones
- Determinacion de BenzoatosDocumento8 páginasDeterminacion de BenzoatosFavio TorihuanoAún no hay calificaciones
- Benzoato de SodioDocumento8 páginasBenzoato de SodioAlejandro PinedaAún no hay calificaciones
- Benzoato de SodioDocumento15 páginasBenzoato de SodioAlvaro FernandezAún no hay calificaciones
- Ácido ButanoicoDocumento3 páginasÁcido ButanoicoArístides PérezAún no hay calificaciones
- Conservantes FisikDocumento25 páginasConservantes Fisikjalvarez_599866100% (1)
- Acido LácticoDocumento5 páginasAcido LácticodiegoAún no hay calificaciones
- Shampoo SavitalDocumento16 páginasShampoo SavitalnayipipeAún no hay calificaciones
- FrutasDocumento21 páginasFrutasDamián AlexanderAún no hay calificaciones
- Reporte Práctica PolvosDocumento9 páginasReporte Práctica PolvosRodrigo Bautista GuzmanAún no hay calificaciones
- Benzato de SodioDocumento39 páginasBenzato de SodioRuben Kapa TiconaAún no hay calificaciones
- Bicarbonato de SodioDocumento8 páginasBicarbonato de SodioJALIR ANDRE HUAYLLAS SOTOAún no hay calificaciones
- Caracteristicas Del Acido Citrico MonohidratadoDocumento3 páginasCaracteristicas Del Acido Citrico Monohidratadojotame87Aún no hay calificaciones
- Practica Sal de EnoDocumento7 páginasPractica Sal de Enoalarconvela100% (3)
- DescarboxilacionDocumento2 páginasDescarboxilacionAndreinaAún no hay calificaciones
- Bebidas GasificadaDocumento14 páginasBebidas GasificadaDeyvi VillanuevaAún no hay calificaciones
- Bebida GasificadaDocumento23 páginasBebida GasificadaJheyson Antonio Bajonero RamosAún no hay calificaciones
- ConservantesDocumento39 páginasConservantesAdriel LouisAún no hay calificaciones
- Ascorbato de SodioDocumento4 páginasAscorbato de SodioCarlos RebazaAún no hay calificaciones
- CONSERVANTESDocumento19 páginasCONSERVANTESgalileaAún no hay calificaciones
- Acido Citrico y Acido LacticoDocumento26 páginasAcido Citrico y Acido LacticoADRIANA MAGDALENA ROMERO DE LA CRUZAún no hay calificaciones
- Investigación ConservadoresDocumento5 páginasInvestigación ConservadoresMich RamosAún no hay calificaciones
- Investigación ConservadoresDocumento5 páginasInvestigación ConservadoresMich RamosAún no hay calificaciones
- Ácido CítricoDocumento7 páginasÁcido CítricoJose andresAún no hay calificaciones
- Práctica 4.1 Caracterización de Polvos EfervescentesDocumento10 páginasPráctica 4.1 Caracterización de Polvos EfervescentesYony RM0% (1)
- Acidos CarboxilicosDocumento26 páginasAcidos CarboxilicosLaura Gomez AnzaldoAún no hay calificaciones
- Determinacion de Acido BenzoicoDocumento9 páginasDeterminacion de Acido BenzoicoAntezana Mejia ElizabethAún no hay calificaciones
- Conservacion Quimica (Parce)Documento36 páginasConservacion Quimica (Parce)Anonymous C06P6LXh9Aún no hay calificaciones
- Practica 6Documento8 páginasPractica 6KaTiita SerQnAún no hay calificaciones
- Informe de Tecnología de BebidasDocumento32 páginasInforme de Tecnología de BebidasFabianaAlejandraLazoPeñarandaAún no hay calificaciones
- Dota 2Documento8 páginasDota 2Manuel LopezAún no hay calificaciones
- Ficha Tecnica Benzoato de SodioDocumento4 páginasFicha Tecnica Benzoato de Sodiomalehm10Aún no hay calificaciones
- Bisulfito Sódico - Wikipedia, La Enciclopedia LibreDocumento5 páginasBisulfito Sódico - Wikipedia, La Enciclopedia LibreVendedor RodriguezAún no hay calificaciones
- Bicarbonato de SodioDocumento5 páginasBicarbonato de SodioAnonymous xCjc7yAún no hay calificaciones
- Evidencia No 8. 2020Documento11 páginasEvidencia No 8. 2020David Leonardo JIMENEZ MUNOZAún no hay calificaciones
- Bioquimica de Los Lipidos - Bioquimica I UPADS 2016Documento150 páginasBioquimica de Los Lipidos - Bioquimica I UPADS 2016Jael Almonte CayoAún no hay calificaciones
- Benzoato de PotasioDocumento3 páginasBenzoato de Potasiomb4000Aún no hay calificaciones
- Conservadores PanificacionDocumento9 páginasConservadores PanificacionDaniiel Marin MontoyaAún no hay calificaciones
- Sesion 5 - Bebidas Carbonatadas PDFDocumento55 páginasSesion 5 - Bebidas Carbonatadas PDFANA LUZ MAMANI QUISPEAún no hay calificaciones
- Informe N°6 - Procesos - Quimicos - IndustrialesDocumento10 páginasInforme N°6 - Procesos - Quimicos - IndustrialesAnnaAncietaAún no hay calificaciones
- BenzoatosDocumento3 páginasBenzoatosSamantha RuizAún no hay calificaciones
- Informe Toxicológico FinalDocumento32 páginasInforme Toxicológico Finalmariolayaquerevalu7129Aún no hay calificaciones
- Los Lipidos en La NutricionDocumento26 páginasLos Lipidos en La NutricionVanessaLevanoPonteAún no hay calificaciones
- Carbonato de SodioDocumento13 páginasCarbonato de SodioDaryl Rucabado Llatas100% (1)
- Cuestionario AditivosDocumento10 páginasCuestionario AditivosKimberly CardenasAún no hay calificaciones
- Chan SantokhiDocumento4 páginasChan SantokhiGustavoCalderinAún no hay calificaciones
- Adalet AğaoğluDocumento3 páginasAdalet AğaoğluGustavoCalderinAún no hay calificaciones
- Juan José García CorralDocumento2 páginasJuan José García CorralGustavoCalderinAún no hay calificaciones
- María Lugones PDFDocumento3 páginasMaría Lugones PDFGustavoCalderinAún no hay calificaciones
- Zindzi MandelaDocumento5 páginasZindzi MandelaGustavoCalderinAún no hay calificaciones
- Extremeño (Lingüística)Documento17 páginasExtremeño (Lingüística)GustavoCalderinAún no hay calificaciones
- Luis Arias GrazianiDocumento2 páginasLuis Arias GrazianiGustavoCalderinAún no hay calificaciones
- Anexo Gran Premio de Estiria de 2020Documento5 páginasAnexo Gran Premio de Estiria de 2020GustavoCalderinAún no hay calificaciones
- Elecciones Al Parlamento de Galicia de 2020Documento8 páginasElecciones Al Parlamento de Galicia de 2020GustavoCalderinAún no hay calificaciones
- Irma LanzasDocumento3 páginasIrma LanzasGustavoCalderin100% (1)
- Ruanda PDFDocumento10 páginasRuanda PDFGustavoCalderinAún no hay calificaciones
- José Antonio Quiroga y PiñeyroDocumento3 páginasJosé Antonio Quiroga y PiñeyroGustavoCalderinAún no hay calificaciones
- Juan Fernández GarcíaDocumento5 páginasJuan Fernández GarcíaGustavoCalderinAún no hay calificaciones
- José Calvo GonzálezDocumento3 páginasJosé Calvo GonzálezGustavoCalderinAún no hay calificaciones
- Oscar BlancoDocumento3 páginasOscar BlancoGustavoCalderinAún no hay calificaciones
- BurundiDocumento13 páginasBurundiGustavoCalderinAún no hay calificaciones
- Marc FumaroliDocumento6 páginasMarc FumaroliGustavoCalderinAún no hay calificaciones
- Javier Prado AránguizDocumento3 páginasJavier Prado AránguizGustavoCalderinAún no hay calificaciones
- Declaración de Independencia de FilipinasDocumento6 páginasDeclaración de Independencia de FilipinasGustavoCalderinAún no hay calificaciones
- Descargar Riesgos de TrabajoDocumento28 páginasDescargar Riesgos de TrabajoAlan Gregorio Becerra TorresAún no hay calificaciones
- Proyecto de Investigacion (Trabajo Final)Documento37 páginasProyecto de Investigacion (Trabajo Final)javier sangeadoAún no hay calificaciones
- ManualDocumento12 páginasManualhomer.cuevas.moraAún no hay calificaciones
- Corea HuntingtonDocumento3 páginasCorea HuntingtonMarvin SalazarAún no hay calificaciones
- Biología 5 Trabajo MARSDocumento4 páginasBiología 5 Trabajo MARS•lara teves•Aún no hay calificaciones
- Cartel de Contenidos en Eba - Edu - RelDocumento61 páginasCartel de Contenidos en Eba - Edu - RelMIGUEL ANGELAún no hay calificaciones
- Ciencia Vs EmpirismoDocumento6 páginasCiencia Vs EmpirismoJanely RodriguezAún no hay calificaciones
- Juan Jose Reyes Patria FinalDocumento37 páginasJuan Jose Reyes Patria Finalalberto parraAún no hay calificaciones
- TR1 Tratamiento de Residuos SólidosDocumento9 páginasTR1 Tratamiento de Residuos Sólidos42824033Aún no hay calificaciones
- Act 5 IO1Documento4 páginasAct 5 IO1Esmeralda GaytanAún no hay calificaciones
- Materialismo CartesianoDocumento4 páginasMaterialismo CartesianoTalento Libre DE PsicologiaAún no hay calificaciones
- Nueva Idea de Proyecto BicicletaDocumento2 páginasNueva Idea de Proyecto BicicletaJesus E. MartinezAún no hay calificaciones
- Memoria de Calculo Cerco PerimetricoDocumento26 páginasMemoria de Calculo Cerco Perimetricojhon alvaAún no hay calificaciones
- LEO PRIMERO DOCENTE Lenguaje Tomo 1 PDFDocumento427 páginasLEO PRIMERO DOCENTE Lenguaje Tomo 1 PDFcatalinaAún no hay calificaciones
- Molino de MaderaDocumento10 páginasMolino de MaderaMario ÁlvarezAún no hay calificaciones
- Importancia de Incorporar Conceptos Ambientales en Diseño y Construccion de Obras CivilesDocumento4 páginasImportancia de Incorporar Conceptos Ambientales en Diseño y Construccion de Obras CivilesAngela Romero SanchezAún no hay calificaciones
- Ejercicios Tarea 3Documento14 páginasEjercicios Tarea 3Luis Feliciano CardenasAún no hay calificaciones
- Ensayo Calidad TotalDocumento6 páginasEnsayo Calidad Totalandovale78% (9)
- Metalurgia IDocumento67 páginasMetalurgia IYash Palomino SantosAún no hay calificaciones
- Manual de Procesos y ProcedimientoDocumento2 páginasManual de Procesos y ProcedimientoEhuvany MartinezAún no hay calificaciones
- Masaje ShiatsuDocumento4 páginasMasaje ShiatsualexcerroblancoAún no hay calificaciones
- 6 Recursos Naturales Renovables y No RenovablesDocumento4 páginas6 Recursos Naturales Renovables y No Renovableslisseth montaño100% (1)
- Planeacion 5Documento3 páginasPlaneacion 5jesus piñaAún no hay calificaciones
- Gasificación e IncineraciónDocumento80 páginasGasificación e IncineraciónAndres Felipe VallejoAún no hay calificaciones
- Representaciones Semioticas en La EScuelaDocumento23 páginasRepresentaciones Semioticas en La EScuelaFel CastAún no hay calificaciones
- Panel de Control 4100 0040 LSDocumento8 páginasPanel de Control 4100 0040 LSCristianAún no hay calificaciones
- Apunte Funciones Por TramosDocumento4 páginasApunte Funciones Por TramosBERYLL ZICARELLIAún no hay calificaciones
- DistalizacionDocumento17 páginasDistalizacionSebastian AguirreAún no hay calificaciones
- API 2 Recursos InformaticosDocumento2 páginasAPI 2 Recursos InformaticosROSANAAún no hay calificaciones
- Sentidos Que Porta La Enseñanza y El AprendizajeDocumento19 páginasSentidos Que Porta La Enseñanza y El AprendizajeFavio BorghinoAún no hay calificaciones