Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cuadro Enzimas PDF
Cargado por
carlos0 calificaciones0% encontró este documento útil (0 votos)
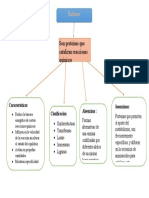
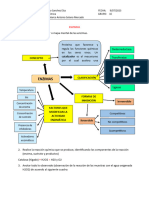
180 vistas1 páginaLas enzimas son moléculas proteicas que catalizan reacciones químicas reduciendo la barrera energética, clasificadas por el tipo de reacción que catalizan como oxidorreductasas, transferasas, hidrolasas, isomerasas, ligasas y liasas. Reciben nombres derivados del sustrato sobre el que actúan o de la reacción catalizada, formando complejos reversibles con el sustrato sin consumirse en la reacción.
Descripción original:
Título original
CUADRO ENZIMAS.pdf
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoLas enzimas son moléculas proteicas que catalizan reacciones químicas reduciendo la barrera energética, clasificadas por el tipo de reacción que catalizan como oxidorreductasas, transferasas, hidrolasas, isomerasas, ligasas y liasas. Reciben nombres derivados del sustrato sobre el que actúan o de la reacción catalizada, formando complejos reversibles con el sustrato sin consumirse en la reacción.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
180 vistas1 páginaCuadro Enzimas PDF
Cargado por
carlosLas enzimas son moléculas proteicas que catalizan reacciones químicas reduciendo la barrera energética, clasificadas por el tipo de reacción que catalizan como oxidorreductasas, transferasas, hidrolasas, isomerasas, ligasas y liasas. Reciben nombres derivados del sustrato sobre el que actúan o de la reacción catalizada, formando complejos reversibles con el sustrato sin consumirse en la reacción.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
Enzimas
Son
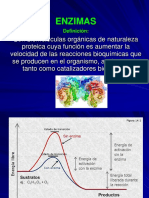
Son moléculas de naturaleza proteica que
catalizan reacciones químicas.
Clasificación Características Nomenclatura
Son proteínas que poseen un efecto Han sido designadas añadiendo el
Óxido- Reacciones de óxido-
catalizador al reducir la barrera sufijo –asa al nombre del sustrato,
reductosasosas reducción
es decir, la molécula sobre la cual
energética de ciertas reacciones ejerce su actividad catalítica.
Transfieren grupos
Transferasas Influyen solo en la velocidad de reacción
funcionales Ureasa
sin alterar en estado del equilibrio Arginasa
Hidrolasas Reacciones de Actúan en pequeñas cantidades
Otras reciben su nombre de
hidrolisis
No se consumen en la reacción, acuerdo a la reacción que
pudiendo actuar una y otra vez catalizan
Reacciones de
Isomerasas
isomerización Forman un complejo reversible con el Gliceraldeido-3-fosfato-
sustrato
Formación de
Ligasas Su producción está directamente
enlaces con
consumo de ATP
Liasas Reacciones de adición a
los dobles enlaces
También podría gustarte
- Mapa ConceptualDocumento1 páginaMapa Conceptualcarlos83% (12)
- Mapa ConceptualDocumento1 páginaMapa Conceptualcarlos83% (12)
- Cuestionario MicroDocumento3 páginasCuestionario Microcarlos100% (1)
- Cuadro EnzimasDocumento1 páginaCuadro EnzimascarlosAún no hay calificaciones
- Bioquimica Nutricional Enzimas-Tema 2Documento56 páginasBioquimica Nutricional Enzimas-Tema 2Ana MedinaAún no hay calificaciones
- Módulo Iv-Ptar-ImprimirDocumento90 páginasMódulo Iv-Ptar-ImprimirArias Espinoza Natalia100% (1)
- EnzimasDocumento16 páginasEnzimasmauro soudrecamposAún no hay calificaciones
- Cuadro EnzimasDocumento1 páginaCuadro Enzimascarlos50% (2)
- ENZIMASDocumento2 páginasENZIMASAngel Andres Ayquipa AlvitesAún no hay calificaciones
- EnzimasDocumento8 páginasEnzimasMARÍA VEGAAún no hay calificaciones
- MercurioDocumento7 páginasMercurioDaniela Cordoba100% (1)
- Cuadro EnzimasDocumento1 páginaCuadro Enzimascarlos0% (1)
- Mapa Conceptual de Las Enzimas 3Documento1 páginaMapa Conceptual de Las Enzimas 3Julieth Camej100% (1)
- Actividad EnzimaticaDocumento6 páginasActividad EnzimaticaYameli Yadira Castellares MamaniAún no hay calificaciones
- Enzimas Bioquimica GralDocumento2 páginasEnzimas Bioquimica GralFernanda E OrtízAún no hay calificaciones
- Mapa EnzimasDocumento1 páginaMapa Enzimasgabrielita030987Aún no hay calificaciones
- Mapa Conceptual de Las Rutas MetabolicasDocumento3 páginasMapa Conceptual de Las Rutas MetabolicasPelukas Riveros ArceAún no hay calificaciones
- GL OsarioDocumento3 páginasGL OsarioDAIDER ALEJANDRO MARTINEZ CARVAJALAún no hay calificaciones
- Las EnzimasDocumento1 páginaLas EnzimasCuenta pruebaAún no hay calificaciones
- Produccinindustrialdevitaminasyenzimas 150513230509 Lva1 App6891Documento53 páginasProduccinindustrialdevitaminasyenzimas 150513230509 Lva1 App6891Anthony Toro CarrilloAún no hay calificaciones
- Proteinas Como CatalizadoresDocumento1 páginaProteinas Como CatalizadoresSofía OrdoñezAún no hay calificaciones
- Mapa Conceptual EnzimasDocumento4 páginasMapa Conceptual EnzimasLiz CastellanosAún no hay calificaciones
- Semana 10 Bioquimica Viviana Magalyortiz MartinezDocumento2 páginasSemana 10 Bioquimica Viviana Magalyortiz MartinezMagaly OrtizAún no hay calificaciones
- Clasificación de Las EnzimasDocumento1 páginaClasificación de Las EnzimasufirAún no hay calificaciones
- Metabolismo CelularDocumento9 páginasMetabolismo CelularamandaAún no hay calificaciones
- Tarjetas de Enzimas Completo 2023Documento4 páginasTarjetas de Enzimas Completo 2023k7hw8hkhmrAún no hay calificaciones
- 6 - Mapa ConceptualDocumento1 página6 - Mapa ConceptualMERCADO BENZAQUEN JOANNA MICHELLEAún no hay calificaciones
- 1.defina A Las Enzimas.: Transformando Vidas"Documento5 páginas1.defina A Las Enzimas.: Transformando Vidas"zulmaAún no hay calificaciones
- Mapa Conceptual de Las Enzimas 6Documento1 páginaMapa Conceptual de Las Enzimas 6Cintia MaldonadoAún no hay calificaciones
- 2021 Proteinas - EnzimasDocumento59 páginas2021 Proteinas - EnzimasjulioAún no hay calificaciones
- Clase 5 Farmacia IDocumento21 páginasClase 5 Farmacia IAngélica Flor LopezAún no hay calificaciones
- Enzimas PDFDocumento53 páginasEnzimas PDFNelson BeltranAún no hay calificaciones
- EnzimasDocumento19 páginasEnzimasMarisol E ContrerasAún no hay calificaciones
- Reacciones Químicas, Mapa MentalDocumento1 páginaReacciones Químicas, Mapa MentalLuciana uguAún no hay calificaciones
- EnzimasDocumento36 páginasEnzimasbossmiguel667Aún no hay calificaciones
- Bioquimica Basica Base Molecular de Los Procesos Fisiologicos Cap 3Documento20 páginasBioquimica Basica Base Molecular de Los Procesos Fisiologicos Cap 3Elda PasosAún no hay calificaciones
- Enzimas - PrácticaDocumento2 páginasEnzimas - PrácticaLeita floresmontoyaAún no hay calificaciones
- Presentación Beto Enzimas Final OkDocumento10 páginasPresentación Beto Enzimas Final OkRobin Buelvas HernandezAún no hay calificaciones
- Accede A Apuntes, Guías, Libros y Más de Tu Carrera: Enzimas 8 PagDocumento9 páginasAccede A Apuntes, Guías, Libros y Más de Tu Carrera: Enzimas 8 PagVIOLETA ELIZABETH SANCHEZ CASTROAún no hay calificaciones
- En ZimasDocumento48 páginasEn ZimasKarla J Kuc VeronAún no hay calificaciones
- Informe EnzimaticoDocumento4 páginasInforme Enzimaticojose franciscoAún no hay calificaciones
- Mapa BioenergéticaDocumento1 páginaMapa BioenergéticaNadiaAún no hay calificaciones
- ENZIMASDocumento5 páginasENZIMASdaciairanAún no hay calificaciones
- Enzimas y CarbohidratosDocumento2 páginasEnzimas y CarbohidratosMaria Camila Garcia TolozaAún no hay calificaciones
- Tarea 14.2 Mapa ConceptualDocumento1 páginaTarea 14.2 Mapa ConceptualShadid AlitzelAún no hay calificaciones
- Las Enzimas PDFDocumento2 páginasLas Enzimas PDFJocelyn Ninaquispe VásquezAún no hay calificaciones
- CARTEL de La Práctica 3, NRC 13959Documento1 páginaCARTEL de La Práctica 3, NRC 13959Berenice Sanchez GalindoAún no hay calificaciones
- EnzimasDocumento31 páginasEnzimasLuisa F PedrazaAún no hay calificaciones
- EnzimasDocumento29 páginasEnzimasmanu92egAún no hay calificaciones
- EnzimasDocumento20 páginasEnzimasjuan carlosAún no hay calificaciones
- U3b MetabolismoMicrobiano 19636Documento50 páginasU3b MetabolismoMicrobiano 19636Johana Andrea Portilla JojoaAún no hay calificaciones
- Presentación Proyecto Científico Doodle Ilustrado Verde y RosaDocumento41 páginasPresentación Proyecto Científico Doodle Ilustrado Verde y RosaJuliette HendersonAún no hay calificaciones
- Las EnzimasDocumento8 páginasLas EnzimasMiriam MercadoAún no hay calificaciones
- Capítulo 4 OchaetaDocumento1 páginaCapítulo 4 OchaetaMARIANA ESCOBAR RIVERAAún no hay calificaciones
- CatabolismoDocumento1 páginaCatabolismoYANINA LISSAY YARANGO NOLASCOAún no hay calificaciones
- Ms. Pablo Chuna Mogollón / Abril - 2015Documento30 páginasMs. Pablo Chuna Mogollón / Abril - 2015victorAún no hay calificaciones
- Infografía de EnzimasDocumento1 páginaInfografía de EnzimasAlma Esquivel100% (2)
- Reacciones QuimicasDocumento2 páginasReacciones QuimicasNoeliaAún no hay calificaciones
- Enzima Transferasas Cuadro Comparativo.Documento1 páginaEnzima Transferasas Cuadro Comparativo.ALBA JINETH ACEVEDOAún no hay calificaciones
- Mapa Conceptual EnzimasDocumento2 páginasMapa Conceptual EnzimasJohn MerchanAún no hay calificaciones
- Concepto de Biotransformación y de BiocatálisisDocumento4 páginasConcepto de Biotransformación y de BiocatálisisArantza CanalesAún no hay calificaciones
- Informe EnzimasDocumento4 páginasInforme EnzimasElzy PeredoAún no hay calificaciones
- PracticaDocumento4 páginasPracticacarlos100% (1)
- Cuadro Sinóptico TaxonomiaDocumento3 páginasCuadro Sinóptico Taxonomiacarlos67% (3)
- Lípidos InsaponificablesDocumento1 páginaLípidos InsaponificablescarlosAún no hay calificaciones
- Cuadro ATPDocumento2 páginasCuadro ATPcarlosAún no hay calificaciones
- Efecto de Dosis y Momento de Aplicación de Lombricomposta en LaDocumento9 páginasEfecto de Dosis y Momento de Aplicación de Lombricomposta en LaPerla Gpe GómezAún no hay calificaciones
- Reporte 4Documento5 páginasReporte 4pamela gonzalezAún no hay calificaciones
- Reseña Historico de La Bioquimica CartaDocumento4 páginasReseña Historico de La Bioquimica CartaLina LopezAún no hay calificaciones
- Comunidades Bióticas y EcosistemasDocumento19 páginasComunidades Bióticas y Ecosistemasfernando_lopera_6Aún no hay calificaciones
- 2015 Solucionario Guía 26 TC Influencia Humana en El Ecosistema Sobreexplotación y ContaminaciónDocumento7 páginas2015 Solucionario Guía 26 TC Influencia Humana en El Ecosistema Sobreexplotación y Contaminaciónlucesita_30Aún no hay calificaciones
- Fabricacion de Jabon Ecologico A Base de Aceites ComestiblesDocumento10 páginasFabricacion de Jabon Ecologico A Base de Aceites ComestiblesAndres CarrilloAún no hay calificaciones
- Exposicion AzufreDocumento16 páginasExposicion AzufreHitson VilcaAún no hay calificaciones
- Sistema Biofloc - Acuicultura en GuatemalaDocumento47 páginasSistema Biofloc - Acuicultura en GuatemalaLuis LinaresAún no hay calificaciones
- Informe 8 Química General 2 UnmsmDocumento19 páginasInforme 8 Química General 2 UnmsmLucíaAún no hay calificaciones
- AP Sesion 3Documento6 páginasAP Sesion 3karen sotoAún no hay calificaciones
- Características Principales Aplicaciones Típicas: Acero Dulce, Celulósico - AWS E6011Documento2 páginasCaracterísticas Principales Aplicaciones Típicas: Acero Dulce, Celulósico - AWS E6011jhosser andres jojoa calderonAún no hay calificaciones
- Quimica QuânticaDocumento31 páginasQuimica QuânticaPedro RosárioAún no hay calificaciones
- Qué Son Las Resinas Acrílicas de Alto ImpactoDocumento4 páginasQué Son Las Resinas Acrílicas de Alto ImpactoCamila PoloAún no hay calificaciones
- Tarea3 G33Documento42 páginasTarea3 G33jairoAún no hay calificaciones
- El Efecto FotoelectricoDocumento23 páginasEl Efecto FotoelectricoDavidSuarezAún no hay calificaciones
- Quimica 1Documento2 páginasQuimica 1Maria De Jesus Roblez VegaAún no hay calificaciones
- PRAC.#1 Reacciones de Reconocimientos de CarbohidratosDocumento4 páginasPRAC.#1 Reacciones de Reconocimientos de CarbohidratosGLORIA MARGARITA GUERRERO REYAún no hay calificaciones
- Factores Que Influyen en El Crecimiento yDocumento8 páginasFactores Que Influyen en El Crecimiento yAnthony BaltazarAún no hay calificaciones
- Anx 5 Conversion CataliticaDocumento3 páginasAnx 5 Conversion CataliticaEthel ZunigaAún no hay calificaciones
- 127 - Planta de Tratamiento de Agua Potable de QuicapataDocumento5 páginas127 - Planta de Tratamiento de Agua Potable de QuicapataOlmedo Aedo HUYHUA ACEVEDOAún no hay calificaciones
- Simulacion de Crudo Por DuctosDocumento78 páginasSimulacion de Crudo Por DuctosDesiree MolinaAún no hay calificaciones
- Diapositivas Sobre Capa de OzonoDocumento29 páginasDiapositivas Sobre Capa de OzonoRosa Edith CardenasAún no hay calificaciones
- Mantenimiento Mecanico 2Documento11 páginasMantenimiento Mecanico 2leunnitAún no hay calificaciones
- Guia Didactica 3-BEDocumento20 páginasGuia Didactica 3-BEOscarPortelaAún no hay calificaciones
- Cinética Química, Práctica de LaboratorioDocumento16 páginasCinética Química, Práctica de LaboratorioMello DigitalAún no hay calificaciones
- Peligros Del PanDocumento4 páginasPeligros Del PanPaula StanwyckAún no hay calificaciones
- Expo Demostracion de Grasas Neutras en Un Corte Histologico MaribelDocumento18 páginasExpo Demostracion de Grasas Neutras en Un Corte Histologico MaribelWilliam Gaston Herrera SolanoAún no hay calificaciones
- EstomagoDocumento1 páginaEstomagoMildret Genezaret Hernández HernándezAún no hay calificaciones