Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Curso Hidrometalurgia Del Ag, Au y Cu PDF
Cargado por
Kv MartinTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Curso Hidrometalurgia Del Ag, Au y Cu PDF
Cargado por
Kv MartinCopyright:
Formatos disponibles
HIDROMETALURGIA DEL Au, Ag, Cu
TERMODINAMICA
CONTENIDO
Generalidades
Diagrama eh-pH del agua
Construccin de los diagramas eh-pH
Influencia de los acomplejants
Usos y Abusos de los diagramas eh-pH
TRANSFERENCIA DE MASA Y CINETICA
CONTENIDO
Introduccin
Cintica Homognea
Cintica Heterognea
1. Efecto de la velocidad del fluido
2. Efecto de la temperatura
3. Naturaleza electroqumica
LIXIVIACIN DE METALES
CONTENIDO
Solubilidad de Au y Ag en soluciones de cianuro
1. Efecto de la concentracin de cianuro
2. Efecto del pH
3. Efecto de la concentracin de cianuro
Cintica de la cianuracin
1. Efecto de iones extraos
METODOLOGIA DE LA HIDROMETALURGIA Au y Ag
CONTENIDO
Lixiviacin en montn
Lixiviacin por agitacin
Adsorcin en carbn activado
Precipitacin con zinc en polvo
Extraccin por solventes orgnicos.
LIXIVIACIN DEL Cu
CONTENIDO
Pgina 2 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Lixiviacin de CuOx
Lixiviacin de sulfuros de Cu
Cintica de la lixiviacin
Lixiviacin en Montn
Lixiviacin por agitacin
RECUPERACIN DEL Cu
CONTENIDO
Precipitacin de Cu con chatarra de Hierro
Extraccin por solventes orgnicos
1. Teora bsica
2. Reaccin principal.
3. Dispersin estable
4. Degradacin de extractants.
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 3 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Introduccin
La hidrometalurgia es la rama de la metalurgia extractiva que comprende los
procesos de obtencin de metales y compuestos, a partir de minerales o fuentes
secundarias, mediante reacciones que tienen lugar en soluciones acuosas u
orgnicas y por lo tanto se desarrollan a temperaturas relativamente bajas.
Las tcnicas empleadas incluyen. Preparacin y pre-tratamiento del mineral o
material inicial, lixiviacin de los valores metlicos usando reactivos qumicos o
accin bacterial, separacin y lavado de residuos slidos, purificacin final del
metal o compuesto deseado.
Para cada una de estas etapas se dispone de una gran variedad de tratamientos
alternativos; as por ejemplo, la lixiviacin puede realizarse por percolacin,
agitacin. In-situ o en pilas y botaderos. La purificacin de las soluciones puede
realizarse por control del pH, intercambi inico, extraccin por solventes
orgnicos, etc. La precipitacin puede ser por cementacin, electrodeposicin o
precipitacin con gases.
Las primeras aplicaciones de la hidrometalurgia moderna las constituyen los
procesos de cianuracin de minerales de oro y plata. Estos procesos dieron
origen a un rpido desarrallo de la mayora de los equipos indispensables en los
procesos hidrometalrgicos actuales: agitadores, espesadores, filtros, bombas de
lodos, etc.
Posteriormente aparecieron procesos tan importantes como el intercambio inico,
extraccin por solventes orgnicos y el carbn activado que abrieron un campo
an ms grande de aplicacin.
Actualmente
se
extraen
refinan,
comercialmente,
mediante
mtodos
hidrometalrgicos, un gran nmero de metales, como por ejemplo: cobre, nquel,
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 4 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
aluminio, oro, plata, cobalto, zinc, uranio, zirconio, hafnio, etc. Pudiendo
emplearse en forma total o parcial para prcticamente todos, excepto 6 o 7, de los
82 elementos metlicos conocidos. Generalmente los metales alcanzan un grado
de pureza mayor que los producidos por otros mtodos.
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 5 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
TERMODINAMICA
Generalidades.
Los Geoquimicos y Gelogos, los diagramas de equilibrio lo representan entre la
Lithosfera, Hidrosfera y Atmsfera; a los Fsicos, Metalurgistas y Qumicos les
provee un grafico muy usual y describe la pasividad, corrosin y disolucin de
minerales.
Las relaciones existentes entre la hidrosfera, lithosfera y atmsfera son
representadas en la siguiente fig.:
Las reacciones son homogneas heterogneas dependiendo sobre si o no ellos
ocurren dentro de una simple fase o en los lmites entre fases.
La Hidrosfera se refiere a la porcin liquida de la tierra, La Lithosfera es la corteza
terrestre y la atmsfera es la parte gaseosa que envuelve la tierra y los gases
dentro de la tierra.
La qumica-fsica de la mineralizacin es una gua importante y usual para los
metalurgistas desde que representa un gran inventario de reacciones importantes
en el sistema hidrometalurgico.
La principal diferencia es que los factores cinticos llega hacerse predominante
para un metalurgista, desde que las reacciones deben ocurrir en un tiempo
relativamente cortos para ser de importancia comercial.
La siguiente fig. ilustra la clase de reacciones de importancia para la
hidrometalurgia. La reaccin I, representa el equilibrio entre la atmosferahidrosfera y la reaccin II entre la hidrosfera-lithosfera, las cuales son de
importancia primaria y deben ser tratadas con detalle.
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 6 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Cada tipo de reaccin tiene especial implicacin para los metalurgistas. Tambin
el agua, el solvente universal, tiene propiedades nicas que hace posible no
solamente una mineralizacin, si no una rpida disolucin, transporte, procesos
de separacin y precipitacin que es vital para la aplicacin comercial en la
hidrometalurgia.
Homogeneas
Reacciones Quimicas
Disociacin Gaseosa
Difusin
atm
Homogeneas
Disociacin Electrolitica
Hidrlisis
Formacin de Complejos
Difusin de iones solubles
Heterogeneas
Disociacin
Disolucin Gaseosa
Evaporacin
Hidro
Tierra
II
Heterogeneo
Sublimacin
Oxidacin
Reduccin
Dehidratacin
Descomposicion
Litho
Homogeneo y
Difusin
Fundicin
Reacciones
Quimicas
Heterogeneo
Precipitacin
Corrosin
Disolucin
(Reacciones Electroquimicas)
Heterogeneo
Nucleacin
Precipitacin
Reacciones
Electroquimicas
La siguiente tabla da los elementos mas importantes en la lithosfera e hidrosfera
(Wells, 1962). Virtualmente todos los metales bases estn presentes en pequeas
cantidades
en
cantidades
trazas. Afortunadamente
los
procesos
de
mineralizacin dentro de la tierra, ambos la hidro y la piro, tienen como resultado
en la concentracin de los metales, bases importante.
Un segundo punto de inters es que sobre un volumen base, sobre el 90% de la
corteza terrestre esta compuesto de oxigeno.
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 7 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
De los metales, tales como el Aluminio, Hierro y magnesio son los mas
abundantes; La slice es el elemento mas abundante y otros como el oxigeno,
Sodio, Magnesio, Calcio y Potasio son componentes prominentes de ambos la
lithosfera y la hidrosfera.
Lithosfera
Hidrosfera
Elemento
Peso (%)
Volumen(%) Elemento Peso (%)
46.59
91.77
85.89
Si
27.72
0.80
10.80
Al
8.13
0.76
Cl
1.93
Fe
5.01
0.68
Na
1.07
Mg
2.09
0.56
Mg
0.13
Ca
3.63
1.48
0.09
Na
2.85
1.60
Ca
0.04
2.60
2.14
0.04
Ti
0.63
0.22
Otros
<0.01
Menas
metlicas,
mineral
Pequeas
cantidade
s
Diagrama Tensin-pH del agua.
a)
Asociacin con minerales .
El agua puede ser parte de la lithosfera cuando se encuentra qumicamente con
ciertos minerales.
Se encuentra en 2 formas:
Agua de Cristalizacin, es agua que esta presente como agua en la estructura del
mineral. Ejemplos son: CaSO4.2H2O y MgCl.6H2O.
La dehydratacin puede resultar en la simple remocin del agua por simple
calentamiento, tal como el caso del Gypsum para la fabricacin del yeso:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 8 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
CaSO4.2H2O + CaSO4 + 2H2O
La forma final es el mineral anhydro anhidrita, en el caso del MgCl 2.6H2O, la
descomposicin puede resultar en la formacin de un xido (McDonald y
Wadsworth, 1972).
MgCl2.6H2O + MgO + 2HCl + 5H2O
El agua puede estar presente como el in hidroxilo en la red de un cristal como es
el caso de la mica potasica KAl3Si3O10(OH)2 como en las arcillas tal como la
caolinita Al2Si2O5(OH)4, remover el in hidroxilo de estos minerales requieren muy
altas temperaturas.
b)
Reacciones dentro de la hidrosfera
Muchos tipos de reacciones homogneas ocurren dentro de la hidrosfera. Una de
estas es la disociacin electroltica. El agua misma es un ejemplo de acuerdo a la
reaccin:
H2O(l) = H+(aq) + OH-(aq)
La constante de Equilibrio K es la constante de Ostwald. En el caso del agua , K
tiene el valor 10-14 a temperatura ambiente y es igual al producto de actividades:
K(Ostwald) = aH+*aOHLa actividad del agua es tomada como la unidad
Por convencin la actividad es interpretada como sigue:
Iones y Molculas en soluciones diluidas:
La actividad es aproximadamente igual a la concentracin en moles /litro.
El solvente en una solucin diluida:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 9 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
La actividad es igual a la fraccin molar del solvente y es aproximadamente
la unidad.
Slidos lquidos puros en equilibrio con una solucin:
La actividad es exactamente la unidad.
Gases en equilibrio con una solucin:
La actividad es la presin parcial del gas en atmsferas.
Mezcla de lquidos:
La actividad de un componente dado es aproximadamente igual a la
fraccin molar.
En una solucin ideal la actividad es proporcional a la fraccin molar X, en
solucin y esta relacionado al potencial qumico por la ecuacin:
= o + RTlnX
o
donde es el potencial qumico estndar.
En una solucin no ideal, la fraccin molar y la actividad no son idnticas,
requiriendo una correccin de la fraccin molar por el coeficiente o
= o + RTlnX = = o + RTlna
para soluciones diluidas la fraccin molar puede ser reemplazada por la
concentracin , normalmente el estado estndar es tomado como la unidad.
La constante de equilibrio K esta relacionado a la energa libre de Gibbs por la
ecuacin:
-RTlnK = G = H-TS
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 10 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
donde
G, H y S
reaccin, en la cual
son la energa libre estndar, entalpa y entropa de la
y
son funciones de la temperatura, pero para
pequeos cambios de temperatura ellos pueden ser asumidos constantes y por lo
tanto
puede se calculada por la ecuacin anterior para alguna temperatura
intermedia.
El cambio de energa libre estndar para cualesquiera reaccin qumica es la
suma de los potenciales qumicos de los productos menos la suma de los
potenciales qumicos de los reactantes.
Por ejemplo para la reaccin del agua:
H2O(l) = H+(aq) + OH-(aq)
G = H+ + OH--H2O
o tambin:
G = producto iproductos - reactantes reactantes
o en forma general:
G = i i
La constante de equilibrio K para esta reaccin es dada por la ecuacin
termodinmica:
K = aH+ * aOH- / aH2O
Para soluciones bastante diluidas el H+ = 1, y lo mismo para OH+ = 1, por lo tanto
se igualan a la concentracin y en el caso del agua como se trata de un lquido
puro la actividad es la unidad de acuerdo a esto tenemos que:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 11 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
K = [ H+][OH-]
Para el caso de una reaccin qumica podemos aplicar la siguiente ecuacin
termodinmica:
G = G + RTlnQ
En el equilibrio : G = 0 , por lo tanto tenemos que :
G = -RTlnK
por lo tanto:
lnK = -G/RT = - i i/RT
Transformando a logaritmo decimal y a temperatura ambiente tenemos:
logK = - i i/1364
En este caso de los potenciales qumicos para el agua se da en la siguiente tabla:
elemento
H+
OH-
H2O
i(cal/mol)
-37,595
-56,690
Por lo tanto tenemos:
G = 19,075 Caloras / mol.
Aplicando la ecuacin tenemos:
log K = -14
entonces
K = 10 14
Para el caso del agua pura tenemos que:
[ H+] = [OH-]
10-14 = [ H+] [OH-]
entonces
[ H+] = [OH-] =10-7
La ecuacin (5) la podemos escribir en forma logartmica:
PK = PH + POH = 14
Por lo tanto para la solucin neutra (agua pura):
PH = 7 = POH = -log[OH-]
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 12 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Si adicionamos H+ al agua pura en la forma de un cido, entonces la
concentracin de iones H+ se incrementa, de acuerdo a la ecuacin (1) el pH
decrece del valor neutro de 7.
Por ejemplo: En una solucin 0.01 molar de H2SO4, la concentracin molar de [H+]
= 0.02 M por lo tanto el
pH = - Log [0.02] = 1.70
En algunas partes del mundo, la acidez de la lluvia cae por debajo de pH=5.6, en
el NE de EE.UU. por ejemplo el pH promedio de las lluvias es 4.6 y no es inusual
tener lluvias con pH=4.0 que es 1,000 veces ms cida que el agua destilada.
Otro tipo de reaccin que puede ocurrir dentro de la hidrosfera es la hidrlisis. Por
ejemplo el in cianuro reacciona con el agua para formar el HCN que se disocia
de acuerdo a la reaccin:
CN- + H2O HCN + OHLa hidrlisis de los iones ferricos en solucin, formndose un producto hidrolizado
soluble para formar la goethita de acuerdo a la reaccin siguiente:
Fe3+ + 2 H2O 4 FeO(OH) + 3 H+
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 13 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
En la construccin de los diagramas eh-pH, lo primero que hacerse es la
construccin de la zona de estabilidad del agua.
Se va a considerar las siguientes especies presentes:
H+, OH-, H2O, O2 y H2
Extrayendo los potenciales qumicos de tablas tenemos:
Compuestos
H+
i(cal/mol)
OH-
H2O
-37,595 -56,690
O2
H2
Las reacciones posibles a considerar son las siguientes se va a considerar los
siguientes parmetros tC= 25, [Mi]= 1M y pi = 1atm:
a) Encima del lmite u oxidacin del agua:
O2 + 4H+ + 4e 2H2O
Aplicando la ecuacin de Nerst tenemos:
De acuerdo a los parmetros se llega a la ecuacin sintetizada siguiente:
Determinando el
tenemos:
G= 2*(-56690) - [1*0 + 1*0] = -113380 cal/mol
Por lo tanto:
= -[-113380/23060*4] = 1.23 V
Por lo tanto la ecuacin a considerar para la oxidacin del agua es:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 14 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
b) Bajo el lmite o reduccin del agua:
Se puede considerar bajo dos formas:
2H+ + 2e H2
2H2O + 2e H2 + 2OH-
1)
2)
Pero el que mas se usa es la reaccin (1)
Aplicando la ecuacin de Nerst tenemos:
De acuerdo a los parmetros se llega a la ecuacin sintetizada siguiente:
Determinando el
tenemos:
G= 1*0 - [2*0] = 0.00 cal/mol
Por lo tanto:
= -[0.00/23060*4] = 0.00 V
Por lo tanto la ecuacin a considerar para la reduccin del agua es:
Encima y bajo el lmite de estabilidad depende de la presin, en un rango de
condiciones de fuerte oxidacin y fuerte reduccin, es tambin interesante que
cambios de presiones grandes afecten el voltaje (o lmites) solo ligeramente:
La siguiente figura ilustra la regin de estabilidad del agua entre una atmsfera de
oxigeno y una atmsfera de hidrogeno:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 15 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Construccin de los diagramas tensin-pH.
Para la construccin de los diagramas eh-pH, hay que tener en cuenta las
siguientes consideraciones:
I.
II.
Listado de todos los compuestos a ser considerados
Ordenamiento en orden creciente de los compuestos de acuerdo a su
estado de oxidacin y por pisos.
Cl. Los Guindos N 140
Telf.: 435-4127
La Molina
Pgina 16 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
III.
IV.
V.
Establecimiento de las reacciones electroqumicas qumicas entre dos
de los compuestos de acuerdo a su estado de oxidacin, completando
las reacciones con H2O, H+ y e-.
Aplicacin de las relaciones termodinmicas sobre el equilibrio
termodinmico qumico.
Dibujar finalmente el diagrama con las reacciones caractersticas del
sistema.
Para mayor claridad, construiremos primero el diagrama Ag-H2O, dada la nobleza
de este metal, es bastante simple y se construye solo con tres ecuaciones ya que
los compuestos estables en el rango de pH de 0-14 son:
Ag, Ag+ y Ag2O
Se puede observar que esta ordenado en forma creciente de acuerdo a su estado
de oxidacin
Luego lo ordenamos en pisos de acuerdo a su estado de oxidacin:
Estado de
oxidacin
+1
0
Ag2O
Ag+
Ag
Luego se entrelaza los compuestos entre los diferentes estados de oxidacin y del
mismo estado de oxidacin, tal como se observa a continuacin:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 17 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Estado de
oxidacin
3
+1
Ag
Ag2O
Ag
De esta forma observamos que solo existen tres reacciones a ser considerados
para la construccin de este diagrama eh-pH.
Luego
estamos
dispuestos
establecer
las
reacciones
qumicas
electroqumicas respectivas:
Comenzaremos con la reaccin 1, observen que estamos poniendo esta en
reduccin:
Ag+ + e Ag
1)
2)
Ag2O + 2H+ + 2e 2Ag + H2O y
Ag2O + 2H+ 2Ag + H2O
3)
Una vez establecido las respectivas reacciones se va a tablas para extraer los
respectivos potenciales electroqumicos:
Compuestos
Ag
Ag+aq
Ag2O
H2O
i(cal/mol)
+18,448
-2,395
-56,690
Y luego se aplica las respectivas relaciones termodinmicas para establecer las
ecuaciones respectivas, considerando una temperatura de 25C y [Mi]= 10-6M:
1)
eth = eth + 0.06log[aAg+]
todos los datos los conocemos a excepcin del eth.
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 18 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
G = 0-[18,448] = -18,448 cal/mol.
eth = -[-18,448/(23060*1)] = 0.78V.
Por lo tanto
eth = 0.78 + 0.06log[Ag+]
Luego tenemos:
Y como vamos a trabajar a una concentracin de todas las especies inicas de
10-6M. tenemos que:
eth= 0.42 V
eth = eth + 0.03log[aAg2O][aH+]2/[aAg][aH2O]
2)
por convencin sabemos que todos los compuestos slidos y lquidos puros sus
actividades es la unidad, por lo tanto tenemos que:
eth = eth + 0.06log [H+]
eth = eth - 0.06pH
Calculando
G = -56,690 + 0 -[-2,395 + 0] = -54,295 Cal/mol.
Por lo tanto
eth = -[-54,295]/(23,060*2)] = 1.18V.
Luego tenemos que:
eth = 1.18 - 0.06pH
3) Como es una reaccin qumica aqu no interviene la ecuacin de Nerst, por lo
tanto tenemos que:
K = [aAg+]2[ aH2O]/[aAg2O][ aH+]2 = [Ag+]2/[ H+]2
Tomando logaritmos, tenemos:
logK = 2log[Ag+] - 2log[ H+]
Calculando G = 2*18,448 56,690 -[-2,395 + 2*0] = -17399 cal/mol.
Por lo tanto:
logK = -(-17399/1364) = 12.75
Luego tenemos que: 12.75 = 2log[Ag+] + 2pH
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 19 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Por lo tanto tenemos que: pH = 6.38 - log[Ag+]
Donde
pH = 12.38
Una vez que tenemos todas estas relaciones, procedemos a realizar los
siguientes clculos:
1) eth= 0.42 V
2) eth = 1.18 - 0.06pH, calculando para pH = O tenemos eth =1.18V y para pH
= 14 tenemos eth =0.34V
3) pH = 12.38
con estos datos se construye el diagrama eth pH para la Ag-H2O, tal como se da
a continuacin:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 20 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Influencia de elementos acomplejants en los diagramas tensin-pH.
Veamos ahora lo que sucede al campo de estabilidad de la plata en presencia de
iones CN- , cunado se construye este diagrama, demostraremos que conocida la
cantidad de CNNa total agregado, es posible encontrar una relacin entre el CN y el pH:
Si agregamos NaCN al agua, tendremos las siguientes relaciones de equilibrio:
NaCN Na+ + CN-
(1)
H+ + CN- HCN
(4)
cuya constante de equilibrio de esta ltima reaccin es: k= 2.512x109 1x109.4
por otra parte sabemos que:
[NaCN]total = [HCN] + [CN-]
(5)
[ HCN ]
log [ H + ][CN ] = 9.4
de (4) tenemos :
(6)
de esta ltima relacin despejamos la concentracin de cianuro:
[CN-] = [HCN]x10(pH-9.4)
(7)
Reemplazando (7) en (5) tenemos:
[NaCN]total = [HCN]x{1 + 10(pH-9.4)}
(8)
Si tomamos logaritmo y transponiendo trminos tenemos:
log[HCN] = log[NaCN]total - log{1 + 10(pH-9.4)} (9)
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 21 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
de la ecuacin (7) tomando logaritmo y transponiendo trminos tenemos:
log[HCN] = log[CN-] pH + 9.4
(10)
Igualando (9) y (10) y despejando la concentracin de CN-:
log[CN-] = log[NaCN]total -log{1 + 10(pH-9.4)} + pH-9.4
(11)
Esta ltima relacin nos permite conocer la concentracin de cianuro libre en
funcin del pH para una concentracin de cianuro de sodio conocida; en funcin
de esto para una [NaCN]total = 10-2M que corresponde aproximadamente a 0.05%
NaCN, podemos determinar la concentracin de cianuro libre para diferentes pH
tal como podemos apreciar en el siguiente cuadro:
pH
14
13
12
11
10
9.4
9
8
2
CN0.0099997488
0.0099974887
0.0099749441
0.0097549663
0.0079923999
0.0050000000
0.0028474725
0.0003828650
0.0000000004
Tal como se puede apreciar en la siguiente grafica:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 22 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Desde el punto de vista termodinmico, la estabilidad del cianuro lo podemos
observar en el diagrama eh-pH para el caso del CN- -H2O si tomamos en
consideracin las siguientes reacciones:
HCNO CNO- + H+
(12)
HCN CN- + H+
(13)
HCNO + 2H+ + 2e HCN + H2O
(14)
CNO- + 3H+ + 2e HCN + H2O
(15)
CNO- + 2H+ + 2e CN- + H2O
(16)
tomando en cuenta la ecuacin de Nerst y los potenciales qumicos de las
sustancias que estn presentes y que se indican a continuacin:
Compuesto
i (Cal/mol)
HCN
CN-
HCNO
CNO-
+29600 +39370 -28980 -23750
H2O
-56690
Podemos obtener el siguiente grafico de eh pH para el CN- - H2O:
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 23 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Para el caso del oro, plata y CN- se tiene que adicionar las siguientes reacciones y
ecuaciones que a continuacin se indican y tomando en cuenta los potenciales
qumicos siguientes:
Compuesto
AgCN2-aq
i (Cal/mol)
+72,047
AgCN
Au+
AuCN2-aq AuCN
+38,499 39,000
Ag+ + 2CN- AgCN2-
4)
K = [AgCN2-]/[Ag+][CN-]2 = 1018.8
log[Ag+]/[Ag(CN)2-] = -2log[CN-] 18.8
pCN = 9.4 + 0.5log[Ag+]/[Ag(CN)2-]
Au+ + 2CN- AuCN2-
4)
K = [AuCN2-]/ [Au+] [CN-]2 = 1038
log[Au+]/[Au(CN)2-] = -2log[CN-] 38
pCN = 9.4 + 0.5log[Au+]/[Au(CN)2-]
AgCN2- + e Ag + 2CN-
5)
eth = eth + 0.06log [AgCN2-]/ [CN-]2
eth = -0.31V
eth = -0.31 - 0.12log[CN-] + 0.06log[AgCN2-]
eth = -0.664 - 0.12log[CN-]
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 24 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
AuCN2- + e Au + 2CN-
5a)
eth = eth + 0.06log[AuCN2-]/[CN-]2
eth = -0.60V
eth = -0.60 - 0.12log[CN-] + 0.06log[AuCN2-]
eth = -0.96 - 0.12log[CN-]
De acuerdo a esto se construyo la figura que se da a continuacin para una
concentracin de CNNa total = 10-2M que corresponde aproximadamente a 0.05%
NaCN,
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 25 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
las actividades del [AuCN2-] y el [AgCN2-] estn a 10-4M que corresponde a una
concentracin de Ag y Au de 10 y 20 g/m3 respectivamente, por lo tanto la
condiciones a la que se ha construido este diagrama es a operaciones practicas.
De este diagrama se puede sacar las siguientes conclusiones:
El Au y la Ag son metales muy nobles ya que se encuentra dentro de la
zona de estabilidad del agua en la regin de bajos pH, pero son menos
nobles a altos pH en soluciones de cianuro. Notablemente la plata es
mucho mas inerte que el oro en presencia de CN-
Las reacciones de oxidacin (5) involucran el ceder un electrn que
necesita ser aceptada por alguna de las siguientes reacciones de
reduccin:
2H+ +2e H2
(1)
O2 + 4H+ + 4e 2H2O
(2)
O2 +2H+ +2e H2O2
(3)
H2O2 + 2H+ + 2e 2H2O
(4)
Estas reacciones son ilustradas asumiendo una actividad unitaria para
el H2O2 y las especies gaseosas.
Muchos investigadores tienen confirmada que la disolucin de Au y Ag
es acompaada por la produccin de H2O2 y de este modo la ecuacin 3
necesita ser considerado como reaccin de reduccin.
Muchos investigadores indican que la fuerza del agente oxidante tal
como el H2O2 puede convertir CN- en cianato, el cual no es capaz de
oxidar el oro y la plata.
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 26 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
La reaccin de disolucin:
ZnCN4-2 + 2e Zn + 4CNEs tambin ploteada, por que la cementacin con Zn es comnmente
usada para recuperar ambos elementos el oro y la plata.
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 27 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 28 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 29 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 30 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
Pgina 31 de 31
Edwilde Yoplac Castromonte
MSc. DCP. Ing. Metalurgista. Consultor en Hidrometalurgia y Beneficio de Minerales
Cl. Los Guindos N 140
La Molina
Telf.: 435-4127
También podría gustarte
- Extraccion de Oro en Pilas de LixiviacionDocumento14 páginasExtraccion de Oro en Pilas de Lixiviacionnickel de la cruz fortuna96% (25)
- Cianuracion Por AgitacionDocumento20 páginasCianuracion Por Agitacionnickel de la cruz fortuna96% (23)
- Apunte Hidro IDocumento103 páginasApunte Hidro IPatricio Mix Sepulveda100% (44)
- Libro Hidrometalurgia UDECDocumento200 páginasLibro Hidrometalurgia UDECFrancisco Javier Alarcón Garrido92% (24)
- Hidromet de OroDocumento54 páginasHidromet de OroJohan Vargas Pando80% (5)
- Pirometalurgia IDocumento219 páginasPirometalurgia IPatricio Mix Sepulveda97% (32)
- Manual de FlotaciónDocumento10 páginasManual de Flotaciónwarrenrr100% (7)
- Metalurgia ExtractivaDocumento37 páginasMetalurgia ExtractivaMarco Andre Alegría60% (5)
- Circuitos de Flotación y Balance MetalurgicoDocumento10 páginasCircuitos de Flotación y Balance Metalurgiconickel de la cruz fortuna83% (29)
- Metalurgia ExtractivaDocumento107 páginasMetalurgia ExtractivaGabriel Inostroza MedinaAún no hay calificaciones
- Fundicion de Precipitados de OroDocumento15 páginasFundicion de Precipitados de OroCarlos Tolentino Tazo100% (3)
- Capitulo VDocumento27 páginasCapitulo VNataniel Linares Gutiérrez100% (1)
- Capitulo Ii Agentes Quimicos de FlotacionDocumento48 páginasCapitulo Ii Agentes Quimicos de Flotacionnlinaresg100% (11)
- Lixiviacion de Cobre Por Agitacion en BotellasDocumento10 páginasLixiviacion de Cobre Por Agitacion en BotellashhhAún no hay calificaciones
- Capitulo IvDocumento44 páginasCapitulo IvNataniel Linares Gutiérrez100% (2)
- Técnicas de caracterización y procedimientos empleados en la mineralogía aplicada al beneficio de mineralesDe EverandTécnicas de caracterización y procedimientos empleados en la mineralogía aplicada al beneficio de mineralesCalificación: 5 de 5 estrellas5/5 (1)
- Geoestadística de Yacimientos de Cobre Chilenos: 35 años de investigación aplicadaDe EverandGeoestadística de Yacimientos de Cobre Chilenos: 35 años de investigación aplicadaAún no hay calificaciones
- Cap 1 Equilibrio Hidrometalurgico (Especiación)Documento65 páginasCap 1 Equilibrio Hidrometalurgico (Especiación)mirtre9912Aún no hay calificaciones
- Clase 1 Introducción A La HidrometalurgíaDocumento37 páginasClase 1 Introducción A La HidrometalurgíaJorge Burgos Ibañez0% (1)
- Clase 1 Metales No FerrososDocumento33 páginasClase 1 Metales No FerrososAnthony Quispe CarbajalAún no hay calificaciones
- Hidrometalurgia (I Unidad)Documento23 páginasHidrometalurgia (I Unidad)ANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Los - Metales - Alcalinos 2 PDFDocumento80 páginasLos - Metales - Alcalinos 2 PDFalanAún no hay calificaciones
- Introducción A La Hidrometalurgia 2023Documento31 páginasIntroducción A La Hidrometalurgia 2023Juan David Benites GarciaAún no hay calificaciones
- Lixiviacion CuDocumento56 páginasLixiviacion CuxanderdakotaAún no hay calificaciones
- HidrometalurgiaDocumento39 páginasHidrometalurgiarodriahum100% (1)
- Clase - 27 08 2019Documento15 páginasClase - 27 08 2019Bart FrienderAún no hay calificaciones
- Tema 2Documento38 páginasTema 2Ary solo yoAún no hay calificaciones
- Compilacion de Geotecnia AmbientalDocumento40 páginasCompilacion de Geotecnia AmbientalRafael OrtizAún no hay calificaciones
- Programa de Hidrometalurgia y ElectroMetDocumento3 páginasPrograma de Hidrometalurgia y ElectroMetjuan manuel paezAún no hay calificaciones
- (PEP I) 2. Lixiviacion y Diagramas de Pourbaix (Clase 02 04 2019)Documento39 páginas(PEP I) 2. Lixiviacion y Diagramas de Pourbaix (Clase 02 04 2019)Bart FrienderAún no hay calificaciones
- PlataDocumento6 páginasPlataJuan Carlos Campos CondoriAún no hay calificaciones
- Torres de Enfriamento TTODocumento84 páginasTorres de Enfriamento TTOJuan Carlos RioboAún no hay calificaciones
- Procesos Hidrometalúrgicos PPT (Unidad 2)Documento21 páginasProcesos Hidrometalúrgicos PPT (Unidad 2)sara richardsAún no hay calificaciones
- Finalicimo HidroDocumento5 páginasFinalicimo HidroAi B de komachiAún no hay calificaciones
- Metales AlcalinoDocumento28 páginasMetales AlcalinoKeyla Milena Romero AldapiAún no hay calificaciones
- 28 - Tarea 4.proponer Solución Del Problema de Contaminación Del SueloDocumento9 páginas28 - Tarea 4.proponer Solución Del Problema de Contaminación Del SueloKntro Yineth IvonAún no hay calificaciones
- Tratamiento de Materia Inorganica en Aguas ResidualesDocumento41 páginasTratamiento de Materia Inorganica en Aguas ResidualesJenn Rizzo100% (1)
- LixiviacionDocumento24 páginasLixiviacionAndres ContrerasAún no hay calificaciones
- Capitulo 1 Introducción Me IIDocumento61 páginasCapitulo 1 Introducción Me IImexalurgiaAún no hay calificaciones
- Procesos de Concentracion de SolucionesDocumento33 páginasProcesos de Concentracion de SolucionesDarioAún no hay calificaciones
- Cuestionario LIXDocumento8 páginasCuestionario LIXAntonia Anastasia PereiraAún no hay calificaciones
- Periodicidad Química - 083423Documento11 páginasPeriodicidad Química - 083423Cesar AguilarAún no hay calificaciones
- Tema 6 - Drenaje Ácido de MinasDocumento41 páginasTema 6 - Drenaje Ácido de MinasOscar ValverdeAún no hay calificaciones
- Reactivos de LixiviacionDocumento13 páginasReactivos de LixiviacionWilsonEnriqueCarhuatantaBonifacio100% (1)
- Metal Ext II Cuestionario 3 VELÁSQUEZ NAYSMARYS.Documento13 páginasMetal Ext II Cuestionario 3 VELÁSQUEZ NAYSMARYS.Ricardo RondonAún no hay calificaciones
- Biorremediación de Metales Pesados Tóxicos Utilizando Autótrofos Acidotermofílicos - Gabriel MartinezDocumento3 páginasBiorremediación de Metales Pesados Tóxicos Utilizando Autótrofos Acidotermofílicos - Gabriel MartinezKevin AguilarAún no hay calificaciones
- Hidrometalurgia PDFDocumento99 páginasHidrometalurgia PDFVictor Alonso67% (3)
- PH de Los Toxicos Adecuado en El Proceso de AbsorcionDocumento7 páginasPH de Los Toxicos Adecuado en El Proceso de AbsorcionThe RojaxAún no hay calificaciones
- Modelos de Corrosión en Matales FundidosDocumento5 páginasModelos de Corrosión en Matales FundidosKATHERINE NICOLE GARCIA CAICEDOAún no hay calificaciones
- Este Artículo Trata Sobre Un Elemento QuímicoDocumento36 páginasEste Artículo Trata Sobre Un Elemento QuímicoAnonymous 2dXspv9ovxAún no hay calificaciones
- GENERALIDADES SOBRE MANGANESO. WWW - Clubdelquimico.tkDocumento23 páginasGENERALIDADES SOBRE MANGANESO. WWW - Clubdelquimico.tkclubdelquimico.blogspot.com100% (1)
- Remediacion Por ElectrodeposicionDocumento7 páginasRemediacion Por ElectrodeposicionJorge AndresAún no hay calificaciones
- Cinetica de La Lixiviacion PDFDocumento25 páginasCinetica de La Lixiviacion PDFHoussein Fernandez YparraguirreAún no hay calificaciones
- Unidad I Hidrometalurgia AglomeraciónDocumento60 páginasUnidad I Hidrometalurgia AglomeraciónAlex RodríguezAún no hay calificaciones
- Capitulo 9-Depresion de Pirita en La Flotacion Minerales de CobreDocumento27 páginasCapitulo 9-Depresion de Pirita en La Flotacion Minerales de Cobrecinthia100% (3)
- Texto Hidro 14.08.20Documento106 páginasTexto Hidro 14.08.20Alberth Jorge Gutierrez FloresAún no hay calificaciones
- Clase #3 Coagulacion y FloculacionDocumento57 páginasClase #3 Coagulacion y Floculacionmiluska garciaAún no hay calificaciones
- Determinación de Metales Pesados en Agua Residualen Proceso de GalvanoplastiaDocumento9 páginasDeterminación de Metales Pesados en Agua Residualen Proceso de GalvanoplastiaAnonymous Qp2rla6Aún no hay calificaciones
- HIDROXIQUINOLINADocumento4 páginasHIDROXIQUINOLINADamAún no hay calificaciones
- Materiales Metálicos y No Metálicos.Documento26 páginasMateriales Metálicos y No Metálicos.josgat10Aún no hay calificaciones
- QW-193.1 Procedimiento Especímenes de Calificación.Documento1 páginaQW-193.1 Procedimiento Especímenes de Calificación.nickel de la cruz fortunaAún no hay calificaciones
- Norma Técnica NTP 350.011-1 PERUANA 2004: 2004-06-10 1 EdiciónDocumento46 páginasNorma Técnica NTP 350.011-1 PERUANA 2004: 2004-06-10 1 Ediciónnickel de la cruz fortuna80% (5)
- Difusión en SólidosDocumento11 páginasDifusión en SólidosDiego Villarroel GuerraAún no hay calificaciones
- Flujograma de Comunicación 1Documento1 páginaFlujograma de Comunicación 1nickel de la cruz fortunaAún no hay calificaciones
- Como Soldar Con TIGDocumento17 páginasComo Soldar Con TIGangelAún no hay calificaciones
- Refinado Del ArrabioDocumento8 páginasRefinado Del Arrabiovfelizro3Aún no hay calificaciones
- Celdas de FlotaciónDocumento14 páginasCeldas de Flotaciónnickel de la cruz fortuna100% (25)
- Tamaño Optimo de MallasDocumento10 páginasTamaño Optimo de Mallasnickel de la cruz fortuna100% (1)
- Abandono de Labores en Mina SubterraneaDocumento16 páginasAbandono de Labores en Mina Subterraneanickel de la cruz fortuna100% (7)
- Circuitos de Flotación y Balance MetalurgicoDocumento10 páginasCircuitos de Flotación y Balance Metalurgiconickel de la cruz fortuna83% (29)
- Liderazgo en SeguridadDocumento2 páginasLiderazgo en SeguridadMauricio Santisteban Campos RoblesAún no hay calificaciones
- Fisico-Quimica de Superficie e InterfasesDocumento9 páginasFisico-Quimica de Superficie e Interfasesnickel de la cruz fortuna100% (3)
- Preparacion Mecanica de MineralesDocumento24 páginasPreparacion Mecanica de Mineralesnickel de la cruz fortuna97% (108)
- Destruccion de Cianuro en Efluentes MinerosDocumento21 páginasDestruccion de Cianuro en Efluentes Minerosnickel de la cruz fortuna100% (11)
- ConminucionDocumento22 páginasConminucionnickel de la cruz fortuna100% (2)
- Tratamiento de Materiales MineralogicosDocumento13 páginasTratamiento de Materiales Mineralogicosnickel de la cruz fortuna100% (3)
- Avances Mediante El Uso de Celdas ColumnasDocumento21 páginasAvances Mediante El Uso de Celdas Columnasnickel de la cruz fortuna100% (7)
- Remolienda en FlotaciónDocumento37 páginasRemolienda en Flotaciónnickel de la cruz fortuna100% (28)
- Selección de EspumantesDocumento10 páginasSelección de Espumantesnickel de la cruz fortuna100% (7)
- Accidentes QuimicosDocumento135 páginasAccidentes Quimicosnickel de la cruz fortuna100% (20)
- Mecanismos de FlotaciónDocumento16 páginasMecanismos de Flotaciónnickel de la cruz fortuna100% (18)
- Reactivos ColectoresDocumento23 páginasReactivos Colectoresnickel de la cruz fortuna100% (3)
- CPTM PDFDocumento11 páginasCPTM PDFfelix colmenaresAún no hay calificaciones
- Las Enseñanzas de Carlos CastanedaDocumento325 páginasLas Enseñanzas de Carlos Castanedajmperezluis100% (7)
- La Sabiduría de La CruzDocumento4 páginasLa Sabiduría de La CruzdanielpablokmAún no hay calificaciones
- Contaminacion de SueloDocumento13 páginasContaminacion de Suelojenni mozoAún no hay calificaciones
- El Viejo y El DiabloDocumento8 páginasEl Viejo y El DiabloFrancisco Triviño50% (2)
- BD+C StudyGuide-ESDocumento246 páginasBD+C StudyGuide-ESredalfsAún no hay calificaciones
- Capitulo 11 SoldaduraDocumento28 páginasCapitulo 11 SoldaduraJonatan Pozo PalaciosAún no hay calificaciones
- 3WT82526AA000AA2 Datasheet EsDocumento4 páginas3WT82526AA000AA2 Datasheet Eslilian cruz alfaroAún no hay calificaciones
- La Historia de Éxito de Kola Real Una de Las Marcas Más Populares de AJE GROUPDocumento4 páginasLa Historia de Éxito de Kola Real Una de Las Marcas Más Populares de AJE GROUPFranco Yarleque LinoAún no hay calificaciones
- Introducción Granjas AmericanasDocumento2 páginasIntroducción Granjas AmericanasRocio Iglesias SampedroAún no hay calificaciones
- Contabilidad Hongos 2Documento27 páginasContabilidad Hongos 2KalbornozQuintulAún no hay calificaciones
- MOTORES Clasificación, Aspectos Teóricos y Principios de FuncionamientoDocumento88 páginasMOTORES Clasificación, Aspectos Teóricos y Principios de FuncionamientoRamón García JiménezAún no hay calificaciones
- Practica de Sensibilidad + Casos ClinicosDocumento12 páginasPractica de Sensibilidad + Casos Clinicosalison.barreraAún no hay calificaciones
- Cantos A La Santisima Virgen MariaDocumento5 páginasCantos A La Santisima Virgen MariakarenmvcAún no hay calificaciones
- CMT Abb Unigear Zs 2012Documento96 páginasCMT Abb Unigear Zs 2012Jhonny Elvis Pariona NarcisoAún no hay calificaciones
- Carcazasbolsos Copia 2Documento1 páginaCarcazasbolsos Copia 2ZAVKA ALFARO MARSCHHAUSENAún no hay calificaciones
- 2015 - EJEMPLOS LEAN HOSPITALES - En.esDocumento11 páginas2015 - EJEMPLOS LEAN HOSPITALES - En.esJohnny SinmalezaAún no hay calificaciones
- MetarurgliaDocumento43 páginasMetarurglialggs773Aún no hay calificaciones
- Corte Fugado Detalle ConstructivoDocumento1 páginaCorte Fugado Detalle ConstructivoHector HernandezAún no hay calificaciones
- Arepas de Chorizo y Plátano de CanariaDocumento2 páginasArepas de Chorizo y Plátano de CanariaGonzalo Rodríguez JoverAún no hay calificaciones
- Polo Ramos Estudio PrefactibilidadDocumento195 páginasPolo Ramos Estudio PrefactibilidadOscar Espejo LanzaraAún no hay calificaciones
- Glosario de InvestigacionDocumento3 páginasGlosario de InvestigacionMARIA CECILIA GARCIA RODRIGUEZAún no hay calificaciones
- Hidroeléctrica de PasadaDocumento6 páginasHidroeléctrica de PasadaBenja NavarroAún no hay calificaciones
- AntecedentesDocumento5 páginasAntecedentesAna Aracelli LázaroAún no hay calificaciones
- ANEMIA INVETIGACION Corregido PaoDocumento30 páginasANEMIA INVETIGACION Corregido PaomarcosAún no hay calificaciones
- ZapatasDocumento4 páginasZapatasLudmerMamaniAún no hay calificaciones
- Genéticas en LinfomasDocumento26 páginasGenéticas en LinfomasJuanCarlosHernandezBalcazarAún no hay calificaciones
- Tema 4 BotánicaDocumento5 páginasTema 4 BotánicaAna Garcia MartinezAún no hay calificaciones
- Guía Artes 5° 2Documento4 páginasGuía Artes 5° 2albaAún no hay calificaciones
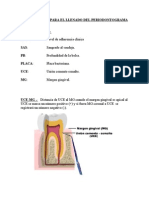
- EXPLICACION Periodontograma IDocumento4 páginasEXPLICACION Periodontograma IYochito75% (4)