Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Hidrometalurgia (I Unidad)
Cargado por
ANTONI KEYVI MENDOZA GUTIERREZTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Hidrometalurgia (I Unidad)
Cargado por
ANTONI KEYVI MENDOZA GUTIERREZCopyright:
Formatos disponibles
HIDROMETALURGIA: I UNIDAD
HIDROMETALURGIA
DEFINICIÓN:
Estudia la extracción y/o refinación de los metales de sus menas (minerales,
concentrados, calcinas, etc.), por medio de soluciones acuosas como agentes
de disolución.
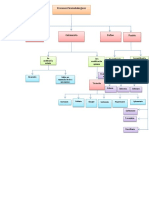
ETAPAS DEL PROCESO GENERAL HIDROMETALÚRGICO:
Alimentación
1º Preparación
Reactivos
2º Lixiviación
Residuos
Separación S/L
Sólidos de lixiv.
3º Purificación
Residuos
Separación S/L
Sólidos de purif.
5º
Recup. Metales Regeneración
4º Recuperación
Secundarios Soluc. Lixiv.
Metal Sub productos Relaves
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 1
HIDROMETALURGIA: I UNIDAD
1º. Preparación de la alimentación:
Física: Secado, trituración, molienda, concentración, etc.
Química: tostación (sulfuros a óxidos, sulfatos a cloruros).
2º. Producción de la solución cargada con el metal(es):
Lixiviación: Disolución de metales presentes en la alimentación.
3º. Purificación de la solución:
Eliminación de impurezas de la solución cargada.
4º. Producción del metal:
Precipitación del metal o metales de la solución.
5º. Regeneración de la solución:
Recuperación del reactivo principal para su reciclo a lixiviación.
VENTAJAS Y DESVENTAJAS DEL PROCESO HIDROMETALÚRGICO:
Ventajas:
Menor contaminación ambiental. Fácil control y automatización. Menor
costo de energía. Se pueden trabajar minerales de baja ley y desperdicios
de minas.
Desventajas:
Tasa de producción relativamente baja, esto implica que el tamaño de la
planta sea muy grande. Manejo de grandes cantidades de soluciones.
Reactivos caros.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 2
HIDROMETALURGIA: I UNIDAD
DIAGRAMA DE FLUJO DEL PROCESO HIDROMETALURGICO
DEL ZINC.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 3
HIDROMETALURGIA: I UNIDAD
LIXIVIACION
a) DEFINICIÓN:
Proceso de extracción de un constituyente soluble de un sólido por medio de
un disolvente. Puede ser parcial o total:
Parcial: Ejemplo la disolución ácida de calcopirita con sulfato férrico a
condiciones estándar (25ºC, 1 atm):
Total: Ejemplo la disolución ácida de calcopirita a elevadas temperaturas
y presiones:
b) MATERIAS PRIMAS:
Metales nativos: , etc.
Metales de deshechos: Escorias, lodos, polvos, etc.
Productos de cementación.
Minerales oxidados: Óxidos, carbonatos, hidróxidos y silicatos.
Calcinas (sulfuros tostados).
Minerales sulfurados de , etc.
c) AGENTES DE LIXIVIACIÓN:
Agua: Para lixiviar calcinas de sulfatos o cloruros.
Ácidos:
Bases: .
Sales en solución acuosa: , ,
(tiosulfato de sodio), (acuoso), , .
Ejemplo : Lixiviación de con persulfato de amonio en presencia de
:
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 4
HIDROMETALURGIA: I UNIDAD
d) REQUERIMIENTOS DEL REACTIVO DE LIXIVIACIÓN:
a) Debe ser selectivo para disolver al metal o metales deseados, sin reaccionar
con los compuestos no deseados (o reaccionar muy lentamente).
b) No debe ser muy corrosivo.
c) No debe ser muy costoso o debe ser fácilmente recuperable.
d) Debe tener suficiente solubilidad para lograr velocidad de reacción
adecuada.
La selectividad depende de la concentración del agente lixiviante, la
temperatura y el tiempo de contacto. Los tres factores incrementan la lixiviación
o disolución del metal e impurezas, por lo tanto se deben identificar los
óptimos para una extracción máxima y un nivel mínimo de impurezas.
TERMODINAMICA DE LA LIXIVIACION
Los diagramas de POURBAIX o diagramas – predicen la posibilidad
termodinámica del proceso de lixiviación. De estas gráficas se pueden determinar:
Las condiciones necesarias para descomponer un mineral y lixiviar un metal
selectivamente.
Las condiciones necesarias para remover el metal de la solución lixiviada,
precipitándolo en alguna forma sólida.
: mide el comportamiento ácido o básico del sistema.
: mide el estado de oxidación o reducción del sistema.
Un alto valor del (medido en voltios) indica que el sistema es esencialmente
oxidante o tiene tendencia hacia un estado oxidado.
Un bajo valor del indica que el sistema es esencialmente reductor o tiene
tendencia hacia un estado reducido.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 5
HIDROMETALURGIA: I UNIDAD
Para aumentar el se adiciona un oxidante al sistema.
Para disminuir el se adiciona un reductor al sistema.
Los oxidantes más comunes son el oxígeno, cloro y peróxido de hidrógeno
Los reductores más comunes son los sulfuros metálicos o los metales
elementales.
1. DISOLUCIÓN DE UNA SAL:
Muchas sales metálicas son fácilmente solubles en agua. Por ejemplo, el sulfato
de cobre puede disolverse en agua para producir una solución de alrededor de
80 g/litro a temperatura ambiente:
Los límites de este tipo de disolución son la disponibilidad de minerales que
sean sales y la solubilidad de estas sales en agua. Otros tipos de sales
importantes en hidrometalurgia incluyen: sulfatos, cianuros, cloruros, nitratos,
cromatos, percloratos, molibdatos, cloratos, etc.
2. LIXIVIACIÓN ÁCIDA DE ÓXIDOS METÁLICOS:
Los metales son frecuentemente hallados en la naturaleza en forma de óxidos.
Muchos de estos minerales oxidados se pueden lixiviar fácilmente con
soluciones acuosas ácidas:
3. LIXIVIACIÓN BÁSICA DE ÓXIDOS METÁLICOS:
La lixiviación básica ha sido practicada por más de 100 años en la industria del
aluminio. El proceso Bayer usa altas temperaturas y soluciones lixiviantes
fuertemente básicas para disolver al aluminio de los minerales de bauxita. El
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 6
HIDROMETALURGIA: I UNIDAD
zinc también es altamente soluble en soluciones básicas y este comportamiento
ha sido aplicado para lixiviar al zinc desde minerales oxidados:
DIAGRAMA DE POURBAIX,
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 7
HIDROMETALURGIA: I UNIDAD
DIAGRAMA DE POURBAIX, –
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 8
HIDROMETALURGIA: I UNIDAD
4. LIXIVIACIÓN CON FORMACIÓN DE IONES COMPLEJOS:
Los iones complejos son formados cuando los metales interactúan con ligandos
que están presentes en la solución. Los ligandos típicamente aumentan la
solubilidad de los metales, mejorando así la lixiviación. Los ligandos más
comunes incluyen al cloro, cianuro, amoniaco y tiosulfato.
Ejemplos de complejos formados con estos ligandos:
5. LIXIVIACIÓN CON OXIDACIÓN:
Muchos minerales se encuentran en la naturaleza conteniendo metales en su
estado reducido. Para lixiviar al metal, el mineral requiere una oxidación con un
agente oxidante. Los oxidantes comunes en hidrometalurgia incluyen al
oxígeno, cloro, ácido nítrico, peróxido de hidrogeno, clorato y el ión férrico
( ). Algunas reacciones comunes de oxidación son las siguientes:
Proceso de lixiviación a presión del :
Proceso de oxidación de la pirita:
Cianuración de oro y plata:
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 9
HIDROMETALURGIA: I UNIDAD
DIAGRAMA DE POURBAIX, – – ,
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 10
HIDROMETALURGIA: I UNIDAD
TRATAMIENTO DE SOLUCIONES DE LIXIVIACION
Precipitación selectiva de los valores metálicos en solución para purificar la
solución lixiviada o recuperar los metales de interés, empleando métodos
químicos, electroquímicos o extracción por solventes.
1. METODOS QUIMICOS:
a) PRECIPITACIÓN DE SULFUROS METÁLICOS:
- El ácido sulfhídrico puede precipitar una serie de iones metálicos mediante
un ajuste adecuado del pH de la solución:
H2S(g) = H2S(ac) = 2H+ + S2-
- A condiciones estándar: .
Pero:
……… (1) Tabla N° 18.1
- Para cualquier sulfuro metálico:
MmSn = m Mz+ + n S2-
……… (2) Tabla N° 18.2
- Relacionando ecuaciones (1) y (2): es posible determinar la tendencia
termodinámica de un sulfuro metálico a precipitar a un pH dado:
Donde:
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 11
HIDROMETALURGIA: I UNIDAD
Entonces:
, Equilibrio: La solución está saturada y
el sistema está en equilibrio con una composición constante.
, No ocurre precipitación del sulfuro: La
solución está insaturada y se puede disolver más sólido hasta alcanzar el
equilibrio.
, Si ocurre precipitación del sulfuro: La
solución está sobresaturada y el sólido se precipitará hasta alcanzar el
equilibrio.
En el esquema anterior se observa que “si en el instante de la mezcla el ,
habrá precipitación”, con lo que se reducen las concentraciones iónicas en solución
hasta que el alcance su valor de equilibrio.
- Gráfica para la precipitación de sulfuros metálicos:
De la ecuación (2):
-1 -
-2 - CuI CuII NiII MnII
-3 -
-4
-60 -45 -30 -15 0
Los sulfuros metálicos precipitan a la derecha de las rectas. Para Y = 0 , se lee los
Kps en las abscisas.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 12
HIDROMETALURGIA: I UNIDAD
b) PRECIPITACIÓN DE HIDRÓXIDOS METÁLICOS (POR CAMBIO DE PH):
- Para cualquier hidróxido metálico:
……… TABLA N° 4.3
Con los datos de es posible determinar la tendencia termodinámica de un
hidróxido metálico a precipitar a un pH dado o calcular el pH al cual la
hidrólisis (precipitación) no puede ocurrir:
Donde:
- Gráfica para la precipitación de hidróxidos metálicos:
Pero:
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 13
HIDROMETALURGIA: I UNIDAD
-2 0 2 4 6 8 10 12 14
0
-1
-2
-3
-4
-2 0 2 4 6 8 10 12 14
pH
La precipitación del hidróxido metálico ocurre a la derecha de las líneas.
c) PRECIPITACIÓN DE CARBONATOS:
- El CO2 (g) se disuelve en agua formando el ácido débil H2CO3(ac):
- A condiciones estándar:
……… (1)
- Para cualquier carbonato metálico:
TABLA N° 4.4 ………. (2)
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 14
HIDROMETALURGIA: I UNIDAD
Relacionando ecuaciones (1) y (2) es posible determinar la tendencia termodinámica
de un carbonato metálico a precipitar a un pH dado:
Donde:
- Gráfica para la precipitación de carbonatos metálicos:
-20 -15 -10 -5 0 5 10 15
0
-1 si ppta. PbCO3
-2 no ppta.
-3
-4
-20 -15 -10 -5 0 5 10 15
La precipitación del carbonato metálico se efectúa a la derecha de las rectas.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 15
HIDROMETALURGIA: I UNIDAD
2. MÉTODOS ELECTROQUÍMICOS:
d) CEMENTACIÓN:
Es la precipitación de un ión metálico de una solución acuosa por la adición de
un metal sólido más activo que el metal a precipitar, formándose una celda de
corrosión galvánica.
La condición termodinámica del proceso radica en la diferencia de los
potenciales de equilibrio. Para reducir un ión metálico en solución es
necesario que el potencial del agente reductor sea más negativo que el
potencial del sistema metálico a reducir.
LADO CATODICO E0 , voltios
1.45
1.20
0.34
0.00 “Potenciales estándar
- 0.25 de reducción”.
- 0.28
- 0.402
- 0.44
- 0.763
LADO ANODICO
Ejemplo:
Cementación de Cu2+ sobre chatarra de Fe:
R.C:
R.A:
--------------------------------------------------------------------------------------------
R.T:
(Convenio Americano)
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 16
HIDROMETALURGIA: I UNIDAD
- A condiciones estándar: P = 1 atm T = 250C (2980K) [ión] = 1M
Por lo tanto si ocurre la cementación a condiciones estándar.
e) PRECIPITACIÓN CON GASES:
R.C:
R.A:
-------------------------------------------------------------------------------------------------------
R.T:
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 17
HIDROMETALURGIA: I UNIDAD
- En el equilibrio:
Pero:
Entonces:
Para una presión dada del H2(g) el equilibrio entre se puede
expresar en términos del pH para una actividad específica del ión metálico en
solución.
- Gráfica E vs pH:
-6 -5 -4 -3 -2 -1 0
-
0.2
0 Mz+ + ze = M
+
E, v z/2 H2(g) = zH + ze
- 0.2
-0.4
0 14
Es decir para precipitar al ión metálico en solución con gas hidrógeno depende del
pH de la solución en la cual se insufla el gas. Este tiene que ser mayor que el pH de
equilibrio para que se cumpla:
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 18
HIDROMETALURGIA: I UNIDAD
3. EXTRACCIÓN POR SOLVENTES:
Es la separación de uno o más solutos metálicos por transferencia de masa entre
dos fases inmiscibles, una de las cuales es una fase orgánica.
La extracción por solventes ofrece la posibilidad de concentrar soluciones con
bajo contenido de soluto y de separar selectivamente a este, incluso en
soluciones con elevado contenido de impurezas.
A. ETAPAS:
1º. Extracción.
2º. Separación o Re-extracción.
Alimentación Solución agotada
acuosa (refino)
EXTRACCION
Extractante Alimentación
cargado orgánica
SEPARACION
Solución Solución
cargada separadora
B. EQUIPO: “Mezclador – Sedimentador” para cada etapa de Extracción o
Separación:
Alimentación acuosa UNA ETAPA DE EXTRACCION
Alimentación orgánica
Recirculación orgánico
Extractante cargado
(a separación)
ORGANICO
ACUOSO
Solución agotada
TK-DE MEZCLADO TK-DE SEDIMENTACION
(reactor)
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 19
HIDROMETALURGIA: I UNIDAD
C. COMPONENTES DE LA FASE ORGÁNICA:
a) Disolvente: Compuesto inerte que disuelve al extractante. Ejemplo: kerosene,
nafteno, etc.
b) Extractante: Compuesto que contiene un grupo funcional que reacciona
químicamente con una especie (soluto) en la fase acuosa. La reacción es
reversible, lo cual constituye un aspecto importante de los sistemas de
extracción con solventes.
Ejemplo: Extracción de de soluciones de :
Como extractante se usa reactivos LIX (nombre comercial), disueltos en un
disolvente (LIX 63N, LIX 64N, LIX 65N, etc.)
LIX: LIQUID ION EXCHANGE EXTRACTANT.
(extractante líquido de intercambio iónico)
Los extractantes se pueden dividir en tres grupos diferentes:
1º. Extractantes Catiónicos: Los extractantes catiónicos en solución acuosa,
liberan protones de acuerdo a la siguiente reacción:
Donde RH es un ácido. El radical orgánico R forma un complejo con el metal
(quelato). La reacción inversa representa el proceso de separación.
Dos tipos diferentes de ácido son involucrados en este grupo de extractantes:
-
- Moléculas orgánicas menos ácidas que forman quelatos muy estables, tales
como las:
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 20
HIDROMETALURGIA: I UNIDAD
2º. Extractantes Aniónicos: Tenemos a las sales
obtenidas de aminas primarias, secundarias y
terciarias. Estos extractantes pueden intercambiar sus aniones con una
especie acuosa aniónica:
3º. Extractantes de Solvatación: Estas moléculas pueden extraer por
solvatación de especies inorgánicas eléctricamente neutras, de acuerdo a la
reacción:
.
Estas moléculas contienen un átomo de oxígeno, el cual proporciona el dipolo
electrónico necesario para el enlace covalente, tal como el:
El éster tributil fosfato diluído en hidroxicarburo es usado para la extracción de
hierro como desde soluciones lixiviadas con de matas de níquel.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 21
HIDROMETALURGIA: I UNIDAD
D. COEFICIENTE DE DISTRIBUCIÓN, D:
Algunas veces llamado como el coeficiente de partición. El coeficiente de
distribución, es la relación de la concentración del ion metálico en la fase
orgánica dividida por la concentración del ion metálico en la fase acuosa, en
equilibrio:
El coeficiente de distribución depende de la constante de equilibrio de la
reacción, la concentración del extractante en la fase orgánica, el pH de la
solución acuosa y la temperatura.
Asumiendo que no hay ninguna otra especie en el sistema, el coeficiente de
distribución podría ser:
E. ISOTERMA DE EXTRACCIÓN:
La isoterma de extracción es probablemente el método mas significante de
caracterizar el sistema de extracción por solventes. Básicamente la isoterma
de extracción es un ploteo de la concentración del elemento metálico en la fase
orgánica vs. La concentración de ese elemento en la fase acuosa; para una
temperatura dada, concentración del extractante en el solvente y el pH de la
fase acuosa.
La forma normal de la isoterma de extracción es caracterizada por una curva
que se eleva rápidamente (mientras más grande es la pendiente, más grande
es el coeficiente de distribución). El coeficiente de distribución es la pendiente
en cualquier punto de la curva, la cual alcanza una meseta en concentraciones
más altas en la fase acuosa, donde la capacidad del extractante ha sido
agotada. Este nivel de la meseta es referido como el punto de máxima carga
donde la relación ha sido esencialmente llevada a término.
Las desviaciones de la isoterma normal (tal como la isoterma tipo “S”), pueden
resultar del hecho que no ha sido permitido un tiempo suficiente para llegar al
equilibrio.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 22
HIDROMETALURGIA: I UNIDAD
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 23
También podría gustarte
- ACS Tema 12 El Problema de La Ruta Mas CortaDocumento5 páginasACS Tema 12 El Problema de La Ruta Mas CortaAldo LealAún no hay calificaciones
- Diseños de Plackett-BurmanDocumento12 páginasDiseños de Plackett-BurmanLuis DominguezAún no hay calificaciones
- Optimizacion de Procesos MetalurgicosDocumento21 páginasOptimizacion de Procesos MetalurgicosIgnacio Medel100% (2)
- LABORATORIO #7 Cinetica MoliendaDocumento12 páginasLABORATORIO #7 Cinetica MoliendaMerrik Omicron100% (1)
- CursoDocumento70 páginasCursotimmy manuel100% (3)
- Cinetica MoliendaDocumento28 páginasCinetica MoliendasebastianAún no hay calificaciones
- CadmioDocumento34 páginasCadmioDenisse Valencia BourjacAún no hay calificaciones
- T2 Ejercicios Del Libro Nuevo EnfoqueDocumento5 páginasT2 Ejercicios Del Libro Nuevo EnfoqueJoel MirandaAún no hay calificaciones
- FiltraciónDocumento34 páginasFiltraciónvinibenalAún no hay calificaciones
- Histograma-Cartas de ControlDocumento44 páginasHistograma-Cartas de ControlWil CarboneAún no hay calificaciones
- Ejercicio 7.1 Fabricacion de Cajas - Diseños Factoriales 3k - Auri ArriagaDocumento6 páginasEjercicio 7.1 Fabricacion de Cajas - Diseños Factoriales 3k - Auri ArriagaauriAún no hay calificaciones
- Indices de CapacidadDocumento18 páginasIndices de CapacidadJuliana Prieto Santiago ⃝⃤Aún no hay calificaciones
- Guía Balance de MasasDocumento3 páginasGuía Balance de Masasjuan topoAún no hay calificaciones
- Curriculum Valentin RiveraDocumento2 páginasCurriculum Valentin RiveraValentinRiveraDectorAún no hay calificaciones
- Protocolo Carga MáximaDocumento2 páginasProtocolo Carga MáximajorgeulloavAún no hay calificaciones
- Factores Que Afectan La FlotaciónDocumento33 páginasFactores Que Afectan La FlotaciónJesus Alberto Saldivar HuyhuaAún no hay calificaciones
- Apunte LaboratorioDocumento32 páginasApunte LaboratorioLuke AndersonAún no hay calificaciones
- A#4 SJMCHDocumento8 páginasA#4 SJMCHSergio Joel MirandaAún no hay calificaciones
- Laboratorio Aglomerado-Curado y Lix en ColumnasDocumento8 páginasLaboratorio Aglomerado-Curado y Lix en ColumnasNicolas Ignacio Olivares MaturanaAún no hay calificaciones
- Actividad 5 Manufactura EsbeltaDocumento6 páginasActividad 5 Manufactura EsbeltaGustavo AldereteAún no hay calificaciones
- Flotacion Selectiva de EnargitaDocumento17 páginasFlotacion Selectiva de EnargitaJose Demons Peña CarvajalAún no hay calificaciones
- Ejercicios Moly CopDocumento4 páginasEjercicios Moly CopMarcelo E. Cerda Araya100% (1)
- ProblemasDocumento15 páginasProblemasCarlos Ramon Vidal TovarAún no hay calificaciones
- Operación Evolutiva de ProcesosDocumento3 páginasOperación Evolutiva de ProcesosrenatoAún no hay calificaciones
- Gemba KaizenDocumento43 páginasGemba KaizenAlan PalmaAún no hay calificaciones
- Cinetica de FlotacionDocumento5 páginasCinetica de FlotacionFederico TitoAún no hay calificaciones
- Taller 160321Documento10 páginasTaller 160321Elenice Sosa LeónAún no hay calificaciones
- Simulación Del Proceso CHEMCADDocumento8 páginasSimulación Del Proceso CHEMCADAngel Mick-ellAún no hay calificaciones
- Solucion DualidadDocumento8 páginasSolucion Dualidadganimedes12001108Aún no hay calificaciones
- Work Index PDFDocumento88 páginasWork Index PDFOrlando HuaytaAún no hay calificaciones
- Diagramas de FlujoDocumento35 páginasDiagramas de FlujoJose Luis Palacios PoloAún no hay calificaciones
- Dimensionamiento de Molino de Bolas-1Documento14 páginasDimensionamiento de Molino de Bolas-1Amilcar Williams Gamarra ContrerasAún no hay calificaciones
- Tutorial Minitab MEIDocumento13 páginasTutorial Minitab MEIDaniela Forero RamírezAún no hay calificaciones
- SilicacionDocumento9 páginasSilicacionJose Aderlin Mejia CamposAún no hay calificaciones
- Antecedentes SMEDDocumento4 páginasAntecedentes SMEDViri RamírezAún no hay calificaciones
- Tarea 2 Procesos de ManufacturaDocumento2 páginasTarea 2 Procesos de ManufacturaAlejandra MoralesAún no hay calificaciones
- Evaluación 1 - Concentración y Procesamiento de Minerales - A - A - A-L-2Documento5 páginasEvaluación 1 - Concentración y Procesamiento de Minerales - A - A - A-L-2moisesAún no hay calificaciones
- Práctica 01 - Cartas de Control de VariablesDocumento12 páginasPráctica 01 - Cartas de Control de VariablesRickert Osbert Vasquez SanchezAún no hay calificaciones
- Ficha de Trabajo 09Documento10 páginasFicha de Trabajo 09Anibal Aldava CrispinAún no hay calificaciones
- Separación de Tamaños PDFDocumento17 páginasSeparación de Tamaños PDFPedro Aquino AquinoAún no hay calificaciones
- Como Instalar Minitab 16 en EspañolDocumento6 páginasComo Instalar Minitab 16 en EspañolVictoria Minaya FloresAún no hay calificaciones
- Resistencia Al Impacto de Un Acero Aisi Sae 1018 Llevado A Temperaturas Intercriticas CorrijiendoloDocumento33 páginasResistencia Al Impacto de Un Acero Aisi Sae 1018 Llevado A Temperaturas Intercriticas Corrijiendolojuan camilo lugo becerraAún no hay calificaciones
- Obtención Del CuSO4Documento11 páginasObtención Del CuSO4Nigia Flora Quecaña MirandaAún no hay calificaciones
- Evaluación y Aplicación de Balance de MateríaDocumento110 páginasEvaluación y Aplicación de Balance de MateríagianpierreAún no hay calificaciones
- Informe 8-EspesamientoDocumento7 páginasInforme 8-EspesamientoOrlandoAún no hay calificaciones
- Mapa Conceptual - PirometalurgiaDocumento1 páginaMapa Conceptual - PirometalurgiaKaren SierraAún no hay calificaciones
- Aglomerado-Curado y Lixiviación en ColumnasDocumento10 páginasAglomerado-Curado y Lixiviación en ColumnasNicola SephAún no hay calificaciones
- Variables de Operación de Un MolinoDocumento3 páginasVariables de Operación de Un MolinoAmanda TuckerAún no hay calificaciones
- Aplicacion Del Six-SigmaDocumento64 páginasAplicacion Del Six-SigmaAnthony Villar YallicoAún no hay calificaciones
- Histograma Del Problema 2.21Documento2 páginasHistograma Del Problema 2.21A23 LxAún no hay calificaciones
- Filtros VacioDocumento12 páginasFiltros VacioQete_argAún no hay calificaciones
- Apuntes Extracción Por Solventes SXDocumento57 páginasApuntes Extracción Por Solventes SXLuciana MaceraAún no hay calificaciones
- Clase 7-Extracción Por Solventes-Determinación EtapasDocumento25 páginasClase 7-Extracción Por Solventes-Determinación Etapaspiscoron8967% (3)
- Metalurgia y Materiales CerámicosDocumento2 páginasMetalurgia y Materiales CerámicosOrlandoAguilarZavalzaAún no hay calificaciones
- Test Sulfatación. PRUEBAS METALURGICASDocumento4 páginasTest Sulfatación. PRUEBAS METALURGICASPablo HurtubiaAún no hay calificaciones
- LixiviacionDocumento24 páginasLixiviacionAndres ContrerasAún no hay calificaciones
- Unidad I Hidrometalurgia AglomeraciónDocumento60 páginasUnidad I Hidrometalurgia AglomeraciónAlex RodríguezAún no hay calificaciones
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSADe EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSAAún no hay calificaciones
- Técnicas de Conformado Plástico para Complementar La Producción de Joyas Por Micro Fusión - GRUPO DDocumento20 páginasTécnicas de Conformado Plástico para Complementar La Producción de Joyas Por Micro Fusión - GRUPO DANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Proyecto de Inversión-PlantillaDocumento1 páginaProyecto de Inversión-PlantillaANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Bi FactorialDocumento18 páginasBi FactorialANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Expo Arthur ActualizadoDocumento13 páginasExpo Arthur ActualizadoANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Técnicas de Conformado Plástico para Complementar La Producción de Joyas Por Micro Fusión - GRUPO DDocumento20 páginasTécnicas de Conformado Plástico para Complementar La Producción de Joyas Por Micro Fusión - GRUPO DANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Bi FactorialDocumento18 páginasBi FactorialANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Proyecto de Inversión-PlantillaDocumento1 páginaProyecto de Inversión-PlantillaANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Proyecto de Inversión-PlantillaDocumento1 páginaProyecto de Inversión-PlantillaANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Analisis Del Marco Legal en El Perú - Mendoza Gutierrez Antoni KeyviDocumento2 páginasAnalisis Del Marco Legal en El Perú - Mendoza Gutierrez Antoni KeyviANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Seguridad y Salud Ocupacional Laboratorio #1 - MENDOZA GUTIERREZ ANTONI KEYVIDocumento4 páginasSeguridad y Salud Ocupacional Laboratorio #1 - MENDOZA GUTIERREZ ANTONI KEYVIANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Expo ResiduosDocumento26 páginasExpo ResiduosANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Laboratorio N 6Documento2 páginasLaboratorio N 6ANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- PetsDocumento3 páginasPetsANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Seguridad y Salud Ocupacional Laboratorio #1 - MENDOZA GUTIERREZ ANTONI KEYVIDocumento4 páginasSeguridad y Salud Ocupacional Laboratorio #1 - MENDOZA GUTIERREZ ANTONI KEYVIANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Joyeria en El PeruDocumento3 páginasJoyeria en El PeruANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- PetsDocumento3 páginasPetsANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Laboratorio N 6Documento2 páginasLaboratorio N 6ANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Fundicion y MoldeoDocumento15 páginasFundicion y MoldeoANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- 14 Tarea - Optimizacionaguirre, Echeverria, LlaveDocumento15 páginas14 Tarea - Optimizacionaguirre, Echeverria, LlaveANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Analisis Del Marco Legal en El Perú - Mendoza Gutierrez Antoni KeyviDocumento2 páginasAnalisis Del Marco Legal en El Perú - Mendoza Gutierrez Antoni KeyviANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Extracto de Balsamo de LimonDocumento29 páginasExtracto de Balsamo de LimonANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- 11 TAREA - Aguirre, Echeverría, Llave, PUNTOS CENTRALES en EL Diseño Factorial 2 Ala 3Documento14 páginas11 TAREA - Aguirre, Echeverría, Llave, PUNTOS CENTRALES en EL Diseño Factorial 2 Ala 3ANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Investigacion FocoDocumento10 páginasInvestigacion FocoMichael G. QuispeAún no hay calificaciones
- 12 TAREA - Aguirre, Echeverria, LLave - MSRDocumento16 páginas12 TAREA - Aguirre, Echeverria, LLave - MSRANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- 12 TAREA - Aguirre, Echeverria, LLave - MSRDocumento16 páginas12 TAREA - Aguirre, Echeverria, LLave - MSRANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- 13 Tarea - Superficie de Respuesta de Segundo OrdenDocumento10 páginas13 Tarea - Superficie de Respuesta de Segundo OrdenANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- 11 TAREA - Aguirre, Echeverría, Llave, PUNTOS CENTRALES en EL Diseño Factorial 2 Ala 3Documento14 páginas11 TAREA - Aguirre, Echeverría, Llave, PUNTOS CENTRALES en EL Diseño Factorial 2 Ala 3ANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- 13 Tarea - Superficie de Respuesta de Segundo OrdenDocumento10 páginas13 Tarea - Superficie de Respuesta de Segundo OrdenANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- 14 Tarea - Optimizacionaguirre, Echeverria, LlaveDocumento15 páginas14 Tarea - Optimizacionaguirre, Echeverria, LlaveANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Clase 11 - Metalurgia Fisica II - Modulo IIDocumento7 páginasClase 11 - Metalurgia Fisica II - Modulo IIANTONI KEYVI MENDOZA GUTIERREZAún no hay calificaciones
- Examen Del Curso de Introduccion A La MetalurgiaDocumento3 páginasExamen Del Curso de Introduccion A La Metalurgiafredc201180Aún no hay calificaciones
- Zinc PresentacionDocumento12 páginasZinc PresentacionVelazquez Garcia Eduardo AntonioAún no hay calificaciones
- Ciencias De.. ProblemasDocumento3 páginasCiencias De.. Problemasluis sandovalAún no hay calificaciones
- LABORATORIO N1 ERGONOMIA TERMINADO OkDocumento7 páginasLABORATORIO N1 ERGONOMIA TERMINADO OkFranz Castro TorresAún no hay calificaciones
- Exposicion Instrumentos de MedicionDocumento13 páginasExposicion Instrumentos de MedicionFco Gabriel LAAún no hay calificaciones
- Analisis de Las Caracteristicas de Los Electrodos Utilizados en El Campo Automotriz en Difrerntes AplicacionesDocumento1 páginaAnalisis de Las Caracteristicas de Los Electrodos Utilizados en El Campo Automotriz en Difrerntes AplicacionesDarwin TapuyoAún no hay calificaciones
- Naranja 2Documento11 páginasNaranja 2Brayan RoldanAún no hay calificaciones
- 00 Prov Adm SNAT-2015-0049Documento7 páginas00 Prov Adm SNAT-2015-0049varios.1Aún no hay calificaciones
- Proceso Productivos Del CobreDocumento28 páginasProceso Productivos Del CobreYerka ColqueAún no hay calificaciones
- Enlace Quimico para Tercer Grado de SecundariaDocumento11 páginasEnlace Quimico para Tercer Grado de SecundariazenaidacamposAún no hay calificaciones
- Tema Nº2 - CobreDocumento13 páginasTema Nº2 - CobreandresfquirogaAún no hay calificaciones
- EL HIDROGENO InorganicaDocumento15 páginasEL HIDROGENO InorganicaMary Kely Chambi ChoqueAún no hay calificaciones
- Metales Restauracion HierroDocumento33 páginasMetales Restauracion HierroCarmen BermudezAún no hay calificaciones
- REVISTA - FIC FRIO - TEMA - DISYUNTORES-VÁLVULA DE EXPANSIÓN-BRASEADO - TECUMSEH - No 95 - 2016 - 03Documento16 páginasREVISTA - FIC FRIO - TEMA - DISYUNTORES-VÁLVULA DE EXPANSIÓN-BRASEADO - TECUMSEH - No 95 - 2016 - 03Hugo MAún no hay calificaciones
- Informe de Laboratorio de SoldaduraDocumento13 páginasInforme de Laboratorio de Soldaduraktcuellar_25Aún no hay calificaciones
- Ceramicos, Polimeros y MetalesDocumento36 páginasCeramicos, Polimeros y MetalesJuan Pacheco84% (45)
- Puros y AleacionesDocumento22 páginasPuros y AleacionesFernanda AcostaAún no hay calificaciones
- Ivoclar - IPS InLine Manual EspanholDocumento84 páginasIvoclar - IPS InLine Manual EspanholJhoonpmAún no hay calificaciones
- IP054-Caso Práctico Fitorremediación XXXDocumento6 páginasIP054-Caso Práctico Fitorremediación XXXLuis Lopez100% (4)
- 131 Diana Elisa Ontiveros de La TorreDocumento189 páginas131 Diana Elisa Ontiveros de La TorreChee Hong LeeAún no hay calificaciones
- Técnicas de Recuperación y Tratamiento de SuelosDocumento12 páginasTécnicas de Recuperación y Tratamiento de SuelosYOHAN SANTIAGO ORTIZ AMADOAún no hay calificaciones
- Compueestos Part IDocumento44 páginasCompueestos Part IJavier JimenezAún no hay calificaciones
- ¿Por Qué Los Metales Son Buenos Conductores de Electricidad?Documento4 páginas¿Por Qué Los Metales Son Buenos Conductores de Electricidad?Marcelo GamboaAún no hay calificaciones
- PolímerosDocumento10 páginasPolímerosYusei D.Aún no hay calificaciones
- Proyecto de Tesis PDFDocumento14 páginasProyecto de Tesis PDFMarcy Espino AlvaAún no hay calificaciones
- Garret Ace 150 250 Manual SpanishDocumento50 páginasGarret Ace 150 250 Manual Spanishp_romero_c0% (1)
- Apunte Quimica General 2022Documento42 páginasApunte Quimica General 2022Luciano Matias Garrido SosaAún no hay calificaciones
- Informe Practica 1 FundicionDocumento6 páginasInforme Practica 1 FundicionMely's Dbk GuevaraAún no hay calificaciones
- Ferroaleciones PDFDocumento24 páginasFerroaleciones PDFDaniel MuñozAún no hay calificaciones
- 2 Presentacion 1 LaminacionDocumento31 páginas2 Presentacion 1 LaminacionJimena TejerinaAún no hay calificaciones