Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Conclusion Lab CQRH P4
Conclusion Lab CQRH P4
Cargado por
Martin Perez0 calificaciones0% encontró este documento útil (0 votos)
10 vistas2 páginasEl autor concluye que los objetivos de la práctica se cumplieron al obtener datos del volumen de tiosulfato de sodio en diferentes tiempos. La concentración de HCrO4- depende del tiempo y es inversamente proporcional a este. El método diferencial se usó para encontrar el orden de reacción cercano a 1 y la constante de velocidad k para ambos sistemas. El sistema 1 tiene una velocidad de reacción menor que el sistema 2 debido a su mayor descenso en la concentración a los 12 minutos.
Descripción original:
CONCLUSION CINETICA
Título original
CONCLUSION-LAB-CQRH-P4
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEl autor concluye que los objetivos de la práctica se cumplieron al obtener datos del volumen de tiosulfato de sodio en diferentes tiempos. La concentración de HCrO4- depende del tiempo y es inversamente proporcional a este. El método diferencial se usó para encontrar el orden de reacción cercano a 1 y la constante de velocidad k para ambos sistemas. El sistema 1 tiene una velocidad de reacción menor que el sistema 2 debido a su mayor descenso en la concentración a los 12 minutos.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
10 vistas2 páginasConclusion Lab CQRH P4
Conclusion Lab CQRH P4
Cargado por
Martin PerezEl autor concluye que los objetivos de la práctica se cumplieron al obtener datos del volumen de tiosulfato de sodio en diferentes tiempos. La concentración de HCrO4- depende del tiempo y es inversamente proporcional a este. El método diferencial se usó para encontrar el orden de reacción cercano a 1 y la constante de velocidad k para ambos sistemas. El sistema 1 tiene una velocidad de reacción menor que el sistema 2 debido a su mayor descenso en la concentración a los 12 minutos.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
CONCLUSIÓN (FLORES SALAS ALDO)
Habiendo finalizado la práctica puedo concluir que los objetivos de la práctica se
cumplieron en su totalidad ya que mediante la experimentación se obtuvieron
datos del volumen de tiosulfato de sodio con lo cual se muestran las habilidades
para la toma de muestras, teniendo las muestras de tiosulfato a los diferentes
tiempos se aplicó el tratamiento de datos para ambos sistemas para pasar los
datos de volumen a concentración con lo cual se observa que la concentración
tiene relación con el tiempo ya que al aumentar el tiempo la concentración de
HCr O−¿¿
4 disminuye por lo cual se concluye que la concentración depende del
tiempo y es inversamente proporcional al mismo, esto se tiene para ambos
sistemas, sin embargo en el sistema 1 se observa que al tiempo de 12 minutos se
tiene un descenso considerable en el volumen gastado de tiosulfato y por ende en
la concentración, para el sistema 2 la concentración tiene una tendencia a
descender de una manera uniforme.
−¿¿
Al tener los datos de concentración de HCr O4 se aplicó el método diferencial
para obtener el orden de reacción y la constante de velocidad por lo que se
concluye que se cumple con el segundo objetivo planteado y a su vez con el
quinto objetivo ya que se determinó usar el método diferencial para encontrar el
orden de reacción y la constante de velocidad, el encontrar las variables ya
mencionadas se concluye que este método funciona adecuadamente pues en
ambos sistemas se obtuvieron valores de orden de reacción cercanos a la unidad
si se redondearan los valores siendo mayor el orden de reacción del sistema 1 ya
que se obtuvo un valor de 1.1515 y para el sistema 2 se obtuvo un valor de
0.9232, para el caso de la constante de velocidad el sistema 1 tiene un valor de k
mayor al del sistema 2 pues en el sistema 1 se tiene una k de 0.1085 y para el
sistema 2 se tiene una k de 0.0702.
Considerando lo anterior se obtienen las ecuaciones de la velocidad de reacción
para ambos sistemas y se concluye que el sistema 2 tiene una velocidad de
reacción mayor al sistema 1 en un mismo tiempo lo cual también se puede
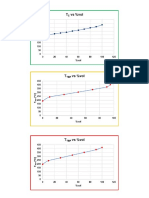
comprobar gráficamente pues en el sistema 1 el descenso de la concentración a
los 12 minutos afecta de forma considerable a la velocidad de reacción es por esto
que en este sistema la velocidad de reacción es menor, en el caso del sistema 2
se tiene una velocidad de reacción mayor ya que la tendencia de la concentración
a disminuir al paso del tiempo es más uniforme.
También podría gustarte
- Caso Clinico #2 CRIMINALISTICADocumento2 páginasCaso Clinico #2 CRIMINALISTICAFredy Gampierr67% (3)
- Oportunidades y Estrategias FiscalesDocumento2 páginasOportunidades y Estrategias FiscalesEstefany OrduzAún no hay calificaciones
- Conclusion Lab CQRH P2Documento2 páginasConclusion Lab CQRH P2Martin PerezAún no hay calificaciones
- Conclusion Lab CQRH P3Documento2 páginasConclusion Lab CQRH P3Martin PerezAún no hay calificaciones
- INF 1 ObrequeDocumento3 páginasINF 1 ObrequeDiego Obreque MoralesAún no hay calificaciones
- Cuestionario EqDocumento2 páginasCuestionario EqJimena CarolinaAún no hay calificaciones
- CAPITULO III-Datos ExperimentalesDocumento34 páginasCAPITULO III-Datos ExperimentalesLaura DsbAún no hay calificaciones
- Metodo Cohen y CoonDocumento1 páginaMetodo Cohen y CoonArte VidriosAún no hay calificaciones
- MANUAL CINETICA Y REACTORES 2015 Prof PDFDocumento86 páginasMANUAL CINETICA Y REACTORES 2015 Prof PDFCeleste PerrinsonAún no hay calificaciones
- Reporte Capacidad CalorificaDocumento12 páginasReporte Capacidad CalorificaNicole CarpioAún no hay calificaciones
- Laboratorio 1° de Química InorgánicaDocumento10 páginasLaboratorio 1° de Química InorgánicaAdrian Joseph Luzuriaga ChumbesAún no hay calificaciones
- Metodos CinéticosDocumento7 páginasMetodos CinéticosBeto0893Aún no hay calificaciones
- Laboratorio Nº6 - Un Experimento Simple de Cinética QuímicaDocumento11 páginasLaboratorio Nº6 - Un Experimento Simple de Cinética QuímicaRavenbachAún no hay calificaciones
- Cuestionario 2 de FisicoquimicaDocumento3 páginasCuestionario 2 de FisicoquimicaVelasquez Quispe Jherson HenryAún no hay calificaciones
- Determinación de La Razón CP y CVDocumento9 páginasDeterminación de La Razón CP y CVOscar PortilloAún no hay calificaciones
- Practica 7 CineticaDocumento6 páginasPractica 7 CineticaPoncho Malagón100% (1)
- Informe de ArticuloDocumento3 páginasInforme de ArticuloKATHERINNE LUZ CHUCO DE LA CRUZAún no hay calificaciones
- Metodos CinéticosDocumento7 páginasMetodos CinéticosBeto0893Aún no hay calificaciones
- Reporte 2 Metodo Diferencial e IntegralDocumento8 páginasReporte 2 Metodo Diferencial e IntegralIsrael Hernández MoralesAún no hay calificaciones
- P2 LIQ 4 Facultad de QuímicaDocumento9 páginasP2 LIQ 4 Facultad de QuímicaMau VelázquezAún no hay calificaciones
- Conservación de La MateriaDocumento11 páginasConservación de La MateriaGraciela CallejasAún no hay calificaciones
- Previo 2 LUFDocumento5 páginasPrevio 2 LUFMau VelázquezAún no hay calificaciones
- Cine TicaDocumento10 páginasCine TicaSeulement GomezAún no hay calificaciones
- Informe Química IIDocumento5 páginasInforme Química IIbenjaminAún no hay calificaciones
- Prácticas #2 - FisicoquímicaDocumento5 páginasPrácticas #2 - FisicoquímicamperezpirelaAún no hay calificaciones
- PRODUCCIÓN DE CO2 A PARTIR DE LA REACCIÓN DE HCL Y NaHCO3Documento15 páginasPRODUCCIÓN DE CO2 A PARTIR DE LA REACCIÓN DE HCL Y NaHCO3Juan Luis Jaime Rodriguez100% (1)
- El Reloj de Yodo.Documento11 páginasEl Reloj de Yodo.Andrés RoblesAún no hay calificaciones
- Reporte MicroMezcladoDocumento7 páginasReporte MicroMezcladoDavid Tapia MtzAún no hay calificaciones
- 18 - Cinética IDocumento15 páginas18 - Cinética IBelén InfantinoAún no hay calificaciones
- Métodos de Determinación de Constantes de Velocidad de ReacciónDocumento6 páginasMétodos de Determinación de Constantes de Velocidad de ReacciónBento PlayerAún no hay calificaciones
- Informe de Cromatografia de GasesDocumento27 páginasInforme de Cromatografia de Gasesjavier calleAún no hay calificaciones
- Informe Primera PracticaDocumento10 páginasInforme Primera PracticaSebastian Felipe ArguelloAún no hay calificaciones
- Conducción de Calor en Estado No EstacionarioDocumento49 páginasConducción de Calor en Estado No Estacionariojhosimar9755% (11)
- Conclusion Lab CQRH P1Documento2 páginasConclusion Lab CQRH P1Martin PerezAún no hay calificaciones
- Practica 10Documento8 páginasPractica 10Tania MorenoAún no hay calificaciones
- Guia - Cinetica UnefmDocumento19 páginasGuia - Cinetica UnefmMaría FaríaAún no hay calificaciones
- Cinetica Quimica 2Documento3 páginasCinetica Quimica 2Bladimir CollantesAún no hay calificaciones
- Experiencia N°6 - Destilación Continua.: Transferencia de Materia - IWQ224Documento3 páginasExperiencia N°6 - Destilación Continua.: Transferencia de Materia - IWQ224Carla AguilarAún no hay calificaciones
- Practica 1Documento9 páginasPractica 1PriscilaAún no hay calificaciones
- Informe 2 Densidad Absoluta de Gases PDFDocumento10 páginasInforme 2 Densidad Absoluta de Gases PDFEctor Adrian Rivadeneyra CardenasAún no hay calificaciones
- Info. BalanceDocumento18 páginasInfo. BalanceojccucastilloAún no hay calificaciones
- Informe FISICOQUIMICA N°2Documento3 páginasInforme FISICOQUIMICA N°2Carolina Alejandra Cardenas JametAún no hay calificaciones
- Informe Relacion Calores EspecificosDocumento10 páginasInforme Relacion Calores EspecificosGermánEdo.OlmosAún no hay calificaciones
- Procesos CuasiestaticosDocumento17 páginasProcesos CuasiestaticosYairContrerasAún no hay calificaciones
- Practica I Simulacion Hidráulica de Cinetica de Reacciones.Documento26 páginasPractica I Simulacion Hidráulica de Cinetica de Reacciones.Eliana ArenasAún no hay calificaciones
- CCQ G1 E1 PrácticaDocumento10 páginasCCQ G1 E1 PrácticaCamilo PerezAún no hay calificaciones
- Catalisis Del H2o2Documento21 páginasCatalisis Del H2o2JulioRaAún no hay calificaciones
- Lab6. - Cinética de Oxidación Del EtanolDocumento8 páginasLab6. - Cinética de Oxidación Del EtanolRoberto Eduardo Quispe MamaniAún no hay calificaciones
- Informe Laboratorio 8Documento8 páginasInforme Laboratorio 8Carlos Zamata Quispe100% (1)
- Determinacion Del Orden de Reaccion QuimicoDocumento13 páginasDeterminacion Del Orden de Reaccion QuimicoMauro Espinosa100% (1)
- Documento 2Documento3 páginasDocumento 2David Alejandro Serrano RodríguezAún no hay calificaciones
- Termodinámica - Laboratorio 2Documento4 páginasTermodinámica - Laboratorio 2Andres Camilo Samaniego VargasAún no hay calificaciones
- Apuntes ExposicionDocumento3 páginasApuntes ExposicionYadir RamírezAún no hay calificaciones
- Act. # 4 Simulador YenkaDocumento17 páginasAct. # 4 Simulador YenkaCristian GaitanAún no hay calificaciones
- CINETICADocumento21 páginasCINETICAANAAún no hay calificaciones
- Cinética Reporte 4Documento23 páginasCinética Reporte 4Paz Cuéllar0% (1)
- Descomposicion Catalitica FinalDocumento20 páginasDescomposicion Catalitica FinalKevin Romero ZeladaAún no hay calificaciones
- Caso de Estudio 1Documento16 páginasCaso de Estudio 1Laura Camila SuarezAún no hay calificaciones
- Saponificación AlcalinaDocumento4 páginasSaponificación AlcalinaYennifer Giselle MartinezAún no hay calificaciones
- Masa Molar de GasesDocumento8 páginasMasa Molar de GasesAlvaro Marcelo Gonzales Rodriguez100% (1)
- UF1026 - Caracterización de procesos e instalaciones frigoríficasDe EverandUF1026 - Caracterización de procesos e instalaciones frigoríficasCalificación: 4 de 5 estrellas4/5 (1)
- Equilibrios de Fases y Transiciones de Fases: Parte IDe EverandEquilibrios de Fases y Transiciones de Fases: Parte IAún no hay calificaciones
- Examen 1CDocumento2 páginasExamen 1CMartin PerezAún no hay calificaciones
- Practica 3 CQRHDocumento15 páginasPractica 3 CQRHMartin PerezAún no hay calificaciones
- GRAFICASDocumento2 páginasGRAFICASMartin PerezAún no hay calificaciones
- Formulario CPPDocumento15 páginasFormulario CPPMartin PerezAún no hay calificaciones
- Eda Ets Ord A-B Cadena (18 6 2019) RespuestaDocumento12 páginasEda Ets Ord A-B Cadena (18 6 2019) RespuestaMartin PerezAún no hay calificaciones
- Segunda Serie de ProblemasDocumento1 páginaSegunda Serie de ProblemasMartin PerezAún no hay calificaciones
- Linea de Tiempo 21Documento1 páginaLinea de Tiempo 21Ingrid K-RolayAún no hay calificaciones
- Dialnet MotivacionYAnsiedadEnJugadoresDeTenis 2278452Documento20 páginasDialnet MotivacionYAnsiedadEnJugadoresDeTenis 2278452Esteban30Aún no hay calificaciones
- Estructura Interna Del Texto Argumentativo: TesisDocumento2 páginasEstructura Interna Del Texto Argumentativo: TesisElber GalargaAún no hay calificaciones
- Clase #4 - Sociologia - UNFV - 2019Documento44 páginasClase #4 - Sociologia - UNFV - 2019Angely20202020Aún no hay calificaciones
- Análisis de La Calidad de Señal en Una Red Wifi Con La Herramienta NetstumblerDocumento12 páginasAnálisis de La Calidad de Señal en Una Red Wifi Con La Herramienta NetstumblerRoxana Janneth MoralesAún no hay calificaciones
- Guide To The Software Engineering Body of Knowledge - 2004 Version Swebok (2004) .En - EsDocumento202 páginasGuide To The Software Engineering Body of Knowledge - 2004 Version Swebok (2004) .En - EsulisesAún no hay calificaciones
- 7 Beneficios de Implementar Un SGSSTDocumento3 páginas7 Beneficios de Implementar Un SGSSTClaudia Victoria Alvarado GonzalezAún no hay calificaciones
- Sesión Primer Grado AdvientoDocumento3 páginasSesión Primer Grado AdvientoJosé Gonzales100% (6)
- TEMA 5 Corrosion y AplicacionesDocumento4 páginasTEMA 5 Corrosion y AplicacionesJesica Cabrera Rocha50% (2)
- Realizar Un Curso en La Plataforma EOMC - v3Documento10 páginasRealizar Un Curso en La Plataforma EOMC - v3David Polonio lucasAún no hay calificaciones
- Palabras PolisémicasDocumento2 páginasPalabras PolisémicasWillian Rocha SevillanoAún no hay calificaciones
- EvidencianRedimensionar 26612d47303e38bDocumento10 páginasEvidencianRedimensionar 26612d47303e38bTalía CharryAún no hay calificaciones
- Los Olivos - VEGA ALVA KIKE LEONCIO CODIGO 41816Documento2 páginasLos Olivos - VEGA ALVA KIKE LEONCIO CODIGO 41816Jesus Ynocencio AmbichoAún no hay calificaciones
- Subjetividad y Medios de ComunicaciónDocumento5 páginasSubjetividad y Medios de ComunicaciónsilvinaAún no hay calificaciones
- m2 Apunte MicrocontroladorDocumento26 páginasm2 Apunte MicrocontroladoroceanmpgAún no hay calificaciones
- Balance General IiDocumento11 páginasBalance General IiMaria ArellanoAún no hay calificaciones
- Presupuesto ApuDocumento41 páginasPresupuesto Apuluis chaconAún no hay calificaciones
- Informe - Ap6 - Corredor Alegrias - 2016Documento203 páginasInforme - Ap6 - Corredor Alegrias - 2016Juan C. RojasAún no hay calificaciones
- Tutorial DSCHDocumento1 páginaTutorial DSCHAlexis ValverdeAún no hay calificaciones
- Conceptos y Fundamentos de Costos IndustrialesDocumento47 páginasConceptos y Fundamentos de Costos Industrialespreppie83100% (2)
- LamidrenDocumento2 páginasLamidrenEdgarRodriguezQAún no hay calificaciones
- Resumen Automatización de Tareas Procedimientos AlmacenadosDocumento20 páginasResumen Automatización de Tareas Procedimientos Almacenadosgina vanessa valencia alomiaAún no hay calificaciones
- Protocolo CartagenaDocumento2 páginasProtocolo CartagenaAlexis Ch CamanAún no hay calificaciones
- Sistemas Montañosos y LagunasDocumento5 páginasSistemas Montañosos y LagunasEnmanuel SantanaAún no hay calificaciones
- Prueba de Matematica 2Documento6 páginasPrueba de Matematica 2Manuel Navarrete TejosAún no hay calificaciones
- P9 - Electricidad y MagnetismoDocumento7 páginasP9 - Electricidad y MagnetismoGonzález Santillán Mayra MonserratAún no hay calificaciones
- Diapositiva Luis VidalDocumento9 páginasDiapositiva Luis VidalEvangelina Vidal RamirezAún no hay calificaciones
- Mapa MentalDocumento1 páginaMapa Mentalcarolina chicoAún no hay calificaciones