Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Aneurisma Cerebral - Glioblastoma
Cargado por
Nataly QHTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Aneurisma Cerebral - Glioblastoma
Cargado por
Nataly QHCopyright:
Formatos disponibles
ANEURISMA CEREBRAL
Los aneurismas cerebrales son protuberancias de paredes delgadas en las arterias intracraneales que
pueden romperse y causar una hemorragia subaracnoidea (HSA), a menudo un evento devastador con
una alta mortalidad y morbilidad. Los aneurismas cerebrales no rotos también pueden manifestarse
clínicamente por su efecto de masa en las estructuras neurológicas adyacentes, o pueden descubrirse
incidentalmente cuando un paciente tiene un estudio de neuroimagen para otra indicación. Los
aneurismas no rotos tienen un riesgo futuro de ruptura y SAH que varía en parte según el tamaño y la
ubicación. La reparación endovascular o quirúrgica es el único tratamiento eficaz para la SAH
aneurismática para prevenir nuevas hemorragias y morbilidad adicional y también se usa para algunos
pacientes con aneurismas cerebrales intactos para prevenir la SAH.
FACTORES DE RIESGO PARA LA FORMACIÓN DE ANEURISMAS
Síndromes hereditarios El mecanismo por el cual las enfermedades del tejido conjuntivo predisponen a
la formación de aneurismas implica presumiblemente una debilidad inherente de la pared arterial
expuesta al patrón de flujo no laminar de la sangre, que luego se expone a esfuerzos cortantes.
-La formación de aneurismas en la hiperaldosteronismo remediable con glucocorticoides puede deberse
en parte a la hipertensión congénita durante las primeras etapas del desarrollo cerebrovascular.
-La hipertensión concurrente también puede contribuir a la poliquistosis renal (PKD)
Aneurismas familiares : los familiares de pacientes con aneurismas intracraneales tienen un mayor
riesgo de tener un aneurisma, incluso en ausencia de un síndrome hereditario conocido
Los aneurismas familiares tienden a romperse con un tamaño más pequeño y una edad más temprana
que los aneurismas esporádicos
Otros factores: debido a que los aneurismas intracraneales son la etiología principal de la SAH, los
factores de riesgo de SAH también pueden ser factores de riesgo de aneurismas intracraneales. Los
factores de riesgo para la SAH incluyen hipertensión, tabaquismo y consumo de alcohol
El hipercolesterolemia y el ejercicio físico regular parecen disminuir el riesgo de formación de aneurismas
Fumar cigarrillos: Aquellos que fumaban y tenían hipertensión tenían un aumento de casi 15 veces en el
riesgo de HSA en comparación con los no fumadores normotenso. El mecanismo por el cual fumar
cigarrillos predispone a la formación de aneurismas puede implicar la disminución de la eficacia de la alfa-
1 antitripsina, un importante inhibidor de proteasas como la elastasa
Hipertensión: la asociación entre la hipertensión y la formación y ruptura de aneurismas ha sido
controvertida, aunque el balance de la evidencia sugiere que la hipertensión es un factor de riesgo, La
presión arterial superior a 160/95.
Deficiencia de estrógeno: hay una preponderancia femenina para los aneurismas, esta pérdida de
colágeno puede contribuir al desarrollo de aneurismas en mujeres posmenopáusicas, de manera análoga
a la situación en pacientes con enfermedades del tejido conectivo.
Las mujeres premenopáusicas sin antecedentes de tabaquismo o hipertensión tenían un riesgo reducido
de hemorragia subaracnoidea en comparación con las
mujeres posmenopáusicas de la misma edad, El uso de la
terapia de reemplazo de estrógenos se asoció con un
riesgo reducido de hemorragia subaracnoidea mujeres
posmenopáusicas.
Coartación de la aorta: Es un defecto de nacimiento en
el cual una parte de la aorta es más estrecha que lo usual,
causa desconocida (resultado de anomalías en el
desarrollo) los pacientes con coartación de la aorta tienen
un mayor riesgo de formación de aneurismas. Esto puede
deberse a hipertensión secundaria los factores de riesgo
morfológicos o genéticos compartidos
FACTORES DE RIESGO
Los más importantes son HTA, tabaquismo y
alcoholismo. También, un mayor riesgo de las mujeres
postmenopáusicas. Y persona con dos familiares de
primer grado con HSA tienen un riesgo mayor.
DX
Cefalea súbita intensa
- Trastorno de conciencia
- Vómitos
- Oftalmoparesia
- Meningismo
- Convulsiones
<- Focalización
Según su patología y etiología se dividen en 4 tipos:
1.- Sacular (90% de AC) - Puntos ramificantes de las arterias grande, parte anterior del polígono de Willis- 25mm a
más son aneurismas gigantes.
2.- Fusiformes ( 7% de AC )- En las salientes de la pared arterial de la parte proximal de las arterias- Más común en
la circulación vertebrovasilar.
3.- Infecciosos o micóticos (0.5% de AC)- Son asociado a la endocarditis y de etiología embolica, muy raras- Localizan
en ramas distales de las arterial cerebrales medias.
4.- Traumáticos - Por fracturas desplazadas de cráneo o lesión traumática cerrada de la bóveda craneal, -
Localizadas en la parte distal de las arterial corticales
GLIOBLASTOMA
El glioblastoma (GB) es el tumor maligno primario del sistema nervioso central (SNC) más común en
adultos (supone más del 50%) y se asocia invariablemente a un mal pronóstico. Solo el 33% de los
pacientes sobrevive al año y el 5% de los pacientes llegan a vivir más de 5 años tras el diagnóstico) .La
Organización Mundial de la Salud (OMS) clasifica los gliomas fundamentalmente por criterios
histopatológicos en: astrocitomas, oligodendrogliomas, oligoastrocitomas y ependimomas. Además,
establece una gradación relacionada con el pronóstico de la enfermedad que identifica a los de alto grado
como astrocitomas de grado III (astrocitoma anaplásico) y grado IV (GB)
Los GB pueden comprometer cualquier estructura neuroanatómica, pero en adultos es más común en los
hemisferios cerebrales, mientras que en los niños lo es en la fosa posterior. Su crecimiento infiltrativo es
extremadamente rápido. Histológicamente está compuesto de células de gran variabilidad morfológica,
algunas bizarras, pleomórficas y multinucleadas; con actividad mitótica elevada; proliferación
microvascular; severa y característica hiperplasia endotelial; microtrombos intravasculares, y necrosis
extensas de carácter isquémico o en forma de pseudoempalizadas. La denominación multiforme se debe
a la gran heterogeneidad que lo caracteriza con variados patrones y rasgos citológicos. En general,
muestran focos bien diferenciados que alternan con otros pobremente diferenciados. Tradicionalmente se
han clasificado en dos subtipos morfológicamente idénticos: primarios (GB1) y secundarios (GB2).
Los GB1 representan la mayoría, aparecen sin que existan lesiones precedentes y es más frecuente en
edad avanzada (edad media de 60 años). La evolución es breve debido al rápido crecimiento tumoral. Los
GB2 representan menos del 10% de los GB, surgen como progresión de astrocitomas de bajo grado
(astrocitoma difuso o astrocitoma anaplásico) y afectan a pacientes jóvenes. Su evolución es más lenta, y
la sobrevida media es significativamente superior debido a la menor edad del debut y al crecimiento
tumoral más lento Ambas entidades constituyen enfermedades distintas que evolucionan a través de vías
moleculares diferentes.
La OMS incluye al GB de células gigantes y al gliosarcoma dentro de la denominación GB (ICD-0 9440/3),
como variedades con algunos rasgos característicos. Adicionalmente, se han descrito entidades con
características propias que se encuentran en actual revisión por la OMS. El GB de células pequeñas se
caracteriza por un predominio citológico de elementos pequeños con alto cociente núcleo/ citoplasma y
elevado índice de proliferación celular, corresponde al 10% del total de GB, que se asocia con un peor
pronóstico. El GB con componente tipo tumor neuroectodérmico primitivo (PNET) es una entidad
infrecuente, más común en niños y adultos jóvenes, probablemente se asocia con un pronóstico
favorable, y se caracteriza por expresión proteica CD56- positivo y vimentina- negativo. El GB con
componente oligodendroglial es también una entidad infrecuente con un pronóstico aún desconocido.
Adicionalmente, el perfil genómico integrado del GB desarrollado con los estudios de la red de
investigación de The Cáncer Genoma Atlas (TCGA) ha revelado varios subtipos moleculares, Estos
subtipos se definen por sus alteraciones más importantes en la expresión génica, y se asocian con
mutaciones específicas y alteraciones del número de copias. Se reconocen los siguientes subtipos de GB:
tipo clásico, tipo mesenquimal, tipo proneural y tipo neural.
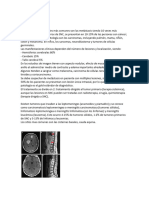
(A) Biopsia estereotaxica (HE,
100x). Glioblastoma de
células pequeñas,
compuesto por células de
núcleos ovalados y aspecto
monótono (cabeza de
flecha) con áreas de
necrosis tipo
pseudopalizada (flecha).
(B) biopsia quirúrgica (HE,
40x). Glioblastoma con
componente de tumor
neuroectodérmico primitivo.
Presencia de proliferación
de células redondas y
aspecto primitivo (cabeza
de flecha), desplazan en un
patrón nodular el
componente gliar (flecha).
(C) Presencia de patrón
rosetoide en el
componente de tumor
neuroectodérmico primitivo (cabeza de flecha) y células pleomórficas (flecha)
(D) Inmunohistoquímica para sinaptofisina. Tinción heterogénea de color café (cabeza de flecha).
El pobre pronóstico asociado con esta neoplasia la convierte en un problema de salud pública. El conocimiento de las
bases biológicas y moleculares de la enfermedad es crucial para la mejor comprensión de esta entidad, manejo diario
de los pacientes y para el desarrollo de estrategias de tratamiento más eficaces. Existe escasa información sobre esta
enfermedad y su manejo en población latina.
EPIDEMIOLOGÍA
Estudios epidemiológicos encuentran diferencias en la incidencia de GB según la etnia/raza de la población y diversos
estudios sugieren que la incidencia es menor en población latina que en población caucásica. Estas diferencias pueden
deberse a desigualdades en la frecuencia de alelos de susceptibilidad a desarrollar GB descritos para diferentes
etnias/razas.
FACTORES DE RIESGO
La carcinogénesis representa un proceso de múltiples pasos complejos y se asocia con factores
biológicos, físicos, químicos y genéticos.
La Agencia Internacional para la Investigación del Cáncer ha evaluado más de 900 posibles agentes
carcinogénicos, incluidas sustancias químicas, mezclas complejas, agentes ocupacionales e infecciosos,
pero solo nueve de estas exposiciones se acompañan de informes sobre posibles asociaciones con
tumores del SNC en seres humanos (berilio, epiclorhidrina, clordano, heptacloro, metil-tiouracilo,
propiltiouracilo, plomo, sulfato de diisopropilo y diclorometano).
-Varios otros productos químicos aumentaron la incidencia de tumores cerebrales (gliomas) en animales
de experimentación, pero sin pruebas concomitantes en humanos (aflatoxina B1, sulfato de dietilo,
acrilamida, etilnitrosourea, metilnitrosourea, clorhidrato de procarbazina, metanosulfonato de metilo,
sulfato de dimetilo, glicidol, dacarbazina, 1,3-propano sultona, acrilonitrilo).
Las enfermedades infecciosas causadas por virus, bacterias y parásitos, se conocen también como
estados asociados o causales, y pueden contribuir a la carcinogénesis cerebral. Cofactores adicionales,
tales como la inmunidad sistémica y la inflamación crónica, cumplen un papel importante en este proceso.
El análisis de citomegalovirus humano (HCMV) en tejido tumoral y sangre periférica de pacientes con GB
vs donantes normales (sanguíneos y quirúrgicos), encontró que más del 90% de muestras de tejido
tumoral y 80% de muestras de sangre están asociados con el ADN de HCMV, mientras que los donantes
normales no mostraron virus detectable, Estos resultados confirman la asociación de HCMV con GB,
y sugieren una reactivación ya sea sistémica del virus en pacientes con GB o derramamiento de ADN viral
a partir de células tumorales infectadas en la periferia.
Algunos estudios apuntan que determinadas ocupaciones se asociarían a mayor riesgo de padecer un
glioma, tales como el uso de plásticos y productos de caucho. Aunque débil, la exposición ocupacional a
cloruro de vinilo puede llevar a desarrollar GB entre los trabajadores con un periodo de exposición media
de 21 años.
Navas et al. refieren este mismo resultado en la exposición ocupacional a arsénico, mercurio y
productos derivados del petróleo
Cocco et al. relacionan los niveles de plomo con mayor riesgo de desarrollar tumores cerebrales
en hombres de raza blanca
Una revisión reciente sugiere que los hidrocarburos aromáticos policíclicos (HAP) y los insecticidas no-
arsenicales pueden comportarse como posibles carcinógenos ocupacionales de tumores cerebrales
.
Por otra parte, varios estudios sugieren que la ocupación de los padres puede influir en el desarrollo de
gliomas pediátricos. En un estudio de casos y controles, los padres que trabajaban en la industria química
tenían mayor riesgo de tener hijos con tumores astrogliales.
Un estudio de casos y controles realizado en siete países encontró un aumento en el riesgo asociado con
el trabajo agrícola para todos los tumores cerebrales infantiles combinados y para los tumores gliales.
También se ha asociado la ocupación de padres con los vehículos de motor a mayor riesgo de sufrir
tumores cerebrales infantiles en general y astrogliales.
RESECCIÓN QUIRÚRGICA: PRIMERA OPCIÓN
El tratamiento principal de los GB y de los astrocitomas anaplásicos es la mayor resección quirúrgica
posible del tumor documentada mediante RMN dentro de las 72 horas de la cirugía. La cirugía guiada por
fluoresceína sódica (FLS-Na) es una técnica quirúrgica en la que se administra una sustancia intravenosa
capaz de penetrar en el área tumoral y en el área dañada de la barrera hemato-encefálica permitiendo así
una mejor identificación de las estructuras y un mayor volumen de resección tumoral o la posibilidad de
que esta sea completa,
Dada por el microscopio OPMI Pentero 900-Zeiss, este equipo permite reducir la cantidad de FLS-Na
inyectada y realizar una cirugía guiada por imágenes con la inyección de datos Multivisión, así como una
visualización digital integrada con cámara de alta definición HD.
TRATAMIENTO ADYUVANTE
El tratamiento adyuvante con radioterapia asociado a quimioterapia, basada en compuestos alquilantes
(agentes que transfieren grupos alquil a las bases de guanina, dañan el DNA y causan muerte celular)
como la carmustina (BCNU) o la temozolomida (TMZ) han demostrado que pueden incrementar la
supervivencia.
Stupp et al. Compararon en un ensayo clínico randomizado fase III multicéntrico el tratamiento de
radioterapia sola con el de radioterapia asociada a temozolomida en 573 pacientes de hasta 70 años,
afectados de GB y buen estado y encontraron un incremento en la supervivencia global de 10,9 a 27,2% a
los 2 años y de 1,9 a 9,8% a los 5 años.
Algunos estudios han evaluado otras rutas de liberación de quimioterapia. Así, la administración de BCNU
utilizando un polímero biodegradable (wafer) localizado intraoperatoriamente, demostró una mejoría
significativa en la sobrevida de pacientes con gliomas malignos (13,9 vs 11,6 semanas). Beneficio que se
mantuvo por 2 a 3 años tras el implante.
El tratamiento con inhibidores de angiogénesis como el anticuerpo monoclonal dirigido contra VEGF, es
un tratamiento de GB recurrentes tras encontrarse altas tasas de respuesta de supervivencia libre de
progresión en tres estudios fase II.
Sin embargo, dos estudios evalúan el agregar bevacizumab al tratamiento estándar de radioterapia
asociada a temozolomida (AVAglio y RTOG-0825) concluyen que a pesar de lograr un incremento en la
sobrevida libre de progresión de 3- 4 meses, no se encontró beneficio en la sobrevida global y los
pacientes presentaron algunas complicaciones secundarias, especialmente de tipo vascular.
Finalmente, Hofland et al. compararon la adición de bevacizumab a temozolomida o irinotecan por 8 ciclos
junto a radioterapia, tras la resección quirúrgica en 63 pacientes y encontraron tasas de supervivencia de
32 y 23%; y periodos libres de progresión de la enfermedad de 7,7 y 7,3 meses, respectivamente
.
La información obtenida en estudios preclínicos ha permitido identificar otros compuestos candidatos
susceptibles de ser evaluados en ensayos clínicos para pacientes con GB. Sin embargo, el desarrollo de
estas estrategias debe tener en cuenta la capacidad de acceso de estas drogas a la lesión cerebral:
polaridad, tamaño de la molécula y lipofilidad. Así, aunque un área de enfermedad bulky ha alterado la
barrera hematoencefálica (BHE), como se puede evidenciar por la presencia de captación de contraste
incrementada en estudios de neuroimágen, los márgenes infiltrativos incluyen células tumorales que han
migrado lejos del epicentro de la masa tumoral y pueden alojarse en zonas de BHE intactas
.
Debido a la alta frecuencia de amplificación de EGFR (40%) y la mutación en EGFRvIII (25%), diversos
ensayos clínicos han evaluado anticuerpos monoclonales o moléculas contra tirosina kinasa dirigidos
contra el receptor EGFR. Solomon et al. publicaron un ensayo clínico en pacientes con astrocitoma
anaplásico y glioblastomas tratados con radiación +/- nimotuzumab que resultó en un incremento en la
sobrevida con el anticuerpo monoclonal. Recientemente se ha publicado el caso de un paciente afecto de
glioblastoma recurrente con amplificación de MET (presente en el 1% de los casos) que obtuvo una
reducción del 40% del volumen de la lesión tras tratamiento con crizotinib, un anticuerpo monoclonal
dirigido contra esta molécula.
También podría gustarte
- Neoplasias PediatricasDocumento17 páginasNeoplasias PediatricasGustavo André Blancas SaucedaAún no hay calificaciones
- NEUROPATOLOGIADocumento8 páginasNEUROPATOLOGIABárbara Bolis0% (1)
- U5ART - Neoplasia Cerebral PDFDocumento5 páginasU5ART - Neoplasia Cerebral PDFFernanda LópezAún no hay calificaciones
- GliomaDocumento4 páginasGliomaJohana Cáceres GutiérrezAún no hay calificaciones
- Tumores MalignosDocumento25 páginasTumores MalignosViri CarbajalAún no hay calificaciones
- Tumores Parenquimatosos SNCDocumento6 páginasTumores Parenquimatosos SNCGiovanni AgredaAún no hay calificaciones
- Neuropatología TumoralDocumento100 páginasNeuropatología Tumoralapi-3742102100% (1)
- Clasificación de Los Tumores OmsDocumento22 páginasClasificación de Los Tumores OmsJesús LoretoAún no hay calificaciones
- Carcinoma BasocelularDocumento7 páginasCarcinoma BasocelularDichany Gutierrez YepesAún no hay calificaciones
- TUMORES Del Sistema NerviosoDocumento10 páginasTUMORES Del Sistema NerviosokatetateAún no hay calificaciones
- Tumores CerebralesDocumento26 páginasTumores CerebralesGabriela MazaAún no hay calificaciones
- Informe 15 Neuropatologia IiDocumento20 páginasInforme 15 Neuropatologia IiNANCY HOYOS DIAZAún no hay calificaciones
- Resumen Patología NeuroDocumento10 páginasResumen Patología Neuronicol villarrealAún no hay calificaciones
- Neurologia Parte 3Documento44 páginasNeurologia Parte 3ane.aAún no hay calificaciones
- Tumores Del SNC ClaseDocumento34 páginasTumores Del SNC ClaseMiguel Angel OsorioAún no hay calificaciones
- Tumores IntracranealesDocumento14 páginasTumores IntracranealesHector BlueAún no hay calificaciones
- Tumores CerebralesDocumento20 páginasTumores CerebralesPriscila EspinozaAún no hay calificaciones
- TumoresDocumento37 páginasTumoresIvanna MorilloAún no hay calificaciones
- Meduloblastoma Pediátrico, Revisión y Puesta Al DíaDocumento12 páginasMeduloblastoma Pediátrico, Revisión y Puesta Al DíabacchiocchipaoloAún no hay calificaciones
- MeduloblastomaDocumento12 páginasMeduloblastomaSoledad Vega DelgadoAún no hay calificaciones
- Sistema Nervioso CentralDocumento33 páginasSistema Nervioso CentralOrozco Vidal Ariadna MontserratAún no hay calificaciones
- As Trocito MasDocumento32 páginasAs Trocito MasYessica Carranza TorresAún no hay calificaciones
- Guia Oncologia 2022Documento17 páginasGuia Oncologia 2022Hello pandiAún no hay calificaciones
- Tumores Del Sistema Nervioso Med LanchipaDocumento89 páginasTumores Del Sistema Nervioso Med LanchipaTRIUNFANDO100% (1)
- Tumores CerebralesDocumento53 páginasTumores CerebraleslizbiancaAún no hay calificaciones
- LEUCEMIA M4eo PDFDocumento13 páginasLEUCEMIA M4eo PDFjessAún no hay calificaciones
- Tumores CerebralesDocumento28 páginasTumores CerebralesArlet Stefany Chiluiza MorochoAún no hay calificaciones
- Tumores CerebralesDocumento15 páginasTumores Cerebralesisabel rivasAún no hay calificaciones
- Tumores RenalesDocumento31 páginasTumores RenalesMarcos OrtizAún no hay calificaciones
- LMA Asociada A MielodisplasiasDocumento4 páginasLMA Asociada A MielodisplasiasDiana Heredia CoronadoAún no hay calificaciones
- Caso Resonancia 12.04.2022Documento20 páginasCaso Resonancia 12.04.2022Irai MartínezAún no hay calificaciones
- AstrocitomaDocumento34 páginasAstrocitomaDiana Paola NeiraAún no hay calificaciones
- Lab MusculoesqueleticoDocumento13 páginasLab MusculoesqueleticoSamanta MozAún no hay calificaciones
- Tumores CerebralesDocumento32 páginasTumores CerebralesAliss Reyes100% (1)
- Neoplasias MalignasDocumento29 páginasNeoplasias MalignasZallely OchoaAún no hay calificaciones
- Morfologia Arterioloesclerosis Hialina y NefroesclerosisDocumento9 páginasMorfologia Arterioloesclerosis Hialina y NefroesclerosisChristian MolinaAún no hay calificaciones
- Neoplasias Sistema NerviosoDocumento7 páginasNeoplasias Sistema NerviosoKenia espinosa mayerliiiAún no hay calificaciones
- Tumores CerebralesDocumento22 páginasTumores CerebralesDaf MonroyAún no hay calificaciones
- Cap 04 PDFDocumento35 páginasCap 04 PDFCarolina A. AlmendraAún no hay calificaciones
- NeuroblastomaDocumento9 páginasNeuroblastomaIan Meneses VallejoAún no hay calificaciones
- ASTROCITOMASDocumento53 páginasASTROCITOMASJuan Carlos LazoAún no hay calificaciones
- Tema 19-Tumores IntracranealesDocumento92 páginasTema 19-Tumores IntracranealesPablo Novoa FernándezAún no hay calificaciones
- Clasificacion de Las Neoplasias Según Su EvolucionDocumento5 páginasClasificacion de Las Neoplasias Según Su EvolucionWillys OdontoAún no hay calificaciones
- Meduloblastoma: ¿Qué Es El Meduloblastoma?Documento7 páginasMeduloblastoma: ¿Qué Es El Meduloblastoma?angieAún no hay calificaciones
- Neoplasias Mielodisplásicas / Mieloproliferativas: Curso Hematología Especial Greenlandia Ferreyros B. Etm - Upch 2021Documento35 páginasNeoplasias Mielodisplásicas / Mieloproliferativas: Curso Hematología Especial Greenlandia Ferreyros B. Etm - Upch 2021Pierina Patricio AlvinoAún no hay calificaciones
- MeduloblastomaDocumento37 páginasMeduloblastomaBeto MendozaAún no hay calificaciones
- NeuroblastomaDocumento7 páginasNeuroblastomaMaria Camila ZafraneAún no hay calificaciones
- Tumores CerebralesDocumento21 páginasTumores CerebralesOmar VenturaAún no hay calificaciones
- Leucemias MieloidesDocumento23 páginasLeucemias MieloidesKike SanthanaAún no hay calificaciones
- Tumores Del Sn.Documento75 páginasTumores Del Sn.Diana Katherine Arroyave CoboAún no hay calificaciones
- Tumores CNS Niños 2Documento38 páginasTumores CNS Niños 2Jose Rodolfo Mafara MartinezAún no hay calificaciones
- Guia de Manejo TumoresDocumento5 páginasGuia de Manejo TumoresGiovana SabarburuAún no hay calificaciones
- Neoplasias GeneralidadesDocumento11 páginasNeoplasias GeneralidadesCristián AndrèsAún no hay calificaciones
- Nódulos en El BazoDocumento6 páginasNódulos en El BazogrihecAún no hay calificaciones
- ¿Qué Son? Enfermedades Clonales de La Célula Madre Hematopoyética, Disfunción de La MédulaDocumento25 páginas¿Qué Son? Enfermedades Clonales de La Célula Madre Hematopoyética, Disfunción de La MédulaEstrella Monserrat Hernandez SanchezAún no hay calificaciones
- Neoplasias. Síntomas y Signos Asociados A Las Neoplasias.Documento7 páginasNeoplasias. Síntomas y Signos Asociados A Las Neoplasias.Víctor AndujaAún no hay calificaciones
- Leucemia Mieloide CrónicaDocumento1 páginaLeucemia Mieloide CrónicaanaAún no hay calificaciones
- Tumores de SNCDocumento9 páginasTumores de SNCAlexis Luna BurgueñoAún no hay calificaciones
- Uso de Derivados del Cannabis en Pacientes con CáncerDe EverandUso de Derivados del Cannabis en Pacientes con CáncerAún no hay calificaciones
- Fundamentos del diagnóstico y tratamiento del cáncer en adultos: Una aproximación inicial para el médico no especialista en cáncerDe EverandFundamentos del diagnóstico y tratamiento del cáncer en adultos: Una aproximación inicial para el médico no especialista en cáncerAún no hay calificaciones
- Tumores CerebralesDocumento4 páginasTumores Cerebralesgiovanna trujillo100% (1)
- Banco NeurooooDocumento40 páginasBanco NeurooooNataly QHAún no hay calificaciones
- Carcinoma-Basocelular 1Documento4 páginasCarcinoma-Basocelular 1Nataly QHAún no hay calificaciones
- Aneurisma Cerebral - GlioblastomaDocumento8 páginasAneurisma Cerebral - GlioblastomaNataly QHAún no hay calificaciones
- COLORACIONESDocumento3 páginasCOLORACIONESNataly QHAún no hay calificaciones
- RR PDFDocumento7 páginasRR PDFjosebernardoAún no hay calificaciones
- T Manejo de QuemadurasDocumento39 páginasT Manejo de QuemadurasNataly QHAún no hay calificaciones
- Sem 1 - 4 Med InterculturalDocumento4 páginasSem 1 - 4 Med InterculturalNataly QHAún no hay calificaciones
- Sem 1 - 4 Med InterculturalDocumento4 páginasSem 1 - 4 Med InterculturalNataly QHAún no hay calificaciones
- Expo - Sexualidad - GeneroDocumento23 páginasExpo - Sexualidad - GeneroNataly QHAún no hay calificaciones
- ValvulopatíasDocumento11 páginasValvulopatíasjbastiasAún no hay calificaciones
- Secuencia de Intubación RapidaDocumento9 páginasSecuencia de Intubación RapidaDiana Janeth García ZamoraAún no hay calificaciones
- Enfermedades de Transmisión Sexual PDFDocumento68 páginasEnfermedades de Transmisión Sexual PDFBrando RomeroAún no hay calificaciones
- Triptico FeminicidioDocumento2 páginasTriptico FeminicidioJosue Caneda100% (3)
- Elementos para La Toma de DesicionesDocumento8 páginasElementos para La Toma de DesicionesFERNANDA HERNANDEZ RAMIREZAún no hay calificaciones
- Insuficiencia CardiacaDocumento7 páginasInsuficiencia CardiacaOriana Carolina Gutierrez OllarvesAún no hay calificaciones
- Preguntas Pediatria CtoDocumento10 páginasPreguntas Pediatria Ctokaroline SernadesAún no hay calificaciones
- Cuestionario ParasitologíaDocumento3 páginasCuestionario ParasitologíaJosé Luis Garcia AlegríaAún no hay calificaciones
- Presentación Del TemaDocumento3 páginasPresentación Del Temaricardo constantAún no hay calificaciones
- Covid 19 Diagnostico Radiologico Escalas de GravedadDocumento19 páginasCovid 19 Diagnostico Radiologico Escalas de GravedadRuben GonzalezAún no hay calificaciones
- Caso ClínicoDocumento8 páginasCaso ClínicoRodrigo Beelze De la CruzAún no hay calificaciones
- EsporotricosisDocumento21 páginasEsporotricosisMicaela TenorioAún no hay calificaciones
- Cuadro NeuropatologíasDocumento33 páginasCuadro NeuropatologíasYara NietoAún no hay calificaciones
- Árbol de Problemas de AnemiaDocumento1 páginaÁrbol de Problemas de AnemiajulietaAún no hay calificaciones
- Primeros Auxilios. Alteración de La ConcienciaDocumento2 páginasPrimeros Auxilios. Alteración de La ConcienciabeiAún no hay calificaciones
- 03 Principios de Dermatología. Enfermedades de Piel II. Dra Hernandez LDocumento69 páginas03 Principios de Dermatología. Enfermedades de Piel II. Dra Hernandez LChristian RosalesAún no hay calificaciones
- Revisión de Articulo2Documento29 páginasRevisión de Articulo2Gabriela CruzAún no hay calificaciones
- Patologia de Pares Craneales VII - XIIDocumento10 páginasPatologia de Pares Craneales VII - XIIRolando ValbuenaAún no hay calificaciones
- Enfermedades Por Mala NutriciónDocumento2 páginasEnfermedades Por Mala NutriciónFidel QuispeAún no hay calificaciones
- Intervenciones de Enfermeria para Prevencion y TX de Cama PDFDocumento78 páginasIntervenciones de Enfermeria para Prevencion y TX de Cama PDFAngel AL ArteagaAún no hay calificaciones
- Accidentes Cerebrovasculares Hemorrágicos ResumoDocumento9 páginasAccidentes Cerebrovasculares Hemorrágicos ResumoVictória FerreiraAún no hay calificaciones
- Discapacidad IntelectualDocumento20 páginasDiscapacidad IntelectualjoseAún no hay calificaciones
- FuncionalDocumento6 páginasFuncionalDIANA PAO HACHAMIZA SUICAAún no hay calificaciones
- Neumonia Adquirida en La Comunidad DGF Marzo 2015Documento60 páginasNeumonia Adquirida en La Comunidad DGF Marzo 2015Ayleen TorresAún no hay calificaciones
- Universidad Central de Nicaragua UCNDocumento12 páginasUniversidad Central de Nicaragua UCNMorelia SandovalAún no hay calificaciones
- Juárez García Veronica PDFDocumento2 páginasJuárez García Veronica PDFAlejandro RamosAún no hay calificaciones
- Hemograma 3Documento57 páginasHemograma 3Dylan RamirezAún no hay calificaciones
- Presentación FarmacéuticaDocumento6 páginasPresentación FarmacéuticaRosa ContrerasAún no hay calificaciones
- Torniquete para HemorragiaDocumento10 páginasTorniquete para HemorragiaAbigail Vanesa VelazquezAún no hay calificaciones
- AbortoDocumento36 páginasAbortoRafael BriceñoAún no hay calificaciones