Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Enzimas PH y Concentracion
Cargado por
vania natalia olvera olguin0 calificaciones0% encontró este documento útil (0 votos)
11 vistas2 páginasenzimas
Título original
Enzimas pH y concentracion
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoenzimas
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
11 vistas2 páginasEnzimas PH y Concentracion
Cargado por
vania natalia olvera olguinenzimas
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
BIOQUÍMICA GENERAL
Práctica: Efecto de la concentración de enzima sobre la velocidad de la
reacción, efecto del pH sobre la velocidad de reacción.
Alumnos: Gonzàlez Severiano Mauricio y Martìnez Capetillo Diana I.
Grupo: 3FV1 Sección: 2 Equipo: 4
Introducción: De acuerdo a la literatura consultada, la
Una enzima es un catalizador biológico invertasa tiene un pH óptimo que va
que acelera las velocidades de las desde 4.5 a 5 por lo que el valor reportado
reacciones químicas. Esta actividad en la reacción coincide con el pH óptimo
depende de ciertas condiciones, entre de la invertasa.
ellas la concentración de la enzima y el (Bioquímica, texto y atlas)
pH del medio. Sin embargo, después de haber
Objetivos: alcanzado la velocidad máxima de la
● Determinar el pH óptimo de la reacción, de acuerdo a la literatura, se
invertasa. esperaría que el valor de absorbancia
● Demostrar que la concentración de disminuyera poco a poco, lo cual no
enzima es directamente proporcional a sucedió.
la velocidad de reacción. Hemos inferido que esto fue ocasionado
● Analizar la importancia del pH del por la posible contaminación de los
medio sobre la velocidad de reacción reactivos.
enzimática y su efecto sobre el Efecto de la concentración de enzima.
carácter iónico de la enzima y del Para este experimento la concentración
sustrato. del sustrato debe ser constante. Teniendo
Resultados: en cuenta lo anterior, se explica que al ir
Anexos en la siguiente página aumentando la concentración de enzima
Discusión: en nuestro medio, más moléculas están
Efecto del pH sobre la velocidad de disponibles para unirse al sustrato,
reacción aumentando su actividad.
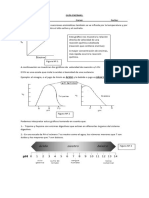
De acuerdo a la estructura primaria de las Como podemos apreciar en la Gráfica 2,
enzimas, contienen diferentes al ir aumentando la concentración de
aminoácidos con grupos ionizables. Es enzima, la velocidad de reacción de igual
por esto, que dependerá del medio en el forma aumentará.
que se lleve a cabo la reacción si es ácido Conclusión:
o básico. En esta práctica determinamos el pH
Cada enzima cuenta con un pH óptimo óptimo de la invertasa, el cual es entre 4.5
que es en donde se alcanza el punto de y 5, además se aprecia en la Gráfica 2
mayor velocidad de reacción. Por ende, al una línea recta con pendiente positiva, por
variar el rango de pH la velocidad de la lo que la relación entre [enzima] y la
reacción se ve afectada, y en valores velocidad de reacción, son directamente
extremos de pH, se desnaturaliza la proporcionales.
enzima. Referencias:
En nuestra experiencia trabajamos con la -Boyer R., “Conceptos de Bioquímica”
enzima invertasa y de acuerdo a la Editorial International Thomson Editores.
Gráfica 1, podemos observar que la 1a Ed. en Español pp. 78- 81 (2000)
velocidad de reacción alcanza el punto -Donald Voet, Judith G. Voet.(2006)
más alto a un pH de 4.5. Bioquímica. ED. Panamericana.
Capítulo 4. Aminoácidos. Pag. 76 -Técnicas de Bioquímica Aplicada.
Plumer, D.T. 1981. Editorial Interamericana.
-Introducción a la Bioquímica Práctica. Mc
Graw Hill.Rendina, G. 1974.
Gráfica 1: Efecto de pH sobre la actividad invertasa.
Tabla 2. Efecto de la [Enzima] sobre la velocidad de reacción.
Tubo 1 2 3 4 5
Absorbencia .271 .688 .625 1.150 1.425
[A.R] 4.16 12.264 11.04 21.234 26.574
U.I .416 1.226 1.104 2.123 2.657
[Enzima] 0.5 1 1.5 2 2.5
Gráfica 2: Unidades de invertasa sobre concentración de enzima
También podría gustarte
- Fundamentos de química aplicados a las ciencias de la saludDe EverandFundamentos de química aplicados a las ciencias de la saludAún no hay calificaciones
- Docsity Informe Del Efecto de PH y Concentracion de EnzimaDocumento3 páginasDocsity Informe Del Efecto de PH y Concentracion de EnzimaHéctor Gerardo Morales ÁlvarezAún no hay calificaciones
- Efecto Del PHDocumento3 páginasEfecto Del PHClaw FollowilAún no hay calificaciones
- Practica 2-7 Bioquimica, Equipo 15Documento5 páginasPractica 2-7 Bioquimica, Equipo 15Victor Del RazoAún no hay calificaciones
- Bitacora de La Practica 6Documento3 páginasBitacora de La Practica 6Nathan Ulises Reyes JimenezAún no hay calificaciones
- REPORTE PH y Sustrato. Sec3Documento3 páginasREPORTE PH y Sustrato. Sec3Macias Guadalupe LizbethAún no hay calificaciones
- PH y TemperaturaDocumento4 páginasPH y TemperaturaHernandez Chavez DavidAún no hay calificaciones
- Efecto de Factores Sobre La Velocidad EnzimáticaDocumento9 páginasEfecto de Factores Sobre La Velocidad EnzimáticaJuan Carlos Caredano PalaciosAún no hay calificaciones
- Bitacora Bioquimica Practica 5 VELOCIDAD DE REACCIÓN" y "EFECTO DE PH SOBRE LA VELOCIDAD DE REACCIÓNDocumento3 páginasBitacora Bioquimica Practica 5 VELOCIDAD DE REACCIÓN" y "EFECTO DE PH SOBRE LA VELOCIDAD DE REACCIÓNDiego AmrAún no hay calificaciones
- PH y Concentrecion EnzimaticaDocumento3 páginasPH y Concentrecion EnzimaticaSaul SalasAún no hay calificaciones
- Guía EnzimasDocumento2 páginasGuía EnzimasFlorencia CeballosAún no hay calificaciones
- T-4 Factores Que Afectan La ActicidadDocumento15 páginasT-4 Factores Que Afectan La ActicidadJOSE CARLOS CASTILLO OTINIANOAún no hay calificaciones
- Informe Practica 5.2 y 5.3-Seccion 1-3IV2Documento1 páginaInforme Practica 5.2 y 5.3-Seccion 1-3IV2Nava Dominguez DanielaAún no hay calificaciones
- Efecto de La Concentración de EnzimasDocumento2 páginasEfecto de La Concentración de EnzimasEdson Sama0% (1)
- PH y Concentracion EnzimaDocumento2 páginasPH y Concentracion EnzimaHector Hdz BenítezAún no hay calificaciones
- ANEXOSDocumento7 páginasANEXOSAndres Felipe Bolaño NarvaezAún no hay calificaciones
- Discusión Práctica#2. Equipo 2. Grupo-3FM2Documento23 páginasDiscusión Práctica#2. Equipo 2. Grupo-3FM2Jimenez Valverde Jesús FranciscoAún no hay calificaciones
- Reporte Práctica 7 y 8 BioquímicaDocumento5 páginasReporte Práctica 7 y 8 BioquímicaNora EdthAún no hay calificaciones
- Escuela Nacional de Ciencias Biológicas (ENCB) Laboratorio de Bioquímica Escobar Ortega Jacobo Eduardo 3IV1Documento6 páginasEscuela Nacional de Ciencias Biológicas (ENCB) Laboratorio de Bioquímica Escobar Ortega Jacobo Eduardo 3IV1Quesito MininoAún no hay calificaciones
- Laboratorio N°11. BioquímicaDocumento3 páginasLaboratorio N°11. BioquímicaJohn CedeñoAún no hay calificaciones
- Practica Actividad EnzimaticaDocumento6 páginasPractica Actividad EnzimaticaCasadevidaTV En LíneaAún no hay calificaciones
- Practica N°9 Factores Que Intervienen en La Velocidad de La Reacción EnzimáticaDocumento7 páginasPractica N°9 Factores Que Intervienen en La Velocidad de La Reacción EnzimáticaHarvi Garcia RangelAún no hay calificaciones
- Laboratorio Virtual: Factores Que Afectan A La Actividad Enzimática.Documento4 páginasLaboratorio Virtual: Factores Que Afectan A La Actividad Enzimática.Rosa BishopAún no hay calificaciones
- 19.05 Factores Que Afectan La Actividad EnzimáticaDocumento3 páginas19.05 Factores Que Afectan La Actividad EnzimáticaJuan GarcíaAún no hay calificaciones
- Practica 2 de BioquimicaDocumento6 páginasPractica 2 de BioquimicaAlexander Fernández LujánAún no hay calificaciones
- Discusión de Bioquímica #2Documento15 páginasDiscusión de Bioquímica #2Steven Vásquez33% (3)
- Cinética Enzimática I y IIDocumento6 páginasCinética Enzimática I y IIGreivin CortésAún no hay calificaciones
- Practica 6 Cinetica Enzimatica.Documento15 páginasPractica 6 Cinetica Enzimatica.Salvador Cruz33% (3)
- Informe Del Factor G de CattellDocumento10 páginasInforme Del Factor G de CattelljorgeAún no hay calificaciones
- Practica 6 Cinetica EnzimaticaDocumento15 páginasPractica 6 Cinetica EnzimaticaMauricio MartínezAún no hay calificaciones
- Efecto de La Concentracion y PH en La Velocidad de Una Reacción EnzimaticaDocumento3 páginasEfecto de La Concentracion y PH en La Velocidad de Una Reacción EnzimaticaPosak HernandezAún no hay calificaciones
- Practica #10 Procesos Biológicos - Enzimas y Respiración Celular OKDocumento4 páginasPractica #10 Procesos Biológicos - Enzimas y Respiración Celular OKRuth JañoAún no hay calificaciones
- Práctica Cinética EnzimáticaDocumento18 páginasPráctica Cinética EnzimáticaFernanda LealAún no hay calificaciones
- Grupo 2. Regulación EnzimaticaDocumento8 páginasGrupo 2. Regulación EnzimaticaMaritzaIraholaZallesAún no hay calificaciones
- Cinética Enzimática y El Efecto de La Concentración de Sustrato y La Temperatura Sobre La Actividad CatalíticaDocumento4 páginasCinética Enzimática y El Efecto de La Concentración de Sustrato y La Temperatura Sobre La Actividad CatalíticaCitlalli Damian VertizAún no hay calificaciones
- Informe #6 Factores Que Afectan La Actividad Enzimática - 2021-2Documento9 páginasInforme #6 Factores Que Afectan La Actividad Enzimática - 2021-2Mayra Esther Barreto SotoAún no hay calificaciones
- Informe Practica 7Documento3 páginasInforme Practica 7MariCarmenAún no hay calificaciones
- EnzimasDocumento6 páginasEnzimasClauMcClauAún no hay calificaciones
- Identificación, Propiedades y Cinética de La CatalasaDocumento11 páginasIdentificación, Propiedades y Cinética de La CatalasaDiana Alexandra Santos RiveraAún no hay calificaciones
- Enzimas y Pancreático ####Documento62 páginasEnzimas y Pancreático ####7z6v7d7dhyAún no hay calificaciones
- Cinetiza EnzimaticaDocumento8 páginasCinetiza EnzimaticaAndy Phy100% (1)
- Actividad EnzimáticaDocumento11 páginasActividad EnzimáticaEnmanuel Samudio100% (1)
- Trabajo Numero 3 en GrupoDocumento23 páginasTrabajo Numero 3 en Grupolizeth gaambaAún no hay calificaciones
- Practica 4 MetabolismoDocumento8 páginasPractica 4 MetabolismoPaloma E. ChavezAún no hay calificaciones
- EnzimasDocumento9 páginasEnzimasYize AbadAún no hay calificaciones
- ENZIMAS LAB#6 (Autoguardado)Documento5 páginasENZIMAS LAB#6 (Autoguardado)yohannyAún no hay calificaciones
- Bioquímica Informe N°8 y 9 - Cinética EnzimáticaDocumento22 páginasBioquímica Informe N°8 y 9 - Cinética EnzimáticaMestizo Sinalefa50% (6)
- T-4 Factores Que Afectan La Acticidad EnzimaticaDocumento18 páginasT-4 Factores Que Afectan La Acticidad EnzimaticaFrank Roldan CalipuyAún no hay calificaciones
- Enzimas (Propiedades)Documento6 páginasEnzimas (Propiedades)Enrique Hernandez100% (6)
- Efecto de La Concentración de Enzima y Del PH Sobre La Velocidad de ReacciónDocumento3 páginasEfecto de La Concentración de Enzima y Del PH Sobre La Velocidad de ReacciónAlain Bleu100% (1)
- Bitacora Curva de Azucares ReductoresDocumento2 páginasBitacora Curva de Azucares ReductoresNadia VargasAún no hay calificaciones
- Efecto de PH y de La ConcentracionDocumento3 páginasEfecto de PH y de La ConcentracionGeovanny AguirreAún no hay calificaciones
- Actividad EnzimaticaDocumento4 páginasActividad EnzimaticaEdisonFabianBarbosaRojas100% (3)
- FAZ-Factores Que Afectan La Actividad EnzimaticaDocumento21 páginasFAZ-Factores Que Afectan La Actividad EnzimaticaKaren ReyesAún no hay calificaciones
- Guía Enzimas 1Documento7 páginasGuía Enzimas 1Diego David CastroAún no hay calificaciones
- PI721-L04 EnzimasDocumento22 páginasPI721-L04 EnzimasAdorian FārAún no hay calificaciones
- Practica N. 5.1 PH y ConcentraciónDocumento2 páginasPractica N. 5.1 PH y ConcentraciónLopez Ocampo ArandyAún no hay calificaciones
- Cardona - Los Enzimas. Introducción A La Enzimología.Documento9 páginasCardona - Los Enzimas. Introducción A La Enzimología.Danher EscalanteAún no hay calificaciones
- Práctica 15. FQDocumento12 páginasPráctica 15. FQEfraínAún no hay calificaciones
- Reporte de Practica Curvas TipoDocumento8 páginasReporte de Practica Curvas Tipovania natalia olvera olguinAún no hay calificaciones
- Bitácora de pH-EDocumento10 páginasBitácora de pH-Evania natalia olvera olguinAún no hay calificaciones
- Práctica 6 - 3FV2Documento10 páginasPráctica 6 - 3FV2vania natalia olvera olguinAún no hay calificaciones
- Práctica 7 BotánicaDocumento10 páginasPráctica 7 Botánicavania natalia olvera olguinAún no hay calificaciones
- Guía N°2 Cinética Química PDFDocumento11 páginasGuía N°2 Cinética Química PDFFernando Samame DelgadoAún no hay calificaciones
- Actividad 2 Química Industrial y SostenibilidadDocumento10 páginasActividad 2 Química Industrial y SostenibilidadDANIEL BENITEZAún no hay calificaciones
- Guía de Laboratorio Reacciones RedoxDocumento2 páginasGuía de Laboratorio Reacciones RedoxKatherine López MontalbánAún no hay calificaciones
- Q5 PAU EquilibrioDocumento24 páginasQ5 PAU EquilibrioÁlex SanAún no hay calificaciones
- Ejercicios de La Sesión 5Documento6 páginasEjercicios de La Sesión 5Julia AdamaryAún no hay calificaciones
- Practica 3 Quimica IndustrialDocumento14 páginasPractica 3 Quimica IndustrialHans PilzAún no hay calificaciones
- Tema 4 - Cambios Qcos (2º ESO)Documento16 páginasTema 4 - Cambios Qcos (2º ESO)Davidhugo BoadacruzAún no hay calificaciones
- Qué Es Oscurecimiento EnzimáticoDocumento3 páginasQué Es Oscurecimiento EnzimáticokatherineAún no hay calificaciones
- 02 AnalisisMateriaEnergia AMAE-03 Rev PDFDocumento28 páginas02 AnalisisMateriaEnergia AMAE-03 Rev PDFLuispanqueAún no hay calificaciones
- BROWN Quim11ed Cap14Documento64 páginasBROWN Quim11ed Cap14Carlos Acosta100% (1)
- Ensayo - Materia y EnergiaDocumento7 páginasEnsayo - Materia y EnergiaMiguel Angel Dzib0% (1)
- Trabajo Domiciliario 1Documento10 páginasTrabajo Domiciliario 1AnthonyPJAún no hay calificaciones
- Qca - 1EM - U01 - G04 Aprendizaje - Representación de Las Reacciones Químicasecuaciones QuímicasDocumento7 páginasQca - 1EM - U01 - G04 Aprendizaje - Representación de Las Reacciones Químicasecuaciones Químicasilse duranAún no hay calificaciones
- ABM Primer Avance - Grupo 2 - VF DavidDocumento70 páginasABM Primer Avance - Grupo 2 - VF DavidJacqueline GodoyAún no hay calificaciones
- Recuperación 2º Eso - F y QDocumento20 páginasRecuperación 2º Eso - F y Qpeisaraca75% (8)
- Cinética de Las Reacciones QuímicasDocumento12 páginasCinética de Las Reacciones QuímicasMatraz23100% (1)
- Polimeros PresentacionDocumento11 páginasPolimeros PresentacionHansel GutierrezAún no hay calificaciones
- Folleto EtanolDocumento14 páginasFolleto EtanolSara SaviAún no hay calificaciones
- J11 B3-TDocumento112 páginasJ11 B3-TRichard Enmanuel Quispe PacoriAún no hay calificaciones
- La Primera Ley de La TermodinámicaDocumento15 páginasLa Primera Ley de La TermodinámicaAngelica OrduzAún no hay calificaciones
- S05.s1 - Material - Equilibrio QuímicoDocumento34 páginasS05.s1 - Material - Equilibrio QuímicoOlger Aragon BerlangaAún no hay calificaciones
- Aprendizajes Esperados Ciencias 3Documento6 páginasAprendizajes Esperados Ciencias 3Anonymous xi1c5Npmjb100% (1)
- QUÍMICA 3er Año Momento 1 Contenido Teórico-Práctico.Documento18 páginasQUÍMICA 3er Año Momento 1 Contenido Teórico-Práctico.Eduardo RequenaAún no hay calificaciones
- Nivelación 01 - QuímicaDocumento6 páginasNivelación 01 - QuímicaCarla RodríguezAún no hay calificaciones
- Norma de Bioseguridad LaboratorioDocumento21 páginasNorma de Bioseguridad Laboratoriopetufredy1972Aún no hay calificaciones
- ManualDocumento124 páginasManualAura CortésAún no hay calificaciones
- Semana 3Documento20 páginasSemana 3Sam FabreyAún no hay calificaciones
- Experimento #7 - Reacciones RedoxDocumento7 páginasExperimento #7 - Reacciones RedoxChristopher Aparicio19Aún no hay calificaciones
- Tarea Semana 7 QuimicaDocumento7 páginasTarea Semana 7 QuimicaMadleenDíazLastarriaAún no hay calificaciones