Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Manual de Endocrinología y Nutrición de La SEEN - Incidentaloma Hipofisario y Silla Turca Vacía
Cargado por
Julieta GarridoTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Manual de Endocrinología y Nutrición de La SEEN - Incidentaloma Hipofisario y Silla Turca Vacía
Cargado por
Julieta GarridoCopyright:
Formatos disponibles
NEUROENDOCRINOLOGÍA
Incidentaloma hipofisario y silla turca vacía
Fernando Pazos Toral. Servicio de Endocrinología. Hospital Marqués de Valdecilla.
ÍNDICE
1. INCIDENTALOMA HIPOFISARIO
2. SILLA TURCA VACÍA
INCIDENTALOMA HIPOFISARIO
Concepto y epidemiología
Entendemos por incidentaloma hipofisario una lesión, referida generalmente como masa o tumor, clínicamente silente tanto
desde el punto de vista endocrinológico como neurooftalmológico, descubierta de manera incidental, que en lo que nos ocupa
ocurre en el contexto de una exploración de imagen mediante resonancia magnética nuclear (RMN) y, en ocasiones, una
tomografía axial computada (TAC), que incluyen el área hipofisaria, y dónde debemos añadir las lesiones detectadas por
tomografía tipo PET (tomografía por emisión de positrones) en estudios de extensión por patología tumoral no relacionada,
utilizando fluorodeoxiglucosa (FDG) y fluorocolina (FCH). Dentro del diagnóstico diferencial de masa hipofisaria los adenomas
representan con mucha diferencia la lesión más frecuente, fundiéndose el concepto de incidentaloma con el de adenoma
hipofisario clínicamente no funcionante asintomático u oligosintomático. Sin embargo, la descripción radiológica o el contexto
clínico pueden plantean otras posibilidades diagnósticas dentro del marco que conocemos clásicamente como diagnóstico
diferencial de masa hipofisaria (tabla 1).
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 1
Tabla 1. Diagnóstico diferencial de masa hipofisaria
1. Neoplasias adenohipofisarias primarias: (clínicamente funcionantes y no-funcionantes) (adenomas típicos y adenomas atípicos)
a. Adenomas productores de PRL, GH, ACTH, TSH, FSH, LH (funcionantes y no funcionantes)
b. Adenoma plurihormonal
c. Adenoma null cell
d. Oncocitoma hipofisario
e. Carcinoma hipofisario
2. Tumores de hipófisis posterior
a. Pituicitoma
b. Tumor de células granulares
c. Gangliocitoma
3. Otros tumores benignos
a. Quistes: quiste de Rathke, epidermoide, dermoide, aracnoideo
b. Mucocele
c. Craneofaringioma
d. Meningioma
4. Tumores malignos
a. Células germinales: germinoma, teratomas, pinealoma ectópico
b. Gliomas, ependimoma, astrocitoma
c. Linfoma
d. Cordoma
e. Enfermedad metastásica
5. Lesiones infecciosas, infiltrativas y granulomatosas
a. Sarcoidosis
b. Histiocitosis de células de Langerhans
c. Granulomatosis de Wegener
d. Plasmocitoma
e. Mucocele
f. Hipofisitis granulomatosa y linfocítica
g. Absceso hipofisario
h. Tuberculosis, histoplasmosis
i. Cisticercosis, hidatidosis
6. Lesiones vasculares
a. Aneurisma. Fístula arteriovenosa
b. Apoplejía hipofisaria frente a hemorragia
7. Miscelánea
a. Hipertrofia-hiperplasia hipofisaria
En autopsias no seleccionadas los adenomas hipofisarios se encuentran en una proporción que oscila entre el 1,5% y el 31%, y
que agrupados revelan una prevalencia media del 10,7%, sin diferencias de distribución en la edad o el sexo. La inmensa mayoría
de los tumores post mortem fueron microadenomas lo que pone de manifiesto el bajo potencial de crecimiento de estos
procesos, o alternativamente aquellos que tienen potencial de crecimiento y evolucionan a macroadenomas llegan a ser
clínicamente evidentes durante la vida del individuo. Estos resultados contrastan con los datos epidemiológicos poblacionales de
tumores con relevancia clínica que muestran una prevalencia estimada del 0,075-0,095 % y una incidencia de 4 y 0,5 casos por
100.000 habitantes/año para tumores e incidentalomas, respectivamente.
En estudios poblacionales no seleccionados los resultados de estudio neurorradiológicos mediante TAC de alta resolución o RMN
fueron similares a los encontrados en las autopsias y que, con ligeras variaciones que dependen del procedimiento realizado, la
utilización o no de contraste o la intervención de uno o varios observadores, han arrojado, en metaanálisis recientes, prevalencias
medias lesiones hipofisarias del 22,5% (4-38%), siendo la inmensa mayoría de tamaños menores de 10 mm. Cabe destacar
igualmente la baja incidencia global de macroadenomas hipofisarios tanto en exploraciones diagnósticas neurorradiológicas
como en las realizadas en una muestra de población normal, que las sitúan entre el 0,16% y el 0,3%. Cuando el análisis es referido
exclusivamente de series de incidentalomas hipofisarios remitidos para evaluación en centros hospitalarios de referencia, la
proporción de macroadenomas aumenta hasta valores superiores al 50% (17-98%), lo que pone de manifiesto que la
trascendencia clínica de estos tumores, aunque sea indirecta, parece ser mayor a lo atribuido en función de los estudios en la
población general y post mortem.
Los hallazgos patológicos de hipófisis en autopsias no seleccionadas y algunos estudios poblacionales ponen de manifiesto un
alto porcentaje de lesiones quísticas. Sin embargo, las lesiones sólidas generalmente adenomas, son las más prevalentes en la
mayoría de las series y objeto fundamental de nuestra exposición. Los análisis inmunohistoquímicos tanto in vivo como en las
muestras de autopsias, demuestran que la positividad de prolactina (PRL) sigue siendo la más frecuente, entre el 22% y el 66% de
los incidentalomas, seguido de lejos por positividades para adrenocorticotropina (ACTH), hormona del crecimiento (GH) e incluso
tireotropina (TSH).
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 2
Clínica de presentación
Muchas son las razones por las que un paciente se realiza una exploración neurorradiológica mediante TAC, RMN o incluso PET
que descubren una masa hipofisaria no sospechada y clínicamente silente. La cefalea (la causa más frecuente), enfermedad
cerebrovascular, sintomatología neurológica como vértigo, deterioro del estado general o durante la evaluación de una
enfermedad metastásica, figuran en términos generales como los motivos más habituales. La media de edad es de 50 años
(17-80 años) y se observa una representación ligeramente superior en mujeres. Estas lesiones inicialmente silentes por definición,
se comportan como adenomas no funcionantes descubiertas de manera incidental, pero muchos de ellos son lo que llamamos,
sensu stricto, adenomas silentes (inmunorreactividad, ultraestructura y factores de transcripción específicos de una determinada
hormona hipofisaria). Y al contrario, en algunos incidentalomas, cuando explorados específicamente, al inicio o durante el
seguimiento, se pone de manifiesto una clínica o bioquímica de hipersecreción hormonal, hipopituitarismo o trastorno visual,
campimétrico, agudeza visual y neurooftalmológico asociado.
En cuanto a la producción, la de prolactina (PRL) es la alteración más frecuente en las diferentes series, tanto por una
inmunorreactividad positiva en piezas quirúrgicas y post mortem (39,5% en 334 adenomas de autopsias), como
hiperprolactinemia en el 12% de las pocas series retrospectivas. Estos hallazgos unidos a que los prolactinomas son la variedad
más frecuente de adenomas, han derivado en la recomendación de realizar una determinación de PRL ante una masa incidental
hipofisaria. Numerosos trabajos han encontrado, aunque en menor frecuencia, adenomas incidentales silentes productores de
ACTH (13,8% en 334 adenomas de autopsias y 6% en series postquirúrgicas). Sin embargo, no disponemos de estudios que
hayan medido la frecuencia de enfermedad de Cushing subclínica o aumento de ACTH en incidentalomas. La producción de GH,
ya sea tumor silente o subclínica, es mucho menos frecuente alcanzando sólo el 2,1% de los adenomas post mortem positivos, y
menos los casos de acromegalia detectados tras estudios hormonales.
En el otro extremo, las deficiencias aisladas o el hipopituitarismo son relativamente frecuentes, generalmente en
macroincidentalomas, con prevalencias del 19,6%, en la serie más larga y un rango entre 0% y 41% en los diferentes autores. Por
razones de tamaño, los microadenomas teóricamente no alteran la función hipofisaria normal, pero Yuen y cols. han encontrado,
en su serie de microadenomas hipofisarios no funcionantes, deficiencia de GH y otras hormonas hipofisarias en casi el 50% de
los pacientes, aunque diagnosticados mediante pruebas funcionales dinámicas y en presencia de IGF-1 normal.
En general, en la evaluación inicial, se detectan alteraciones visuales y campimétricas en el 5% de los macroadenomas,
aumentando esta prevalencia hasta el 21% en las series quirúrgicas.
Historia natural
El conocimiento de la historia natural evolutiva es fundamental en la planificación de la actitud terapéutica. Sin embargo, las
series publicadas son limitadas tanto en el número de pacientes como en el tiempo de observación y, además, no se refieren a
una población general no seleccionada sometida a un estudio prospectivo, sino a pacientes derivados a centros hospitalarios de
referencia. La mayoría de los estudios son retrospectivos, y casi siempre macroadenomas o tumores sólidos no funcionantes. En
el estudio retrospectivo japonés de 506 pacientes, el de mayor número, 258 fueron sometidos a neurocirugía en el diagnóstico
mientras que 248 lo fueron en seguimiento hormonal y radiológico durante un periodo de 2,2 años (6 meses y 14,5 años). De
estos 258, el 12,5% aumentaron de tamaño en un período medio de 45,5 meses, 10 fueron microadenomas y 20 macroadenomas.
Este estudio, que se refiere genéricamente a incidentalomas hipofisarios, presupone que sólo 115 de los 248 pacientes en
seguimiento lo son a título de adenomas hipofisarios no funcionantes, siendo el resto quistes u otro tipo de lesiones, lo que
permite concluir globalmente que el 20% de los adenomas hipofisarios incidentales específicamente considerados
experimentaron crecimiento, mientras que el 9,6% mostraron reducción durante el periodo de observación.
En un intento de sintetizar y agrupar las diferentes series de incidentalomas hipofisarios generalmente adenomas no
funcionantes, en la revisión sistemática y metaanálisis de Fernández-Balsells y cols., y utilizando los datos de 11 estudios
longitudinales y observacionales con un total de 902 pacientes seguidos una media de 3,9 años (1-15a), han intentado ponderar
los factores pronóstico de progresión (crecimiento tumoral o necrosis y/o clínica hormonal y/o defecto campimétrico) y
expresarlos como incidencia por 100 pacientes/año. Este estudio identificó que los macroincidentalomas tienen un mayor
potencial de crecimiento (12,5% vs 3,32%% en microincidentalomas) y que es mayor en lesiones sólidas (5,7% vs 0,1% en
quísticas). La incidencia de apoplejía hipofisaria fue baja (0,2%), ligeramente superior en macroadenomas, aunque no
estadísticamente significativo, y claramente relacionada con crecimientos superiores a 3,5 mm. También se encontró una baja
incidencia de defectos campimétricos en el seguimiento (0,65%), sin diferencias entre macro o micro adenomas, pero sí en
relación con crecimiento significativo de la masa tumoral. El desarrollo de alteraciones hormonales, generalmente
hipopituitarismo, es del orden del 2,4% por año y aunque ligeramente superior en macroincidentalomas, no consigue significación
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 3
estadística.
Evaluación y seguimiento funcional y radiológico
Según lo anteriormente expuesto la evaluación hormonal en el manejo de los incidentalomas hipofisarios, al inicio o durante el
seguimiento, van desde determinaciones aisladas de una o varias hormonas, siguiendo criterios de coste efectividad o de la
sintomatología asociada, hasta una valoración exhaustiva de la función hipotálamo-hipofisaria, que en cualquier caso deviene
obligada en el caso de macroincidentalomas hipofisarios, y siempre dependiendo de la estrategia de tratamiento establecida. Es
importante en esta fase una valoración clínica completa que nos dirija las determinaciones y pruebas funcionales hormonales.
La determinación de los niveles séricos de PRL se recomiendan ante cualquier lesión hipofisaria tanto por la mayor frecuencia de
prolactinomas in vivo y la positividad en estudios post mortem, como siguiendo criterios de coste-efectividad en pacientes
asintomáticos. Asimismo, cobra especial relieve, previo al diagnóstico de prolactinoma, una interpretación cuidadosa de los
resultados de los niveles de prolactina en el contexto de fenómenos de compresión del tallo hipofisario, secundaria a fármacos,
así como fenómenos de interferencia analítica como macroprolactinemia y el efecto gancho.
Para el diagnóstico de sospecha de acromegalia suele ser suficiente una determinación de IGF-1 y en caso necesario se confirma
mediante la supresión de GH tras sobrecarga oral de glucosa. De igual forma, para el diagnóstico un adenoma hipofisario
productor de ACTH tanto el test de supresión con dexametasona o una cortisoluria de 24 horas pueden servir como
procedimientos de despistaje. Especial importancia tienen los estudios hormonales en el diagnóstico del síndrome de Cushing
subclínico o silente, concepto inicialmente basado en la secreción autónoma de origen suprarrenal, ya extrapolado al
microadenoma hipofisario productor de ACTH. Si a todo ello añadimos el desarrollo de procedimientos diagnósticos de
despistaje de alta sensibilidad y especificidad como el cortisol salivar nocturno, esto ha rentabilizado el estudio de enfermedad de
Cushing silente en el contexto de pacientes con diabetes, hipertensión arterial, obesidad, osteoporosis y enfermedad
cardiovascular, o lo que es lo mismo con criterios de síndrome metabólico e incidentaloma hipofisario.
En cuanto al diagnóstico del hipopituitarismo seguimos los procedimientos habituales de análisis de cada uno de los ejes
hormonales con significado clínico, esto es: GH, ACTH-cortisol, gonadotropinas-estrógenos-testosterona y TSH-hormonas
tiroideas. La deficiencia de GH, en adultos, se pone de manifiesto mediante estimulación de la secreción de GH tras hipoglucemia
insulínica con respuestas de GH inferiores a 3 µg/l, u otros estímulos complejos tales como hormona liberadora de GH (GHRH) y
arginina con respuestas de GH inferiores a 9 µg/l, test de glucagón y otros. El diagnóstico de la deficiencia de gonadotropinas se
basa en la presencia de gonadotropinas normales o bajas en sangre asociadas con: amenorrea y bajos niveles de estrógenos en
sangre en mujeres, y en hombres, con valores de testosterona bajos en sangre. La deficiencia de TSH o hipotiroidismo secundario
o terciario se basa en el hallazgo de niveles bajos de tiroxina libre y de TSH.
En cuanto a la deficiencia de ACTH y considerando tanto el ritmo circadiano como el estrés, y en ausencia de valores basales
mayores de 20 μg/dl (500 nmol/l) que la descartan o menores de 4 μg/dl (100 mmol/l) que establecen una deficiencia de cortisol,
en general, se necesitan pruebas dinámicas de confirmación de la deficiencia de ACTH. El test de tolerancia a la insulina o
hipoglucemia insulínica (ITT) para cortisol está considerado como el estándar, aunque no es válido o seguro en todos los
contextos clínicos. Alternativamente, la respuesta de cortisol durante el test corto de Synacthen (250 μg de cosintropina) tiene una
buena correlación con la respuesta observada durante el ITT. Se acepta como valor de corte normal un cortisol sérico superior a
20 μg/dl (500 nmol/l). Recientemente se ha sugerido que la utilización de concentraciones inferiores de cosintropina (1 μg) en un
procedimiento denominado “Test corto de Synacthen de dosis baja” pudiera poner de manifiesto deficiencias subclínicas, hecho
no demostrado mediante la reciente comparación sistemática entre 250 μg y 1μg de Synacthen.
El procedimiento neurorradiológico fundamental en la evaluación inicial y durante el seguimiento de un incidentaloma hipofisario
es la RMN hipofisaria, con o sin contraste, tanto para diferenciar el tipo de lesión y tamaño como la magnitud del crecimiento
tumoral durante el periodo de observación. Los diferentes estudios que han comparado la TAC y la RMN han puesto en evidencia
la superior especificidad de esta última en la evaluación de lesiones hipofisarias principalmente de microadenomas (menores de
10 mm). La TAC del área hipofisaria sigue teniendo un papel como exploración básica neurorradiológica en el diagnóstico inicial
de masas hipofisarias calcificadas como meningiomas y craneofaringiomas y en el estudio del hueso esfenoidal. En
contraposición, la RMN se demuestra ineficaz al diferenciar macroadenomas de otras neoplasias tales como tumores de células
germinales, condrosarcomas, cordomas, gangliocitomas y pituicitomas, entre otros, aunque son de muy baja prevalencia.
Una exhaustiva evaluación visual y neurooftalmológica, mediante la realización de campimetría visual (perimetría), agudeza
visual, potenciales evocados visuales y oculomotora, se devienen fundamentales ante la presencia de macroincidentalomas
sobre todo en lesiones próximas al quiasma óptico o que lo desplazan o comprimen. Es igualmente recomendado ante
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 4
crecimientos significativos de la lesión hipofisaria o las que durante el crecimiento se acercan a las vías visuales o quiasma.
No existen recomendaciones de estudio genético de procesos asociados con tumores hipofisarios en el caso de incidentalomas,
solo el contexto clínico y el estudio familiar orientarán hacia este tipo de análisis. Esto sería el caso de MEN1, o adenomas
hipofisarios familiares.
Estrategia terapéutica y seguimiento
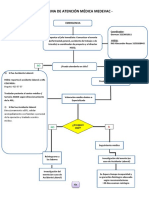
Nuestra propuesta diagnóstica y terapéutica se sintetiza en el algoritmo de la figura 1.
Figura 1. Protocolo de actuación ante un incidentaloma hipofisario. PET: tomografía por emisión de positrones; PRL: prolactina; RMN: resonancia
magnética nuclear; TAC: tomografía axial computarizada.
Las diferentes estrategias tratan de identificar las lesiones que precisan tratamiento en el momento de la presentación
diferenciándolas de aquellas en que la actitud más recomendable es el seguimiento clínico, bioquímico, hormonal y radiológico,
midiendo los parámetros de progresión e identificando los factores de riesgo que nos ayuden a decidir cuándo debemos realizar
una intervención terapéutica. Todo el debate se centra en saber qué lesiones se benefician del tratamiento neuroquirúrgico de
aquellas que tienen un comportamiento benigno y anodino.
El tratamiento, médico y/o neuroquirúrgico, estará indicado en cualquiera de los síndromes clínicos de hipersecreción tumoral,
generalmente identificados en el momento inicial de la presentación. La determinación de PRL, el caso más frecuente de
hipersecreción, identifica a los prolactinomas subsidiarios de tratamiento con agonistas dopaminérgicos. Los niveles de
prolactina suelen ser moderadamente altos en pacientes asintomáticos por lo que debemos siempre diferenciar la
hiperprolactinemia por desconexión, macroprolactinemia y el efecto gancho. En el caso de los raros tumores asintomáticos
productores de GH, aunque el tratamiento primario sigue siendo la exéresis del tumor, la disponibilidad de agentes
farmacológicos eficaces tales como los agonistas somatostatinérgicos e inhibidores del receptor de GH, apuntan al contexto
clínico la decisión terapéutica de cada caso. En el resto de los síndromes de hipersecreción, siempre excepcionales, se impone la
opción neuroquirúrgica y/o radioterapia, como tratamiento primario.
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 5
Aunque es en presencia de macroincidentalomas donde tiene sentido y utilidad clínica la realización de pruebas funcionales que
evidencien un hipopituitarismo, más allá de las determinaciones basales, estudios recientes han dado paso a planteamientos
similares en microincidentaloma, demostrando la presencia de hipopituitarismo y fundamentalmente deficiencia de GH con
relativa frecuencia. Se puede concluir que cualquier lesión hipofisaria, aunque benigna y pequeña, puede derivar en una alteración
de la dinámica hormonal intrahipofisaria que puede originar una insuficiencia hormonal, requiriéndose un alto índice de sospecha
y protocolización en el seguimiento que permitan una detección precoz, evitando una morbilidad y mortalidad, al menos,
teóricamente aumentada. Estos hallazgos plantean cuestiones importantes en relación con las implicaciones de estos procesos
en el riesgo cardiovascular global (Cushing silente, deficiencia de GH e hipopituitarismo) y en la predisposición biológica a la
enfermedad tumoral (estudios genéticos y familiares). En lo que parece existir acuerdo es en la necesidad de evaluar deficiencias
hormonales hipofisarias, por su prevalencia, en presencia de macroadenomas hipofisarios silentes incidentales.
En la deficiencia hormonal e hipopituitarismo, el tratamiento hormonal será el sustitutivo de cada uno de los ejes hormonales
alterados, clínicamente significativos y en función de la edad del individuo. La GH a dosis habituales de 0,2-1 mg/día por vía
subcutánea. La levotiroxina en dosis habitual media de 100 µg/día por vía oral. La testosterona mediante la utilización de las
diferentes formas medicamentosas tales como geles, parches, o parenteral, y mediante los procedimientos de control y
seguimiento clínico habituales. El cortisol generalmente en la forma de hidrocortisona por vía oral en dosis de 15-25 mg/día bid o
tid, como tratamiento crónico y en dosis de 100-50 mg por vía intravenosa dos o tres veces al día durante episodios de estrés
agudo. Los estrógenos y los progestágenos, en período premenopáusico, siguiendo tratamiento secuencial habitual mediante la
dosificación de cualquiera de las formas medicamentosas existentes en el mercado como tratamiento sustitutivo hormonal o
como anticonceptivos orales. La dosificación y el control de efectos secundarios de cada uno de los tratamientos sustitutivos
hormonales se realizarán siguiendo los procedimientos habituales en régimen ambulatorio.
El tamaño y la progresión de la lesión serán los elementos determinantes en la necesidad de un procedimiento neuroquirúrgico
(tabla 2) o sólo tratamiento médico al inicio o durante el seguimiento del paciente. Y esto es así porque el tamaño y progresión
determinan el daño o riesgo de afectación de las vías visuales y el quiasma que representan la racionalidad de la exéresis
quirúrgica y, en menor medida, la disfunción hormonal. El tratamiento quirúrgico consigue, en una proporción significativa de
casos, controlar la masa tumoral, mejorar la clínica y el pronóstico visuales, prevenir una necrosis hemorrágica, recuperar la
función hormonal e incluso establecer un diagnóstico patológico que nos ayude en el tratamiento y pronóstico posterior. Por todo
ello es diferente que nos encontremos ante una lesión de menos de 10 mm, esto es un micro, o una superior o macro, con o sin
invasión o compresión de las estructuras adyacentes. Estamos hablando de tamaños que establecen los estudios
neurorradiológicos.
Tabla 2. Incidentaloma hipofisario: indicaciones y recomendaciones de tratamiento neuroquirúrgico y/o radioterapia
• Alteraciones campimétricas, al inicio o durante el seguimiento, relacionadas con la lesión hipofisaria
• Otras alteraciones neurooftalmológicas relacionadas con lesión hipofisaria
• Lesión que contacta, comprime o desplaza quiasma o vías ópticas
• Apoplejía hipofisaria con compromiso visual o clínica neurológica relacionada
• Síndromes de hipersecreción con indicación quirúrgica
• Tamaño mayor de 2 cm (recomendación algunos autores)
• Crecimiento significativo durante seguimiento (recomendación)
• Invasión de seno cavernoso (neurocirugía vs radioterapia)
• Hipofunción hormonal parcial o total de una o varios ejes al inicio o durante el seguimiento (algunos autores)
• Cefalea persistente, probable relación con lesión (recomendación)
• Tumor próximo a quiasma y programación de embarazo (recomendación)
Lesiones menores de 10 mm o microincidentalomas
En ausencia de signos clínicos que sugieran disfunción hormonal se recomienda la realización de RMN de área-hipotálamo
hipofisaria en un año y posteriormente cada 1-2 años durante los primeros 3 años. La racionalidad de un seguimiento posterior se
basará en criterios clínicos dada la ausencia de estudios prospectivos a largo plazo. Se recomienda tratamiento ante un
crecimiento significativo de la masa tumoral. Igualmente se recomienda tratamiento ante una disfunción hormonal que se
manifieste durante el seguimiento. En general, no se recomienda, durante el seguimiento, una valoración de función hipofisaria,
ante un microincidentaloma que no cambia de tamaño con el tiempo y en ausencia de clínica sugestiva.
Lesiones ≥ 10 mm
En presencia de alteraciones hormonales el tratamiento será el específico de cada uno de los síndromes de hipersecreción e
hipopituitarismo. En general, son indicaciones de tratamiento neuroquirúrgico cuando existen alteraciones campimétricas u otras
neurooftalmológicas relacionadas con la lesión hipofisaria y cuando el tumor contacta, desplaza o comprime el quiasma o las
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 6
vías ópticas. También se indica en la apoplejía hipofisaria con clínica visual y neurológica relacionadas. Ante tumores clínica y
hormonalmente silentes superiores a 20 mm algunos autores recomiendan tratamiento neuroquirúrgico de entrada ya que han
demostrado su potencialidad de crecimiento. Son igualmente recomendaciones de tratamiento crecimientos significativos del
tumor, la aparición de nuevos defectos hormonales, la planificación de un embarazo en una lesión de riesgo o incluso la cefalea
severa persistente y relacionada con el tumor. Si el tamaño o la clínica no indican su exéresis, una actitud expectante con
evaluación radiológica mediante RMN cada 6 meses el primer año y posteriormente cada año durante 3 a 5 años, unido a una
valoración hormonal y neurooftalmológica serán los elementos de guía y orientación terapéutica. De los datos publicados no
podemos deducir cuánto tiempo debemos mantener el seguimiento, aunque se ha sugerido periodos de hasta 22 años, que es el
tiempo de observación de crecimiento de algunas lesiones y siempre en series limitadas en número. Al igual que en el caso de los
micro, y con iguales criterios indicativos de progresión, un crecimiento significativo de la masa tumoral, el contacto o compresión
del quiasma, la aparición de defectos campimétricos y de agudeza visual, incluso nuevas deficiencias hormonales pueden indicar
la neurocirugía.
Debemos también considerar la radioterapia, convencional o radiocirugía estereotáxica según los casos, por razones de edad,
riesgo quirúrgico significativo, o ante un crecimiento lateral con invasión del seno cavernoso sin riesgo visual. El control de la
masa tumoral se consigue, pero aumenta el riesgo de hipopituitarismo posterior. El tumor asintomático sin riesgo de afectación
visual puede admitir un periodo de prueba de tratamiento farmacológico, con agentes dopaminérgicos o análogos de
somatostatina asumiendo que menos de un 20% responderán parcialmente. No hay evidencia suficiente para recomendar el
tratamiento farmacológico como alternativa de tratamiento en este tipo de lesiones.
SILLA TURCA VACÍA
Concepto y clasificación
Una silla turca vacía (SV) se refiere a un aumento del tamaño de la silla turca, total o parcialmente ocupada por líquido
cefalorraquídeo (LCR) por herniación del espacio subaracnoideo, con ausencia casi total o parcial de tejido hipofisario. Es una
entidad morfológica detectada en el curso de una exploración radiológica hipotálamo-hipofisaria en el contexto de un paciente,
que al contrario que el incidentaloma hipofisario, se presenta con o sin clínica de disfunción hormonal y/o neurooftalmológica. Es
una entidad presente entre el 6% y el 23% de las autopsias no seleccionadas y, por tanto, frecuente, que suele permanecer
asintomática durante la vida del individuo. Se estima una prevalencia entre el 8% y el 35% de la población adulta. Se clasifica
generalmente como primaria o secundaria. También podemos distinguir una SV parcial con menos del 50% de ocupación del
espacio sellar con LCR o SV completa con una ocupación de LCR por encima del 50% y un grosor de remanente glandular menor
de 2 mm.
La SV secundaria es una SV observada al inicio o en el curso de una enfermedad hipofisaria conocida o probable, generalmente
tumoral, inflamatoria, vascular, autoinmune o traumática que sufre un proceso de involución espontánea o tras tratamiento
médico, quirúrgico o radioterápico y en dónde previamente se habría ocasionado una lesión generalmente expansiva sellar en
relación con la patología de base conocida o sospechada con involución posterior.
La SV primaria presente en el paciente sin sospecha o presunción previas de lesión hipofisaria, entidad a la que dedicamos la
presente revisión, se denomina síndrome de la silla turca vacía (SSV), en la que una incompetencia del diafragma sellar, congénito
o adquirido, y/o un aumento de la presión intracraneal se sitúan en el origen probable del proceso. Las series publicadas de SSV
reconocen que en muchos pacientes no se ha podido determinar la presión intracraneal ni se ha podido descartar causa
secundaria de manera fehaciente permaneciendo el proceso como un hallazgo ante una exploración neurorradiológica por otras
razones o en el estudio de hipopituitarismo generalmente parcial.
Etiopatogenia y factores de riesgo
El SSV es una entidad heterogénea y, por tanto, existe controversia en cuanto a su patogénesis. Estudios recientes, basándose en
la incidencia de alteraciones en diafragma sellar que se aproxima al 100% cuando existe SSV, concluyen que una alteración en el
diafragma sellar, congénito o adquirido y por supuesto no conocido, es una condición necesaria, pero no suficiente en la
instauración de una SSV y, en consecuencia, el aumento en la presión intracraneal o alteraciones en la propia glándula hipofisaria
se postulan también como factores en este proceso. Los hallazgos de que un aumento en la presión intracraneal (HTIC) o
alteración en la dinámica del LCR, continua o intermitente, detectada en el 60-80% en la series de SSV y de una asociación de esta
última en presencia de HTIC benigna o pseudotumor cerebri, hidrocefalia, tumores cerebrales y malformación de Arnold-Chiari,
demuestran el papel predominante de la HTIC.
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 7
El tercer factor, hipofisario, postula que la involución brusca que sigue a un aumento en el volumen hipofisario que ocurre en
situaciones fisiológicas, por ejemplo, embarazo, o patológicas, por ejemplo, hipotiroidismo primario, en presencia de alteraciones
en el diafragma selar pueden, teóricamente, originar un proceso de estas características.
Desde un punto de vista epidemiológico es más frecuente en mujeres (relación 4:1), con un pico de incidencia entre los 40 y 50
años, y con sobrepeso u obesidad. Se han buscado otras asociaciones como son la presencia de enfermedades autoinmunes
como tiroiditis crónica, ya que el daño autoinmune hipofisario pudiera ser la causa teórica en ciertos casos, aunque muy difícil de
demostrar. Los factores epidemiológicos se han relacionado con la patogénesis (embarazo) y en el caso de la obesidad al papel
que la retención de carbónico puede tener en la génesis de HTIC, sin embargo, series recientes atribuyen un papel marginal a la
obesidad mórbida. Igualmente la presencia de diabetes mellitus tipo 2, hipertensión arterial y algunos fármacos se han asociado
con esta entidad.
Cuadro clínico neurooftalmológico y funcional
La complejidad de la expresión clínica del SSV dificulta la diferenciación entre lo que son síntomas que motivan una exploración
neurorradiológica inicial o los que se evidencian dentro del estudio del SSV. La clínica neurológica que suele derivar en una
exploración neurorradiológica incluye cefalea, variable en el curso y en la intensidad como sintomatología más frecuente, mareo,
vértigo, alteraciones de pares craneales con o sin síntomas visuales o diplopía y ocasionalmente papiledema. Las alteraciones
visuales resultado del prolapso o compresión del quiasma o nervios ópticos, se describen entre el 1,6% y el 16% de los casos de
SSV, siendo una indicación del tratamiento quirúrgico. La importancia de la rinorrea espontánea de LCR, detectada en el 6,5% de
SSV, siguiendo la serie más amplia, radica en ser una indicación, igualmente, de tratamiento quirúrgico dado el riesgo de
meningitis asociada, alta incidencia de recidiva posterior y sirve de base fisiopatológica de la existencia de HTIC.
El rango del cuadro clínico endocrinológico va desde un individuo completamente asintomático hasta síndromes de hiperfunción
e hipopituitarismo. También la clínica característica y su transcendencia varían en función de la edad del individuo. En el paciente
pediátrico, la presencia de una SV está generalmente asociada con síndromes de hipofunción (plurihormonales) y de causa
congénita. Esto implica que el SSV en este rango de edad requiere siempre un estudio exhaustivo hormonal funcional y genético.
Entre los síndromes de hiperfunción, la presencia de hiperprolactinemia, de grado moderado, sintomática o asintomática, hayan
motivado la exploración radiológica o aparecido durante el estudio del síndrome, ocurre en un 10% de los pacientes con SSV
siendo la alteración endocrinológica más frecuente. El diagnóstico de hipopituitarismo puede tener lugar en el contexto de un
cuadro de presentación aguda de deterioro del estado general o de la enfermedad de base del paciente con anemia e
hiponatremia que cede tras tratamiento con corticoides y hallazgos radiológicos de SV. Sin embargo, es más frecuente que una o
varias deficiencias hormonales se pongan de manifiesto tras la realización de las pruebas hormonales basales o dinámicas
hipofisarias. Entre los ejes hormonales alterados la deficiencia de GH es el más frecuente que puede llegar hasta el 65% de SSV,
según las series, representando la deficiencia de ACTH, gonadotropinas, TSH e incluso hormona antidiurética en menos del 5% de
los pacientes.
Evaluación clínica
El diagnóstico inicial mediante TAC del área hipotálamo hipofisaria suele requerir confirmación y exclusión de patología
subyacente mediante RMN. Pueden coexistir SV y un microadenoma hipofisario.
Un estudio campimétrico y neurooftalmológico se requiere en pacientes con trastornos visuales, campimétricos o de agudeza
visual relacionados, en el diagnóstico o durante la evolución, así como en los casos de imagen radiológica de compresión u
herniación de las vías visuales. Adquiere especial relevancia el diagnóstico de rinorrea de LCR detectado mediante la
determinación de glucosa, proteínas o electrolitos o más específicamente β-2 transferrina u otros marcadores específicos en
fosas nasales. La localización del defecto en la base del cráneo origen de la rinorrea se lleva a cabo mediante TAC de alta
definición o cisternografía mediante TAC, RMN o radiotrazadores. En ciertos pacientes el diagnóstico de localización sólo se
obtiene intraoperatoriamente.
No existe suficiente evidencia de que, en el paciente asintomático, requiera una evaluación endocrinológica exhaustiva. Sin
embargo, se recomienda una determinación de prolactina y la realización de determinaciones basales que excluyan la presencia
de hipopituitarismo. Es evidente que una clínica endocrinológica aguda o crónica dirigirá al clínico en la realización de las pruebas
especificas, basales o funcionales, que permitan descartar la presencia de síndromes de hiperfunción y fundamentalmente de
hipofunción, incluido, por su frecuencia en este proceso, el déficit de hormona del crecimiento, siguiendo lo expuesto previamente
para el caso del incidentaloma hipofisario. Mención especial merece la hiponatremia aguda como clínica de presentación de una
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 8
insuficiencia hipofisaria o específicamente de ACTH, que en su estudio aparece una imagen de SV en RMN del área hipotálamo-
hipofisaria.
Tratamiento
La mayoría de los pacientes con SSV requieren un estudio inicial y un seguimiento clínico, bioquímico y hormonal y radiológico
que justifiquen una intervención terapéutica. Las opciones de tratamiento se dirigen a las alteraciones endocrinológicas
hipofisarias, así como aquellas cuyo objetivo es una corrección quirúrgica de las alteraciones neurooftalmológicas.
El tratamiento hormonal será el sustitutivo y el de los síndromes de hiperfunción. En el tratamiento de la hiperprolactinemia
sintomática (amenorrea, galactorrea, disfunción eréctil) se sigue la pauta habitual en cuanto a la indicación primaria y utilización
de los agonistas dopaminérgicos. También incluimos la acetazolamida, topiramato, metazolamida y los corticoides como
opciones de tratamiento médico para el control de la presión intracraneal y de la clínica compresiva sobre vías visuales.
El tratamiento quirúrgico está indicado en pacientes con rinorrea de LCR, papiledema, cefalea severa que no responde a
tratamiento conservador y alteraciones visuales severas o progresivas, en los casos en que se demuestra alteraciones en la
presión y dinámica del LCR o signos radiográficos evidentes de herniación del quiasma óptico en silla turca asociado con
alteraciones visuales instauradas y progresivas. Son varias las opciones de tratamiento quirúrgico. En primer lugar, la colocación
de una válvula de derivación de LCR en los casos que se demuestra HTIC y/o rinorrea. Otras técnicas referidas como
quiasmapexia que se refieren a fijación del quiasma o las vías ópticas mediante el relleno de la cavidad de la silla turca con grasa,
fascia, implantes de silastic u otros materiales. Variedades quirúrgicas de relleno de silla turca han recibido diferentes nombres
como remodelación selar o aracnoidopexia. La descompresión o reparación quirúrgica directa requieren, generalmente, la
asociación de técnicas derivativas de LCR dado la alta incidencia de recidiva.
Bibliografía
1. Buurman H, Saeger W. Subclinical adenomas in postmortem pituitaries: classification and correlations to clinical data. Eur J
Endocrinol. 2006;154:753-758.
2. De Marinis L, Bonadonna S, Bianchi A, Maira G, Giustina A. Primary empty sella. J Clin Endocrinol Metab. 2005;90:5471-5477.
3. Fernández-Balsells MM, Murad MH, Barwise A, Gallegos-Orozco JF, Paul A, Lane MA, et al. Natural history of nonfunctioning
pituitary adenomas and incidentalomas: a systematic review and metaanalysis. J Clin Endocrinol Metab. 2011;96:905-12.
4. Freda PU, Beckers AM, Katznelson L, Molitch ME, Montori VM, Post KD, et al. Pituitary incidentaloma: an endocrine society
clinical practice guideline. J Clin Endocrinol Metab. 2011;96:894-904.
5. Giustina A, Aimaretti G, Bondanelli M, Buzi F, Cannavo S, Cirillo S, et al. Primary empty sella: Why and when to investigate
hypothalamic-pituitary function. J Endocrinol Invest. 2010;33:343-346.
6. Hyun SH, Choi JY, Lee KH, Choe YS, Kim BT. Incidental focal 18F-FDG uptake in the pituitary gland: clinical significance and
differential diagnostic criteria. J Nucl Med. 2011;52:547-550.
7. Losa M, Donofrio CA, Barzaghi R, Mortini P. Presentation and surgical results of incidentally discovered nonfunctioning
pituitary adenomas: evidence for a better outcome independently of other patients’ characteristics. Eur J Endocrinol.
2013;169:735-742.
8. Molitch ME. Management of incidentally found nonfunctional pituitary tumors. Neurosurg Clin N Am. 2012;23:543-553.
9. Raappana A, Koivukangas J, Ebeling T, Pirila T. Incidence of pituitary adenomas in Northern Finland in 1992-2007. J Clin
Endocrinol Metab. 2010; 95:4268-4275.
10. Yuen KC, Cook DM, Sahasranam P, Patel P, Ghods DE, Shahinian HK, et al. Prevalence of GH and other anterior pituitary
hormone deficiencies in adults with nonsecreting pituitary microadenomas and normal serum IGF-1 levels. Clin Endocrinol
(Oxf). 2008;69:292-298.
ec-europe - ISBN 978–84–606–8570–8 - 11/02/2022 9
También podría gustarte
- Simposio II ParteDocumento22 páginasSimposio II ParteJonathan David Dionicio Chun100% (1)
- Tumores Hipofisiarios y Casos ClinicosDocumento70 páginasTumores Hipofisiarios y Casos ClinicosCecilia CóndorAún no hay calificaciones
- Prolactina - RMDocumento11 páginasProlactina - RMAlex PomaAún no hay calificaciones
- Patologias Del Hipotalamo y Cuarto VentriculoDocumento9 páginasPatologias Del Hipotalamo y Cuarto VentriculoAnthonny MoyaAún no hay calificaciones
- Caso clínico de tumoración tiroideaDocumento7 páginasCaso clínico de tumoración tiroideaJesús Aguirre ReyesAún no hay calificaciones
- Art 5Documento7 páginasArt 5pepe pipaAún no hay calificaciones
- Adenomas Hipofisiario Cuadro ResumenDocumento2 páginasAdenomas Hipofisiario Cuadro ResumenAngelo PeraltaAún no hay calificaciones
- Adenomas HipofisiariosDocumento16 páginasAdenomas HipofisiariosetcAún no hay calificaciones
- FEOCROMOCITOMADocumento12 páginasFEOCROMOCITOMAAnarelysAún no hay calificaciones
- Patología Quirúrgica de La Glándula TiroidesDocumento6 páginasPatología Quirúrgica de La Glándula TiroidesBañuelos NormaAún no hay calificaciones
- Craneofaringioma 01Documento6 páginasCraneofaringioma 01Gustavo Gonzalez CabreraAún no hay calificaciones
- AHPF: los tumores más frecuentes de la región selarDocumento7 páginasAHPF: los tumores más frecuentes de la región selarEmilio MaslucanAún no hay calificaciones
- Cancer de Tiroides PDFDocumento12 páginasCancer de Tiroides PDFScarlett OlmedoAún no hay calificaciones
- CAP29Documento42 páginasCAP29Mayra Alejandra Posada SuarezAún no hay calificaciones
- Revision FeocromoDocumento7 páginasRevision FeocromoRose YuleidiAún no hay calificaciones
- 3891-Texto Del Artículo-3795-1-10-20211115Documento21 páginas3891-Texto Del Artículo-3795-1-10-20211115Drdionisio TeleradAún no hay calificaciones
- Nódulo TiroideoDocumento6 páginasNódulo TiroideoEmma ReutemannAún no hay calificaciones
- Preguntas Proyecto SPNDocumento14 páginasPreguntas Proyecto SPNHuang Shan Lin100% (1)
- Complicaciones Post Operatorias en La Tiroidectomía Total Por Bocio Multinodular en El Instituto Nacional Del CáncerDocumento13 páginasComplicaciones Post Operatorias en La Tiroidectomía Total Por Bocio Multinodular en El Instituto Nacional Del CáncerMdacAún no hay calificaciones
- Feocromocitoma Nathalie Borbor G4Documento4 páginasFeocromocitoma Nathalie Borbor G4Joffre LavidAún no hay calificaciones
- Adenoma HipofisiarioDocumento5 páginasAdenoma HipofisiarioLolita GonzalezAún no hay calificaciones
- Adenomas Hipofisarios FuncionantesDocumento12 páginasAdenomas Hipofisarios FuncionantesCARLOS DANIEL GALLO VELASCOAún no hay calificaciones
- Hipopituitarismo. PanhipopituitarismoDocumento9 páginasHipopituitarismo. PanhipopituitarismoAndrés SeguraAún no hay calificaciones
- Nodulos TiroideosDocumento5 páginasNodulos TiroideosMaricris_85100% (1)
- Tumores HipofisiariosDocumento55 páginasTumores HipofisiariosCruz Garcia JesusAún no hay calificaciones
- Seminario N°3 - Neoplasias Endocrinas MúltiplesDocumento19 páginasSeminario N°3 - Neoplasias Endocrinas MúltiplesTony Vicent EulogioAún no hay calificaciones
- Paragangliomas de Cabeza y CuelloDocumento3 páginasParagangliomas de Cabeza y CuelloDaniela Tapia100% (1)
- Tiroides Cancer PDFDocumento10 páginasTiroides Cancer PDFpedromejiaquevedoAún no hay calificaciones
- ECOGRAFIA-TIROIDES-PARATIROIDESDocumento7 páginasECOGRAFIA-TIROIDES-PARATIROIDESKARINA MIRANDA RIVERAAún no hay calificaciones
- TRADUCCIONDocumento28 páginasTRADUCCIONEzZ ScaReCroWAún no hay calificaciones
- Tumores de HipófisisDocumento7 páginasTumores de HipófisisJorge Carlos Rodriguez CanteroAún no hay calificaciones
- Enfoque Del Paciente Con Nodulo Tiroideo. A Propósito de Un Caso ClínicoDocumento4 páginasEnfoque Del Paciente Con Nodulo Tiroideo. A Propósito de Un Caso ClínicoJuan Pablo Illanes CastroAún no hay calificaciones
- Seminario de CitologiaDocumento27 páginasSeminario de Citologiaori rodriguezAún no hay calificaciones
- 10-Protocolo Diagnóstico Del Nódulo TiroideoDocumento4 páginas10-Protocolo Diagnóstico Del Nódulo TiroideoCerdocristoAún no hay calificaciones
- Tumores Neuroendocrinos de PancreasDocumento9 páginasTumores Neuroendocrinos de PancreasKarla Paola Sandoval TorresAún no hay calificaciones
- Patologia Del Sistema EndocrinoDocumento40 páginasPatologia Del Sistema EndocrinoRene Alexander Villalta VelasquezAún no hay calificaciones
- Gammagrafia Con Sup 99m Sup TC Sestamibi en Hiperparatiroidismo Con Diagnostico Histologico de Carcinoma de ParatiroidesDocumento3 páginasGammagrafia Con Sup 99m Sup TC Sestamibi en Hiperparatiroidismo Con Diagnostico Histologico de Carcinoma de ParatiroidesRuben Darío Rojas MuñozAún no hay calificaciones
- 02.018 Cáncer de TiroidesDocumento12 páginas02.018 Cáncer de TiroidesGustavo AraujoAún no hay calificaciones
- Plasmocitoma Extramedular en Otorrinolaringología: ENT Extramedullary PlasmocytomaDocumento8 páginasPlasmocitoma Extramedular en Otorrinolaringología: ENT Extramedullary PlasmocytomaKarla Quijije MeroAún no hay calificaciones
- Cirugía Endocrino. Tema 2Documento12 páginasCirugía Endocrino. Tema 2María MeryAún no hay calificaciones
- Sem. 13 Cancer de TiroidesDocumento42 páginasSem. 13 Cancer de Tiroidesfiorella alexandra vasquez perezAún no hay calificaciones
- Acromegalia y GigantismoDocumento9 páginasAcromegalia y GigantismoGabriel Enrique Giler ReyesAún no hay calificaciones
- Caso Clínico Patologico Nro 8Documento4 páginasCaso Clínico Patologico Nro 8Michael Asto EstebanAún no hay calificaciones
- Neuroblastoma ArticuloDocumento4 páginasNeuroblastoma ArticuloHUGO CÉSAR YAÑEZ BALDERASAún no hay calificaciones
- Nodulo TiroideoDocumento4 páginasNodulo TiroideoAnia SoToAún no hay calificaciones
- Revisión FeocromocitomaDocumento16 páginasRevisión FeocromocitomaEnyel Ángel MirandaAún no hay calificaciones
- Sindromes ParaneoplasicosDocumento10 páginasSindromes ParaneoplasicosenriqueAún no hay calificaciones
- Carcinoides PulmonaresDocumento20 páginasCarcinoides PulmonaresJuan DupouyAún no hay calificaciones
- Bocio Nodular InformeDocumento8 páginasBocio Nodular InformeCinthia ChalacoAún no hay calificaciones
- Tumores Paratesticulares ModificadoDocumento2 páginasTumores Paratesticulares ModificadoSara NuñezAún no hay calificaciones
- Carcinoma Papilar Tiroideo Con Met Stasis Osteol Ti 2016 Medicina General yDocumento5 páginasCarcinoma Papilar Tiroideo Con Met Stasis Osteol Ti 2016 Medicina General yhricaabiAún no hay calificaciones
- Ca TesticularDocumento8 páginasCa Testiculark95mf8rvjpAún no hay calificaciones
- Enfermedad Trofoblástica GestacionalDocumento6 páginasEnfermedad Trofoblástica GestacionalJonathan FabianAún no hay calificaciones
- Prevalencia E Incidencia de Los Principales Trastornos Endocrinos Y MetabólicosDocumento7 páginasPrevalencia E Incidencia de Los Principales Trastornos Endocrinos Y MetabólicosmiguelalmenarezAún no hay calificaciones
- FeocromocitomaDocumento13 páginasFeocromocitomaJorge NuñezAún no hay calificaciones
- CA TiroidesDocumento42 páginasCA TiroidesRamiro Apata EscalanteAún no hay calificaciones
- Libro HematologiaDocumento251 páginasLibro HematologiaSilvana VelazquezAún no hay calificaciones
- Fundamentos del diagnóstico y tratamiento del cáncer en adultos: Una aproximación inicial para el médico no especialista en cáncerDe EverandFundamentos del diagnóstico y tratamiento del cáncer en adultos: Una aproximación inicial para el médico no especialista en cáncerAún no hay calificaciones
- Enfermedades sistémicas en el consultorio odontológico: Conocimientos básicos odontológicos, #3De EverandEnfermedades sistémicas en el consultorio odontológico: Conocimientos básicos odontológicos, #3Calificación: 5 de 5 estrellas5/5 (1)
- EUTIRADSDocumento7 páginasEUTIRADSJulieta GarridoAún no hay calificaciones
- Guías 2019 DislipidemiasDocumento70 páginasGuías 2019 DislipidemiasMariana SgAún no hay calificaciones
- TiroiditisDocumento18 páginasTiroiditisJulieta GarridoAún no hay calificaciones
- Hipotiroidismo: causas, síntomas y tratamientoDocumento14 páginasHipotiroidismo: causas, síntomas y tratamientoJulieta GarridoAún no hay calificaciones
- OsteoporosisDocumento11 páginasOsteoporosisJulieta GarridoAún no hay calificaciones
- Cardio MetabólicoDocumento261 páginasCardio MetabólicoJulieta GarridoAún no hay calificaciones
- Art RosisDocumento9 páginasArt RosisJulieta GarridoAún no hay calificaciones
- Anti ConcepcionDocumento2 páginasAnti ConcepcionJulieta GarridoAún no hay calificaciones
- Consejo ContraconceptivoDocumento7 páginasConsejo ContraconceptivoJulieta GarridoAún no hay calificaciones
- Cardio PrimariaDocumento171 páginasCardio PrimariaJulieta GarridoAún no hay calificaciones
- Cartera de Servicios de Salud de Complejidad CrecienteDocumento25 páginasCartera de Servicios de Salud de Complejidad CrecientepersegAún no hay calificaciones
- PAE TB MiliarDocumento18 páginasPAE TB MiliarMiriam ColqueAún no hay calificaciones
- Presentación1 JulyDocumento26 páginasPresentación1 JulyDulce Maria de LaraAún no hay calificaciones
- ESCABIASISDocumento17 páginasESCABIASISLluvia Neftaly EstradaAún no hay calificaciones
- Ejemplo de Queja Ante Ministerio de Salud (Hospital)Documento3 páginasEjemplo de Queja Ante Ministerio de Salud (Hospital)TechData Ciudad SandinoAún no hay calificaciones
- Infografia Actividad FisicaDocumento1 páginaInfografia Actividad FisicaLuisa CifuentesAún no hay calificaciones
- Obstetricia CriticaDocumento7 páginasObstetricia CriticaRosy ZapataAún no hay calificaciones
- S1M4C2y3 Podo R PDFDocumento122 páginasS1M4C2y3 Podo R PDFGerardo LopezAún no hay calificaciones
- Tuberculosis pleural: frecuencia, manifestaciones clínicas y métodos diagnósticosDocumento6 páginasTuberculosis pleural: frecuencia, manifestaciones clínicas y métodos diagnósticosMariann BarahonaAún no hay calificaciones
- AIEPI LibroClinico201120octubreDocumento572 páginasAIEPI LibroClinico201120octubreEdisson Rodriguez0% (1)
- Carta Gantt Protocolos MINSALDocumento11 páginasCarta Gantt Protocolos MINSALjonathan diazAún no hay calificaciones
- Por Qué Las Falsas Terapias Parecen FuncionarDocumento9 páginasPor Qué Las Falsas Terapias Parecen FuncionarJoaquinAún no hay calificaciones
- Infecciones de Transmision SexualDocumento4 páginasInfecciones de Transmision SexualJOEL XILOJAún no hay calificaciones
- Manual ENF MAT INF P. Estudiante 2 Correcciòn Por Comite de Calidad P PDFDocumento149 páginasManual ENF MAT INF P. Estudiante 2 Correcciòn Por Comite de Calidad P PDFJames Owen Sullivan.Aún no hay calificaciones
- ACV isquémico: caso clínico de 38 añosDocumento28 páginasACV isquémico: caso clínico de 38 añosCristobal Valencia100% (1)
- Infografico Fiebre Niños CinfasaludDocumento1 páginaInfografico Fiebre Niños Cinfasaludassarath1Aún no hay calificaciones
- Fase 5 - MelissaDiaz - Grupo 6Documento10 páginasFase 5 - MelissaDiaz - Grupo 6Lith PadillaAún no hay calificaciones
- Deberes y DerechosDocumento22 páginasDeberes y DerechosSARA ANGELICA RIVADENEIRA ARIASAún no hay calificaciones
- Ductus Arterioso Persistente PDFDocumento9 páginasDuctus Arterioso Persistente PDFRoberto TejedaAún no hay calificaciones
- Pets Desmontaje y Montaje de Monoriel y Columnas de Viga HDocumento11 páginasPets Desmontaje y Montaje de Monoriel y Columnas de Viga HWilfredo Jose Nuñez RojoAún no hay calificaciones
- Maduración CervicalDocumento6 páginasMaduración CervicaljapibluaniAún no hay calificaciones
- Seminario 7.daniel Mendoza QuispeDocumento9 páginasSeminario 7.daniel Mendoza Quispemanchaluna0% (1)
- Tema 2 - Aislamiento Dental AbsolutoDocumento16 páginasTema 2 - Aislamiento Dental Absolutopaco ruizAún no hay calificaciones
- Universidad Católica de Santa María: Facultad de Obstetricia Y PuericulturaDocumento10 páginasUniversidad Católica de Santa María: Facultad de Obstetricia Y PuericulturaAriana TejadaAún no hay calificaciones
- (CRISTAL) Cartilla Esmeralda161023Documento21 páginas(CRISTAL) Cartilla Esmeralda161023Alberto Montes De OcaAún no hay calificaciones
- PLANILLA DE METRADOS CovidDocumento5 páginasPLANILLA DE METRADOS CovidMagno Alberto Araujo JamancaAún no hay calificaciones
- NANDA, Nic, NocDocumento4 páginasNANDA, Nic, Nocluz.adri7Aún no hay calificaciones
- 01 - Medevac - Proyecto BogotaDocumento1 página01 - Medevac - Proyecto BogotaAlexaander ReyesAún no hay calificaciones
- XILACINADocumento6 páginasXILACINAMario Gaitán Santana0% (1)
- El Arte y La Ciencia en La AnamnesisDocumento7 páginasEl Arte y La Ciencia en La AnamnesisLucero FloresAún no hay calificaciones