Documentos de Académico
Documentos de Profesional
Documentos de Cultura
LC3. Chaperonas
Cargado por
Camila Belen LazoDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
LC3. Chaperonas
Cargado por
Camila Belen LazoCopyright:
Formatos disponibles
Chaperonas moleculares como elementos reguladores de las redes celulares
Molecular chaperones as regulatory elements of cellular networks
Csaba So˝ ti, Csaba Pa, Bala´ zs Papp y Peter Csermely. Current Opinion in Cell Biology 2005, 17:210–215
Las chaperones ayudan a cientos de moléculas señal a mantenerse activas y en estado competente, regulan diversos
procesos que van desde la señalización en la membrana plasmática hasta la transcripción. Además de estos roles
específico, estudios recientes han revelado que actúan como reguladores genéticos que estabilizan los fenotipos de las
células. Esto puede estar relacionado con su baja afinidad por las proteínas con que interactúan, lo que significa que
representan eslabones débiles en las redes de proteínas. Las chaperonas pueden desacoplar proteínas de señalización,
de membrana, organelas y redes transcripcionales durante el estrés, lo que da a la célula protección adicional. Las
mismas redes son remodeladas en diversas enfermedades y en el envejecimiento, por lo que pueden ayudar a diseñar
nuevas estrategias terapéuticas y anti-envejecimiento.
Introducción
El término de 'Chaperonas moleculares' se refiere a una gran familia de proteínas que abundan en todas partes de la
célula y que forman un antiguo sistema de defensa de nuestras células. Las chaperonas promueven la supervivencia de
la célula debido a que secuestran células dañadas y previenen su agregación. En condiciones de estrés, como un
aumento de la temperatura, evitan la agregación de proteínas al facilitar el replegamiento o la eliminación de proteínas
mal plegadas. La respuesta al estrés inducida por daños a proteínas, induce la síntesis de varias chaperonas y otras
proteínas promotoras de supervivencia, es un sistema regulador sofisticado, que abarca varias funciones celulares en
paralelo. Por lo tanto, muchas de las chaperones se conocen como proteínas de estrés o "choque térmico" en referencia
al arquetipo de estrés celular, el choque térmico. Además de su papel durante el estrés, las chaperonas tienen múltiples
funciones en condiciones normales. Promueven el transporte de macromoléculas (por ejemplo, proteínas o ARN) y
participar en casi todos los eventos de remodelación que implica grandes complejos de proteínas, incluida la
señalización celular, transcripción, división, migración, diferenciación, etc. Las multiples funciones de las chaperonas ha
agrandado el término, ahora se utiliza para describir casi cualquier proteína (o ARN) que transitoriamente acompaña a
otras moléculas y promueve su transporte o el montaje de grandes complejos. Así se han descripto chaperonas de ARN,
iones y lípidos. Algunas chaperonas están especializadas en una única proteína o en una pequeña clase de proteínas,
como las chaperonas de catenina, colágeno, el complejo principal de histocompatibilidad, miosina y otros. El término de
'Chaperona intramoleculares” se ha acuñado para los segmentos de proteínas que ayudan al plegamiento del resto de
las proteína. Además, los compuestos pueden ser pequeños y se denominan "chaperonas químicas ', y se utilizan en
prácticas clínicas para curar enfermedades de falta de plegamiento de proteínas.
Las chaperonas de proteínas tienen múltiples sustratos y en su mayoría tienen baja afinidad, forman interacciones
dinámicas y temporales (enlaces débiles) en las redes celulares. Dado que las chaperonas tienen generalmente un gran
número de socios, se comportan como centros de conexiones en redes de interacción proteína-proteína.
Además, muchos efectos chaperona (por ejemplo, la supervivencia celular o cambios en la diversidad fenotipo) son
propiedades integradoras típicas, que rara vez pueden ser comprendidos por el estudio individual de las interacciones
exclusivamente. Así, el enfoque de red es una herramienta prometedora para explicar algunos aspectos clave de la
función de las chaperonas. Se pondrá de relieve varias conexiones posibles entre contactos de chaperonas individuales
de proteínas y redes celulares, se explicará cómo algunos aspectos de la red se pueden utilizar para comprender las
propiedades de integración de regulación mediada por chaperonas. Por último, vamos a mostrar cómo el enfoque de
red está ligado a estrategias terapéuticas y anti-envejecimiento relacionadas a chaperonas.
Chaperonas y las redes celulares
Las Chaperonas formar grandes complejos y tienen un gran número de co-chaperonas para regular su actividad, sus
propiedades y su función de unión. Estos complejos de chaperona regulan las redes locales de proteínas, tales como la
proteína del aparato de transporte y montaje mitocondrial, la especificidad de sustrato del principal sistema
citoplásmico proteolítico, el proteosoma.
Chaperonas y la señalización, redes y organelos
Las principales chaperona reguladoras de redes celulares están relacionadas con las señales de membrana y la
transcripción. Se ha propuesto el término de “señalosoma” al conjunto de elementos que participan de la señalización,
las chaperonas pueden ser elementos importantes en la promoción de la coordinación de los diferentes procesos. El
complejo chaperona Hsp90 promueve la maduración de los sustratos de la proteína quinasa, incluyendo varios
miembros de la vía de señalización relacionada las proteínas Raf-1, con proteínas que participan de la apoptosis, con las
señales que detienen la proliferación celular, en particular la Hsp70 (proteína de choque) (Figura 1). Otra función
conocida mediada por chaperonas vía de señalización, es la activación de la sintasa de óxido nítrico, esta enzima actúa
sobre complejos asociados a balsas lipídicas que contiene Hsp90 (90-kDa proteína de choque térmico) y a quinasa Akt
(proteína quinasa B) y calmodulina. La formación de este complejo es ayudado por las estatinas, hoy se están usando
estas como drogas anti-ateroscleróticas. La proteína Rab es una pieza clave en la exocitosis dependiente de Ca, y
también está regulada por las Hsp90 y Hsp70/ proteínas chaperonas del complejo en las membranas sinápticas. Se
demostró además que las chaperonas pueden tener un papel general en estabilización de membrana. Todos estos
ejemplos enlazan a las chaperonas a la red de membrana de la célula, lo cual integra la membrana plasmática, el retículo
endoplasmático (ER), diferentes vesículas, la membrana nuclear y las mitocondria. Por otra parte, las chaperonas
pueden facilitar el tráfico citoplasmático. Los vínculos entre el RE, mitocondrias y citoplasma ya han sido demostrados
en el estrés celular. Las chaperonas pueden actuar como estabilizadoras y reguladoras de la conectividad y el tráfico de
estas importantes redes. Las conexiones entre los elementos de la red mitocondrial, la membrana del RE, el
citoesqueleto nuclear y citoplasmático pueden ser puntos clave para la integridad celular y la transferencia de
información, favoreciendo una protección eficaz contra cualquier daño celular. Las chaperonas se necesitan para un
acoplamiento eficiente de estas redes celulares. Desacoplar los elementos de la red y los módulos es utilizado como un
método para detener la propagación de daños. En caso de estrés, el principal papel de las chaperonas son detectar las
proteínas dañadas y la translocación de las chaperonas al núcleo inducida por el estrés, esto podría dar lugar a una
disociación "automática" de los elementos de la red y módulos, proporcionando a la célula una cantidad adicional
medidas de seguridad (Figura 2).
Chaperonas y red transcripcional
Las chaperonas son bien conocidas por proteger el núcleo celular después del estrés. La Hsp70 actúa sobre las proteínas
nucleares dañadas, limpia a otros componentes nucleares de proteínas mal plegadas y disminuye el peligro de
agregación generalizada. De acuerdo con estos resultados, las chaperonas promueven el transporte de subunidades
ribosomales y el movimiento de receptores de esteroides en el interior del núcleo. Las chaperonas regulan la activación
y el desmontaje de numerosos complejos transcripcionales (Figura 1). Por lo tanto, las chaperonas emergen como
reguladores de la red transcripcional. El estrés induce la translocación nuclear de chaperones para conservar la
capacidad nuclear durante la remodelación del entorno y evitar daños protegiendo la integridad del ADN.
Las propiedades emergentes de la regulación de las redes celulares por medio de las chaperonas se han demostrado en
trabajos en la que se vio que las chaperonas están involucradas en la regulación de las señales, orgánulos, membrana,
citoesqueleto y redes transcripcional (Figura 2). Sin embargo, se sabe relativamente poco acerca de cómo trabajan las
chaperonas, y sus propiedades emergentes de celular funciones. Uno de los avances más importantes en esta área vino
cuando se descubrió que la Hsp90 actúa como amortiguador de los cambios genéticos en Drosophila y en Arabidopsis.
Se ha sugerido que este efecto podría tener propiedades epigenéticas y la Hsp90 podría inducir cambios heredables en
la estructura de la cromatina.
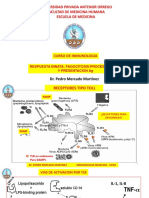
Fig. 1: Las Chaperones moleculares en la regulación de la señalización: algunos avances recientes. Las chaperonas desempeñan un papel esencial en
la maduración y activación de cientos de proteínas quinasas. BAG1, la co-chaperona de Hsp70, Hsp90 pueden activar a la quinasa dependiente de
Raf-1. El secuestro de la proteína BAG1 por Hsp70 durante el estrés proporciona un mecanismo de para a la proliferación celular durante
situaciones de estrés. Las chaperonas participan en balsas de señalización de Enós y proteínas G. Las Chaperones también ayudan al tráfico
subnuclear y desmontaje de los factores de transcripción y la relación de complejos. (Tenga en cuenta que los miembros del complejo asociada a la
chaperona Hsp90 varían en las diferentes vías y se muestran con el mismo símbolo sólo para mayor claridad.)
Chaperones como reguladores de redes celulares
Las chaperonas emergen como reguladores que integran señales de transcripción, citoesqueleto y membrana /
orgánulos celulares. Las chaperonas se pueden modificar y así afectar a la mayoría de las otras funciones celulares
conectadas. Como ejemplo, el estrés (enfermedad o envejecimiento) pueden inducir un desacoplamiento de la
integridad celular mediada por chaperonas de-acoplamiento, por ruptura de las conexiones entre los orgánulos (por
ejemplo, mitocondrias, el ER, la membrana nuclear y vesículas) así como la detención del tráfico citoplasmático. Las
señales y la regulación de la transcripción también es probable que se deterioren. El estrés se acompaña de la
translocación de las chaperonas al núcleo, donde trabajan para mantener la capacidad de remodelación en el núcleo,
mientras que la promoción de la temporal fragmentación de todas las redes en la periferia de la célula. Los enlaces
residuales o de nueva formación entre los miembros de la red son típicamente más débiles que las conexiones
originales, lo que puede disminuir el caos celular y proporcionar un nivel adicional de estabilización del sistema. Los
círculos negros indican elementos proteínas de las redes del citoesqueleto y la señalización / transcripcional. Las líneas
de puntos delimitar distintas redes entre sí. Obviamente todas estas redes se solapan en el contexto celular.
Conclusiones
Las chaperonas regulan las funciones celulares en dos niveles, interactúan con una proteína diana específica y ayudan a
que se pliegue después de la síntesis, o re-pliegue después del estrés. Estas interacciones fuertes hacen a las chaperonas
importantes elementos centrales en las redes celulares, señalización, membrana y orgánulos de la red y ranscripción. Sin
embargo, en la mayoría de los casos las chaperonas tienen sólo una baja afinidad, interacción temporal y débil con la
mayoría de sus objetivos (Figura 2). Los cambios en estas interacciones no afectan el comportamiento general de toda la
red celular. Sin embargo, la inhibición de estas interacciones débiles podría conducir a un aumento en la
desestabilización celular y la desintegración de toda la red. Esta desestabilización es utilizada en el diseño de algunas
drogas como una promoción de una "catástrofe de error ' para ayudar a combatir el cáncer. En contraste, la activación
de chaperonas podría disminuir el ruido celular, y la consiguiente estabilización de células podría ayudar de forma
adicional e indirecta para prevenir las enfermedades de mal plegamiento de proteínas incluyendo diversas formas de
neurodegeneración, tales como la esclerosis amiotrófica lateral, Alzheimer, Parkinson y Huntington.
Además de detener o revertir el desarrollo de estas enfermedades, las terapias basadas en chaperona también pueden
beneficiar al organismo en el envejecimiento mediante la estabilización de sus funciones celulares.
También podría gustarte
- Chaperopatia El Correcto PlegamientoDocumento8 páginasChaperopatia El Correcto PlegamientoOscar Cardona PantojaAún no hay calificaciones
- Interacciones MAPK-tumoresDocumento5 páginasInteracciones MAPK-tumoresJesus GomezAún no hay calificaciones
- Chaperones MolecularesDocumento13 páginasChaperones MolecularesricardoAún no hay calificaciones
- Mecanismos de Señalización CelularDocumento4 páginasMecanismos de Señalización CelularDafne Uribe DiazAún no hay calificaciones
- Control expresión génica celularDocumento7 páginasControl expresión génica celularTony MartínezAún no hay calificaciones
- ChaperonasDocumento7 páginasChaperonasOscar Cardona PantojaAún no hay calificaciones
- Plegamiento de Proteínas in VivoDocumento17 páginasPlegamiento de Proteínas in VivoElkinAAún no hay calificaciones
- UntitledDocumento8 páginasUntitledPuquiki HAún no hay calificaciones
- Guia de Biologia CelularDocumento9 páginasGuia de Biologia CelularMaria Fernanda Hernandez CastañedaAún no hay calificaciones
- Actividad 11Documento7 páginasActividad 11fiorella pahuachonAún no hay calificaciones
- Sesión 14Documento7 páginasSesión 14Devora GilAún no hay calificaciones
- Vias de SeñalizaciónDocumento9 páginasVias de SeñalizaciónKaren GonzalesAún no hay calificaciones
- Neuroplasticidad PLP DLP AprendizajeDocumento32 páginasNeuroplasticidad PLP DLP AprendizajeMagdalena MachucaAún no hay calificaciones
- Taller 8 CompletoDocumento12 páginasTaller 8 CompletoThania GonzlezAún no hay calificaciones
- Ensayo Hallmarks of Cancer The Next GenerationDocumento2 páginasEnsayo Hallmarks of Cancer The Next GenerationDAYANA VICTORIA HERRERA OLIVOSAún no hay calificaciones
- EL GENOMA DE UNA CÉLULA y SISTEMAS ENERGETICOS SUBCELULARESDocumento5 páginasEL GENOMA DE UNA CÉLULA y SISTEMAS ENERGETICOS SUBCELULARESRodrigoMendozaAún no hay calificaciones
- Receptores GlucosaDocumento13 páginasReceptores Glucosamanu rendonAún no hay calificaciones
- Vias de SeñalizaciónDocumento3 páginasVias de Señalizacióncamilo ortiz intriagoAún no hay calificaciones
- ParcialDocumento5 páginasParcialJonny FernandoAún no hay calificaciones
- Señalización CelularDocumento8 páginasSeñalización CelularGiss ZuritaAún no hay calificaciones
- Taller Sobre Lectura Crítica - Ana Milena RuizDocumento4 páginasTaller Sobre Lectura Crítica - Ana Milena RuizAna Milena Ruiz RomeroAún no hay calificaciones
- Más allá del ADN: La Revolución Epigenética: Desde Mecanismos Celulares hasta Factores Ambientales: Cómo la Epigenética Moldea Nuestro Destino Biológico y las Implicaciones para la Salud, el Comportamiento y el Futuro de la InvestigaciónDe EverandMás allá del ADN: La Revolución Epigenética: Desde Mecanismos Celulares hasta Factores Ambientales: Cómo la Epigenética Moldea Nuestro Destino Biológico y las Implicaciones para la Salud, el Comportamiento y el Futuro de la InvestigaciónAún no hay calificaciones
- Apuntes RandomDocumento5 páginasApuntes RandomSamuel SierraAún no hay calificaciones
- RegexprgenicaDocumento40 páginasRegexprgenicaMelanie Valeria Pulido SanchezAún no hay calificaciones
- MonografiaDocumento4 páginasMonografiaJose Juan Torres MartinezAún no hay calificaciones
- Capítulo 1Documento21 páginasCapítulo 1John DittelAún no hay calificaciones
- Introducción A La Transcripción Del ADNDocumento97 páginasIntroducción A La Transcripción Del ADNMikado NidomeAún no hay calificaciones
- Compartimentos Intracelulares y Sorting de ProteínasDocumento9 páginasCompartimentos Intracelulares y Sorting de ProteínasFelipe Calderon AvendañoAún no hay calificaciones
- Foro Preguntas Ciclo Celular. Técnicas.: 1-: Doc. Juan BurdissoDocumento5 páginasForo Preguntas Ciclo Celular. Técnicas.: 1-: Doc. Juan BurdissoLuciano David PelliAún no hay calificaciones
- CASO 1-2 - Biología Celular y MolecularDocumento6 páginasCASO 1-2 - Biología Celular y MoleculardianaAún no hay calificaciones
- Tema 6 AcabadoDocumento13 páginasTema 6 AcabadoMagdalena Oñate SerranoAún no hay calificaciones
- Via de Señalizacion de Mapks en PlantasDocumento30 páginasVia de Señalizacion de Mapks en PlantasMonteagudo JorgeAún no hay calificaciones
- Transporte VesicularDocumento3 páginasTransporte VesicularHoligaan De BuhoradoAún no hay calificaciones
- Capitulo 1 Célula (Final)Documento7 páginasCapitulo 1 Célula (Final)Maria Camila GonzálezAún no hay calificaciones
- Fichas 7Documento7 páginasFichas 7Noelita RiveraAún no hay calificaciones
- Tema 5 - Los RibosomasDocumento3 páginasTema 5 - Los RibosomasÁngel Bordallo NavarroAún no hay calificaciones
- RTKsDocumento3 páginasRTKsValeria TorresAún no hay calificaciones
- Señalización CelularDocumento5 páginasSeñalización CelularLoaiza Morales JazmínAún no hay calificaciones
- Tarea Proteínas Chaperonas_González Roque Eréndira_2204Documento2 páginasTarea Proteínas Chaperonas_González Roque Eréndira_2204320006940Aún no hay calificaciones
- Citoesqueleto PDFDocumento10 páginasCitoesqueleto PDFAradya GrajalesAún no hay calificaciones
- Introducción a la regulación y señalización molecular durante el desarrollo embrionarioDocumento9 páginasIntroducción a la regulación y señalización molecular durante el desarrollo embrionariojoha leivaAún no hay calificaciones
- Capítulo 4 - Transducción de Señales en El CerebroDocumento56 páginasCapítulo 4 - Transducción de Señales en El CerebroEnrique GonzálezAún no hay calificaciones
- Regulación génica pre-transcripcionalDocumento10 páginasRegulación génica pre-transcripcionaltaricura estebanAún no hay calificaciones
- SeminarioDocumento11 páginasSeminarioMoisés AranaAún no hay calificaciones
- IFAPsDocumento42 páginasIFAPsCarlos Abeal PenaAún no hay calificaciones
- Retículo Endoplasmático RugosoDocumento7 páginasRetículo Endoplasmático Rugosoarmando jeffryAún no hay calificaciones
- Ensayo Final Control de La Morfologia Celular.Documento13 páginasEnsayo Final Control de La Morfologia Celular.Lindy Rivera Benavides100% (1)
- El citoesqueleto de actina: una perspectiva desde la biología molecular del cáncerDocumento8 páginasEl citoesqueleto de actina: una perspectiva desde la biología molecular del cáncerLupita JimeAún no hay calificaciones
- Cuestionario (1) .Documento6 páginasCuestionario (1) .OscarJimenezAún no hay calificaciones
- Mutaciones y Síntesis de ProteínasDocumento3 páginasMutaciones y Síntesis de ProteínasAdriana AvilésAún no hay calificaciones
- Capitulo 1. Embriología MédicaDocumento16 páginasCapitulo 1. Embriología MédicaYessenia MillaAún no hay calificaciones
- El Nucleo Celular y El Control de Expresión GenéticaDocumento10 páginasEl Nucleo Celular y El Control de Expresión GenéticaKary FarfánAún no hay calificaciones
- Unidad II (Proteinas 1)Documento19 páginasUnidad II (Proteinas 1)jesus sanchez coelhoAún no hay calificaciones
- Síntesis Conceptuales de Biología Celular 4 - Regulación de La Expresión Génica (Otra Vez)Documento15 páginasSíntesis Conceptuales de Biología Celular 4 - Regulación de La Expresión Génica (Otra Vez)Acis SamuelAún no hay calificaciones
- Capítulo 1 - Introducción A La Regulación y La Señalización MolecularesDocumento2 páginasCapítulo 1 - Introducción A La Regulación y La Señalización MolecularesDarkinfire WesternAún no hay calificaciones
- Embriologia GuiaDocumento14 páginasEmbriologia GuiaAlexis HernandezAún no hay calificaciones
- Biologia 08 - Resumen Orne 2do ParcialDocumento13 páginasBiologia 08 - Resumen Orne 2do ParcialSantino CerezoAún no hay calificaciones
- Resumen 3 - APBDocumento4 páginasResumen 3 - APBAlejandro Pesqueira BojorquezAún no hay calificaciones
- Ensayo CelularDocumento4 páginasEnsayo CelularSánchez Ibarra Gerardo DanielAún no hay calificaciones
- Plantas no vasculares: briófitas, hepáticas, antoceros y musgosDocumento4 páginasPlantas no vasculares: briófitas, hepáticas, antoceros y musgosCamila Belen LazoAún no hay calificaciones
- Tema 1 - IntroduccionDocumento6 páginasTema 1 - IntroduccionCamila Belen LazoAún no hay calificaciones
- 12Documento8 páginas12Julieta Da CostaAún no hay calificaciones
- Imagenes FurmanDocumento1 páginaImagenes FurmanCamila Belen LazoAún no hay calificaciones
- Documento Pcial E.S.I. 2011Documento40 páginasDocumento Pcial E.S.I. 2011Arpia_ceAún no hay calificaciones
- Observacion Microscopica de La CelulaDocumento1 páginaObservacion Microscopica de La CelulaCamila Belen LazoAún no hay calificaciones
- Capacidades y CompetenciasDocumento2 páginasCapacidades y CompetenciasCamila Belen LazoAún no hay calificaciones
- Método de BradfordDocumento2 páginasMétodo de BradfordAbril AranaAún no hay calificaciones
- Función y Disfunción EndotelialDocumento3 páginasFunción y Disfunción EndotelialGeraldin HenostrozaAún no hay calificaciones
- Cuestionario 2 Enzimas 2023Documento3 páginasCuestionario 2 Enzimas 2023karmaAún no hay calificaciones
- Divergencia Vias de SeñalizaciónDocumento12 páginasDivergencia Vias de SeñalizaciónEvelynNicoleCutipaCalcinaAún no hay calificaciones
- 2do Parcial Bioqui 2021Documento4 páginas2do Parcial Bioqui 2021Coraline MendozaAún no hay calificaciones
- Seminario BioquímicaDocumento60 páginasSeminario BioquímicaPepe Rojas YachasAún no hay calificaciones
- Citoesqueleto y Mo-Lidad Intracelular: Microtubulos y Filamentos IntermediosDocumento38 páginasCitoesqueleto y Mo-Lidad Intracelular: Microtubulos y Filamentos IntermediosAlejandro MartínezAún no hay calificaciones
- Citoesqueleto HDocumento7 páginasCitoesqueleto HNahy Kelis ChingaliAún no hay calificaciones
- Fisiologia de La Coagulacion PDFDocumento6 páginasFisiologia de La Coagulacion PDFTecnoTutosAndroid TTAAún no hay calificaciones
- Recambio ProteicoDocumento11 páginasRecambio ProteicoAlber DiazAún no hay calificaciones
- Práctica 12. Digestión y Metabolismo de ProteínasDocumento7 páginasPráctica 12. Digestión y Metabolismo de ProteínasKatherin Arcaya CruzAún no hay calificaciones
- (Presentación Proteínas - (2 - ) (Modo de Compatibilidad) )Documento47 páginas(Presentación Proteínas - (2 - ) (Modo de Compatibilidad) )Arturo ChavezAún no hay calificaciones
- Universidad Privada Antenor Orrego Facultad de Medicina Humana Escuela de MedicinaDocumento19 páginasUniversidad Privada Antenor Orrego Facultad de Medicina Humana Escuela de MedicinaMonica García GutierrezAún no hay calificaciones
- Cinética enzimática y generalidades de las enzimasDocumento14 páginasCinética enzimática y generalidades de las enzimasJohan Cardenas orozcoAún no hay calificaciones
- Proteasa Bioquima de Las ProteinasDocumento40 páginasProteasa Bioquima de Las Proteinasfrancisco gironAún no hay calificaciones
- HemostasiaDocumento6 páginasHemostasiaLetty LopezAún no hay calificaciones
- "Las Proteínas en Los Seres Vivos" - Trabajo N°21Documento5 páginas"Las Proteínas en Los Seres Vivos" - Trabajo N°21Victoria Selena GonzalezAún no hay calificaciones
- Enzimas 1Documento9 páginasEnzimas 1Laura Lizeth Díaz OrtizAún no hay calificaciones
- Aminoácidos LeerDocumento43 páginasAminoácidos LeerExvoxAún no hay calificaciones
- Unionescelulares 140423084421 Phpapp01Documento19 páginasUnionescelulares 140423084421 Phpapp01marcorenxAún no hay calificaciones
- Qué Es Un PrionDocumento4 páginasQué Es Un PrionKevin Fredy Zenteno VeraAún no hay calificaciones
- Practica 18Documento5 páginasPractica 18Rosa M. Alcalá100% (2)
- CitoesqueletoDocumento41 páginasCitoesqueletokremenchutzkyAún no hay calificaciones
- Factor VIII Deficient Plasma SPDocumento3 páginasFactor VIII Deficient Plasma SPconstanza castellanosAún no hay calificaciones
- Informe Seminario 2 Grupo 6Documento5 páginasInforme Seminario 2 Grupo 6Delay gGAún no hay calificaciones
- ActinaDocumento16 páginasActinaMarcelo TorresAún no hay calificaciones
- Anticuerpos y Antígenos Por Abel Esaú Reyes CórdovaDocumento9 páginasAnticuerpos y Antígenos Por Abel Esaú Reyes CórdovaAbel ReyesAún no hay calificaciones
- Citocinas ExpoDocumento44 páginasCitocinas ExpoANGELAún no hay calificaciones
- Banco de Preguntas PROTEÍNAS - BF4 - P1Documento15 páginasBanco de Preguntas PROTEÍNAS - BF4 - P1David FernandoAún no hay calificaciones