75% encontró este documento útil (4 votos)
748 vistas9 páginasReacciones de Aldehídos y Cetonas en Química
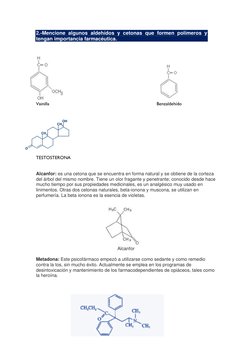
Este documento presenta los procedimientos y resultados de una práctica de laboratorio sobre las reacciones de caracterización de aldehídos y cetonas. Incluye las ecuaciones químicas y observaciones de las reacciones de 2,4-dinitrofenilhidracina, Schiff, Tollens, Fehling y bisulfito de sodio para diferentes compuestos como el benzaldehído y la ciclohexanona. También menciona algunos aldehídos y cetonas de importancia farmacéutica como la vainilla, el benzaldeh
Cargado por
Diego Padilla SantosDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd
75% encontró este documento útil (4 votos)
748 vistas9 páginasReacciones de Aldehídos y Cetonas en Química
Este documento presenta los procedimientos y resultados de una práctica de laboratorio sobre las reacciones de caracterización de aldehídos y cetonas. Incluye las ecuaciones químicas y observaciones de las reacciones de 2,4-dinitrofenilhidracina, Schiff, Tollens, Fehling y bisulfito de sodio para diferentes compuestos como el benzaldehído y la ciclohexanona. También menciona algunos aldehídos y cetonas de importancia farmacéutica como la vainilla, el benzaldeh
Cargado por
Diego Padilla SantosDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd