Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Crioscopia Informe Casi Completo
Cargado por
Marvin AguirreDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Crioscopia Informe Casi Completo
Cargado por
Marvin AguirreCopyright:
Formatos disponibles
MR08FQD
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
FACULTAD DE QUIMICA E
INGENERIA QUIMICA
DEPARTAMENTO ACADEMICO DE FISICOQUIMICA
LABORATORIO DE FISICOQUIMICA
CRIOSCOPIA
Profesora: Carasas Consuelo
Alumno: Cornelio Vidal Ruth Estefany
Cdigo: 15070134
Fecha de realizacin de la prctica: 07/09/16
Fecha de entrega de informe: 14/09/16
Lima-Per
2016-1
INDICE:
1. INTRODUCCION
2. RESUMEN
3. PRINCIPIOS TEORICOS
3.1
CRIOSCOPIA
3.11
3.12
3.13
3.14
Definicin
Punto de solidificacin
Punto de ebullicin
Punto de congelacin
Determinacin Crioscpica del peso molecular
3.2
TERMOMETRO DE BECKMANN
4. DETALLES EXPERIMENTALES
5. TABULACION DE DATOS Y RESULTADOS
6. CALCULOS
13
7. ANALISIS Y DISCUCIION DE RESULTADOS
15
8. CONCLUCIONES Y RECOMENDACIONES
16
9. APENDICE
17
9.1
9.2
9.3
10.
HOJA DE DATOS
CUESTIONARIO
GRAFICOS
18
19
BIBLIOGRAFIA
20
INTRODUCCION
Crioscopa Observacin del enfriamiento, se encarga del estudio de la temperatura de solidificacin
de las soluciones.
Se sabe que el punto de congelacin del agua u otro lquido disminuye por la adicin de un soluto
solido no voltil y fue puntualizado por Blagden hace cien aos, donde se tiene que la depresin en el
punto de congelacin es directamente proporcional a la concentracin de la solucin.
La adicin de un soluto baja la presin de de vapor del solvente, segn la ley de Raoult, es en base a
esta ley que existen algunos mtodos para el estudio de los solutos en cualquier tipo de disolvente. El
descenso de la presin de vapor depende solamente de la formacin molar del soluto, es
independiente de cualquier otra propiedad del mismo.
Determinacin Crioscpica del peso molecular
Una de las utilidades ms importantes de la crioscopia es la utilizacin de diversas
sales
para evitar la congelacin de diversos lquidos a bajas temperaturas ya que disminuye el punto de
congelacin de los lquidos como los combustibles, y del agua. Ya que en diversos pases polares la
temperatura en invierno esta bajo cero lo cual hara que el lquidos puros se congelen en las
tuberas y no habra flujo.
La crioscopia tiene diversas aplicaciones una de las ms importantes es la determinacin
experimental del peso molecular del soluto. El mtodo empleado es el de beckmann quien se basa
en el descenso del punto de congelacin, que consta de un termmetro el cual tiene un deposito de
mercurio en la parte superior, por medio del cual es posible variar la cantidad de mercurio de la
cubeta, de forma que pueda utilizarse amplia gama de temperaturas.
RESUMEN
La presente prctica experimental tuvo como finalidad determinar el peso molecular de una sustancia
disuelta en un solvente, teniendo en cuenta el descenso del punto de congelacin del solvente. Para
cumplir este fin se emple el mtodo de Beckmann que consiste en la determinacin crioscpica del
peso molecular.
Esta prctica se realiz a condiciones de laboratorio de 19C de temperatura, 756 mmHg de presin y
93% de humedad relativa.
La masa molecular de una sustancia desconocida o no identificada puede determinarse midiendo la
cantidad que desciende el punto de solidificacin de un disolvente, cuando se disuelve en l una
cantidad conocida de la sustancia no identificada. Este proceso que determina las masas moleculares
se denomina crioscopa.
El procedimiento experimental a llevarse a cabo para lograr cumplir los objetivos anteriormente
planteados se dividen en dos partes, la primera parte, donde se debe calibrar el termmetro de
3
Determinacin Crioscpica del peso molecular
Beckmann, y la segunda parte donde se la determina las alturas en el termmetro
Beckmann para cada intervalo de tiempo de 20 segundos.
de
Luego de haber desarrollado el experimento y con los datos tomados se hicieron los clculos
respectivos dando los siguientes resultados:
El peso molecular de la urea hallado experimentalmente es de 67.45 g/mol
y en comparacin
con el terico que cuyo valor es de
g
60.055
mol
, encontramos un porcentaje de error de
12.3% .
Para esta experiencia se considera que el descenso del punto de congelacin es una propiedad
coligativa que depende de las caractersticas del soluto, y de la cantidad del soluto disuelto en el
solvente.
Para obtener resultados con pequeos errores se recomienda un calibrado adecuado del termmetro
Beckmann.
MARCO TEORICO
Crioscopa.
La masa molecular de una sustancia desconocida o no identificada puede determinarse midiendo la
cantidad que desciende el punto de solidificacin de un disolvente, cuando se disuelve en l una
4
Determinacin Crioscpica del peso molecular
cantidad conocida de la sustancia no identificada. Este proceso que determina las
masas moleculares se denomina crioscopa.
Punto de solidificacin o punto de congelacin.
Temperatura a la que un lquido sometido a una presin determinada se transforma en slido.
El punto de solidificacin de un lquido puro (no mezclado) es en esencia el mismo que el punto de
fusin de la misma sustancia en su estado slido, y se puede definir como la temperatura a la que el
estado slido y el estado lquido de una sustancia se encuentran en equilibrio. El punto de
solidificacin de la mayora de las sustancias puede elevarse aumentando la presin. No obstante, en
sustancias que se expanden al solidificarse (como el agua), la presin rebaja el punto de
solidificacin.
Punto de ebullicin y punto de congelacin
Tanto la elevacin del punto de ebullicin como el descenso del punto de congelacin son
proporcionales al descenso de la presin de vapor, siempre que slo se consideren disoluciones
diluidas de solutos no voltiles. Para una masa fija de 1 kg de disolvente, el cambio de temperatura
viene dado por :
T = Km/M
Donde m es la masa de soluto, M la masa molecular relativa del soluto y K la constante ebulloscpica
o crioscpica, caracterstica de cada disolvente.
Descenso del punto de congelacin de las soluciones
Al enfriar una solucin diluida, se alcanza eventualmente una temperatura en la cual un solvente
slido comienza a separarse. La temperatura en que comienza tal separacin se conoce como punto
de congelacin de la solucin, que de una manera ms general se define como aquella temperatura
en la cual una solucin particular se halla en equilibrio con el solvente slido. Las soluciones se
congelan a temperaturas menores que el solvente puro. El descenso del punto de congelacin de
5
Determinacin Crioscpica del peso molecular
una solucin es, otra vez, una consecuencia directa de la disminucin de la presin
de
vapor del solvente por el soluto disuelto. Para darnos cuenta de este hecho,
consideremos el diagrama de presin de vapor-temperatura en el cual AB es la curva de sublimacin
del solvente slido, mientras que CD es de presin de vapor del lquido solvente puro. En el punto de
congelacin de este ltimo, se hallan en equilibrio la fase slida y la liquida y en consecuencias
ambas deben poseer idntica presin de vapor. El nico punto de la grfica en la cual ambas formas
del solvente puro tienen igual presin de vapor es en B, interseccin de AB y CD, y, por tanto, To, que
corresponde a B, debe ser el punto de congelacin del solvente puro.
Cuando en este se disuelve un soluto, hay un descenso de la presin de vapor de este ltimo, y ya
no hay equilibrio a To, sino que se alcanza de nuevo cuando la curva de presin de vapor de la
solucin, corta la de sublimacin, y entonces
tendremos el punto de congelacin de la solucin. Como la curva de presin de vapor de la solucin,
EF, queda debajo de la del solvente puro, la interseccin de EF y AB tiene lugar solamente en un
punto tal como E para el cual la temperatura es menor que To. De aqu que cualquier solucin deba
tener un punto de congelacin T, menor que la del solvente To.
Termmetro de Beckmann:
El termmetro diferencial de Beckmann tiene una escala de 30 cm de largo,
aproximadamente con una escala total de 5 a 6 grados C. en divisiones. de 0.01 de
grado. Est construido de suerte que una parte del mercurio del bulbo puede ser
trasladada a un depsito de manera que lleve el extremo de la columna de mercurio a la
seccin graduada para las zonas de temperaturas en que se han de medir las diferencias.
Determinacin Crioscpica del peso molecular
Se emplea slo para medir diferencias de
temperatura. La exactitud conseguida est
0.002 y 0.005 grados en la medida de
cualquier intervalo dentro de los lmites de la
escala.
DETALLES EXPERIMENTALES
Materiales y reactivos:
Aparato crioscpico de beckmann.
Termmetro
Pipeta aforada de 25ml
Vasos
Solvente agua
Soluto: urea, sal comn
entre
Determinacin Crioscpica del peso molecular
Determinacin del peso molecular de un soluto
solucin:
en
a) Calibrar el termmetro Beckmann a una escala de temperatura adecuada, siempre en
cuando de acuerdo a
b) l punto de congelacin del solvente, lo cual utilizamos para ello un bao de temperatura
que se encuentre a la temperatura de congelacin del solvente.
c) Armar el equipo adecuadamente y con los materiales bien limpios y secos, sobre todo la
pipeta aforada, ya que con esta se realiza la medicin del volumen del solvente quien se
debe encontrar puro.
d)
Vierta 25ml del solvente en un tubo y coloque el termmetro Beckmann calibrado y el
agitador.
e) Colocar el tubo dentro de la chaqueta de aire como se muestra en la figura siguiente.
Determinacin Crioscpica del peso molecular
f)
Sumergir todo este conjunto en un bao de enfriamiento que debe encontrarse a una
temperatura 5 menor que la temperatura de cristalizacin del solvente.
g)
Agite suavemente el contenido del tubo, y lea la temperatura cada 20 segundos desde 5C,
hasta obtener varios valores constante, que corresponden al punto de congelacin del
solvente puro.
h) Retire la chaqueta de aire y funda el solvente, mediante calentamiento con las manos.
i)
Pese de 0.4 a 0.8g de soluto y agrguelo al tubo que contiene al solvente.
j)
Agite la mezcla hasta disolver completamente el soluto y luego coloque el tubo en la chaqueta
de aire.
k) Determine el punto de congelacin de la solucin repitiendo el quinto y sexto paso. Tener
presente que la solucin no congela a temperatura constante.
l)
Al terminar el experimento retire cuidadosamente el termmetro de Beckmann de la solucin,
y deje el equipo completamente limpio.
Determinacin Crioscpica del peso molecular
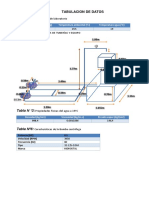
5.-TABULACIN:
1) Condiciones de laboratorio
Tabla N1:
Temperatura: T(C)
Presin atmosfrica
(mmHg)
%humedad
relativa(HR)
23
754
93
2) Datos experimentales:
Determinacin del peso molecular de un soluto en solucin
Tabla N2: Para el agua
T ( segundos)
T ( C)
20
6.1
40
5.92
60
5.83
80
5.75
100
5.83
120
5.62
140
5.55
160
5.49
180
5.44
200
5.12
220
4.98
10
Determinacin Crioscpica del peso molecular
240
4.9
1000
2.82
1020
2.82
1040
2.8
1060
2.8
1080
2.84
1100
2.89
1120
2.94
1140
3.09
1160
3.13
1180
3.39
1200
3.44
1220
3.53
1240
3.6
1260
3.75
1280
3.78
1300
3.81
1320
3.85
1340
3.87
1360
3.9
1380
3.95
1400
3.97
1420
1440
4.09
Tabla N3: Para 25 ml de agua con 0.3908 gramos de urea
T ( segundos)
T ( C)
5.9
20
5.81
11
Determinacin Crioscpica del peso molecular
40
5.75
60
5.6
80
5.51
100
5.4
120
5.3
140
5.2
160
5.01
180
4.92
200
4.78
220
4.75
240
4.65
260
4.59
280
4.51
300
4.43
320
4.36
340
4.26
360
4.21
380
4.16
400
4.09
420
4.04
440
460
3.95
480
3.91
1060
2.6
1080
2.55
1100
2.5
1120
2.48
1140
2.46
1160
2.45
1180
2.31
1200
2.21
1220
1.91
12
Determinacin Crioscpica del peso molecular
1240
1.86
1260
1.89
1280
1.91
1300
1.93
1320
2.02
1340
2.04
1360
2.03
1380
2.01
1400
1.97
13
Universidad Nacional Mayor de San Marcos - 2016
3) Datos Tericos:
Tabla N4: Determinacin del peso molecular de un soluto en solucin
Peso molecular de una solucin
Volumen del agua
25.00ml
Masa de la Urea
0.3908g
1.86(K.Kg.sol.vol.Mol-1)
Kcte Crioscopia(Kf)
Punto de Congelacin
0.0C
Densidad de agua a 23C
1g/ml
4) Resultados y porcentaje de error:
Tabla 7: Determinacin del peso molecular de un soluto en solucin
Resultados
T1: Temperatura de congelacin del agua
3.90C
T2: Temperatura de congelacin del agua
con urea
3.04C
1.86C
Peso molecular de la Urea
15.63
Error del peso molecular
73.98 %
Siendo el 3.45C el 0.0 C en el termmetro de Beckmann
Crioscopa
Pgina 14
Universidad Nacional Mayor de San Marcos - 2016
6.-CLCULOS:
a) Graficas de las curvas de enfriamiento:
Para el agua:
T ( C)Vs tiempo(s)
7
6
5
4
T(C) 3
2
1
0
200
400
600
800
1000
1200
1400
1600
tiempo(s)
Crioscopa
Pgina 15
Universidad Nacional Mayor de San Marcos - 2016
Para el agua con urea:
T(C) vs tiempo(s)
3.5
3
2.5
2
T(C) 1.5
1
0.5
0
800
900
1000
1100
1200
1300
1400
1500
tiempo(s)
b) De los grficos anteriores, determine los puntos de congelacin del
solvente(T1) y solucin (T2), y el T correspondiente
T1=
3.75+ 3.78+ 3.81+ 3.85+3.87+3.9+3.95+3.97+ 4.0+ 4.09
=3.90C
10
T2=2.04C
T=3.90-2.04=1.86C
C)Usando la siguiente formula se calcula el peso molecular del soluto
disuelto
Donde:
M: peso molecular del soluto=?
W: peso en g de solvente = 25.00g
W: peso en g de soluto = 0.3908g
Crioscopa
Pgina 16
Universidad Nacional Mayor de San Marcos - 2016
Tf: descenso del punto de congelacin=TC(2)-TC(1)= 1.86 C
Kf: cte crioscopia = 1.86
Los valores de Tc(1) y Tc(2) obtenidos de sus respectivas grficas.
Adems:
M (TEORICO)=60.06g/mol
M=
10001.860.3908
25.001.86
M = 15.63 g/mol
PORCENTAJE DE ERROR:
%ERROR =
Valor teoricoValor experimental
100
Valor teorico
%ERROR =
60.0615.63
*100
60.06
%ERROR = 73.98%
Crioscopa
Pgina 17
Universidad Nacional Mayor de San Marcos - 2016
ANALISIS Y DISCUCION DE
RESULTADOS
o Las curvas de presin de vapor como funcin de la temperatura que se dan
para los disolventes puros y para las disoluciones, muestran de una forma
mas o menos clara su proximidad al punto de congelacin.
o Para estos diagramas se da que el slido, cuya presin de vapor no esta
afectada por la presencia del soluto en la disolucin, est en equilibrio con
la disolucin a temperatura ms baja que la que corresponde al equilibrio
con el disolvente puro. A partir de esto se puede deducir la ecuacin para
determinar la constante crioscpica, que no depende sino de las
caractersticas propias y particulares del disolvente considerndose como
una propiedad coligativa.
o La eleccin del disolvente esta determina, en la mayora de las ocasiones
por la solubilidad y reactividad qumica de la sustancia, cuyo peso
molecular se quiere medir. Se consiguen resultados de mayor garanta
cuando se utiliza un disolvente cuya constante de descenso del punto de
congelacin tenga un valor elevado.
Crioscopa
Pgina 18
Universidad Nacional Mayor de San Marcos - 2016
CONCLUSIONES Y
RECOMENDACIONES
CONCLUSIONES:
La variacin de energa depende de diversas propiedades propias de las
sustancias qumicas, como el calor especific.
El cambio de la cantidad de calor depende de diversos factores como la
presin, temperatura y el volumen.
La energa o calor en las reacciones de neutralizacin casi siempre es
exotrmica debido a la formacin de agua en estos procesos qumicos.
Todos los cambios de estado fsico y las reacciones qumicas estn
acompaados de una variacin en la cantidad de energa interna.
RECOMENDACIONES:
Para llegar a un equilibrio trmico, y poder hallar la cantidad de calor
ganado o perdido se debe aislar trmicamente.
Se debe tener cuidado en la manipulacin de los reactivos como los cidos
y las base.
Se debe usar pipetas diferentes para tomar los reactivos y de esta manera
evitar contaminarlos.
Tener bastante precisin en la titulacin y valoracin de las soluciones del
acido clorhdrico e hidrxido de sodio, para obtener datos ms exactos.
Crioscopa
Pgina 19
Universidad Nacional Mayor de San Marcos - 2016
APENDICE
I.
CUESTIONARIO
1. Defina el concepto general de una propiedad coligativa.
Propiedades coligativas, propiedades de las disoluciones que dependen del
nmero de partculas en un volumen de disolvente determinado, y si son
electrolitos o no electrolitos. Entre las propiedades coligativas figuran el
descenso de la presin de vapor, la elevacin del punto de ebullicin, el
descenso del punto de congelacin y la presin osmtica. Las medidas de
estas propiedades en una disolucin acuosa diluida de un soluto no
ionizado, como la urea o la glucosa, pueden permitir determinar con
precisin las masas moleculares relativas. En el caso de solutos ionizados,
las medidas pueden llevar a una estimacin del porcentaje de ionizacin
que tiene lugar. Las modificaciones debidas a solutos gaseosos son
despreciables.
2. Explique la diferencia de las propiedades coligativas entre soluciones
electrolticas y no electrolticas.
Las propiedades coligativas se dividen en dos partes: Aquellos disoluciones
que tienen solutos electrolticos y los no electrolticos la diferencia principal
entre estos dos solutos es que lo electrolticos en disolucin se disocian en
iones; por lo tanto, cuando se disuelve una molcula de un compuesto de
un electrolito se separa en dos o ms partculas. A diferencia que los no
electrolitos que no se ionizan y se mantienen como una solo partcula.
Crioscopa
Pgina 20
Universidad Nacional Mayor de San Marcos - 2016
Esta diferencia afecta a todas las propiedades coligativas ya que estas
dependen del nmero de partculas en un determinado volumen de
solvente.
Para explicar este efecto, se define una cantidad denominada factor de
vant Hoff que est dada por:
i=
n mero real de particulas en disoluci n despues de la disocianci n
n mero de unidades formula inicialmente disueltas en ladisolucion
Asi , i debe ser 1 para todos los no electrolitos. Para electrolitos fuertes
como el NaCl y el KNO3, I debe ser dos y para electrolitos fuertes del tipo
de Na2SO4 y CaCl2, i debe ser 3. En consecuencias las ecuaciones de las
propiedades coligativas deben modificarse como siguen:
T b=i k b m
T f =ik f m
=iMRT
3. Mencione algunas limitaciones del mtodo crioscopico en la
determinacin de pesos moleculares
Se tienen diferentes limitaciones en la determinacin del peso molecular,
por el mtodo crioscopico y entre ellos tenemos:
Error en la determinacin del peso molecular por la cantidad no tan exacta
de la masa del soluto, solvente, y la imprecisin en medicin del
termmetro.
Se necesita datos tericos adicionales como la temperatura de fusin,
constante universal R, entalpia de formacin y peso molecular del solvente
para la determinacin de la constante crioscopica.
Crioscopa
Pgina 21
Universidad Nacional Mayor de San Marcos - 2016
BIBLIOGRAFIA
Alberty R., Daniels F., "Fisicoqumica ", versin SI, Ira ed, Cia Ed. Continental,
Mxico, 1984.
Atkins P.W., " Fisicoqumica", 2da ed., Ed. Addison Wesley, Iberoamerican, Mxico,
1988.
Barrow G., "Qumica Fsica", Tomos I y II, 3ra ed.. Ed. Revert, Barcelona, 1975
Castellan G., "Fisicoqumica ", Ira ed. Fondo Educativo Interamericano, Mxico,
1978.
CRC, " Handbook of Chemistry and Physics", 54 th ed., Ed CRC Press., 1975.
Marn S., Land J., "Fisicoqumica Fundamental", Ira ed.. Ed. Limusa, Mxico,
1978.
"Norbert Adolph Lange " Handbook of Chemistry", Ed. Me Graw Hill, Cleveland.
Palmer W.G., "Qumica Fsica Experimental", Ed. Eudeba, Buenos Aires, 1966.
Pons Muzzo, Gastn, " Fisico-quimica ", Primera ed.. Edit. Universo S.A. 1969
Lange, "Handboof of Chemistry", Ed. Me Graw Hill.
Jose Huapaya Barrientos Fisico-quimica Teoria y Problemas
CRC. "
Crioscopa
Pgina 22
También podría gustarte
- Curso Práctico de Química GeneralDe EverandCurso Práctico de Química GeneralCalificación: 4 de 5 estrellas4/5 (4)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Speech y Manejo de ObjecionesDocumento2 páginasSpeech y Manejo de ObjecionesMarvin AguirreAún no hay calificaciones
- 30 - Diferencia de WATTS RMS Y WATTS PEAKDocumento2 páginas30 - Diferencia de WATTS RMS Y WATTS PEAKfransober100% (4)
- Curso Bombas Lineales Mecanicas Material PDFDocumento113 páginasCurso Bombas Lineales Mecanicas Material PDFRomulo Fernando Astudillo BravoAún no hay calificaciones
- Constante CrioscopicaDocumento7 páginasConstante Crioscopicavanesa nonsoqueAún no hay calificaciones
- INFORME N°5 LABORATORIO - Terminado.Documento18 páginasINFORME N°5 LABORATORIO - Terminado.Melany Fernández.100% (1)
- FQ I Practica N - 6 Determinacion Crioscopica Del Peso MolecularDocumento18 páginasFQ I Practica N - 6 Determinacion Crioscopica Del Peso MolecularCarlos PalaciosAún no hay calificaciones
- Informe 5 Labo CriosDocumento22 páginasInforme 5 Labo CriosRosa María Quispe AznaránAún no hay calificaciones
- Fiqui N°6Documento14 páginasFiqui N°6Luis FrancoAún no hay calificaciones
- Informe de Viscosidad y DensidadDocumento23 páginasInforme de Viscosidad y DensidadEricBryanDagninoReyesAún no hay calificaciones
- Determinación Crioscópica Del Peso MolecularDocumento17 páginasDeterminación Crioscópica Del Peso Molecularcelina ninaAún no hay calificaciones
- Informe Oficial Fiqui CriosDocumento18 páginasInforme Oficial Fiqui CriosJuan Rodolfo Gomez RamosAún no hay calificaciones
- Determinacion Crioscopica Del Peso Molecular FinalDocumento13 páginasDeterminacion Crioscopica Del Peso Molecular FinalPier Navarro100% (1)
- Tecnicas de Laboratorio Cap. 7Documento14 páginasTecnicas de Laboratorio Cap. 7salamancagrossoAún no hay calificaciones
- Crioscopia LaboDocumento7 páginasCrioscopia Labosueño profundoAún no hay calificaciones
- Informe Peso Molecular FIQUIDocumento16 páginasInforme Peso Molecular FIQUIEDITH CAROL SUCAPUCA ESPIRITUAún no hay calificaciones
- Labo 6 - Determinacion Crioscópica Del Peso MolecularDocumento19 páginasLabo 6 - Determinacion Crioscópica Del Peso MolecularCarlos Jhozimar Gonzáles Caramantín67% (3)
- CrioscópiaDocumento15 páginasCrioscópiaLuis Iriarte LayaAún no hay calificaciones
- Práctica #4 Descenso Del Punto de Congelación de Un Solvente PuroDocumento21 páginasPráctica #4 Descenso Del Punto de Congelación de Un Solvente PuroMaría de los Ángeles Moreno CoronadoAún no hay calificaciones
- Crioscopia InformeDocumento21 páginasCrioscopia InformeRicardo Mercdz PAún no hay calificaciones
- CRIOSDocumento21 páginasCRIOSEduardo Manrique Hidalgo100% (1)
- CRIOSCOPICADocumento20 páginasCRIOSCOPICAAllen Steven SegoviaAún no hay calificaciones
- Propiedades Coaligativas Del Punto de CongelaciónDocumento3 páginasPropiedades Coaligativas Del Punto de CongelaciónKmilo OspinaAún no hay calificaciones
- Informe CriosDocumento17 páginasInforme CriosEdgar Ormeño RamirezAún no hay calificaciones
- LAB3DETFWDEPREFREEZPNTDocumento8 páginasLAB3DETFWDEPREFREEZPNTMichelleAún no hay calificaciones
- TP 5 Crioscopia RehechoDocumento17 páginasTP 5 Crioscopia RehechosicilianomarAún no hay calificaciones
- Practica 4 Laboratorio de Fisicoquímica IiDocumento19 páginasPractica 4 Laboratorio de Fisicoquímica IiLuis Angel GomezAún no hay calificaciones
- Determinación Del Peso Molar Por CrioscopíaDocumento5 páginasDeterminación Del Peso Molar Por CrioscopíaAlexa BedoyaAún no hay calificaciones
- METODOS FISICOS EN CONTROL DE CALIDAD TRABAJO FINAL - Wilver Cruz Ramos #36Documento8 páginasMETODOS FISICOS EN CONTROL DE CALIDAD TRABAJO FINAL - Wilver Cruz Ramos #36Wilver Crz RmsAún no hay calificaciones
- Expo de FisicoquimicaDocumento4 páginasExpo de FisicoquimicaKarla LHAún no hay calificaciones
- Fisicoquimica Informe Peso MolecularDocumento17 páginasFisicoquimica Informe Peso MolecularedithAún no hay calificaciones
- Guía Teórico Práctica: Unidad Nº2Documento14 páginasGuía Teórico Práctica: Unidad Nº2cristianAún no hay calificaciones
- Informe Físicoquímica-CriosDocumento19 páginasInforme Físicoquímica-CriosDaniel Carmen OrozcoAún no hay calificaciones
- Crioscopia 1Documento7 páginasCrioscopia 1Gatita CrissAún no hay calificaciones
- Practica 11 Termodinámica Del EquilibrioDocumento14 páginasPractica 11 Termodinámica Del EquilibrioMiguel Angel Burgos MercadoAún no hay calificaciones
- Informe 2Documento10 páginasInforme 2JeanCarloNoreñaAún no hay calificaciones
- Crioscopia Labo de Fiqui UNMSMDocumento12 páginasCrioscopia Labo de Fiqui UNMSMAlan J. López DíazAún no hay calificaciones
- CRIOSDocumento14 páginasCRIOScelina ninaAún no hay calificaciones
- Inf 6 Fiqui AiDocumento11 páginasInf 6 Fiqui AiKATHERINNE LUZ CHUCO DE LA CRUZAún no hay calificaciones
- Crioscopia FiquiDocumento14 páginasCrioscopia FiquiElion Vicente Fuentes RuizAún no hay calificaciones
- Constantes Fisicas Compuestos OrganicosDocumento9 páginasConstantes Fisicas Compuestos Organicosgiordan_13Aún no hay calificaciones
- Informe de Laboratorio Fisicoquímica N°5Documento7 páginasInforme de Laboratorio Fisicoquímica N°5Maricielo CerroAún no hay calificaciones
- Informe ColigativasDocumento14 páginasInforme ColigativasJose R. HernandezAún no hay calificaciones
- Guia Lab 4 FQ - Det Peso Molecular 2023 - 2Documento5 páginasGuia Lab 4 FQ - Det Peso Molecular 2023 - 2fiorella.flores.mAún no hay calificaciones
- Guía Práctica 6a - DCDocumento5 páginasGuía Práctica 6a - DCSebasas GonzalezAún no hay calificaciones
- 2 Disminucionpuntconge 2012Documento9 páginas2 Disminucionpuntconge 2012Damian Ashton J. DominguezAún no hay calificaciones
- Propiedades ColigativasDocumento8 páginasPropiedades ColigativasJhon Fuentes GallegoAún no hay calificaciones
- Lab 3Documento37 páginasLab 3Gabriela BenaventeAún no hay calificaciones
- Crioscopia Lab QuimicaDocumento8 páginasCrioscopia Lab QuimicaRosa PatiñoAún no hay calificaciones
- Propiedades ColigativasDocumento4 páginasPropiedades ColigativasHector Ivan Cordoba BuenoAún no hay calificaciones
- Determinacion D Masa Molar Mediante CriosDocumento6 páginasDeterminacion D Masa Molar Mediante Crios.:("*"BLacK BuLLeT"*"):.100% (2)
- Propiedades Coligativas ReporteDocumento16 páginasPropiedades Coligativas ReporteRick RodriguezAún no hay calificaciones
- Informe N°6 de Fisicoquímica AIDocumento14 páginasInforme N°6 de Fisicoquímica AIConstanza Coronado RiveraAún no hay calificaciones
- Informe 10 CriosDocumento7 páginasInforme 10 CriosMi LeAún no hay calificaciones
- Informe 8 - DETERMINACION MICROSCOPICA DE LA MASA MOLARDocumento9 páginasInforme 8 - DETERMINACION MICROSCOPICA DE LA MASA MOLARMarLoNzHiTOoº XikoAún no hay calificaciones
- #1 CriosDocumento12 páginas#1 CrioscristianAún no hay calificaciones
- Informe de Laboratorio Experiencia #2 Propiedades ColigativasDocumento6 páginasInforme de Laboratorio Experiencia #2 Propiedades ColigativasKEISY CAROLINA MARRIAGA TORRESAún no hay calificaciones
- Temperatura de EbullicionDocumento13 páginasTemperatura de EbullicionCarolina De La Cruz ContrerasAún no hay calificaciones
- Informe 2. Determinación de Masas Moleculares de Solutos No VolatilesDocumento8 páginasInforme 2. Determinación de Masas Moleculares de Solutos No VolatilesJUAN MIGUEL VELEZ GARCIAAún no hay calificaciones
- Modelo de Encuesta de ReciclajeDocumento2 páginasModelo de Encuesta de ReciclajeMarvin AguirreAún no hay calificaciones
- IQ1 Info1 Bombas Centrífugas FinalDocumento56 páginasIQ1 Info1 Bombas Centrífugas FinalMarvin AguirreAún no hay calificaciones
- Modelo de Encuesta de MercadoDocumento3 páginasModelo de Encuesta de MercadoMarvin AguirreAún no hay calificaciones
- Avance Del Informe de SecadorDocumento46 páginasAvance Del Informe de SecadorMarvin AguirreAún no hay calificaciones
- Proceso de VentaDocumento24 páginasProceso de VentaMarvin AguirreAún no hay calificaciones
- Organizador GráficoDocumento1 páginaOrganizador GráficoMarvin AguirreAún no hay calificaciones
- Diseño de Una Columna de DestilaciónDocumento9 páginasDiseño de Una Columna de DestilaciónMarvin AguirreAún no hay calificaciones
- Tabulacion de DatosnuevoDocumento29 páginasTabulacion de DatosnuevoMarvin AguirreAún no hay calificaciones
- Obra CorazonDocumento18 páginasObra CorazonMarvin AguirreAún no hay calificaciones
- Raman - F. PortocarreroDocumento9 páginasRaman - F. PortocarreroMarvin AguirreAún no hay calificaciones
- Informe Hospedaje Milan 2.0Documento86 páginasInforme Hospedaje Milan 2.0kiaraAún no hay calificaciones
- Coeficiente de RepartoDocumento13 páginasCoeficiente de Repartoangie yaneth100% (1)
- DiaposDocumento16 páginasDiaposDiegoAún no hay calificaciones
- Puerto de Coveñas Electiva ViDocumento15 páginasPuerto de Coveñas Electiva ViJENNY ACUNA RINCONAún no hay calificaciones
- Proyecto de InnovcionDocumento47 páginasProyecto de InnovcionJavier Quispe Hualpa100% (1)
- CalderosDocumento9 páginasCalderosValery GarciaAún no hay calificaciones
- Analisis Funcional de CSVDocumento36 páginasAnalisis Funcional de CSVEduardo PintoAún no hay calificaciones
- Condensador HorizontalDocumento6 páginasCondensador HorizontalJulian VelezAún no hay calificaciones
- Kundera Instalar Modulo AllienwindowsDocumento18 páginasKundera Instalar Modulo AllienwindowsedilmerpAún no hay calificaciones
- CV Luis Pucutay LeonDocumento2 páginasCV Luis Pucutay LeonLuis Pucutay LeónAún no hay calificaciones
- Ficha Tecnica Perno Expansivo 1Documento2 páginasFicha Tecnica Perno Expansivo 1Pedro Mendoza100% (1)
- UNI-SGS-FO-B4 Cronograma de Charla de Inicio en Obra y Capacitaciones en Obra Ver. 00Documento1 páginaUNI-SGS-FO-B4 Cronograma de Charla de Inicio en Obra y Capacitaciones en Obra Ver. 00Gian SPAún no hay calificaciones
- Trabajo Final de FluidosDocumento4 páginasTrabajo Final de FluidossebastianAún no hay calificaciones
- Flujograma de Procesos de La Esterilización de Los MaterialesDocumento1 páginaFlujograma de Procesos de La Esterilización de Los MaterialesEnny Vaca33% (3)
- Desarrollo de Aplicaciones para Ambientes DistribuidosDocumento19 páginasDesarrollo de Aplicaciones para Ambientes DistribuidosHemerson MartinezAún no hay calificaciones
- La Importancia de La TelevisiónDocumento2 páginasLa Importancia de La TelevisiónWilson OrtizAún no hay calificaciones
- Diagrama Árbol PDFDocumento4 páginasDiagrama Árbol PDFEsteban TecoAún no hay calificaciones
- Ejercicios de Estadistica en ExcelDocumento7 páginasEjercicios de Estadistica en ExcelLitz Norma TFAún no hay calificaciones
- Pajuelo-De La Cruz-Vera FinalDocumento82 páginasPajuelo-De La Cruz-Vera Finaljskd3643Aún no hay calificaciones
- Seminario 1 Ley TermodinámicaDocumento2 páginasSeminario 1 Ley TermodinámicaDiego MillaAún no hay calificaciones
- PCP Ii WRD-S3.1Documento28 páginasPCP Ii WRD-S3.1gemaAún no hay calificaciones
- DeadlockDocumento3 páginasDeadlockjoss_majoAún no hay calificaciones
- 6 Tratamientos Termicos y TermoquimicosDocumento22 páginas6 Tratamientos Termicos y TermoquimicosJesus Presa PerezAún no hay calificaciones
- ID - Solucionario Ud01 PDFDocumento12 páginasID - Solucionario Ud01 PDFReda Allaiouti El HammamAún no hay calificaciones
- Gabriel Alejandro Buitrago Colorado PDFDocumento4 páginasGabriel Alejandro Buitrago Colorado PDFDigital Print NorteAún no hay calificaciones
- Cuerpo NegroDocumento11 páginasCuerpo NegroCarolina Livier RecioAún no hay calificaciones
- Procedimiento para La Aplicación de Ensayos No Destructivos: Líquidos PenetrantesDocumento15 páginasProcedimiento para La Aplicación de Ensayos No Destructivos: Líquidos PenetrantesJesus Ysidro IsidroAún no hay calificaciones
- Propiedades Extensivas de La MateriaDocumento4 páginasPropiedades Extensivas de La MateriaAnder LopezAún no hay calificaciones