Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Gms 071 C
Gms 071 C
Cargado por
Ana GabyTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Gms 071 C
Gms 071 C
Cargado por
Ana GabyCopyright:
Formatos disponibles
medigraphic
Fisiologa del sistema de coagulacin
Jaime Garca-Chveza, Ral Carrillo-Esperb y Abraham Majluf-Cruzc,*
Artemisa en lnea
aDepartamento de Hematologa, UMAE Antonio Fraga Mouret. Centro Mdico Nacional La Raza, IMSS, Mxico, D.F., Mxico bColegio Mexicano de Anestesia, Mxico, D.F., Mxico cUnidad de Investigacin Mdica en Trombosis, Hemostasia y Aterognesis. Hospital General Regional Gabriel Mancera, IMSS, Mxico,
D.F., Mxico
RESUMEN
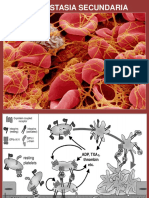
El endotelio intacto mantiene la sangre en estado lquido por diversos mecanismos. Ante una lesin, la hemostasia detiene la hemorragia en dos fases. La hemostasia primaria controla la hemorragia por vasoconstriccin y activacin plaquetaria y es temporal. A la formacin de fibrina se le llama hemostasia secundaria. La formacin del cogulo plaquetario requiere de diversos pasos comprendidos en la fisiologa plaquetaria incluyendo la adhesin plaquetaria, su conversin en esferas con pseudpodos y la secrecin de agonistas que permiten la agregacin. La hemostasia requiere de una red de fibrina para fortificar al cogulo plaquetario. La fase fluida convierte al fibringeno en fibrina mediante trombina. La formacin de esta depende de dos vas que difieren en la manera de activar al factor X (FX) ya que comparten una va comn despus de activarlo. El fibringeno activado o monmero de fibrina se polimeriza y forma fibrillas. Adems, la trombina activa otros factores; se autoactiva y activa y agrega plaquetas. La activacin directa por la va extrnseca es breve e insuficiente para sostener la hemostasia por lo que la intrnseca es indispensable para la persistencia hemosttica. La fibrinolisis y hemostasia se relacionan estrechamente formando y degradando fibrina. La fibrinolisis previene el depsito de fibrina en el vaso e impide la obstruccin del flujo sanguneo y depende de la enzima plasmina la cual hidroliza al fibringeno (fibringenolisis) y a la fibrina (fibrinolisis) produciendo productos de degradacin del fibringeno o de la fibrina. La formacin del cogulo ocurre y se mantiene slo donde y cuando es necesario. Su inicio, crecimiento y mantenimiento estn estrechamente regulados, temporal y espacialmente. El plasma tiene agentes que inhiben la actividad de factores hemostticos y fibrinolticos, los cuales limitan y localizan la hemostasia y la fibrinolisis.
ABSTRACT
The endothelium has several functions. While intact it maintains blood in a fluid state due to the action of several anticoagulant mechanisms. After wound occurred, hemostasis stops bleeding in two steps. The first is not permanent but helps controlling hemorrhage by vasoconstriction and platelet activation. Secondary hemostasis encompasses the fibrin formation process. Platelet cloth requires platelet adhesion, conversion of platelets into spheres, and secretion of agonists that allow platelet aggregation. Hemostasis requires a fibrin network in order to strength the platelet cloth. Fluid phase of hemostasis converts fibrinogen into fibrin by using thrombin at the end of these reactions. Thrombin generation depends on two pathways that differ in the way they activate FX although they follow a common pathway after activation of this last factor. Activated fibrinogen, also called fibrin monomer, polymerizes and forms fibrils. Moreover, thrombin auto-activates and activates several other hemostatic factors and platelets. Direct activation of secondary hemostasis through extrinsic pathway is brief and insufficient to hold hemostasis properly. Therefore, intrinsic pathway is a condition to achieve an adequate hemostatic function. Both, fibrinolysis and hemostasis deeply interact each other forming and degrading fibrin. Fibrinolysis prevents fibrin deposition in the vessel impeding obstruction of blood flow. It depends on plasmin which hidrolyses fibrinogen (fibrinogenlysis) and fibrin (fibrinolysis). Cloth formation occurs and persists only when and it is necessary. Starting, growing and maintenance of cloths are closely regulated in time and space. Human plasma has several agents that inhibit the activity of hemostatic and fibrinolytic factors and that may localize and regulate the hemostatic and fibrinolytic processes.
Palabras clave Hemostasia, fibrinolisis, plaquetas, trombina, plasmina.
Key words Hemostasis, fibrinolysis, platelets, thrombin, plasmin.
Introduccin
El endotelio tiene numerosas funciones. El endotelio intacto expresa anticoagulantes y profibrinolticos; vasodilatadores que inhiben a las plaquetas (prostaciclina y xido ntrico); expresa glicosaminoglicanos semejantes a la heparina que activan a la antitrombina (AT) para inhibir factores hemostticos activados; expresa trombomodulina
(Tm) que se une a la trombina para hacerla antihemosttica (el exceso de trombina intravascular se une a la Tm y activan a la protena C (PC), la cual detiene la generacin de trombina).
Hemostasia
Ante una lesin la hemostasia se activa para detener la hemorragia. Tiene dos fases. La hemostasia primaria controla la
* Correspondencia y solicitud de sobretiros: Abraham Majluf Cruz. Unidad de Investigacin Mdica en Trombosis, Hemostasia y Aterognesis Hospital General Regional Gabriel Mancera, IMSS Apartado Postal 12-1100, Mxico 12, D.F., Mxico
Gac Md Mx Vol. 143 Supl 1, 2007
Fisiologa de la coagulacin hemorragia mediante vasoconstriccin y activacin plaquetaria y es temporal. Al fenmeno de la formacin de la fibrina se le denomina hemostasia secundaria y su funcin es reforzar el tapn hemosttico. La vasoconstriccin es crucial en el control rpido de la hemorragia.1 El endotelio controla todo el sistema. Luego de una lesin, el endotelio antihemosttico se vuelve prohemosttico: secreta factor tisular (FT), genera trombina, permite la adhesin plaquetaria y produce activadores de plaquetas, leucocitos y monocitos.2 El flujo sanguneo cambia la fluidez y hemostasia normales,3 facilita el transporte de plaquetas y factores a la lesin y limpia el rea de plaquetas y factores activados. Los leucocitos y los eritrocitos intervienen en la hemostasia; estos ltimos influencian la hemostasia al liberar adenosn difosfato para la adhesin plaquetaria y aumentan la reactividad plaquetaria. Los neutrfilos inhiben la activacin plaquetaria y su reclutamiento, modulando el tamao del cogulo. La conversin depende de la trombina. La formacin de trombina depende de dos vas o cascadas de reacciones. La va extrnseca se activa cuando la sangre se pone en contacto con los tejidos ya que el nico factor que se encuentra fuera de la circulacin (extrnseco), es el FT. La va intrnseca se llama as porque todos sus factores se encuentran en la sangre; se inicia al contacto del FXII con superficies extraas. Las vas difieren en la manera de activar el FX ya que comparten una va comn despus de activarlo. Existen mecanismos de retroalimentacin e interaccin entre ambas por lo que es difcil identificar un factor como perteneciente a una sola va. En la fase fluida los zimgenos se convierten en enzimas y esta enzima activa al zimgeno siguiente en la cascada.5 Se amplifica un estmulo pequeo inicial que progresa hasta trombina. Las reacciones hemostticas ocurren slo en presencia de membranas activadas de plaquetas, leucocitos o endotelio lo que limita la hemostasia al sitio de lesin. El fibringeno se convierte en fibrina por efecto de la trombina.6 El fibringeno activado o monmero de fibrina se polimeriza y forma fibrillas que se degradan fcilmente por la plasmina. El FII se convierte en trombina al final de la fase fluida. La conversin del FII depende del FXa en presencia de FV activado (FVa), fosfolpidos y calcio (complejo de protrombinasa). 7 La trombina cumple varias funciones hemostticas. Rompe al fibringeno y produce fibrina; activa a los factores XIII, V, VIII, XI y PC; se autoactiva; y activa y agrega plaquetas. Realmente, la fase fluida se inicia por la va extrnseca, sin embargo, la intrnseca se requiere para mantener y amplificar la formacin de fibrina. Luego de una lesin el FT se pone en contacto con la sangre donde se une inmediatamente al FVII convirtindolo en FVIIa.8 La va extrnseca se inicia con el complejo FT-FVII9 que activa al FX y al FIX.10 En el FX convergen las vas intrnseca y extrnseca; la activacin directa depende del complejo FT-FVIIa y la indirecta del FIXa pero ambas vas son necesarias en la hemostasia normal. La activacin directa por la va extrnseca es breve e insuficiente para sostener la hemostasia por lo que la va intrnseca es indispensable para la persistencia hemosttica.11 La va intrnseca se inicia al contacto de la sangre con clulas no hemticas o con superficies extraas al vaso (12). El FIX se activa por ambas vas de la fase fluida y se convierte en FIXa que a su vez convierte al FX en FXa en presencia del FVIIIa, fosfolpidos y calcio (complejo "diezasa").13,14
Plaquetas
Son restos citoplasmticos de los megacariocitos. Tienen grnulos que contienen mltiples factores hemostticos e inflamatorios y actina que retrae el cogulo y que permite el cambio de forma y contraccin plaquetarias. El sistema canalicular citoplasmtico le permite intercambiar sustancias con el plasma. Su membrana activada acelera la hemostasia. La formacin del cogulo plaquetario tiene varias etapas. Primero se adhieren al subendotelio expuesto a la sangre, se unen al colgeno vascular y luego se convierten en esferas con pseudpodos. Despus inicia la secrecin de sustancias que aceleran la formacin del cogulo y la reparacin tisular. Los agonistas se unen a sus receptores plaquetarios y permiten la unin a otras plaquetas haciendo crecer el cogulo (agregacin). El fibringeno y su receptor, la glicoprotena IIb/ IIIa, son necesarios para la agregacin. Las plaquetas activas aceleran la formacin de fibrina al proveer los fosfolpidos de las reacciones de la fase fluida. La membrana activada expone fosfolpidos negativos, expresa ligandos para los factores Va, VIIIa, IX, IXa y Xa y ofrece una superficie ideal para las reacciones hemostticas.
Fase fluida de la hemostasia
La hemostasia requiere de una red de fibrina insoluble formada en la fase fluida de la hemostasia para fortificar al cogulo plaquetario. Los factores permanecen en la sangre aunque algunos son extravasculares en concentraciones mnimas. El FT extravascular se activa al contacto con la sangre. Los factores II, VII, IX y X, dependen de la vitamina K para su sntesis heptica. Tienen diez a doce cidos -carboxiglutmico que se unen al calcio, puente entre los factores y la superficie de fosfolpidos.4 Si los factores no tienen completos sus cidos -carboxiglutmico por deficiencia de vitamina K, son intiles hemostticamente. Los anticoagulantes orales inhiben el reciclaje heptico de la vitamina K lo que resulta en una deficiencia de cido -carboxiglutmico en los factores dependiente de la vitamina K. El objetivo de la fase fluida es convertir una protena plasmtica soluble, el fibringeno, en otra insoluble, la fibrina.
Fibrinolisis
Aunque opuestos aparentemente, fibrinolisis y hemostasia se relacionan estrechamente formando y degradando fibrina. La fibrinolisis o disolucin de cogulos fibrinoides previene el depsito de fibrina en el vaso e impide la obstruccin del flujo sanguneo. La lisis prematura del cogulo produce hemorragia o su reactivacin en la lesin. La fibrinolisis depende de la enzima plasmina que se encuentra en el plasma como plasmingeno. La fibrinolisis es una cascada de zimgenos, enzimas activas y sus inhibidores. Normalmente, se encuentra en reposo. Como se activa y regula para disolver la fibrina circulante sin lisar el cogulo verdadero depende de la produccin y liberacin endotelial del activador tisular del plasmingeno (aTP) y su inhibidor (IaTP-1); de la depuracin de aTP; de la
Gac Md Mx Vol. 143 Supl 1, 2007
Garca-Chvez y cols. activacin del plasmingeno; y de la inhibicin de la activacin y efecto de la plasmina.15 La activacin de la fibrinolisis ocurre sobre la membrana celular en donde la plasmina queda protegida de la inactivacin. El plasmingeno se encuentra en el plasma y otros fluidos. La plasmina hidroliza al fibringeno (fibringenolisis) y a la fibrina (fibrinolisis) produciendo productos de degradacin del fibringeno o de la fibrina.16 Existen activadores del plasmingeno intrnsecos y extrnsecos. Los primeros actan cuando la sangre contacta superficies extraas. Los extrnsecos estn fuera de la sangre en casi todos los tejidos: aTP, el activador del plasmingeno tipo urocinasa y la urocinasa. El aTP liberado del endotelio tiene una gran afinidad por la fibrina y es clave en la fibrinolisis. La urocinasa se excreta por orina y activa al plasmingeno del endotelio urogenital.17 La estreptocinasa, derivada del cultivo de estreptocos b-hemolticos, activa al plasmingeno cuando hace complejo con l. por un receptor endotelial para trombina, la Tm. sta inhibe la activacin del fibringeno, FV y plaquetas por trombina; permite la activacin de la PC por trombina; y aumenta la inhibicin de la trombina por AT.19 La PC activada se une a la PS e inhibe a los factores Va y VIIIa en un fenmeno anticoagulante trascendental.
Referencias
1. Zucker MB. Platelet agglutination and vasoconstriction as factors in spontaneous hemostasis in normal, thrombocytopenic, heparinized, and hypothrombinemic rats. Am J Phyisol 1947;148:275-278. Geng JG, Bevilacqua MP, Moore KL, McIntyre TM, Prescott SM, Kim JM, et al. Rapid neutrophil adhesion to activated endothelium mediated by GMP-140. Nature 1990;343:757-760. Slack SM, Cui Y, Turitto VT. The effects of flow on blood coagulation and thrombosis. Thromb Haemost 1993;70:129-134. Stenflo J, Fernlund P, Egan W, Roepstorff P. Vitamin Kdependent modifications of glutamic acid residues in prothrombin. Proc Natl Acad Sci USA 1974;71:2730-2733. Furie B, Furie C. Molecular and cellular biology of blood coagulation. N Engl J Med 1992;326:800-806. Blombck B, Blombck M. The molecular structure of fibrinogen. Ann NY Acad Sci 1972;202:77-97. Mann KG, Jenny RJ, Krishnaswamy S. Cofactor proteins in the assembly and expression of blood clotting enzyme complexes. Annu Rev Biochem 1988;57:915956. Bevilacqua MP, Pober JS, Majeau GR. Interleukin 1 (IL-1) induces biosynthesis and cell surface expression of procoagulant activity in human vascular endothelial cells. J Exp Med 1984;160:618-623. Yamamoto M, Nakagaki T, Kisiel W. Tissue factor-dependent autoactivation of human blood coagulation factor VII. J Biol Chem 1992;267:19089-19094. Osterud B, Rapaport SI. Activation of factor IX by the reaction product of tissue factor and factor VII: Additional pathway for initiating blood coagulation. Proc Natl Acad Sci USA 1977;74:5260-5264. Davie EW, Fujikawa K, Kisiel W. The coagulation cascade: Initiation, maintenance, and regulation. Biochemistry 1991;30:10363-10370. Majluf-Cruz A, DeLa Cadena R. El sistema de contacto: su papel en la hemostasia y su relacin con otros sistemas biolgicos. En: Martnez-Murillo C, Quintana-Gonzlez S. Manual de hemostasia y trombosis. Editorial Prado, 1996. Bauer KA, Kass BL, ten Cate H, Hawiger JJ, Rosenberg RG. Factor IX is activated in vivo by the tissue factor mecahnism. Blood 1990;76:731-736. Ruggeri ZM, Ware J. von Willebrand factor. FASEB J 1993;7:308-316. Loskutoff DJ, Sawdey M, Keeton M, Schneiderman J. Regulation of PAI-1 gene expression in vivo. Thromb Haemost 1993;70:135-137. Marder VJ, Shulman NR, Carroll, WR. High molecular weight derivatives of human fibrinogen produced by plasmin. I. Physicochemical and immunological characterization. J Biol Chem 1969;244:2111-2119. Sappino AP, Huarte J, Vassalli J-D, Belin D. Sites of synthesis of urokinase and tissue-type plasminogen activators in the murine kindey. J Clin Invest 1991;87:762-770. Rosenberg RD, Rosenberg SJ. Natural anticoagulant mechanisms. J Clin Invest 1984;74:1-6. Esmon CT. The roles of protein C and thrombomodulin in the regulation of blood coagulation. J Biol Chem 1989;264:4743-4746.
2.
3. 4.
5.
Regulacin del sistema de coagulacin
Al lesionarse un vaso se forma el cogulo que no se extiende a lo largo del lumen ni tampoco lo ocluye. La formacin del cogulo ocurre y se mantiene slo donde y cuando es necesario. Con el tiempo, se reemplaza por tejido conectivo. El inicio, crecimiento y mantenimiento del cogulo estn estrechamente regulados, temporal y espacialmente. Dos fenmenos limitan la propagacin del cogulo, el endotelio anticoagulante y la dependencia de hemosttica y fibrinoltica de una superficie celular. El movimiento de la sangre limpia el sitio de lesin del exceso de factores y plaquetas activados. Para que el trombo se forme se requieren estasis venosa y estado protrombtico. Adems, el plasma tiene agentes que inhiben la actividad de factores hemostticos y fibrinolticos. Los naturales son la AT, el cofactor II de la heparina, la 2-antiplasmina, IaTP-1, el inhibidor de la PCa y el inhibidor de la va del factor tisular (IVFT) los cuales limitan y localizan la hemostasia y la fibrinolisis. La AT es el inhibidor ms importante de la trombina y de los factores XIIa, XIa, Xa, IXa, TF-VIIIa, calicrena y plasmina.18 Su efecto es acelerado por la heparina. El IVFT modula la va extrnseca inhibiendo al complejo FT-FVIIa. La fibrinolisis se considera como el principal modulador de la hemostasia. La generacin de trombina est regulada por mecanismos que regulan las cascadas siendo el ms importante el de la PC, compuesto por dos protenas K-dependientes, PC y S (PS), y
6. 7.
8.
9. 10.
11. 12.
13. 14. 15. 16.
17.
18. 19.
Gac Md Mx Vol. 143 Supl 1, 2007
También podría gustarte
- 8468015210Documento9 páginas8468015210nanitalr0% (1)
- Curso HEMACRIT PDFDocumento266 páginasCurso HEMACRIT PDFJose Antonio Giron Mombiela100% (1)
- Resumen de La HemostasiaDocumento4 páginasResumen de La HemostasiaPuga Octavio100% (1)
- Cascada de La Cuagulacion y Anemia - Irm GuamancelaDocumento10 páginasCascada de La Cuagulacion y Anemia - Irm GuamancelaCristian Geovanny GuamancelaAún no hay calificaciones
- Hemostáticos y Fármacos en El EmbarazoDocumento10 páginasHemostáticos y Fármacos en El EmbarazoJORGE ADAN RUIZ SANCHEZAún no hay calificaciones
- HEMOSTASIADocumento6 páginasHEMOSTASIAAracely Morales SanchezAún no hay calificaciones
- T23. Hemostasia y CoagulaciónDocumento6 páginasT23. Hemostasia y Coagulaciónjulia.casteraAún no hay calificaciones
- Diatesis HemorragicaDocumento9 páginasDiatesis HemorragicaAlexis M-cAún no hay calificaciones
- Hemostasia SecundariaDocumento26 páginasHemostasia SecundariaMonserrat Duarte MunozAún no hay calificaciones
- Desórdenes de La CoagulaciónDocumento56 páginasDesórdenes de La CoagulaciónJorge Adrián Laura BasurcoAún no hay calificaciones
- pracTICA N9Documento26 páginaspracTICA N9Ernesto GarciaAún no hay calificaciones
- Fisiopatología de La HemostasiaDocumento3 páginasFisiopatología de La HemostasiaGianPier MonjeAún no hay calificaciones
- Unidad 16Documento10 páginasUnidad 16Jose floAún no hay calificaciones
- T6 LuciaDocumento8 páginasT6 LuciaRocio GonzalezAún no hay calificaciones
- Importancia Fisiologica de La HemostasiaDocumento14 páginasImportancia Fisiologica de La HemostasiaKarenLópezAragónAún no hay calificaciones
- Hemostasia, Exposición OralDocumento10 páginasHemostasia, Exposición OralLeo SarapuraAún no hay calificaciones
- Proceso de La CoagulacionDocumento3 páginasProceso de La CoagulacionPablo Ramirez EspinozaAún no hay calificaciones
- Cascada de CoagulaciónDocumento13 páginasCascada de CoagulaciónDaniela SandovalAún no hay calificaciones
- Tema 2: Alteraciones de La Hemostasia: Diátesis Hemorrágica Y Diátesis TrombóticaDocumento11 páginasTema 2: Alteraciones de La Hemostasia: Diátesis Hemorrágica Y Diátesis TrombóticaMarina Navarro SavallAún no hay calificaciones
- Fisiología de La CoagulaciónDocumento16 páginasFisiología de La CoagulaciónAndony De Los RíosAún no hay calificaciones
- Fin 17Documento3 páginasFin 17Maria Virginia Sosa RodriguezAún no hay calificaciones
- Hemostasia PDFDocumento11 páginasHemostasia PDFM Cristina Pg100% (1)
- Pasos de La HemostasiaDocumento10 páginasPasos de La HemostasiaVANESSA ITZEL GUTIERREZ HERNANDEZAún no hay calificaciones
- Clase 13 HematologiaDocumento43 páginasClase 13 HematologiaKATHERINE ANDREA JULCA ALARCÓNAún no hay calificaciones
- ATT 1371307276175 Modulo 2 Curso MedTransfDocumento35 páginasATT 1371307276175 Modulo 2 Curso MedTransfCarlos Picó RodríguezAún no hay calificaciones
- Coagulacion SANGUINEADocumento12 páginasCoagulacion SANGUINEANarcisa LeonAún no hay calificaciones
- Fisiología de La Coagulación. ResumenDocumento3 páginasFisiología de La Coagulación. ResumenAna HernandezAún no hay calificaciones
- G4 HemostasiaDocumento8 páginasG4 HemostasiaAldana Mabel AlmarazAún no hay calificaciones
- HemostasiaDocumento3 páginasHemostasiaAbileneAún no hay calificaciones
- Hemtatologia Tema 7Documento8 páginasHemtatologia Tema 7Lauren Hunyi SánchezAún no hay calificaciones
- CoagulaciónDocumento18 páginasCoagulaciónAnildibethAún no hay calificaciones
- Trastornos de La HemostasiaDocumento12 páginasTrastornos de La Hemostasiaarios_409594Aún no hay calificaciones
- Hemostasia TrabajoDocumento15 páginasHemostasia Trabajogabriela correaAún no hay calificaciones
- T4 - Ciru - Hemostasia y Transfusion SanguineaDocumento14 páginasT4 - Ciru - Hemostasia y Transfusion SanguineaPablo Segales BautistaAún no hay calificaciones
- Charla de HemaDocumento15 páginasCharla de HemaYaxuri Yuil JaénAún no hay calificaciones
- 2 - HemostasiaDocumento31 páginas2 - Hemostasiacarelia2Aún no hay calificaciones
- TrombofiliaDocumento13 páginasTrombofiliaAnny Diaz DussanAún no hay calificaciones
- HemostasiaDocumento9 páginasHemostasiaCarmina FernándezAún no hay calificaciones
- Hemostasia y TrombosisDocumento61 páginasHemostasia y TrombosisLorena ZepedaAún no hay calificaciones
- Pruebas de Hemostasia y Grupo Sanguineo 1Documento36 páginasPruebas de Hemostasia y Grupo Sanguineo 1LUIS DAVID SOLIS FLORESAún no hay calificaciones
- Monografia HemorragiaDocumento33 páginasMonografia HemorragiaRikardo C-b75% (4)
- Hemostasia - Wikipedia, La Enciclopedia Libre PDFDocumento19 páginasHemostasia - Wikipedia, La Enciclopedia Libre PDFEnrique Alfonso Martinez VegaAún no hay calificaciones
- Coagulación Eq5Documento23 páginasCoagulación Eq5Layna RiAún no hay calificaciones
- Practica de Homeostasia y CoagulaciónDocumento6 páginasPractica de Homeostasia y CoagulaciónnicolehurtadosAún no hay calificaciones
- Hemostasia - SeminarioDocumento16 páginasHemostasia - SeminarioJose LaizaAún no hay calificaciones
- Cascada de Coagulación..Documento15 páginasCascada de Coagulación..2207073Aún no hay calificaciones
- Cascada de CoagulacionDocumento6 páginasCascada de CoagulacionShanniaAún no hay calificaciones
- Exposicion PatologiaDocumento4 páginasExposicion PatologiaEmily TandazoAún no hay calificaciones
- Practica HemostasiaDocumento11 páginasPractica HemostasiaMariciell Larissa Gonzales TiconaAún no hay calificaciones
- Hemostasia y CoagulacionDocumento30 páginasHemostasia y CoagulacionEsme p.Aún no hay calificaciones
- Hemostasia y Trombosis AnatopatoDocumento10 páginasHemostasia y Trombosis Anatopatoss501100% (1)
- CoagulaciónDocumento19 páginasCoagulaciónRazo MateoAún no hay calificaciones
- HemostasiaDocumento16 páginasHemostasiaEderth CorderoAún no hay calificaciones
- HemostasiaDocumento3 páginasHemostasiaLuzAún no hay calificaciones
- Hemostasia PDFDocumento5 páginasHemostasia PDFFernanda GranilloAún no hay calificaciones
- Mecanismos de La HemostasiaDocumento18 páginasMecanismos de La HemostasiaAndres PelayoAún no hay calificaciones
- Httpseva - Uca.edu - Arpluginfile.php4320537mod - resourcecontent0Hemostasia20UCA - PDF 6Documento22 páginasHttpseva - Uca.edu - Arpluginfile.php4320537mod - resourcecontent0Hemostasia20UCA - PDF 6Francesca R. BettucciAún no hay calificaciones
- Tema 9-10. Técnicas de Análisis Hematologico en La Serie Plaquetaria. Alteraciones.Documento10 páginasTema 9-10. Técnicas de Análisis Hematologico en La Serie Plaquetaria. Alteraciones.juropopinarAún no hay calificaciones
- Hemostasia SecundariaDocumento7 páginasHemostasia Secundariala72559663Aún no hay calificaciones
- Trombopoyesis T - 3Documento43 páginasTrombopoyesis T - 3Josue Mosso Zarate100% (3)
- Coagulación Para Todos: Medicina Para TodosDe EverandCoagulación Para Todos: Medicina Para TodosCalificación: 4.5 de 5 estrellas4.5/5 (3)
- Trabajo Monografico EJE TEMATICO N°5 (Luciana Salina)Documento12 páginasTrabajo Monografico EJE TEMATICO N°5 (Luciana Salina)Luciana SalinaAún no hay calificaciones
- Algoritmo de Floyd-WarshallDocumento3 páginasAlgoritmo de Floyd-WarshallDiego FigueroaAún no hay calificaciones
- Sexsologia ForenceDocumento2 páginasSexsologia ForenceNATALLY RUIZAún no hay calificaciones
- Ochure Programa Integrado Consultor de Obras 29-03-2023Documento34 páginasOchure Programa Integrado Consultor de Obras 29-03-2023DAVID ISRAEL LAZO QUISPEAún no hay calificaciones
- Astrología y TarotDocumento7 páginasAstrología y TarotÀlexAún no hay calificaciones
- Investigación01-Darlenis FarrierDocumento6 páginasInvestigación01-Darlenis FarrierDarlenis FarrjerAún no hay calificaciones
- Hierro FundidoDocumento14 páginasHierro FundidoJose Luis TorresAún no hay calificaciones
- Curriculum Vitae 01Documento4 páginasCurriculum Vitae 01GermainLaymeMamaniAún no hay calificaciones
- Importancia de Sistema Ferroviario y Sus ComponentesDocumento6 páginasImportancia de Sistema Ferroviario y Sus ComponentesSheyla Iridian Cuadros PortugalAún no hay calificaciones
- M2S1 P1 RMP Practica 05 Mantenimiento PreventivoDocumento2 páginasM2S1 P1 RMP Practica 05 Mantenimiento PreventivoDAVID ESTEBAN BOJORQUEZ ANGULOAún no hay calificaciones
- Cuestionario de Septimo GradoDocumento2 páginasCuestionario de Septimo Gradoalejogames2202Aún no hay calificaciones
- MIN 2500-6000TL-X Quick GuideDocumento2 páginasMIN 2500-6000TL-X Quick Guidedavid mendozsAún no hay calificaciones
- Gaiman, Neil - Nieve Manzanas y Cristal AzogadoDocumento19 páginasGaiman, Neil - Nieve Manzanas y Cristal AzogadoNegenevAún no hay calificaciones
- Modelo 2024 28-02-2024Documento5 páginasModelo 2024 28-02-2024jeiconoxAún no hay calificaciones
- Factor Común Por Agrupación de TérminosDocumento5 páginasFactor Común Por Agrupación de TérminosCarlos Marcos Gutierrez LopezAún no hay calificaciones
- Aplicación de Las Medidas de Tendencia Central en Un Conjunto de Datos Cuantitativos AgrupadosDocumento21 páginasAplicación de Las Medidas de Tendencia Central en Un Conjunto de Datos Cuantitativos Agrupadosjaiome ramosAún no hay calificaciones
- Cuadernillo Estudiante 5to - GradoDocumento21 páginasCuadernillo Estudiante 5to - GradoItzel MendezAún no hay calificaciones
- Informe 1 Bandas de FrecuenciaDocumento7 páginasInforme 1 Bandas de FrecuenciaCesar Gaspar ChavezAún no hay calificaciones
- Examen EI 1 B 2020Documento2 páginasExamen EI 1 B 2020roberto garciaAún no hay calificaciones
- Capitulo #1 Quimica OrganicaDocumento11 páginasCapitulo #1 Quimica OrganicaNatac1onAún no hay calificaciones
- Producto Academico 3Documento3 páginasProducto Academico 3Zoilita Altamirano LeonAún no hay calificaciones
- Ejercicio Practico No 2 Administracion de InventariosDocumento2 páginasEjercicio Practico No 2 Administracion de InventariosricardoAún no hay calificaciones
- Diseño y Maquetación Web Con HTML5, CSS3 y JavaScriptDocumento5 páginasDiseño y Maquetación Web Con HTML5, CSS3 y JavaScriptjoseAún no hay calificaciones
- Matrix y El Mito de CavernaDocumento13 páginasMatrix y El Mito de CavernaFiorella GambaroAún no hay calificaciones
- Exp. Aprend. 7 Sesion 1Documento8 páginasExp. Aprend. 7 Sesion 1dey mamaniAún no hay calificaciones
- Informe Proyecto StemDocumento4 páginasInforme Proyecto StemEsteban MarinAún no hay calificaciones
- HDV Nijob 2022Documento16 páginasHDV Nijob 2022Nico OrtegónAún no hay calificaciones
- Estructuras de Acero - Ejemplo de Diseño de Edificio SMF y EBF PDFDocumento56 páginasEstructuras de Acero - Ejemplo de Diseño de Edificio SMF y EBF PDFCesar Lopez SequeiraAún no hay calificaciones
- Tensiometro de Correa - Tensometro Btm-400plusDocumento5 páginasTensiometro de Correa - Tensometro Btm-400plusJosé RodríguezAún no hay calificaciones