Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Actividad Fisicoquímica
Cargado por
Alvarado Fernández Juan Carlos0 calificaciones0% encontró este documento útil (0 votos)
11 vistas2 páginasFisicoquímica
Título original
Actividad fisicoquímica
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoFisicoquímica
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
11 vistas2 páginasActividad Fisicoquímica
Cargado por
Alvarado Fernández Juan CarlosFisicoquímica
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
- Alvarado Fernández Juan Carlos
- Pérez Galindo Yeraldi
- Sanchez Valdez Llanquiray
- Vázquez Mayo Isaías Daniel
Actividad fisicoquímica
1. ¿Cómo se clasifican los sistemas azeótropos según su punto de
ebullición?
- Azeotropos positivos (de ebullición mínima)
- Azeotropos negativos (de ebullición máxima)
2. ¿Cuál es la problemática de la separación de los compuestos
azeotrópicos en un sistema binario de componentes volátiles?
- La problemática en separar los compuestos azeotrópicos se
debe a que su volatilidad no es variada, ya que al hervir, su
fase de vapor tendrá la misma composición que la fase
líquida.
3. ¿Cómo se pueden separar los compuestos azeotrópicos en estás
condiciones?
- Seleccionando un tercer componente “arrastrador”, para
mejorar la volatilidad relativa de los componentes originales.
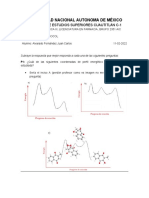
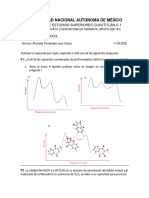
4. Dibuja los diagramas correspondientes a un azeótropo de ebullición
mínima
5. Dibuja los diagramas correspondientes a un azeótropo de ebullición
máxima
6. ¿Cómo se le denomina a la mezcla que tiene una presión de vapor
máxima o mínima?
Mezcla azeotrópica
7. ¿En qué caso se presenta una desviación positiva?
- En estos casos, Pi > Pideal i , o lo que es lo mismo γi > 1.
8. ¿En qué caso se presenta una desviación negativa?
-Un caso muy frecuente puede ser cuando las soluciones de
sustancias que puedan formar entre sí enlaces por puentes de
hidrógeno (ej. acetona-cloroformo), en cuyo caso Pi < Pideal i y γi
< 1.
9. ¿Cuando se presenta una desviación de la idealidad?
-Cuando las interacciones intermoleculares en la solución son más
débiles que en los líquidos puros, lo que implica que “las moléculas
pueden pasar a la fase gaseosa con mayor facilidad”.
También podría gustarte
- TAREADocumento5 páginasTAREAkevin santiagoAún no hay calificaciones
- Investigación Desviaciones de La IdealidadDocumento6 páginasInvestigación Desviaciones de La IdealidadAlvarado Fernández Juan CarlosAún no hay calificaciones
- AZEOTROPOSDocumento13 páginasAZEOTROPOSLuis Angel Murillo Perez100% (1)
- Sistemas Materiales Clase 4Documento6 páginasSistemas Materiales Clase 4roccovivio8Aún no hay calificaciones
- Liquido Vapor CorregidoDocumento21 páginasLiquido Vapor CorregidoGiselle SanchezAún no hay calificaciones
- Práctica 4. Laboratorio de TermodinámicaDocumento24 páginasPráctica 4. Laboratorio de TermodinámicaUlises Barrientos SánchezAún no hay calificaciones
- AZEÓTROPODocumento4 páginasAZEÓTROPOedyaspiAún no hay calificaciones
- Masa IIDocumento4 páginasMasa IIMaricruz LeónAún no hay calificaciones
- Destilación Tequila XalixcoDocumento6 páginasDestilación Tequila XalixcoJesus VillanuevaAún no hay calificaciones
- 2 .Informe de Quimica OrganicaDocumento4 páginas2 .Informe de Quimica OrganicaSergio CeronAún no hay calificaciones
- Ley de RaoultDocumento16 páginasLey de RaoultMara ArellanoAún no hay calificaciones
- Cuestionario Yamile CasalDocumento21 páginasCuestionario Yamile CasalFlores Villca GilbertoAún no hay calificaciones
- Sistema MaterialDocumento6 páginasSistema MaterialAlejandra Romero FracalossiAún no hay calificaciones
- Practica 4 "Destilación Simple y Fraccionada" AntecedentesDocumento1 páginaPractica 4 "Destilación Simple y Fraccionada" AntecedentesIthalya OlveraAún no hay calificaciones
- AzeótroposDocumento3 páginasAzeótroposSaul Abraham Marcial RodríguezAún no hay calificaciones
- Sistemas Homogeneos y Heterogeneos - RespuestasDocumento2 páginasSistemas Homogeneos y Heterogeneos - Respuestasvicenzobit2022Aún no hay calificaciones
- EXPERIMENTO No1 Clasificación y Propiedades de La MateriaDocumento5 páginasEXPERIMENTO No1 Clasificación y Propiedades de La MateriaMilagros GonzalezAún no hay calificaciones
- Equilibrio Líquido Vapor en Un Sistema No IdealDocumento3 páginasEquilibrio Líquido Vapor en Un Sistema No IdealDeyaniraAún no hay calificaciones
- Reporte 1LQOBequipo7Documento4 páginasReporte 1LQOBequipo7Jose GonzalesAún no hay calificaciones
- Transferencia de Masa II - Destilación AzeotrópicaDocumento9 páginasTransferencia de Masa II - Destilación AzeotrópicaEdwin Galvez TorresAún no hay calificaciones
- Portafolio DisolucionesDocumento11 páginasPortafolio Disolucionessamir osmaAún no hay calificaciones
- Trabajo Final de InvestigaciónDocumento5 páginasTrabajo Final de InvestigaciónAguirre Carbajal José LeonardoAún no hay calificaciones
- Cuestionario Experimento 1Documento6 páginasCuestionario Experimento 1Angel Javier100% (1)
- Vasquez Gutierrez-Química 2Documento8 páginasVasquez Gutierrez-Química 2damarisester73Aún no hay calificaciones
- Cuestionario CristalizacionDocumento4 páginasCuestionario CristalizacionAzul CuartenAún no hay calificaciones
- Tercera Actividad Domiciliaria de Ciencias NaturalesDocumento5 páginasTercera Actividad Domiciliaria de Ciencias Naturalesmansillag923Aún no hay calificaciones
- AzeotropoDocumento11 páginasAzeotropoDiamante Hernandez MeridaAún no hay calificaciones
- Cuestionario TP1Documento3 páginasCuestionario TP1Christian AssperianoAún no hay calificaciones
- Pre1 OperacionesDocumento6 páginasPre1 OperacionesIngeniera Pau JerezAún no hay calificaciones
- AzeótropoDocumento3 páginasAzeótroporicva_rjAún no hay calificaciones
- Mezclas Azeotropicas y Como SepararlasDocumento2 páginasMezclas Azeotropicas y Como SepararlasJordy Jimenez Infantes50% (2)
- Wuolah EnzimologíaDocumento8 páginasWuolah EnzimologíaRocio Piñero PérezAún no hay calificaciones
- Qué Son Los Azeótropos?: Azeotrópica. México D.F: Unam. Edición. España: Mcgraw-HillDocumento2 páginasQué Son Los Azeótropos?: Azeotrópica. México D.F: Unam. Edición. España: Mcgraw-HillProject ElizabethAún no hay calificaciones
- MezclasDocumento9 páginasMezclasVivian Simone Gariazzo CoutoAún no hay calificaciones
- Tarea - P2Documento9 páginasTarea - P2GIOISY MAILYN VALERIANO QUIROZAún no hay calificaciones
- Sistemas Materiales, 2021Documento6 páginasSistemas Materiales, 2021Soledad Rocio Quispe GuarachiAún no hay calificaciones
- Correccion Parcial Lab de Organic ADocumento6 páginasCorreccion Parcial Lab de Organic AjulianAún no hay calificaciones
- S1 Materia y Sus Propiedades 2022-20Documento34 páginasS1 Materia y Sus Propiedades 2022-20Diana Rebecca Rodríguez RuizAún no hay calificaciones
- AZEOTROPODocumento14 páginasAZEOTROPOThalia Milagros Siccha QuezadaAún no hay calificaciones
- Mezcla AzeotrópicaDocumento3 páginasMezcla AzeotrópicaYerson GuerraAún no hay calificaciones
- Examen de Ope 2 Falta Preguntas ChicasDocumento6 páginasExamen de Ope 2 Falta Preguntas ChicasALEXEY PATRICIO ZARATE RODRIGUEZAún no hay calificaciones
- Fisico Quimica - Sistemas MaterialesDocumento4 páginasFisico Quimica - Sistemas MaterialesEsteban VillarAún no hay calificaciones
- Soluciones - QuIMICADocumento11 páginasSoluciones - QuIMICAFederica HernandezAún no hay calificaciones
- Guia de Estudios 1Documento7 páginasGuia de Estudios 1Alfredo AlfaroAún no hay calificaciones
- Traduccion Del PaviaDocumento30 páginasTraduccion Del PaviaKarla Contreras de GonzalezAún no hay calificaciones
- Practica 7 - BalanceDocumento11 páginasPractica 7 - Balance1701635jAún no hay calificaciones
- Reporte Pruebas de SolubilidadDocumento6 páginasReporte Pruebas de SolubilidadHuesoVázquezAún no hay calificaciones
- Solubilidad y SolucionesDocumento5 páginasSolubilidad y SolucionesEdgar RomeroAún no hay calificaciones
- Quimica ExperimentoDocumento3 páginasQuimica ExperimentoLainiker IguaranAún no hay calificaciones
- Actividad 2Documento10 páginasActividad 2Adrian SantomilAún no hay calificaciones
- Informe QuimicaDocumento12 páginasInforme QuimicaKaren White OssandónAún no hay calificaciones
- Taller de EnzimasDocumento9 páginasTaller de EnzimasLau Ortiz TerrazaAún no hay calificaciones
- F.Q 3 Diagn-SticoDocumento28 páginasF.Q 3 Diagn-SticoGabriela R BellittiAún no hay calificaciones
- Material de Apoyo Propiedades ColigativasDocumento29 páginasMaterial de Apoyo Propiedades ColigativasHansAcevedoAún no hay calificaciones
- AZEOTROPOSDocumento2 páginasAZEOTROPOSjose luis pacheco100% (1)
- CUESTIONARIO TerminadoDocumento3 páginasCUESTIONARIO TerminadoDilver AsisAún no hay calificaciones
- Mezclas HomogeneasDocumento10 páginasMezclas HomogeneasYolandita CuevasAún no hay calificaciones
- DrugbankDocumento5 páginasDrugbankAlvarado Fernández Juan CarlosAún no hay calificaciones
- Alvarado Fernández Tarea AbsorciónDocumento3 páginasAlvarado Fernández Tarea AbsorciónAlvarado Fernández Juan CarlosAún no hay calificaciones
- Reporte Freccionamiento Celular y CloroplastosDocumento27 páginasReporte Freccionamiento Celular y CloroplastosAlvarado Fernández Juan CarlosAún no hay calificaciones
- Reporte PotenciometriaDocumento6 páginasReporte PotenciometriaAlvarado Fernández Juan CarlosAún no hay calificaciones
- Determinación de La Energía Libre Estándar de Micelización.Documento11 páginasDeterminación de La Energía Libre Estándar de Micelización.Alvarado Fernández Juan CarlosAún no hay calificaciones
- Avance de Reporte Fraccionamiento Celular y CloroplastosDocumento4 páginasAvance de Reporte Fraccionamiento Celular y CloroplastosAlvarado Fernández Juan CarlosAún no hay calificaciones
- Farmacia Hospitalaria Receta MédicaDocumento7 páginasFarmacia Hospitalaria Receta MédicaAlvarado Fernández Juan CarlosAún no hay calificaciones
- Cualitativa Ácido-BaseDocumento6 páginasCualitativa Ácido-BaseAlvarado Fernández Juan CarlosAún no hay calificaciones
- PosologíaDocumento20 páginasPosologíaAlvarado Fernández Juan CarlosAún no hay calificaciones
- Reporte MicrosDocumento8 páginasReporte MicrosAlvarado Fernández Juan CarlosAún no hay calificaciones
- Actividad Integradora Sistema DigestivoDocumento2 páginasActividad Integradora Sistema DigestivoAlvarado Fernández Juan CarlosAún no hay calificaciones
- Tarea FG BiotransformaciónDocumento8 páginasTarea FG BiotransformaciónAlvarado Fernández Juan CarlosAún no hay calificaciones
- Laboratorio Virtual Practica No.3 2 NitrotiofenoDocumento11 páginasLaboratorio Virtual Practica No.3 2 NitrotiofenoAlvarado Fernández Juan CarlosAún no hay calificaciones
- Equipo 4 - Actividad Integradora 2 - Sistema SomatosensorialDocumento11 páginasEquipo 4 - Actividad Integradora 2 - Sistema SomatosensorialAlvarado Fernández Juan CarlosAún no hay calificaciones
- Investigacion Previa Anatomía ComparadaDocumento8 páginasInvestigacion Previa Anatomía ComparadaAlvarado Fernández Juan CarlosAún no hay calificaciones
- Exposicion Del Previo 1 FisicoquímicaDocumento14 páginasExposicion Del Previo 1 FisicoquímicaAlvarado Fernández Juan CarlosAún no hay calificaciones
- Previo 1 FarmacologiaDocumento8 páginasPrevio 1 FarmacologiaAlvarado Fernández Juan CarlosAún no hay calificaciones
- Examen 1 - EpóxidoDocumento2 páginasExamen 1 - EpóxidoAlvarado Fernández Juan CarlosAún no hay calificaciones
- Investigación Previa Practica No.1 OxiranoDocumento15 páginasInvestigación Previa Practica No.1 OxiranoAlvarado Fernández Juan CarlosAún no hay calificaciones
- Investigación Previa Dihidropiridina Síntesis de HantzschDocumento16 páginasInvestigación Previa Dihidropiridina Síntesis de HantzschAlvarado Fernández Juan CarlosAún no hay calificaciones
- Reporte Freccionamiento Celular y CloroplastosDocumento4 páginasReporte Freccionamiento Celular y CloroplastosAlvarado Fernández Juan CarlosAún no hay calificaciones
- Practica 3 - Alvarado - Juan CarlosDocumento7 páginasPractica 3 - Alvarado - Juan CarlosAlvarado Fernández Juan CarlosAún no hay calificaciones
- Investigación Previa Formación Del BenzimidazolDocumento8 páginasInvestigación Previa Formación Del BenzimidazolAlvarado Fernández Juan CarlosAún no hay calificaciones
- Diagrama de Ven MicroscopiosDocumento2 páginasDiagrama de Ven MicroscopiosAlvarado Fernández Juan CarlosAún no hay calificaciones
- Examen 1 - EpóxidoDocumento2 páginasExamen 1 - EpóxidoAlvarado Fernández Juan CarlosAún no hay calificaciones
- Planos CorporalesDocumento6 páginasPlanos CorporalesAlvarado Fernández Juan CarlosAún no hay calificaciones
- Laboratorio VirtualDocumento17 páginasLaboratorio VirtualAlvarado Fernández Juan CarlosAún no hay calificaciones
- Reporte Practica No.1 Obtencion de Halogenuros de AlquiloDocumento18 páginasReporte Practica No.1 Obtencion de Halogenuros de AlquiloAlvarado Fernández Juan CarlosAún no hay calificaciones