Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Epilepsia
Epilepsia
Cargado por
lorien0 calificaciones0% encontró este documento útil (0 votos)
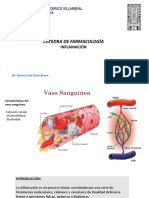
9 vistas2 páginasLas neuronas anormales que forman parte del foco de epileptogénesis muestran alteraciones estructurales y cambios en sus características eléctricas debido a la actividad de receptores ionotrópicos y metabotrópicos. Estos cambios condicionan modificaciones en los flujos iónicos y la transmisión sináptica que pueden producir brotes epilépticos cuando grupos de células anormales disparan descargas de potenciales de forma rítmica y sincrónica. Aunque la liberación de acetilcolina puede
Descripción original:
Título original
epilepsia
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoLas neuronas anormales que forman parte del foco de epileptogénesis muestran alteraciones estructurales y cambios en sus características eléctricas debido a la actividad de receptores ionotrópicos y metabotrópicos. Estos cambios condicionan modificaciones en los flujos iónicos y la transmisión sináptica que pueden producir brotes epilépticos cuando grupos de células anormales disparan descargas de potenciales de forma rítmica y sincrónica. Aunque la liberación de acetilcolina puede
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
9 vistas2 páginasEpilepsia
Epilepsia
Cargado por
lorienLas neuronas anormales que forman parte del foco de epileptogénesis muestran alteraciones estructurales y cambios en sus características eléctricas debido a la actividad de receptores ionotrópicos y metabotrópicos. Estos cambios condicionan modificaciones en los flujos iónicos y la transmisión sináptica que pueden producir brotes epilépticos cuando grupos de células anormales disparan descargas de potenciales de forma rítmica y sincrónica. Aunque la liberación de acetilcolina puede
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
Las neuronas anormales que forman parte del foco de epileptogénesis muestran
alteraciones estructurales en su membrana que condicionan modificaciones sustanciales
en sus características electrotónicas y, por ende, en su potencial de equilibrio y velocidad
de conducción. Los procesos moleculares que convergen con la aparición de esta serie
de alteraciones dieléctricas dependen fundamentalmente de la actividad de receptores
tanto ionotrópicos como metabotrópicos, los que no solo condicionan severas
modificaciones en los flujos iónicos, sino en la transmisión sináptica y en la comunicación
intracelular. Cuando la interneurona facilitadora libera Glu y este actúa sobre un receptor
específico, se activa una proteincinasa que al promover un influjo sostenido de Ca++, da
lugar a la formación del complejo Ca++/calmodulina, el que estimula a su vez a otros
receptores facilitadores que además de incrementar la liberación de más
neurotransmisores al medio, produce alteraciones en la función mitocondrial que
repercuten en la supervivencia de la célula.
No obstante que la liberación presináptica de acetilcolina puede ser el estímulo
desencadenante del fenómeno dieléctrico, es el ácido glutámico el que refuerza y sostiene
el proceso. Cuando se abate su liberación o síntesis o bien, disminuye el número de
receptores postsinápticos sobre los cuáles actúa, decrece la electronegatividad del
potencial de equilibrio, permitiendo que estímulos de menor intensidad, desencadenen la
despolarización de la membrana, con la consecuente formación de potenciales de acción
que se propagan rápidamente a través de la neurona postsináptica.
Si bien, los epileptogenesis emergen constantemente breves brotes de descargas de
potenciales propagados, que son disparados de manera rítmica y sincrónica, por grupos
de células anormales que toman la función de marcapaso. Por lo tanto, estos trenes de
descarga pueden en un momento dado potenciar sus estímulos, los que, al hacer crecer
su frente de onda, despolarizan áreas circunvecinas conformadas por estructuras
neuronales anatómica y funcionalmente normales, que se prestan por sus características
dieléctricas a la conducción y propagación del estímulo anormal. También de esta forma
el foco de epileptogénesis estructura y organiza sus propios circuitos, que siendo
anormales, los conecta con redes neuronales normales ya establecidas, y que no
obstante que su función es por completo distinta e independiente a la de las neuronas que
forman parte del proceso patológico, permiten que el estímulo circule de manera
reverberante o repetitiva, hasta que los cambios dieléctrios que sufren las membranas de
las neuronas involucradas provocan el desgaste y la suspensión del proceso, a través de
fenómenos.
También resulta imposible sustraernos de la influencia que los procesos inmunes ejercen
sobre el organismo en sí mismo y, sobre todo, sobre el sistema nervioso tanto central
como periférico, a pesar de la protección que la evolución le ha proporcionado al dotarlo
de una barrera vascular y de un fluido periencefálico, por lo que podemos considerar que
la presencia en el espacio interneuronal o intersticial de neurotransmisores
neuroexcitatorios por ejemplo, o simplemente de substancias capaces de relajar al
músculo liso produciendo vasodilatación, o bien la síntesis, liberación o activación de
sustancias mediadoras del dolor, como las bradicininas, el tromboxano A2 o el
neuropéptido.
De modo que la simple asociación entre la presencia de algunos de los mediadores de la
inflamación con crisis convulsivas no necesariamente implica que, dentro de su
fisiopatología, sea la inmunidad la que juega el papel preponderante, ya que su activación
también podría ser el resultado indirecto de la participación de otra serie de fenómenos
ajenos a los desencadenados por este sistema biológico.
Este proceso no necesariamente es el resultado de la activación del sistema inmune ni de
la participación de mediadores de la inflamación, cuya influencia dentro del SNC no se
limitaría a la producción de crisis epilépticas, sino que potencialmente podría provocar,
incluso, encefalitis. Pero lo que sí es factible es que la producción de factores
neuroquímicos que fuera del SNC intervienen en la activación de cascadas proteicas de
inflamación, participen dentro del mismo en la producción de focos de epileptogénesis sin
desencadenar, necesariamente, un fenómeno de naturaleza inflamatoria.
Una vez establecido el diagnóstico y la clasificación de la enfermedad, y habiendo
descartado un posible factor etiológico, es imperativo considerar, antes de decidir una
intervención terapéutica, el riesgo de recurrencia, la edad de aparición y el pronóstico, y
sopesar objetivamente las ventajas y desventajas de la prescripción farmacológica a largo
plazo.
También podría gustarte
- Señalización Celular en Isquemia RenalDocumento15 páginasSeñalización Celular en Isquemia RenalDanielaCarvajalAún no hay calificaciones
- Manual de Garantía y Mantenimiento DFSKDocumento19 páginasManual de Garantía y Mantenimiento DFSKFrancis Amaury NJ Presinat100% (3)
- BLADDocumento10 páginasBLADNatalia GonzálezAún no hay calificaciones
- Neurotransmisores de La EpilepsiaDocumento2 páginasNeurotransmisores de La EpilepsiaandreacamachogonAún no hay calificaciones
- Los Fenómenos Bioeléctricos Corresponden A La Actividad de La CélulasDocumento2 páginasLos Fenómenos Bioeléctricos Corresponden A La Actividad de La CélulasDiego ZambranoAún no hay calificaciones
- Resumen de Fisiopatología Del Sistema Nervioso CentralDocumento21 páginasResumen de Fisiopatología Del Sistema Nervioso Centralpuchurrox onyxAún no hay calificaciones
- Capitulo 7Documento35 páginasCapitulo 7Soraya CarguaytongoAún no hay calificaciones
- Muerte Celular y Adaptación CelularDocumento10 páginasMuerte Celular y Adaptación CelularPaola MacedoAún no hay calificaciones
- Las Neuronas y Las Clases de SinapsisDocumento8 páginasLas Neuronas y Las Clases de SinapsisVenus Delta Ticona FloresAún no hay calificaciones
- Amplificadores de RF de Potencia FinalDocumento20 páginasAmplificadores de RF de Potencia FinalRespaldo Diego Elias Hernandez PerezAún no hay calificaciones
- Fisiopatologia de La EpilepsiaDocumento9 páginasFisiopatologia de La EpilepsiacarlosAún no hay calificaciones
- Capítulo 6Documento4 páginasCapítulo 6Monserrat Sánchez NietoAún no hay calificaciones
- Actvs Tema 10 y 11Documento7 páginasActvs Tema 10 y 11Eva MartinAún no hay calificaciones
- UPV Fisiopatología Guía 03 - InflamaciónDocumento3 páginasUPV Fisiopatología Guía 03 - InflamaciónCristhián Ignacio Jerez FernándezAún no hay calificaciones
- Mecanismo de Señalización SinápticasDocumento10 páginasMecanismo de Señalización SinápticasDeborah LopezAún no hay calificaciones
- Guía SinapsisDocumento2 páginasGuía SinapsisMaria Eleonora Foitzick PalmaAún no hay calificaciones
- Capítulo 6 - MergedDocumento6 páginasCapítulo 6 - MergedMonserrat Sánchez NietoAún no hay calificaciones
- Word Preguntas FisiologiaDocumento3 páginasWord Preguntas Fisiologiasarai villenaAún no hay calificaciones
- Plasticidad NeuronalDocumento20 páginasPlasticidad NeuronalvioletaAún no hay calificaciones
- Final de Huamana 2Documento10 páginasFinal de Huamana 2Gonzalo Nahuel LemosAún no hay calificaciones
- Taller 1 y 2 Biologia Celular y MolecularDocumento53 páginasTaller 1 y 2 Biologia Celular y MolecularVanessa NúñezAún no hay calificaciones
- 2015 Práctica I GenéticaDocumento7 páginas2015 Práctica I GenéticaMario Orlando Chumioque SanchezAún no hay calificaciones
- Tema 5 Principios de SEÑALIZACIÓN CELULARDocumento11 páginasTema 5 Principios de SEÑALIZACIÓN CELULARdelimarrpAún no hay calificaciones
- Deber 2 MorfofuncionDocumento7 páginasDeber 2 MorfofuncionChiluisa EdisonAún no hay calificaciones
- Taller Fisiología GeneralDocumento30 páginasTaller Fisiología GeneralCamila NarvaezAún no hay calificaciones
- 2023 Mediadores de La InflamaciónDocumento2 páginas2023 Mediadores de La InflamaciónLuís Angel Del Angel GarcíaAún no hay calificaciones
- Investigación 1 - Aguilar Flores Juan FranciscoDocumento3 páginasInvestigación 1 - Aguilar Flores Juan FranciscoFrancisco AguilarAún no hay calificaciones
- Vias de SeñalizaciónDocumento3 páginasVias de Señalizacióncamilo ortiz intriagoAún no hay calificaciones
- Patología Sistema NerviosoDocumento6 páginasPatología Sistema NerviosomanuelAún no hay calificaciones
- Qué Es El Ciclo CelularDocumento5 páginasQué Es El Ciclo CelularSu SaucedoAún no hay calificaciones
- Medicina LegalDocumento20 páginasMedicina LegalGenessis CardenasAún no hay calificaciones
- Comunicación Intracelular 66yDocumento31 páginasComunicación Intracelular 66ymelisa isabella OrtizAún no hay calificaciones
- SinaptogenesisDocumento18 páginasSinaptogenesisAldo AguilarAún no hay calificaciones
- Señalizacion de MembranaDocumento5 páginasSeñalizacion de MembranaLokatikaAún no hay calificaciones
- Sinapsis ResumenDocumento9 páginasSinapsis ResumenAniretac Neko Seyer50% (4)
- Fisiologia Toxina BotulinicaDocumento6 páginasFisiologia Toxina BotulinicaJosselyn LoorAún no hay calificaciones
- Marta Bernad RodríguezEPILEPSIA-CANALESIONICOSDocumento10 páginasMarta Bernad RodríguezEPILEPSIA-CANALESIONICOSMart Bernad RodríguezAún no hay calificaciones
- NeurotransmisoresDocumento30 páginasNeurotransmisoresAmni JF100% (1)
- Proceso InflamatorioDocumento17 páginasProceso InflamatorioDel valleAún no hay calificaciones
- Migracion de Los Leucocitos A Los TejidosDocumento6 páginasMigracion de Los Leucocitos A Los TejidosVíctor ArticaAún no hay calificaciones
- Las Neuronas Se Comunican Con Otras Neuronas y Con Células Efectoras a Través de Sinapsis Las Sinapsis Son Relaciones Continuas Especializadas Entre Neuronas Que Facilitan La Transmisión de Impulsos de Una Neurona PresinápticDocumento4 páginasLas Neuronas Se Comunican Con Otras Neuronas y Con Células Efectoras a Través de Sinapsis Las Sinapsis Son Relaciones Continuas Especializadas Entre Neuronas Que Facilitan La Transmisión de Impulsos de Una Neurona Presinápticsheyla fernandezAún no hay calificaciones
- Muerte CelularDocumento6 páginasMuerte CelularangyAún no hay calificaciones
- Articulo Sobre Plasticidad SinápticaDocumento6 páginasArticulo Sobre Plasticidad SinápticaMANUEL ENRIQUE AGUIRRE DE LA CRUZAún no hay calificaciones
- Seminario 3 Neurotransmisores y NeuropeptidosDocumento35 páginasSeminario 3 Neurotransmisores y NeuropeptidosBeatriz VillarrealAún no hay calificaciones
- Señalización CelularDocumento5 páginasSeñalización CelularLoaiza Morales JazmínAún no hay calificaciones
- Puncion Seca - Puntos GatillosDocumento54 páginasPuncion Seca - Puntos GatilloskamlagriAún no hay calificaciones
- Ficha Clinica ACVDocumento15 páginasFicha Clinica ACVoscar arturo gutierrez ramosAún no hay calificaciones
- El Complejo Promotor de La AnafaseDocumento12 páginasEl Complejo Promotor de La AnafaseDavicho SánchezAún no hay calificaciones
- Apunte U2Documento12 páginasApunte U2Manzanita ConfitadaAún no hay calificaciones
- Funcion Biologia de Las EnzimasDocumento15 páginasFuncion Biologia de Las EnzimasDaniela Jibaja MechatoAún no hay calificaciones
- Plasticidad Neuronal y Tecnocomunicacion Vanessa BritoDocumento23 páginasPlasticidad Neuronal y Tecnocomunicacion Vanessa BritovaniavanessaAún no hay calificaciones
- Medicina Interna Modulo BasicoDocumento76 páginasMedicina Interna Modulo BasicoNATALIA PATRICIA MOSCOSO CORREAAún no hay calificaciones
- Daryenel Huitron Autocoides y Segundos MensajerosDocumento22 páginasDaryenel Huitron Autocoides y Segundos MensajerosDaryenel HuitrónAún no hay calificaciones
- Seminario 3-1Documento7 páginasSeminario 3-1laura sanchez gomisAún no hay calificaciones
- Plasticidad CerebralDocumento26 páginasPlasticidad CerebralJhosep Choque100% (1)
- Plasticidad NeuronalDocumento13 páginasPlasticidad NeuronalEcyor Hidalgo ReinosoAún no hay calificaciones
- Farmacología. Edema e Inflamación PDFDocumento43 páginasFarmacología. Edema e Inflamación PDFEDITHAún no hay calificaciones
- Comunicación Celular y Contracción MuscularDocumento11 páginasComunicación Celular y Contracción MuscularCamila AndradeAún no hay calificaciones
- Psiconeuropatologia y Sistema InmuneDocumento7 páginasPsiconeuropatologia y Sistema InmuneneriaguquiAún no hay calificaciones
- Parcial de Fisiología AnimalDocumento8 páginasParcial de Fisiología AnimalJorge Isaac SanmiguelAún no hay calificaciones
- Bronquitis CrónicaDocumento16 páginasBronquitis CrónicalorienAún no hay calificaciones
- Neumonía AtípicaDocumento15 páginasNeumonía AtípicalorienAún no hay calificaciones
- TosDocumento5 páginasToslorienAún no hay calificaciones
- Enfermedad Von Willebrand DiapoDocumento14 páginasEnfermedad Von Willebrand DiapolorienAún no hay calificaciones
- Sindromes de Las Vías AéreasDocumento6 páginasSindromes de Las Vías AéreaslorienAún no hay calificaciones
- Manual Otorrino LorienDocumento27 páginasManual Otorrino LorienlorienAún no hay calificaciones
- Fisiopatología de Los Trastornos Del Estado de ÁnimoDocumento3 páginasFisiopatología de Los Trastornos Del Estado de ÁnimolorienAún no hay calificaciones
- Examen Mental ManiaDocumento4 páginasExamen Mental ManialorienAún no hay calificaciones
- Cambios Termicos de Un SistemaDocumento4 páginasCambios Termicos de Un SistemaPaola Doğranmış0% (1)
- 1er Examen de Ginecologia Con ClaveDocumento13 páginas1er Examen de Ginecologia Con ClaveTalo GuzmanAún no hay calificaciones
- Plan de Curso de Capacitación Unid Posgrado Fimca Unh - OctubreDocumento3 páginasPlan de Curso de Capacitación Unid Posgrado Fimca Unh - OctubrePosgrado Minas UnhAún no hay calificaciones
- Ensayo 2 (Propiedades de Los Semiconductores)Documento8 páginasEnsayo 2 (Propiedades de Los Semiconductores)Abril HernandezAún no hay calificaciones
- Misa Brotes de OlivoDocumento9 páginasMisa Brotes de OlivoShandell SolAún no hay calificaciones
- CT 2° EDA1 s1 EXPLICA Qué Diferencia A Los Seres Vivos de Los Elementos InertesDocumento7 páginasCT 2° EDA1 s1 EXPLICA Qué Diferencia A Los Seres Vivos de Los Elementos InertesAnthony Gonzales LagoAún no hay calificaciones
- Manual CTP RDCDocumento32 páginasManual CTP RDCLorena PalaciosAún no hay calificaciones
- Lab. No6 Destilacion SimpleDocumento9 páginasLab. No6 Destilacion SimpleEva IngridAún no hay calificaciones
- Examen de Conciliación BancariaDocumento1 páginaExamen de Conciliación BancariaAugusto J CarmonaAún no hay calificaciones
- Inducción T5Documento14 páginasInducción T5AlexaMS00Aún no hay calificaciones
- Orthogon User Manual 0150 A 20180405 1331 (Spanish)Documento80 páginasOrthogon User Manual 0150 A 20180405 1331 (Spanish)Hernan Gimenez LemmeAún no hay calificaciones
- Monografia Universal Plastic & Pack FinalDocumento105 páginasMonografia Universal Plastic & Pack FinalDoll PazAún no hay calificaciones
- 3.6 Riesgos Infecto BiologicosDocumento20 páginas3.6 Riesgos Infecto BiologicosMartinez AndonAún no hay calificaciones
- Errores Frecuentes en La Producción TextualDocumento11 páginasErrores Frecuentes en La Producción TextualMariela ZúñigaAún no hay calificaciones
- Deber Legislacion Matriz Requisitos LegalesDocumento58 páginasDeber Legislacion Matriz Requisitos LegalesJenny Zerna NavarreteAún no hay calificaciones
- Terapia Sistémica - ¿Qué Es y en Qué Principios Se BasaDocumento8 páginasTerapia Sistémica - ¿Qué Es y en Qué Principios Se BasaAnonymous n6ARRoMAún no hay calificaciones
- Preguntas para El Examen OralDocumento12 páginasPreguntas para El Examen OralJhonatan LeonAún no hay calificaciones
- Tema 2 TerremotosDocumento58 páginasTema 2 TerremotosBAún no hay calificaciones
- Malawi S PizzaDocumento10 páginasMalawi S PizzaJhonny LealAún no hay calificaciones
- Rio Yucaes CaudalDocumento31 páginasRio Yucaes CaudalYesabel Candy Humareda CorasAún no hay calificaciones
- Diversidad de Equipos de Alto RendimientoDocumento16 páginasDiversidad de Equipos de Alto RendimientoEstefania Ponce ArteagaAún no hay calificaciones
- Evaluacion Presion HidrostaticaDocumento3 páginasEvaluacion Presion HidrostaticaIuis Alfredo Narvaez CujarAún no hay calificaciones
- Referencias Cruzadas en CDocumento13 páginasReferencias Cruzadas en Cmaria otilia canonAún no hay calificaciones
- Actividad 1 Herrera Méndez WendyDocumento5 páginasActividad 1 Herrera Méndez WendyWendy Herrera100% (1)
- Pets Trazo Reemplanteo y Control TopográficoDocumento3 páginasPets Trazo Reemplanteo y Control TopográficoOrlando AstoAún no hay calificaciones
- Segundo Examen ParcialDocumento5 páginasSegundo Examen ParcialwrdnAún no hay calificaciones
- Longchenpa Encontrando Descanso en La Ilusión.Documento26 páginasLongchenpa Encontrando Descanso en La Ilusión.Maximino Miyar TejaAún no hay calificaciones
- 1° Informe (Datación Absoluta y Relativa)Documento18 páginas1° Informe (Datación Absoluta y Relativa)Franco Espinoza CastroAún no hay calificaciones
- Key SeatDocumento2 páginasKey SeatAnderson Camilo Arias SolarteAún no hay calificaciones