Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ich Q6B
Cargado por
Arturo LinaresDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Ich Q6B
Cargado por
Arturo LinaresCopyright:
Formatos disponibles
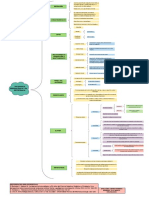
ICH Q6B
SPECIFICATIONS: TEST PROCEDURES AND ACCEPTANCE CRITERIA FOR
BIOTECHNOLOGICAL/BIOLOGICAL PRODUCTS
PRINCIPIOS A CONSIDERAR AL
INTRODUCCIÓN
ESTABLECER
ESPECIFICACIONES
Caracterización
Establecer y justificar un conjunto
OBJETIVOS uniforme de especificaciones
internacionales para productos
biotecnológicos y biológicos Es necesaria para permitir establecer las especificaciones pertinentes.
Los CA deben establecerse y justificarse basándose en datos obtenidos
de lotes utilizados en estudios preclínicos y/o clínicos, datos de lotes
Aplica a proteínas y polipéptidos, utilizados para demostrar la consistencia de fabricación y datos de
ALCANZE sus derivados y productos de los estudios de estabilidad y datos de desarrollo relevantes
que son componentes
NO
Antibióticos Incluirá una determinación de la composición, propiedades físicas y
Péptidos y polipéptidos Propiedades estructura primaria del producto deseado. Dado que la heterogeneidad
Pueden aplicarse a otros tipos de
sintéticos fisicoquímicas de estos productos define su calidad, se debe caracterizar el grado y
productos, como proteínas y
Heparinas polipéptidos aislados de tejidos y perfil de esta heterogeneidad, para asegurar la consistencia lote a lote
Vitaminas fluidos corporales.
Metabolitos celulares
Productos de ADN Describe la habilidad o capacidad específica de un producto para
Actividad
lograr un efecto biológico definido. El fabricante debe proporcionar un
Extractos alergénicos biológica
No recomienda PP o CA específicos ensayo biológico válido para medir la actividad biológica. Ej: EBBA,
Vacunas convencionales
ni se aplica a la regulación de EBBCC,EB
Células
material de investigación preclínica
Sangre total y componentes
y/o clínica. Propiedades
sanguíneos celulares Deben realizarse ensayos de unión del anticuerpo a antígenos
inmunoquímicas purificados y regiones definidas de antígenos para determinar la
afinidad, la avidez y la inmunorreactividad (incluida la reactividad
P e I: Se evalúa mediante una combinación de cruzada)
procedimientos analíticos.
}
Pureza, impurezas Debe determinarse mediante un ensayo apropiado, generalmente de
C: incluyen todos los materiales introducidos Cantidad
y contaminantes naturaleza fisicoquímica.
accidentalmente que no están destinados a ser parte del
proceso de fabricación, como materiales químicos y
bioquímicos (por ejemplo, proteasas microbianas) y / o
especies microbianas
ICH Q6B
SPECIFICATIONS: TEST PROCEDURES AND ACCEPTANCE CRITERIA FOR
BIOTECHNOLOGICAL/BIOLOGICAL PRODUCTS
PRINCIPIOS A CONSIDERAR AL
CONCEPTOS GENERALES
ESTABLECER
ESPECIFICACIONES
Estándares y materiales de referencia
Pueden ser internacionales, nacionales, o propuestos
Consideraciones
por el fabricante preparado a partir de lotes
analiticas Generalmente incluyen, pero no se limitan
representativos. En este último caso, se debe
contrastar contra el material de referencia internacional a pruebas de esterilidad, endotoxinas,
Especificaciones de la
o nacional límites microbianos, volumen en el
farmacopea
recipiente, uniformidad de las unidades de
Validación de procedimientos dosificación y material particulado.
deben haber validado los procedimientos analíticos
utilizados en las especificaciones de acuerdo a
ICH Q2A e ICH Q2B Se refiere al establecimiento de límites
más estrictos para la liberación que para
la vida útil del fármaco o producto
Consideraciones relacionadas con el proceso Límites de lanzamiento frente
farmacéutico. En algunas regiones, el
a límites de vida útil
concepto de límites de emisión solo puede
Diseño adecuado y el conocimiento de su
aplicarse a los límites internos y no a los
capacidad son parte de la estrategia utilizada para
límites reglamentarios de vida útil.
desarrollar un proceso de fabricación que sea
controlado y reproducible
Controles de Criterios de aceptación en proceso y límites de acción
proceso Se debe aplicar un análisis estadístico
Pruebas se realizan en pasos críticos de toma de apropiado, cuando sea necesario, a los
decisiones y en otros pasos donde los datos sirven datos cuantitativos reportados. Los
para confirmar la consistencia del proceso métodos de análisis, incluida la Conceptos estadísticos
justificación y el fundamento, deben
Especificaciones de materias primas y excipientes describirse en detalle.
La calidad de las materias primas utilizadas en la
producción de la sustancia farmacéutica (o
producto farmacéutico) debe cumplir con las
normas adecuadas para el uso previsto.
ICH Q6B
SPECIFICATIONS: TEST PROCEDURES AND ACCEPTANCE CRITERIA FOR
BIOTECHNOLOGICAL/BIOLOGICAL PRODUCTS
Justificación de la especificación Especificaciones
Es parte de una estrategia de control general que incluye el control de Los criterios de aceptación deben establecerse y
materias primas y excipientes, pruebas durante el proceso, justificarse en función de los datos obtenidos de los lotes
evaluación o validación del proceso, adherencia a las buenas utilizados en estudios preclínicos y / o clínicos, los datos
prácticas de fabricación, pruebas de estabilidad y pruebas de de los lotes utilizados para demostrar la consistencia de la
consistencia de un montón fabricación y los datos de los estudios de estabilidad y los
datos de desarrollo relevantes
Vinculadas a
Deben basarse en datos obtenidos de lotes
Proceso de
utilizados para demostrar la consistencia de Apariencia y Identidad
fabricación
fabricación descripción
SF Cantidad
Pureza e Potencia
El fabricante debería proponer un perfil indicador
impurezas
Estabilidad de estabilidad. El resultado de este perfil
de SF y PF indicador de estabilidad proporcionará la
garantía de que se detectarán cambios en la
calidad del producto
Deben basarse en los datos obtenidos para los Apariencia y Identidad
lotes utilizados en estudios preclínicos y clínicos. descripción
Estudios clínicos
y preclínicos La calidad del material elaborado a escala PF Cantidad
comercial debe ser representativa de los lotes
utilizados en estudios preclínicos y clínicos. Pureza e Potencia
impurezas
Los atributos de calidad críticos pueden incluir
elementos como la potencia, la naturaleza y la
Pruebas Pruebas adicionales
Procedimientos cantidad de sustancias relacionadas con el
generales para formas de
analíticos producto, impurezas relacionadas con el
dosificación únicas
producto e impurezas relacionadas con el
proceso
Abreviaturas
CA._ Criterios de aceptación
PP._ Procedimiento de pruebas
SF._ Sustancias farmacéuticas
PF._ Productos farmacéuticos
I ._ Impurezas
P._ Pureza
C._ Contaminantes
EBBA._ Ensayos biológicos basados en animales
EBBCC._ Ensayos biológicos basados en cultivos celulares
EB._ Ensayos bioquímicos
Referencia
- ICH Q6A. SPECIFICATIONS: TEST PROCEDURES AND ACCEPTANCE CRITERIA FOR BIOTECHNOLOGICAL/BIOLOGICAL PRODUCTS. Consejo Internacional
para la Armonización de Requisitos Técnicos para Productos Farmacéuticos de Uso Humano; 2005
Elaboro: Arturo Linares Verona QFB Grupo: 73
También podría gustarte
- Manual de Microbiología General: Principios Básicos de LaboratorioDe EverandManual de Microbiología General: Principios Básicos de LaboratorioCalificación: 3.5 de 5 estrellas3.5/5 (5)
- Preinforme - Tecnología Farmacéutica DETERMINACION DE TIEMPO OPTIMO DE MEZCLA Y SEPARACION Y CLASIFICACION DE PARTICULAS POR TAMAÑODocumento14 páginasPreinforme - Tecnología Farmacéutica DETERMINACION DE TIEMPO OPTIMO DE MEZCLA Y SEPARACION Y CLASIFICACION DE PARTICULAS POR TAMAÑOOLGA PATRICIA MUÑOZ GARZON100% (1)
- PNO para La Obtención, Manejo, Conservación y Desecho de SueroDocumento25 páginasPNO para La Obtención, Manejo, Conservación y Desecho de SueroSerguei AcidcherryAún no hay calificaciones
- USP 40-61-62 Limite MicrobianoDocumento15 páginasUSP 40-61-62 Limite MicrobianoSPAC_MICROBIOLOGYAún no hay calificaciones
- ICH - Q14 - Document - Step2 - Guideline - 2022 - 0324-1-26 Es - UnlockedDocumento44 páginasICH - Q14 - Document - Step2 - Guideline - 2022 - 0324-1-26 Es - Unlockededurdo100% (1)
- Protocolo de Validacion de Un Metodo Analítico Hplc-1-1 Final¡¡¡¡¡¡¡Documento15 páginasProtocolo de Validacion de Un Metodo Analítico Hplc-1-1 Final¡¡¡¡¡¡¡ReyAún no hay calificaciones
- Protocolo de Fotoestabilidad de Un MedicamentoDocumento37 páginasProtocolo de Fotoestabilidad de Un MedicamentoMIGUEL0% (1)
- FEUM Agua para Uso Farmaceútico PDFDocumento9 páginasFEUM Agua para Uso Farmaceútico PDFAlhanPalaciozAún no hay calificaciones
- Línea Del Tiempo FarmacovigilanciaDocumento5 páginasLínea Del Tiempo FarmacovigilanciaJiménez Tovilla Katherine Airam100% (1)
- Pno-Llenado de CapsulasDocumento6 páginasPno-Llenado de CapsulasQuique De La LuzAún no hay calificaciones
- Buenas Practicas de LaboratorioDocumento16 páginasBuenas Practicas de LaboratorioJhon Alexander Marroquin Vargas100% (1)
- Examen DA 2013 2 ValidaciónDocumento5 páginasExamen DA 2013 2 ValidaciónKaryRiveraAún no hay calificaciones
- Parasitología ResumenDocumento24 páginasParasitología ResumenMiguel Ángel Mora TobarAún no hay calificaciones
- Ich Q6aDocumento31 páginasIch Q6aJose David Perez Navarro100% (1)
- Almacen Farmacia ProcedimientosDocumento262 páginasAlmacen Farmacia ProcedimientosCocotzin ItzaAún no hay calificaciones
- Emlb Cuadro Sinoptico de Tolerancia Inmunologica PDFDocumento1 páginaEmlb Cuadro Sinoptico de Tolerancia Inmunologica PDFElzy MariteAún no hay calificaciones
- Manual de Normas Tecnicas de InvimaDocumento6 páginasManual de Normas Tecnicas de Invimaandres100% (1)
- Ich Q6aDocumento4 páginasIch Q6aArturo Linares50% (2)
- USP-NF 〈1072〉 Disinfectants and AntisepticsDocumento7 páginasUSP-NF 〈1072〉 Disinfectants and AntisepticsMariana Gonzalez LariosAún no hay calificaciones
- Mapa Conceptual. Error e IncertidumbreDocumento3 páginasMapa Conceptual. Error e IncertidumbreArturo LinaresAún no hay calificaciones
- Bayona Caballero Maria Esther PDFDocumento257 páginasBayona Caballero Maria Esther PDFSharai MoraniAún no hay calificaciones
- Teoria 09 - Defensa Del Huesped Frente A Las NeoplasiasDocumento89 páginasTeoria 09 - Defensa Del Huesped Frente A Las NeoplasiasAlexis Pérez100% (1)
- 2.6.12 y 2.6.13 PhEur 6Documento39 páginas2.6.12 y 2.6.13 PhEur 6Silvia Palacios100% (3)
- Informe Final Trazas LaproffDocumento9 páginasInforme Final Trazas LaproffSebiitas Lpz Porras LiveAún no hay calificaciones
- Validación de Métodos Analíticos Q2A ICHDocumento7 páginasValidación de Métodos Analíticos Q2A ICHNadesh8329Aún no hay calificaciones
- Inspecciones Industria FarmacéuticaDocumento75 páginasInspecciones Industria Farmacéuticaarjom01Aún no hay calificaciones
- NMX-EC-15189-IMNC-2008 Vs 2015Documento14 páginasNMX-EC-15189-IMNC-2008 Vs 2015rafael valdes0% (1)
- 51 Pruebas de Eficacia AntimicrobianaDocumento4 páginas51 Pruebas de Eficacia Antimicrobianatania zenaida oviedo latorre100% (1)
- Estudio in Vitro de Los Extractos de Marañón (Anacardium Occidentales) Con Acción Hipoglicémica para Su Uso Como Alimento Nutracéuticos 6 de Abril TerminadoDocumento39 páginasEstudio in Vitro de Los Extractos de Marañón (Anacardium Occidentales) Con Acción Hipoglicémica para Su Uso Como Alimento Nutracéuticos 6 de Abril TerminadoLucia NovoaAún no hay calificaciones
- Protocolo Validacion Laproter JbeDocumento8 páginasProtocolo Validacion Laproter JbeAlvin Reyes50% (2)
- I - Autoinspeccion - Auditorias CLASE 291020Documento23 páginasI - Autoinspeccion - Auditorias CLASE 291020Yuri Carrasco ReateguiAún no hay calificaciones
- Informe de Validacion de Metodos AnaliticosDocumento26 páginasInforme de Validacion de Metodos AnaliticosMariela Elizabeth Carmen Zenón100% (1)
- PnoDocumento72 páginasPnoEsteban Galicia100% (1)
- Guia de Ejercicios Farmacia IndustrialDocumento5 páginasGuia de Ejercicios Farmacia IndustrialFlorent TobarAún no hay calificaciones
- HPLC CalificacionDocumento45 páginasHPLC CalificacionJuan Carlos Vazquez100% (1)
- IBG 10 - Equipo #4Documento9 páginasIBG 10 - Equipo #4Rigoberto Huamani TincoAún no hay calificaciones
- IE-B.3.2.3-LF-01 - BPM - Laboratorios - Nacionales DIC 18 PDFDocumento412 páginasIE-B.3.2.3-LF-01 - BPM - Laboratorios - Nacionales DIC 18 PDFLipsi Merchán100% (1)
- Especificaciones de Calidad de Los Productos TerminadosDocumento10 páginasEspecificaciones de Calidad de Los Productos TerminadosROSA LUZAún no hay calificaciones
- Manual de Funciones de LaboratorioDocumento11 páginasManual de Funciones de LaboratorioHinojosa RoblesAún no hay calificaciones
- Resolucionministerialn437 1998 Sa DMDocumento4 páginasResolucionministerialn437 1998 Sa DMAlexandra Barrientos CabanaAún no hay calificaciones
- Biofarmacia y Farmacociné Tica 2020 PDFDocumento441 páginasBiofarmacia y Farmacociné Tica 2020 PDFKaterin Rondo TolentinoAún no hay calificaciones
- Jonathan Urbina Soto-Validación Del Método Analítico de Valoración de Ácido SalicílicoDocumento16 páginasJonathan Urbina Soto-Validación Del Método Analítico de Valoración de Ácido SalicílicoJonathan UrbinaAún no hay calificaciones
- EvaluacionDocumento17 páginasEvaluacionpatty tsAún no hay calificaciones
- Formula Cuali Cuantitativa - 1Documento2 páginasFormula Cuali Cuantitativa - 1Carlos MercadoAún no hay calificaciones
- MGA-MD1241-procedimientos de Muestreo y Tablas de Inspeccion Por AtributosDocumento23 páginasMGA-MD1241-procedimientos de Muestreo y Tablas de Inspeccion Por AtributosAlejandra LopezAún no hay calificaciones
- Estabilidad Del IbuprofenoDocumento13 páginasEstabilidad Del IbuprofenoLuisha Cop AguiAún no hay calificaciones
- Protocolo para El Estudio de Estabilidad Del AcetaminofenDocumento6 páginasProtocolo para El Estudio de Estabilidad Del AcetaminofenHarold Betancourt PerezAún no hay calificaciones
- Elaboración y Control de JarabesDocumento6 páginasElaboración y Control de JarabesErika Lopez ArandaAún no hay calificaciones
- Cross-Linking Gelita RLXDocumento8 páginasCross-Linking Gelita RLXedwardollAún no hay calificaciones
- Investigación de La Desviación de Resultados MicrobiológicosDocumento39 páginasInvestigación de La Desviación de Resultados MicrobiológicosSolutam MoraleAún no hay calificaciones
- TMP 6 C95Documento415 páginasTMP 6 C95Frontiers50% (2)
- Elaboracion de CapsulasDocumento23 páginasElaboracion de CapsulasKeila Mariana Campos ChambiAún no hay calificaciones
- Evaluacion de Calidad de Los AlimentosDocumento16 páginasEvaluacion de Calidad de Los AlimentosJefry Jose González LopezAún no hay calificaciones
- 9 Farmacos y AditivosDocumento17 páginas9 Farmacos y AditivosEdiLber AnTony BassAún no hay calificaciones
- Criterios Microbiologicos Principios y Directrices para El EstablecDocumento29 páginasCriterios Microbiologicos Principios y Directrices para El EstablecAntonio Javier Loor Delgado (Tonny)Aún no hay calificaciones
- Mga 0251. Densidad Relativa: Factor de Coleo T - 'Documento2 páginasMga 0251. Densidad Relativa: Factor de Coleo T - 'Mariana SaldivarAún no hay calificaciones
- Gráfico OPSpecsDocumento6 páginasGráfico OPSpecsCatalina Alarcon NavarroAún no hay calificaciones
- PRT-711.02-047 V 3 Determinación de Vit B1 en Harina-HPLC-FLDocumento7 páginasPRT-711.02-047 V 3 Determinación de Vit B1 en Harina-HPLC-FLPatricia PhillipsAún no hay calificaciones
- Biorremediación Con Pseudomonas SPPDocumento10 páginasBiorremediación Con Pseudomonas SPPAdriian PortilloAún no hay calificaciones
- Plano LaboratorioDocumento1 páginaPlano LaboratorioVivianaGaitanAún no hay calificaciones
- Ich Q6BDocumento4 páginasIch Q6BArturo LinaresAún no hay calificaciones
- Product OsDocumento122 páginasProduct OsSammy MeloAún no hay calificaciones
- U1-4 RRSS Productos NaturalesDocumento60 páginasU1-4 RRSS Productos Naturalesedwin salazarAún no hay calificaciones
- Análisis ClínicosDocumento16 páginasAnálisis Clínicosdepartvh09Aún no hay calificaciones
- Apunte Unidad 1Documento1 páginaApunte Unidad 1Arturo LinaresAún no hay calificaciones
- Mapa Regulacion y ArmonizacionDocumento2 páginasMapa Regulacion y ArmonizacionArturo LinaresAún no hay calificaciones
- Ich Q6BDocumento4 páginasIch Q6BArturo LinaresAún no hay calificaciones
- AGLUTINACIÓNDocumento8 páginasAGLUTINACIÓNLuis Fernando CMagaña100% (1)
- 3er Pacial MicrobiologiaDocumento58 páginas3er Pacial MicrobiologiaMoreno Mendoza Evelin MichelAún no hay calificaciones
- InmunoparasitologíaDocumento8 páginasInmunoparasitologíaMirtha GutierrezAún no hay calificaciones
- 1º Certamen de MicrobiologíaDocumento7 páginas1º Certamen de MicrobiologíapendejahAún no hay calificaciones
- El Sistema Inmune en Los Estados de Salud y EnfermedadDocumento9 páginasEl Sistema Inmune en Los Estados de Salud y EnfermedadEdgardo Ivan Esparza RicoAún no hay calificaciones
- Trabajo de Investigación InmunologíaDocumento7 páginasTrabajo de Investigación Inmunologíacarlina villamarAún no hay calificaciones
- Una Vacuna Es Una Suspensión de Microorganismos Vivos AtenuadosDocumento4 páginasUna Vacuna Es Una Suspensión de Microorganismos Vivos AtenuadosLina PérezAún no hay calificaciones
- Histología, Nombre de Tejidos y EnfermedadDocumento15 páginasHistología, Nombre de Tejidos y EnfermedadADRIANA HERNANDEZ COTOCAún no hay calificaciones
- Determiancion de Grupo SanguineoDocumento9 páginasDetermiancion de Grupo SanguineoK'anchaq RamArAún no hay calificaciones
- Complejo de Mayor HistocompatibilidadDocumento7 páginasComplejo de Mayor HistocompatibilidadJonatán Eliseo Morales JeronimoAún no hay calificaciones
- Uss-2015-II. - Patologia I. - Inmunopatologia (10 Setiembre 2015)Documento103 páginasUss-2015-II. - Patologia I. - Inmunopatologia (10 Setiembre 2015)Laura Esthefany OrdoñezAún no hay calificaciones
- Español El Guion RadiofónicoDocumento8 páginasEspañol El Guion Radiofónicobetsii bustamanteAún no hay calificaciones
- Inmunomodulación PDFDocumento26 páginasInmunomodulación PDFCruz J Gutiérrez A100% (1)
- AnatomíaDocumento91 páginasAnatomíaMa ChAún no hay calificaciones
- Antigenos Inmunogenos y HaptenosDocumento27 páginasAntigenos Inmunogenos y HaptenosSalicilatoAún no hay calificaciones
- Neuroinmunología (Relación Sistema Nervioso-Sistema Inmune) : Principios de NeuroanatomíaDocumento12 páginasNeuroinmunología (Relación Sistema Nervioso-Sistema Inmune) : Principios de NeuroanatomíaBarbara FigueroaAún no hay calificaciones
- 2023 Caracterizacion Importancia MicoplasmosisDocumento25 páginas2023 Caracterizacion Importancia Micoplasmosisjuan valenciaAún no hay calificaciones
- Artículos de Interés Sobre FitoterapiaDocumento85 páginasArtículos de Interés Sobre FitoterapiasanpedrolagunillasAún no hay calificaciones
- (Proceso de Produccion Deinmunoglobulina) PDFDocumento38 páginas(Proceso de Produccion Deinmunoglobulina) PDFWigermadrid Wiger MadridAún no hay calificaciones
- Ensayo CIENCIAS-BIOLOGÍA 2019Documento33 páginasEnsayo CIENCIAS-BIOLOGÍA 2019FITOAún no hay calificaciones
- Familia SpirochaetaceaeDocumento15 páginasFamilia SpirochaetaceaeAresth GV0% (1)
- RESUMEN de Inmunoglobulinas M FinalDocumento5 páginasRESUMEN de Inmunoglobulinas M FinalMaría IsabelAún no hay calificaciones
- Trasplante y RechazoDocumento24 páginasTrasplante y RechazoSoni HE100% (1)
- Bacterias FitopatogenasDocumento23 páginasBacterias FitopatogenasAsher Burton100% (6)
- Inmunidad RebañoDocumento4 páginasInmunidad Rebañolalo guaAún no hay calificaciones
- Los Componentes Del Sistema InmunitarioDocumento11 páginasLos Componentes Del Sistema InmunitarioDaniela Garcés QuirogaAún no hay calificaciones
- Aglutinación GuiaDocumento5 páginasAglutinación GuiaAna GutiérrezAún no hay calificaciones