Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Lou - 6to Destilación Discontinua
Cargado por
Raví García AreuDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Lou - 6to Destilación Discontinua
Cargado por
Raví García AreuCopyright:
Formatos disponibles
Destilación a Relación de Reflujo Constante y Composición de Destilado
Variable
Llamocca Manco, J. (20151469B); Cutipa Mendoza, C. (20152035F); Gamarra Estrada, G. (20151332G);
Paredes Tocas, J. (20152684D)
Escuela de Ingeniería Petroquímica, FIP-UNI.
Operaciones Unitarias II, sección A, 18/11/2019
jllamoccam@fip.uni.edu.pe; ccutipam@fip.uni.edu.pe; ggamarre@fip.uni.edu.pe; jparedest@fip.uni.edu.pe
Resumen: En el presente laboratorio se realizó la destilación de una mezcla en la que uno de los componentes
es más volátil, usando un reflujo constante de 60%. Se obtuvieron como resultado los valores experimentales
de la composición i-ésima del destilado y la composición i-ésima del residuo de la destilación. Posteriormente
se utilizaron los modelamientos de Ley de Raoult, Ley de Raoult Modificada y volatilidad para calcular la
composición de destilado. Concluyendo que según los resultados experimentales y/o teóricos el método que
más se asemeja es el que utiliza la Ley de Raoult.
Abstract: En el presente laboratorio se realizará la destilación de una mezcla en la que uno de los
componentes es más volátil, utilizando un reflujo constante de 60%. Se obtuvieron como resultado los valores
experimentales de la composición i-ésima del destilado y la composición i-ésima del residuo de la destilación.
Posteriormente se utilizarán los modelamientos de Ley de Raoult, Ley de Raoult Modificada y volatilidad para
calcular la composición de destilado. Concluyendo que según los resultados experimentales y / o teóricos el
método que más se asemeja es el que utiliza la Ley de Raoult.
1. INTRODUCCIÓN resolución analítica de los problemas de destilación,
La destilación es una técnica que nos permite y los aparatos en los que se lleva a cabo esta
separar mezclas, comúnmente líquidas, de
sustancias que tienen distintos puntos de ebullición. operación han de suministrar un íntimo contacto
Cuanto mayor sea la diferencia entre los puntos de entre el vapor y el líquido, para que estas fases
ebullición de las sustancias de la mezcla, más eficaz alcancen la condición de equilibrio.
será la separación de sus componentes; es decir, los
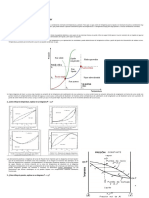
componentes se obtendrán con un mayor grado de Equilibrios a Presión Constante: Para una sección
pureza. típica a presión constante (figura 1). La curva
La técnica consiste en calentar la mezcla hasta que superior proporciona la relación entre la temperatura
ésta entra en ebullición. En este momento los y la composición del vapor (t-y*); la curva inferior,
vapores en equilibrio con el líquido se enriquecen la relación entre la temperatura y la composición del
en el componente de la mezcla más volátil (el de líquido (t-x). Las mezclas de líquido y vapor en el
menor punto de ebullición). A continuación, los equilibrio están a la misma temperatura y presión,
vapores se dirigen hacia un condensador que los de forma que las líneas de unión, como la línea DF,
enfría y los pasa a estado líquido. El líquido unen las mezclas en el equilibrio en D y F. Hay un
destilado tendrá la misma composición que los número infinito de dichas líneas de unión para este
vapores y; por lo tanto, con esta sencilla operación diagrama. Una mezcla en la curva inferior, como en
habremos conseguido enriquecer el líquido el punto D, es un líquido saturado; una mezcla en la
destilado en el componente más volátil. Por curva superior, como en F, es un vapor saturado.
consiguiente, la mezcla que quede en el matraz de Una mezcla en E es una mezcla de dos fases, que
destilación se habrá enriquecido en el componente consta de una fase líquida de composición en D y
menos volátil. una fase vapor de composición en F, en proporción
tal que la composición promedio de toda la mezcla
Relaciones de Equilibrio: Para separar los se representa mediante E.
componentes de una mezcla liquida por destilación
es condición necesaria que la composición del vapor
producido en la ebullición de la mezcla sea diferente
de la composición del líquido de partida; por ello el
equilibrio entre ambas fases es necesario para la
Este comportamiento ideal se presenta en mezclas
cuyas constituciones muestran una gran semejanza
química, estas disoluciones obedecen la Ley de
Raoult, el cual establece que la Presión de Vapor de
cada componente es igual al producto de la fracción
molar de dicho componente en la fase liquida por la
Presión de Vapor del componente puro a la misma
Temperatura.
p A =x A∗P vA
pB =x B∗PvB =( 1−x A )∗PvB
Volatilidad Relativa: La volatilidad es una relación
entre su presión parcial de vapor y su concentración
en la fase liquida.
pA
volatilidad de A=
xA
pB
volatilidad de B=
xB
A la relación entre el componente más volátil entre
Fig 1. Fracción mol de A vs T. el menos volátil se le conoce como volatilidad
relativa.
Mediante un diagrama de composición x vs y* p A/ x A y A xB
(figura 2), también se puede mostrar las diferentes α= =
pB/ xB yB x A
composiciones vapor – liquido.
De la cual:
α xA
y A=
1+(α −1)x A
El Método Mc. Cabe – Thiele:
El método Mc.Cabe-Thiele se aplica en su forma
clásica simplificada a una columna ideal. Se
considera una columna ideal cuando el número de
moles de vapor que la atraviesan, es constante, lo
cual requiere cumplir con ciertas condiciones
teóricas importantes:
Que las pérdidas de calor en la columna
sean pequeñas.
Que los componentes sean de naturaleza
similar.
Que tanto el destilado retornado a la
Fig 2. Fracción mol de A en el líquido vs columna, como la alimentación, entren a su
Fracción mol de A en el vapor. temperatura de ebullición.
Las diferencias de presión no afecten la
Ley de Raoult: Para disoluciones ideales se puede relación de equilibrio
determinar los datos para las construcciones de los
diagramas a partir de las Presiones de Vapor de los
componentes puros.
Sea un fraccionador, con su respectiva En esta zona los flujos de Liquido (L) y Vapor(G)
Alimentación, Destilado y Residuo: se mantienes constantes, pero las composiciones
cambian. Dichos platos son teóricos, por ello la
composición de vapor del n-simo plato está en
equilibrio con el líquido que sale de ese mismo
plato. (xn, yn).
Un balance de materia en esta zona:
G−L+ D=D( R+1)
Balance por componente:
G y n+1=L x n+ D x D
Donde la recta de operación de la sección de
enriquecimiento será:
L D
y n+ 1= xn+ xD
G G
R xD
y n+ 1= xn +
R+1 R+1
Fig 3. Corrientes de Materia y Entalpia de un
Fraccionador.
El fraccionador se divide en dos zonas; la primera
situada por encima del plato de alimentación
denominada zona de enriquecimiento; por otro lado,
la que se encuentra por debajo del plato de
alimentación, denominada zona de agotamiento. Fig 5. Recta de la sección de Enriquecimiento.
Sección de Enriquecimiento: Sección de Agotamiento:
Fig 4. Balance de Materia en la Zona de Fig 6. Balance de Materia en la Zona de
Enriquecimiento. Agotamiento.
Los platos en esta sección siguen siendo teóricos y F+ L+ Ǵ=G+ Ĺ
los flujos de Liquido ( Ĺ ¿ y de Vapor (Ǵ ¿ son
constantes, pero no necesariamente iguales de plato Balance Global de materia:
a plato. F z F =W x w + D x D
Un balance de materia en esta zona:
Ĺ=Ǵ+W Definiremos q, como:
Ĺ−L H G −H F
Balance por componente: = =q
F H G−H L
Ĺ xm =Ǵ y m+1 +W x w
Por lo que: Ǵ−G=F(q−1)
Donde la recta de operación de la sección de
enriquecimiento será: Restando las ecuaciones de la sección de
Ĺ W agotamiento y de enriquecimiento:
y m +1= x m− x w
Ǵ Ǵ ( Ǵ−G ) y =( Ĺ−L ) x−(W x w + D x D )
Entonces:
q zF
y= x−
q−1 q−1
La línea q nos ayuda a simplificar la localización
del plato de alimentación y esta depende de qué tipo
de mezcla este sea F.
Fig 7. Recta de la sección de Agotamiento.
Introducción de la mezcla de Alimentación:
Fig 9. Localización de la línea q para condiciones
típicas de alimentación.
Fig 8. Introducción de la Alimentación. Razón de reflujo constante y composición del
destilado variable: Suponiendo también
En este plato las corrientes de Liquido y Vapor despreciables las acumulaciones de líquido y vapor
cambian, debido a que la mezcla de alimentación en la columna frente a la carga líquida de la caldera,
puede estar compuesta por Liquido, Vapor o una para un intervalo diferencial de tiempo t, se tendría:
mezcla de ambos.
Un balance en este plato: d ( Sx ¿¿ s)=−x D dV ¿
Sabiendo que dV =−dS El cálculo de la integral se realizará en base al
método del Trapecio.
dS dx
= Eficiencia Global: La eficiencia global se calcula
S x D −x
determinando el número de etapas ideales entre el
La ecuación diferencial que integrada entre límites número de platos reales.
que abarquen todo el período de rectificación
conduciría a: Teniendo en cuenta esto, los objetivos serán:
Comparar los datos obtenidos
xS experimentalmente y teóricamente mediante
S d xs 2
los métodos de Ley de Raoult (LR), Ley de
ln ( 1 )=∫ … Ec. 10
S 2 x x D−x sS1
Raoult Modificada (LRM) y Volatilidad.
Modelar el sistema con las teorías de LR,
A su vez un balance del componente más volátil LRM y Volatilidad.
extendido a todo el tiempo que dura la rectificación Comprender como se maneja y como
conduce a la siguiente expresión de la composición funciona un equipo de destilación.
media del destilado:
2. METODOS Y MATERIALES
S 1 x S −S 2 x S Los elementos necesarios para la realización de esta
xD = 1 2
práctica son:
m
S 1−S 2 Equipo UDCC o UDDC.
Solución de etanol y agua destilada al 1:1
Para el cálculo de esta integral se procede así: para molar.
la columna y operación de rectificación de que se
trate, en un diagrama de equilibrio x-y, a partir de Para el desarrollo de esta práctica se siguió el
distintos puntos de la diagonal correspondientes a siguiente procedimiento:
distintas composiciones x D , dentro de los límites
adecuados, se trazan rectas de operación paralelas 1. Se carga el calderín con 1.5 litros de una
con el valor de la razón de reflujo L/V que se desee mezcla etanol / agua, con una concentración
como pendiente. Se dibujan entre cada una de ellas aproximada de 60% en masa de etanol.
y la curva de equilibrio, partiendo siempre de su 2. Se hace pasar agua fría por el circuito de
cruce con la diagonal, tantos escalones como pisos refrigeración.
de equilibrio tenga la columna en cuestión. Para 3. Se enciende la interface, el ordenador y se
cada una de las citadas rectas de operación, la carga el programa de control pulsando en el
vertical del escalón más bajo indicará el icono SACED-UDDC o SACED-UDDC.
correspondiente valor de x s, indispensable para 4. Se programa la temperatura que se puede
poder efectuar la integración gráfica. alcanzar en el calderín. Use cualquiera de
los tres controladores disponibles, PID,
todo/nada o PWM.
5. Ahora se programa el valor deseado para la
razón de reflujo expresado en porcentaje de
salida (hay que tener en cuenta que la
variación de la razón de reflujo con el
porcentaje es lineal, correspondiéndole al
valor 0% el caso en que todo el vapor
condensado se devuelve a la columna y al
valor 100% el caso en que todo el vapor
condensado se extrae como destilado).
6. Una vez que se estabilice el flujo de
destilado, se han de tomar un total de 6
muestras, separadas entre sí un tiempo no
Fig. 10 Graficas de las rectas de operación menor de 5 minutos, del destilado y del
residuo a través de las válvulas V-2 y V-1. xSi xDi 1/(Xd - Xs)
Estas serán enfriadas rápidamente y cerrado 0.560 0.767 4.8403
el tubo que las contiene. Se realizará el 0.450 0.667 4.6083
análisis de las muestras por el método
0.389 0.580 5.2323
elegido, obteniendo las fracciones molares
del destilado y del residuo También se 0.330 0.488 6.3593
anotará el volumen de destilado recogido. 0.272 0.423 6.6077
0.220 0.383 6.1093
3. RESULTADOS Y DISCUSION
3.1 Resultados El área teórica se calculó mediante la regla del
Tablas trapecio, donde tenemos lo siguiente:
xSi: Composición i-ésima del residuo de la
destilación [adimensional]. b
∫ f ( x ) dx= h2 [f ( a )+2 f ( a+h ) +2 f ( a+ 2h )+ …+f ( b ) ]
xDi: Composición i-ésima del destilado a
[adimensional].
I: Integral obtenida mediante métodos numéricos b−a
Donde: h=
(método del trapecio). n
S2: moles de residuo final de la destilación.
D: moles de destilado.
xD: Composición global del destilado. Tabla 4. Resultados para un valor de n=5 y el
xS: Composición global del del calderín valor de la integral.
Alfa: Método del cálculo según Volatilidad. Para n=5 1/(Xd - Xs)
LR: Método del cálculo según la Ley de Raoult. h 0.057 0.0567
LRM: Método del cálculo según la Ley de Raoult f (1) 4.8403 9.6805
Modificada. f (2) 4.6083 9.2166
f (3) 5.2323 10.4646
Tabla 1. IR y temperaturas para el destilado. f (4) 6.3593 12.7186
DESTILADO f (5) 6.6077 13.2155
T T IR f (6) 6.1093 6.1093
Muestra IR xD
(°C) (°C) (25°C) Σ 61.4619
38 1 28 1.3616 1.3630 0.7666
38 2 28 1.3624 1.3638 0.6670 El valor de la integral es 1.7436
38 3 28 1.3621 1.3635 0.5800
39 4 29 1.3612 1.3630 0.4875
39 5 29 1.3608 1.3626 0.4231
39 6 29 1.3602 1.3620 0.3833 Tabla 5. Comparación de los datos obtenidos
experimentalmente en base de los cálculos
Tabla 2. IR y temperaturas para el calderín. teóricos mediante Balance de masa.
CALDERIN TEORICO EXP
T T IR S2 4.48107 27.27866
Muestra IR xs
(°C) (°C) (25°C)
D 21.14120 6.49908
39 1 35 1.3589 1.3634 0.5600
xD 0.63216 0.5614
39 2 35 1.3582 1.3627 0.4500
38 3 34 1.358 1.3621 0.3889
38 4 34 1.3569 1.3610 0.3303
38 5 34 1.3545 1.3586 0.2717
38 6 34 1.3521 1.3562 0.2196
Tabla 6. Comparación de los datos obtenidos
experimentalmente con los tres diferentes
Tabla 3. Datos utilizados para el cálculo del Área
métodos usados Ley de Raoult, Ley de Raoult
teórica determinada a una razón de reflujo de
Modificada y Volatilidad. Realizados en Matlab.
60%
Experimenta LR LRM Alfa
l Tabla 7. Tabla de correlación de composición vs
I 1.8678 0.93077 0.66073 0.34587 IR.
S2 3.9581 10.103 13.235 18.133 x1 IR
D 21.668 15.523 12.391 7.4929 0.000 1.3326
xD 0.62211 0.61431 0.68354 0.59161 0.100 1.3473
0.200 1.3553
0.300 1.3599
0.333 1.3611
Gráficos 0.400 1.3623
0.500 1.3631
Densidad vs composición 0.600 1.3636
1050 0.667 1.3638
f(x) = 123.69 x⁴ − 538.98 x³ + 788.4 x² − 585.92 x + 1027.46 0.700 1.3636
R²1000
=1 0.800 1.3627
t=25°c 0.900 1.3619
950 P=1BAR 1.000 1.3610
g/L
ρ (g/L)
Polyno
900 mial
(t=25°c
P=1BAR
850 g/L)
1.3700
1.3600
f(x) = − 0.12 x⁴ + 0.34 x³ − 0.36 x² + 0.17 x + 1.33
800 1.3500
R² = 1
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1 1.3400
IR
xs 1.3300
Gráfico 1. Curva de densidad vs composición a 1.3200
25ºC. 1.3100
0.000 0.200 0.400 0.600 0.800 1.000
Composición
Experimental
8.0000
Gráfico 3. Validación de los datos que se
6.0000 encuentran calibrados.
1/(Xd - Xs)
f(x) = − 648.51 x⁴ + 1414.51 x³ − 1039.25 x² + 303.71 x
−4.0000
23.96
R² = 0.99
2.0000 4. CONCLUSIONES
• Se obtuvieron valores muy cercanos al
0.0000
0 0 0 0 0 0 0 0 0 experimental por cada uno de los tres
20 .25 .30 .35 .40 .45 .50 .55 .60
0. 0 0 0 0
Xs 0 0 0 0 modelamientos utilizados y comparándolos con los
que nos brinda la teoría.
• Se obtuvo un resultado más cercano al
Gráfico 2. Curva obtenida con los datos
experimental por el método de la Ley de Raoult.
experimentales que sirvieron para el cálculo de la
integral
5. RECOMENDACIONES
3.2 Discusión
• Se recomienda hacer uso del Refractómetro
Para el cálculo de las composiciones se tuvo que
con mucho cuidado pues de los datos obtenidos en
realizar una corrección en la temperatura debido a
este equipo se obtienen cada una de las
un error en la medición de esta por parte del
composiciones, las cuales son fundamentales para el
refractómetro. Dicha variación se hizo de tal forma
desarrollo de esta experiencia.
que las composiciones obtenidas se encuentren en el
• Es muy importante la etapa de enfriamiento
rango de la tabla N°7.
de las muestras para así detener inmediatamente la
reacción y obtener la composición en el tiempo Mediante la Tabla 3 y Tabla 4 se obtiene la integral
deseado. (I) con lo cual mediante la Ec. 10, se obtendrá el
• Es muy importante retirar todo el exceso de cálculo teórico de S2.
destilado, para obtener composiciones adecuadas
entre cada tiempo. S2 = S1 * e^(-I)
Y mediante Balance de masa global se sabe que:
6. REFERENCIAS BIBLIOGRAFICAS D = S2 – S1
J. Ocon garcía y G. Tojo Barreiro, Problemas de
ingeniería Química Operaciones Básicas Tomo Obteniendo así el valor de las moles de destilado, y
II, vol. II, Aguilar. mediante balance de masa por componente se sabe
R. E. Treybal, Operaciones de Transferencia de que:
Masa, McGRAW-HILL, pp. 307-369.
C. Ruiz, «DESTILACIÓN A RELACIÓN DE xD * D = xS2 * S2 – xS1 * S1
REFLUJO CONSTANTE Y COMPOSICIÓN xD = (xS2 * S2 – xS1 * S1)/ D
DE DESTILADO VARIABLE,» Lima, Peru,
2018. Obteniendo así teóricamente, la composición global
de destilado. Los resultados se muestran en la Tabla
APENDICE 5 y Tabla 6.
METODO EXPERIMENTAL
Usando la Gráfica 1. y la ecuación de la densidad a
25 ºC, se puede hallar los siguientes resultados:
Para S1
V =1 L
x s 1=0.560
g
d=864.13465
L
masa=864.13465 g
n=25.62227 moles=S 1
Para S2
V =0.708 L
x s 2=0.220
g
d=931.44773
L
masa=659.46499 g
n=27.278664 moles=S2
Para D
V =0.254 L
IR=1.3630
x s 2=0.561418
g
d=863.9603
L
masa=219.44592 g
n=6.4990765 moles=D
METODO TEORICO
También podría gustarte
- Psicometría. Principios básicos y protocolos experimentales diversosDe EverandPsicometría. Principios básicos y protocolos experimentales diversosAún no hay calificaciones
- DESTILACIÓNDocumento41 páginasDESTILACIÓNFernandoAún no hay calificaciones
- Informe T BurbujaDocumento14 páginasInforme T BurbujaRicardo Felipe Cortes CruzAún no hay calificaciones
- Clase-Semana 6 - DestilaciónDocumento42 páginasClase-Semana 6 - DestilaciónjhonAún no hay calificaciones
- Informe Labo IIDocumento18 páginasInforme Labo IIDilam Diaz RamirezAún no hay calificaciones
- Unidad 4 Destilacion FinishDocumento21 páginasUnidad 4 Destilacion Finishalara-731450Aún no hay calificaciones
- 2 Equilibrio Líquido - VaporDocumento11 páginas2 Equilibrio Líquido - VaporMeliza Bravo CastilloAún no hay calificaciones
- Informe de Laboratorio #04Documento20 páginasInforme de Laboratorio #04ruttAún no hay calificaciones
- Lecciones de RepasoDocumento18 páginasLecciones de RepasoRicardoAún no hay calificaciones
- Marco Teorico TxyDocumento4 páginasMarco Teorico TxyCraven HorrorsAún no hay calificaciones
- Diferencia Entre Gas y VaporDocumento8 páginasDiferencia Entre Gas y VaporJosé TorrezAún no hay calificaciones
- Equilibro de Fases InformeDocumento13 páginasEquilibro de Fases InformeJuly Nym NeylaAún no hay calificaciones
- OPE III - Sesión 10 DestilaciónDocumento9 páginasOPE III - Sesión 10 DestilaciónDiego Francisco Pizarro LlazaAún no hay calificaciones
- Informe 2 Curva Eq. X-YDocumento12 páginasInforme 2 Curva Eq. X-YJuan Jose LlamoccaAún no hay calificaciones
- Resumen 4.1Documento4 páginasResumen 4.1Rebeca CadenaAún no hay calificaciones
- Resumen 4.1 EquilibrioDocumento4 páginasResumen 4.1 EquilibrioAlex Mendoza AyaviriAún no hay calificaciones
- Tarea 4.1 EquilibrioDocumento4 páginasTarea 4.1 Equilibriopaola poma gutierrezAún no hay calificaciones
- Aqui Editar111Documento14 páginasAqui Editar111SHsaavedraAún no hay calificaciones
- Tarea2 Jhoyosb JsmorenolaDocumento11 páginasTarea2 Jhoyosb JsmorenolaJuan David Hoyos BohorquezAún no hay calificaciones
- LOU II - 1er LaboDocumento14 páginasLOU II - 1er LaboJuan Jose LlamoccaAún no hay calificaciones
- 00EQUILIBRIO LIQUIDO VAPOR. Coeficientes de ActividadDocumento14 páginas00EQUILIBRIO LIQUIDO VAPOR. Coeficientes de ActividadCbrera JoseAún no hay calificaciones
- Tarea 2.2 EquilibrioDocumento8 páginasTarea 2.2 Equilibriopaola poma gutierrez0% (1)
- ANEXO 4 Cuest de La Ley de RoultDocumento5 páginasANEXO 4 Cuest de La Ley de Roultluis alonso fernandez alvirdeAún no hay calificaciones
- Equilibrio Liquido VaporDocumento6 páginasEquilibrio Liquido VaporAlexChacónAún no hay calificaciones
- Equilibrio Liquido VaporDocumento8 páginasEquilibrio Liquido VaporARNOLD BRAVO RAMIREZAún no hay calificaciones
- ANEXO 4 Cuest de La Ley de RoultDocumento6 páginasANEXO 4 Cuest de La Ley de Roultluis alonso fernandez alvirdeAún no hay calificaciones
- Ecuación de Van Laar (Destilación)Documento50 páginasEcuación de Van Laar (Destilación)Mayumy Aguilar SilvaAún no hay calificaciones
- Lab 3Documento20 páginasLab 3ASTRID ELIZABET CUEVA GUTIERREZAún no hay calificaciones
- BinariosDocumento100 páginasBinariosOscar RodriguezAún no hay calificaciones
- Practica 3Documento14 páginasPractica 3Brisa janeth Ortiz paredesAún no hay calificaciones
- T de BurbujaDocumento7 páginasT de BurbujaangieAún no hay calificaciones
- Informe de DestilacionDocumento44 páginasInforme de DestilacionReina PinedoAún no hay calificaciones
- Previo Práctica 3. Equilibrio Líquido-VaporDocumento3 páginasPrevio Práctica 3. Equilibrio Líquido-VaporJireh Carral RojasAún no hay calificaciones
- 11 Destilaci NDocumento72 páginas11 Destilaci NRojasJosuesAún no hay calificaciones
- Equilibrio Liquido-Vapor Etanol-AguaDocumento3 páginasEquilibrio Liquido-Vapor Etanol-Aguaanon_214710Aún no hay calificaciones
- Procesos LLDocumento8 páginasProcesos LLJohnny Martin Ramos DíazAún no hay calificaciones
- Introducción TeóricaDocumento20 páginasIntroducción TeóricaMontserrat CartagenaAún no hay calificaciones
- DestilaciónDocumento14 páginasDestilaciónAna BelenAún no hay calificaciones
- Equilibrio de FasesDocumento30 páginasEquilibrio de FasesPablo CabreraAún no hay calificaciones
- Sist Homog Multicom. - SOLUC NO ELECTROLI Parte 2Documento76 páginasSist Homog Multicom. - SOLUC NO ELECTROLI Parte 2Austin de los BackyardigansAún no hay calificaciones
- Equilibrio L - VDocumento12 páginasEquilibrio L - VTakeshi Tanohuye TanohuyeAún no hay calificaciones
- Ley de Dalton y HenryDocumento62 páginasLey de Dalton y HenryLaura ReyesAún no hay calificaciones
- 2 Equilibrio Vapor - LíquidoDocumento11 páginas2 Equilibrio Vapor - LíquidoEdwin Cirilo ChaucaAún no hay calificaciones
- Equilibrio de FasesDocumento7 páginasEquilibrio de FasesKido JazzAún no hay calificaciones
- Resumen IIQ FinDocumento3 páginasResumen IIQ FinALEJANDRA GABRIELA CASTRO SAMAYOAAún no hay calificaciones
- Informe de FaseDocumento24 páginasInforme de FaseLlocclla Ccasani GloriaAún no hay calificaciones
- Op1 Pre1Documento5 páginasOp1 Pre1FernandoAún no hay calificaciones
- LOpU1 Pre1 GascónCastilloAsafJoshuaDocumento4 páginasLOpU1 Pre1 GascónCastilloAsafJoshuaAsaf Joshua Gascón CastilloAún no hay calificaciones
- Pack 3 ApuntesDocumento30 páginasPack 3 ApuntesIris Anahi Melgoza MadrigalAún no hay calificaciones
- L3.1 Destilacion Flash y DiferencialDocumento35 páginasL3.1 Destilacion Flash y DiferencialYoloo JdrAún no hay calificaciones
- Destilación Operaciones Unitarias 1Documento20 páginasDestilación Operaciones Unitarias 1milanyely castilloAún no hay calificaciones
- Informe N°13 DestilacionDocumento32 páginasInforme N°13 DestilacionRosa Mariia Quezada ArteagaAún no hay calificaciones
- Ley de Raoult InformeDocumento17 páginasLey de Raoult InformeMaría Argomedo ReyesAún no hay calificaciones
- Marco Teórico PetroDocumento8 páginasMarco Teórico PetroEstefany Vania Nina ZuritaAún no hay calificaciones
- Presentacion DestilacionDocumento108 páginasPresentacion DestilacionFrancisco SanchezAún no hay calificaciones
- TP Teoría 2-FisicoquímicaDocumento8 páginasTP Teoría 2-FisicoquímicaNacho MalaspinaAún no hay calificaciones
- Destilacion - Rectificacion 3Documento62 páginasDestilacion - Rectificacion 3gonzalog3Aún no hay calificaciones
- Lab06 - Grupo ADocumento13 páginasLab06 - Grupo ADaniel Marcelo VelasquezAún no hay calificaciones
- Informe Equilibrio L VDocumento6 páginasInforme Equilibrio L Vjuan carlosAún no hay calificaciones
- Teorico OP PDFDocumento297 páginasTeorico OP PDFAlberto José Moreira BohórquezAún no hay calificaciones
- Tercera Práctica CalificadaDocumento1 páginaTercera Práctica CalificadaRaví García AreuAún no hay calificaciones
- Matriz de LocalizaciónDocumento2 páginasMatriz de LocalizaciónRaví García AreuAún no hay calificaciones
- La Ética en La Vida CotidianaDocumento4 páginasLa Ética en La Vida CotidianaRaví García Areu100% (1)
- Taller de ÉticaDocumento2 páginasTaller de ÉticaRaví García AreuAún no hay calificaciones
- Laboratorio Absorción - GRUBO B - 2020 - 1Documento5 páginasLaboratorio Absorción - GRUBO B - 2020 - 1Raví García AreuAún no hay calificaciones
- Horario 2020-1Documento2 páginasHorario 2020-1Raví García AreuAún no hay calificaciones
- Taller de Ética - GarcíaDocumento4 páginasTaller de Ética - GarcíaRaví García AreuAún no hay calificaciones
- Repaso QuimicaDocumento40 páginasRepaso QuimicaRaví García AreuAún no hay calificaciones
- Pérdida de Carga en TuberíasDocumento9 páginasPérdida de Carga en TuberíasRaví García AreuAún no hay calificaciones
- Parámetros Inorganicos y Calidad Del AguaDocumento9 páginasParámetros Inorganicos y Calidad Del AguaRaví García AreuAún no hay calificaciones
- Transferencia de Calor II INFORME - Lou 1Documento6 páginasTransferencia de Calor II INFORME - Lou 1Raví García AreuAún no hay calificaciones
- Informe Parámetros Inorganicos y Calidad Del AguaDocumento9 páginasInforme Parámetros Inorganicos y Calidad Del AguaRaví García AreuAún no hay calificaciones
- Trabjo Petro RaviDocumento26 páginasTrabjo Petro RaviRaví García AreuAún no hay calificaciones
- Precalentador InfoDocumento6 páginasPrecalentador InfoRaví García AreuAún no hay calificaciones
- PI135 Lab5 2019-1Documento11 páginasPI135 Lab5 2019-1Raví García AreuAún no hay calificaciones
- Medidor de Flujo UltrasónicoDocumento2 páginasMedidor de Flujo UltrasónicoRaví García AreuAún no hay calificaciones
- Ciclo Otto DieselDocumento34 páginasCiclo Otto DieselNOELIA MILAGROS CONDO SILVAAún no hay calificaciones
- Malla de Progreso Curricular 11, Año 2021Documento4 páginasMalla de Progreso Curricular 11, Año 2021Luis Uribe MartínezAún no hay calificaciones
- Capitulo 4Documento38 páginasCapitulo 4Gabriel MacíasAún no hay calificaciones
- Informe LaboratorioDocumento10 páginasInforme LaboratorioAlejandro Hernandez Lara0% (1)
- Rectificación - Mezclas Binarias DefinitivooDocumento53 páginasRectificación - Mezclas Binarias DefinitivooJohnny Alejandro Samaniego MacíasAún no hay calificaciones
- Taller 3 - Conducción de Calor en Estado EstacionarioDocumento19 páginasTaller 3 - Conducción de Calor en Estado EstacionarioDaniel R RodriguezAún no hay calificaciones
- Clase 5 - TermodinámicaDocumento54 páginasClase 5 - Termodinámicayuri DávilaAún no hay calificaciones
- Unidad 1. Ejemplos 9 y 10Documento4 páginasUnidad 1. Ejemplos 9 y 10Alexander RodriguezAún no hay calificaciones
- Torre de EnfriamientoDocumento11 páginasTorre de EnfriamientoArea51 IpnAún no hay calificaciones
- Tarea III. Leslie Marquez R. 8C IQDocumento8 páginasTarea III. Leslie Marquez R. 8C IQHector Rivera CasasAún no hay calificaciones
- Ejercicios CORREJIDOS lUIS CARRERADocumento14 páginasEjercicios CORREJIDOS lUIS CARRERADaniel Jose Ortiz LopezAún no hay calificaciones
- Guía de Practicas Física - 102Documento16 páginasGuía de Practicas Física - 102Sipudieras VerAún no hay calificaciones
- Producto Moreno Ulloa FaltaDocumento22 páginasProducto Moreno Ulloa FaltaStacy Horna AnguloAún no hay calificaciones
- Conveccion Forzada Exterior PDFDocumento12 páginasConveccion Forzada Exterior PDFDaniel NuñezAún no hay calificaciones
- Guia de Usuario CM901Documento18 páginasGuia de Usuario CM901Felipe OrdoñezAún no hay calificaciones
- Taller Equilibrio de Fases 2020Documento8 páginasTaller Equilibrio de Fases 2020Andres RodriguezAún no hay calificaciones
- Clases Teoria RQyB 2021 PDFDocumento224 páginasClases Teoria RQyB 2021 PDFFabricio RamirezAún no hay calificaciones
- Ciclos Biogeoquimicos y Leyes de La TermodinamicaDocumento3 páginasCiclos Biogeoquimicos y Leyes de La TermodinamicaMiguel Ángel MHAún no hay calificaciones
- Opt Taller de Física Octavo Periodo III Guia 5 OSDocumento7 páginasOpt Taller de Física Octavo Periodo III Guia 5 OSNazly Judith Rojas MartínezAún no hay calificaciones
- Ex - 3 Termo Ing. Ind. Ucsm 2022-Par CiclosDocumento6 páginasEx - 3 Termo Ing. Ind. Ucsm 2022-Par CiclosBraulio Rodrigo Roque ArivilcaAún no hay calificaciones
- Trabajo de Fisica II (Temperatura) ErikaDocumento2 páginasTrabajo de Fisica II (Temperatura) ErikaluisAún no hay calificaciones
- RUBRICA Informe TERMODINAMICA IDocumento4 páginasRUBRICA Informe TERMODINAMICA IJovy Garay ArceAún no hay calificaciones
- Practica # 4Documento14 páginasPractica # 4Lizbeth CallejasAún no hay calificaciones
- Practica 4 Solucion Parcialmente MisciblesDocumento19 páginasPractica 4 Solucion Parcialmente MisciblesJULIO HUMBERTO TIRADO VASQUEZAún no hay calificaciones
- UntitledDocumento328 páginasUntitledPaula RojasAún no hay calificaciones
- GUIA DE CIENCIAS NATURALES SEGUNDO PERIODO NovenoDocumento25 páginasGUIA DE CIENCIAS NATURALES SEGUNDO PERIODO NovenoLuis Gabriel Fuentes MorenoAún no hay calificaciones
- Fisica - Ii - Blooque 2 Calor y TemperaturaDocumento28 páginasFisica - Ii - Blooque 2 Calor y TemperaturacruzzznahiAún no hay calificaciones
- EXAMEN FINAL TransferenciaDocumento4 páginasEXAMEN FINAL TransferenciaCristian Najar OcharanAún no hay calificaciones
- Informe Abet Plantas Andres GomezDocumento50 páginasInforme Abet Plantas Andres GomezMateo VanegasAún no hay calificaciones
- EIQ 453 2016 10 Estanque de CalentamientoDocumento29 páginasEIQ 453 2016 10 Estanque de CalentamientoFelipe Ortiz MorenoAún no hay calificaciones