Documentos de Académico
Documentos de Profesional
Documentos de Cultura
ABC Paratohormona
Cargado por
Moisés AndradeDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
ABC Paratohormona
Cargado por
Moisés AndradeCopyright:
Formatos disponibles
ABC del laboratorio
Paratohormona
Parathyroid Hormone
Código SCPC (Sociedad Colombiana de Patología Clínica): 41500.
Código CUPS (Codificación Única de Procedimientos en salud): 904912.
Sección: Química Clínica.
Nivel de complejidad: alto.
Metodología: inmunoensayo quimioluminiscente.
Sinónimos: hormona paratiroidea molécula intacta, PTH intacta, PTH.
Definición
Esta prueba consiste en un inmunoensayo lo que suprime la secreción de la paratohor-
quimioluminiscente in vitro para la deter- mona, mientras que cuando son bajos provo-
minación cuantitativa de la paratohormona can un aumento en la liberación de la misma.
humana en muestras de suero, de utilidad La paratohormona, además, estimula la sín-
en el diagnóstico diferencial de los valores de tesis renal de la 1,25-dihidroxi vitamina D y
hipercalcemia e hipocalcemia resultantes de la reabsorción renal de calcio. La vida media
desórdenes en el metabolismo del calcio. de esta hormona es de dos a cinco minutos.
La determinación de la paratohormona se
Espectro utiliza junto con la del calcio para evaluar los
clínico de aplicación trastornos en el metabolismo del calcio. No
obstante, esta medición es difícil debido a la
La paratohormona (PTH), también conocida heterogeneidad de los péptidos que se produ-
como hormona paratiroidea, es un polipép- cen tanto en la glándula como en la circulación.
tido de una sola cadena de 84 aminoácidos,
secretada y almacenada por la glándula pa- La paratohormona se sintetiza en las glándu-
ratiroides y uno de los reguladores más im- las paratiroideas como un precursor de 115
portantes del metabolismo mineral. Tiene aminoácidos que se convierte por proteólisis
un rol determinante en mantener las con- en la hormona aminoácida biológicamente
centraciones adecuadas de calcio y fósforo activa de 84 aminoácidos. Además, se da la
en la sangre, así como en el desarrollo y formación de algunos fragmentos que con-
mantenimiento de la salud ósea. tienen porciones de la molécula, tanto en
el carboxilo terminal (C-terminal) como el
La secreción de la paratohormona (1-84) está N-terminal, por degradación en la glándula
regulada principalmente por la concentra- o por descomposición proteolítica posterior
ción de calcio extracelular, que es detectada cuando la paratohormona es liberada en la
por los receptores sensibles al calcio en las circulación a través de los riñones y el hígado.
células de la superficie de la glándula para-
tiroides. De esta manera, cuando los niveles La eliminación de los fragmentos C-terminal
de calcio son altos se activan los receptores, es más lenta que la de la hormona intacta y
Medicina & Laboratorio Volumen 23, Números 1-2, 2017 95
ABC del laboratorio
dependiente de la función renal, lo que lleva proporcionales a la concentración de para-
a su acumulación y a concentraciones muy tohormona intacta presente en la muestra.
elevadas en los pacientes con falla renal gra-
ve o terminal. Control de calidad
La medición de la paratohormona está indica- Es recomendable efectuar un control de ca-
da en pacientes en estudio de hipercalcemia, lidad por día de uso, o bien de conformidad
control intraoperatorio de paratohormona, con las normas o los requisitos de acredita-
enfermedad renal crónica, paciente en estu- ción locales y los procedimientos de control
dio de hipocalcemia, estudio de enfermedad de calidad del laboratorio. En el Laboratorio
ósea metabólica y estudio de nefrolitiasis. Clínico Hematológico se realiza un control
idóneo de la prueba para utilizar o reportar
los resultados de los pacientes. Además, se
Fundamento realiza un control de calidad externo evalua-
do por el Colegio Americano de Patólogos
La determinación de paratohormona se rea-
(CAP) con periodicidad de tres retos anuales.
liza mediante un ensayo modificado de dos
pasos, tipo sándwich, que utiliza dos anti-
cuerpos policlonales de cabra para capturar Preparación del paciente
y detectar la paratohormona intacta. En el y manejo de las muestras
primer paso se realiza la incubación de la
muestra, calibrador o control con un tampón
y un primer anticuerpo policlonal conjugado Preparación del paciente
con un derivado de isoluminol dirigido contra El paciente no requiere preparación es-
la región N-terminal (aminoácidos 1-34) de la pecial; aunque es recomendable tomar
molécula intacta de paratohormona (1-84). la muestra en ayunas. La paratohormona
Durante la incubación, la paratohormona se presenta un ciclo circadiano, por lo tanto,
une a la fase sólida y, posteriormente, el anti- se recomienda tomar la muestra antes de
cuerpo conjugado con isoluminol se une a la las 10:00 a. m. La muestra sérica debe ser
paratohormona inmovilizada. tomada de acuerdo con los procedimientos
establecidos por cada laboratorio.
Luego de la incubación el material no uni-
do se elimina con un ciclo de lavado y se
agregan a la reacción partículas magnéticas
Tipo de muestra
revestidas por un segundo anticuerpo po- Suero humano a partir de sangre venosa
liclonal dirigido contra la región C-terminal recolectado en tubos secos (tapa roja) o en
(aminoácidos 39-84) de la molécula de tubos separadores de suero (tapa amarilla).
paratohormona 1-84, incubándose nueva-
Plasma con EDTA y heparina de litio.
mente. Después de la segunda incubación,
se realiza otro ciclo de lavado y se añaden
los reactivos iniciadores que dan paso a Manejo y conservación
una reacción quimioluminiscente rápida. de las muestras
Esta reacción produce una señal de luz que La correcta manipulación de las muestras
es medida en un fotomultiplicador como es crucial para garantizar la integridad de la
unidades relativas de luz (URL), que son paratohormona intacta.
96 Volumen 23, Números 1-2, 2017 Medicina & Laboratorio
Paratohormona
Debido a la baja estabilidad y vida media
de la molécula, la muestra debe tomarse en
Interpretación
baño frío (recipiente con hielo molido para de resultados
que se garantice la distribución homogénea
La concentración de paratohormona en las
de la temperatura en la muestra). Asimis-
muestras analizadas se expresa en pg/mL.
mo, los tubos deben prepararse a 4 °C antes
Para convertir los resultados a unidades del
de tomar la muestra.
sistema internacional se aplica la siguiente
Las muestras deben ser centrifugadas en formula: pg/mL x 0,103= pmol/L.
dispositivos refrigerados a 4 °C y separar el
Los resultados de la medición de la molé-
suero del coágulo inmediatamente luego
cula intacta de la paratohormona se deben
de este proceso. El suero separado debe
analizar junto con otros datos clínicos y de
ser almacenado a -80 °C. Para las muestras
laboratorio para ayudar a decidir el trata-
analizadas por el sistema DiaSorin LIAI-
miento a aplicar en cada paciente.
SON® la paratohormona es estable en el
suero congelado hasta por nueve meses a La interpretación de los resultados de para-
-80 °C. Las muestras de suero previamente tohormona intacta se debe hacer teniendo
separado del coágulo se pueden conservar en cuenta los resultados del calcio, el fósfo-
a una temperatura entre 2 °C y 8 °C si van ro y la creatinina en suero y la correlación de
a ser analizadas máximo en las ocho horas estos analitos en los trastornos en los que
siguientes. intervienen.
Si las muestras han sido congeladas estas Este ensayo no detecta la paratohormona
deben ser descongeladas completamente no intacta, como los fragmentos de para-
para su procesamiento. Una vez desconge- tohormona 7-84. Esto puede resultar en
ladas deben ser mezcladas por inversión 10 resultados de paratohormona falsamente
veces o más si es necesario hasta que estén elevados en pacientes con función renal
visiblemente homogéneas. anormal, debido a que estos pacientes tie-
nen en sangre diversas concentraciones de
Para el envío de muestras se deben utilizar
los fragmentos de paratohormona 7-84. Es
contenedores estériles y se deben empacar
por esto que se recomienda precaución en
según las normativas gubernamentales rela-
la interpretación de los resultados en este
tivas al transporte de agentes biológicos. El
grupo de pacientes y abstenerse de tomar
suero debe separarse de las células/coágulo
alguna conducta clínica solo con base en los
y congelarse a -20 °C o menos y enviarse con
resultados de la paratohormona intacta.
hielo seco. Durante el proceso de envío la
temperatura no debe ser mayor de -20 °C. El Los valores aumentados de la paratohormo-
volumen mínimo para el análisis es de 300 µL. na también se pueden encontrar en estados
de enfermedad aguda, posejercicio inten-
Valores esperados so y por otros factores fisiológicos como la
edad (aumenta desde los 20 hasta los 90
Los valores esperados por el método qui- años), la menopausia, la obesidad y la raza.
mioluminiscente del sistema DiaSorin LIAI-
SON® N-TACT PTH Gen II son: 14,5 pg/mL a La paratohormona se puede encontrar dis-
87,1 pg/mL. minuida en los neonatos, durante el emba-
Medicina & Laboratorio Volumen 23, Números 1-2, 2017 97
ABC del laboratorio
razo y la lactancia materna, pacientes con rio para ayudar a decidir cuál tratamiento se
alcoholismo crónico e ingestión de alcohol aplica en cada paciente.
o con hemodiálisis.
No se recomienda utilizar otro tipo de
muestra o tubos de recolección a los ante-
Interferentes riormente especificados.
Como se citó anteriormente la adecuada
manipulación de la muestra es crucial para Observaciones adicionales
garantizar la calidad del analito.
La prueba de la molécula intacta de la pa-
El tipo de muestra utilizado (suero o plasma ratohormona hace parte del portafolio de
con heparina de litio) puede afectar la me- servicios del Laboratorio Clínico Hematoló-
dición de la paratohormona intacta. Es por gico, Medellín, Colombia y está disponible
esto que se recomienda realizar los contro- para todo el país mediante el sistema de re-
les de los niveles de paratohormona intacta ferencia y contrarreferencia de laboratorios
utilizando el mismo tipo de muestra y bajo el clínicos.
mismo método de medición a lo largo del pe-
riodo de seguimiento del paciente para evi-
tar desviaciones (sesgos) en los resultados.
Bibliografía recomendada
Armitage EK. Parathyrin (parathyroid hormone): metabo-
La contaminación bacteriana de las muestras lism and methods for assay. Clin Chem 1986; 32: 418-424.
o los ciclos repetidos de congelación y des- Cavalier E, Carlisi A, Chapelle JP, Delanaye P. False
congelación pueden afectar los resultados. positive PTH results: an easy strategy to test and
detect analytical interferences in routine practice.
Los anticuerpos heterófilos y el factor reu- Clin Chim Acta 2008; 387: 150-152.
matoideo presentes en el suero humano Diasorin Inc. LIAISON® N-TACT® PTH II Assay. Italia. 2012.
pueden reaccionar con las inmunoglobulinas Kumar V, Barnidge DR, Chen LS, Twentyman JM,
de los reactivos o con otro material de los Cradic KW, Grebe SK, et al. Quantification of serum
mismos e interferir con la reacción in vitro. 1-84 parathyroid hormone in patients with hyper-
parathyroidism by immunocapture in situ digestion
liquid chromatography-tandem mass spectrometry.
No se recomienda el uso de muestras he-
Clin Chem 2010; 56: 306-313.
molizadas ni lipémicas.
Khundmiri SJ, Murray RD, Lederer E. PTH and Vita-
min D. Compr Physiol 2016; 6: 561-601.
Limitaciones Morales-García AI, Górriz-Teruel JL, Plancha-Man-
sanet MC, Escudero-Quesada V, Pallardó-Mateu
Para resultados fiables es necesario atener- LM. Análisis de la variabilidad en la determinación
de la PTH según el método empleado para procesar
se estrictamente a los estándares de buen la muestra. Nefrologia (Madr) 2009; 29: 331-335.
manejo y toma de la muestra.
Silva BC, Costa AG, Cusano NE, Kousteni S, Bilezi-
kian JP. Catabolic and anabolic actions of parathy-
Los resultados obtenidos deben utilizarse roid hormone on the skeleton. J Endocrinol Invest
junto con otros datos clínicos o de laborato- 2011; 34: 801-810.
98 Volumen 23, Números 1-2, 2017 Medicina & Laboratorio
También podría gustarte
- PP T 0000033Documento12 páginasPP T 0000033sylviusAún no hay calificaciones
- Cierre CIV CIADocumento6 páginasCierre CIV CIACristhian ValenzuelaAún no hay calificaciones
- Resumen Pagina 422 - 423 Higado (Gartner)Documento4 páginasResumen Pagina 422 - 423 Higado (Gartner)Edwin Chávez HuamánAún no hay calificaciones
- HemocomDocumento17 páginasHemocomguillermoAún no hay calificaciones
- Trabajo Dinamica de Fluidos FLUJO SANGUINEODocumento9 páginasTrabajo Dinamica de Fluidos FLUJO SANGUINEORicardo Rivera RamosAún no hay calificaciones
- Segmentos Pulmonares y 1221284423293986 8Documento26 páginasSegmentos Pulmonares y 1221284423293986 8Alejandro Mejía Galván100% (1)
- Fisiología RenalDocumento30 páginasFisiología RenalFatima AcostaAún no hay calificaciones
- Metabolismo Del Agua y Los ElectrolitosDocumento16 páginasMetabolismo Del Agua y Los Electrolitosbiofisica2011100% (1)
- Laboratorio de Bioquimica Ii - Otoño 2023Documento10 páginasLaboratorio de Bioquimica Ii - Otoño 2023Erandi Meza RiveraAún no hay calificaciones
- Estructura y circunvoluciones del telencéfaloDocumento5 páginasEstructura y circunvoluciones del telencéfaloangeldeluz_morena1390Aún no hay calificaciones
- 06 AntigenosDocumento53 páginas06 AntigenosJemima MedinaAún no hay calificaciones
- Practica 10-Masa ProteicaDocumento5 páginasPractica 10-Masa ProteicaVictor J. OreAún no hay calificaciones
- CesarDocumento10 páginasCesarapi-3699557100% (1)
- Farmacologia Tabla de Antiarritmicos 281365 Downloable 840722Documento12 páginasFarmacologia Tabla de Antiarritmicos 281365 Downloable 840722Karen HernándezAún no hay calificaciones
- Funciones y circulación del LCR enDocumento4 páginasFunciones y circulación del LCR enJulio Jesus Sanchez Ordoñez100% (1)
- Fisiología del músculo liso gastrointestinalDocumento17 páginasFisiología del músculo liso gastrointestinalFelipe Ignacio Gutierrez BarriosAún no hay calificaciones
- Fisiología de la sangre: sus componentes y funciones vitales enDocumento109 páginasFisiología de la sangre: sus componentes y funciones vitales enNia Avellaneda100% (1)
- AterosclerosisDocumento21 páginasAterosclerosisSarita Esther S MAún no hay calificaciones
- Programa LepraDocumento37 páginasPrograma Lepraapi-26041148Aún no hay calificaciones
- Miembros SuperioresDocumento13 páginasMiembros SuperioresSofia OrellanaAún no hay calificaciones
- Estenosis Aórtica: Anatomía, Causas y SíntomasDocumento5 páginasEstenosis Aórtica: Anatomía, Causas y SíntomasMelissa Rios AlbinoAún no hay calificaciones
- Rigidez por descerebraciónDocumento3 páginasRigidez por descerebraciónAndrea Lucía Rodríguez100% (1)
- Capitulo 18 FisiologiaDocumento40 páginasCapitulo 18 FisiologiaBrenda Mota100% (1)
- Anatomía e Histología Del HígadoDocumento18 páginasAnatomía e Histología Del Hígadomiguel100% (1)
- Repaso. Capítulo 64Documento8 páginasRepaso. Capítulo 64johan manuel candelario de la rosaAún no hay calificaciones
- Póster Glucólisis AnaeróbicaDocumento1 páginaPóster Glucólisis AnaeróbicaNaomi SacaAún no hay calificaciones
- Tejido MuscularDocumento36 páginasTejido MuscularGiovanniMonsalvoAún no hay calificaciones
- Alteraciones de La Caja TorácicaDocumento71 páginasAlteraciones de La Caja Torácicaluis163100% (2)
- Funcion RenalDocumento4 páginasFuncion RenalRuben Dario RamirezAún no hay calificaciones
- Guia VI - Metabolismo de Sustancias Nitrogenadas PDFDocumento11 páginasGuia VI - Metabolismo de Sustancias Nitrogenadas PDFnathalyAún no hay calificaciones
- Incompativilidad RHDocumento12 páginasIncompativilidad RHBryanAlfredoGuillenCahuanaAún no hay calificaciones
- Insufiencia AdrenalDocumento20 páginasInsufiencia AdrenalOmar Camilo Martinez Serrano100% (1)
- Diureticos-Isaza Ocr PDFDocumento10 páginasDiureticos-Isaza Ocr PDFSantiago Figueroa TorresAún no hay calificaciones
- Creatin in ADocumento31 páginasCreatin in AAlix SantamariaAún no hay calificaciones
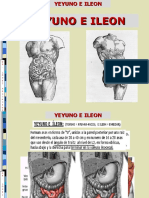
- Yeyuno e IleonDocumento34 páginasYeyuno e IleonEdson Barba Patiño100% (2)
- Metabolismo de Los CarbohidratosDocumento3 páginasMetabolismo de Los CarbohidratosMaria Melissa Tapias PerezAún no hay calificaciones
- Cruralgia síntomas nervio femoralDocumento2 páginasCruralgia síntomas nervio femoralNataly CaleroAún no hay calificaciones
- Capítulo 62 GuytonDocumento31 páginasCapítulo 62 Guytonaike7Aún no hay calificaciones
- Sistema Endocrino 4Documento35 páginasSistema Endocrino 4DANIEL ALEJANDROAún no hay calificaciones
- Histología de La Artrosis de RodillaDocumento9 páginasHistología de La Artrosis de RodillaAntonio VazquezAún no hay calificaciones
- Circulación RenalDocumento56 páginasCirculación Renalkokun123Aún no hay calificaciones
- El Consumo Energético Interno Como Flujo de Energía A Nivel Humano Individual Montenegro Tarres Up4Documento9 páginasEl Consumo Energético Interno Como Flujo de Energía A Nivel Humano Individual Montenegro Tarres Up4joaquín dunxAún no hay calificaciones
- Fisiología Del Aparato RespiratorioDocumento9 páginasFisiología Del Aparato RespiratorioAndieLopezAún no hay calificaciones
- Informe Anatomía Humana II Sesión 3Documento7 páginasInforme Anatomía Humana II Sesión 3Angie Flores MamaniAún no hay calificaciones
- Sistema de conducción cardíaco y ECGDocumento2 páginasSistema de conducción cardíaco y ECGJerson Joel Romero Llamoga80% (5)
- Anatomía Pulmonar - 19 Abril 2023 - Dr. ChávezDocumento6 páginasAnatomía Pulmonar - 19 Abril 2023 - Dr. Chávezalguiensoy9512Aún no hay calificaciones
- Adsorción de NutrientesDocumento15 páginasAdsorción de NutrientesMaria MagdalenaAún no hay calificaciones
- Los Aminoácidos y Las Proteinas Como ElectrolitosDocumento21 páginasLos Aminoácidos y Las Proteinas Como ElectrolitosAnonymous TTQWLEvLr67% (3)
- Eritrocitos, Anemia y PolicitemiaDocumento5 páginasEritrocitos, Anemia y PolicitemiaAngelica Sarahi CantuAún no hay calificaciones
- Histología Del Sistema Tegumentario (Autoaprendizaje)Documento8 páginasHistología Del Sistema Tegumentario (Autoaprendizaje)Heylling SoteloAún no hay calificaciones
- Anatomía macroscópica del riñónDocumento1 páginaAnatomía macroscópica del riñónAngieLomeliFarelas100% (2)
- Tabla de ParásitosDocumento12 páginasTabla de Parásitosyose100% (1)
- Distensibilidad Vascular y Funciones de Los Sistemas Arterial y VenosoDocumento6 páginasDistensibilidad Vascular y Funciones de Los Sistemas Arterial y VenosoJosé Luis Juárez VegaAún no hay calificaciones
- Articulo TermodinamicaDocumento15 páginasArticulo Termodinamicanathalycruz100% (1)
- Aislamiento de PBMCDocumento2 páginasAislamiento de PBMCEdison Sánchez CepedaAún no hay calificaciones
- APTT: Tiempo de Tromboplastina Parcial ActivadaDocumento2 páginasAPTT: Tiempo de Tromboplastina Parcial ActivadaDariforiAún no hay calificaciones
- Inserto PTHDocumento4 páginasInserto PTHmaria del carmenAún no hay calificaciones
- Insert Haptoglobin 11935992001 V14 EsDocumento3 páginasInsert Haptoglobin 11935992001 V14 EsFelipe MuñosAún no hay calificaciones
- 11849-Texto Del Artículo-25437-1-10-20161209Documento10 páginas11849-Texto Del Artículo-25437-1-10-20161209Maria CamilaAún no hay calificaciones
- TPT PDFDocumento9 páginasTPT PDFLilian PaolaAún no hay calificaciones
- Proposiciones Acerca Del Núcleo de Las CélulasDocumento2 páginasProposiciones Acerca Del Núcleo de Las CélulasNéstor Raúl Henao Sierra100% (1)
- Prensas de Chatarra ABECOMDocumento1 páginaPrensas de Chatarra ABECOMJ Ferreyra LibanoAún no hay calificaciones
- SociologiaDocumento4 páginasSociologiaDahiana ConceAún no hay calificaciones
- La Introspeccion y El Experimento Según WundtDocumento23 páginasLa Introspeccion y El Experimento Según WundtMarielisVivasAún no hay calificaciones
- Fundamentos ingeniería tránsitoDocumento9 páginasFundamentos ingeniería tránsitoسوسيدا اسماعيلAún no hay calificaciones
- Lectura Semana 29 de MayoDocumento21 páginasLectura Semana 29 de MayoEscuela Timoteo Araya Alegria Villa AlegreAún no hay calificaciones
- Reglamento de Construccion Urbanismo y Ornato para El Municipio de Villa NuevaDocumento34 páginasReglamento de Construccion Urbanismo y Ornato para El Municipio de Villa NuevaHenry GarciaAún no hay calificaciones
- Estructura Objetivos de Aprendizajes Sala Cuna OkDocumento9 páginasEstructura Objetivos de Aprendizajes Sala Cuna OkMaria jose Malmborg varelaAún no hay calificaciones
- Catalogo PlanosDocumento39 páginasCatalogo PlanosMartinAún no hay calificaciones
- Materia y EnergiaDocumento6 páginasMateria y EnergiaPaul AlegreAún no hay calificaciones
- Informe Nro 6 Abrams Canaviri JhonDocumento10 páginasInforme Nro 6 Abrams Canaviri JhonJhon Kevin Canaviri MamaniAún no hay calificaciones
- Estandares - Minimos PHVADocumento1 páginaEstandares - Minimos PHVACata Bobadilla HenaoAún no hay calificaciones
- Demo FCM v5 1.ppsDocumento21 páginasDemo FCM v5 1.ppsJesùs AlbertoAún no hay calificaciones
- Preguntas y Porblemas Resolver Hasta El 31.26Documento4 páginasPreguntas y Porblemas Resolver Hasta El 31.26Josué Lucio MejíaAún no hay calificaciones
- Afc Caso A. Rebecamantari010721Documento12 páginasAfc Caso A. Rebecamantari010721MilagrosMoralesZapataAún no hay calificaciones
- Cristian Roco Control4Documento8 páginasCristian Roco Control4rokacioAún no hay calificaciones
- El trueque en la economía andinaDocumento2 páginasEl trueque en la economía andinanfnAún no hay calificaciones
- AXIpremium XL HC 430-455 Wp módulos fotovoltaicos de alto rendimientoDocumento2 páginasAXIpremium XL HC 430-455 Wp módulos fotovoltaicos de alto rendimientoJimmy F HernandezAún no hay calificaciones
- Lectura Sesion 3Documento21 páginasLectura Sesion 3SandraZavaletaZevallosAún no hay calificaciones
- Peladora de PapasDocumento4 páginasPeladora de PapasDaniela GonzalezAún no hay calificaciones
- Ficha Técnica Persona Bajo La LluviaDocumento3 páginasFicha Técnica Persona Bajo La LluviaRicardo Sol100% (1)
- Juegos de herramientas en cajas de metal y bandejasDocumento123 páginasJuegos de herramientas en cajas de metal y bandejaswilliamrgvAún no hay calificaciones
- Gasistas PDFDocumento68 páginasGasistas PDFEnzo Martin100% (1)
- Parafusos Rosca MétricaDocumento22 páginasParafusos Rosca MétricasilvaAún no hay calificaciones
- Cita Mama 2Documento1 páginaCita Mama 2Alcira Socarrás CárdenasAún no hay calificaciones
- Flujo de Caja - Operativo y FinancieroDocumento12 páginasFlujo de Caja - Operativo y FinancierouniverensAún no hay calificaciones
- El Ingeniero Clínico y Su Rol en Un HospitalDocumento5 páginasEl Ingeniero Clínico y Su Rol en Un Hospitalmi.ni.pe.Aún no hay calificaciones
- Central de Autobuses747Documento9 páginasCentral de Autobuses747raulAún no hay calificaciones
- Proyecto ingeniería LEGO Mindstorms EV3Documento17 páginasProyecto ingeniería LEGO Mindstorms EV3Daniel UrquijoAún no hay calificaciones
- Identidad y Simbolismo Del Copal Prehispanico y Reciente.Documento12 páginasIdentidad y Simbolismo Del Copal Prehispanico y Reciente.Chapis YeyetziiAún no hay calificaciones