Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Streptococcus Pneumoniae
Cargado por
Abel YPTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Streptococcus Pneumoniae
Cargado por
Abel YPCopyright:
Formatos disponibles
Streptococcus pneumoniae
Microbiología
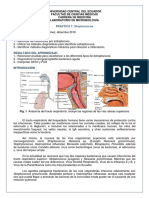
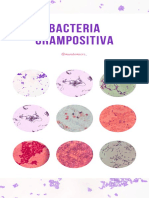
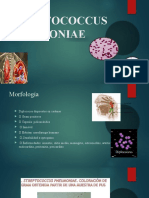
Fisiología y estructura. S. pneumoniae es una cocácea Gram positiva, capsulada.
Las células bacterianas tienen una forma lanceolada, miden 0,5 a 1,2 m de
diámetro y se disponen en pares o diplos. Son anaerobias facultativas. Para su
crecimiento y multiplicación tiene requerimientos específicos, como aportes de
proteínas y suplementos hematológicos, por lo que es considerada una bacteria
fastidiosa.
Condiciones para el crecimiento en medios de cultivo. Los medios artificiales que
aportan los nutrientes necesarios para el crecimiento de S. pneumoniae son medios
enriquecidos como agar soya tripticasa o agar infusión cerebro/corazón con adición
de 10% de sangre de cordero (entera o calentada lo que constituye el agar
chocolate). Carece de la enzima catalasa, la cual debe ser aportada en forma
exógena; en la práctica es proporcionada por la sangre. El crecimiento y desarrollo
bacteriano se ve facilitado en un ambiente con 8 a 10% de CO 2. En los medios de
cultivo antes señalados este patógeno crece formando colonias redondas, mucosas
y no pigmentadas, de 1 a 3 mm de diámetro, las cuales al cabo de 48 horas
presentan un aspecto umbilicado, con una depresión central producida por una
autolisis celular progresiva. En estos medios con sangre las colonias producen una a
hemólisis, es decir digestión parcial de la hemoglobina y la colonia se rodea de un
halo verdoso.
S. pneumoniae es sensible a la optoquina y en presencia de bilis o sales biliares se
produce una destrucción o lisis bacteriana; estas características fenotípicas son la
base para la identificación de especie. La susceptibilidad a optoquina se debe
determinar sembrando un inóculo denso en placa de agar sangre de cordero y
colocando en la superficie un disco impregnado con 5 mg de optoquina; si después
de 18 horas de incubación de la cepa a 37º C se observa un halo de inhibición del
crecimiento (dependiendo del disco comercial) > a 14 mm si es BBL o >16 mm si
es Oxoid, y además se solubiliza en presencia de sales biliares a una concentración
de 10%, esta cepa se define como S. pneumoniae.
Cápsula. Entre las estructuras interesantes de esta bacteria hay que mencionar
una cápsula externa a la pared celular, de naturaleza polisacárida compleja. Es la
piedra angular de la patogénesis de las infecciones neumocóccicas. La composición
antigénica de la cápsula es variable en diferentes cepas y permite agrupar a
losS. pneumoniae en más de 90 diferentes serotipos capsulares y
aproximadamente 45 serogrupos. Se definen como pertenecientes a un mismo
serogrupo, los serotipos que presentan inmunogenicidad cruzada, por ej. 6A y 6B.
La identificación de cada serotipo se realiza mediante una reacción antígeno-
anticuerpo utilizando antisueros específicos, lo que da como resultado una
hinchazón de la cápsula, fenómeno conocido como "quellung", término que en
alemán significa hinchazón. También se utilizan hoy en día otras técnicas para la
serotipificación, como aglutinación con látex o amplificación génica mediante RPC.
Todas estas técnicas de tipificación están disponibles sólo en laboratorios de
referencia.
La complejidad antigénica capsular de S. pneumoniae explica en parte la elevada
incidencia y severidad de las infecciones por este agente. La inmunidad es serotipo
específica, lo que significa que teóricamente un sujeto puede tener cerca de 90
infecciones neumocóccicas durante su vida. Esto podría ser verdad si la virulencia
de cada serotipo fuera similar y la inmunidad fuera de larga duración y homogénea
para todos los serotipos, pero en la realidad la calidad y duración de la inmunidad
depende del serotipo, de la edad del paciente y de otros parámetros aún no bien
definidos.
Si bien se han descrito 90 serotipos diferentes de S. pneumoniae, la experiencia
clínica mundial acumulada muestra que son pocos los serotipos con mayor impacto
clínico y es así como 12 serotipos: 1 - 3 - 4 - 5 - 6 - 7 - 8 - 9 - 14 - 18 - 19 y 23,
son responsables del 80% o más de las infecciones neumocóccicas invasoras. La
distribución geográfica y por grupo etario de estos serotipos también tiene
variaciones; se ha observado que los serotipos 1 y 5 son más frecuentes en
regiones del mundo de menor desarrollo socioeconómico.
La regulación genética de esta cápsula es también compleja y es así que algunas
cepas pueden experimentar una transformación o cambio de serotipo. Este
fenómeno publicado por Coffey en 1991, no había sido detectado previamente y, si
bien su frecuencia es baja, se presenta en cepas con resistencia a los
antimicrobianos y asociadas a colonización e infecciones en niños. Estos cambios de
serotipo en una cepa ocurren por mecanismo de recombinación genética en que se
modifica y reemplaza el locus (parte del genoma) que codifica para la expresión de
la cápsula. Uno de estos ejemplos es el serotipo 19F que surgió como variante de
un clon serotipo 23F multiresistente detectado en España y el cual se ha
diseminado a diferentes países. El análisis molecular de estas cepas mediante
diferentes técnicas de tipificación muestra una total identidad genética entre ellas,
diferenciándose sólo en el serotipo capsular. Como estas variantes han surgido en
las cepas resistentes a antimicrobianos, ya sea a penicilina o multiresistentes, se
podría plantear hipotéticamente que mutaciones o reordenamientos genéticos que
llevan a resistencia antimicrobiana se asocian a otras recombinaciones genéticas
resultando en cepas mejor adaptadas para persistir en el tiempo. Esto nos lleva a
otra reflexión obligada..., como estas variantes son cepas resistentes a los
antibióticos, la presión y selección de los antimicrobianos puede influir en forma
importante en un aumento potencial de su prevalencia y facilitar la diseminación de
estas variantes. Esto obliga a la vigilancia de este fenómeno y al uso racional de
antimicrobianos.
La capacidad de recombinación genética que posee S. pneumoniae se había puesto
en evidencia desde hace mucho tiempo. Ya en 1944 los investigadores Avery,
MacLeod y McCarty observaron un fenómeno muy peculiar en S. pneumoniae:
cepas acapsuladas, no virulentas, también denominadas R pueden transformarse
en cepas capsuladas o S, virulentas, en contacto con cepas S en un modelo in
vitro o también in vivo inoculándolas en ratón; esto ocurre por incorporación activa
de material genético desde el ambiente al genoma bacteriano y también por
mutaciones retrógadas espontáneas. Esta transformación genética está presente en
muy pocos microorganismos.
Pared bacteriana. La pared celular de S. pneumoniae tiene la estructura general
de las cocáceas Gram positivas, con una capa importante de peptidoglicano
constituida por subunidades alternadas de N-acetilglucosamina y ácido N-acetil
murámico enlazadas por puentes peptídicos (Figura 1). Un componente importante
de esta pared es el ácido teicoico, rico en galactosamina, fosfato y en colina; esta
última sustancia es exclusiva de esta bacteria y cumple una función reguladora
importante en la hidrólisis de la pared. El ácido teicoico se dispone de dos formas
en la pared celular, una expuesta en la superficie celular, (conocido como sustancia
C) y otra forma unida en forma covalente a los lípidos de la membrana
citoplasmática (Figura 1). En esta pared también están presentes la proteína R,
especie específica y la proteína M tipo específica. Ninguna de estas proteínas tiene
un papel en la virulencia.
También podría gustarte
- Transferencia de inmunidad en el binomio madre-cría: Estudio comparativo entre especiesDe EverandTransferencia de inmunidad en el binomio madre-cría: Estudio comparativo entre especiesAún no hay calificaciones
- Conceptos Microbiológicos de S. PneumoniaeDocumento5 páginasConceptos Microbiológicos de S. PneumoniaeEdgar OrtizAún no hay calificaciones
- Uso de Derivados del Cannabis en Pacientes con CáncerDe EverandUso de Derivados del Cannabis en Pacientes con CáncerAún no hay calificaciones
- Estrepto Neumonia BsesDocumento4 páginasEstrepto Neumonia BsesBarbara Seminario RamirezAún no hay calificaciones
- Streptococcus AgalactiaeDocumento5 páginasStreptococcus AgalactiaeWagner CastilloAún no hay calificaciones
- Histoplasma CapsulatumDocumento12 páginasHistoplasma CapsulatumCésar Hugo AparicioAún no hay calificaciones
- Streptococcus PneumoniaeDocumento7 páginasStreptococcus Pneumoniaelila margarita villa cervantesAún no hay calificaciones
- Info Staphylococcus AureusDocumento8 páginasInfo Staphylococcus Aureusdeceano2015Aún no hay calificaciones
- Info Flashcards 2Documento12 páginasInfo Flashcards 2Jaime De la CruzAún no hay calificaciones
- CUESTIONARIO-IDENTIFICACION DE COCOS GRAM + ResueltoDocumento29 páginasCUESTIONARIO-IDENTIFICACION DE COCOS GRAM + ResueltoJaghnna Cristhel Cruz CastellonAún no hay calificaciones
- Capitulo 19 y 22Documento7 páginasCapitulo 19 y 22Ingrid PootAún no hay calificaciones
- El Estreptococo PneumoniaeDocumento8 páginasEl Estreptococo PneumoniaeEdgar Uriel BallinasAún no hay calificaciones
- Caso Clinico de Infeccion Por Coco Gram PositivoDocumento2 páginasCaso Clinico de Infeccion Por Coco Gram PositivoJesusAcostaAún no hay calificaciones
- P NeumococoDocumento9 páginasP NeumococoAngel Jose Vargas VarelaAún no hay calificaciones
- Haemophilus Influenzae.Documento9 páginasHaemophilus Influenzae.DANNA STEPHANNY SOUZA PLASCENCIAAún no hay calificaciones
- Practica # 7 EstreptococoDocumento8 páginasPractica # 7 EstreptococoEddie RobAún no hay calificaciones
- Tarea Integradora AntraxDocumento8 páginasTarea Integradora AntraxMiguel De la torreAún no hay calificaciones
- Presentacion Proyecto de Epidemiologia y Salud Ilustrativo VerdeDocumento44 páginasPresentacion Proyecto de Epidemiologia y Salud Ilustrativo VerdeAlondra Guadalupe Chuc PinzonAún no hay calificaciones
- Chlamydia y Bacilos Gram Negativos Informe Final FinalDocumento19 páginasChlamydia y Bacilos Gram Negativos Informe Final FinalBASTI�N FRANCISCO CAMPOS VARGASAún no hay calificaciones
- Expo Chlamydophila PneumoniaeDocumento5 páginasExpo Chlamydophila PneumoniaeMarcela Ivette Fernández VelázquezAún no hay calificaciones
- Microbiología y Patogenia de Streptococcus Pneumoniae - UpToDateDocumento15 páginasMicrobiología y Patogenia de Streptococcus Pneumoniae - UpToDateAstridKarolinaQuezadaQuezada100% (1)
- Angiomatosis BacilarDocumento2 páginasAngiomatosis BacilarJuan SolísAún no hay calificaciones
- Cap 18 - Bacterias - STREPTOCOCCUS Y ENTEROCOCCUSDocumento10 páginasCap 18 - Bacterias - STREPTOCOCCUS Y ENTEROCOCCUSapi-3697245100% (1)
- Cap 20 - Bacterias - Neisserias, Haemophilus, Bordetella y BrucellaDocumento17 páginasCap 20 - Bacterias - Neisserias, Haemophilus, Bordetella y Brucellaapi-369724567% (3)
- EstafilococosDocumento36 páginasEstafilococosMax A. Carrillo Flores88% (8)
- S AureusDocumento7 páginasS AureusMarcela JataAún no hay calificaciones
- Staphylococcus Aureus - Bacteria Patogena PDFDocumento7 páginasStaphylococcus Aureus - Bacteria Patogena PDFCarlos Sierra LandinAún no hay calificaciones
- Estafilococo 2020Documento34 páginasEstafilococo 2020Chavez DaynaAún no hay calificaciones
- Staphylococcus AureusDocumento9 páginasStaphylococcus AureusAlberto TorresAún no hay calificaciones
- Factor Virulencia Staphylococcus AureusDocumento5 páginasFactor Virulencia Staphylococcus AureusValeria Rodriguez ValdiviaAún no hay calificaciones
- Streptococcus PyogenesDocumento8 páginasStreptococcus PyogenesGonzalo Ferreiros MiguelAún no hay calificaciones
- Resúmen BacteriasDocumento87 páginasResúmen BacteriasNEDRA JOANA PEREZ GARCIAAún no hay calificaciones
- Diagnóstico Microbiológico en La Detección e Identificación de StaphylococcusDocumento7 páginasDiagnóstico Microbiológico en La Detección e Identificación de StaphylococcusMaria Jose Rodriguez GaonaAún no hay calificaciones
- M PneumoniaeDocumento2 páginasM PneumoniaePaulina SoberanesAún no hay calificaciones
- Bacterias Gram Positivas.Documento29 páginasBacterias Gram Positivas.karen sofia sierra camposAún no hay calificaciones
- Micoplasma y Bacterias Con Pared Defectuosa.Documento27 páginasMicoplasma y Bacterias Con Pared Defectuosa.Yaritza Pinargt0% (1)
- Strep To CocusDocumento16 páginasStrep To CocusElsaAún no hay calificaciones
- GENERALIDADESDocumento4 páginasGENERALIDADESLina Marcela Quintero VargasAún no hay calificaciones
- Casos Clinicos VANEDocumento14 páginasCasos Clinicos VANEKevinSalinas0% (1)
- Microcap 50Documento5 páginasMicrocap 50Hellen MendezAún no hay calificaciones
- Investigación BacteriologíaDocumento16 páginasInvestigación BacteriologíaCarmen ReyesAún no hay calificaciones
- StreptococcusDocumento9 páginasStreptococcusMonserratAún no hay calificaciones
- Microbiología EstafilococosDocumento9 páginasMicrobiología EstafilococosMarcoAún no hay calificaciones
- Generalidades NeumococosDocumento3 páginasGeneralidades NeumococosJazmin Marte BaezAún no hay calificaciones
- Laboratorio #3Documento6 páginasLaboratorio #3Maria Jose Feris CastellonAún no hay calificaciones
- Tarea 1 - Microbiología - Camila AguileraDocumento5 páginasTarea 1 - Microbiología - Camila Aguileracamila aguilera garzonAún no hay calificaciones
- StreptococcusDocumento20 páginasStreptococcusSoy SamAún no hay calificaciones
- Practica 7Documento9 páginasPractica 7Janeth YépezAún no hay calificaciones
- S PneumoniaeDocumento14 páginasS PneumoniaeTANIA VIRACA CATALANAún no hay calificaciones
- Inmunidad-Humoral Naegleria FowleriDocumento2 páginasInmunidad-Humoral Naegleria Fowlerisaul enriquezAún no hay calificaciones
- EnterobacteriasDocumento14 páginasEnterobacteriasPamela Ramos ParedesAún no hay calificaciones
- Neisseria GonorrhoeaeDocumento7 páginasNeisseria GonorrhoeaeFidel QuiñonezAún no hay calificaciones
- Acfrogcqdjc7rbitozk2nyk0blqctbkunb Ln7n4moqzaz1nztuj0oke3wf6qatyjvy1b4duxoi6u7pcdv8lvk Q7z7k93mmxgyo13me 3y Clgckxclmcgiwinrm533jyjxhafycydrlgcakvceDocumento19 páginasAcfrogcqdjc7rbitozk2nyk0blqctbkunb Ln7n4moqzaz1nztuj0oke3wf6qatyjvy1b4duxoi6u7pcdv8lvk Q7z7k93mmxgyo13me 3y Clgckxclmcgiwinrm533jyjxhafycydrlgcakvcejuanAún no hay calificaciones
- Curva de Crecimiento Bacteria NoDocumento15 páginasCurva de Crecimiento Bacteria NoPepe Joshi SanAún no hay calificaciones
- Microbiologia by Slidesgo 2 Microbiologia TopicosDocumento21 páginasMicrobiologia by Slidesgo 2 Microbiologia TopicosJavi AnainAún no hay calificaciones
- Taller CocosDocumento4 páginasTaller CocosIngri Natalia Muñoz PachajoaAún no hay calificaciones
- Características Neisseria GonorrhoeaeDocumento5 páginasCaracterísticas Neisseria GonorrhoeaePaula BatistaAún no hay calificaciones
- Micoplasma Gallisepticum PDFDocumento33 páginasMicoplasma Gallisepticum PDFAlejandro BoteroAún no hay calificaciones
- Cap 17 - Bacterias - ESTAFILOCOCOSDocumento12 páginasCap 17 - Bacterias - ESTAFILOCOCOSapi-3697245100% (7)
- Cocos Gram Positivos - : Streptococcus y EnterococcusDocumento67 páginasCocos Gram Positivos - : Streptococcus y EnterococcusMakarena RiquelmeAún no hay calificaciones
- Degradacion de PlaguicidasDocumento8 páginasDegradacion de PlaguicidasAbel YPAún no hay calificaciones
- ParacoccidioidomicosisDocumento1 páginaParacoccidioidomicosisAbel YPAún no hay calificaciones
- VibrioDocumento1 páginaVibrioAbel YPAún no hay calificaciones
- BrucellaDocumento2 páginasBrucellaAbel YPAún no hay calificaciones
- Informe de Demanda Bioquimica de Oxigeno DboDocumento3 páginasInforme de Demanda Bioquimica de Oxigeno DboAbel YPAún no hay calificaciones
- Capnocytophaga y DysgonomonasDocumento1 páginaCapnocytophaga y DysgonomonasAbel YPAún no hay calificaciones
- AmazonasDocumento1 páginaAmazonasAbel YPAún no hay calificaciones
- INVESTIGACIÓNDocumento2 páginasINVESTIGACIÓNAbel YPAún no hay calificaciones
- PicornavirusDocumento2 páginasPicornavirusAbel YPAún no hay calificaciones
- Plasm OdiumDocumento1 páginaPlasm OdiumAbel YPAún no hay calificaciones
- MICELIOSDocumento1 páginaMICELIOSAbel YPAún no hay calificaciones
- Ozono Tera PiaDocumento1 páginaOzono Tera PiaAbel YPAún no hay calificaciones
- SarnaDocumento1 páginaSarnaAbel YPAún no hay calificaciones
- Parásitos IntestinalesDocumento1 páginaParásitos IntestinalesAbel YPAún no hay calificaciones
- Inmunidad AdquiridaDocumento1 páginaInmunidad AdquiridaAbel YPAún no hay calificaciones
- Día Internacional de Las MontañasDocumento2 páginasDía Internacional de Las MontañasAbel YPAún no hay calificaciones
- Estudios de AlimentosDocumento1 páginaEstudios de AlimentosAbel YPAún no hay calificaciones
- Transfusion de SangreDocumento1 páginaTransfusion de SangreAbel YPAún no hay calificaciones
- MicrobiosDocumento1 páginaMicrobiosAbel YPAún no hay calificaciones
- HelmintosDocumento1 páginaHelmintosAbel YPAún no hay calificaciones
- Celulas ViablesDocumento1 páginaCelulas ViablesAbel YPAún no hay calificaciones
- Inocuidad AlimentariaDocumento1 páginaInocuidad AlimentariaAbel YPAún no hay calificaciones
- Tiposdehipotesis Asi Como FuncionesDocumento3 páginasTiposdehipotesis Asi Como FuncionesmayaresAún no hay calificaciones
- Instrucción 1Documento1 páginaInstrucción 1Abel YPAún no hay calificaciones
- Inmunidad InnataDocumento1 páginaInmunidad InnataAbel YPAún no hay calificaciones
- Brucelosis BovinaDocumento2 páginasBrucelosis BovinaAbel YPAún no hay calificaciones
- Teoria de La RelatividadDocumento1 páginaTeoria de La RelatividadAbel YPAún no hay calificaciones
- Vacuna NeumococoDocumento3 páginasVacuna NeumococoAbel YPAún no hay calificaciones
- Brucelosis BovinaDocumento2 páginasBrucelosis BovinaAbel YPAún no hay calificaciones
- NEUMOCOCODocumento3 páginasNEUMOCOCOAbel YPAún no hay calificaciones
- Carta Descriptiva Respuesta Inmune ENF02A 20-2Documento18 páginasCarta Descriptiva Respuesta Inmune ENF02A 20-2Ruth Cobo RosalesAún no hay calificaciones
- GlomerulonefritisDocumento7 páginasGlomerulonefritisRuben GomezAún no hay calificaciones
- Clasificación de Los Virus Patógenos Humanos PDFDocumento1 páginaClasificación de Los Virus Patógenos Humanos PDFarnaldops333Aún no hay calificaciones
- Cuestionarios de Biologia Molecular. CAP. 10 LODISHDocumento4 páginasCuestionarios de Biologia Molecular. CAP. 10 LODISHaquilessalvadorAún no hay calificaciones
- PlacadentalbiofilmDocumento59 páginasPlacadentalbiofilmAna María AramayoAún no hay calificaciones
- HBV y Embarazo Oscar Andres Cuellar ClarosDocumento18 páginasHBV y Embarazo Oscar Andres Cuellar ClarosARLES VISCAYA YOSAAún no hay calificaciones
- AntibioticosDocumento9 páginasAntibioticosStephanie PittiAún no hay calificaciones
- Caracterizacion de Moniliophthora RoreriDocumento177 páginasCaracterizacion de Moniliophthora RoreriCarlos RiveraAún no hay calificaciones
- Condilomatosis 2015 PDFDocumento10 páginasCondilomatosis 2015 PDFvictor raul arohuanca apazaAún no hay calificaciones
- Librito EnfermeriaDocumento93 páginasLibrito EnfermeriaModamania ElquinaAún no hay calificaciones
- ANEXO 4. Cromosomas, Genes y ADNDocumento5 páginasANEXO 4. Cromosomas, Genes y ADNMarisol alcantaraAún no hay calificaciones
- Tec Lacteos CrucigramaDocumento1 páginaTec Lacteos Crucigramaoscar figueroa quevedo0% (1)
- Guia 3.2 ParcialDocumento9 páginasGuia 3.2 ParcialKarla MartinezAún no hay calificaciones
- Betalactámicos - Farmacología BásicaDocumento32 páginasBetalactámicos - Farmacología BásicaSharon MejiaAún no hay calificaciones
- Microbiologia NotasDocumento75 páginasMicrobiologia NotasJazmin LopezAún no hay calificaciones
- Algoritmos de Pbas ConfirmatoriasDocumento20 páginasAlgoritmos de Pbas ConfirmatoriasPedro C. JardonAún no hay calificaciones
- Examen GastroenterologiaDocumento4 páginasExamen GastroenterologiaCesar BianchetAún no hay calificaciones
- Factores de Virulencia BacterianaDocumento28 páginasFactores de Virulencia BacterianaAldo Enrique Castañeda CuevasAún no hay calificaciones
- Neoplasia Endocrina MultipleDocumento2 páginasNeoplasia Endocrina MultipleClaudia VargasAún no hay calificaciones
- Virus - Control BiológicoDocumento21 páginasVirus - Control BiológicoricardoAún no hay calificaciones
- Pathophysiological Mechanisms in Acute Pancreatitis Current Understanding - En.esDocumento14 páginasPathophysiological Mechanisms in Acute Pancreatitis Current Understanding - En.esmetafan_1Aún no hay calificaciones
- 4 ARNs y Transcripción (2021 PS) - Clase 4Documento170 páginas4 ARNs y Transcripción (2021 PS) - Clase 4KATALINA IGNACIA AZÓCARAún no hay calificaciones
- Carcinoma VerrucosoDocumento9 páginasCarcinoma VerrucosoJazmín SabinesAún no hay calificaciones
- Merino 2Documento27 páginasMerino 2Claudio Daniel UbillaAún no hay calificaciones
- Proceso Infeccioso GeneralizadoDocumento51 páginasProceso Infeccioso GeneralizadoMelissa Sanchez Ordoñez0% (1)
- Cronología de Las EnfermedadesDocumento9 páginasCronología de Las EnfermedadesAlfonsina EncarnacionAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa Conceptualkatherine67% (3)
- CitocinaDocumento6 páginasCitocinaJairo BenitezAún no hay calificaciones
- APROBADO Biología 2BGU Herencia-Ligada-Al-SexoDocumento2 páginasAPROBADO Biología 2BGU Herencia-Ligada-Al-SexoKatherine MorochoAún no hay calificaciones
- Informe Sobre Las EubacteriasDocumento18 páginasInforme Sobre Las EubacteriasKatherine QuirozAún no hay calificaciones