0% encontró este documento útil (0 votos)
56 vistas19 páginasEnfermedad de Hirschsprung: Diagnóstico y Tratamiento
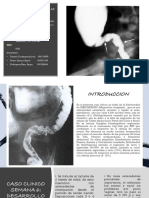
La enfermedad de Hirschsprung es una malformación congénita causada por la ausencia de células ganglionares en parte del colon, lo que causa obstrucción intestinal. Se debe a anomalías en el desarrollo de las crestas neurales durante la gestación. El diagnóstico se basa en la presencia o ausencia de células ganglionares en el plexo mientérico mediante biopsia. El tratamiento es quirúrgico mediante resección del segmento afectado. Existen varios genes asociados como RET y EDN3, a
Cargado por
Xiomara CabellosDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
56 vistas19 páginasEnfermedad de Hirschsprung: Diagnóstico y Tratamiento
La enfermedad de Hirschsprung es una malformación congénita causada por la ausencia de células ganglionares en parte del colon, lo que causa obstrucción intestinal. Se debe a anomalías en el desarrollo de las crestas neurales durante la gestación. El diagnóstico se basa en la presencia o ausencia de células ganglionares en el plexo mientérico mediante biopsia. El tratamiento es quirúrgico mediante resección del segmento afectado. Existen varios genes asociados como RET y EDN3, a
Cargado por
Xiomara CabellosDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd