Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Infecciones Por Bacilos Gramnegativos No Fermentadores - Pseudomonas Aeruginosa
Cargado por
Diego OssesDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Infecciones Por Bacilos Gramnegativos No Fermentadores - Pseudomonas Aeruginosa
Cargado por
Diego OssesCopyright:
Formatos disponibles
ACTUALIZACIÓN
Infecciones por bacilos gramnegativos
no fermentadores: Pseudomonas aeruginosa,
Acinetobacter baumannii y Stenotrophomonas
maltophilia
A. Callejas Díaz*, A. Muñoz Serrano y A. Fernández Cruz
Servicio de Medicina Interna. Hospital Universitario Puerta de Hierro. Majadahonda. Madrid. España. Universidad Autónoma de Madrid. Madrid. España.
Instituto de Investigación Sanitaria Puerta de Hierro Segovia de Arana (IDIPHISA). Majadahonda. Madrid. España.
Palabras Clave: Resumen
- Pseudomonas Los bacilos gramnegativos no fermentadores constituyen un conjunto de microorganismos con gran ca-
- Acinetobacter pacidad de adaptación al medio, por lo que su distribución es universal y tienen facilidad para el desarro-
llo de resistencias a la mayoría de los antibióticos. Los más importante a nivel clínico son Pseudomonas
- Stenotrophomonas aeruginosa, Acinetobacter baumannii y Stenotrophomonas maltophilia. Se trata de microorganismos de
- Infección ámbito hospitalario y carácter oportunista que afectan preferentemente a pacientes inmunodeprimidos o
críticamente enfermos. Por ello, algunos de los principales factores de riesgo para la colonización e in-
fección por dichos microorganismos son la presencia de dispositivos invasivos y el uso previo de antibió-
ticos. Las infecciones producidas por bacilos gramnegativos suelen ser nosocomiales, fundamentalmen-
te la neumonía asociada a ventilación mecánica invasiva. Otras infecciones frecuentes son la bacterie-
mia asociada a catéter venoso o la infección urinaria asociada a catéter vesical. En el caso de P.
aeruginosa, también es destacable su papel en la infección crónica en pacientes con fibrosis quística y
enfermedad pulmonar obstructiva crónica. Este grupo de microorganismos tiene un patrón de resistencia
intrínseca distinto a otros bacilos gramnegativos. Además, dado que tienen la capacidad de desarrollar
múltiples mecanismos de resistencia, instaurar un tratamiento correcto puede ser todo un reto en la
práctica clínica. Por ello, es fundamental disponer de una adecuada política de antibióticos y potenciar
las medidas preventivas.
Keywords: Abstract
- Pseudomonas Nonfermenting Gram-negative bacilli infections: Pseudomonas aeruginosa,
- Acinetobacter Acinetobacter baumannii, and Stenotrophomonas maltophilia
- Stenotrophomonas Nonfermenting Gram-negative bacilli are a group of microorganisms with great capacity for adaptation to
- Infection their environment. For that reason, they are ubiquitous and can develop resistance to most antibiotics
easily. Clinically, the most important bacilli are Pseudomonas aeruginosa, Acinetobacter baumannii, and
Stenotrophomonas maltophilia. They are opportunistic microorganisms present in the hospital setting that
preferentially affect immunosuppressed or critically ill patients. Therefore, some of the main risk factors
for colonization or infection by these microorganisms are the presence of invasive devices and prior use
of antibiotics. Infections caused by Gram-negative bacilli tend to be nosocomial, mainly invasive
mechanical ventilation-associated pneumonia. Other frequent infections are bacteremias associated
with venous catheters or bladder catheter-associated urinary tract infections. In the case of P.
aeruginosa, its role in chronic infections in patients with cystic fibrosis and chronic obstructive
pulmonary disease is also remarkable. This group of microorganisms has an intrinsic resistance pattern
that differs from other Gram-negative bacilli. In addition, given its capacity to develop multiple
mechanisms of resistance, starting appropriate treatment can be a challenge in clinical practice.
Therefore, it is fundamental to have an adequate antibiotics policy and promote preventive measures.
*Correspondencia
Correo electrónico: alejandro.callejasdiaz@gmail.com
Medicine. 2022;13(51):2961-71 2961
ENFERMEDADES INFECCIOSAS (III)
Introducción Acinetobacter baumannii
Es un BGN aerobio estricto, poco exigente e inmóvil. Es ubi-
Los bacilos gramnegativos (BGN) no fermentadores (BGNNF) cuo en el medio. Habitualmente prolifera formando biopelí-
constituyen un grupo de microorganismos de distinto géne- culas que le permiten persistir en diferentes superficies a lo
ro, pero con características microbiológicas comunes que se largo de semanas2. Al igual que P. aeruginosa, puede aislarse en
plasman en un comportamiento similar a nivel clínico. Se sistemas de suministro de agua. En el ser humano, coloniza la
trata de microorganismos con gran resistencia a condiciones piel y las mucosas (cavidad oral, tracto respiratorio y tracto
ambientales adversas, por lo que se aíslan en diferentes me- digestivo). Los pacientes pueden permanecer colonizados du-
dios y con diferente carácter oportunista, colonizando e rante largos períodos de tiempo. A. baumannii es la especie
infectando a pacientes inmunodeprimidos o críticamente con mayor relevancia clínica del género, ya que es responsable
enfermos. Por ello son causantes de infecciones fundamen- de la mayoría de las infecciones3. En general se considera un
talmente en el medio hospitalario, con especial impacto en microorganismo de baja capacidad patogénica, salvo en pa-
Unidades de Cuidados Intensivos (UCI). cientes inmunodeprimidos o críticamente enfermos3.
Stenotrophomonas maltophilia
Microbiología Es un BGN aerobio estricto, poco exigente y móvil, muy
relacionado con el género Pseudomonas. Al igual que P. aeru-
Conceptos generales ginosa y A. baumannii, S. maltophilia tiene predilección por
los medios acuáticos. Así, es frecuente aislarla en la superficie
Se trata de un grupo heterogéneo de microorganismos BGN de diferentes dispositivos, sistemas de suministro de agua e
cuya característica común es que no son capaces de fermen- incluso en soluciones desinfectantes4. En el ser humano,
tar la lactosa en agar MacConkey. En dicho medio, los mi- S. maltophilia es la única especie de su género capaz de pro-
croorganismos fermentadores producirán un ambiente ácido ducir infección. Coloniza la piel y las mucosas como paso
que teñirá de color rosa el medio, al contrario que los BGNNF previo a la infección, especialmente en pacientes con exposi-
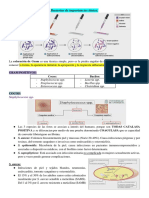
que producirán colonias incoloras (fig. 1). ción previa a carbapenémicos5.
Dentro de este grupo, cabe destacar algunas especies de
especial relevancia clínica como Pseudomonas aeruginosa, Aci-
netobacter baumannii y Stenotrophomonas maltophilia. Otras Patogenia: factores de virulencia
especies incluidas en este grupo a tener en cuenta en deter-
minados contextos clínicos son otras especies de Pseudomo- Pseudomonas aeruginosa
nas, Burkholderia cepacia o Achromobacter xylosoxidans.
Movimiento, adhesión e invasión
Pseudomonas aeruginosa P. aeruginosa suele presentar flagelos, que le otorgan capaci-
Se trata de un BGN aerobio estricto, poco exigente y móvil. dad de movimiento, y fimbrias, útiles para la adhesión a su-
Es ubicua en el medio, con especial predilección por los en- perficies y la formación de biopelículas. Tanto el flagelo
tornos húmedos. Puede producir biopelículas en sistemas de como las fimbrias son capaces de iniciar la respuesta inmu-
conducción de agua, por lo que es frecuente encontrarla en ne6. Los pili, estrechamente relacionados con las fimbrias,
el agua de piscinas, jacuzzis o humidificadores1. Del mismo son determinantes para la transferencia de material genético
modo, puede contaminar el agua estéril o las soluciones para con otros individuos. Además, produce múltiples enzimas
lentes de contacto. En el ser humano, puede colonizar la piel capaces de modificar el medio para favorecer la invasión de
(especialmente el conducto auditivo externo, las axilas y el tejidos, como las elastasas, proteasas y fosfolipasa C.
periné) o las mucosas respiratoria y digestiva.
Formación de biopelículas y cepas mucoides
Esta característica es posible gracias a la agregación bacteria-
na mediada por las fimbrias y a la síntesis de una cápsula del
polisacárido alginato que protege frente a la fagocitosis y
dificulta la acción de los antibióticos7.
Desarrollo de sepsis y toxicidad directa (endotoxina
y exotoxinas)
La principal endotoxina bacteriana de los BGN es el lípido
A, que forma parte del lipopolisacárido (LPS) de superficie y
lo ancla a la membrana bacteriana. El principal papel del
Fig. 1. Placas de agar MacConkey. En la imagen de la izquierda puede observar- LPS es proteger al microorganismo de la acción del comple-
se el crecimiento de colonias de E. coli, bacilo gramnegativo fermentador de mento y de la activación de vías de señalización por citoqui-
lactosa, que crea un medio ácido que tiñe de rosa las colonias. En la imagen nas. El lípido A se denomina endotoxina por su capacidad
de la derecha puede observarse el crecimiento de colonias de P. aeruginosa,
bacilo gramnegativo no fermentador, por lo que las colonias no presentan colo- para activar el TLR-4, con la consecuente cascada de cito-
ración. Figura cortesía de Marcos López Dosil. quinas que lleva al desarrollo de sepsis8. Por otro lado, las
2962 Medicine. 2022;13(51):2961-71
INFECCIONES POR BACILOS GRAMNEGATIVOS NO FERMENTADORES: PSEUDOMONAS AERUGINOSA,
ACINETOBACTER BAUMANNII Y STENOTROPHOMONAS MALTOPHILIA
exotoxinas están estrechamente relacionadas con la lesión Epidemiología y factores de riesgo
directa sobre algunos tejidos, aunque no se ha conseguido
identificar ninguna que, de forma aislada, guarde relación
del hospedador
directa con el desarrollo de sepsis. Las exotoxinas más im-
De forma global, son mucho más frecuentes las infecciones
portantes de P. aeruginosa pertenecen al sistema de secreción
por cocos grampositivos o enterobacterias que las infeccio-
de tipo III, mediante el cual las toxinas pueden ser inyectadas
nes por BGNNF. Sin embargo, dado su carácter oportunis-
directamente en el citoplasma de las células, siendo las más
ta, su presencia es mucho más frecuente en pacientes inmu-
importantes exoS, exoT y exoU9,10. La actividad citolítica,
nodeprimidos, críticos o con disrupción de las barreras
apoptótica e inhibitoria que poseen favorece, por acción so-
epiteliales (posquirúrgicos, portadores de dispositivos inva-
bre neutrófilos y macrófagos, la evasión de la fagocitosis y,
sivos como ventilación mecánica invasiva —VMI—, catéter
por su efecto sobre las células de superficie, la penetración a
venoso central —CVC— o sonda vesical —SV—). Gracias
través de los epitelios.
a su facilidad para el desarrollo de resistencias a los antibió-
P. aeruginosa expresa unos factores de virulencia u otros
en función del ambiente en el que se encuentra. Según esto, ticos, es más frecuente su aislamiento en pacientes con an-
se pueden describir dos fenotipos: tecedente de exposición a los mismos, especialmente aque-
1. Fenotipo invasor, con mayor producción de factores llos de mayor espectro. Todo ello explica que la mayoría de
de toxinas, implicado en infecciones agudas y asociado al de- las infecciones por estos microorganismos se den en medio
sarrollo de bacteriemia y sepsis, especialmente en pacientes hospitalario. Según el estudio EPINE16, estudio epidemio-
inmunodeprimidos y críticamente enfermos. lógico de prevalencia de infecciones relacionadas con la
2. Fenotipo colonizador, resultado de múltiples mutacio- asistencia sanitaria, P. aeruginosa fue el segundo microorga-
nes que favorecen su permanencia en las vías respiratorias, nismo más frecuentemente aislado en el año 2019 (10,23%
con menor capacidad virulenta, mayor resistencia a los me- de los aislamientos). A. baumannii y S. maltophilia se situa-
canismos de defensa del hospedador y a los antibióticos11. ron muy por debajo, con una frecuencia de aislamiento del
Suele afectar a pacientes con fibrosis quística (FQ), enferme- 1,03% y 1,23%, respectivamente. En el caso de las infeccio-
dad pulmonar obstructiva crónica (EPOC) o bronquiec- nes respiratorias de origen nosocomial, la prevalencia de
tasias. estos microorganismos fue mucho mayor (P. aeruginosa
19,42%, A. baumannii 3,24% y S. maltophilia 5,45%). Las
UCI son el lugar donde los BGNNF cobran mayor rele-
Acinetobacter baumannii vancia, y más concretamente P. aeruginosa. Así, fue el mi-
croorganismo aislado con más frecuencia en infecciones
Adhesión, formación de biopelículas y cápsula e invasión nosocomiales de inicio en la UCI según el último estudio
Dicha función es posible gracias a la presencia de fimbrias y ENVIN-HELICS17, con un 13,99% de los aislamientos,
a otras proteínas como Biofilm-associated protein (Bap) y Outer siendo el microorganismo más aislado en neumonía asocia-
membrane protein A (OmpA)12-14. La formación de biopelícu- da a VMI (NAVM; 21,96%) y el segundo en infecciones
las y cápsula de polisacáridos permite la colonización de di- urinarias asociadas a SV (12,17%), bacteriemia de origen
ferentes superficies y la supervivencia en condiciones am- desconocido o relacionada con CVC (6,82%) y bacteriemia
bientales adversas, así como prevenir la activación del secundaria a otros focos (12,01%). En el mismo estudio, las
complemento y evadir la fagocitosis. Por otro lado, OmpA infecciones por A. baumannii y S. maltophilia fueron mucho
induce la apoptosis celular que facilita la invasión tisular, in- menos frecuentes, aunque ambos microorganismos tuvie-
hibe la activación del complemento y tiene un papel activo ron un papel destacado en NAVM. En el caso de A. bau-
en la expulsión activa de los antibióticos. Además, A. bau- mannii, es frecuente que produzca brotes en las unidades de
mannii sintetiza diversas fosfolipasas y proteasas que poten- críticos3.
cian su capacidad invasora. Además de los críticos, los inmunodeprimidos son el otro
gran grupo de pacientes con especial riesgo para infecciones
Secuestro de hierro por BGNNF. En el caso de P. aeruginosa y S. maltophilia,
A. baumannii es capaz de captar hierro del hospedador gra- también son factores de riesgo la diabetes mellitus (DM), las
cias a la expresión de sideróforos12,15. quemaduras extensas y la neutropenia. De hecho, en el pasa-
do, P. aeruginosa fue el principal microorganismo implicado
en la neutropenia febril, especialmente en pacientes con neo-
Stenotrophomonas maltophilia plasias hematológicas (actualmente son los cocos gramposi-
tivos). Actualmente, sigue siendo una causa importante de
Los factores de virulencia de S. maltophilia son menos cono- morbimortalidad, por lo que su cobertura debe ser universal
cidos que los de P. aeruginosa y A. baumannii, aunque com- en el tratamiento empírico de estos pacientes18. Por otro
parten muchos mecanismos patogénicos como la movilidad, lado, P. aeruginosa es capaz de colonizar la vía aérea de forma
la adhesión (fimbrias, hemaglutinina) y formación de biope- persistente en pacientes con patología respiratoria crónica
lículas, los mecanismos de adquisición de hierro, los compo- como FQ, EPOC y bronquiectasias. Las cepas con esta ca-
nentes de la membrana externa, los sistemas de secreción de pacidad se conocen como mucoides y han perdido gran par-
proteínas y enzimas extracelulares (proteasas, fosfolipasas, te de los factores de virulencia a favor de la adquisición de
hemolisinas), etc.4. más mecanismos de resistencia11.
Medicine. 2022;13(51):2961-71 2963
ENFERMEDADES INFECCIOSAS (III)
Manifestaciones clínicas endoftalmitis, por complicación de una infección superficial
(úlcera penetrante), traumatismo, cirugía ocular o disemina-
ción hematógena.
Pseudomonas aeruginosa
Infecciones óticas
Infecciones respiratorias
El espectro de las infecciones óticas es amplio y depende
Como ya se ha descrito, las infecciones respiratorias por
fundamentalmente del hospedador y el mecanismo por el
P. aeruginosa pueden clasificarse en dos tipos fundamentales:
que se produce la infección. En pacientes sanos con antece-
las infecciones agudas en forma de traqueobronquitis o neu-
dente de contacto con agua (piscinas) puede producir otitis
monía y las infecciones crónicas, que se producirán en dos
externa. Sin embargo, en pacientes mayores con DM puede
poblaciones de pacientes bien diferenciadas. Así, la traqueo-
producir otitis externa maligna, infección invasiva capaz de
bronquitis aguda y la neumonía son más frecuentes en
extenderse al cartílago, hueso temporal y apófisis mastoides.
pacientes inmunodeprimidos y críticos, siendo los principa-
Como complicaciones, puede producir parálisis de nervios
les factores de riesgo para su desarrollo la edad avanzada, la
craneales (típicamente el facial) o meningitis. Otras infeccio-
neutropenia, la infección por el virus de la inmunodeficien- nes óticas por P. aeruginosa son la otitis media y la condritis
cia humana (VIH), la hospitalización, el ingreso en la UCI, del pabellón auricular, habitualmente relacionada con la co-
el uso de VMI y la exposición previa a antibióticos. P. aeru- locación de pendientes.
ginosa es el microorganismo más frecuentemente aislado en
neumonía nosocomial, asociada o no a VMI, siendo la causa Infecciones de piel y partes blandas
de en torno al 20% de los casos en la mayoría de las se- Al igual que en el caso de las infecciones oculares y óticas, las
ries16,17. Las infecciones crónicas por P. aeruginosa son carac- características del paciente y el mecanismo de infección son cla-
terísticas de pacientes con FQ, EPOC avanzada con uso ve para el desarrollo de una infección u otra. Dentro de las in-
frecuente de antibióticos y corticoides y bronquiectasias. En fecciones leves, se encuentran el síndrome de las uñas verdes
el caso de la FQ, la infección crónica desencadena una res- (infección del lecho ungueal), la paroniquia o la foliculitis (ante-
puesta inflamatoria mantenida en el tiempo, con un deterio- cedente de contacto con agua de piscinas o jacuzzi). Dentro de
ro lentamente progresivo de la función pulmonar, la princi- las infecciones cutáneas invasivas, destaca la infección de herida
pal causa de muerte en esta entidad19. En el caso de la EPOC, quirúrgica, la infección de úlceras por presión y la infección de
coloniza la vía aérea en períodos de estabilidad clínica, sien- tejidos profundos (objetos punzantes). En el extremo más grave
do su presencia más frecuente conforme avanza la enferme- del espectro de las infecciones cutáneas se encuentran la infec-
dad, aunque la existencia de cepas mucoides es mucho más ción en pacientes quemados (causa frecuente de bacteriemia en
rara que en FQ20. En la EPOC, se asocia a mal control sin- este contexto) y el ectima gangrenoso en el contexto de bacte-
tomático, mayor frecuencia de exacerbaciones y empeora- riemia en pacientes neutropénicos (fig. 2). El ectima gangreno-
miento de la función pulmonar21. so suele comenzar como una mácula superficial o un nódulo
subcutáneo que evoluciona a necrosis cutánea, fruto de la inva-
Infecciones urinarias sión bacteriana y de la trombosis de pequeños vasos.
Suelen producirse en pacientes portadores de SV, antece-
dentes de manipulación urológica e infecciones urinarias de Infecciones osteoarticulares
repetición con uso de múltiples ciclos de antibiótico. P. aeru- Habitualmente se producen por contigüidad (traumatismo,
ginosa constituye el tercer microorganismo en frecuencia de cirugías, úlceras por presión) o por diseminación hematóge-
aislamiento en el ámbito nosocomial16. na en bacteriemias (usuarios de drogas por vía parenteral).
Los tipos de infección más frecuentes en este grupo son la
Bacteriemias e infecciones intravasculares artritis, la osteomielitis y la espondilodiscitis.
P. aeruginosa es el quinto microorganismo aislado con más
frecuencia en bacteriemia nosocomial y el segundo en bacte- Infecciones del sistema nervioso central
riemia en la UCI17,22. Los principales factores de riesgo para La infección del sistema nervioso central (SNC) puede pro-
el desarrollo de bacteriemia por P. aeruginosa son similares a ducir meningitis o abscesos cerebrales en pacientes con an-
infecciones de otro tipo. Los más importantes son la edad, la tecedentes de traumatismo, cirugía, foco contiguo (como
hospitalización, la inmunodepresión (ID), las quemaduras otitis) o diseminación hematógena (pacientes en hemodiáli-
extensas, el uso de dispositivos invasivos y la exposición re- sis, quemados).
ciente a antibióticos (especialmente betalactámicos —BL—).
La mortalidad de la bacteriemia por P. aeruginosa es muy Infecciones abdominales
alta, en torno al 20%-40%. En algunos pacientes puede pro- P. aeruginosa no es un microorganismo frecuentemente im-
ducir endocarditis infecciosa. plicado en infecciones intraabdominales. Habitualmente
suele existir un antecedente concreto como factor de riesgo.
Infecciones oculares Así, puede causar enterocolitis en prematuros, tiflitis en neu-
Suelen producirse en pacientes con alteraciones de la barrera tropénicos o colangitis en relación con manipulación de la
epitelial (traumatismo), uso de lentes de contacto o corticoi- vía biliar. También puede aislarse en infecciones polimicro-
des tópicos. Suele producir conjuntivitis y queratitis con o bianas de pacientes con antecedentes de cirugía reciente y
sin úlceras corneales. En algunas ocasiones puede producir administración de antibióticos de amplio espectro.
2964 Medicine. 2022;13(51):2961-71
INFECCIONES POR BACILOS GRAMNEGATIVOS NO FERMENTADORES: PSEUDOMONAS AERUGINOSA,
ACINETOBACTER BAUMANNII Y STENOTROPHOMONAS MALTOPHILIA
colonización e infección. Esto ocurre típicamente en las in-
fecciones cutáneas o en la orina, donde la colonización aso-
ciada a SV es mucho más frecuente que la infección. Tam-
bién puede producir infecciones oculares, osteoarticulares
(normalmente como complicación de una infección más su-
perficial), del SNC (meningitis nosocomial) e intraabdomi-
nales (peritonitis asociada a diálisis peritoneal).
Stenotrophomonas maltophilia
Infecciones respiratorias
Al igual que en P. aeruginosa y A. baumannii, las infecciones
respiratorias son las más frecuentemente producidas por
S. maltophilia y también suelen asociarse a ingreso en UCI y
VMI. El uso de antibióticos, especialmente carbapenémicos,
y la ID tienen un papel especialmente importante24. Se ha
descrito una variante hemorrágica en pacientes con neopla-
sias hematológicas, rápidamente progresiva y con mayor
mortalidad25. Por otro lado, es un microorganismo que colo-
niza e infecta de forma crónica a pacientes con FQ, aunque
su implicación en el deterioro respiratorio progresivo no está
tan claro como con P. aeruginosa26.
Bacteriemia
Fig. 2. Ectima gangrenoso en el muslo de un paciente con neutropenia. Imagen La bacteriemia es la segunda infección más frecuente produ-
cortesía de Ana Fernández Cruz.
cida por S. maltophilia. La mayoría de las veces está asociada
a la presencia de CVC. Otros focos de origen probable son
el respiratorio, el gastrointestinal y la mucositis en pacientes
Acinetobacter baumannii neutropénicos. La endocarditis es una complicación rara de
la bacteriemia por S. maltophilia.
Infecciones respiratorias
La infección más frecuente por A. baumannii es la neumonía Otras infecciones
nosocomial. Habitualmente se produce en pacientes con co- Se han descrito múltiples infecciones por S. maltophilia, pero
lonización previa de piel y mucosas, por lo que en ocasiones son mucho menos frecuentes que las infecciones respirato-
es difícil discernir entre esta última y la infección verdade- rias y las bacteriemias. Entre las más importantes se encuen-
ra23. El paciente tipo es un paciente ingresado en la UCI, con tran las urinarias, de piel y partes blandas (celulitis, infección
VMI y múltiples comorbilidades. La neumonía suele ser más de herida quirúrgica y úlceras por presión, ectima gangreno-
tardía que con otros microorganismos. La sinusitis nosoco- so, etc.), osteoarticulares, meningitis, oculares, etc.
mial se ha descrito en pacientes con VMI y neumonía asocia-
da a la misma.
Diagnóstico
Bacteriemia
La bacteriemia es la segunda infección más frecuente por Los BGNNF crecen en medios habituales y no tiñen el me-
A. baumannii23. Habitualmente se produce de forma secun- dio de MacConkey. P. aeruginosa crece formando colonias
daria a la presencia de un CVC o una neumonía. Otros fac- con un olor característico (similar a las uvas) y color azul
tores de riesgo, algunos de ellos comunes a P. aeruginosa, son verdoso por producción de piocianina y pioverdina. Suele
la estancia prolongada, el ingreso en la UCI, la VMI, la ID, formar parejas en la tinción de Gram y es catalasa y oxidasa
el uso de antibióticos o los antecedentes de traumatismo, ci- positiva (fig. 3). A. baumannii puede verse con forma de co-
rugía, quemaduras o malignidad. El shock séptico se produce cobacilos y estableciendo parejas en la tinción de Gram y es
en aproximadamente un 30% de los pacientes y la mortali- catalasa positivo y oxidasa negativo. S. maltophilia, al igual
dad se sitúa en torno al 20%-60%, siendo más alta cuando la que P. aeruginosa, es catalasa y oxidasa positiva. El uso de
bacteriemia es secundaria a foco respiratorio y menor cuan- MALDI-TOF (matrix-assisted laser desorption/ionization time
do se asocia a CVC. La endocarditis por A. baumannii está of flight) permite la identificación de la especie y detectar de
descrita, pero es rara. forma precoz diversos mecanismos de resistencia de forma
mucho más rápida que los métodos tradicionales. Además, se
Otras infecciones puede utilizar directamente sobre algunas muestras micro-
A. baumannii puede colonizar la piel y las mucosas con cierta biológicas, como los hemocultivos positivos, adelantando el
facilidad, por lo que en ocasiones es difícil distinguir entre proceso de identificación hasta 24-48 horas. Su uso está va-
Medicine. 2022;13(51):2961-71 2965
ENFERMEDADES INFECCIOSAS (III)
múltiples antibióticos, entre los que se encuentran las peni-
cilinas, aminopenicilinas, cefalosporinas de primera, segunda
y algunas de tercera generación, macrólidos, ácido nalidíxico,
tetraciclinas, sulfonamidas, trimetroprim, nitrofurantoínas y
cloranfenicol.
La resistencia adquirida es mucho más variable e impre-
decible, pudiendo desarrollarse durante el tratamiento. Los
principales mecanismos son3,27:
1. Disminución de la penetración de los antibióticos gra-
cias a la mutación en los genes que codifican OprD (outer
membrane porin D), implicada en la penetración de carbape-
némicos en el interior de la célula, sin conferir resistencia
cruzada a otros BL.
2. Aumento de la expulsión de los antibióticos, que suele
afectar a BL, aminoglucósidos y fluoroquinolonas.
3. Inactivación enzimática de los antibióticos, sobre todo
Fig. 3. Panel cromogénico de identificación y resistencias. En la parte superior mediante la producción de betalactamasas. Cada tipo de be-
derecha del panel se encuentran los pocillos que permiten la identificación del talactamasa tiene un espectro de actuación distinto y una
microorganismo, P. aeruginosa en este caso. En la parte inferior del panel se estrategia terapéutica diferente. P. aeruginosa puede producir
testan las resistencias bacterianas. En este caso, los pocillos en los que crece
P. aeruginosa se tiñen de verde por los pigmentos que esta produce. Imagen
betalactamasas del grupo A (betalactamasas de espectro ex-
cortesía de Marcos López Dosil. tendido o BLEE de tipo TEM, SHV, PER, VEB, GES y
CTX-M), B (metalobetalactamasas tipo VIM, IMP, SPM y
GIM), C (AmpC, que son cefalosporinasas inducibles capa-
lidado para algunos BGNNF como P. aeruginosa o A. bau- ces de conferir resistencia a todos los BL; normalmente más
mannii, pero es menos fiable para otras especias como Achro- activas frente a imipenem que a meropenem) o D (OXA).
mobacter spp. y Burkholderia cepacia. Las enzimas con capacidad carbapenemasa suelen estar den-
tro del grupo de las metalobetalactamasas, aunque también
existen ejemplos en el resto de grupos. P. aeruginosa tam-
Mecanismos de resistencia bién es capaz de inducir modificaciones en la estructura de
los aminoglucósidos, disminuyendo su afinidad por la subu-
Los mecanismos de resistencia bacterianos pueden ser intrín- nidad 30S de los ribosomas.
secos o adquiridos y, a su vez, constitutivos o inducibles. La 4. Modificación de la diana de los antibióticos, como las
adquisición de resistencia suele producirse por mutaciones mutaciones en los genes gyrA y parC que confieren cambios en
cromosómicas, por transferencia horizontal de genes a través la DNA girasa y la topoisomerasa, que suele ser el mecanismo
de plásmidos, integrones, transposones o transformación o de resistencia más importante frente a fluoroquinolonas. Otro
por una combinación de estos mecanismos. Los tipos de resis- ejemplo es la metilación en la subunidad 16S de los ribosomas,
tencia más habituales en las bacterias son los siguientes: que confiere resistencia a los aminoglucósidos.
1. Disminución de la penetración de los antibióticos, La resistencia a los antimicrobianos en P. aeruginosa se
condicionada por el número de porinas en la membrana de asocia con una mayor duración de la hospitalización y una
la bacteria que permiten el paso al interior. mayor mortalidad28. El uso previo de carbapenémico, inclui-
2. Aumento de la expulsión de los antibióticos, provoca- do ertapenem (que no tiene actividad antipseudomonas), se
da por la presencia de bombas de expulsión activa. ha identificado repetidamente como un factor de riesgo de
3. Inactivación enzimática de los antibióticos. Suele ser el resistencia a los carbapenémicos29. Existe una clasificación
mecanismo de resistencia más importante de todos, especial- que permite denominar las cepas de P. aeruginosa como mul-
mente para los BL. tirresistentes, extremadamente resistentes o panresistentes
4. Modificación de la diana de los antibióticos. en función del número de fármacos o grupos disponibles
para su tratamiento30. Sin embargo, esta clasificación pone a
Los BGNNF suelen presentar resistencia a los antibióti- todos los antibióticos antipseudomónicos al mismo nivel,
cos por combinación de los primeros tres mecanismos, pese a que hay diferencias en cuanto a eficacia y toxicidad.
mientras que el cuarto es más frecuente en cocos gramposi- Por dicho motivo, se ha definido el nuevo concepto de diffi-
tivos. cult-to-treat resistance (DTR), que se refiere a la resistencia a
los agentes de primera línea: BL y fluoroquinolonas31.
Pseudomonas aeruginosa
Acinetobacter baumannii
La resistencia intrínseca de P. aeruginosa se debe a varios me-
canismos que coexisten de forma habitual: limitación de las La elevada resistencia intrínseca de A. baumannii se debe en
porinas de membrana, sistemas de expulsión activa y enzimas gran parte a la baja permeabilidad de la membrana (baja con-
hidrolíticas. Así, P. aeruginosa es intrínsecamente resistente a centración y tamaño de las porinas de la membrana). Además,
2966 Medicine. 2022;13(51):2961-71
INFECCIONES POR BACILOS GRAMNEGATIVOS NO FERMENTADORES: PSEUDOMONAS AERUGINOSA,
ACINETOBACTER BAUMANNII Y STENOTROPHOMONAS MALTOPHILIA
presenta dos enzimas hidrolíticas: ADC (Acinetobacter-derived ción del antibiótico, tanto en tratamiento empírico como en
cephalosporinase) y OXA-5112,23. La ADC es un tipo de AmpC dirigido. En primer lugar, la presencia de resistencia intrín-
codificada cromosómicamente que de forma habitual solo seca a algunos antibióticos de uso común obliga a tener un
confiere resistencia a ampicilina. Sin embargo, cuando su ex- alto índice de sospecha en el momento de decidir la cobertu-
presión se intensifica, puede extenderse a piperacilina, cefo- ra antibiótica. Además, su facilidad para la adquisición de
taxima, ceftazidima, cefepime y aztreonam. OXA-51 puede resistencia adquirida hace que sea fundamental conocer los
ser responsable de resistencia a carbapenémicos. aislamientos previos del paciente y la prevalencia de determi-
La resistencia adquirida por A. baumannii también puede nados microorganismos resistentes en la unidad en la que se
producirse por múltiples mecanismos12,23. Tiene gran capaci- encuentra. Por último, un problema añadido es la posibilidad
dad de captar e incorporar material genético externo. Al de aparición de resistencias durante el tratamiento, que ha de
igual que P. aeruginosa, el mecanismo más importante es la sospecharse siempre en casos de mala evolución.
producción de betalactamasas, que pueden ser de tipo A
(TEM, PER, VEB, KPC), B (VIM, IMP, SIM, SPM o
NDM) o D (OXA de diferente tipo). Otros mecanismos de Pseudomonas aeruginosa
resistencia frecuentemente encontrados en A. baumannii son
los cambios en porinas de membrana (Omp 33–36, CarO, Existen múltiples antibióticos con actividad frente a P. aerugi-
OmpW), bombas de expulsión (como el sistema AdeABC, nosa (tabla 1). Como fármacos de primera línea se consideran
responsable de la resistencia a BL, fluoroquinolonas, tetraci- los BL y las fluoroquinolonas, ya que se trata de agentes con
clinas, cloranfenicol o tigeciclina) y modificación de las pro- alta eficacia y baja toxicidad. Dentro de los BL de primera lí-
teínas de unión a penicilina. Los mecanismos de resistencia nea contamos con piperacilina/tazobactam, ceftazidima, cefe-
adquirida a otros antibióticos son similares a los encontrados pime, aztreonam y los carbapenémicos. Las fluoroquinolonas
en P. aeruginosa (bombas de expulsión, modificaciones en las con actividad antipseudomónica son ciprofloxacino y levo-
proteínas girasa y topoisomerasa —fluoroquinolonas— y en floxacino. Habitualmente se usan las fluoroquinolonas en te-
las subunidades 16S de los ribosomas —aminoglucósidos—). rapia secuencial, en infecciones leves y en aquellas donde los
Se ha descrito heterorresistencia, caracterizada por subpo- BL no penetran adecuadamente (otitis media maligna, prosta-
blaciones resistentes dentro de una sola cepa de Acinetobacter. titis, traqueobronquitis en FQ)27. Como fármacos de segunda
línea, se dispone de ceftazidima/avibactam, ceftolozano/tazo-
bactam, cefiderocol, imipenem-cilastatina/relebactam, los
Stenotrophomonas maltophilia aminoglucósidos (incluida la plazomicina) y las polimixinas
(colistina). Estos fármacos deben reservarse para el tratamien-
La resistencia intrínseca de S. maltophilia a múltiples BL se to empírico en situaciones con alto riesgo de resistencia o
debe fundamentalmente a la combinación de varios mecanis- cuando existe resistencia a fármacos de primera línea27,32. El
mos: escasa concentración de antibióticos en el interior de la porcentaje de cepas sensibles a ceftolozano/tazobactam suele
bacteria, gracias a la escasa permeabilidad de su membrana y ser mayor que a ceftazidima/avibactam e imipenem-cilastati-
a las bombas de expulsión activa, y a la presencia de betalac- na/relebactam, porque ceftolozano tiene actividad intrínseca
tamasas inducibles L1 y L2. L1 es la responsable de la resis- frente a las cepas resistentes de P. aeruginosa32,33. Cefiderocol
tencia intrínseca a todos los BL salvo aztreonam, mientras no debe considerarse como la primera opción fuera del foco
que L2 tiene actividad cefalosporinasa, siendo sensible a cla- urinario. Los aminoglucósidos se asocian a mayor riesgo de
vulánico. La mayoría de las cepas de S. maltophilia son resis- fracaso terapéutico cuando se utilizan en monoterapia34, por lo
tentes a los aminoglucósidos, mientras que el porcentaje de que habitualmente se emplean en combinación. Sin embargo,
cepas sensibles a fluoroquinolonas es mayor. en infección urinaria sí podrían plantearse como tratamiento
único si existe resistencia a los fármacos de primera línea27,32.
En el caso de colistina, debe evitarse su uso siempre que sea
Tratamiento posible por el alto riesgo de toxicidad renal.
La forma de empleo de los antibióticos en infecciones
De forma general, la elección del antibiótico depende funda- por P. aeruginosa difiere de la que se aplica en infecciones por
mentalmente de la situación clínica del paciente, la localiza- otros microorganismos (tabla 1). Por ello, existen algunos
ción de la infección, los aislamientos microbiológicos, la pre- aspectos que se deben tener en cuenta:
valencia de resistencias en el hospital y/o la unidad, la
toxicidad de los fármacos y el historial de alergias. Otros as- Dosis
pectos a tener en cuenta son la importancia de iniciar pre- Algunos de los antibióticos antipseudomónicos deben usarse
cozmente un tratamiento adecuado, el posible beneficio de en dosis más altas de las que se recomiendan de forma gene-
usar tratamiento combinado en algunos pacientes de alto ral27. Además, en muchas ocasiones se recomienda la adminis-
riesgo y la importancia de conseguir un control del foco in- tración en perfusión extendida con el objetivo de mantener las
feccioso cuando sea posible. En el caso de los BGNNF, dicha concentraciones sobre la CMI el máximo tiempo posible.
elección puede suponer un reto importante, especialmente
en el momento de instaurar un tratamiento empírico. Su pa- Tratamiento combinado
trón de resistencias puede suponer un problema importante Existen múltiples estudios en los que se ha observado que el
que se hace especialmente patente en el momento de la elec- tratamiento combinado no supone ninguna ventaja sobre la
Medicine. 2022;13(51):2961-71 2967
ENFERMEDADES INFECCIOSAS (III)
TABLA 1
Antibióticos potencialmente activos frente a Pseudomonas aeruginosa
P. aeruginosa Comentarios
Penicilinas
Piperacilina/tazobactam 2/0,25-4/0,5 g cada 6-8 h
Cefalosporinas
Ceftazidima 1-2 g cada 8 h
Ceftazidima/avibactam 2/0,5 g cada 8 h
Cefepima 1-2 g cada 8-12 h
Ceftolozano/tazobactam 1/0,5-2/1 g cada 8 h Betalactámico con mayor actividad intrínseca frente
a P. aeruginosa
Cefiderocol 2 g cada 8 h
Monobactames
Aztreonam 1 g cada 6-8 h (hasta 2 g cada 8 h)
Aztreonam/avibactam (aztreonam + ceftazidima/avibactam) 2 g cada 8 h + 1/0,5-2/1 g cada 8 h
Carbapenémicos
Imipenem/cilastatina 0,5-1 g cada 6-8 h Potente inductor de AmpC, por lo que se debe evitar
Imipenem/cilastatina/relebactam 0,5/0,25 mg cada 6 h
Meropenem 0,5-1 g cada 6-8 h (hasta 2 g cada 8 h)
Meropenem/vaborbactam 2/2 g cada 8 h
Fluoroquinolonas Usar en combinación o como terapia puente
Ciprofloxacino 400 mg cada 8-12 h (i.v.)/500-750 mg cada 12 h (v.o.) De elección en otitis media maligna, prostatitis y
traqueobronquitis en pacientes con fibrosis quística
Levofloxacino 500-750 mg cada 24 h (hasta 750 mg cada 12 h)
Aminoglucósidos Usar en combinación
Gentamicina 5-7 mg/kg/día (hasta 9 mg/kg/día)
Amikacina 15-20 mg/kg/día (hasta 30 mg/kg/día) Aminoglucósido activo frente a un mayor número de cepas
Tobramicina 5-7 mg/kg/día (hasta 9 mg/kg/día) Aminoglucósido con mayor actividad frente a P. aeruginosa
Plazomicina 15 mg/kg/día
Polimixinas Usar en combinación
Colistina 9 MU (1ª dosis) + 4,5 MU cada 12 h Evitar en la medida de lo posible por nefrotoxicidad
Los antibióticos de primera línea se marcan en negrita. i.v.: intravenoso; MU: millones de unidades; v.o.: vía oral.
monoterapia en infecciones por
P. aeruginosa35. Sin embargo, el uso de
tratamiento empírico con asociaciones Criterios
de antibióticos acelera la disminu- Sepsis/shock séptico
ción de la población bacteriana inicial, Foco con alta carga bacteriana (neumonía extensa o con necrosis/cavitación)
evita la selección de cepas mutantes Inmunodepresión grave (neutropenia < 500 neutrófilos/mm3)
Riesgo de colonización por P. aeruginosa multirresistente*
y aumenta la probabilidad de que al
menos uno de los fármacos sea ade-
cuado27,32, especialmente útil en las Ningún criterio Algún criterio
primeras 24-72 horas (fig. 4). La com-
binación más utilizada suele ser la de Betalactámico activo frente
Betalactámico activo frente
un BL con un aminoglucósido (habi- a P. aeruginosa
a P. aeruginosa
tualmente amikacina) o una fluoroqui- Ceftolozano-tazobactam/ceftazidima-
Piperacilina-tazobactam/ceftazidima/
nolona (habitualmente ciprofloxaci- avibactam/meropenem/ceftazidima/
meropenem
no). En algunas ocasiones se puede piperacilina-avibactam
plantear el tratamiento combinado
con polimixinas o fosfomicina. Si la ± +
cepa de P. aeruginosa es sensible a un
betalactámico, en la mayoría de las Amikacina/fluorquinolona
Amikacina/colistina
(ciprofloxacino o levofloxacino)
ocasiones se podrá suspender el anti-
biótico adyuvante tras 48-72 horas. En
el tratamiento dirigido se suele optar Fig. 4. Elección de los antibióticos en infecciones por P. aeruginosa. *Uso de betalactámicos con actividad
por la monoterapia, aunque en algu- frente a P. aeruginosa en los últimos 90 días, prevalencia de P. aeruginosa multirresistente en el hospital > 10%-
20% o historia de colonización/infección por P. aeruginosa multirresistente. Adaptada de Mensa J, et al.27.
nos casos podría plantearse la combi-
2968 Medicine. 2022;13(51):2961-71
INFECCIONES POR BACILOS GRAMNEGATIVOS NO FERMENTADORES: PSEUDOMONAS AERUGINOSA,
ACINETOBACTER BAUMANNII Y STENOTROPHOMONAS MALTOPHILIA
TABLA 2
Antibióticos potencialmente activos frente a Acinetobacter baumannii y Stenotrophomonas maltophilia
A. baumannii S. maltophilia Comentarios
Penicilinas
Ampicilina/sulbactam 1/0,5-2/1 cada 6-8 h4 – Sulbactam tiene actividad directa frente a A. baumannii
Piperacilina/tazobactam 2/0,25-4/0,5 g cada 6-8 h 2/0,25-4/0,5 g cada 6-8 h Activa frente a algunos aislados de S. maltophilia
Cefalosporinas
Ceftazidima 1-2 g cada 8 h 1-2 g cada 8 h Activa frente a algunos aislados de S. maltophilia
Ceftazidima/avibactam – 2/0,5 g cada 8 h Activa frente a algunos aislados de S. maltophilia
Cefepima 1-2 g cada 8-12 h –
Ceftolozano/tazobactam 1/0,5-2/1 g cada 8 h 1/0,5-2/1 g cada 8 h Activa frente a algunos aislados de S. maltophilia
Cefiderocol 2 g cada 8 h 2 g cada 8 h Muy buena actividad in vitro
Monobactames
Aztreonam – –
Aztreonam/avibactam (aztreonam + – 2 g cada 8 h + 1/0,5-2/1 g cada 8 h Activo frente al 98% de aislados de S. maltophilia
ceftazidima/avibactam)
Carbapenémicos
Imipenem/cilastatina 0,5-1 g cada 6-8 h –
Imipenem/cilastatina/relebactam 0,5/0,25 mg cada 6 h –
Meropenem es menos activo que imipenem
Meropenem 0,5-1 g cada 6-8 h (hasta 2 g cada 8 h)5 – en A. baumannii
Meropenem/vaborbactam 2/2 g cada 8 h –
Fluoroquinolonas
400 mg cada 8-12 h (i.v.)/500-750 mg cada 12 h
Ciprofloxacino –
(v.o.)
500-750 mg cada 24 h (hasta 750 mg
Levofloxacino 500-750 mg cada 24 h (hasta 750 mg cada 12 h) cada 12 h)
Moxifloxacino – 400 mg cada 24 h
Aminoglucósidos Usar en combinación
Gentamicina 5-7 mg/kg/día (hasta 9 mg/kg/día) –
Amikacina 15-20 mg/kg/día (hasta 30 mg/kg/día) –
Tobramicina 5-7 mg/kg/día (hasta 9 mg/kg/día) –
Plazomicina 15 mg/kg/día –
Polimixinas Usar en combinación
Colistina 9 MU (1ª dosis) + 4,5 MU cada 12 h 9 MU (1ª dosis) + 4,5 MU cada 12 h
Tetraciclinas
Minociclina 200 mg (1ª dosis) + 100 mg cada 12 h 200 mg (1ª dosis) + 100 mg cada 12 h Tetraciclina más activa frente a S. maltophilia
100 mg (1ª dosis) + 50 mg cada 12 h (se Puede ser sinérgica con cotrimoxazol, amikacina
Tigeciclina 100 mg (1ª dosis) + 50 mg cada 12 h puede doblar 1ª dosis y mantenimiento) y colistina para S. maltophilia
Eravaciclina 1 mg/kg cada 12 h 1 mg/kg cada 12 h
Diaminopirimidina/sulfamidas
Trimetroprim/sulfametoxazol 160/800 mg 8-12 h 160/800 mg 8-12 h Activo frente al 95% de aislados de S. maltophilia
Rifamicinas
Rifampicina 600 mg cada 12-24 h 600 mg cada 12-24 h
Con las dosis habituales no se alcanza la Cmáx
Rifabutina 150-300 mg cada 24 h – necesaria para tratar A. baumannii
Los antibióticos de primera línea se marcan en negrita. Cmáx: concentración máxima; i.v.: intravenoso; MU: millones de unidades; v.o.: vía oral.
nación: shock séptico, endocarditis, infecciones del SNC, neu- Acinetobacter baumannii
tropenia grave (menos de 500 células/mm3) o resistencia a BL27.
Entre las opciones terapéuticas para cubrir A. baumannii po-
Vías especiales de administración demos contar con cefalosporinas (ceftazidima, cefepime, ce-
En función de la localización de la infección, se puede plan- fiderocol), carbapenémicos (imipenem, meropenem), amino-
tear el uso de antibióticos tópicos. En este sentido, lo más glucósidos (amikacina, tobramicina), quinolonas (levofloxacino),
utilizado han sido los aminoglucósidos y colistina por vía tetraciclinas (doxiciclina, tigeciclina, minociclina), colistina y
inhalada como terapia adyuvante en pacientes con infeccio- otros antibióticos como sulbactam, rifampicina, rifabutina o
nes respiratorias por P. aeruginosa, sobre todo en pacientes cotrimoxazol (tabla 2). Piperacilina/tazobactam puede ser
con FQ y en infecciones por cepas resistentes27. sensible in vitro, pero debe evitarse. Con respecto a los car-
Medicine. 2022;13(51):2961-71 2969
ENFERMEDADES INFECCIOSAS (III)
bapenémicos, debe conocerse que la sensibilidad frente a uno neutropenia, situación crítica, gravedad de la comorbilidad).
de ellos no suele predecir sensibilidad frente al resto. Ade- Las neumonías y las bacteriemias son el tipo de infección con
más, imipenem es activo con mayor probabilidad que mero- mayor mortalidad, especialmente cuando se asocian a shock.
penem, mientras que ertapenem no es activo. Sulbactam en En el caso de P. aeruginosa, la mortalidad de la bacteriemia se
dosis altas tiene efecto directo sobre las PBP de A. bauman- sitúa en torno al 20%-40% y se concentra en los primeros
nii. Solo existe coformulado con ampicilina. En pacientes días desde el inicio de los síntomas. El retraso en el inicio del
con infecciones leves y/o baja probabilidad de cepas resisten- tratamiento antibiótico y el tratamiento empírico no adecua-
tes, puede usarse ampicilina/sulbactam, cefepime o imipe- do son factores clave en el grueso de los estudios de morta-
nem en monoterapia. En el caso de infecciones graves o con lidad. En este sentido, existen varios estudios que han ob-
alto riesgo de resistencia, se recomienda el uso en combina- servado una mayor mortalidad con cepas resistentes de
ción de varios de estos antibióticos, a poder ser un BL con P. aeruginosa y A. baumannii28,40, lo cual podría estar relacio-
aminoglucósido, fluoroquinolona o colistina. Deben evitarse nado con la menor probabilidad de instaurar un tratamiento
las combinaciones de meropenem y colistina por el alto ries- empírico correcto.
go de fracaso terapéutico36. En caso de resistencia a los BL,
los regímenes recomendados suelen basarse en colistina o
tigeciclina. Cefiderocol podría ser una buena opción tera- Responsabilidades éticas
péutica, especialmente frente a las cepas resistentes a carba-
penémicos, pero hacen falta más estudios37. La terapia com- Protección de personas y animales. Los autores declaran
binada con ampicilina/sulbactam, meropenem y colistina es que para esta investigación no se han realizado experimentos
activa incluso frente a cepas panresistentes en modelos in en seres humanos ni en animales.
vitro38. El uso de antibióticos inhalados ha sido utilizado para
infecciones por A. baumannii con resultados variables. Confidencialidad de los datos. Los autores declaran que en
este artículo no aparecen datos de pacientes.
Stenotrophomonas maltophilia Derecho a la privacidad y consentimiento informado.
Los autores declaran que en este artículo no aparecen datos
El tratamiento de elección de las infecciones por S. maltophi- de pacientes.
lia es trimetoprim-sulfametoxazol (cotrimoxazol), que ha
demostrado su eficacia en estudios in vitro (activo frente al Conflicto de intereses
95% de los aislados) y en estudios clínicos (tabla 2). En las Los autores declaran no tener ningún conflicto de intereses.
situaciones en las que no se pueda usar cotrimoxazol, la al-
ternativa más utilizada son las fluoroquinolonas, especial-
mente levofloxacino. Sin embargo, la principal desventaja es Bibliografía
su susceptibilidad al desarrollo de resistencias. Otros trata-
mientos disponibles son colistina o las tetraciclinas (tigecicli- r Importante rr Muy importante
na, minociclina)39, aunque tigeciclina no se recomienda para ✔ Metaanálisis ✔ Artículo de revisión
el tratamiento de neumonías ni de bacteriemias. Los amino-
glucósidos y los BL no suelen ser activos y se debe evitar su
✔ Ensayo clínico controlado ✔ Guía de práctica clínica
uso, independientemente de los estudios de sensibilidad, in-
✔ Epidemiología
cluso para los carbapenémicos. El tratamiento combinado
puede ser sinérgico in vitro. Así, se han propuesto distintas ✔
1. Walker J, Moore G. Pseudomonas aeruginosa in hospital water systems:
biofilms, guidelines, and practicalities. J Hosp Infect. 2015;89(4):324-7.
combinaciones de cotrimoxazol, fluoroquinolonas y BL (es- ✔
2. Bernards AT, Harinck HIJ, Dijkshoorn L, van der Reijden TJK, van den
Broek PJ. Persistent Acinetobacter baumannii? Look inside your medical
pecialmente ceftazidima), que podrían ser útiles en trata- equipment. Infect Control Hosp Epidemiol. 2004;25(11):1002-4.
miento empírico hasta conocer resistencias o en pacientes 3. rr Fariñas MC, Martínez-Martínez L. Infecciones causadas por
✔ bacterias gramnegativas multirresistentes: enterobacterias, Pseudo-
seleccionados. Aunque no existe suficiente evidencia, es po- monas aeruginosa, Acinetobacter baumannii y otros bacilos gram-
sible que cefiderocol y la combinación de aztreonam con negativos no fermentadores. Enferm Infecc Microbiol Clin. 2013;
avibactam sean alternativas eficaces para cepas multirresis- 31(6):402-9.
tentes39. Al igual que con P. aeruginosa y A. baumannii, exis- ✔
4. Brooke JS. Advances in the Microbiology of Stenotrophomonas malto-
philia. Clin Microbiol Rev. 34(3):e0003019.
ten algunos estudios que han demostrado un posible papel de ✔
5. Aitken SL, Sahasrabhojane PV, Kontoyiannis DP, Savidge TC, Arias CA,
Ajami NJ, et al. Alterations of the oral microbiome and cumulative car-
la vía inhalatoria en colonizaciones o infecciones respirato- bapenem exposure are associated with Stenotrophomonas maltophilia infec-
rias. tion in patients with acute myeloid leukemia receiving chemotherapy.
Clin Infect Dis. 2021;72(9):1507-13.
✔
6. Miao EA, Andersen-Nissen E, Warren SE, Aderem A. TLR5 and Ipaf:
dual sensors of bacterial flagellin in the innate immune system. Semin
Pronóstico ✔
7.
Immunopathol. 2007;29(3):275-88.
Lee K, Yoon SS. Pseudomonas aeruginosa Biofilm, a programmed bacterial
life for fitness. J Microbiol Biotechnol. 2017;27(6):1053-64.
El pronóstico de las infecciones por BGNNF no solo depen- ✔
8. Heumann D, Roger T. Initial responses to endotoxins and Gram-nega-
tive bacteria. Clin Chim Acta. 2002;323(1-2):59-72.
de de la virulencia de los microorganismos y las característi- ✔
9. Hattemer A, Hauser A, Diaz M, Scheetz M, Shah N, Allen JP, et al.
Bacterial and clinical characteristics of health care- and community-ac-
cas de la infección, sino que cobra especial importancia la quired bloodstream infections due to Pseudomonas aeruginosa. Antimi-
situación del paciente en el momento de la infección (ID, crob Agents Chemother. 2013;57(8):3969-75.
2970 Medicine. 2022;13(51):2961-71
INFECCIONES POR BACILOS GRAMNEGATIVOS NO FERMENTADORES: PSEUDOMONAS AERUGINOSA,
ACINETOBACTER BAUMANNII Y STENOTROPHOMONAS MALTOPHILIA
✔
10. El-Solh AA, Hattemer A, Hauser AR, Alhajhusain A, Vora H. Clinical
outcomes of type III Pseudomonas aeruginosa bacteremia. Crit Care
✔
26. Hansen CR. Stenotrophomonas maltophilia: To be or not to be a cystic
fibrosis pathogen. Vol. 18, Current Opinion in Pulmonary Medicine.
Med. 2012;40(4):1157-63. Curr Opin Pulm Med; 2012. p. 628-31.
✔
11. Malhotra S, Hayes D Jr, Wozniak DJ. Cystic fibrosis and Pseudomonas 27. rr Mensa J, Barberán J, Soriano A, Llinares P, Marco F, Cantón R,
✔
aeruginosa: the host-microbe interface. Clin Microbiol Rev. 2019;32(3): et al. Antibiotic selection in the treatment of acute invasive infec-
e00138-18. tions by Pseudomonas aeruginosa: Guidelines by the Spanish soci-
12. rr Ayoub Moubareck C, Hammoudi Halat D. Insights into Aci-
✔ ety of chemotherapy. Rev Esp Quimioter. 2018;31(1):78-100.
netobacter baumannii: A review of microbiological, virulence, and
resistance traits in a threatening nosocomial pathogen. Antibiotics
✔
28. Thaden JT, Park LP, Maskarinec SA, Ruffin F, Fowler VG, Van Duin D.
Results from a 13-year prospective cohort study show increased mortal-
(Basel). 2020;9(3):119. ity associated with bloodstream infections caused by pseudomonas aeru-
✔
13. Gaddy JA, Tomaras AP, Actis LA. The Acinetobacter baumannii 19606
OmpA protein plays a role in biofilm formation on abiotic surfaces and
ginosa compared to other bacteria. Antimicrob Agents Chemother. 2017;
61(6):e02671-16.
in the interaction of this pathogen with eukaryotic cells. Infect Immun. 29. r
✔ Cohen MJ, Block CS, Moses AE, Nir-Paz R. Exposure to ertape-
2009;77(8):3150-60. nem is possibly associated with Pseudomonas aeruginosa antibiotic
✔
14. Richards AM, Abu Kwaik Y, Lamont RJ. Code blue: Acinetobacter bau-
30. r
resistance. Clin Microbiol Infect. 2014;20(3):O188-96.
mannii, a nosocomial pathogen with a role in the oral cavity. Mol Oral
Microbiol. 2015;30(1):2-15.
✔ Magiorakos A-P, Srinivasan A, Carey RB, Carmeli Y, Falagas
ME, Giske CG, et al. Multidrug-resistant, extensively drug-resis-
15. r
✔ Dorsey CW, Tolmasky ME, Crosa JH, Actis LA. Genetic organi- tant and pandrug-resistant bacteria: an international expert pro-
zation of an Acinetobacter baumannii chromosomal region har- posal for interim standard definitions for acquired resistance. Clin
bouring genes related to siderophore biosynthesis and transport. Microbiol Infect. 2012;18(3):268-81.
Microbiology (Reading). 2003;149(Pt 5):1227-38. ✔
31. Kadri SS, Adjemian J, Lai YL, Spaulding AB, Ricotta E, Rebecca Prevots
✔
16. Sociedad Española de Medicina Preventiva Salud Pública e Higiene. ES-
TUDIO EPINE-EPPS no 30: 2019 Informe España. Estud EPiNE.
D, et al. Difficult-to-treat resistance in gram-negative bacteremia at 173
US hospitals: Retrospective cohort analysis of prevalence, predictors, and
2019;33-6. outcome of resistance to all first-line agents. Clin Infect Dis. 2018;67(12):
✔
17. Palomar M, Alvarez F, Olaechea P, Gimeno R, Gracia MP, Seijas I et al.
32. r
1803-14.
ENVIN HELICS - Sociedad Española De Medicina Intensiva Crítica Y
Unidades Coronarias (SEMICYUC) Grupo de Trabajo de Enfermedades
✔ Tamma PD, Aitken SL, Bonomo RA, Mathers AJ, Van Duin D,
Clan CJ. Infectious Diseases Society of America Guidance on the
Infecciosas y Sepsis. 2019. Treatment of Extended-Spectrum β-lactamase Producing Entero-
✔
18. Taplitz RA, Kennedy EB, Bow EJ, Crews J, Gleason C, Hawley DK, et
al. Outpatient management of fever and neutropenia in adults treated for
bacterales (ESBL-E), Carbapenem-Resistant Enterobacterales (CRE),
and Pseudomonas aeruginosa with Difficult-to-Treat Resistance
malignancy: American Society of Clinical Oncology and Infectious Dis- (DTR-P. aeruginosa). Clin Infect Dis. 2021;72(7):1109-16.
eases Society of America Clinical practice guideline update. J Clin Oncol. 33. r
✔ Del Barrio-Tofinõ E, Zamorano L, Cortes-Lara S, López-Caus-
2018;36(14):1443-53. ape C, Sánchez-Diener I, Cabot G, et al. Spanish nationwide survey
✔
19. Hogardt M, Hoboth C, Schmoldt S, Henke C, Bader L, Heesemann J.
Stage-specific adaptation of hypermutable Pseudomonas aeruginosa iso-
on Pseudomonas aeruginosa antimicrobial resistance mechanisms
and epidemiology. J Antimicrob Chemother. 2019;74(7):1825-35.
lates during chronic pulmonary infection in patients with cystic fibrosis.
J Infect Dis. 2007;195(1):70-80.
✔
34. Phe K, Bowers DR, Babic JT, Tam VH. Outcomes of empiric aminogly-
coside monotherapy for Pseudomonas aeruginosa bacteremia. Diagn Mi-
✔
20. Murphy TF, Brauer AL, Eschberger K, Lobbins P, Grove L, Cai X, et al. crobiol Infect Dis. 2019;93(4):346-8.
Pseudomonas aeruginosa in chronic obstructive pulmonary disease. Am J
Respir Crit Care Med. 2008;177(8):853-60.
✔
35. Pena C, Suarez C, Ocampo-Sosa A, Murillas J, Almirante B, Pomar V, et
al. Effect of adequate single-drug vs combination antimicrobial therapy
21. r
✔ Zhang M, Li Q, Zhang X-Y, Ding X, Zhu D, Zhou X. Relevance on mortality in Pseudomonas aeruginosa bloodstream infections: a post
of lower airway bacterial colonization, airway inflammation, and Hoc analysis of a prospective cohort. Clin Infect Dis. 2013;57(2):208-16.
pulmonary function in the stable stage of chronic obstructive
pulmonary disease. Eur J Clin Microbiol Infect Dis. 2010;29(12):
✔
36. Paul M, Daikos GL, Durante-Mangoni E, Yahav D, Carmeli Y, Benattar YD,
et al. Colistin alone versus colistin plus meropenem for treatment of severe
1487-93. infections caused by carbapenem-resistant Gram-negative bacteria: an open-
22. r
✔ Sociedad Española de Medicina Preventiva Salud Pública e Hi- label, randomised controlled trial. Lancet Infect Dis. 2018;18(4):391-400.
giene. European Centre for Disease Prevention and Control. Estu-
dio de Prevalencia de las Infecciones Nosocomiales en España: In-
✔
37. Isler B, Doi Y, Bonomo RA, Paterson DL. New treatment options
against carbapenem-resistant Acinetobacter baumannii Infections. Antimi-
forme Global EPINE-EPPS 2015. Disponible en: http://hws. crob Agents Chemother. 2018;63(1):e01110-18.
vhebron.net/epine/; 2015 [Co. 2015. 38. rr
✔ Lenhard JR, Smith NM, Bulman ZP, Tao X, Thamlikitkul V,
23. r
✔ Lee CR, Lee JH, Park M, Park KS, Bae IK, Kim YB, et al. Biol- Shin BS, et al. High-dose ampicillin-sulbactam combinations combat
ogy of Acinetobacter baumannii: Pathogenesis, antibiotic resistance polymyxin-resistant Acinetobacter baumannii in a hollow-fiber infec-
mechanisms, and prospective treatment options. Front Cell Infect tion model. Antimicrob Agents Chemother. 2017;61(3):e01268-16.
Microbiol. 2017;7:55. 39. r
✔ Biagi M, Tan X, Wu T, Jurkovic M, Vialichka A, Meyer K, et al.
✔
24. Saugel B, Eschermann K, Hoffmann R, Hapfelmeier A, Schultheiss C,
Phillip V, et al. Stenotrophomonas maltophilia in the respiratory tract of
Activity of potential alternative treatment agents for stenotroph-
omonas maltophilia isolates nonsusceptible to levofloxacin and/or
medical intensive care unit patients. Eur J Clin Microbiol Infect Dis. trimethoprim-sulfamethoxazole. J Clin Microbiol. 2020 Jan 28;58(2):
2012;31(7):1419-28. e01603-19.
✔
25. Tada K, Kurosawa S, Hiramoto N, Okinaka K, Ueno N, Asakura Y, et 40. rr
✔ Lemos E V., de la Hoz FP, Einarson TR, Mcghan WF, Que-
al. Stenotrophomonas maltophilia infection in hematopoietic SCT re- vedo E, Castañeda C, et al. Carbapenem resistance and mortality in
cipients: High mortality due to pulmonary hemorrhage. Bone Marrow patients with Acinetobacter baumannii infection: Systematic review
Transplant. 2013;48(1):74-9. and meta-analysis. Clin Microbiol Infect. 2014;20(5):416-23.
Medicine. 2022;13(51):2961-71 2971
También podría gustarte
- Pseudomona Multi RDocumento13 páginasPseudomona Multi RLucila MurdochAún no hay calificaciones
- Clasificar Los Bacilos Gram Negativos No FermentadoresDocumento9 páginasClasificar Los Bacilos Gram Negativos No FermentadoresMaría Fernanda GarcíaAún no hay calificaciones
- s 0210569122002844Documento11 páginass 0210569122002844Jose Manuel C TAún no hay calificaciones
- Acinetobacter y otros BNFDocumento11 páginasAcinetobacter y otros BNFkateryn94Aún no hay calificaciones
- Documento A4 Portada de Proyecto Ilustrado Infantil Multicolor - 20240129 - 090726 - 0000Documento7 páginasDocumento A4 Portada de Proyecto Ilustrado Infantil Multicolor - 20240129 - 090726 - 0000Sarai de NavarroAún no hay calificaciones
- Mecanismos de Resistencia en Pseudomonas Aeruginosa PDFDocumento8 páginasMecanismos de Resistencia en Pseudomonas Aeruginosa PDFGerald D. FrizAún no hay calificaciones
- 70000281Documento5 páginas70000281Fabiola TiempoAún no hay calificaciones
- Tratamiento Fungiosis InvasorasDocumento39 páginasTratamiento Fungiosis InvasorasValentina RojasAún no hay calificaciones
- Bacilos Gram NegativosDocumento0 páginasBacilos Gram Negativospizzini79Aún no hay calificaciones
- Enterobacterias PDFDocumento8 páginasEnterobacterias PDFpaoordiAún no hay calificaciones
- PSEUDOMONA, pylori y CLOSTRIDIUMDocumento47 páginasPSEUDOMONA, pylori y CLOSTRIDIUMKaruAún no hay calificaciones
- 11.037 Infecciones Por Pseudomonas y Otros Bacilos Gramnegativos No FermentadoresDocumento11 páginas11.037 Infecciones Por Pseudomonas y Otros Bacilos Gramnegativos No FermentadoresMarialina PereiraAún no hay calificaciones
- Salud 5af95879ccd87 IRASMMRDocumento9 páginasSalud 5af95879ccd87 IRASMMRDaniel OlveraAún no hay calificaciones
- Microbiología Seminario PseudomonasDocumento47 páginasMicrobiología Seminario PseudomonasAle GonzalezAún no hay calificaciones
- Mecanismos de Resistencia BacterianaDocumento5 páginasMecanismos de Resistencia BacterianaBeele Rojas LobosAún no hay calificaciones
- Protocolo de Manejo de Infecciones Graves Por S.ADocumento8 páginasProtocolo de Manejo de Infecciones Graves Por S.AGabriel RuedaAún no hay calificaciones
- Pseumonas AeruginosaDocumento4 páginasPseumonas AeruginosaNaydelin TorresAún no hay calificaciones
- Bacteriologia Bacilos Gram No FermentadoresDocumento4 páginasBacteriologia Bacilos Gram No FermentadoresShezira Terán CéspedesAún no hay calificaciones
- 10 1016@j Medcli 2019 11 002Documento7 páginas10 1016@j Medcli 2019 11 002LIZBETH GETSEMANI MEDRANO VALADEZAún no hay calificaciones
- IPT Ceftazidima Avibactam Zavicefta AntibioticosDocumento11 páginasIPT Ceftazidima Avibactam Zavicefta AntibioticosAlexander Melo AnguloAún no hay calificaciones
- INFORME Bacilos No FermentadoresDocumento17 páginasINFORME Bacilos No Fermentadoresdani leninAún no hay calificaciones
- BacteriasGramDocumento10 páginasBacteriasGramGreys GarciaAún no hay calificaciones
- Flora Microbiana Normal - MurrayDocumento5 páginasFlora Microbiana Normal - MurrayMARIAMNE AZUCENA IBARRA RESENDIZAún no hay calificaciones
- Multirresistencia Acinetobacter baumanniiDocumento2 páginasMultirresistencia Acinetobacter baumanniikitAún no hay calificaciones
- Non-fermenting Gram-negative bacilli antibiogram interpretationDocumento9 páginasNon-fermenting Gram-negative bacilli antibiogram interpretationMario Fernando CartagenaAún no hay calificaciones
- Acinetobacter BaumanniiDocumento5 páginasAcinetobacter BaumanniiAlondra Hernani PachecoAún no hay calificaciones
- Pseudomonas y Moo RelacionadosDocumento5 páginasPseudomonas y Moo RelacionadosJatziriAún no hay calificaciones
- 3 - Practica 6 Bacilo Cocobacilo GDocumento14 páginas3 - Practica 6 Bacilo Cocobacilo GRosa Nery ChulleAún no hay calificaciones
- Infecciones Por Gérmenes Gram Negativos, Gram PositivosDocumento42 páginasInfecciones Por Gérmenes Gram Negativos, Gram PositivosPABLO FERNANDEZ CONTRERASAún no hay calificaciones
- Samaniego AntibioticosDocumento106 páginasSamaniego AntibioticosKatherine Gissele Poveda CruzAún no hay calificaciones
- Farmacos AntiinfecciososDocumento11 páginasFarmacos AntiinfecciososRICHARAún no hay calificaciones
- Actualización en Otras Infecciones Bacterianas Crónicas - Actinomicosis y BrucelosisDocumento11 páginasActualización en Otras Infecciones Bacterianas Crónicas - Actinomicosis y BrucelosisDiego OssesAún no hay calificaciones
- MMM7ma-17-21 Flora Microbiana Comensal y Patogena en El Ser HumanoDocumento5 páginasMMM7ma-17-21 Flora Microbiana Comensal y Patogena en El Ser HumanoSheryl SuazoAún no hay calificaciones
- Endocarditis InfecciosaDocumento5 páginasEndocarditis Infecciosaricardo vallejosAún no hay calificaciones
- Bacillus AnthracisDocumento12 páginasBacillus AnthracisPedro GonzalezAún no hay calificaciones
- Mecanismos de Resistencia A Los AntibióticosDocumento30 páginasMecanismos de Resistencia A Los AntibióticosAliceAún no hay calificaciones
- ACINETOBACTER Bau FinDocumento38 páginasACINETOBACTER Bau FinrojasguimarayAún no hay calificaciones
- AcinetobacterDocumento14 páginasAcinetobacterCamilo Andrés PáezAún no hay calificaciones
- Infección odontogénica: endógena, polimicrobiana y dinámicaDocumento51 páginasInfección odontogénica: endógena, polimicrobiana y dinámicaHarDmando LauraAún no hay calificaciones
- Articulo Sobre Salmonella y ShigellaDocumento8 páginasArticulo Sobre Salmonella y ShigellaeamegtAún no hay calificaciones
- Infección Odontogénica ResumenDocumento51 páginasInfección Odontogénica ResumenHarDmando Laura100% (1)
- Bacilos Gram Negativos NO Fermentadores de Importancia ClínicaDocumento7 páginasBacilos Gram Negativos NO Fermentadores de Importancia Clínicamam.gimenezAún no hay calificaciones
- Infecciones Por Bacilos Gram Negativos PDFDocumento6 páginasInfecciones Por Bacilos Gram Negativos PDFKarol M.Aún no hay calificaciones
- Microbiologia de IaasDocumento53 páginasMicrobiologia de IaasfelipeAún no hay calificaciones
- Infecciones Por Anaerobios de Piel y Partes Blandas, Orofaringe y Parénquima PulmonarDocumento10 páginasInfecciones Por Anaerobios de Piel y Partes Blandas, Orofaringe y Parénquima PulmonarDiego OssesAún no hay calificaciones
- Stenotrophomonas ExpoDocumento18 páginasStenotrophomonas ExpoDiego Padilla SantosAún no hay calificaciones
- PseudomonaDocumento1 páginaPseudomonacamilae.solanoAún no hay calificaciones
- Sesion Practica 6 - Bacilo y Cocobacilos Gram (-) Final 2023-2Documento14 páginasSesion Practica 6 - Bacilo y Cocobacilos Gram (-) Final 2023-2stephanny palomino quispeAún no hay calificaciones
- Boletín FarmacológicoDocumento5 páginasBoletín FarmacológicoDaniel Aaron Trinidad RamirezAún no hay calificaciones
- Investigación - BacteriasDocumento3 páginasInvestigación - Bacteriasdennise knightAún no hay calificaciones
- Cap 22 TuberculosisDocumento5 páginasCap 22 TuberculosisDiana AlfaroAún no hay calificaciones
- RESUMEN BGNNF, BACTER LABDocumento1 páginaRESUMEN BGNNF, BACTER LABAline FélixAún no hay calificaciones
- 09Documento16 páginas09Jose Armando GonzalezAún no hay calificaciones
- Bacterias Gram (-) oportunistas en UCIDocumento5 páginasBacterias Gram (-) oportunistas en UCIKyriath RuizAún no hay calificaciones
- RESISTENCIA A LOS ANTIMICROBIANOSDocumento15 páginasRESISTENCIA A LOS ANTIMICROBIANOSlesslyAún no hay calificaciones
- Agentes Infecciosos en La CirugiaDocumento3 páginasAgentes Infecciosos en La CirugiaFlores Argüello ValeriaAún no hay calificaciones
- Infecciones Abdominales y Del Tracto Reproductor Femenino Por AnaerobiosDocumento10 páginasInfecciones Abdominales y Del Tracto Reproductor Femenino Por AnaerobiosDiego OssesAún no hay calificaciones
- ACTIVIDAD LAB BACTERIOLOGIA BGNNFDocumento6 páginasACTIVIDAD LAB BACTERIOLOGIA BGNNFSARAHI V. PEREZ LUISAún no hay calificaciones
- AcinetobacterDocumento5 páginasAcinetobacterRocio Yasminy Mamani YucraAún no hay calificaciones
- Los bacteriófagos: Los virus que combaten infeccionesDe EverandLos bacteriófagos: Los virus que combaten infeccionesAún no hay calificaciones
- Infecciones Por EnterococosDocumento10 páginasInfecciones Por EnterococosDiego OssesAún no hay calificaciones
- Asma BronquialDocumento9 páginasAsma BronquialDiego OssesAún no hay calificaciones
- Infecciones Por Listeria, Corynebacterium y BacillusDocumento10 páginasInfecciones Por Listeria, Corynebacterium y BacillusDiego OssesAún no hay calificaciones
- Osteoporosis en La MujerDocumento7 páginasOsteoporosis en La MujerDiego OssesAún no hay calificaciones
- Indicaciones y Tratamiento FotoprotectorDocumento4 páginasIndicaciones y Tratamiento FotoprotectorJames Valera SaavedraAún no hay calificaciones
- Alteraciones Endocrinológicas Prevalentes en La AdolescenciaDocumento11 páginasAlteraciones Endocrinológicas Prevalentes en La AdolescenciaDiego OssesAún no hay calificaciones
- Delirium en Los Pacientes MayoresDocumento10 páginasDelirium en Los Pacientes MayoresDiego OssesAún no hay calificaciones
- Infecciones Por Estreptococo: ResumenDocumento8 páginasInfecciones Por Estreptococo: ResumenILSE ESMERALDASAún no hay calificaciones
- Trastorno BipolarDocumento15 páginasTrastorno Bipolarjorge sarmientoAún no hay calificaciones
- Artritis Idiopática JuvenilDocumento11 páginasArtritis Idiopática JuvenilDiego OssesAún no hay calificaciones
- Enfermedades Metabólicas Óseas - OsteomalaciaDocumento10 páginasEnfermedades Metabólicas Óseas - OsteomalaciaDiego OssesAún no hay calificaciones
- Protocolo diagnóstico dolor lumbarDocumento5 páginasProtocolo diagnóstico dolor lumbarFernando OrtizAún no hay calificaciones
- Actualización Clínica de Los Trastornos Depresivos PDFDocumento11 páginasActualización Clínica de Los Trastornos Depresivos PDFfantomas_Aún no hay calificaciones
- Arbovirosis EndemoepidémicasDocumento17 páginasArbovirosis EndemoepidémicasMARIA CECILIA RODRIGUEZ ABADAún no hay calificaciones
- Protocolo Diagnostico y Terapeu - B. Lopez CarpinteroDocumento4 páginasProtocolo Diagnostico y Terapeu - B. Lopez CarpinteroFideoPereAún no hay calificaciones
- Trastornos Somatomorfos y FacticiosDocumento9 páginasTrastornos Somatomorfos y FacticiosDiego OssesAún no hay calificaciones
- Protocolo Diagnóstico y Terapéutico de La Depresión en El AncianoDocumento6 páginasProtocolo Diagnóstico y Terapéutico de La Depresión en El AncianoDiego OssesAún no hay calificaciones
- TrastornosDocumento2 páginasTrastornosDiego OssesAún no hay calificaciones
- Trastornos de AnsiedadDocumento7 páginasTrastornos de AnsiedadDiego OssesAún no hay calificaciones
- Trastornos DiasociativosDocumento9 páginasTrastornos DiasociativosCarolina ValenciaAún no hay calificaciones
- Concentración y Dilución UrinariaDocumento72 páginasConcentración y Dilución UrinariaDiego OssesAún no hay calificaciones
- MEMORIA PRÁCTICAS 1 EVALUACIÓN NoaDocumento51 páginasMEMORIA PRÁCTICAS 1 EVALUACIÓN NoaNoa CastroAún no hay calificaciones
- Guia Parte 3 y 4 Unidad Morfofisiolgia Ii (Perez Mendoza, Cielo Kayra)Documento72 páginasGuia Parte 3 y 4 Unidad Morfofisiolgia Ii (Perez Mendoza, Cielo Kayra)Cielo Perez MendozaAún no hay calificaciones
- Informe 4 Identificacion de Hongos, Artropodos, EctDocumento84 páginasInforme 4 Identificacion de Hongos, Artropodos, EctChristian MezaAún no hay calificaciones
- Doppler Espectral PDFDocumento77 páginasDoppler Espectral PDFFederico Villarreal OrbegosoAún no hay calificaciones
- F.T. Young FaceDocumento6 páginasF.T. Young FaceJohn DíazAún no hay calificaciones
- Materias Primas y Proceso de ProduccionDocumento4 páginasMaterias Primas y Proceso de ProduccionJorge CéspedesAún no hay calificaciones
- Métodos InmunológicosDocumento19 páginasMétodos Inmunológicosmariipiii100% (3)
- Diagrama de ArbolDocumento5 páginasDiagrama de ArbolJILIBETH PATRICIA BURGOS BRITOAún no hay calificaciones
- Voladura en bancos y cráteresDocumento5 páginasVoladura en bancos y cráteresalexAún no hay calificaciones
- Informe Final ANDRES BELLO UNFVDocumento39 páginasInforme Final ANDRES BELLO UNFVJorge Omar EspinozaAún no hay calificaciones
- Demanda de Nulidad y Restablecimiento Del DerechoDocumento18 páginasDemanda de Nulidad y Restablecimiento Del DerechokarevitzAún no hay calificaciones
- DESPERTARDocumento19 páginasDESPERTARHenry holguin riveraAún no hay calificaciones
- Bio Kine SisDocumento12 páginasBio Kine Siseriro10Aún no hay calificaciones
- Calificacion Profesores INTAP 2024Documento3 páginasCalificacion Profesores INTAP 2024RossmeryUscataAún no hay calificaciones
- Apuntes de Genética Aplicada.Documento371 páginasApuntes de Genética Aplicada.luis alejandroAún no hay calificaciones
- Práctica 1 BiologíaDocumento4 páginasPráctica 1 BiologíaEdu MolinaAún no hay calificaciones
- Info Fracaso EscolarDocumento10 páginasInfo Fracaso EscolarJesús UrrutiaAún no hay calificaciones
- Practica de CorazonDocumento21 páginasPractica de Corazonmalejasuescun0324Aún no hay calificaciones
- 2014 Eficacia Del Tratamiento Conservador en La Hernia Discal Lumbar Mecanica en Comparacion Con El Tratamiento QuirurgicoDocumento39 páginas2014 Eficacia Del Tratamiento Conservador en La Hernia Discal Lumbar Mecanica en Comparacion Con El Tratamiento QuirurgicoDonal Damián Contreras RojasAún no hay calificaciones
- Estructura de Los Ácidos Nucleicos y Las ProteínasDocumento3 páginasEstructura de Los Ácidos Nucleicos y Las ProteínasJADER GEOVANY GIL RAMIREZAún no hay calificaciones
- Los Estímulos y Receptores SensorialesDocumento1 páginaLos Estímulos y Receptores SensorialesDixi PixiAún no hay calificaciones
- CizañaDocumento21 páginasCizañaANDREA MIRANDAAún no hay calificaciones
- 15-Guía Contracción Isometrica y DinamometrosDocumento4 páginas15-Guía Contracción Isometrica y DinamometrosCatalina WallisAún no hay calificaciones
- Desarrollo de Un Prototipo SimuladorDocumento231 páginasDesarrollo de Un Prototipo SimuladorcesamavAún no hay calificaciones
- Rutas Metabolicas en DiabetesDocumento28 páginasRutas Metabolicas en Diabetesdavid sanchez0% (1)
- ONAM Complementariopdf - En.esDocumento24 páginasONAM Complementariopdf - En.esEvelyn GomezAún no hay calificaciones
- Examen de Ranking Lenguaje y Razonamiento VerbalDocumento7 páginasExamen de Ranking Lenguaje y Razonamiento VerbalRafael Eduardo100% (1)
- Horizontes - 4 Premio Ibo Experiencia en UruguayDocumento64 páginasHorizontes - 4 Premio Ibo Experiencia en UruguayJose Carlos Risco MendozaAún no hay calificaciones
- RRB-Teorias Ps Dsallo Humano - 21-9-2020Documento27 páginasRRB-Teorias Ps Dsallo Humano - 21-9-2020Román Rodríguez BenjumeaAún no hay calificaciones
- Charles DarwinDocumento22 páginasCharles DarwinJessica CarvajalAún no hay calificaciones