Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Imiquimod
Cargado por
Nekro Gore666Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Imiquimod
Cargado por
Nekro Gore666Copyright:
Formatos disponibles
INSALUD
Hoja de Evaluación de
Medicamentos de
Castilla la Mancha
Nº 3 Año 2.000
IMIQUIMOD
Martínez Escudero J A (Farmacéutico de Atención Primaria), Baeza Berruti JE (Dir .Médico Atención Primaria).
Las verrugas anogenitales son transmitidas sexualmente, con un elevado promedio de transmisión y
significativa morbilidad psicosocial. El agente causal es el papiloma virus humano (HPV) que infecta las células
epiteliales. La forma más común de presentarse es el condiloma acuminado que en pacientes inmunocomprometidos
puede presentarse particularmente extendido y persistente. Se estima que la incidencia de verrugas anogenitales es de
unos 20 millones de casos a nivel mundial por año. No existe tratamiento antiviral y ninguno de los métodos de
tratamiento local son satisfactorios. El tratamiento con podofilotoxina, que posee actividad antimicótica, presenta una
alta recurrencia. La eliminación química o quirúrgica es preferible en condilomas extendidos. El empleo de interferón
α, β ó γ puede ser útil en el tratamiento de verrugas anogenitales persistentes. Imiquimod es un fármaco, aprobado
desde el mes de septiembre de 1998 por la Agencia Europea del Medicamento y comercializado recientemente en
España, que presenta una acción modificadora de la respuesta inmune estimulando los anticuerpos que ayudan a
combatir la infección viral, se presenta en forma de crema y su indicación es el tratamiento de las verrugas provocadas
por alguno de los 30 tipos de papilomavirus humanos con capacidad de infectar el aparato genital humano.
MECANISMO DE ACCION eliminación de las verrugas genitales o perianales visibles
Imiquimod es un inmunomodulador, o durante un máximo de 16 semanas 4,6. La crema está
modificador de la respuesta inmune, careciendo de contenida en un sobre de un solo uso y es capaz de cubrir
efectos antivirales o antineoplásicos directos. La una superficie de 20 cm2.
principal acción farmacológica es la promoción de las
respuestas inmunes innatas y adaptativas, mediante la EFICACIA CLINICA
estimulación de monocitos y macrófagos, para producir La eficacia terapéutica demostrada en el proceso
la liberación de un conjunto de citocinas, tales como el de registro de la especialidad farmacéutica que contiene
interferón alfa (IFN-alfa), factor de necrosis tumoral imiquimod, se deriva de la presentación de 5 ensayos
(TNF) e interleucinas 1, 6 y 8 (IL-1, IL-6, IL-8), también clínicos controlados randomizados, doble ciego,
parece inducir la liberación de interferón gamma e paralelos con el control, uno de fase II y cuatro de fase
interleucina 12, todo lo anterior conduce al aumento de la III, que incluían 1.031 pacientes, 421 tratados con
respuesta inmune mediada por células tipo Th-1, similar imiquimod crema al 5%, 192 con crema al 1% y 418 con
a la hipersensibilidad de tipo retardado; desde el punto de la crema sin principio activo 4,7,8.
vista celular induce la proliferación y diferenciación de En los citados ensayos clínicos con una
linfocitos B 1-6. duración de 16 semanas, con aplicaciones tópicas diarias,
3 días por semana, es capaz de eliminar por completo las
FARMACOCINETICA verrugas en el 50% de los pacientes (11% con placebo),
Por vía tópica menos del 0,9% de una dosis siendo más eficaz en mujeres (60-70%) que en varones
única llega a circulación sistémica. Después de una o (40-45%). La eliminación parcial de las verrugas
varias dosis no se detectaron concentraciones plasmáticas (descenso superior a un 50% del área afectada) se
cuantificables (>5ng/ml). La cantidad absorbida se consigue en el 90% de las mujeres (frente a 45% el
excreta rápidamente por la orina y heces en proporción placebo) 4,5,7. El porcentaje de recidivas a largo plazo (12
3:1 4,6. meses) está entre el 13-19%, mientras que en pacientes
tratados con pofilotoxina es superior al 35% 4,8.
INDICACIONES
Imiquimod está indicado en el tratamiento, por EFECTOS ADVERSOS
vía tópica, de verrugas genitales y perianales externas Generalmente son moderados y transitorios,
(condiloma acuminado) en pacientes adultos. La afectando a la zona de aplicación del fármaco. Suelen
utilización será de 1 aplicación, tres veces por semana, remitir a las 2-3 semanas de suspender el tratamiento.
antes de dormir, debiendo permanecer en la piel durante Consisten esencialmente en reacciones locales de tipo
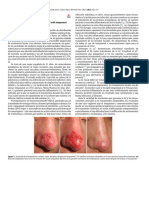
6 a 10 horas. El tratamiento debe prolongarse hasta la irritativo: En los ensayos realizados hasta el 79% de los
CONCLUSIONES
1.- Imiquimod parece ser un fármaco relativamente eficaz y
pacientes presentaron algún tipo de reacción, en mujeres: seguro en el tratamiento del condiloma acuminado, con un
prurito (32%), quemazón (26%), dolor (8%), y en nuevo enfoque terapéutico basado en la modificación de la
varones: prurito (22%), quemazón (12%), dolor (2%), respuesta inmune.
además en menor proporción en ambos, eritema, 2.- Es importante el menor porcentaje de recidivas
observados con el tratamiento con imiquimod y los
excoriación, descamación, edema., induración. Las
porcentajes de eliminación completa de las áreas afectadas
reacciones sistémicas fueron similares a placebo (cefalea, que son razonablemente altos frente a otras alternativas no
síntomas gripales, mialgia) 4,6,9,10. muy eficaces y más agresivas. No ha sido evaluado en el
tratamiento de recurrencias.
CONTRAINDICACIONES 3.- La facilidad de aplicación es un hecho importante frente
- Hipersensibilidad al medicamento. al uso de podofilotoxina o tricloroacético que requiere
- No aplicar en zonas irritadas o en heridas abiertas. aplicación especializada cuando el área genital afectada es
- Verrugas en el prepucio. Hay experiencia clínica muy relativamente amplia (más de 4 cm2).
limitada en el tratamiento de verrugas en la zona 4.- La formulación en sobre monodosis, que impide la
prepucial en pacientes no circuncidados. La experiencia posible contaminación del resto del producto no utilizado y la
corresponde a menos de 100 pacientes en los que no se consecuente autoinoculación, es un hecho de importancia
frente a un agente tan marcadamente infeccioso como es el
siguió la higiene diaria del prepucio, hubo 2 casos de
papilomavirus humano.
fimosis grave y otro de estenosis grave que provocó la
5.- La ausencia de estudios comparativos con otras
circuncisión. Los signos precoces de estenosis son alternativas hace que sea difícil evaluar el nivel de aportación
erosión, ulceración, edema, endurecimiento o mayor terapéutica de imiquimod. Probablemente podofilotoxina
dificultad para retraer el prepucio. Uso no recomendado. podría quedar como tratamiento de elección en pacientes
- Verrugas genitales internas (uretrales, intravaginales, capaces de aplicárselo ellos mismos correctamente, en el
rectales o intraanales): falta experiencia clínica por lo que resto y en mujeres, imiquimod puede ser el tratamiento de
no se recomienda su uso. elección.
- No utilizar vendajes oclusivos. 4,6,10.
BIBLIOGRAFIA
PRECAUCIONES 1.- Slade HB. Cytoquine induction and modifyng the immune response to
- No aplicar sobre zonas irritadas o heridas abiertas. human papilloma virus with imiquimod. Eur J Dermatol 1998; 8(7 suppl):13-6.
2.- Miller RL, Gerster JF, Owens ML, Slade HB, Tomai MA. Imiquimod
- Lavar las manos antes y después de la aplicación. applied topically: a novel immune response modifier and new class of drug. Int
- En caso de reacción cutánea intolerable, eliminar la J Immunopharmacol 1999; 21(1):1-14.
crema con agua y jabón, pudiendo reanudarse el 3.- Arany I, Tyring SK, Stanley MA, Tomai MA, Miller RL, Smith MH,
McDermott DJ, Slade HB. Enhacement of the innate cellular immune response
tratamiento cuando haya remitido la reacción. in patients with genital warts treated with topical imiquimod cream 5%.
- No se recomienda utilizar la crema hasta que la piel Antiviral Res 1999; 43(1):55-63.
genital o perianal se haya recuperado de cualquier 4.- EMEA. Committee for propietary medicinal products European Public
Assesment report (EPAR). Aldara,(imiquimod) 18 septiembre 1998.
tratamiento quirúrgico o con fármacos. 5.-Anónimo. Nuevos medicamentos comercializados en España: Imiquimod.
- Este medicamento puede alterar los preservativos y Panoraama Aactual Med 1999; 23 (224):391-393.
el diafragma, por lo que no se aconseja la utilización 6.- BOT, base de datos de Medicamentos 1999. Consejo General de Colegios
Oficiales de Medicamentos.
7.- Perry CM, Lamb HM. Topical imiquimod: a review of its use in genital
warts. Drugs 1999; 58 (2): 375-90.
ESPECIALIDADES CON IMIQUIMOD 8.- Edwards L. Imiquimod in clinical practice. Australas J Dermatol 1998; 39
(suppl 1): S14-6.
Nombre Presentación Precio (pts)
9.- Gilson RJ, Shupack JL, Friedman-Kein AE, Conant MA, Weber JN,
ALDARA 5% CREMA, 12 SOBRES 12,5 MG 15.209,-
Nayagam AT, Swann RV, Pietig DC, Smith MH, Owens ML. A randomized,
(91,41 euros)
controlled, safety study using imiquimod for the topical treatment of anogenital
PRINCIPIO ACTIVO DOSIS Recomendada COSTE/TTO warts in HIV-infected patients. Imiquimod Study Group. AIDS 1999; 13 (17):
IMIQUIMOD* 12,5 mg/3 veces semana 60.836; - (365 2397-04.
euros) 10.- Product Monograph. Aldara (imiquimod) cream, 5%. 5/1997. 3M
Pharmaceuticals.
Comité de Redacción: Arroyo Pineda, Virginia; González Gero, Yolanda; Heredia Checa, Consuelo; Izquierdo María,
Roberto; Lloret Callejo, Mª Angeles; Martínez Escudero, Juan Antonio; Montero Fernández, Mª José; Muñiz Gavilán,
Angela; Morales Ventura López, Purificación.
Edita, INSALUD, Dirección Territorial de Castilla la Mancha: Gerencias de Atención Primaria de Albacete,
Alcazar de San Juan, Ciudad Real, Cuenca, Guadalajara, Puertollano, Talavera y Toledo
Buzón de Correo: Montero Fernández, Mª José: c/Barcelona, 2- 45005 Toledo. Teléfono: 925-25.99.11, Fax: 925-
21.54.50. e-mail: mmontero@gapto08.insalud.es
También podría gustarte
- Manejo fitosanitario del cultivo del plátano (Medidas para la temporada invernal)De EverandManejo fitosanitario del cultivo del plátano (Medidas para la temporada invernal)Aún no hay calificaciones
- ANTIMICÓTICOSDocumento9 páginasANTIMICÓTICOSJuliette Melendez López100% (1)
- Vacuna contra el Virus del Papiloma Humano: La única vacuna cuestionada incluso por gran parte de la comunidad médicaDe EverandVacuna contra el Virus del Papiloma Humano: La única vacuna cuestionada incluso por gran parte de la comunidad médicaAún no hay calificaciones
- Antimicóticos OralesDocumento32 páginasAntimicóticos OralesOmar de la CruzAún no hay calificaciones
- En defensa propia: Aventuras y desventuras del sistema inmunológicoDe EverandEn defensa propia: Aventuras y desventuras del sistema inmunológicoCalificación: 5 de 5 estrellas5/5 (1)
- Monografico de Hospitalaria 1Documento37 páginasMonografico de Hospitalaria 1Kehi MeybiAún no hay calificaciones
- Inmunoglobulina Humana: Tratamiento en inmunodeficiencias, autoinmunidad, inflamación y COVID-19De EverandInmunoglobulina Humana: Tratamiento en inmunodeficiencias, autoinmunidad, inflamación y COVID-19Aún no hay calificaciones
- AntimicóticosDocumento56 páginasAntimicóticosFrida victoria Ledesma lopezAún no hay calificaciones
- INMUNOMODULADORESDocumento5 páginasINMUNOMODULADORESVicky SanAún no hay calificaciones
- Tratamiento Condiloma AcimunadoDocumento2 páginasTratamiento Condiloma Acimunadoeddu_9975Aún no hay calificaciones
- Mupirocina PDFDocumento4 páginasMupirocina PDFbeix91Aún no hay calificaciones
- PE Spectroderm UnguentoDocumento6 páginasPE Spectroderm UnguentoAngel CanalesAún no hay calificaciones
- Antifungico, Hoy AyerDocumento12 páginasAntifungico, Hoy AyermedicinahumaAún no hay calificaciones
- Medicamentos Dermatologicos Topicos PDFDocumento55 páginasMedicamentos Dermatologicos Topicos PDFMelodyElizabethCordovaGarciaAún no hay calificaciones
- Anti Mico TicosDocumento10 páginasAnti Mico Ticosdelfi hanccoAún no hay calificaciones
- Trabajo FarmacologíaDocumento21 páginasTrabajo FarmacologíaJesus RivasAún no hay calificaciones
- Articulo FTD y OnicomicosisDocumento11 páginasArticulo FTD y Onicomicosisdr.rogelioayalaAún no hay calificaciones
- ANTIMICOTICOSDocumento25 páginasANTIMICOTICOSEUDES JUAN ROJAS LAURAAún no hay calificaciones
- BifonazolDocumento6 páginasBifonazolDANIELAAún no hay calificaciones
- Modulo 1 Actualización en Infecciones ViralesDocumento35 páginasModulo 1 Actualización en Infecciones ViralesGaldamez HernándezAún no hay calificaciones
- Guia Antibi Ticos 2009Documento6 páginasGuia Antibi Ticos 2009keithgaymerAún no hay calificaciones
- Anti Mico TicosDocumento4 páginasAnti Mico TicosDouglasTenorio100% (2)
- FichaTecnica 62221.html PDFDocumento5 páginasFichaTecnica 62221.html PDFJD CayambeAún no hay calificaciones
- Citostaticos ResumenDocumento16 páginasCitostaticos ResumenOiram ChipoAún no hay calificaciones
- Cutaneous Leishmaniasis of The Face Treated With Imiquimod 3.75%Documento2 páginasCutaneous Leishmaniasis of The Face Treated With Imiquimod 3.75%HEBELIN CARMEN CUMPA SALDA�AAún no hay calificaciones
- CLOTRIMAZOL CremaDocumento8 páginasCLOTRIMAZOL CremaCeline Chavez HilarioAún no hay calificaciones
- 89 MupaxDocumento2 páginas89 MupaxAmaliaArroyoAún no hay calificaciones
- Guia de Antimicoticos y AntiviralesDocumento7 páginasGuia de Antimicoticos y AntiviralesJose David CortezAún no hay calificaciones
- Farmacologia HOYDocumento15 páginasFarmacologia HOYAlvaro GamboaAún no hay calificaciones
- 90 Mupax NasalDocumento2 páginas90 Mupax NasaltedejoAún no hay calificaciones
- Tratamiento LesionesDocumento5 páginasTratamiento LesionesErick Barradas HernándezAún no hay calificaciones
- ANTIMICOTICOS DocconfiguradoDocumento2 páginasANTIMICOTICOS DocconfiguradoJulia Canchari GuerreroAún no hay calificaciones
- Anticoticos o Antifungicos InformeDocumento11 páginasAnticoticos o Antifungicos InformeIvan Martinez HuallpaAún no hay calificaciones
- Herpes y CondilomaDocumento8 páginasHerpes y CondilomaJeanette MartínezAún no hay calificaciones
- Verrugas Papulas WilliamsDocumento5 páginasVerrugas Papulas WilliamsJC HernándezAún no hay calificaciones
- MonoclonalDocumento4 páginasMonoclonalLuisa ManriquezAún no hay calificaciones
- ANTIMICOTICODocumento26 páginasANTIMICOTICONorys TimaureAún no hay calificaciones
- Material - Revisión de Antibioticoterapia 2-2Documento5 páginasMaterial - Revisión de Antibioticoterapia 2-2Coordinación Académica UHGAún no hay calificaciones
- ANTIMICÓTICOSDocumento5 páginasANTIMICÓTICOSIsaí PQAún no hay calificaciones
- Tarea 5 Analisis - Ramona BarrosDocumento8 páginasTarea 5 Analisis - Ramona BarrosLizeth HernándezAún no hay calificaciones
- Farmacos AntimicoticosDocumento5 páginasFarmacos AntimicoticosAna CayumilAún no hay calificaciones
- Farmaco ParactamolDocumento7 páginasFarmaco ParactamolpaucarcajaAún no hay calificaciones
- Deber Farmaco Mecanismos de AcciónDocumento13 páginasDeber Farmaco Mecanismos de Acciónyomismo 18Aún no hay calificaciones
- 172 Pioderma Canina Espanol - 1172488dfDocumento7 páginas172 Pioderma Canina Espanol - 1172488dfjorgeAún no hay calificaciones
- 172 Pioderma Canina Espanol - 1172488dfDocumento7 páginas172 Pioderma Canina Espanol - 1172488dfBRANDON STEVEN RONDON CASTILLOAún no hay calificaciones
- Clase 6 FármacoDocumento4 páginasClase 6 FármacoJaviera LilloAún no hay calificaciones
- PO Antibioticos Antivirales TopicosDocumento2 páginasPO Antibioticos Antivirales TopicosPetra Marquez GentoAún no hay calificaciones
- INFAC - Vol - 26 - 7 - Infecciones CutáneasDocumento9 páginasINFAC - Vol - 26 - 7 - Infecciones CutáneasVa Bla VaAún no hay calificaciones
- Medicamentos Dermatologicos TopicosDocumento55 páginasMedicamentos Dermatologicos TopicosYOMIRAANGELA67% (3)
- IPTBDocumento36 páginasIPTBcamilo herreraAún no hay calificaciones
- Efectos Adversos de Los Fármacos-1Documento30 páginasEfectos Adversos de Los Fármacos-1Lucia QuessAún no hay calificaciones
- ANEXO N2 Informe TecnicoDocumento5 páginasANEXO N2 Informe TecnicoNestor Arzubialde Zamalloa100% (1)
- FichaTecnica 58868.htmlDocumento5 páginasFichaTecnica 58868.htmlBárbara Robles GoyanesAún no hay calificaciones
- ToxicodermiasDocumento33 páginasToxicodermiasDavid SilvaAún no hay calificaciones
- Farmacologia IIDocumento22 páginasFarmacologia IIMiguel Valle100% (1)
- Glucopeptidos, LipoglucopeptidosDocumento6 páginasGlucopeptidos, LipoglucopeptidosCátedra de Farmacología de la Escuela de Medicina de La UNIVERSIDAD DEL ZULIAAún no hay calificaciones
- FarmacologiaDocumento8 páginasFarmacologiaDeolinda PortilloAún no hay calificaciones
- DEBER - Molusco ContagiosoDocumento7 páginasDEBER - Molusco ContagiosoMaria Cristina Feijóo JaramilloAún no hay calificaciones
- Ficha FarmacologicaDocumento25 páginasFicha FarmacologicaDilia Romero FernandezAún no hay calificaciones
- ImiquimodDocumento8 páginasImiquimodLuis Alexander MartinezAún no hay calificaciones
- Influencias Ambientales Factores MaternoDocumento6 páginasInfluencias Ambientales Factores MaternoOtto Carballo100% (1)
- Protocolo Anestesia Local Odontologica PDFDocumento3 páginasProtocolo Anestesia Local Odontologica PDFROCIO BELEN OLATE MELOAún no hay calificaciones
- Anorexia Texto ArgumentativoDocumento3 páginasAnorexia Texto Argumentativodoremi fasolasiAún no hay calificaciones
- Ilovepdf MergedDocumento131 páginasIlovepdf MergedSusana ChinchillaAún no hay calificaciones
- 2021 Semana 20sDocumento4 páginas2021 Semana 20sEmily SharpAún no hay calificaciones
- Trombastenia de GlanzmannDocumento5 páginasTrombastenia de GlanzmannDANNA JENDAY MARTINEZ POSADASAún no hay calificaciones
- 77 Generalidades Sobre Cirugía Cardiocirculatoria PDFDocumento46 páginas77 Generalidades Sobre Cirugía Cardiocirculatoria PDFOctavo CicloAún no hay calificaciones
- Neuroblastoma Vs Nef Rob Last OmaDocumento2 páginasNeuroblastoma Vs Nef Rob Last OmaEAlbertiAún no hay calificaciones
- Matriz de RiesgosDocumento12 páginasMatriz de RiesgosCamila LeytonAún no hay calificaciones
- Emo-Mo114!08!19 (Oscar Lee E.I.R.L. - Protocolo Petrotal Contratistas)Documento13 páginasEmo-Mo114!08!19 (Oscar Lee E.I.R.L. - Protocolo Petrotal Contratistas)oscar leeAún no hay calificaciones
- Caso Clinico de MeningitisDocumento2 páginasCaso Clinico de MeningitisMARCELINA HUAYTA CUMBAAún no hay calificaciones
- Patología Testicular - Juan Ignacio OñateDocumento2 páginasPatología Testicular - Juan Ignacio OñateJuan Ignacio Oñate RiedererAún no hay calificaciones
- Fibrodisplasia Osificante Progresiva AvancesDocumento1 páginaFibrodisplasia Osificante Progresiva AvancesFrank RitikonAún no hay calificaciones
- Resumen de La Historia Clínica OdontológicaDocumento4 páginasResumen de La Historia Clínica OdontológicaMaría Mercedes Cevallos VenturaAún no hay calificaciones
- CLASIFICACIÓNDocumento10 páginasCLASIFICACIÓNmarthaquevedoAún no hay calificaciones
- Certificado MedicoDocumento6 páginasCertificado MedicoBETTOAún no hay calificaciones
- Programas Sustantivos 2022 A Cargo de La Jefatura de Valoracion y TratamientoDocumento4 páginasProgramas Sustantivos 2022 A Cargo de La Jefatura de Valoracion y TratamientoWendy MartinezAún no hay calificaciones
- Insuficiencia Cardiaca en NiñosDocumento6 páginasInsuficiencia Cardiaca en NiñosJOSE PATRICIO FUENTES GALLARDOAún no hay calificaciones
- Recomendaciones HistaminaDocumento2 páginasRecomendaciones HistaminamarisolAún no hay calificaciones
- Cuidados Paliativos en El DomicilioDocumento16 páginasCuidados Paliativos en El DomicilioJhon Alexander OrmazaAún no hay calificaciones
- Repaso OftalmoDocumento8 páginasRepaso Oftalmocarolina hyeinAún no hay calificaciones
- Ferrer Protocolo Anestesia Cirugia Urologica Cirugia Laparotomia Prostatectomia Bricker Sartd Chguv1!2!11Documento43 páginasFerrer Protocolo Anestesia Cirugia Urologica Cirugia Laparotomia Prostatectomia Bricker Sartd Chguv1!2!11Salvador Yana RocaAún no hay calificaciones
- Status EpilepticoDocumento118 páginasStatus Epilepticorepre64Aún no hay calificaciones
- Historia Clínica y Semiología.Documento9 páginasHistoria Clínica y Semiología.Claudia Gutiérrez.Aún no hay calificaciones
- PAZ MARYELIS Leucemia Mieloide AgudaDocumento7 páginasPAZ MARYELIS Leucemia Mieloide AgudaMaryelis PazAún no hay calificaciones
- Cuánta Agua Necesitamos BeberDocumento4 páginasCuánta Agua Necesitamos BeberFrancisco Villicaña MaldonadoAún no hay calificaciones
- Infografia Canula Nasal de Alto FlujoDocumento2 páginasInfografia Canula Nasal de Alto FlujoErika Alejandra Diaz PantojaAún no hay calificaciones
- Portafolio de ParasitologiaDocumento66 páginasPortafolio de ParasitologiaBRYAN SAAVEDRAAún no hay calificaciones
- Neumonia Adquirida en La Comunidad FINALDocumento39 páginasNeumonia Adquirida en La Comunidad FINALOscar Augusto Lora Acevedo100% (1)
- Como Disganosticar La DiabetesDocumento2 páginasComo Disganosticar La DiabetesvictoriaAún no hay calificaciones
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- GuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisDe EverandGuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisCalificación: 4 de 5 estrellas4/5 (9)
- Homo antecessor: El nacimiento de una especieDe EverandHomo antecessor: El nacimiento de una especieCalificación: 5 de 5 estrellas5/5 (1)
- Terapia cognitiva: Conceptos básicos y profundizaciónDe EverandTerapia cognitiva: Conceptos básicos y profundizaciónCalificación: 5 de 5 estrellas5/5 (1)
- Neuroanatomía: Fundamentos de neuroanatomía estructural, funcional y clínicaDe EverandNeuroanatomía: Fundamentos de neuroanatomía estructural, funcional y clínicaCalificación: 4 de 5 estrellas4/5 (16)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- El concepto Mulligan de terapia manual (Color)De EverandEl concepto Mulligan de terapia manual (Color)Calificación: 5 de 5 estrellas5/5 (3)
- Cardiología y enfermedades cardiovascularesDe EverandCardiología y enfermedades cardiovascularesCalificación: 5 de 5 estrellas5/5 (1)
- Prescripción de ejercico físico para la saludDe EverandPrescripción de ejercico físico para la saludCalificación: 5 de 5 estrellas5/5 (1)
- Sana tu Cuerpo, Calma tu Mente: Desintoxicar Hígado, Intestino Permeable, Salud Hormonal, Curación Emocional, Relajación, Ansiedad y Sanidad mental, Atención Plena, Psicoterapia y NutriciónDe EverandSana tu Cuerpo, Calma tu Mente: Desintoxicar Hígado, Intestino Permeable, Salud Hormonal, Curación Emocional, Relajación, Ansiedad y Sanidad mental, Atención Plena, Psicoterapia y NutriciónCalificación: 5 de 5 estrellas5/5 (4)
- 50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaDe Everand50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaCalificación: 4 de 5 estrellas4/5 (37)
- Muchas Vidas, Muchos Sabios (Many Lives, Many Masters): (Many Lives, Many Masters)De EverandMuchas Vidas, Muchos Sabios (Many Lives, Many Masters): (Many Lives, Many Masters)Calificación: 4 de 5 estrellas4/5 (475)
- Cambiar el pasado: Superar las experiencias traumáticas con la terapia estratégicaDe EverandCambiar el pasado: Superar las experiencias traumáticas con la terapia estratégicaCalificación: 5 de 5 estrellas5/5 (4)
- Shiatsu: Conozca las técnicas y tratamientos de una de las terapias más antiguasDe EverandShiatsu: Conozca las técnicas y tratamientos de una de las terapias más antiguasAún no hay calificaciones
- Notas de clase. Manual de farmacognosia: Análisis microscópico y fitoquímico, y usos de plantas medicinalesDe EverandNotas de clase. Manual de farmacognosia: Análisis microscópico y fitoquímico, y usos de plantas medicinalesAún no hay calificaciones
- Nuestra mente nos engaña: Sesgos y errores cognitivos que todos cometemosDe EverandNuestra mente nos engaña: Sesgos y errores cognitivos que todos cometemosCalificación: 3.5 de 5 estrellas3.5/5 (6)
- Neuropsicología: Los fundamentos de la materiaDe EverandNeuropsicología: Los fundamentos de la materiaCalificación: 5 de 5 estrellas5/5 (1)
- La Dieta Mediterránea Para Principiantes, Guía Paso A Paso Con Recetas Para Comer Mejor Y Bajar De PesoDe EverandLa Dieta Mediterránea Para Principiantes, Guía Paso A Paso Con Recetas Para Comer Mejor Y Bajar De PesoCalificación: 5 de 5 estrellas5/5 (2)
- Fisiopatología de las enfermedades cardiovascularesDe EverandFisiopatología de las enfermedades cardiovascularesCalificación: 5 de 5 estrellas5/5 (1)
- TDAH en Adultos. Cómo Reconocer y Tratar a un Adulto con TDAH en 30 Fáciles PasosDe EverandTDAH en Adultos. Cómo Reconocer y Tratar a un Adulto con TDAH en 30 Fáciles PasosCalificación: 4 de 5 estrellas4/5 (8)
- El cerebro del niño explicado a los padresDe EverandEl cerebro del niño explicado a los padresCalificación: 4.5 de 5 estrellas4.5/5 (147)
- Sistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)De EverandSistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)Calificación: 5 de 5 estrellas5/5 (9)
- El libro conciso de la punción seca: Manual del terapeuta para las aplicaciones en los puntos gatillo miofasciales (Color)De EverandEl libro conciso de la punción seca: Manual del terapeuta para las aplicaciones en los puntos gatillo miofasciales (Color)Calificación: 3 de 5 estrellas3/5 (2)
- Altas Dosis: Los efectos milagrosos de dosis extremadamente altas de vitamina D3. El gran secreto que la industria farmacéutica quiere ocultarle.De EverandAltas Dosis: Los efectos milagrosos de dosis extremadamente altas de vitamina D3. El gran secreto que la industria farmacéutica quiere ocultarle.Calificación: 5 de 5 estrellas5/5 (4)