Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Tema 1.1 - Química - Mapa Conceptual
Cargado por
Angelica Olivares0 calificaciones0% encontró este documento útil (0 votos)
20 vistas1 páginaEl documento describe los estados de la materia (sólido, líquido y gas), los métodos científicos y las propiedades fundamentales de la materia. Explica que un sólido tiene partículas muy juntas, un líquido tiene partículas un poco separadas y un gas tiene partículas muy separadas. También resume los principales métodos para separar mezclas como filtración, evaporación y destilación.
Descripción original:
Título original
Tema 1.1_Química_mapa conceptual
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEl documento describe los estados de la materia (sólido, líquido y gas), los métodos científicos y las propiedades fundamentales de la materia. Explica que un sólido tiene partículas muy juntas, un líquido tiene partículas un poco separadas y un gas tiene partículas muy separadas. También resume los principales métodos para separar mezclas como filtración, evaporación y destilación.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
20 vistas1 páginaTema 1.1 - Química - Mapa Conceptual
Cargado por
Angelica OlivaresEl documento describe los estados de la materia (sólido, líquido y gas), los métodos científicos y las propiedades fundamentales de la materia. Explica que un sólido tiene partículas muy juntas, un líquido tiene partículas un poco separadas y un gas tiene partículas muy separadas. También resume los principales métodos para separar mezclas como filtración, evaporación y destilación.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
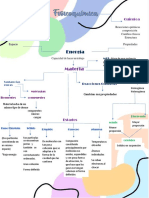
Propiedades
Cambios de estado Método científico fundamentales: masa,
Sólido: partículas muy juntas,
densidades altas, fuerzas de cohesión
energía, tiempo y espacio.
elevadas, volumen y forma definida. Subdivisiones Generales o
Líquido: partículas un poco Química orgánica extensivas: dependen de
separadas, densidades medias, Química inorgánica
Química analítica
la cantidad de masa pero no permiten
fuerzas de cohesión intermedias,
Fisicoquímica distinguir una sustancia de otra (peso,
volumen constante y forma variable.
GAS: partículas muy separadas,
Bioquímica inercia, volumen, impenetrabilidad…)
densidades bajas, fuerzas de Específicas o
cohesión nulas, volumen y forma Ciencias con las intensivas: permiten
variable. que se relaciona
distinguir las sustancias y no dependen
Matemáticas
Física de la cantidad de masa (densidad,
Estados de agregación Biología
punto de fusión y ebullición…)
Estadística
Medicina Se dividen en físicas y químicas
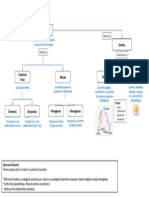
Cambio físico vs cambio químico
QUÍMICA Ecología
Sustancias puras y mezclas
proviene de la voz árabe "kimiya" (piedra filosofal") , que a su vez proviene de "kimi" (negro),
Se genera una nueva sustancia término con que se nombraba a Egipto por ser la civilización que más avances realizó en
Es generalmente irreversible técnicas químicas).
Elementos y
Cambios internos, propiedades y composición de la materia, Homogéneas y
Compuestos
Métodos de separación de mezclas: así como leyes que rigen dichos cambios. heterogéneas
Filtración Tamizado Imantación o Evaporación – Centrifugación Decantación Destilación Cromatografía
magnetismo Cristalización 1.-Sólido insoluble –
Sólido insoluble – Sólido - Sólido Sólido insoluble y Líquido Líquidos Líquidos o
Líquido Diferentes tamaños Sólido - Sólido Sólido soluble – de tamaño muy Se sedimenta y escurre miscibles gases
Uso de mallas características Líquido
Medio filtrante Líquido pequeño – Puntos de Solvente
magnéticas
Calentamiento Fuerza ebullición selectivo, fase
Uso de un imán
para evaporar el centrífuga para distintos fija y fase
líquido sedimentar al móvil
sólido
2.- Líquidos
inmiscibles
Distintas densidades
observando más de una Elaboró:Gabriela García Márquez
Profesora:
fase Profesora: Gabriela García Márquez
También podría gustarte
- QuimicaaaaDocumento8 páginasQuimicaaaaJohn Olivera DolmosAún no hay calificaciones
- Añade Aquí Una Idea IncreíbleDocumento1 páginaAñade Aquí Una Idea IncreíbleSharon CubaAún no hay calificaciones
- Diapositiva 1. Introducción A La QuimicaDocumento26 páginasDiapositiva 1. Introducción A La QuimicaMăřčêłô LľůłłůnăAún no hay calificaciones
- MATERIA, ENERGIA y PROPIEDADES - NI ADocumento12 páginasMATERIA, ENERGIA y PROPIEDADES - NI AJulian DiazAún no hay calificaciones
- FisicoquimicaDocumento3 páginasFisicoquimicaChristian MartinezAún no hay calificaciones
- 5° QuimicaDocumento91 páginas5° QuimicaMaximoovAún no hay calificaciones
- Actividad 1. Mapa Conceptual Equipo 10Documento3 páginasActividad 1. Mapa Conceptual Equipo 10Alejandra Ibarra herregonAún no hay calificaciones
- Quimica Sesión 1Documento35 páginasQuimica Sesión 1Roberto GarciaAún no hay calificaciones
- Sesión #01: Química - Materia: PRE-Facultad de Medicina / Escuela de Medicina HumanaDocumento26 páginasSesión #01: Química - Materia: PRE-Facultad de Medicina / Escuela de Medicina HumanaLucia GomezAún no hay calificaciones
- SESION 1-Introduccion QuimicaDocumento20 páginasSESION 1-Introduccion QuimicaGabriel Armando Orellana NolascoAún no hay calificaciones
- Informe #1Documento13 páginasInforme #1Adrian ConcepcionAún no hay calificaciones
- 1 MateriaDocumento1 página1 MateriaLuis WeyAún no hay calificaciones
- La MateriaDocumento1 páginaLa MateriaAlex JuárezAún no hay calificaciones
- Antologia de QuimicaDocumento27 páginasAntologia de QuimicaIku Serinuma100% (1)
- Resumen Tema1Documento7 páginasResumen Tema1Claudia Alvarez GonzalezAún no hay calificaciones
- Materia Energía y CambiosDocumento5 páginasMateria Energía y CambiosJairo CAún no hay calificaciones
- La MateriaDocumento1 páginaLa Materiaraquel juarezAún no hay calificaciones
- A#1 AcgDocumento1 páginaA#1 AcgAdalberto CGAún no hay calificaciones
- UNIDAD 1-Estequiometria-Parte 1Documento31 páginasUNIDAD 1-Estequiometria-Parte 1antoparranio98Aún no hay calificaciones
- Sistemas MaterialesDocumento8 páginasSistemas Materiales•Nomi•Aún no hay calificaciones
- SESIÓN01PREUSATDocumento44 páginasSESIÓN01PREUSATHumberto Zapata AhumadaAún no hay calificaciones
- Trabajo de BiologiaDocumento11 páginasTrabajo de BiologiaAcosta Sandoval, Camila Michelle.Aún no hay calificaciones
- Analitica Mapa #2Documento2 páginasAnalitica Mapa #2Abigail Aveiga TorresAún no hay calificaciones
- Resumen Quimica1Documento2 páginasResumen Quimica1Terry BleAún no hay calificaciones
- La Materia y Su ComposiciónDocumento16 páginasLa Materia y Su ComposiciónFiorella HorqqueAún no hay calificaciones
- Objetivos de La ClaseDocumento3 páginasObjetivos de La Clasequilliestefania359Aún no hay calificaciones
- 01 QuimicaDocumento4 páginas01 QuimicaRoyer Aurelio Laura AtencioAún no hay calificaciones
- El AtomoDocumento97 páginasEl AtomohoalAún no hay calificaciones
- Unidad 1Documento20 páginasUnidad 1Jhordin Dario León AlvaradoAún no hay calificaciones
- Cta Mapa ConceptualDocumento7 páginasCta Mapa Conceptualfabian rondoyAún no hay calificaciones
- Mapa Conceptual - QuímicaDocumento1 páginaMapa Conceptual - QuímicaRelc AlightAún no hay calificaciones
- Química GeneralDocumento28 páginasQuímica GeneralNadine CeredinAún no hay calificaciones
- Trabajos de RecuperaciónDocumento8 páginasTrabajos de RecuperaciónmonseeAún no hay calificaciones
- Lectura Interactiva 1 Química Propiedades y TranformacionesDocumento10 páginasLectura Interactiva 1 Química Propiedades y TranformacionesSofia MaguirreAún no hay calificaciones
- Bienvenido A La Quimica (68 D)Documento68 páginasBienvenido A La Quimica (68 D)Moises David Valladares AlvaradoAún no hay calificaciones
- QUIMICADocumento128 páginasQUIMICAErik Michael Laura FloresAún no hay calificaciones
- #1 La Materia, Unidades y Medidas Química FundamentalDocumento19 páginas#1 La Materia, Unidades y Medidas Química FundamentalDaniela YustyAún no hay calificaciones
- Quimica I Periodo ISPADocumento1 páginaQuimica I Periodo ISPAmateo gordilloAún no hay calificaciones
- M1 00 MAPA Qímica MateriaDocumento1 páginaM1 00 MAPA Qímica MateriaJorge A. Gutiérrez P.Aún no hay calificaciones
- Organizador Grafico N°3Documento1 páginaOrganizador Grafico N°3MOISES AARONAún no hay calificaciones
- A1 AdzDocumento3 páginasA1 AdzBerna TepatziAún no hay calificaciones
- Introduccion A La Quimica TeoriaDocumento7 páginasIntroduccion A La Quimica TeoriaHugo BingoAún no hay calificaciones
- A1 CMRCDocumento7 páginasA1 CMRCmariamAún no hay calificaciones
- UNIDAD 1 Sistema de Materiales NSZDocumento22 páginasUNIDAD 1 Sistema de Materiales NSZnataliazadorozneAún no hay calificaciones
- Tema3sustanciaspurasmezclasydisoluciones 150409065958 Conversion Gate01Documento16 páginasTema3sustanciaspurasmezclasydisoluciones 150409065958 Conversion Gate01Lucía RocaAún no hay calificaciones
- Propiedades de La Materia PPTDocumento39 páginasPropiedades de La Materia PPTtkk ppioupAún no hay calificaciones
- El Estudio Del Cambio.Documento18 páginasEl Estudio Del Cambio.Caleb HernándezAún no hay calificaciones
- Introducción A La Química - Unidad IDocumento18 páginasIntroducción A La Química - Unidad ILukian LukianAún no hay calificaciones
- IOQ. Bloque II. Interrelación de Materia y EnergíaDocumento40 páginasIOQ. Bloque II. Interrelación de Materia y EnergíaEdna Alejandra Matus CundapiAún no hay calificaciones
- Introducción A La Química: Unidad 1Documento26 páginasIntroducción A La Química: Unidad 1CarolinaAún no hay calificaciones
- Unidad 1Documento26 páginasUnidad 1CarolinaAún no hay calificaciones
- Unidad 1 Fundamentos Leyes Nomenclatura Estequiometria PDFDocumento30 páginasUnidad 1 Fundamentos Leyes Nomenclatura Estequiometria PDFLeandro AlvarezAún no hay calificaciones
- Cuadernillo - Física Ii - 2023 - NDocumento56 páginasCuadernillo - Física Ii - 2023 - NRodríguez Galván AlbertoAún no hay calificaciones
- 2023-4-13 - Colegio Universitario Central - TAP 2 - TAM. UNIDAD I. QCADocumento22 páginas2023-4-13 - Colegio Universitario Central - TAP 2 - TAM. UNIDAD I. QCAsilvina dominguezAún no hay calificaciones
- Tema - 01 - Introduccion y Sistemas MaterialesDocumento42 páginasTema - 01 - Introduccion y Sistemas MaterialesMaria RegeneaAún no hay calificaciones
- Programación de AulaDocumento8 páginasProgramación de AulaFede PerezAún no hay calificaciones
- Materia y Modelos AtómicosDocumento12 páginasMateria y Modelos AtómicosWilmar SalcedoAún no hay calificaciones
- Estequiometria 3Documento61 páginasEstequiometria 3JOSELINEAún no hay calificaciones
- Fundamentos de procesos químicosDe EverandFundamentos de procesos químicosCalificación: 5 de 5 estrellas5/5 (3)
- Previo EquipoDocumento9 páginasPrevio EquipoIvonne MojicaAún no hay calificaciones
- Peugeot p2562Documento4 páginasPeugeot p2562Salva Garcia BasAún no hay calificaciones
- Alumbrado PublicoDocumento34 páginasAlumbrado Publicoreivin27Aún no hay calificaciones
- Lab 6. Gases y PropiedadesDocumento2 páginasLab 6. Gases y PropiedadesJOSE DAVID VALENCIA ESPINOSA100% (1)
- Informe de Lab.1 - Extraccion de Adn (2020)Documento4 páginasInforme de Lab.1 - Extraccion de Adn (2020)Ivan HerreraAún no hay calificaciones
- Haluros 2019Documento82 páginasHaluros 2019LAURA MELISSA ESPAÑA CAICEDOAún no hay calificaciones
- De Los Procesos Químicos para La Despolimerización de PETDocumento10 páginasDe Los Procesos Químicos para La Despolimerización de PETAlex Condori100% (1)
- TermocuplasDocumento28 páginasTermocuplasLuis Fernando Armas AlmeidaAún no hay calificaciones
- Test Cantidad de Materia y NomenclaturaDocumento2 páginasTest Cantidad de Materia y NomenclaturadashrafAún no hay calificaciones
- Cuestionario de PolimerosDocumento6 páginasCuestionario de PolimerosErick Reyes PanduroAún no hay calificaciones
- Resolución 2674 de 2013 - DefinicionesDocumento7 páginasResolución 2674 de 2013 - Definicionesqclarena0% (1)
- Obtencion de EtenoDocumento6 páginasObtencion de EtenoLuis Zamora0% (1)
- Pisos, Falso Piso, ContrapisoDocumento15 páginasPisos, Falso Piso, ContrapisoJohnnyCarbajalGuzman50% (2)
- Quimica de Las Plantas Medicinales PDFDocumento43 páginasQuimica de Las Plantas Medicinales PDFAlexis Rosell100% (3)
- Guia de Practicas de Laboratorio - Bioquimica 2023-2Documento6 páginasGuia de Practicas de Laboratorio - Bioquimica 2023-2Geancarlos Rivas NavarroAún no hay calificaciones
- Ocon Tojo - Absorcion de Gases WordDocumento22 páginasOcon Tojo - Absorcion de Gases WordKenyi Solano PortalesAún no hay calificaciones
- Plan Fertlizacion Cebolla, G5Documento10 páginasPlan Fertlizacion Cebolla, G5Nataly PozuelosAún no hay calificaciones
- Evaluacion T1 IC1 1952 2022-2Documento3 páginasEvaluacion T1 IC1 1952 2022-2johanAún no hay calificaciones
- Od. Andrea CarateDocumento10 páginasOd. Andrea Carateandrea carateAún no hay calificaciones
- B1º-Pract-Act2 Cyt U2Documento2 páginasB1º-Pract-Act2 Cyt U2jeefryAún no hay calificaciones
- Resumen Tfiqm45Documento3 páginasResumen Tfiqm45ONCEAún no hay calificaciones
- Introducción A Las Baterías de LitioDocumento27 páginasIntroducción A Las Baterías de LitioSORAYA MARTINEZ MAYGUAAún no hay calificaciones
- Calculos Diluciones DesinfectantesDocumento2 páginasCalculos Diluciones DesinfectantesAndrés YépezAún no hay calificaciones
- Ácidos y BasesDocumento12 páginasÁcidos y BasesCarlos Alfonso Jara Benites100% (2)
- Conceptos BasicosDocumento2 páginasConceptos BasicosJaazmiin ToorreesAún no hay calificaciones
- Determinación de Calcio y Magnesio en Un Agua Natural Mediante Espectroscopía de Absorción AtómicaDocumento6 páginasDeterminación de Calcio y Magnesio en Un Agua Natural Mediante Espectroscopía de Absorción AtómicaMaximilianoRGAún no hay calificaciones
- Avances Recientes de Nanomateriales de Magnetita para Eliminar El Arsénico Del Agua - PMC - En.esDocumento15 páginasAvances Recientes de Nanomateriales de Magnetita para Eliminar El Arsénico Del Agua - PMC - En.esIsis MonteroAún no hay calificaciones
- Balances de Materia en Torres de DestilacionDocumento4 páginasBalances de Materia en Torres de Destilacionanon_682990377Aún no hay calificaciones
- Actividad 1 Refractarios EstructuralesDocumento21 páginasActividad 1 Refractarios EstructuralesFernando Sanchez VillalobosAún no hay calificaciones
- Instrumentos Internacionales Signados Por México en Materia de Narcotráfico PDFDocumento79 páginasInstrumentos Internacionales Signados Por México en Materia de Narcotráfico PDFMarco Antonio Nataren RamosAún no hay calificaciones