Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Capitulo IV Nutricion. Enzimas
Cargado por
KARINA ANDREA CASTILLO CALLE0 calificaciones0% encontró este documento útil (0 votos)
11 vistas28 páginasTítulo original
Capitulo IV Nutricion. Enzimas.pptx
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
11 vistas28 páginasCapitulo IV Nutricion. Enzimas
Cargado por
KARINA ANDREA CASTILLO CALLECopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 28
Nutrición
• Son procesos que realizan los organismos
vivos con la finalidad de incorporar
sustancias que son necesarias para vivir.
• Sustancias que le permite crecer, renovación
de células o los tejidos gastados y obtener
energía útil que le sirve, para cumplir con sus
funciones vitales.
• La finalidad de la nutrición es mantenerse
vivos y la conservación de los seres vivos
Procesos de la Nutrición.-
Comprende las siguientes fase:
• Digestión
• Circulación
• Respiración
• Excreción
• Digestión. Se inicia con la ingestión de los
alimentos, su transformación y absorción de
sustancias útiles atraves de la sangre (nutrientes)
y la liberación de sustancias tóxicas. Metabolismo
• Circulación.- consiste en el transporta de los
nutrientes a las células. De preferencia en la
sangre van los nutrientes, incluye O2 y el CO2.
• Respiración.-aporta el oxígeno para la liberación
de la energía que el organismo necesita para vivir
• Excreción.-Elimina las sustancias desechables,
principalmente a través de los organos excretores
Clases de Nutrición:
• NUTRICION AUTOTROFA.-
La realizan los organismos vivos que son capaces
de sintetizar sus propios alimentos y que no
dependen de otro organismo vivo para vivir.
Entre ellos se encuentran las plantas y los
organismos más simples que solamente necesitan
agua, CO2, sales inorgánicas y una fuente de
energía para sintetizar sus alimentos.
MODALIDADES.- a) Quimio sintéticos y b)
Fotosintéticos
FOTOSINTETICOS, son organismos vivos que para
sintetizar sus alimentos utilizan una fuente de luz,
principalmente la luz solar, como fuente de energía.
Mediante la fotosíntesis., se transforma la energía
luminosa en energía química y moléculas de ATP.
QUIMIOSINTéTICOS , son organismos vivos que para
sintetizar sus alimentos utilizan como fuente de energía
reacciones de sustancias inorgánicas. Por ejemplo
bacterias: Nitrobacter, Sulfobacterium y Ferrobacterium.
Nutrición Heterótrofa.-
• La realizan los organismos vivos del reino animal, los
hongos y algunas bacterias, que no tienen la capacidad
de sintetizar sus propios alimentos y necesitan de
materia orgánica para alimentarse. Estos organismos
siempre dependen de otros organismos para vivir.
- Los heterotrofos tienen que vivir a expensa de
organismos autótrofos o de materia orgánica viva o en
descomposición.
- los organismos heterótrofos son consumidores de los
alimentos que elaboran los productores.
Modalidades :
• a)Holozoica.- la realizan los organismos vivos que
comen, ingieren alimentos solidos, los transforman
o digieren y lo asimilan y parten lo excretan. Es
propia de todos los animales herbívoros, carnívoros
y omnívoros que dependen de un organismo
autótrofo.
• b) Saprofítica.- la realizan los organismos que se
desarrolla en cuerpos de animales y vegetales en
descomposición o productos de deshechos y que
absorben sus alimentos directamente a través de la
membrana celular
• c) Parasítica.- Es propia de algunos animales y
plantas que desarrollan en líquidos y tejidos vivos y
que obtienen sus alimentos por ingestíon de
partículas sólidas o por absorción de moléculas
orgánicas a través de sus paredes celulares
ENZIMAS. Concepto
• Son sustancias de naturaleza proteicas que se forman
en las células vivas.
• Su función es regular la velocidad y especificidad de
una reacción química sin modificar el punto final de la
reacción y sin consumirse durante la misma.
• Las enzimas participan las reacciones de todos los
procesos vitales: respiración, crecimiento,
contracción, conducción nerviosa, digestión,
fotosíntesis, otros etc.
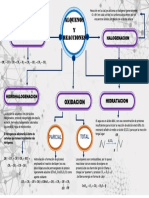
NOMENCLATURA.-
• Algunas enzimas reciben el nombre del sustrato
donde actúan añadiendo a su raíz la terminación
"asa" por ejemplo lactasa, sacarasa lipasa,
deshidrogenasa.
• Otras enzimas reciben nombres como pepsina,
tripsina.
• Otras enzimas reciben el nombre según su grupo
activo por ejemplo enzimas cúpricas, enzimas de
hierro- porfirinas.
• Otras enzimas reciben el nombre según la reacción
donde intervienen. Oxido reducción
Grupo Accion ejemplos
Catalizan reacciones de oxido reducción. Tras la acción Dehidrogenasas
catálica quedan modificados en su grado de oxidación por
lo que debe ser transformados antes de volver a actuar de Aminooxidasa
nuevo.
1. Oxidoreductasas Deaminasas
Catalasas
Transfieren grupos activos (obtenidos de la ruptura de Transaldolasas
2. Transferasas ciertas moléculas)a otras sustancias receptoras. Suelen Transcetolasas
actuar en procesos de interconversiones de azucares, de
aminoácidos, etc Transaminasas
Glucosidasas
Verifican reacciones de hidrólisis con la consiguiente Lipasas
3. Hidrolasas obtención de monómeros a partir de polímeros. Suele ser Peptidasas
de tipo digestivo, por lo que normalmente actúan en primer
lugar Esterasas
Fosfatasas
Actúan sobre determinadas moléculas obteniendo de ellas Isomerasas de
sus isómeros de función o de posición. Suelen actuar en azúcar
4. Isomerasas procesos de interconversion
Epimerasas
Mutasas
Realizan la degradación o síntesis (entonces se llaman Aldolasas
sintetasas) de los enlaces denominados fuertes sin ir
5. Liasas acoplados a sustancias de alto valor energético. Decarboxilasas
Realizan la degradación o síntesis de los enlaces fuertes Carboxilasas
mediante el acoplamiento a sustancias ricas en energía
ESTRUCTURA.
• Algunas enzimas están formadas solo por proteínas como por
ejemplo la pepsina.
• Otras tienen dos partes una de las cuales es proteínas y se
llama apoenzima y otra no proteica se llama coenzima o
cofactores
• La apoenzima y la coenzima separadas carecen de actividad
catalítica, su actividad solo es posible cuando se junten ambos
elementos a este conjunto se le llama Holoenzima.
• Las coenzimas en su estructura contienen algunas vitaminas
como por ejemplo tiamina, niacina, riboflavina, piridoxina etc.
• Los cofactores son por lo regular iones metálicos u otros iones.
Por ejemplo Mg++(Glucosa) Cl- (amilasa), ion Cobre.
Estructura de la triosafosfato isomerasa . Conformación en forma de diagrama de cintas rodeado
por el modelo de relleno de espacio de la proteína. Esta proteína es una eficiente enzima
involucrada en el proceso de transformación de azúcares en energía en las células.
PROPIEDADES.-
a) Especificidad.- varían en el grado de su especificidad por ejemplo Proteasas
participan en la hidrólisis de todas las proteínas. La Amilasa actúa degradando al
almidón y glucógeno y la Ureasa solo hidroliza a la urea.
b) Poder catalítico.- es muy alto y en algunas es extraordinario por ejemplo la
catalasa logra el desdoblamiento de unas 5 millones de moléculas del peróxido
de hidrogeno por minuto a cero grado
c) Solubilidad.- La mayoría de la enzimas son solubles en agua o en soluciones
salinas diluidas a excepción las que se encuentran en las mitocondrias que son
insolubles en agua
d) Precipitación.- pueden precipitarse añadiendo cantidades suficiente de alcohol,
sales metálicos (sulfato de cobre y cloruros de mercurio)
e) Sensibilidad a la Temperatura.- pueden ser afectados por la temperatura pero
tan solo entre ciertos límites por ejemplo La sacarasa a 0ºC es imperceptible su
acción. Su acción se acelera hasta los 40ºC, pero de 41ºC a 50ºC, su actividad se
disminuye y si la temperatura se aumenta se inhibe totalmente
FACTORES QUE AFECTAN A LA ENZIMA
1.- Temperatura.- Por lo general las enzimas del
cuerpo humano y de muchos organismos vivos
a 50ºC a 60ºC se inactivan, y es irreversible,
por lo tanto todos los organismos vivos
mueren por una breve exposición a
temperaturas altas. Las enzimas no son
inactivadas por la congelación, las reacciones
se dan muy lentas, pero la actividad catalítica
reaparece si la temperatura vuelve a su
normalidad
2. Concentración de Hidrogeniones (pH).- son
sensibles a los cambios del pH. La pepsina
actúa en medio muy ácido, contrario a la
tripsina que actua muy bien en pH alcalino
(8,5). La mayor parte de enzimas
intracelulares tienen pH óptimos en medios
neutros.
• Concentración de la Enzima.- la intensidad de la
reacción es directamente proporcional a la
cantidad de la enzima presente
• Concentración del Sustrato.- la intensidad de la
reaccion es directamente proporcional a la
cantidad de sustrato. Constante de Michaellis
La cinética de Michaelis-Menten
Describe la velocidad de reacción de muchas
reacciones enzimaticas.
Recibe este nombre en honor a Leonor Michaelis y
Maude Menten.
El modelo sólo es válido cuando la concentración del
sustrato es mayor que la concentración de la
enzima, y para condiciones de estado estacionario,
es decir, cuando la concentracion del complejo
enzima-sustrato es constante.
Determinación de constantes
Para determinar la velocidad máxima de
una reacción enzimática, la concentración
de sustrato ([S]) se aumenta hasta alcanzar
una velocidad constante de formación de
producto. Esa es la velocidad máxima
(Vmax) de la enzima. En ese momento, los
sitios activos de la enzima están saturados
con sustrato.
Diagrama de velocidad de reacción y
constante de Michaelis-Menten
Velocidad de reacción
La velocidad V indica el número de moléculas del
sustrato que se convierten en producto por segundo.
Con concentraciones crecientes de sustrato[S], la
enzima va acercándose asintóticamente a su velocidad
máxima Vmax, pero nunca la alcanza. Por esta razón, no
hay un valor de [S] determinado para la Vmax. De todas
formas, se puede definir un parámetro característico
de la enzima empleando la concentración de sustrato
a la cual se alcanza la mitad de la velocidad máxima
(Vmax/2).
Constante de Michaelis
Es imposible medir exactamente la concentración de
sustrato que da Vmax, sin embargo las enzimas pueden
caracterizarse a traves de la concentración de sustrato a
la cual la velocidad de reacción es la mitad de la
velocidad máxima. Esta concentración de sustrato se
conoce como constante de Michaelis-Menten (KM).
Las enzimas que exhiben una cinética de
Michaelis-Menten simple esta constante representa la
constante de disociacion del complejo enzima-sustrato
(ES) (o la inversa de la afinidad entre enzima y sustrato).
Valores bajos indican que el complejo ES está unido muy
fuertemente y raramente se separan sin que el sustrato
reaccione para dar producto.
Muchas Gracias
jchapilliquen@uni.edu.pe
También podría gustarte
- Detox Dual Ionico ManualcedipsDocumento11 páginasDetox Dual Ionico ManualcedipsAlfredo Montiel Barrios100% (1)
- Curso Completo de HTML Jorge Ferrer Victor Garcia Rodrigo Garcia HTML Programacion ManualDocumento447 páginasCurso Completo de HTML Jorge Ferrer Victor Garcia Rodrigo Garcia HTML Programacion ManualT-Punisher100% (2)
- Síntesis Química Del PETDocumento36 páginasSíntesis Química Del PETRosmery Bracamonte LeónAún no hay calificaciones
- En ZimasDocumento21 páginasEn ZimasVictor Temponi100% (1)
- Banco Icfes Enlaces QuimicosDocumento6 páginasBanco Icfes Enlaces Quimicoshermann peñaloza sernaAún no hay calificaciones
- 1.44 y 1.45Documento3 páginas1.44 y 1.45Jose HuamanAún no hay calificaciones
- MSDS Nalcool 2000 EspDocumento14 páginasMSDS Nalcool 2000 EspEstevan huertas100% (1)
- Composicion de AlimentosDocumento34 páginasComposicion de AlimentosBoris Anthony Coveñas LunaAún no hay calificaciones
- EnzimasDocumento20 páginasEnzimasRA DO100% (2)
- Bloque IiDocumento196 páginasBloque IiGuillermo MazariegosAún no hay calificaciones
- EnzimasDocumento73 páginasEnzimasAnonymous BXO5lCb5x4Aún no hay calificaciones
- Unidad 2 Diseño 2Documento38 páginasUnidad 2 Diseño 2Cesar Guttierez FabianAún no hay calificaciones
- Laboratorio de Petrología ProsecusiónDocumento104 páginasLaboratorio de Petrología ProsecusiónRodrigo Droguett EspinozaAún no hay calificaciones
- Presentacion BiocatalizadoresDocumento23 páginasPresentacion BiocatalizadoresDario Neri CortezAún no hay calificaciones
- PROTEÍNASDocumento30 páginasPROTEÍNASluciaAún no hay calificaciones
- Tema 3 ENZIMASDocumento145 páginasTema 3 ENZIMASPaulina Campoy RamirezAún no hay calificaciones
- En ZimasDocumento10 páginasEn ZimasLily ContrerasAún no hay calificaciones
- Prueba Acceso GS Biología Enzimas y VitaminasDocumento19 páginasPrueba Acceso GS Biología Enzimas y VitaminasNIEVESAún no hay calificaciones
- Metabolismo CelularDocumento9 páginasMetabolismo CelularamandaAún no hay calificaciones
- ENZIMASDocumento9 páginasENZIMASAlfonso Rios HurtadoAún no hay calificaciones
- Proteinas y EnzimasDocumento8 páginasProteinas y EnzimasNahir NunoAún no hay calificaciones
- En ZimasDocumento16 páginasEn ZimasErickAlmoraxdAncasiAún no hay calificaciones
- Como Se Clasifican Las EnzimasDocumento17 páginasComo Se Clasifican Las EnzimasKaterin Molina Lasprilla100% (2)
- ENZIMAS, Biologia BachilleratoDocumento7 páginasENZIMAS, Biologia BachilleratoLiaAún no hay calificaciones
- Captura 2023-03-11 A Las 17.05.36Documento46 páginasCaptura 2023-03-11 A Las 17.05.36Noelia Rodriguez SuarezAún no hay calificaciones
- Preguntas Sobre EnzimasDocumento3 páginasPreguntas Sobre EnzimasyuriAún no hay calificaciones
- Metabolismo CelularDocumento1 páginaMetabolismo CelularArtic AAún no hay calificaciones
- EzimasDocumento6 páginasEzimasdifat franciscoAún no hay calificaciones
- Clasificación de Las EnzimasDocumento1 páginaClasificación de Las EnzimasufirAún no hay calificaciones
- Actividad 2 Enzimologìa y BioenergèticaDocumento25 páginasActividad 2 Enzimologìa y BioenergèticaEvelis G GAún no hay calificaciones
- Aprendizaje 10Documento8 páginasAprendizaje 10ricardo moralesAún no hay calificaciones
- EnzimaDocumento3 páginasEnzimaAdrianyela TeixeiraAún no hay calificaciones
- Sebastian Luna Documento La Química de La BiologíaDocumento19 páginasSebastian Luna Documento La Química de La BiologíaOscar Chay LopezAún no hay calificaciones
- Enzimas e Introduccion Al MetabolsimoDocumento27 páginasEnzimas e Introduccion Al MetabolsimoTino JFAún no hay calificaciones
- ENZIMASDocumento2 páginasENZIMASRomina DiazleccaAún no hay calificaciones
- 4° Año-Teoría 16Documento3 páginas4° Año-Teoría 16Jackson López LaviAún no hay calificaciones
- B Informe Lab Bioq 2023 1 Práctica 5 Actividad Enzimática en La DigestiónDocumento9 páginasB Informe Lab Bioq 2023 1 Práctica 5 Actividad Enzimática en La DigestiónYeiner BautistaAún no hay calificaciones
- EnzimasDocumento6 páginasEnzimasKei D RamirezAún no hay calificaciones
- PROTEINAS Enzimas Breve RepasoDocumento11 páginasPROTEINAS Enzimas Breve Repasohilda fullanaAún no hay calificaciones
- Las EnzimasDocumento8 páginasLas EnzimasMiriam MercadoAún no hay calificaciones
- 1 Enzimas Química-1Documento20 páginas1 Enzimas Química-1Yadira JayaAún no hay calificaciones
- Bioquimica Tercer ParcialDocumento39 páginasBioquimica Tercer Parcialsabriii Mapofseul7 BTSAún no hay calificaciones
- Unidad IvDocumento11 páginasUnidad IvLlencis ColónAún no hay calificaciones
- ENZIMASDocumento25 páginasENZIMASBRiAnKo AlKaTrAzAún no hay calificaciones
- Balotario de Biotecnologia G 8Documento27 páginasBalotario de Biotecnologia G 8TOCAS MALCA VICTOR ANDREAún no hay calificaciones
- CELULA Proceso Celulares 1Documento49 páginasCELULA Proceso Celulares 1erikajacquez135Aún no hay calificaciones
- Trabajo de EnzimasDocumento47 páginasTrabajo de EnzimasMarii Cl ToAún no hay calificaciones
- Taller Enzimología 1Documento5 páginasTaller Enzimología 1Miguel RuizAún no hay calificaciones
- Presentación Biología Células Infantil Orgánico Verde y Azul-1Documento21 páginasPresentación Biología Células Infantil Orgánico Verde y Azul-1María Celeste De Lira CortésAún no hay calificaciones
- Cuestionario EnzimasDocumento6 páginasCuestionario EnzimasLUZ DARY SERRANO SERRANOAún no hay calificaciones
- Enzimas y CoenzimasDocumento12 páginasEnzimas y CoenzimasJIMENA LETICIA MACHACA MAMANI100% (1)
- EnzimasDocumento9 páginasEnzimasFernando Rodriguez ChavezAún no hay calificaciones
- En ZimasDocumento2 páginasEn ZimasAdriana RicoAún no hay calificaciones
- Definición de Enzima y EstructuraDocumento10 páginasDefinición de Enzima y EstructuraImnova TecAún no hay calificaciones
- Informe EnzimasDocumento17 páginasInforme EnzimasJunior Andrade JaqueAún no hay calificaciones
- ENZIMAS Sesión 2Documento33 páginasENZIMAS Sesión 2Christian YoveraAún no hay calificaciones
- Monografia de EnzimasDocumento7 páginasMonografia de EnzimasJINX XNIJAún no hay calificaciones
- ENZIMASDocumento22 páginasENZIMASKimberly CarrilloAún no hay calificaciones
- Enzimas y CoenzimasDocumento11 páginasEnzimas y CoenzimasAntonella Elda CarrizoAún no hay calificaciones
- Tarea 3 Bioquimica I Brenda GarciaDocumento5 páginasTarea 3 Bioquimica I Brenda Garciabree garciaAún no hay calificaciones
- Catalizadores y EnzimasDocumento24 páginasCatalizadores y EnzimasElias BoychukAún no hay calificaciones
- Enzimas 2023Documento80 páginasEnzimas 2023Elianita LópezAún no hay calificaciones
- Downloadfile-26 - Morfo IDocumento61 páginasDownloadfile-26 - Morfo IAna Mercedes Ramones FloresAún no hay calificaciones
- EnzimasDocumento6 páginasEnzimasFrancisco Javier Navarro GalvezAún no hay calificaciones
- Resumen-Introducción A La Microbiología-Ochoa RuizDocumento9 páginasResumen-Introducción A La Microbiología-Ochoa RuizVALENTINA OCHOA RUIZAún no hay calificaciones
- BAMBUCHADocumento27 páginasBAMBUCHAremixxx5Aún no hay calificaciones
- TrabajoDocumento9 páginasTrabajoYumely OsunaAún no hay calificaciones
- Diapositivas de Enzimas Estructura y ClasificaciónDocumento23 páginasDiapositivas de Enzimas Estructura y ClasificaciónVini GallegosAún no hay calificaciones
- Modelo Lab 2Documento28 páginasModelo Lab 2KARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Silicatos y Minerales Formadores de Las RocasDocumento28 páginasSilicatos y Minerales Formadores de Las RocasKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- DinámicaDocumento63 páginasDinámicaKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Detalle AIE #2 - PAJ 2022 - IIDocumento2 páginasDetalle AIE #2 - PAJ 2022 - IIKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Practica 04 - Propiedades y Reconocimiento de Mat. Org. de Materia Viva-15.06.2022Documento6 páginasPractica 04 - Propiedades y Reconocimiento de Mat. Org. de Materia Viva-15.06.2022KARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Cifras SignificativasDocumento3 páginasCifras SignificativasAndre BarrantesAún no hay calificaciones
- Examen Parcial 2020-1Documento2 páginasExamen Parcial 2020-1KARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Lenguaje de Programacion JavaScript 5Documento25 páginasLenguaje de Programacion JavaScript 5Javier BladimirAún no hay calificaciones
- Alcanos 01Documento39 páginasAlcanos 01KARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Examen Parcial 2019-1 SolucionarioDocumento3 páginasExamen Parcial 2019-1 SolucionarioKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Temario Guía de JSDocumento3 páginasTemario Guía de JSKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Silabo - Lenguaje de Programacion - 2020Documento3 páginasSilabo - Lenguaje de Programacion - 2020KARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Historia Lenguaje de Programacion - 2020Documento27 páginasHistoria Lenguaje de Programacion - 2020ANDRHEE GHIANCARLO BARRANTES PUPUCHEAún no hay calificaciones
- EP 21-2 SoluciónDocumento1 páginaEP 21-2 SoluciónKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Laboratorio 1 - Quimica IiDocumento9 páginasLaboratorio 1 - Quimica IiKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Análisis Orgánico ElementalDocumento7 páginasAnálisis Orgánico ElementalalexAún no hay calificaciones
- Alcanos 02Documento28 páginasAlcanos 02Andre BarrantesAún no hay calificaciones
- Laboratorio 3 - Quimica IiDocumento5 páginasLaboratorio 3 - Quimica IiKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Poli Funcional EsDocumento8 páginasPoli Funcional EsKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Metano ImportanciaDocumento19 páginasMetano ImportanciaKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- SILABUSDocumento4 páginasSILABUSKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Alcoholes y Fenoles 01-1Documento62 páginasAlcoholes y Fenoles 01-1Derian Giovani Toro ZubietaAún no hay calificaciones
- Parcial 2018 - IiDocumento4 páginasParcial 2018 - IiKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Clase 13 ReproduccionDocumento57 páginasClase 13 ReproduccionKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Silabo de Calculo Integral 2022-1Documento3 páginasSilabo de Calculo Integral 2022-1KARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Seminario 3Documento2 páginasSeminario 3KARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- 2021-2 Examen Final de Física 1 (Final)Documento4 páginas2021-2 Examen Final de Física 1 (Final)KARINA ANDREA CASTILLO CALLE0% (1)
- Sílabo 2022-IDocumento3 páginasSílabo 2022-IKARINA ANDREA CASTILLO CALLEAún no hay calificaciones
- Causas de Los IncendiosDocumento3 páginasCausas de Los IncendiosJoselyn Madeleine Hurtado SilvaAún no hay calificaciones
- Cap. 5 Enlace IonicoDocumento6 páginasCap. 5 Enlace IonicoCarlos Gracia CardosoAún no hay calificaciones
- Sistemas de Varias EtapasDocumento3 páginasSistemas de Varias EtapasGaby GabrielaAún no hay calificaciones
- Tarea 2. POC Temas Unidad 1.Documento10 páginasTarea 2. POC Temas Unidad 1.Claudia Janeth Rivera FuentesAún no hay calificaciones
- Oscar Felipe Mayorga Mazabuel: Gabriela Dulcey Montero Carlos Manuel Cano: Lina Marcela OrdoñezDocumento4 páginasOscar Felipe Mayorga Mazabuel: Gabriela Dulcey Montero Carlos Manuel Cano: Lina Marcela Ordoñezbonacera nonAún no hay calificaciones
- Segundo Taller de Transferencia de Calor Ii-2020Documento4 páginasSegundo Taller de Transferencia de Calor Ii-2020JzuzPinto0% (1)
- Mapa AlquenosDocumento1 páginaMapa AlquenosYaz MooreAún no hay calificaciones
- Análisis MicroscópicoDocumento4 páginasAnálisis MicroscópicoiamdempAún no hay calificaciones
- Cromatografia y SintesisDocumento43 páginasCromatografia y SintesisMario CorralAún no hay calificaciones
- Comportamiento Del Gas Natural y Comportamiento de FasesDocumento21 páginasComportamiento Del Gas Natural y Comportamiento de FasesSambya Naysa Cardenas CandiottiAún no hay calificaciones
- Temperatura - Volumen y PresiónDocumento16 páginasTemperatura - Volumen y PresiónFJ JMAún no hay calificaciones
- Geo Pac RDDocumento9 páginasGeo Pac RDKevin GomezAún no hay calificaciones
- Qgii Unidad II Cinética Química 4Documento19 páginasQgii Unidad II Cinética Química 4Luis RicardoAún no hay calificaciones
- Breve Revision de LiteraturaDocumento3 páginasBreve Revision de LiteraturaErnesto GulichAún no hay calificaciones
- Micronutrientes en CitricosDocumento3 páginasMicronutrientes en CitricosDennis Daniel DanduAún no hay calificaciones
- Jarabe de Maíz de Alta Fructosa Jmaf (Sirope) )Documento27 páginasJarabe de Maíz de Alta Fructosa Jmaf (Sirope) )paula posada100% (2)
- I Laboratorio Virtual de Quimica GeneralDocumento3 páginasI Laboratorio Virtual de Quimica GeneralLincy MartinezAún no hay calificaciones
- Circular Técnica de Combustibles para Motores DeutzDocumento33 páginasCircular Técnica de Combustibles para Motores DeutzFranco MayangaAún no hay calificaciones
- LDGF Informe01 Jacome Osorio Gr5Documento9 páginasLDGF Informe01 Jacome Osorio Gr5Klinsmann DiegoAún no hay calificaciones
- Aislamiento de La Piperina 6Documento8 páginasAislamiento de La Piperina 6Wido Saavedra RomanAún no hay calificaciones
- Sis SimbologiaDocumento12 páginasSis Simbologiafrank ronnyAún no hay calificaciones
- El Átomo A Través Del TiempoDocumento8 páginasEl Átomo A Través Del Tiempoorlando pachecoAún no hay calificaciones