Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Glándulas Paratiroideas
Cargado por
Saira Alexandra Ullaguari CuencaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Glándulas Paratiroideas
Cargado por
Saira Alexandra Ullaguari CuencaCopyright:
Formatos disponibles
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
17
C A P Í T U L O
Trastornos de las paratiroides,
y del metabolismo
del calcio y fósforo
Dolores M. Shoback, MD
y Deborah E. Sellmeyer, MD
En este capítulo se presenta una perspectiva general de las hormo homeostasis mineral. Se presentan los síntomas y signos origina
nas clave que participan en la regulación del calcio, fosfato y el dos por exceso o deficiencia de las hormonas calciotrópicas, junto
metabolismo mineral óseo. Entre ellas se cuentan hormona pa- con la evolución natural del hiperparatiroidismo primario, hi-
ratiroidea, vitamina D —principalmente el metabolito 1,25-(OH)2 percalcemia hipocalciúrica familiar (benigna), hipercalcemia
vitamina D (1,25-dihidroxicolecalciferol)—, calcitonina y factor de enfermedad maligna, diferentes formas de hipoparatiroidis
de crecimiento de fibroblastos-23 (FGF). El ciclo de la remode mo y el carcinoma medular de la tiroides. Se revisan dos de las
lación ósea se describe como una base para entender el manteni causas más frecuentes de masa ósea baja —osteoporosis y osteo
miento normal de la integridad del esqueleto en adultos y de la malacia—, junto con exposiciones sobre su patogenia.
REGULACIÓN NORMAL DEL METABOLISMO DEL CALCIO Y FÓSFORO
GLÁNDULAS PARATIROIDES lación con remanentes del timo. Un sitio frecuente de glándulas
ectópicas es el mediastino anterior. Las ubicaciones ectópicas me
nos frecuentes son la vaina carotídea, pericardio y submucosa
Anatomía faríngea. Alrededor de 10% de las personas tiene glándulas parati
Las glándulas paratiroides normales pesan, cada una, 30 a 40 mg roides adicionales (supernumerarias). Esto se convierte en un tema
y son de color grisáceo amarillento. Cada individuo por lo regu de importancia crucial cuando esas glándulas ectópicas causan
lar tiene cuatro glándulas, de modo que la masa de tejido parati hiperparatiroidismo.
roideo total promedio en adultos es de 120 a 160 mg.
El par superior de glándulas paratiroides se deriva de las cuar
tas bolsas branquiales en el embrión. Estas glándulas se encuen Histología
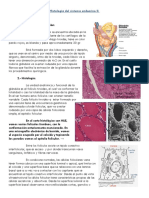
tran cerca del punto de intersección de la arteria tiroidea media Las paratiroides están compuestas de tres tipos de células: prin-
y el nervio laríngeo recurrente. Las glándulas paratiroides supe cipales, claras y oxifílicas. Las primeras tienen diámetro peque
riores pueden estar fijas a la cápsula tiroidea en posición pos ño (4 a 8 μm) con núcleo central, y se cree que se encargan de la
terior o, rara vez, embebidas en la glándula tiroides misma. Las síntesis y secreción de la hormona paratiroidea (PTH). En su
ubicaciones alternativas son el surco traqueoesofágico y el es estado activo, tienen retículo endoplásmico prominente y regio
pacio retroesofágico. El riego sanguíneo de las glándulas parati nes de Golgi densas donde se sintetiza PTH y se empaca para
roideas superiores proviene de la arteria tiroidea inferior o, con la secreción. Las células claras quizá son células principales con
menor frecuencia, de la arteria tiroidea superior. contenido aumentado de glucógeno. Las oxifílicas aparecen en
Las glándulas paratiroides inferiores se desarrollan a partir de las glándulas paratiroides después de la pubertad; son de mayor
la tercera bolsa branquial, al igual que el timo; éstas yacen de ma tamaño que las células principales (6 a 10 μm) y su número se in
nera típica en el polo inferior de la tiroides o cerca del mismo, en crementa con la edad. No está claro si estas células secretan PTH
posición lateral a la tráquea. Las glándulas inferiores reciben su y si se derivan de las principales.
riego sanguíneo a partir de las arterias tiroideas inferiores. La Las paratiroides del adulto normal contienen grasa. La con
ubicación de las paratiroides inferiores es variable. Cuando hay tribución relativa de la grasa a la masa glandular aumenta con
glándulas ectópicas, de modo característico se encuentran en re la edad y en los ancianos alcanza 60 a 70% del volumen de las
483
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
484 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
glándulas. Si ocurren hiperplasia o cambios adenomatosos, el El calcio ionizado sérico controla funciones celulares vitales, como
componente de las glándulas que es grasa disminuye de manera la secreción y acción de hormonas, contracción muscular, trans
evidente. misión neuromuscular y coagulación de la sangre. La unión de
calcio a albúmina depende del pH; se incrementa con la alcalosis
y disminuye con la acidosis. De esta manera, si el calcio ionizado
Fisiología
está bajo, la acidosis tiende a proteger contra hipocalcemia sinto
Alrededor de 99% del calcio corporal total se encuentra en el mática, por el contrario, la alcalosis predispone a hipocalcemia
esqueleto y los dientes; el resto está en los líquidos extracelulares; sintomática.
en éstos, el calcio existe en tres formas: ionizado, unido a proteí Las concentraciones circulantes de PTH pueden cambiar en
na y en complejos. Casi 47% del calcio sanguíneo total está unido cuestión de segundos luego de una alteración del calcio sérico.
a proteína, de modo predominante a albúmina, pero también a Los índices de secreción de PTH se relacionan con las cifras séri
globulinas; una fracción similar está ionizada. El resto forma com cas de calcio ionizado por medio de una relación sigmoidea in
plejos con iones orgánicos, como citrato, fosfato y bicarbonato. versa (figura 17-1). Las concentraciones bajas de calcio ionizado
estimulan al máximo la secreción, mientras que los aumentos del
calcio suprimen la producción y liberación de PTH. La secreción
100
de PTH es en extremo sensible a cambios muy pequeños de las
Respuesta de PTH máxima (%)
cifras de calcio, que tienen efectos considerables sobre el índice
80
de síntesis y liberación de hormona.
El receptor detector de calcio extracelular (CaSR), expresado
60 por células paratiroideas y muchas otras, detecta cambios de la
concentración extracelular de calcio. Este receptor se activa por
40 incrementos de las cifras de calcio y se acopla a vías intracelula
res que producen inhibición de la secreción de hormona (figura
20 17-2) y proliferación de células paratiroideas. Los CaSR también
son expresados en los riñones, las células C tiroideas, el cerebro
0 y muchos otros tejidos. El CaSR también detecta hipocalcemia, y
1.0 1.25 1.5
se estimula la secreción de PTH. La hipocalcemia crónica estimu
Calcio ionizado [Ca2+], mmol/L la la proliferación de células paratiroideas, lo que finalmente da
lugar a hiperplasia glandular. De este modo, el CaSR controla la
secreción y la proliferación en direcciones apropiadas para mos
100
trar respuesta a necesidades fisiológicas.
La PTH se sintetiza en las glándulas paratiroides como una mo
Liberación de PTH (% del máximo)
lécula precursora de 115 aminoácidos (preproPTH) que se divi
de sucesivamente dentro de la célula para formar el péptido de
84 aminoácidos maduro, PTH(1-84) (figura 17-3); esta forma
50
Célula
Receptor
paratiroidea
de calcio
“Punto de ajuste”
(–)
0 1.0 2.0 3.0
Incremento del
[Ca2+], mmol/L
calcio sérico
FIGURA 17–1 Relación sigmoidea inversa entre la liberación de hor
mona paratiroidea (PTH) y las cifras extracelulares de calcio en estudios
en humanos (panel superior) e in vitro en células paratiroideas de huma
PTH
no (panel inferior). Los estudios que se muestran en el panel superior se
realizaron al administrar calcio y el quelante del calcio, EDTA, por vía in
Hueso,
travenosa lenta, a sujetos normales. La PTH intacta sérica se midió me
riñón
diante una valoración inmunorradiométrica en dos sitios. En el panel
inferior, la PTH se midió en el medio que circunda a las células paratiroi FIGURA 17–2 Secuencia de eventos mediante los cuales la concen
deas in vitro por medio de una valoración para PTH intacta. El punto me tración de ion de calcio es detectada por el receptor detector de calcio
dio entre los índices secretorios máximo y mínimo se define como el paratiroideo (CaSR). La activación de este receptor al final está enlazada
punto de ajuste para la secreción. (Redibujada, con autorización, de Brown E. Ex por medio de vías de transducción de señal intracelular con la inhibición
tracellular Ca2+ sensing, regulation of parathyroid cell function, and role of Ca2+ and other de la secreción de PTH y la proliferación de células paratiroideas. (Redibuja
ions as extracellular [first] messengers. Physiol Rev. 1991;71: 371.) da, con modificación, de Taylor R. A new receptor for calcium ions. J NIH Res. 1994;6:25.)
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 485
Transcripción
Célula paratiroidea Fase
del gen Marca
que codifica para sólida
PTH en el núcleo +
CaR
Ca2+ PTH PTH
↑ [Ca2+]i Ab1 Ab2
Muestra de suero
mRNA que contiene
PTH intacta
Ribosoma
N y C
Fragmentos de PTH
N C
84 84
1 84
84 84
–1 1 1
–6 –1 1 1
PreproPTH
–6 –6 84
–29 (115 aminoácidos) PTH
1 84
Retículo endoplásmico
Gránulo 1 Ab1 Ab2
Aparato
secretor
de Golgi
FIGURA 17–3 Eventos biosintéticos en la producción de hormona pa Molécula de PTH intacta
ratiroidea (PTH) dentro de las células paratiroideas. El gen que codifica
para preproPTH se transcribe hacia su mRNA, que se traduce en los ribo FIGURA 17–4 Representación esquemática del principio de la valo
somas hacia preproPTH (aminoácidos -29 a +84). La presecuencia se eli ración de dos sitios para hormona paratiroidea (PTH), aquí PTH(1-84)
mina dentro del retículo endoplásmico, lo que da proPTH (-6 a +84). Otro biointacta de longitud completa. La etiqueta puede ser una sonda lumi
fragmento de seis aminoácidos se elimina en el aparato de Golgi. La niscente o 125I en la valoración inmunoquimioluminométrica o inmu
PTH(1-84) madura liberada desde el aparato de Golgi se empaca en grá norradiométrica, respectivamente. Se usan dos anticuerpos específicos
nulos secretorios y se libera hacia la circulación en presencia de hipocal para región, diferentes (Ab1 y Ab2). El epítopo para Ab1 está en el N-térmi
cemia. Se propone que el receptor detector o sensor de calcio (CaSR) o no extremo, lo que asegura que en la valoración sólo se cuenta la especie
CaR detecta cambios del calcio extracelular que afectan tanto la libera de hormona que contiene inmunodeterminantes tanto N como C termi
ción de PTH como la transcripción del gen que codifica para preproPTH. nal/de región media.
Las cifras altas de calcio extracelular también promueven la degradación
intracelular de PTH. (Redibujada, con autorización, de Habener JF et al. Biosynthesis
of parathyroid hormone. Recent Prog Horm Res. 1977;33:249.) Mecanismo de acción
de la hormona paratiroidea
de la hormona se empaca hacia gránulos secretorios y se libera Hay dos tipos de receptores de PTH. El receptor tipo 1 reconoce
hacia la circulación. La PTH(1-84) es la forma de PTH que tiene PTH y péptido relacionado con hormona paratiroidea (PTHrP)
actividad biológica en células blanco, y tiene una vida media y, además, se denomina receptor PTH-1. El receptor tipo 2 es es
muy breve in vivo, de casi 10 minutos. La PTH(1-84) se metabo pecífico para PTH. La PTH y el PTHrP (que se describe más
liza en el hígado y otros tejidos hacia formas de la región media adelante) se unen al receptor tipo 1 mediante residuos en sus do
y carboxilo terminal que probablemente son inactivas desde el minios amino terminal. La PTH activa la adenilil ciclasa y produ
punto de vista biológico. Esos fragmentos circulantes se acumu ce el segundo mensajero cAMP (figura 17-5). El receptor tipo 1
lan hasta concentraciones muy altas en pacientes con insuficiencia también se acopla a la estimulación de actividad de fosfolipasa C,
renal, porque los riñones son un importante sitio de depuración lo que da pie a la generación de trifosfato de inositol y diacil
de PTH desde el organismo. Las valoraciones de PTH intacta glicerol (figura 17-5). La activación de esta vía de transducción
en uso sistemático miden la PTH(1-84) usando métodos inmu de señal induce movilización de calcio intracelular y activación de
norradiométricos o inmunoquimioluminométricos en los que se proteína cinasa C en células con capacidad de respuesta a PTH
emplean dos anticuerpos: uno dirigido contra un epítopo amino y PTHrP. El receptor de PTH tipo 2 se expresa en tejidos blanco
terminal, que está marcado, y el otro dirigido contra un epítopo de PTH no clásicos (es decir, cerebro, páncreas, testículo y pla
carboxilo terminal de la PTH(1-84), que se inmoviliza (figura centa). No se cree que este receptor participe en el equilibrio de
17-4). Ahora está claro que estas valoraciones de PTH “intacta” minerales y su ligando natural tal vez sea un péptido hipotalámi
también detectan fragmentos de hormona truncados en el amino co llamado péptido tubuloinfundibular.
terminal, como PTH(7-84) que se acumulan en especial en el
suero de enfermos urémicos. Se estima que 30 a 50% de la “PTH
intacta” circulante en el suero de urémicos quizá represente estos
Efectos de la hormona
fragmentos amino terminal. Esto condujo a la creación de valo paratiroidea
raciones de “PTH entera” que sólo detectan PTH(1-84). El anti Las cifras séricas de calcio y fosfato ionizados reflejan la trans
cuerpo amino terminal en estas valoraciones reconoce de modo ferencia neta de estos iones desde el hueso, el tracto gastro
específico los primeros seis aminoácidos de la PTH(1-84); esas intestinal y el filtrado glomerular. La PTH y la 1,25-(OH)2D
valoraciones, empero, aún no han reemplazado a las valoracio desempeñan funciones clave en la regulación del equilibrio del
nes intactas originales para uso clínico rutinario. calcio y fosfato (figura 17-6). Cuando la concentración sérica de
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
486 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
PTH El principal efecto de la PTH sobre el manejo del fosfato es
promover su excreción por medio de inhibición del transpor
te de fosfato dependiente de sodio en los túbulos proximales. Se
cree que las cifras séricas de fosfato influyen sobre los índices
Gs PTH-R G
AC PLC
de secreción de PTH de modo directo; la hiperfosfatemia sirve
como un estímulo para la secreción de PTH mediante un meca
PIP2
nismo incierto. La hipofosfatemia aumenta la conversión de 25-
AMP (OH)D en 1,25-(OH)2D en los riñones, que por medio de sus
ATP cíclico efectos intestinales y renales promueve la retención de fosfato. La
Diacilglicerol
hiperfosfatemia también inhibe la producción de 1,25-(OH)2D
1,4,5-InsP3
(véase más adelante) y disminuye el calcio sérico al formar com
plejos con el mismo en la circulación.
Activación Movilización
de proteína de calcio
La PTH además incrementa la excreción urinaria de bicar
cinasa C intracelular bonato mediante su acción sobre el túbulo proximal; esto puede
producir acidosis tubular renal proximal. Tales respuestas fisio
FIGURA 17–5 Vías de transducción de señal activadas por la unión lógicas a la PTH son la base de la hipofosfatemia y acidosis hi
de la hormona paratiroidea (PTH) al receptor PTH-1 (PTH-R) en una célula
perclorémica que por lo general se observan en pacientes con
blanco. La PTH interactúa con su receptor. Esto aumenta la unión de tri
fosfato de guanosina a la proteína G estimuladora de adenilil ciclasa Gs,
hiperparatiroidismo. La deshidratación también es frecuente en
que activa la enzima. Se forma adenosina monofosfato cíclico (cAMP). La la hipercalcemia moderada a grave de cualquier origen, lo que se
PTH también incrementa la activación (dependiente de proteína G) de fos debe al efecto de la hipercalcemia sobre la acción de la vaso
folipasa C (PLC), que cataliza la desintegración del fosfolípido de mem presina en la rama ascendente gruesa medular del riñón. Las
brana fosfatidilinositol 4,5-bisfosfato (PIP2). Esto produce los segundos concentraciones altas de calcio, quizá al interactuar con CaSR
mensajeros, inositol trifosfato (1,4,5-InsP3) y diacilglicerol. El 1,4,5-InsP3 mo renales, disminuyen la capacidad de la vasopresina endógena
viliza calcio intracelular, y el diacilglicerol activa a la proteína cinasa C. para estimular la resorción de agua. De esta manera, la hipercal
cemia induce diabetes insípida nefrogénica resistente a la vaso
presina.
calcio disminuye, se libera con rapidez PTH, y actúa con celeri Conjuntamente con la 1,25-(OH)2D, la PTH incrementa la re
dad para promover la resorción de calcio en el túbulo distal y en sorción ósea para restituir normocalcemia (véase más adelante).
la rama ascendente gruesa medular del asa de Henle. También la La PTH aumenta la actividad osteoclástica por medio de la es
PTH estimula la liberación de calcio desde el hueso. Estas accio timulación de RANK-L (ligando de receptor activador del factor
nes sirven para restituir las cifras de calcio sérico a lo normal. nuclear κB), que es expresado por células de la línea osteoblástica
La acción renal de la PTH es rápida; sucede minutos después (incluso células del estroma y osteoblastos). El RANK-L interac
de un aumento de la hormona, sin embargo, el efecto general de túa con su receptor RANK sobre células de la línea de osteoclas
la PTH sobre los riñones depende de varios factores. Cuando hay tos para estimular su diferenciación y función, que es la resorción
hipocalcemia y la PTH está alta, la excreción urinaria de calcio es ósea (figura 17-7). Una vez que cesa la resorción, se forma hueso,
baja. Esto refleja la expresión completa del efecto renal primario porque los procesos de resorción y formación están acoplados.
de la PTH para incrementar la resorción renal de calcio. Cuan En los hiperparatiroidismos primario y secundario, cuando las
do las concentraciones de PTH son altas en el hiperparatiroidismo tasas de producción de PTH son excesivas, puede ocurrir pérdi
primario, la hipercalcemia se produce por movilización aumen da ósea neta con el tiempo, quizá porque aun cuando los proce
tada de calcio desde el hueso e incremento de la absorción intes sos de formación y resorción están acoplados, pueden no llevarse
tinal de calcio. Estos eventos elevan el aporte de calcio al filtrado a cabo con 100% de eficacia.
glomerular. Dado que se filtra más calcio, se excreta más en la
orina, a pesar de las cifras altas de PTH. Si la carga filtrada de
calcio es normal o baja en un paciente con hiperparatiroidismo PÉPTIDO RELACIONADO
primario —debido a ingestión baja de calcio en la dieta o a hueso CON LA HORMONA PARATIROIDEA
desmineralizado—, la excreción urinaria de calcio puede ser
normal o incluso baja. De esta manera, puede haber variabilidad El PTHrP es un péptido de 141 aminoácidos que es homólogo
considerable de la excreción de calcio entre pacientes con hiper con la PTH en su región amino terminal (figura 17-8) y es reco
paratiroidismo. nocido por el receptor de PTH tipo 1. En consecuencia, el PTHrP
Si la función renal es normal, el incremento crónico de la PTH tiene efectos similares a los de la PTH sobre el hueso y el riñón;
sérica aumenta la producción renal de 1,25-(OH)2D. Esta hormo aumenta la resorción ósea y la excreción de fosfato, y reduce la
na esteroide estimula la absorción tanto de calcio como de fosfato excreción renal de calcio. El PTHrP se secreta por células tumo
por el intestino delgado (figura 17-6). El efecto requiere al me rales, y de manera original se identificó como la causa de la hi
nos 24 horas para aparecer por completo, y empezar a restituir percalcemia de la enfermedad maligna, un síndrome que puede
las concentraciones normales de calcio. El logro de eucalcemia imitar hiperparatiroidismo primario (véase más adelante).
conduce entonces a reajuste hacia abajo del índice secretor de A diferencia de la PTH, que se sintetiza de modo exclusivo en
PTH. Cualquier incremento de la 1,25-(OH)2D sirve para inhi las células paratiroideas, el PTHrP se produce en muchos tejidos.
bir más la síntesis de PTH al unir a vitamina D los receptores en Funciona de forma principal como un factor de crecimiento y
la paratiroides. diferenciación de tejido en el ámbito local, y como regulador del
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 487
Calcio ionizado bajo
A
Cuatro
glándulas
paratiroides
Liberación de
Inhibición por Inhibición por
PTH(1-84) hacia
retroalimentación retroalimentación
la circulación
de la síntesis de de la secreción de
PTH PTH
Células de los túbulos renales Hueso
• Estimula la resorción • Estimula la liberación de calcio
de calcio a partir del compartimiento
• Inhibe la resorción de fosfato mineral óseo
• Estimula la producción • Estimula células osteoblásticas
de 1,25-(OH)2D • Estimula la resorción ósea por
medio del efecto indirecto sobre
osteoclastos
• Aumenta la degradación
de matriz ósea
• Incrementa la resorción Aumenta el calcio sérico
intestinal de calcio
B Fósforo ↑Conversión de
sérico bajo 25-(OH)D →1,25-(OH)2D
• Libera fosfato • Incrementa la resorción
de la matriz de fosfato
FIGURA 17–6 Principales acciones de la hormona paratiroidea (PTH) y 1,25-(OH)2D en el mantenimiento de la homeostasis del calcio y el fosfa
to. (Redibujada, con autorización, de Chandrasoma P et al., eds. Concise Pathology, 3a ed. Originalmente publicada por Appleton & Lange. Copyright © 1998 por McGraw-Hill Compa
nies, Inc.)
tono de músculo liso. En el desarrollo normal del cartílago y el la piel, los folículos pilosos, los dientes y la mama. El PTHrP tie
hueso, el PTHrP estimula la proliferación de condrocitos e inhi ne una función importante en la determinación del contenido de
be la mineralización de cartílago. Los embriones sin PTHrP no calcio en la leche de animales que amamantan.
son viables, y presentan múltiples anormalidades de hueso y car A pesar de la unión del PTHrP al mismo receptor PTH-1
tílago. El PTHrP también parece regular el desarrollo normal de (véase antes) para alcanzar casi todos sus efectos fisiológicos,
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
488 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
1 5 modo, hay varias maneras mediante las cuales las células pueden
Ala Val Ser Glu His Gln Leu Leu His 10 reaccionar de modo diferencial a estos péptidos similares.
H 2N
Asp
Lis PUNTO DE CONTROL
Gli
1. Describa los tipos de células en las glándulas paratiroides.
Lis 2. ¿De qué modo la concentración sérica de albúmina y el pH
20 15
Ser de la sangre influyen sobre la distribución del calcio hacia
Fen Fen Arg Arg Arg Leu Asp Gln IIe fracciones ionizada y unida a proteína?
Leu
25 3. ¿Qué avances han ocurrido en las inmunovaloraciones de
His
dos sitios para PTH que afectan a pacientes urémicos?
His 4. ¿Cuáles son las acciones de la PTH y 1,25-(OH)2D sobre hue
so, riñones y tracto gastrointestinal?
Leu 5. ¿Qué es el PTHrP? ¿En qué se parece su acción a, y en qué
30 34
IIe difiere de, la de la PTH?
Ala Glu IIe His Tre Ala
FIGURA 17–7 Interacciones entre una célula y otra, y moléculas esen HUESO
ciales para la diferenciación de osteoclastos y la activación de los mismos.
Una molécula de superficie celular conocida como RANK-L sobre células El hueso tiene dos compartimientos. En el exterior está el hueso
del estroma de la médula ósea osteoblástica puede interactuar con célu cortical o compacto, que representa 80% de la masa del esquele
las precursoras osteoclásticas en la médula ósea (derivadas de células
to y cumple con una función importante para otorgarle su fuerza
de la línea monocítica) por medio de sus moléculas de superficie celu
al hueso. Por debajo de la corteza yace el otro compartimiento: el
lar designadas RANK. Esta interacción, en presencia de suficiente factor
estimulante de colonias de macrófagos (mCSF), promueve la diferen hueso trabecular o esponjoso, que constituye 20% de la masa de
ciación y la fusión de estas células finalmente para formar osteoclastos esqueleto. El hueso trabecular consiste en placas interconectadas,
maduros, y permite que osteoclastos por lo demás quiescentes resorban las trabéculas, que están cubiertas por células óseas y son sitios
hueso. Estas vías son interferidas por la elaboración de una molécula re de remodelado activo. Los espacios de este “panal de abejas” irre
ceptora señuelo secretada para RANK-L conocida como OPG, que blo gular están llenos de médula ósea, ya sea médula roja (en la cual
quea la activación de osteoclastos y la diferenciación de los mismos. (Oc, la hematopoyesis es activa) o médula blanca (que es principalmen
osteoclasto.) (Redibujada, con autorización, de Goltzman D. Osteolysis and cancer. J te grasa). A causa de su alta proporción entre superficie y volumen,
Clin Invest. 2001;107:1219.) y actividad celular abundante, el hueso trabecular se remodela con
mayor rapidez que el cortical. Debido a la proporción baja entre
superficie y volumen, el hueso cortical se remodela con lentitud.
nuevos estudios indican que las consecuencias de la interacción A fin de comprender el proceso de remodelado, es importan
de la PTH y el PTHrP con el receptor son sorprendentemente te saber algo acerca de las células óseas.
distintas. Cada péptido tiene efectos diferentes sobre el estado Los osteocitos, las células más abundantes en el hueso, deri
conformacional y la magnitud de activación del receptor. El van de la línea de osteoblastos y residen en planos profundos en
PTHrP también puede transcribirse a partir de un promotor que la matriz; los cuales funcionan como mecanorreceptores; detec
sortea el péptido señal. Esto permite que el PTHrP (y no la PTH) tan tensión sobre el hueso y emiten señales para cambios del re
entre al núcleo y medie efectos biológicos adicionales ahí. De este modelado óseo. Los osteoclastos, células gigantes multinucleadas
Célula del estroma
osteoblástico Resorción ósea
Oc quiescente
OPG
M-CSF
RANK-L Ac
tiv
ac
OPG ión
n
sió
M-CSF RANK-L
Fu
RANK Diferen-
RANK-L Oc activo
ciación
OPG M-CSF
Oc precursor Pre-Oc
RANK
FIGURA 17-8 La secuencia de aminoácidos del residuo de 34 aminoácidos en el péptido relacionado con hormona paratiroidea (PTH) N terminal.
Los aminoácidos que son idénticos a los que se encuentran en la PTH se muestran con bordes de color amarillo oscuro. (Redibujada, con autorización, de Felig
P et al., eds. Endocrinology and Metabolism, 3a ed. McGraw-Hill, 1995.)
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 489
que se especializan en la resorción de hueso, son células con de manera simultánea rompe la matriz ósea por secreción de co
diferenciación terminal que surgen de manera continua a par lagenasa y proteasas. Una proteasa importante es la catepsina K,
tir de precursores hematopoyéticos en la línea de monocitos y una enzima que se está estudiando como un blanco potencial
macrófagos. La formación de osteoclastos requiere el factor para el tratamiento farmacológico de la pérdida de hueso. Los pép
de crecimiento hematopoyético factor estimulante de colonias de tidos de colágeno resultantes tienen enlaces covalentes piridino
macrófagos (m-CSF) y una señal proveniente de células del es lina que pueden valorarse en la orina como una medida de los
troma de la médula ósea. La señal crucial, RANK-L, reside en la índices de resorción ósea. La resorción ósea puede controlarse de
superficie de células del estroma de la médula ósea y células os dos maneras: al regular la formación de osteoclastos y al regu
teoblásticas o es secretada hacia el ambiente extracelular. Esta lar la actividad de osteoclastos maduros. El osteoblasto o célula
molécula, que se requiere para la diferenciación de osteoclastos y formadora de hueso, se deriva de un precursor mesenquimato
la activación de los mismos, se une a su receptor RANK sobre so inducido para diferenciarse en el estroma de la médula ósea.
precursores de osteoclastos y señaliza al interior de la célula. Di Cuando está formando hueso de modo activo, el osteoblasto es
versas células, entre ellas las de la médula ósea, producen un re una célula alta, rechoncha, con un aparato de Golgi abundante.
ceptor señuelo secretado, soluble, la osteoprotegerina (OPG), En superficies donde se está formando hueso de modo activo, los
que se une a RANK-L, lo que evita su interacción con RANK y osteoblastos se encuentran lado a lado, y depositan matriz ósea
suspende la diferenciación y activación de osteoclastos (figura al secretar proteínas y proteoglucanos. La proteína más impor
17-7). Conforme los osteoclastos maduran, adquieren la capaci tante de la matriz ósea es el colágeno tipo I, que constituye 90%
dad para producir enzimas específicas para osteoclasto y al final de la matriz ósea, y se deposita en capas regulares que sirven como
se fusionan para producir las células multinucleadas maduras. El el principal armazón para el depósito de minerales.
proceso de maduración se acelera por hormonas que generan Después de depositar matriz ósea, los osteoblastos la minera
resorción de hueso, como PTH y 1,25-(OH)2D, tal vez por medio lizan al depositar cristales de hidroxiapatita en una disposición
de sus efectos sobre el sistema RANK-L/OPG. ordenada sobre las capas de colágeno para producir hueso lami
Para resorber el hueso, el osteoclasto se posa sobre una super nar. El proceso de mineralización se entiende poco, pero requie
ficie ósea y sella un área al formar un anillo adhesivo en el cual las re un aporte adecuado de calcio y fosfato extracelulares, así como
integrinas celulares se unen de modo estrecho a proteínas de la la enzima fosfatasa alcalina, secretada en grandes cantidades por
matriz ósea (figura 17-9). Una vez que aísla un área de superficie osteoblastos activos.
ósea, el osteoclasto desarrolla por arriba de la superficie una es El remodelado óseo sucede en un ciclo ordenado en el cual
tructura de membrana plasmática complejamente invaginada primero se resorbe el hueso antiguo y luego se deposita hueso
que se denomina borde arrugado, el cual es un organelo separa nuevo. El hueso cortical se remodela desde dentro al cortar conos
do, pero actúa en esencia como un enorme lisosoma que disuelve (figura 17-10), grupos de osteoclastos que hacen túneles a tra
el mineral óseo al secretar ácido sobre la superficie ósea aislada y vés del hueso compacto. Les siguen los osteoblastos, que revisten
Cl–
Receptor de Resorción
Intercambio calcitonina (cono de corte)
de Cl– /HCO–3
K+ Núcleo
Na+-K+-ATPasa
Na+ Reversión
cAMP
Núcleo Núcleo
Anhidrasa carbónica
Fosfatasa ácida H2O + CO2 H++ HCO3–
resistente H+-K+-ATPasa Formación
al tartrato (cono de cierre)
K+ Canales del Ca2+
Canal
del Cl–
Cl– H+
Catepsina K Enzimas
Integrina pH ~ 4 lisosomales Integrina
(αVβ3) RGD Hueso RGD (αVβ3)
Hoyuelo
de resorción Borde en Proteína de
cepillo la matriz ósea
Reposo
FIGURA 17–9 Esquema de un osteoclasto activo. Se muestran los re
ceptores de calcitonina, el borde en cepillo, así como las enzimas y los
canales involucrados en la secreción de ácido hacia la superficie ósea. Las
integrinas (αV, β3) son receptores transmembrana sobre osteoclastos,
que se unen a determinantes (RGD) en proteínas de la matriz ósea como
las fibronectinas. Las integrinas se encargan de la fijación estrecha de os
teoclastos a la superficie ósea. La catepsina K y otras enzimas lisosomales
son secretadas hacia el hoyuelo de resorción para disolver la matriz. (Re FIGURA 17–10 Un cono de corte que remodela hueso cortical. (Re
dibujada, con autorización, de Felig P et al., eds. Endocrinology and Metabolism, 3a ed. dibujada, con autorización, de Felig P et al., eds. Endocrinology and Metabolism, 3a ed.
McGraw-Hill, 1995.) McGraw-Hill, 1995.)
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
490 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
1. Reclutamiento y activación de osteoclasto así los osteoclastos. Los osteoclastos aislados no muestran res
puesta a la PTH o la vitamina D, salvo en presencia de osteoblas
tos. Este mecanismo de acoplamiento asegura que cuando la PTH
activa la resorción de hueso (p. ej., para proporcionar calcio para
corregir hipocalcemia) la formación de hueso también aumenta
rá, lo que tiende a reponer el hueso perdido.
2. Resorción y reclutamiento de osteoblasto
PUNTO DE CONTROL
6. Describa los dos compartimientos del hueso.
7. ¿Cómo se controla la resorción ósea por osteoclastos?
3. Formación de hueso osteoblástica
8. ¿Cuál es la función de los osteoblastos en la formación de
hueso? ¿De qué manera están acopladas las acciones de los
osteoblastos y osteoclastos?
4. Ciclo de remodelado completado
VITAMINA D
La vitamina D en realidad es una prohormona producida en la
FIGURA 17–11 Pasos secuenciales en el remodelado de hueso tra dermis en respuesta a la exposición a la luz ultravioleta B (UVB),
becular. (Redibujada, con autorización, de Felig P et al., eds. Endocrinology and Metabo- y metabolizada hacia sus formas activas primero en el hígado y
lism, 3a ed. McGraw-Hill, 1995.)
después en los riñones. La cantidad de exposición a la luz solar
necesaria para producir suficiente vitamina D es difícil de esti
mar debido a diferencias individuales de la pigmentación de la
los túneles y depositan un cilindro de nuevo hueso sobre sus pa piel, la latitud, y la hora del día. Las fuentes en la dieta tienen con
redes, de manera que los túneles se estrechan de modo progresi tenido relativamente modesto de vitamina D. Por ejemplo, los
vo hasta que todo lo que resta son los delgados canales de Havers, peces ingieren esteroides radiados con luz ultravioleta (en el fito
por medio de los cuales se alimentan las células que se quedan plancton y el zooplancton) que son convertidos en vitamina D y
como osteocitos residentes. almacenados en su hígado.
En el hueso trabecular, el proceso de remodelado ocurre en la
superficie (figura 17-11). Los osteoclastos primero excavan un
hueco y a continuación los osteoblastos lo llenan con hueso nue Fisiología
vo. En un adulto normal, este ciclo dura ~200 días. En cada sitio El 7-dehidrocolesterol, almacenado en la epidermis, es convertido
de remodelado, la resorción de hueso y la formación de hueso en vitamina D3 (colecalciferol) por la luz ultravioleta (longitu
nuevo por lo regular se encuentran de forma estrecha acopladas, des de onda de 280 a 310 nm) (figura 17-12). Ese paso comprende
de manera que en un estado de balance óseo neto de cero, la rompimiento del anillo B de la estructura del colesterol para pro
cantidad de hueso nuevo formado equivale exactamente a la can ducir un secoesteroide; las hormonas con un núcleo coleste
tidad de hueso antiguo resorbido; empero, este grado de equili rol intacto (p. ej., el estrógeno) se llaman esteroides. Ocurre un
brio es breve. Desde la edad de ~20 a 30 años, la masa ósea se proceso similar en vegetales, con una diferencia estructural
consolida tras los incrementos de crecimiento y de depósito de pequeña, que da lugar a vitamina D2 más que a vitamina D3. La
mineral que se lograron durante la adolescencia. Después de los vitamina D2 es activada de modo similar a la D3 en seres huma
30 o 35 años de edad, las mujeres empiezan a perder hueso poco nos, pero parece tener una afinidad de unión disminuida por
a poco. No se conoce por completo cómo se comunican los os la proteína de unión a vitamina D, lo cual da lugar a depuración
teoclastos y osteoblastos para lograr el acoplamiento que asegura aumentada. Esto es en particular evidente cuando se utilizan
el balance óseo perfecto (o casi perfecto); parece ser que las seña médicamente dosis intermitentes grandes (esto es, una vez a la
les importantes son locales, no sistémicas. Aun cuando no se han semana) en lugar de dosis diarias únicas en el tratamiento de
identificado con certeza, un candidato es RANK-L (véase antes). deficiencia de vitamina D.
El RANK-L en la superficie celular o como una molécula soluble Aunque la síntesis cutánea de vitamina D puede ser suficiente
se une a precursores de osteoclastos y apoya su desarrollo y dife para prevenir raquitismo (la manifestación esquelética visible a
renciación. RANK-L también se une a RANK sobre osteoclastos simple vista de la deficiencia de vitamina D), no está claro que
maduros, y esto tal vez medie el acoplamiento de la formación pueda obtenerse exposición a la luz solar en cantidades suficien
y resorción óseas. El proceso de remodelado de hueso no nece tes para optimizar las reservas de vitamina D sin consecuencias
sita en absoluto hormonas sistémicas excepto para asegurar un cutáneas adversas. Además, en casi todas las latitudes en Estados
aporte adecuado de calcio y fosfato. Con todo, las hormonas sis Unidos, hay radiación UVB insuficiente en la luz solar durante
témicas emplean el hueso como una fuente de minerales para la los meses de invierno para inducir producción cutánea de vitami
regulación de la homeostasis de calcio extracelular. Los osteo na D. En 2011, el Institute of Medicine revisó las ingestiones reco
blastos tienen receptores para PTH y 1,25-(OH)2 vitamina D, no mendadas de vitamina D, y recomendó el consumo de 400 IU/día
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 491
Acetato cutánea de vitamina D. La vitamina D formada en la piel es una
sustancia lipofílica que es transportada al hígado unida a albúmi
7-dehidrocolesterol na y a una proteína de unión a vitamina D (DBP) específica. La
vitamina D ingerida es transportada al hígado por medio de qui
lomicrones, ahí, la vitamina D es hidroxilada para producir 25-
hidroxivitamina D (25-[OH]D) (figura 17-12); dicho proceso no
HO
está regulado estrechamente. La 25-(OH)D es transportada me
Piel/ diante la DBP en el suero hacia tejidos blanco, y es almacenada
luz UV en el hígado y en tejidos adiposos. El análisis clínico para deficien
Previtamina D3 cia de vitamina D es la medición de la concentración sérica de
HO 25-(OH)D.
El paso de procesamiento metabólico final en la síntesis de la
hormona activa circulante, 1,25-(OH)2D, tiene lugar principal
CH3 mente en los riñones, aunque muchos tejidos pueden activar lo
Piel/temperatura
calmente la vitamina D para funciones paracrinas y autocrinas.
La conversión de 25-(OH)D en 1,25-(OH)2D por la 25-(OH)D
Vitamina D3
1-hidroxilasa en la corteza renal está estrechamente regulada. La
síntesis de 1,25-(OH)2D es aumentada por la PTH, lo que enla
za así estrechamente la formación de 1,25-(OH)2D a la PTH en el
control integrado de la homeostasis del calcio. La producción de
CH2 1,25-(OH)2D también es estimulada por hipofosfatemia e hipo
HO calcemia. Por otro lado, la hipercalcemia, la hiperfosfatemia, el fac
tor de crecimiento de fibroblastos (FGF)-23, y la PTH disminuida
Absorción intestinal reducirán la producción de 1,25-(OH)2D. Como un control adi
Circulación
cional, la 1,25-(OH)2D induce la enzima 24-hidroxilasa, que ca
Vitamina D
taboliza la 25-(OH)D y la 1,25-(OH)2D, lo que reduce así sus
Intestino 25-hidroxilasa Hígado
concentraciones. El control coordinado por la PTH, la concen
OH
tración sanguínea de mineral, y el aporte de vitamina D es muy
25-hidroxivitamina D3
(25-OH-D3) eficiente. La concentración sérica de 1,25-(OH)2D varía sólo un
poco dentro de un enorme rango de tasas de producción de vita
mina D, pero muestra respuesta con precisión a cambios de la con
CH2 centración sérica de calcio y fosfato dentro del rango normal.
HO
Acción de la vitamina D
25-vitamina D 1α-hidroxilasa Riñón El receptor de la vitamina D es un miembro de la superfamilia de
receptor de esteroide de receptores de unión a DNA nuclear. En
1,25-dihidroxivitamina D3
(1,25-(OH)2-D3) OH el momento de la unión a ligando, el receptor se fija a sitios au
mentadores en genes blanco, y regula de manera directa su trans
cripción. De este modo, muchos de los efectos de la vitamina D
comprenden nueva síntesis de RNA y proteína. Aunque muchos
CH2 metabolitos de la vitamina D son reconocidos por el receptor,
la 1,25-(OH)2D tiene una afinidad aproximadamente 1 000 veces
HO OH
mayor que la de la 25-(OH)D. La 25-(OH)D está presente en la
FIGURA 17–12 La formación y activación de vitamina D. (Redibujada, circulación en cantidades de nanogramo, mientras que la 1,25-
con autorización, de Felig P et al., eds. Endocrinology and Metabolism, 3a ed. McGraw-Hill, (OH)2D circula en cantidades de picogramo; de este modo, otros
1995.) metabolitos de la vitamina D además de la 1,25-(OH)2D tal vez
interactúen con el receptor de vitamina D para producir efectos
clínicos.
en tanto no se cumpla un año de edad, 600 IU/día para individuos Los órganos blanco primarios para la 1,25-(OH)2D son el in
de 1 a 70 años de edad, y 800 IU/día para los de más de 70 años. testino y el hueso. La acción más esencial de la 1,25-(OH)2D es
En Estados Unidos, la leche es complementada con 400 IU de vi estimular el transporte intestinal activo de calcio en el duodeno.
tamina D por cada cuarto de galón (0.940 L). Los complementos El calcio también puede absorberse de manera pasiva por medio
de vitamina D en la dieta constan de vitamina D2 (ergocalciferol) de una ruta paracelular en todo el intestino delgado. Sin embar
y vitamina D3 (colecalciferol). go, particularmente a ingestiones bajas de calcio, casi toda la ab
Si bien hay regulación mínima de la producción de vitamina sorción gastrointestinal de calcio está mediada por el proceso
D en la piel, la exposición aumentada al Sol no da lugar a toxici mediado por vitamina D activa. La 1,25-(OH)2D también induce
dad por vitamina D, puesto que hay fotoconversión de vitamina el transporte activo de fosfato, pero la absorción pasiva domina
D hacia metabolitos inactivos cuando aumenta la concentración este proceso, y el efecto neto de la 1,25-(OH)2D es pequeño.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
492 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
En el hueso, la 1,25-(OH)2D regula varias funciones osteoblás FACTOR DE CRECIMIENTO
ticas. La deficiencia de vitamina D lleva a raquitismo, un defecto
de la mineralización. Aun así, dicho defecto se produce princi
DE FIBROBLASTOS 23
palmente por aporte disminuido de calcio y fosfato hacia sitios
de mineralización. La 1,25-(OH)2D también estimula a los os Propiedades bioquímicas del FGF-23
teoclastos para que resorban hueso, lo que libera calcio para El FGF-23 es un miembro de una familia grande de FGF, factores
mantener las cifras de calcio extracelular. Quizá esto se produce locales que son importantes en el control de la proliferación y
por activación de la vía de señalización RANK-L/RANK por la diferenciación celulares. El FGF-23, en contraste con otros miem
1,25-(OH)2D. bros de la familia de FGF, desempeña una función fundamental
Para demostrar la interrelación entre calcio, fósforo, PTH en la regulación de la homeostasis sistémica de fosfato, el meta
y vitamina D, considere a una persona que cambia desde una bolismo de la vitamina D, y la mineralización ósea. Estudios de
ingestión normal alta de calcio y fosfato hacia una baja: desde familias con trastornos genéticos raros, así como de modelos
1 200 hacia 300 mg al día de calcio (el equivalente de eliminar de ratones transgénicos y con deleción (knockout) que establecen
tres vasos de leche de la dieta). La absorción neta de calcio dismi como objetivo moléculas esenciales en las cascadas de señaliza
nuye de manera aguda, lo que da lugar a una reducción transito ción de FGF-23, han demostrado la importancia del FGF-23 en
ria de la concentración sérica de calcio. Esto activa una respuesta el metabolismo del fosfato y la mineralización del esqueleto.
homeostática guiada por un aumento de la PTH. El incremento
de las cifras de PTH estimula la liberación de calcio desde el hue
so y la retención de calcio por el riñón. Además, el aumento de la Fisiología del FGF-23
PTH, la disminución de calcio y el decremento concomitante de El FGF-23 se sintetiza en muchos tejidos del organismo, pero sus
la concentración sérica de fosfato (debido tanto a menor inges principales fuentes parecen ser las células óseas, en particular los
tión como a la fosfaturia inducida por PTH) activan la síntesis re osteocitos. Un regulador crucial de la producción de FGF-23 es
nal de 1,25-(OH)2D. La 1,25-(OH)2D incrementa la fracción de la concentración sérica de fosfato (figura 17-13). En condiciones
calcio que se absorbe a partir del intestino, aumenta más la li fisiológicas normales, cuando las cifras de fosfato se incremen
beración de calcio desde el hueso, y restituye el calcio sérico a lo tan (p. ej., dieta con alto contenido de fosfato, insuficiencia re
normal. La 1,25-(OH)2D también promueve la absorción intes nal), también lo hacen las de FGF-23. Cuando las cifras séricas
tinal de fósforo, aunque la absorción de fósforo está mucho me de fosfato disminuyen (p. ej., decremento de fosfato, dieta baja
nos regulada que la de calcio. Si bien estos mecanismos pueden en fosfato), sucede lo mismo con las de FGF-23. En estados de
compensar una ingestión baja de calcio en la dieta, y mantener con exceso de fosfato, el FGF-23 reduce la expresión de cotranspor
centraciones séricas normales de calcio y fósforo, esto es a expen tadores de fosfato de sodio (NaPi 2a y 2c) en el riñón y el intesti
sas de movilizar calcio almacenado desde el hueso, y mantener no. Esto conduce a la excreción rápida de fosfato por los riñones,
una concentración alta de PTH. A largo plazo, estos mecanis y a descenso de la absorción intestinal del mismo lo que, a su
mos compensadores darán lugar a disminución del calcio esque vez, restituye a lo normal la concentración sérica de fosfato. Para
lético, resorción ósea aumentada, y alteración de la integridad controlar más el fosfato enviado a la circulación, el FGF-23 tam
del esqueleto. bién inhibe la producción renal de 1,25-(OH)2D (figura 17-13),
Concentración sérica baja de PO43– Cifras séricas altas de PO43–
↓Producción de FGF-23 ↑Producción de FGF-23
↑Expresión de ↓Expresión de
↑Producción de ↓Producción de
NaPi 2a, 2c en el NaPi 2a, 2c en el
1,25(OH)2D 1,25(OH)2D
riñón y el intestino riñón y el intestino
↑Absorción ↑Absorción renal, ↓Absorción ↓Absorción renal,
intestinal de PO43– intestinal de PO43– intestinal de PO43– intestinal de PO43–
Regreso de PO43– sérico a lo normal
FIGURA 17–13 La homeostasis del fosfato se mantiene mediante las acciones coordinadas del FGF-23 y la 1,25(OH)2D. Las concentraciones séricas
bajas de fosfato (PO43-) suprimen la producción de FGF-23, lo que aumenta la producción de 1,25(OH)2D y la expresión de transportadores de fosfato
renales e intestinales (NaPi 2a, 2c). Como resultado, la resorción intestinal y renal de fosfato se incrementa para restituir el difosfato de regreso a lo nor
mal. Cuando las cifras séricas de fosfato aumentan, también lo hacen las concentraciones de FGF-23, lo que suprime estas mismas vías bioquímicas y
restituye el equilibrio de fosfato sérico.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 493
lo cual disminuye más la absorción intestinal de fósforo. Estas Las células C son células fusiformes o poligonales pequeñas dis
acciones directas del FGF-23 están mediadas por receptores de tribuidas en toda la tiroides. Contienen gránulos, mitocondrias
FGF y su proteína transmembrana correceptora klotho. y aparato de Golgi abundantes; pueden estar presentes como cé
lulas únicas o dispuestas en nidos, cordones y hojas dentro del
parénquima tiroideo. Suelen encontrarse dentro de folículos ti
Función del FGF-23 en la enfermedad
roideos, son de mayor tamaño que las células foliculares y mues
Varios trastornos raros han servido para definir las acciones tran tinción positiva para calcitonina.
del FGF-23 en el metabolismo del fosfato y la vitamina D en
humanos. Los trastornos de exceso de FGF-23 son el raquitis-
mo hipofosfatémico ligado a X, el raquitismo hipofosfatémico Fisiología
autosómico dominante y la osteomalacia inducida por tumor La calcitonina es una hormona peptídica de 32 aminoácidos con
(cuadro 17-12 y véase la sección sobre Osteomalacia, más ade un anillo disulfuro amino terminal de siete miembros y prolina
lante). La hipofosfatemia y la osteomalacia que se producen por mida carboxilo terminal (figura 17-14). El procesamiento dife
pérdida de fosfato con una cifra sérica 1,25-(OH)2D baja o ina rencial del gen que codifica para la calcitonina puede llevar a la
propiadamente normal son los datos característicos de estos tras producción de calcitonina en las células C o del péptido relacio
tornos. En contraste, la pérdida de la función del FGF-23, debida nado con el gen de la calcitonina en neuronas. Si bien este último
a trastornos genéticos raros, muestra vínculo con síndromes de péptido y la calcitonina tienen efectos cardiovasculares y neuro
calcificación ectópica, mineralización anormal e hiperfosfatemia. lógicos en dosis farmacológicas, se desconoce su función a cifras
La función del FGF-23 en la hiperfosfatemia y la osteodistrofia de fisiológicas normales. Los tumores de células C pueden liberar am
la enfermedad renal crónica se está investigando de modo activo. bos péptidos.
La hipercalcemia estimula la liberación de calcitonina median
te activación de CaSR en células C. En condiciones normales se
PUNTO DE CONTROL necesitan cambios considerables del calcio sérico para modular
la liberación de calcitonina. Se ignora si los cambios fisiológicos
9. ¿Cómo se sintetiza la vitamina D a partir del 7-dehidroco pequeños del calcio sérico, que modulan con rapidez la secreción
lesterol? de PTH, desencadenan cambios importantes de las concentracio
10. ¿Dónde se almacena la vitamina D? nes de calcitonina. Las hormonas gastrointestinales (GI), colecis
11. ¿Dónde tiene lugar el paso final en la activación de la vita tocinina y gastrina también son secretagogos para la calcitonina.
mina D y cómo está regulado? La secreción de calcitonina in vivo se evalúa al medir las cifras
12. ¿Cuáles son las acciones de la vitamina D? séricas con una radioinmunovaloración de dos sitios.
Acciones de la calcitonina
CÉLULAS PARAFOLICULARES La calcitonina interactúa con receptores en los riñones y el hue
(CÉLULAS C) so; dicha interacción estimula la actividad de adenilil ciclasa y
la generación de cAMP (como se muestra en la figura 17-5 para la
PTH). En los riñones, los receptores de calcitonina están locali
Anatomía e histología zados en la rama ascendente cortical del asa de Henle, mientras
Las células C de la tiroides secretan la hormona peptídica calci que en el hueso se encuentran en osteoclastos.
tonina. Constituyen 0.1% o menos de la masa de células tiroideas La principal función de la calcitonina es disminuir el calcio
y están distribuidas en las partes centrales de los lóbulos laterales sérico, y esta hormona se libera con rapidez en respuesta a la hi
de la tiroides, en especial entre los tercios superior y medio de los percalcemia. La calcitonina inhibe la resorción osteoclástica de
lóbulos. Éstas son células neuroendocrinas derivadas del cuerpo hueso, y bloquea con rapidez la liberación de calcio y fosfato des
ultimobranquial, una estructura que se fusiona con la tiroides. de el hueso. Este último efecto es evidente en cuestión de minu
Calcitonina humana
Asn Gli NH2
Leu
Cis 1
10 20
Ser
Tre Cis Met Leu Gli Tre Tir Tre Gln Asp Fen Asn Lis Fen His Tre Fen Pro Gln Tre Ala
IIe
Gli
Val
Gli
O Ala 30
C Pro
H2N
FIGURA 17–14 Secuencia de aminoácidos de la calcitonina del humano, que demuestra sus características bioquímicas, incluso un puente disulfu
ro amino terminal y prolinamida carboxilo terminal.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
494 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
tos luego de la administración de calcitonina. Tales efectos al tomía, que elimina todas las células C funcionantes. De modo si
final dan pie a una reducción del calcio y fosfato séricos. milar, la calcitonina típicamente aumenta hasta cifras muy altas en
La calcitonina actúa de modo directo sobre los osteoclastos y pacientes con carcinoma medular de la tiroides, sin efecto mani
bloquea la resorción de hueso, inducida por hormonas como la PTH fiesto sobre la concentración sérica de calcio.
y la vitamina D. La potencia de la calcitonina depende del índice
subyacente de resorción ósea y también tiene efecto moderado
sobre los riñones para producir fosfaturia leve. Con la adminis PUNTO DE CONTROL
tración prolongada de calcitonina, ocurre “escape” de sus efectos.
No está clara la importancia general de la calcitonina en el man 13. ¿Cuáles son las acciones de la calcitonina?
tenimiento de la homeostasis del calcio. Las concentraciones 14. ¿Qué efecto tiene la tiroidectomía sobre el calcio sérico?
séricas de calcio son normales en pacientes después de tiroidec
FISIOPATOLOGÍA DE TRASTORNOS SELECCIONADOS
DEL METABOLISMO DEL CALCIO
HIPERPARATIROIDISMO minantes (cuadro 17-2). En pacientes con MEN-1, causada por
mutaciones en el gen MEN-1, que codifica para la proteína me-
PRIMARIO Y SECUNDARIO nina, hay penetrancia alta de hiperparatiroidismo, que afecta
hasta a 95% de los pacientes. Cuando sus glándulas se examinan
Etiología al microscopio, por lo general hay anormalidades en las cuatro
El hiperparatiroidismo primario se debe a producción y libe
ración excesivas de PTH por las glándulas paratiroides. La preva
CUADRO 17–2 Datos clínicos de síndromes
lencia de hiperparatiroidismo es de alrededor de 1:1 000 en EUA,
de neoplasia endocrina múltiple
y la incidencia de la enfermedad se incrementa con la edad. El
grupo con mayor frecuencia afectado es el de las mujeres posme MEN-1
nopáusicas.
El hiperparatiroidismo primario puede producirse por cua Tumores paratiroideos benignos (muy frecuentes)
lesquiera de los trastornos que siguen: adenoma, hiperplasia o Tumores pancreáticos (benignos o malignos)
carcinoma (cuadro 17-1). Los adenomas de células principales
son la causa más frecuente; explican casi 85% de los casos. Casi Gastrinoma
todos los adenomas paratiroideos suceden de modo esporádico
Insulinoma
y son solitarios.
Hiperplasia paratiroidea se refiere a un agrandamiento o anor Glucagonoma, VIPoma (ambos raros)
malidad de las cuatro glándulas. En las formas atípicas de hi
Tumores hipofisarios
perplasia es posible que sólo haya una glándula agrandada, pero
las otras tres glándulas de manera típica muestran por lo menos Secretores de hormona de crecimiento
anormalidades microscópicas leves, como aumento de la celula
Secretores de prolactina
ridad y disminución del contenido de grasa. La distinción entre
hiperplasia y adenomas múltiples es desafiante, y por lo general Secretores de ACTH
requiere el examen de las cuatro glándulas. Las características cla
ve para juzgar si una glándula es normal o no son su tamaño, peso Otros tumores: lipomas, carcinoides, adenomas suprarrenales y tiroideos
y características histológicas. MEN-2A
La hiperplasia paratiroidea puede formar parte de los sín
dromes de neoplasia endocrina múltiple (MEN) autosómicos do Carcinoma medular de la tiroides
Feocromocitoma (benigno o maligno)
CUADRO 17–1 Causas de hiperparatiroidismo Hiperparatiroidismo (raro)
primario MEN-2B
Adenomas solitarios 80 a 85% Carcinoma medular de la tiroides
Feocromocitoma
Hiperplasia 10%
Neuromas de la mucosa, ganglioneuromas
Adenomas múltiples ≈2%
Hábito marfanoide
Carcinoma ≈2 a 5%
Clave: ACTH, hormona adrenocorticotrópica; VIP, polipéptido intestinal vasoactivo.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 495
glándulas. En estos pacientes se observa a menudo hiperpara
tiroidismo recurrente, incluso luego de intervención quirúrgica 100 Hiperplasia 1°
al principio exitosa. El hiperparatiroidismo también ocurre en Adenoma
Liberación de PTH (% del máximo)
la MEN-2A, aunque a una frecuencia mucho menor (alrededor
80
de 20%). Es característico que el hiperparatiroidismo familiar,
sin otras características de síndromes de MEN, afecte las cuatro
glándulas, pero a menudo hay sincronía en la presentación del 60
hiperparatiroidismo. Se considera que las familias con hiperpara Punto de ajuste
tiroidismo aislado y mutaciones en menin son variantes alélicas
de la MEN-1. Tanto el síndrome de hiperparatiroidismo-tumor 40
mandibular como el hiperparatiroidismo aislado familiar son cau
sas de hiperparatiroidismo autosómico dominante. El primero a
menudo incluye fibromas osificantes de la mandíbula y tumores
renales, y se origina por mutaciones de la línea germinal desac
tivantes en el gen HRPT2 que codifica para la proteína parafi-
bromina. 0.5 1.0 1.5 2.0
El carcinoma paratiroideo es una enfermedad maligna rara, [Ca2+], mmol/L
pero el diagnóstico debe considerarse en un paciente con hiper
FIGURA 17–15 Secreción de PTH in vitro a partir de células paratiroi
calcemia grave y una masa cervical palpable. En la intervención
deas de humano, de pacientes con adenomas e hiperplasia paratiroideos.
quirúrgica, los cánceres son más firmes que los adenomas y tie El punto de ajuste para la secreción es la concentración de calcio a la cual
nen mayor probabilidad de estar fijos a estructuras adyacentes. A la liberación de PTH se suprime 50%. Esto se desvía hacia la derecha en
veces es difícil distinguir entre carcinomas y adenomas parati casi todos los adenomas paratiroideos en comparación con tejidos nor
roideos con base en los datos histológicos. La invasión vascular o males, en los cuales el punto de ajuste está alrededor de 1.0 mmol/L de
capsular por células tumorales es un buen indicador de enferme calcio ionizado. (Redibujada, con autorización, de Brown EM et al. Dispersed cells pre
dad maligna, pero estas características no siempre están presen pared from human parathyroid glands: Distinct calcium sensitivity of adenomas vs pri
tes. En muchos casos, las recurrencias locales o las metástasis a mary hyperplasia. J Clin Endocrinol Metab. 1978;46:267.)
distancia hacia el hígado, pulmones o hueso son los datos clíni
cos que apoyan el diagnóstico. Alrededor de 20% de los pacien
tes con el síndrome de hiperparatiroidismo-tumor mandibular y manera estos dos defectos interactúan en la patogenia de la en
mutaciones de la línea germinal en el gen HRPT2 (véase antes) pre fermedad.
senta cáncer paratiroideo. Más aún, también se han encontrado Los defectos genéticos de los cuales depende el hiperparati
mutaciones en HRPT2 en el hiperparatiroidismo aislado familiar roidismo primario han recibido considerable atención. Se cree
y en cánceres paratiroideos esporádicos. Se desconoce la función que los genes que regulan el ciclo celular son importantes en la
celular normal de la parafibromina. patogenia de un subgrupo importante de tumores paratiroideos.
El hiperparatiroidismo secundario implica hiperplasia glan El gen PRAD1 (adenoma por reordenamiento paratiroideo), cuyo
dular difusa que se produce por un defecto fuera de las paratiroi producto es una ciclina D1, ha quedado implicado en la apari
des. El hiperparatiroidismo secundario en pacientes con función ción de tumor paratiroideo y en la patogenia de varios tumores
renal normal puede observarse en sujetos con graves estados de malignos (linfomas de células B, cánceres mamario, pulmonar y
deficiencia de calcio y vitamina D (véase más adelante). En pa de células escamosas de cabeza y cuello). Las ciclinas son proteí
cientes con insuficiencia renal crónica hay muchos factores cau nas reguladoras del ciclo celular. El gen PRAD1 está ubicado en
sales que contribuyen al agrandamiento con frecuencia notorio de el brazo largo del cromosoma 11, al igual que el gen que codifica
las glándulas paratiroides; entre ellos se incluyen disminución para PTH. El análisis de DNA de tumor paratiroideo sugiere que
de la producción de 1,25-(OH)2D, absorción de calcio intestinal sucedió un evento de inversión cromosómica, que llevó a yuxta
reducida, resistencia del esqueleto a la PTH y retención renal de posición del dominio 5-regulador del gen PTH torrente arriba
fosfato. respecto al gen PRAD1 (figura 17-16). Puesto que secuencias re
guladoras en el gen PTH se encargan de su transcripción especí
fica para célula, de inicio se postuló que esta inversión conduce a
Patogenia una sobreproducción específica para célula paratiroidea del pro
La secreción de PTH en el hiperparatiroidismo primario es exce ducto del gen PRAD1. La ciclina excesiva incrementaría el poten
siva dada la concentración del calcio sérico. En el ámbito celu cial proliferativo de las células que portan esta inversión y, dado
lar, hay tanto aumento de la masa celular como un defecto de suficiente tiempo, podría inducir exceso de PTH. Un modelo de
secreción; este último se caracteriza por sensibilidad disminuida ratón transgénico en el cual la ciclina D1 está sobreexpresada en
de la secreción de PTH a la supresión por las cifras séricas de tejido paratiroideo bajo el control del promotor del gen PTH pro
calcio. Tal defecto regulador cualitativo es más frecuente que la porciona pruebas para el mecanismo patogénico del hiperparati
secreción en verdad autónoma. De esta manera, las glándulas pa roidismo primario.
ratiroides de pacientes con hiperparatiroidismo primario de modo El gen del cual depende la MEN-1, que produce el producto
típico están agrandadas e, in vitro, demuestran una “desviación proteínico menina, se identificó en 1997. Se cree que funciona
hacia la derecha” en su punto de ajuste del calcio para secre como un gen supresor tumoral. En consonancia con la hipóte
ción (figura 17-15). Queda por dilucidar por completo de qué sis de “dos golpes” de la oncogénesis, los pacientes con MEN-1
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
496 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
Codificación de PTH Codificación de PTH Codificación de PTH
Rotura
Región flanqueante
de PTH 5'
Región flanqueante
de PTH 5'
Región flanqueante
de PTH 5'
Rotura
PRAD1 PRAD1 PRAD1
Normal Inversión
FIGURA 17–16 Reordenamiento genético propuesto del cromosoma 11 en un subgrupo de adenomas paratiroideos esporádicos. Una inversión de
la secuencia de DNA cerca del centrómero del cromosoma 11 coloca la región 5’-reguladora del gen PTH (también en el cromosoma 11) adyacente al
gen PRAD1, cuyo producto participa en el control del ciclo celular. Esto pone al gen PRAD1 bajo el control de secuencias reguladoras de PTH, que se
predeciría que fueran muy activas en las células paratiroideas. (Redibujada, con autorización, de Arnold A. Molecular genetics of parathyroid gland neoplasia. J Clin Endo
crinol Metab. 1993;77:1109.)
heredan de un progenitor un alelo MEN-1 anormal o desacti roides (véase más adelante). No se ha dilucidado de qué modo
vado; este defecto de la línea germinal se encuentra en todas las las mutaciones de RET alteran el crecimiento de células parati
células. Durante la vida posnatal, el otro alelo MEN-1 en una cé roideas o la secreción de PTH.
lula paratiroidea, por ejemplo, sufre mutación o deleción espon
tánea. Si esta segunda mutación confiere una ventaja en cuanto a Manifestaciones clínicas
crecimiento sobre las células descendientes, hay brote clonal de El hiperparatiroidismo puede presentarse de diversas maneras.
células que portan la segunda mutación, y al final se forma un Los pacientes con esta enfermedad pueden estar en verdad asin
tumor. En casi 25% de los adenomas paratiroideos benignos no tomáticos y se diagnostican mediante análisis de laboratorio de
familiares, hay pérdida alélica de DNA del cromosoma 11, donde detección. Otros pueden tener complicaciones en el esqueleto o
está localizado el gen MEN-1. nefrolitiasis. Dado que el calcio afecta el funcionamiento de casi
La menina se localiza en el núcleo, donde se une al factor de todos los sistemas, los síntomas y signos de hipercalcemia son
transcripción JunD in vitro y suprime la transcripción. Se desco variados (cuadro 17-3). Dependiendo de la naturaleza de las mo
noce la función de la menina en la fisiología normal y los meca lestias, en aquellos con hiperparatiroidismo primario puede sos
nismos por medio de los cuales promueve la formación de tumor pecharse un trastorno psiquiátrico, una enfermedad maligna o,
en hipófisis, páncreas y paratiroides. Ratones con deleción diri con menor frecuencia, una enfermedad granulomatosa, como la
gida de ambos genes que codifican para los homólogos de me tuberculosis o sarcoidosis.
nina murinos (o Men-1) mueren in utero. Los ratones heterocigotos El hiperparatiroidismo es un trastorno crónico en el cual el
para deleción de Men-1 sobreviven, pero con la edad presentan exceso de PTH y la hipercalcemia de larga evolución pueden pro
tumores en los islotes pancreáticos, las cortezas suprarrenales y ducir síntomas crecientes, en particular síntomas por cálculos
las glándulas paratiroides, tiroides e hipófisis, lo que sirve como renales o masa ósea baja. En 10 a 15% de los pacientes con hiper
modelo para el síndrome de MEN-1. paratiroidismo primario ocurren cálculos recurrentes de fosfato
Se dispone de pruebas genéticas para detectar mutaciones en u oxalato de calcio. La nefrolitiasis puede complicarse por obstruc
el gen MEN-1 de manera que pueda efectuarse manejo de casos ción del tracto urinario, infección e insuficiencia renal progresiva.
apropiado y consejo genético. Aquellos con exceso importante de PTH pueden experimentar
El hiperparatiroidismo en la MEN-2A se produce por muta recambio óseo aumentado y pérdida progresiva de la masa ósea,
ciones en la proteína RET. Está claro que la RET tiene impor sobre todo en posmenopáusicas. Esto se refleja en resorción sub
tancia en la patogenia de los otros tumores endocrinos en estos perióstica, osteoporosis (en particular de hueso cortical) e inclu
síndromes, así como en el carcinoma medular familiar de la ti so fracturas patológicas.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 497
CUADRO 17–3 Síntomas y signos de hiperparatiroidismo primario
Sistémicos Oculares Del esqueleto y reumatológicos
Debilidad Queratopatía en banda Osteopenia
Fatigabilidad fácil Cardiacos Fracturas patológicas
Pérdida de peso Intervalo QT acortado Tumores pardos de hueso
Anemia Hipertensión Dolor óseo
Anorexia Renales Gota
Prurito Cálculos Seudogota
Calcificaciones ectópicas Poliuria, polidipsia Condrocalcinosis
Neuropsiquiátricos y neuromusculares Acidosis metabólica Osteítis fibrosa quística
Depresión Defectos de concentración Gastrointestinales
Concentración inadecuada Nefrocalcinosis Enfermedad ulcerosa péptica
Déficit de memoria Pancreatitis
Neuropatía sensorial periférica Estreñimiento
Neuropatía motora Náuseas
Debilidad muscular proximal y generalizada Vómitos
Cabe señalar que una proporción considerable de pacientes intacta. Una PTH alta o de manera inapropiada normal en la si
con hiperparatiroidismo primario es asintomática; pueden expe tuación de hipercalcemia es el dato clave para hacer el diagnós
rimentar deterioro clínico nulo si el hiperparatiroidismo se vigi tico de hiperparatiroidismo primario, la causa más común de
la en lugar de tratarlo con intervención quirúrgica. Debido a que hipercalcemia dependiente de PTH (cuadro 17-5).
es difícil identificar con certeza a estos enfermos cuando se hace Los pacientes con hiperparatiroidismo secundario pueden te
el diagnóstico de hiperparatiroidismo, es indispensable el se ner cifras de calcio normales o subnormales (véase más adelan
guimiento regular. Estudios recientes indican que la masa ósea te). Si la función renal es normal, a menudo existe decremento
puede deteriorarse de modo importante, por lo común en sitios del fosfato sérico, debido a los efectos fosfatúricos de las cifras
corticales (esto es, cadera, antebrazos) después de seguimien elevadas de PTH. Aunque la PTH está alta, el estado de desmi
to conservador más allá de 8 a 10 años. Tales observaciones han neralización del hueso y la deficiencia crónica de vitamina D, se
reabierto el tema acerca de lo recomendable de la observación combinan para producir una carga filtrada baja de calcio; por
médica a largo plazo en esta enfermedad. En comparación, los tanto, la excreción urinaria de calcio suele ser bastante baja. La
pacientes con enfermedad leve en quienes se practica interven concentración de 25-(OH)D también es baja o indetectable en la
ción quirúrgica paratiroidea definitiva experimentarán mejorías deficiencia de vitamina D ocasionada por diversas causas.
de la masa ósea con el tiempo. Estos datos suscitan la pregun
ta de cómo un hiperparatiroidismo primario leve inocuo su
puesto puede ser perjudicial para el esqueleto. HIPERCALCEMIA HIPOCALCIÚRICA
Los datos radiográficos del hiperparatiroidismo primario se FAMILIAR (BENIGNA)
originan por los efectos crónicos de la PTH excesiva sobre el hue
so, entre ellos se cuentan resorción subperióstica (más evidente
en las clavículas y las falanges distales), masa ósea baja generali Etiología
zada y los tumores pardos característicos, pero ahora raros. Con En pacientes con hipercalcemia asintomática debe considerarse el
poca frecuencia, puede producirse osteoesclerosis por acción ex diagnóstico de hipercalcemia hipocalciúrica familiar (benig-
cesiva de la PTH sobre el hueso. Las radiografías de abdomen pue na). Los individuos con esta enfermedad tienen de modo típico
den mostrar nefrocalcinosis o nefrolitiasis. calcio y magnesio séricos altos, concentraciones de PTH norma
En todo sujeto con esta anormalidad debe considerarse el diag les o un poco altas e hipocalciuria (cuadro 17-5). Este trastorno
nóstico diferencial completo de la hipercalcemia (cuadro 17-4). se hereda de una manera autosómica dominante y de forma ca
El hiperparatiroidismo primario explica la mayor parte de los racterística se debe a mutaciones puntuales en un alelo del gen
casos de hipercalcemia en pacientes ambulatorios (>90%). El que codifica para CaSR. En familias con este modo de hipercal
diagnóstico de hiperparatiroidismo primario se confirma por cemia benigna, hay casos raros de hiperparatiroidismo prima-
medio de al menos dos mediciones simultáneas de calcio y PTH rio grave neonatal. Los lactantes que presentan esta forma de
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
498 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
CUADRO 17–4 Diagnóstico diferencial hiperparatiroidismo, que a menudo depende de consanguinidad,
de hipercalcemia por lo regular han heredado dos copias de genes que codifican
para CaSR mutante.
Hiperparatiroidismo primario
Adenoma Patogenia
El CaSR, un miembro de la superfamilia de receptores acopla
Carcinoma
dos a proteína G, tiene expresión acentuada en las paratiroides y
Hiperplasia los riñones. En las paratiroides, la molécula funciona para detec
tar cambios de las cifras séricas de calcio ambiente y luego ajusta
Hipercalcemia hipocalciúrica familiar (benigna) el índice de secreción de PTH. En los riñones, ajusta la excreción
urinaria de calcio, con base en su percepción de la concentra
Hereditaria: mutaciones de CaSR
ción sérica de calcio.
Adquirida: autoanticuerpos que bloquean la detección por el CaSR En la hipercalcemia hipocalciúrica familiar y el hiperparati
del calcio o traducción de señal roidismo neonatal grave, la capacidad para detectar calcio sérico
es mala tanto en los riñones como en las paratiroides. La hiper
Hipercalcemia relacionada con enfermedad maligna
calcemia hipocalciúrica familiar se debe a una reducción parcial
Tumores sólidos (casi todos con producción excesiva de PTHrP) —y en el hiperparatiroidismo neonatal a una disminución no
toria— de la capacidad para detectar el calcio extracelular. Las
Mieloma múltiple células principales paratiroideas detectan de modo erróneo las ci
fras séricas de calcio como bajas, y hay secreción de PTH cuando
Leucemia y linfoma de células T del adulto
debiera estar suprimida (figura 17-2); esto se traduce en concen
Otros linfomas traciones de PTH inapropiadamente normales o un poco elevadas.
En el riñón, las cifras séricas de calcio también se detectan (de ma
Tirotoxicosis nera inapropiada) como bajas y se retiene calcio. Esto da lugar a
Medicamentos
la hipocalciuria típica de esta enfermedad. Dependiendo de la do
sis del gen mutante, los síntomas clínicos tienden a ser leves en la
Tiazidas hipercalcemia hipocalciúrica familiar y graves o en potencia mor
tales en el hiperparatiroidismo neonatal.
Litio
Intoxicación por vitamina D o A Manifestaciones clínicas
Enfermedades granulomatosas Los pacientes con hipercalcemia hipocalciúrica familiar de for
ma típica tienen incrementos asintomáticos del calcio sérico du
Sarcoidosis rante toda la vida. De cualquier modo, no se cree que sufran las
consecuencias de la disfunción de órgano terminal característica
Tuberculosis
del hiperparatiroidismo y la hipercalcemia de larga evolución. Es
Histoplasmosis (y otras micosis) tos individuos por lo regular no presentan la nefrolitiasis, la masa
ósea baja ni la disfunción renal que pueden ocurrir en aquellos
Síndromes de leche y alcalinos con hiperparatiroidismo primario. La paratiroidectomía no re
Clave: CaSR, receptor sensor de calcio; PTHrP, péptido relacionado con la hormona sulta benéfica para individuos que tienen hipercalcemia hipocal
paratiroidea. ciúrica familiar; la hipercalcemia no remite con la operación a
CUADRO 17–5 Datos de laboratorio en la hipercalcemia por diversas causas
Ca2+ sérico PO43− sérico PTH intacta PTHrP 1,25- (OH)2D sérica Ca2+ urinario
Hiperparatiroidismo primario ↑ ↓, N ↑ N, Ind. N, ↑ N, ↑1
Hipercalcemia vinculada con enfermedad maligna ↑ ↓, N Ind. ↑2 N, ↓ ↑
Hipercalcemia hipocalciúrica familiar (benigna) ↑ N N, ↑3 Ind. N ↓
Hipercalcemia dependiente de vitamina D ↑ N, ↑ ↓ Ind. N, ↑4 ↑
Clave: Ind., indetectable; N, normal; PTH, hormona paratiroidea; PTHrP, péptido relacionado con la PTH.
1
También puede estar bajo dependiendo del calcio en la dieta y de la carga de calcio filtrada.
2
En 70 a 80% de los pacientes con cáncer y una base humoral para hipercalcemia.
3
Se han informado aumentos leves de la PTH en hasta 25% de los pacientes.
4
La 1,25-(OH)2D quizá no esté francamente alta en pacientes con intoxicación por vitamina D2 o D3.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 499
menos que se realice una paratiroidectomía total. No se reco primario y se produce por un incremento difuso de la resorción
mienda intervención quirúrgica porque la enfermedad es benigna. ósea inducido por concentraciones circulantes altas de PTHrP.
En contraste, los lactantes con hiperparatiroidismo neonatal El síndrome se exacerba por la capacidad del PTHrP para redu
tienen hipercalcemia intensa, aumentos notorios de la PTH sérica, cir la excreción renal de calcio y la capacidad de la hipercalcemia
desmineralización ósea en el momento del nacimiento, hipoto (al actuar mediante CaSR renales) para disminuir la capacidad re
nía y falta acentuada de crecimiento y desarrollo. Dichos infantes nal de concentración, lo que origina deshidratación progresiva.
por lo general necesitan paratiroidectomía total durante el perio El mieloma múltiple causa hipercalcemia por medio de un me
do neonatal para sobrevivir. canismo distinto; las células de mieloma inducen resorción ósea
En el hipercalcémico asintomático deben obtenerse anteceden local u osteólisis en la médula ósea, quizá al liberar citocinas con
tes familiares detallados en un esfuerzo por documentar hipercal actividad de resorción ósea, como interleucina-1 y factor de ne
cemia o casos de paratiroidectomía fallida en otros miembros de crosis tumoral. Rara vez, los linfomas suscitan hipercalcemia hu
la familia. Es necesario medir de manera simultánea las concentra moral al secretar 1,25-(OH)2D.
ciones séricas y urinarias de calcio y creatinina con el fin de excluir Por último, aun cuando muchos pacientes con hipercalcemia
hipercalcemia hipocalciúrica familiar. En esta enfermedad, las ci tienen metástasis óseas, éstas pueden no contribuir de modo di
fras urinarias de calcio están bajas y casi siempre son de menos de recto a la patogenia de la hipercalcemia.
100 mg/24 horas (cuadro 17-5). El índice de depuración de cal
cio-creatinina derivado de recolecciones de orina de 24 horas por
Manifestaciones clínicas
lo general es de menos de 0.01, pero puede ser tan alto como 0.02.
La proporción se calcula como calcio urinario (mg/dl) × creatini A diferencia de los pacientes con hiperparatiroidismo primario,
na sérica (mg/dl)/calcio sérico (mg/dl) × creatinina urinaria (mg/ que a menudo presentan síntomas mínimos, aquellos con hiper
dl). Las pruebas genéticas para mutaciones del gen que codifica calcemia propia de enfermedad maligna de manera típica están
para CaSR están disponibles en el comercio en varios laborato muy enfermos. Es característico que la hipercalcemia ocurra en
rios y es el mejor método para llegar a un diagnóstico definitivo. la enfermedad maligna avanzada —la supervivencia promedio
de quienes presentan hipercalcemia por lo general es de varias se
manas a meses— y el tumor casi siempre es obvio en el examen del
paciente. Además, la hipercalcemia suele ser grave y sintomática,
PUNTO DE CONTROL con náuseas, vómitos, deshidratación, desorientación o coma. En
el aspecto bioquímico, la hipercalcemia vinculada con enferme
15. ¿Cuál es la causa más frecuente de hiperparatiroidismo pri dad maligna se caracteriza por fosfato sérico disminuido y con
mario? centración suprimida de PTH intacta (cuadro 17-5). Con casi
16. ¿Cuál es la frecuencia de hiperparatiroidismo en los sín todos los tumores sólidos, las cifras séricas de PTHrP están au
dromes de neoplasia endocrina múltiple? mentadas; estos datos, junto con las diferencias de la presentación
17. ¿En qué estados o enfermedades sucede el hiperparatiroi clínica, por lo regular hacen que la diferenciación entre este sín
dismo secundario? ¿Por medio de qué síntomas y signos se drome e hiperparatiroidismo primario sea relativamente fácil.
distingue del hiperparatiroidismo primario?
18. ¿Cuáles son los síntomas y signos frecuentes del hiperpara
tiroidismo primario? ¿De qué modo el hiperparatiroidismo
primario puede distinguirse de la hipercalcemia hipocal PUNTO DE CONTROL
ciúrica familiar? ¿Cuál es el mecanismo de esta diferencia?
19. ¿Qué tumores suelen dar por resultado hipercalcemia?
20. ¿Cuáles son los mecanismos por los que un tumor puede
originar hipercalcemia?
21. ¿Cuáles son los síntomas y signos clínicos de la hipercalce
HIPERCALCEMIA PROPIA mia de la enfermedad maligna?
DE LA ENFERMEDAD MALIGNA
Etiología
Se observa hipercalcemia en casi 10% de las enfermedades malig HIPOPARATIROIDISMO
nas, por lo general en tumores sólidos, en particular carcinomas Y SEUDOHIPOPARATIROIDISMO
de células escamosas (p. ej., pulmones, esófago), carcinoma renal
y carcinoma mamario. La hipercalcemia sucede en más de una
Etiología
tercera parte de los pacientes con mieloma múltiple, pero es poco
común en linfomas y leucemias. El calcio sérico total comprende las contribuciones de formas de
calcio ionizado, unido a proteína y en complejos. No obstante, es
necesario reconocer que los síntomas de hipocalcemia sólo su
Patogenia ceden si hay decremento de la fracción ionizada de calcio. Más
Los tumores sólidos por lo regular dan por resultado hipercalce aún, sólo los pacientes con concentraciones bajas de calcio ioni
mia al secretar PTHrP, cuyas propiedades ya se describieron. Se zado deben evaluarse respecto a la posibilidad de un trastorno
trata de hipercalcemia humoral, que imita el hiperparatiroidismo con hipocalcemia.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
500 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
Una causa frecuente de calcio total sérico bajo es la hipoalbu CUADRO 17–6 Diagnóstico diferencial
minemia. Una albúmina sérica baja sólo reduce el calcio unido a de hipocalcemia
proteína y no el ionizado. Así, éstos no requieren evaluación para
trastornos de minerales; a fin de determinar si un paciente que Fracaso para secretar hormona paratiroidea (PTH)
presenta hipoalbuminemia tiene calcio ionizado bajo, este pará
Hipoparatiroidismo (véase cuadro 17-7)
metro puede medirse de manera directa. Si este análisis de labo
ratorio no se encuentra fácilmente disponible, una alternativa Resistencia a la acción de la PTH
viable es corregir el calcio sérico total para la albúmina sérica baja,
Seudohipoparatiroidismo (tipos 1a, 1b, 2)
lo cual se efectúa al ajustar el calcio sérico total en dirección as
cendente, 0.8 mg/dl por cada disminución de 1 g/dl de albúmi Hipocalcemia vinculada con sepsis
na sérica. Esta corrección simple por lo general lleva el calcio total
Fracaso de la secreción de PTH y resistencia a la acción de la PTH
sérico ajustado hacia el rango normal.
El diagnóstico diferencial de un calcio ionizado bajo es am Disminución crónica de magnesio como resultado de:
plio (cuadro 17-6). La hipocalcemia puede producirse por decre
Diarrea, malabsorción
mento de la secreción de PTH causado por hipoparatiroidismo
o hipomagnesemia. Además, puede deberse a capacidad de res Alcoholismo
puesta reducida de órgano terminal a la PTH pese a cifras de
Fármacos: antibióticos aminoglucósidos, diuréticos de asa, cisplatino,
hormona adecuadas o incluso excesivas; esto se denomina seu- anfotericina B
dohipoparatiroidismo.
Las formas de hipoparatiroidismo son raras (cuadro 17-7). Nutrición parenteral
La mayor parte de los casos se produce a causa de traumatismo, Pérdida renal primaria de magnesio
extirpación, o desvascularización inadvertido de las paratiroides
durante operación paratiroidea. La incidencia de hipoparati Fracaso de la producción de 1,25-(OH)2D
roidismo posoperatorio (rango: 0.2 a 30%) depende de la exten Deficiencia de vitamina D como resultado de causas nutricionales
sión de la intervención quirúrgica antecedente y de la capacidad
del cirujano para identificar tejido paratiroideo normal y preser Enfermedad del hígado
var su riego sanguíneo. La hipocalcemia posoperatoria suele ser Colestasis
transitoria o permanente. Algunos enfermos también pueden que
dar con reserva paratiroidea disminuida. Trastornos del intestino delgado que ocasionan malabsorción
Diversas causas que no son complicaciones posquirúrgicas
Insuficiencia renal
pueden producir un estado de deficiencia absoluta o relativa de
PTH (cuadro 17-7), entre ellas se cuentan destrucción autoin Raquitismo tipo 1 dependiente de vitamina D: actividad defectuosa
munitaria, decremento de magnesio, hipoparatiroidismo auto de 1α-hidroxilasa (muy rara)
sómico dominante o recesivo o ligado a X, hipoparatiroidismo Osteomalacia inducida por tumor
producido por mutaciones activadoras del CaSR o anticuerpos
estimuladores dirigidos contra el CaSR (véase más adelante) e Resistencia a la acción de la 1,25-(OH)2D
hipoparatiroidismo ocasionado por sobrecarga de hierro o por Raquitismo tipo 2 dependiente de vitamina D: defecto del receptor
enfermedad de Wilson. En el síndrome de DiGeorge se obser de vitamina D (raro)
va desarrollo anormal de las glándulas, lo que se traduce en gra
Raquitismo tipo 3 dependiente de vitamina D: producción excesiva de
vedad variable de hipoparatiroidismo. Este síndrome se puede
una proteína de unión a elemento de respuesta a hormona que interfiere
presentar durante la lactancia, niñez o incluso adultez y acom con la unión del heterodímero de receptor de vitamina D-receptor
pañar de anomalías de la inmunidad mediada por células y otras de ácido retinoico a DNA blanco
anomalías congénitas (cuadro 17-7). Las mutaciones en el gen
Desafíos agudos para los mecanismos homeostáticos
que codifica para el factor de transcripción célula glial faltante-B
(GCMB), que es esencial en el desarrollo de las glándulas parati Pancreatitis (formación de sales de calcio en la grasa retroperitoneal)
roides, están enlazadas con hipoparatiroidismo aislado familiar.
Inducida por medicamentos (p. ej., EDTA, citrato, bisfosfonatos, fosfato,
Las mutaciones en el factor de transcripción GATA3 dan lugar a
foscarnet)
desarrollo anormal de la vesícula ótica, riñones y glándulas para
tiroides, lo que da por resultado sordera, anormalidades renales Trasplante de hígado (el citrato no se metaboliza, lo que forma complejos
e hipoparatiroidismo. de citrato de calcio y disminuye el calcio ionizado)
Hay dos variedades del síndrome de insuficiencia polien Rabdomiólisis
docrina autoinmunitaria (APS). Los pacientes con APS-1 por lo
regular tienen candidosis mucocutánea, enfermedad de Addison Síndrome del hueso hambriento (incremento del depósito hacia hueso
(insuficiencia suprarrenal) e hipoparatiroidismo y menos a me desmineralizado)
nudo insuficiencia ovárica y disfunción tiroidea. Diversos com Metástasis osteoblásticas (p. ej., cáncer mamario o prostático)
ponentes del APS-1 se presentan durante la segunda década de la
vida o principios de la tercera (figura 17-17). Síndrome de lisis tumoral (carga aguda de fosfato liberado a partir
de células tumorales como resultado de terapia citolítica)
En la mayoría de estos pacientes se observan autoanticuerpos
contra tejido suprarrenal y paratiroideo. A la postre puede haber Clave: EDTA, ácido etilendiaminotetraacético.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 501
CUADRO 17–7 Causas de hipoparatiroidismo Candidosis mucocutánea
Hipoparatiroidismo
Complicación de intervención quirúrgica tiroidea, paratiroidea o laríngea Enfermedad de Addison
100
Destrucción autoinmunitaria (95%)
Aislado
80 (80%)
Síndrome de insuficiencia poliendocrina autoinmunitaria tipo 1 (APS-1)
(66%)
Pacientes (%)
Consecutivo a reducción de magnesio o hipermagnesemia 60
Después de terapia con 131I para enfermedad de Graves o cáncer tiroideo
40
Consecutivo a acumulación de hierro (talasemia, hemocromatosis)
o cobre (enfermedad de Wilson)
20
Formas genéticas de hipoparatiroidismo
Síndrome de DiGeorge o deleción de 22q 0
1 2 5 10 15 20
Mutaciones autosómicas recesivas o dominantes en el gen que Edad (años)
codifica para pre-proPTH
FIGURA 17–17 Incidencia acumulativa de tres manifestaciones fre
Hipoparatiroidismo ligado a X cuentes de insuficiencia poliglandular autoinmunitaria tipo 1 (APS-1) com
parada con la edad al inicio en una cohorte de 68 pacientes. Las cifras
Mutaciones de factores de transcripción involucrados en el desarrollo entre paréntesis reflejan las incidencias a los 20 años de edad. (Datos gra
de las paratiroides (p. ej., GCMB, GATA3) ficados a partir de Ahonen P et al. Clinical variation of autoimmune polyendocrinopathy-
candidiasis-ectodermal dystrophy [APECED] in a series of 68 patients. N Engl J Med.
Mutaciones de DNA mitocondrial
1990;322:1829.)
Mutaciones activadoras del CaSR
Síndrome autoinmunitario adquirido causado por autoanticuerpos
que activan el CaSR pie a reducción de la absorción intestinal de calcio. En ausencia
de 1,25-(OH)2D y PTH adecuadas, la movilización de calcio desde
Invasión tumoral (muy rara)
el hueso es anormal. Dado que la PTH es deficiente, la excreción
urinaria de calcio suele ser alta, a pesar de la hipocalcemia.
La disminución de magnesio es una causa frecuente de hi
afección de otras glándulas endocrinas (p. ej., gónadas, tiroides y pocalcemia. La patogenia de la hipocalcemia en esta situación
páncreas). El APS-1 es un trastorno autosómico recesivo debido clínica se relaciona con un estado funcional y reversible de hipo
a mutaciones en el gen regulador autoinmunitario (AIRE). El AIRE paratiroidismo. También hay decremento de la capacidad de res
se expresa de modo normal en una subpoblación de células epi puesta de los riñones y del esqueleto a la PTH. La reducción de
teliales en el timo, que se cree que participan en la selección ne magnesio puede suceder por diversas causas, entre ellas alcoholis
gativa de células T autorreactivas durante selección clonal. Estas mo crónico, diarrea y fármacos como diuréticos de asa, antibióti
clonas de células T participan en el reconocimiento de lo pro cos, aminoglucósido, anfotericina B y cisplatino (cuadro 17-6). El
pio y se cree que el fracaso para eliminarlas fundamenta la des magnesio se requiere para mantener respuestas de secreción de
trucción autoinmunitaria de las células endocrinas afectadas en PTH normales. Una vez que se reabastecen las reservas corpora
el APS-1. les de magnesio, las cifras de PTH se incrementan de modo apro
El APS-2 o síndrome de Schmidt se caracteriza por hipopara piado en respuesta a la hipocalcemia y se corrige el desequilibrio
tiroidismo e insuficiencia suprarrenal y no afecta las paratiroides mineral.
(véase capítulo 21). En el seudohipoparatiroidismo las concentraciones de PTH
por lo general están altas, pero la capacidad de los tejidos blanco
(en especial los riñones) para mostrar respuesta a la hormona es
Patogenia subnormal. En el seudohipoparatiroidismo tipo 1, la capacidad de
La patogenia del hipoparatiroidismo es sencilla. La alteración de la PTH para generar un aumento del segundo mensajero cAMP
los minerales ocurre porque la cantidad de PTH liberada es in está disminuida. En pacientes con el tipo 1a, esto se debe a una
adecuada para mantener concentraciones séricas normales de deficiencia del contenido celular de la subunidad α de la proteí
calcio, principalmente debido a pérdida de los efectos conserva na G estimuladora (Gs-α) que acopla el receptor de PTH a la
dores de calcio renales de la PTH y la incapacidad para generar enzima adenilil ciclasa. En aquellos con el tipo 1b, las cifras de
1,25-(OH)2D. Sobreviene hipocalcemia, y se observa además hi proteína Gs-α son normales y en algunos casos hay regulación
perfosfatemia porque se pierde el efecto de la PTH sobre los tú alterada de la transcripción del gen que codifica para Gs-α de
bulos proximales para promover la excreción de fosfato. Puesto bido a metilación anormal de DNA. En sujetos con seudohi
que la PTH se necesita para estimular la producción renal de poparatiroidismo tipo 2, el cAMP urinario es normal, pero hay
1,25-(OH)2D, las cifras de esta última están bajas en pacientes con decremento de la respuesta a la PTH administrada. La patoge
hipoparatiroidismo. La hiperfosfatemia suprime más la síntesis nia de esta forma más rara de resistencia a la PTH aún no se ha
de 1,25-(OH)2D. Las concentraciones bajas de 1,25-(OH)2D dan dilucidado.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
502 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
Los enfermos con mutaciones activadoras del CaSR típicamen
te se presentan con hipocalcemia e hipercalciuria autosómicas
dominantes. Ambos defectos se deben a CaSR demasiado sensi
bles, que desactivan la secreción de PTH y la resorción renal de
calcio a concentraciones séricas de calcio subnormales. Estos
individuos rara vez experimentan síntomas de su hipocalcemia a
menudo leve, pero si reciben vitamina D, están propensos a hiper
calciuria notoria, nefrocalcinosis e incluso insuficiencia renal.
Manifestaciones clínicas
Los síntomas y signos de hipocalcemia son similares, al margen
de la causa subyacente (cuadro 17-8). Los enfermos pueden ser
asintomáticos o tener tetania latente o manifiesta. La tetania se FIGURA 17–18 Posición de los dedos en el espasmo carpiano produ
describe como contracciones musculares crónicas espontáneas. cido por tetania hipocalcémica. (Redibujada, con autorización, de Ganong WF.
Los espasmos dolorosos del carpo y el estridor laríngeo son ma Review of Medical Physiology, 16a ed. McGraw-Hill, 1983.)
nifestaciones notorias de la tetania. La tetania latente puede de
mostrarse al llevar a cabo pruebas para los signos de Chvostek y
de Trousseau. El signo de Chvostek se produce al percutir sobre el nervio facial en posición anterior a la oreja. Las contracciones
espasmódicas de los músculos faciales ipsolaterales indican resul
tado positivo de la prueba. Un signo de Trousseau se demuestra
CUADRO 17–8 Síntomas y signos de hipocalcemia al inflar el manguito del esfigmomanómetro alrededor del brazo
por arriba de la presión arterial sistólica durante 3 minutos. En
Sistémicos Desorientación hipocalcémicos, esto causa contracciones dolorosas y espasmos
de músculos del carpo (figura 17-18). Si la hipocalcemia es grave
Debilidad
y no se reconoce, pueden ocurrir alteración de las vías respirato
Retraso mental rias, estado mental alterado y crisis convulsivas generalizadas e
incluso la muerte.
Cambios conductuales
La hipocalcemia crónica puede producir calcificaciones intra
Neuromusculares Parestesias craneales que tienen una predilección por los ganglios basales. És
tas pueden ser detectables mediante tomografía computarizada
Psicosis
(CT), resonancia magnética (MRI) o radiografías de cráneo. La
Crisis convulsivas hipocalcemia crónica también puede incrementar la calcifica
ción del cristalino y la formación de cataratas.
Espasmos carpopedales
Además de los síntomas y signos de hipocalcemia, los pacientes
Signos de Chvostek y Trousseau con seudohipoparatiroidismo tipo 1a pueden tener un conjunto
de datos que se conocen en grupo como osteodistrofia heredi-
Depresión
taria de Albright. Comprenden estatura corta, obesidad, retra
Calambres so mental, facies redonda, cuarto y quinto huesos metacarpianos
y metatarsianos acortados, y osificaciones subcutáneas. La situa
Parkinsonismo
ción clínica debe guiar el diagnóstico diferencial de hipocalce
Irritabilidad mia. Un antecedente familiar es muy importante para apoyar un
diagnóstico de seudohipoparatiroidismo y otras formas heredi
Calcificaciones en los ganglios basales
tarias de hipoparatiroidismo (cuadro 17-7). Lo más probable es
Cardiacos Intervalo QT prolongado en el ECG que el enfermo con hipocalcemia, hiperfosfatemia y una creati
nina sérica normal, tenga hipoparatiroidismo. Debe buscarse un
Cambios del segmento ST-onda T en el ECG
antecedente de operación en el cuello. En el hipoparatiroidismo
Insuficiencia cardiaca congestiva posquirúrgico es posible que haya un periodo latente prolonga
do antes de que se presente hipocalcemia sintomática. El examen
Oculares Cataratas
físico puede ser útil si identifica signos de hipocalcemia, estigmas
Dentales Hipoplasia del esmalte de osteodistrofia hereditaria de Albright u otros datos de APS-1
(es decir, vitíligo, candidosis mucocutánea, insuficiencia suprarre
Formación defectuosa de la raíz
nal). Los pacientes con seudohipoparatiroidismo tipo 1a suelen
Fracaso de la erupción de los dientes permanentes tener otras anormalidades endocrinas, como hipotiroidismo pri
mario o insuficiencia gonadal.
Respiratorios Laringospasmo
En el diagnóstico diferencial de hipocalcemia, los datos de la
Broncospasmo boratorio son en extremo útiles (cuadro 17-9). El fosfato sérico a
menudo (pero no siempre) está alto en el hipoparatiroidismo y
Estridor
seudohipoparatiroidismo. En la reducción de magnesio, el fosfato
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 503
CUADRO 17–9 Datos de laboratorio en la hipocalcemia
Respuesta de cAMP urinario
Ca2+ sérico PO43− sérico PTH intacta 25-(OH)D3 a la administración de PTH
Hipoparatiroidismo ↓ ↑, N ↓, N1 N N
Seudohipoparatiroidismo ↓ ↑, N ↑ N ↓2
Disminución de magnesio ↓ N ↓, N1 N N
Hiperparatiroidismo secundario3 ↓ N, ↓ ↑ ↓ N
Clave: PTH, hormona paratiroidea; cAMP, monofosfato de adenosina cíclico.
1
Puede ser normal, pero inapropiada para la concentración de calcio sérico.
2
Las respuestas de cAMP urinario a la administración de PTH son subnormales en el seudohipoparatiroidismo tipos 1a y 1b.
3
Como resultado de deficiencia de vitamina D, por ejemplo, excreción urinaria de calcio por lo general de menos de 50 mg/24 horas.
sérico por lo general es normal. En el hiperparatiroidismo secun na D. En todos los pacientes así tratados debe realizarse vigilan
dario que no se debe a insuficiencia renal, el fosfato sérico de cia periódica del calcio sérico y urinario, y de la función renal.
manera típica está bajo. Las cifras séricas de PTH son cruciales Los pacientes con hiperparatiroidismo autoinmunitario también
en la determinación de la causa de la hipocalcemia. La PTH clá deben ser examinados con regularidad por si apareciera insufi
sicamente está alta en el seudohipoparatiroidismo no tratado, a ciencia suprarrenal, así como malabsorción, hepatitis crónica, que
diferencia del hipoparatiroidismo o la disminución de magnesio. ratitis, anemia perniciosa, alopecia, vitíligo y otras complicaciones
La PTH intacta puede ser indetectable, o estar baja o normal en no endocrinas del APS-1.
pacientes con hipoparatiroidismo, según la reserva funcional de
las paratiroides. En aquellos con hiperparatiroidismo secunda
rio suscitado por defectos en la producción o la biodisponibili PUNTO DE CONTROL
dad de vitamina D, la situación clínica suele sugerir un problema
con la vitamina D (p. ej., enteritis regional, resección intestinal, 22. ¿Cuáles son las causas del hipoparatiroidismo?
enfermedad del hígado). La presencia de una concentración baja 23. ¿Cuál es el mecanismo del seudohipoparatiroidismo?
de 25-(OH)D y una PTH aumentada confirman el diagnóstico. 24. ¿Cuáles son los síntomas y signos de hipocalcemia?
La medición del magnesio sérico es el primer paso para ex 25. ¿Cómo pueden emplearse los estudios de laboratorio para
cluir decremento de magnesio como la causa de hipocalcemia y distinguir entre diversas causas de hipocalcemia?
debe formar parte de la evaluación inicial. Si el magnesio urina
rio es inapropiadamente alto en relación con el magnesio sérico,
hay pérdida renal de magnesio. Las cifras de PTH en este contexto
son de forma característica bajas o normales. Sin embargo, las con
centraciones normales de PTH son inapropiadas en presencia de CARCINOMA MEDULAR
hipocalcemia. DE LA TIROIDES
Los pacientes con hipoparatiroidismo autoinmunitario debi
do a mutaciones de AIRE pueden sospecharse en clínica al tener
al menos dos de las tres características del síndrome. Investiga Etiología
ción reciente indica que más de 95% de los pacientes con APS-1 El carcinoma medular de la glándula tiroides, una neoplasia de cé
tiene autoanticuerpos contra interferón-α o interferón-ω, y son lulas C, explica sólo 5 a 10% de las enfermedades malignas tiroi
una excelente prueba para detectar el trastorno. deas. Alrededor de 80% es esporádico y 20% es familiar, y ocurre
El diagnóstico de seudohipoparatiroidismo puede confirmarse en síndromes de MEN-2A y MEN-2B autosómicos dominantes,
al administrar PTH(1-34) humana sintética y medir las respues y en síndromes no de MEN. En casos esporádicos, el tumor ge
tas de cAMP y fosfato urinarios. Dicha maniobra está diseña neralmente es unilateral. No obstante, en formas hereditarias, los
da para probar que hay resistencia de órgano terminal a la PTH tumores a menudo son bilaterales y multifocales. Se sabe que
y para determinar si el diagnóstico es seudohipoparatiroidismo las mutaciones activadoras de la línea germinal en el protoon
tipo 1 o 2. cogén RET en el cromosoma 10 desempeñan un papel causal en
La gravedad del hipoparatiroidismo y, en consecuencia, la ne tres formas de carcinoma medular, entre ellas se cuentan casos de
cesidad de implementar terapia, pueden variar. En algunos su carcinoma medular de la tiroides aislado familiar, MEN-2A, y
jetos con reserva paratiroidea reducida, sólo las situaciones de MEN-2B. Más de la mitad de los casos de carcinoma medular de
incremento de la demanda sobre las glándulas, como embarazo la tiroides que ocurre de manera esporádica tiene una mutación
o amamantamiento, inducen hipocalcemia. En otros, la deficien somática idéntica a la que causa los síndromes familiares. Empe
cia de PTH es un trastorno sintomático crónico que exige terapia ro, dado que la mutación sólo está presente en el tumor y no en
de por vida con complementos de calcio y análogos de la vitami el DNA genómico, estos casos no son heredables.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
504 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
Patogenia nódulos fríos. En la ultrasonografía estos nódulos son sólidos.
La biopsia por aspiración con aguja fina muestra la lesión de cé
El modelo de crecimiento del carcinoma medular es lento, pero
lulas C característica con inmunotinción positiva para calcitoni
progresivo y suele haber invasión local de estructuras adyacentes.
na. La aspiración con aguja fina puede no ser diagnóstica en más
El tumor se disemina por vía hematógena, con metástasis típica
de la mitad de los individuos con carcinoma medular de la tiroides.
mente hacia ganglios linfáticos, hueso y pulmones. La progresión
La tinción para calcitonina puede mejorar la sensibilidad diag
clínica de este cáncer es variable. Aun cuando en hasta 70% de los
nóstica; sin embargo, el diagnóstico de carcinoma medular de la
pacientes puede haber metástasis tempranas hacia ganglios lin
tiroides puede no ser evidente sino hasta que se examinan lami
fáticos cervicales y mediastínicos, el tumor por lo regular todavía
nillas de especímenes de corte congelado durante intervención
se comporta de una manera indolente. En una minoría de los en
quirúrgica o, más tarde, de laminillas anatomopatológicas finales
fermos se ha notado un modelo más agresivo de crecimiento del
de la tiroides resecada. El tumor tiende a contener calcificacio
tumor. La detección temprana en individuos de alto riesgo, como
nes grandes, que pueden observarse en radiografías del cuello.
aquellos con antecedente familiar de carcinoma medular, o de
Las metástasis óseas suelen tener aspecto lítico o esclerótico y las
MEN-2A o MEN-2B, es crucial para prevenir enfermedad avan
pulmonares pueden estar rodeadas de reacciones fibróticas.
zada y metástasis a distancia. Se estima que la supervivencia ge
El análisis de laboratorio más importante en la determinación
neral es de 80% a cinco años y de 60% a 10 años. Algunos estudios
de la presencia y la extensión de carcinoma medular es la concen
sugieren que los individuos de menos de 40 años de edad en el mo
tración de calcitonina. Las cifras de calcitonina en la circulación
mento del diagnóstico pueden tener tasas de supervivencia más
están altas en la mayoría de los pacientes y las concentraciones
altas que los individuos de edad más avanzada. La mutación del
séricas se correlacionan con la carga tumoral. En la hiperplasia
protooncogén RET en el codón 918 observada en cerca de 95% de
de células C, la calcitonina basal puede o no estar alta. Con todo,
los casos de MEN-2B presagia un peor pronóstico.
estos pacientes por lo general muestran resultados anormales en
Los pacientes con MEN-2 presentan carcinoma medular a fre
pruebas de provocación. Se inyecta gluconato de calcio (2 mg/kg
cuencias de casi 100%. En la MEN-2A y la MEN-B, las lesiones
de calcio elemental) por vía intravenosa durante 1 minuto, seguido
tiroideas son malignas. La hiperplasia de células C típicamente pre
por el análogo de gastrina sintético, pentagastrina (0.5 μg/kg),
cede a la aparición de cáncer y permite la detección antes de que
durante 5 segundos. Las pruebas de provocación se basan en la
haya enfermedad maligna, y consideración de tiroidectomía pro
capacidad del calcio y la pentagastrina para estimular la libera
filáctica. Los feocromocitomas asociados con MEN-2A o MEN-
ción de calcitonina en individuos con masa aumentada de cé
2B son malignos con poca frecuencia. El hiperparatiroidismo en
lulas C producida por hiperplasia o carcinoma. Un incremento
la MEN-2A, que es poco frecuente, por lo general se debe a hiper
de la calcitonina sérica, más de dos veces la respuesta normal, se
plasia difusa y no a una enfermedad maligna de paratiroides. La
considera anormal. Hay que tener en mente que pueden ocurrir
hipercalcitoninemia crónica como resultado del tumor también
resultados falsos positivos en pruebas de provocación para calci
puede contribuir a la patogenia de la hiperplasia de las paratiroi
tonina. Las pruebas desencadenantes para detectar hiperplasia de
des. La hiperplasia paratiroidea rara vez se observa en pacientes
células C (y, por ende, aumento de la calcitonina sérica) en fami
con MEN-2B o carcinoma medular esporádico.
liares de pacientes con carcinoma medular de la tiroides han que
dado reemplazadas en su mayor parte por análisis genéticos para
Manifestaciones clínicas mutaciones de la línea germinal que se sabe que causan MEN o
El carcinoma medular esporádico ocurre con frecuencia casi igual síndromes de carcinoma medular de la tiroides familiar.
en varones y mujeres y de modo típico se encuentra después de Las mediciones seriadas de las concentraciones de calcitoni
los 50 años de edad. En la MEN-2A o la MEN-2B, el tumor su na son un parámetro útil para vigilar respuestas terapéuticas en
cede a una edad mucho más joven, a menudo durante la niñez. pacientes con carcinoma medular o para diagnosticar una re
De hecho, el carcinoma medular en un paciente de menos de 40 currencia, junto con examen clínico y procedimientos de imá
años de edad debe sugerir carcinoma medular familiar o MEN- genes. Las cifras de calcitonina por lo regular reflejan la extensión
2A o MEN-2B. El carcinoma medular puede presentarse como de la enfermedad. Si el tumor se hace menos diferenciado, las
un nódulo único o como múltiples nódulos tiroideos. Los sujetos concentraciones de calcitonina quizá ya no reflejen la carga tu
con carcinoma medular esporádico a menudo tienen linfadeno moral. Otro marcador tumoral útil para carcinoma medular es el
patía cervical palpable. antígeno carcinoembrionario (CEA), el cual suele estar alto en
Puesto que las células C son neuroendocrinas, estos tumores pacientes con carcinoma medular y se halla presente en todos los
tienen la capacidad de liberar calcitonina y otras hormonas, estadios de la enfermedad. Los aumentos rápidos del CEA predi
como prostaglandinas, serotonina, adrenocorticotropina, soma cen peor evolución clínica.
tostatina y péptido relacionado con el gen de la calcitonina. La se La intervención quirúrgica es la piedra angular de la terapia
rotonina, calcitonina o prostaglandinas han quedado implicadas para pacientes con carcinoma medular de la tiroides. Se reco
en la patogenia de la diarrea secretora que se observa en casi 25% mienda tiroidectomía total porque los tumores a menudo son
de aquéllos con carcinoma medular. Si hay diarrea, por lo general multicéntricos. Los pacientes deben vigilarse por tiempo indefi
indica carga tumoral grande o enfermedad metastásica. Los en nido por si hubiera recurrencias porque estos tumores pueden
fermos también pueden tener rubor, que se ha atribuido a la pro ser muy indolentes. También se requiere vigilancia por tiempo
ducción por el tumor de sustancia P o péptido relacionado con el indefinido porque los individuos con probable carcinoma me
gen de la calcitonina, de los cuales ambos son vasodilatadores. dular de la tiroides familiar han presentado feocromocitoma o
En pacientes con sospecha de carcinoma medular, una gam hiperparatiroidismo mucho tiempo después de su diagnóstico
magrafía tiroidea con radionúclido puede demostrar uno o más de carcinoma medular de la tiroides y, así, finalmente se encuen
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 505
tra que tienen MEN-2A en lugar de carcinoma medular de la ti Nutrición y actividad
física adecuadas Menopausia
roides familiar. En todos los pacientes con carcinoma medular de
la tiroides, sea familiar o esporádico, deben practicarse pruebas
para mutaciones del oncogén RET; tales pruebas se hallan dispo
Masa ósea
nibles en el comercio y han suplantado a la prueba desencade
nante con calcitonina. Se ha encontrado que más de 95% de los
Nutrición y actividad
pacientes con MEN-2 alberga mutaciones de RET. También deben física inadecuadas
efectuarse pruebas en casos esporádicos de carcinoma medular
de la tiroides para detectar la aparición de una nueva mutación res
pecto a la cual puede investigarse a otros miembros de la familia. 0 10 20 30 40 50 60 70
Las pruebas de DNA efectuadas correctamente son en esencia Edad
inequívocas en la predicción del estado de portador de gen, y FIGURA 17–19 Masa ósea en mujeres en función de la edad, que de
pueden usarse prospectivamente para recomendar tiroidectomía muestra el efecto potencial de la nutrición y actividad física subóptimas
profiláctica en pacientes jóvenes y niños con MEN-2 antes de durante el periodo crucial de acumulación de hueso durante la niñez y la
que aparezca hiperplasia de células C o carcinoma manifiesto. adolescencia. (Redibujada, con autorización, de Heaney RP et al. Peak bone mass. Os
En pacientes con MEN-2A o MEN-2B, incluso en ausencia de teo Int. 2000;11:985.)
síntomas, deben practicarse pruebas de detección para la posi
bilidad de feocromocitoma, mientras que sólo los pacientes con
MEN-2A necesitan pruebas de detección para hiperparatiroidis ejercicio con carga de peso y la exposición a esteroides sexuales
mo antes de intervención quirúrgica de la tiroides. Estos análisis pueden tener repercusiones negativas sobre la adquisición de su
incluyen la cuantificación del calcio y la PTH séricos, junto con ficiente masa ósea máxima. Una vez completado el crecimien
metanefrinas fraccionadas plasmáticas, y análisis bioquímicos o to óseo, la masa ósea está determinada por la magnitud de la
estudios de imágenes adicionales según sea necesario. Los feocro masa ósea máxima que se alcanzó y por el índice de pérdida sub
mocitomas pueden ser silenciosos en clínica en el momento en siguiente. La genética es muy importante en la determinación de
que se diagnostica carcinoma medular, y deben extirparse antes la masa ósea. Desde hace mucho tiempo se ha reconocido que los
de tiroidectomía para evitar complicaciones quirúrgicas en poten individuos de raza negra tienen mayor masa ósea máxima que
cia graves por secreción descontrolada de catecolamina. En pre los de raza blanca o los asiáticos y están relativamente protegidos
sencia de hiperparatiroidismo, debe tratarse quirúrgicamente en contra osteoporosis. Ahora parece ser que, dentro de la pobla
el momento de tiroidectomía a fin de evitar una segunda opera ción caucásica, más de la mitad de la variación de la masa ósea
ción en el cuello (capítulo 12). está determinada por mecanismos genéticos. Aun así, varios fac
tores hormonales y ambientales suelen disminuir la masa ósea
PUNTO DE CONTROL máxima determinada genéticamente o acelerar la pérdida de mi
neral óseo y, de este modo, representan importantes factores de
26. ¿De qué manera puede hacer el diagnóstico de carcinoma
riesgo para osteoporosis (figura 17-19, cuadro 17-10). El factor
medular de la tiroides?
causal de mayor importancia en la osteoporosis es la deficiencia
27. ¿Cuál es el tratamiento para carcinoma medular?
de esteroides sexuales. La deficiencia de estrógeno que sucede des
28. ¿Cuáles pacientes tienen riesgo alto de carcinoma medular?
pués de la menopausia acelera la pérdida de masa ósea; las pos
menopáusicas tienen de modo constante masa ósea más baja que
los varones y una mejor incidencia de fracturas osteoporóticas.
En lo que se refiere al remodelado óseo en varones, la testostero
OSTEOPOROSIS na desempeña algunas de las mismas funciones que el estrógeno
en mujeres, pero el estradiol generado por la aromatización peri
férica de testosterona es el esteroide gonadal crucial que media
Etiología el desarrollo de la masa ósea masculina y la preservación de la
La osteoporosis se define como masa ósea baja. El hueso tiene com misma. Los varones hipogonadales experimentan pérdida ósea
posición normal, pero está disminuido en cantidad. La masa ósea acelerada; quienes están recibiendo terapia de privación de an
se acumula con rapidez durante toda la niñez y con mucha rapi drógenos por cáncer de próstata tienen incremento del riesgo de
dez en la adolescencia; la mitad de la densidad mineral ósea del pérdida ósea y fractura. Otro factor importante para la pérdida
adulto se logra en los años de la adolescencia (figura 17- 19). ósea es el uso de corticosteroides o el exceso de cortisol endóge
La masa ósea máxima se alcanza en la tercera década de la no en el síndrome de Cushing. La osteoporosis inducida por glu
vida. A continuación la masa ósea permanece estable de manera cocorticoides es una de las complicaciones más devastadoras de
relativa durante los años de la adultez, lo cual va seguido por la terapia crónica con estos agentes. Varios medicamentos, entre
pérdida rápida de hueso en mujeres en el momento de la meno ellos hormona tiroidea, anticonvulsivos y terapia crónica con he
pausia. En las etapas más tardías de la vida, tanto los varones parina, inmovilización, abuso del consumo de alcohol y tabaquis
como las mujeres siguen perdiendo hueso, aunque a un índice mo crónicos, también son factores de riesgo para osteoporosis.
más lento que el que se observa en el momento de la menopausia. Incluso la dieta es importante. Como se comenta más adelante,
El logro de una masa ósea máxima depende de nutrición una ingestión adecuada de calcio y vitamina D es necesaria para
óptima, actividad física, salud general y exposición hormonal construir masa ósea máxima óptima, y para minimizar el índi
durante la niñez y la adolescencia. La nutrición inadecuada, el ce de pérdida. Además otros factores de la dieta pueden ser im
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
506 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
CUADRO 17–10 Causas de osteoporosis incremento de la excreción urinaria de calcio y de productos de
desintegración del colágeno tipo 1 (p. ej., telopéptidos N y C), y
Osteoporosis primaria los números de osteoclastos y las superficies de resorción están
Envejecimiento aumentados. La tasa de formación de hueso también está aumen
Juvenil tada, con un incremento de la fosfatasa alcalina sérica y la con
centración sérica de la proteína de la matriz ósea osteocalcina, de
Idiopática (adultos jóvenes)
los cuales ambos reflejan actividad osteoblástica aumentada. La
Enfermedades del tejido conjuntivo formación de hueso, aunque está aumentada, no corre parejas
Osteogénesis imperfecta con la resorción ósea, y hay una pérdida neta de masa ósea en el
Homocistinuria momento de la menopausia. Ese estado de recambio alto es el re
sultado directo de deficiencia de estrógeno y puede revertirse
Síndrome de Ehlers-Danlos
mediante terapia de reemplazo de estrógeno.
Síndrome de Marfan La fase acelerada de la pérdida de hueso con deficiencia de es
Inducida por fármacos trógeno empieza de manera inmediata después de la menopausia
Corticosteroides (natural o quirúrgica). Es más evidente en el hueso trabecular, el
compartimiento que se remodela con mayor rapidez. Hasta 5 a
Alcohol
10% del mineral óseo trabecular se pierde cada año en posme
Hormona tiroidea nopáusicas y las fracturas osteoporóticas en mujeres que se en
Heparina crónica cuentran en etapas tempranas después de la menopausia suelen
Anticonvulsivos ocurrir en la columna vertebral, un sitio de hueso principalmen
te trabecular. Luego de 5 a 15 años, el índice de pérdida de hueso
Hematológicas
se hace más lento, de modo que después de los 65 años de edad
Mieloma múltiple los índices son similares en ambos sexos.
Mastocitosis sistémica La base celular para la activación de la resorción ósea en el es
Inmovilización tado de deficiencia de estrógeno no se ha entendido del todo, pero
implica liberación aumentada de citocinas como la interleucina-6
Endocrinas
de células en el microambiente óseo en la deficiencia de estróge
Hipogonadismo nos. Dichas citocinas aumentan la expresión de RANK-L y dismi
Hipercortisolismo nuyen la expresión de OPG en células del estroma y osteoblastos.
Hipertiroidismo Estos cambios críticos juntos promueven un desequilibrio en el
remodelado óseo que favorece la osteogénesis aumentada y la re
Hiperparatiroidismo
sorción ósea.
Trastornos gastrointestinales La patogenia de la pérdida de hueso relacionada con la edad
Gastrectomía subtotal está menos bien definida. La masa ósea es relativamente estable
Síndromes de malabsorción durante la cuarta y quinta décadas de la vida, la pérdida de hueso
se acelera durante 5 a 10 años en las mujeres en el momento de la
Ictericia obstructiva
menopausia y después continúa durante toda la vida a una tasa
Cirrosis biliar más lenta que es similar en ambos sexos.
Un factor importante en la patogenia de la pérdida de hueso
relacionada con la edad es una deficiencia relativa de calcio y
portantes. La osteoporosis es más prevaleciente en sociedades 1,25-(OH)2D en la dieta. La capacidad del intestino para absor
occidentales, y se ha especulado que su ingestión aumentada de ber calcio disminuye con la edad; puesto que las pérdidas renales
proteína y cloruro de sodio en la dieta, junto con ingestión sub de calcio son obligatorias, una reducción de la eficiencia de la ab
óptima de potasio o factores relacionados, pueden predisponer sorción de calcio significa que la ingestión de calcio en la dieta se
a osteoporosis, quizá por aumento de la pérdida de calcio en la debe incrementar para prevenir balance negativo de calcio. Se es
orina. Muchos otros trastornos que afectan los sistemas GI, he tima que después de los 65 años de edad se necesitan alrededor
matológico y de tejido conjuntivo pueden contribuir a la apari de 1 200 mg/día de calcio elemental para mantener el balance de
ción de osteoporosis (cuadro 17-10). calcio (cuadro 17-11). Las mujeres estadounidenses en este gru
po de edad típicamente ingieren 500 a 600 mg de calcio al día; las
ingestiones de calcio en varones son un poco más altas. Además,
Patogenia los individuos de edad más avanzada pueden tener deficiencia de
Puesto que el remodelado óseo comprende resorción acoplada de vitamina D, lo que altera más su capacidad para absorber calcio.
hueso por osteoclastos y depósito de hueso nuevo por osteoblas La 25-(OH)D muestra variabilidad con las estaciones del año; son
tos, la pérdida de hueso podría producirse por resorción ósea au evidentes cifras más bajas e hiperparatiroidismo secundario leve
mentada, formación de hueso disminuida, o una combinación de al final del invierno.
ambos procesos. Los individuos más jóvenes con masa ósea baja La concentración de PTH aumenta con la edad debido a cam
típicamente han experimentado formación de hueso baja y acumu bios en múltiples sistemas con el envejecimiento. Con la edad, hay
lación insuficiente de hueso, mientras que la osteoporosis pos un decremento de la masa de tejido renal funcionante, que po
menopáusica es la consecuencia de resorción ósea acelerada. Hay dría llevar a síntesis renal disminuida de 1,25-(OH)2D, que libe
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 507
CUADRO 17–11 Ingestiones recomendadas de las tasas de formación de hueso y de la concentración sérica de
de calcio y vitamina D osteocalcina. Es probable que los glucocorticoides produzcan un
síndrome de osteoporosis devastador debido a la pérdida rápida
Edad Calcio (mg/dl) Vitamina D (IU/día) de hueso que sobreviene por franca depresión de la formación de
0 a 6 meses 200 400 hueso en presencia de resorción ósea normal o incluso aumenta
da. Además, los glucocorticoides disminuyen la absorción intes
6 a 12 meses 260 400
tinal de calcio y vitamina D, e incrementan las pérdidas de calcio
1 a 3 años 700 600 en la orina.
4 a 8 años 1 000 600 La forma de osteoporosis secundaria vinculada con inmoviliza
ción es otro ejemplo de un estado de resorción con desacoplamien
9 a 13 años 1 300 600
to notorio de la resorción y formación de hueso, y se caracteriza
14 a 18 años 1 300 600 por hipercalciuria y supresión de la PTH. Cuando los individuos
19 a 30 años 1 000 600 que tienen un estado preexistente alto de remodelado óseo (p.
ej., adolescentes y pacientes con hipertiroidismo o enfermedad
31 a 50 años 1 000 600
de Paget) quedan inmovilizados, la resorción ósea puede acele
51 a 70 años (mujeres) 1 200 600 rarse lo suficiente como para producir hipercalcemia.
51 a 70 años (varones) 1 000 600
Más de 70 años 1 200 800 Manifestaciones clínicas
Clave: IU, unidades internacionales. La osteoporosis es asintomática hasta que ocasiona fracturas y
deformidad. Las fracturas osteoporóticas típicas ocurren en la
columna vertebral, cadera y muñeca (fractura de Colles). En mu
raría directamente la secreción de PTH de su inhibición normal jeres, la incidencia de fracturas de muñeca aumenta en la me
por la 1,25-(OH)2D. La concentración disminuida de 1,25-(OH)2D nopausia y luego permanece relativamente estable a este índice
también reduciría la absorción de calcio, lo que exacerbaría una incrementado con la edad. La incidencia de fracturas de la cadera
incapacidad intrínseca del intestino en envejecimiento para ab y de vértebras aumenta con rapidez con el envejecimiento tanto
sorber calcio de manera normal. A continuación sobrevendría en varones como en mujeres (figura 17-20). Puede haber aplas
hiperparatiroidismo secundario por los efectos dobles de la defi tamiento de los cuerpos vertebrales, lo que se traduce en pérdida
ciencia de 1,25-(OH)2D sobre las paratiroides y el intestino. Más de estatura, o los cuerpos vertebrales pueden adoptar forma de
aún, la capacidad de respuesta de las paratiroides a inhibición cuña en dirección anterior, lo que origina pérdida de estatura y
por calcio se reduce con el envejecimiento. Así, el hiperparatiroi cifosis. La cifosis dorsal de ancianas (“giba de viuda”) se produce
dismo propio de esta edad puede producirse por los efectos com porque múltiples vértebras torácicas adoptan forma de cuña. Las
binados de la edad sobre los riñones, intestino y paratiroides. fracturas espinales pueden ser agudas y dolorosas o suceder de
Un complemento de la dieta con una cantidad adecuada de vi modo gradual y sólo manifestarse como cifosis o pérdida de es
tamina D disminuye el índice de pérdida de hueso vinculado con tatura.
la edad y protege contra fracturas. Esto sugiere que el decremen La complicación de la osteoporosis con la morbilidad y mor
to de la absorción del calcio y el hiperparatiroidismo secundario, talidad más altas es la fractura de cadera. Las fracturas de cadera
tienen importancia en la patogenia de la osteoporosis en ancia típicamente ocurren en ancianos; hay un aumento agudo de la
nos. No obstante, los complementos de calcio y vitamina D solos incidencia en ambos sexos después de los 80 años de edad. Esto
no aminoran por completo el riesgo de fractura. se debe a diversos factores, entre ellos la tendencia a una tasa
En la osteoporosis secundaria asociada con administración de más lenta de pérdida del hueso cortical que constituye la cadera
glucocorticoides o con alcoholismo, hay una notoria reducción en comparación con el hueso predominantemente trabecular de
4 000 Varones Mujeres
Incidencia/100 000 personas-año
3 000
Cadera
2 000 Cadera Vértebras
Vértebras
1 000
Colles Colles
35 45 55 65 75 ≥85 35 45 55 65 75 ≥85
Edad, años
FIGURA 17–20 Incidencias específicas para edad de fracturas de muñeca, cadera y vértebras en varones y mujeres, derivadas de datos de Roches
ter, Minnesota. (Redibujada, con autorización, de Cooper C et al. Epidemiology of osteoporosis. Trends Endo Metab. 1992;3:224.)
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
508 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
la columna vertebral, así como función motora y visual dismi Los individuos que tienen riesgo de osteoporosis se benefician
nuida con el envejecimiento que da lugar a caídas más frecuen a partir de una ingestión total de calcio de alrededor de 1 200 a
tes. Los costos personales y sociales de la fractura de cadera son 1 500 mg/día. Esto puede lograrse con productos lácteos u otros
enormes. Una tercera parte de las mujeres estadounidenses que alimentos ricos en calcio, con alimentos enriquecidos con calcio,
sobreviven más allá de los 80 años de edad sufrirá una fractura de o con un complemento de calcio, como carbonato de calcio o ci
cadera. La mortalidad a seis meses es de casi 20%, gran parte de la trato de calcio. La vitamina D debe proporcionarse en dosis apro
cual se produce por complicaciones de la inmovilización de per piadas para la edad (600 a 800 IU/día). Persisten las controversias
sonas frágiles en una cama de hospital. Las complicaciones son respecto a cuál es la concentración sérica de 25-(OH)D que re
embolia pulmonar y neumonía. Alrededor de la mitad de los an presenta insuficiencia; el Institute of Medicine recomienda una
cianos con una fractura de cadera nunca volverá a caminar de ma cifra de 20 ng/ml, mientras que muchos expertos en los aspectos
nera libre. Los costos a largo plazo del cuidado crónico de estas metabólicos del hueso recomiendan una cifra de más de 32 ng/ml.
personas son una importante preocupación social. El cuadro 17-11 presenta las ingestiones recomendadas en la ac
La osteoporosis en ocasiones se diagnostica con radiografías, tualidad para calcio y vitamina D. Los complementos de calcio en
pero en general éstas constituyen un recurso diagnóstico poco idó individuos más jóvenes pueden aumentar la masa ósea máxima
neo. En una radiografía de tórax pasará inadvertido 30 a 50% de y reducir la pérdida de hueso premenopáusica, pero no se ha de
los casos de osteoporosis espinal y, si está demasiado penetrada, terminado su función óptima en este grupo de edad. El reempla
puede llevar al diagnóstico de osteoporosis en una persona con una zo de estrógeno aminora la pérdida de hueso, alivia los bochornos
masa ósea normal. La mejor manera de diagnosticar osteoporo luego de la menopausia y disminuye el riesgo de fractura. Exige
sis es al medir la densidad mineral ósea mediante absorciometría el uso concomitante de progestinas en mujeres en quienes no se
radiográfica de doble energía (DXA). La técnica es exacta, rápi ha practicado una histerectomía con el objeto de prevenir carci
da y poco costosa. La relación entre la densidad mineral ósea y el noma endometrial e incrementa también el riesgo de cáncer ma
riesgo de fractura es continua (esto es, mientras más baja es la mario, apoplejía, infarto de miocardio y tromboembolia venosa.
densidad mineral ósea, más alto es el riesgo de fractura). La Or El perfil de los efectos secundarios de los estrógenos ha limitado
ganización Mundial de la Salud (OMS) ha definido a la osteo su uso a la terapia a corto plazo en el momento de la menopau
porosis como un valor de densidad mineral ósea 2.5 desviaciones sia, típicamente en mujeres que sufren bochornos. Otros agentes
estándar o más por debajo del valor normal en un adulto joven antirresorción disponibles para el tratamiento de osteoporosis son
(es decir, una puntuación T de -2.5 o menos). Este límite se selec alendronato, risedronato, ibandronato, ácido zoledrónico, calci
cionó con base en la observación de que 16% de las caucásicas pos tonina, raloxifeno y denosumab. Los primeros cuatro fármacos
menopáusicas a la edad de 50 años tendrá valores de densidad son bisfosfonatos que inhiben de modo directo la resorción ósea
ósea en el cuello femoral por debajo de -2.5, y esta población osteoclástica. Administrada en dosis terapéuticas, la calcitonina
tiene un riesgo durante toda la vida de 16% de fractura de cade disminuye la resorción ósea y puede proteger contra la pérdida
ra. No obstante, es necesario recordar que no hay umbral a este de hueso y fracturas vertebrales. El raloxifeno, un modulador se
valor, y que las mediciones de la densidad mineral ósea necesi lectivo de la respuesta a estrógenos, inhibe la resorción ósea como
tan interpretarse a la luz de otros factores de riesgo para fractura, lo hace el estrógeno. El raloxifeno no induce cambios endome
como edad y propensión a caídas. La OMS creó de modo recien triales y tiene acciones antagonistas de estrógeno en células de la
te un algoritmo para el cálculo del riesgo absoluto de fractura a mama que parecen reducir la incidencia de carcinoma mamario
10 años (denominado FRAX). El algoritmo incorporó valores de en posmenopáusicas. El denosumab es un anticuerpo monoclonal
densidad mineral ósea en la cadera y varios factores de riesgo contra el ligando de RANK, e inhibe el desarrollo de osteoclastos
para determinar la probabilidad de un individuo de una fractu y la activación de los mismos. El único agente disponible hoy día
ra osteoporótica de cadera importante a 10 años. La URL www. que puede estimular la formación de hueso es la hormona para
shef.ac.uk/FRAX/ proporciona acceso al calculador de riesgo abso tiroidea (PTH1-34) (teriparatida). En contraste con la resorción
luto de fractura, de la OMS. Este recurso es útil para determinar ósea causada por aumentos continuos de la PTH como sucede en
la necesidad de tratamiento, además de los valores de densidad el hiperparatiroidismo, una inyección diaria única de PTH es
ósea en sí mismos. timula la formación de hueso y, en menor grado, la resorción ósea,
Además, es importante percatarse de que no todo el riesgo de lo que da lugar a ganancias netas de la densidad ósea y disminu
fractura se observa en mediciones de la densidad mineral ósea ción del riesgo de fractura.
porque la fuerza del hueso también está en función de la calidad
del mismo. Dicha calidad, determinada por la microestructura
de un hueso, su fuerza mecánica, sus propiedades materiales y su PUNTO DE CONTROL
capacidad para soportar la tensión, puede ser considerablemente
distinta en dos individuos que tienen la misma densidad mineral 29. ¿Cuál es la importancia relativa de factores hereditarios en
ósea. Se están investigando de modo activo técnicas para evaluar contraposición con ambientales u hormonales en la contri
la calidad ósea de manera no invasiva. bución a osteoporosis?
Los ancianos con osteoporosis es poco probable que sufran una 30. ¿Cuáles son los factores de riesgo para la osteoporosis?
fractura de cadera a menos que tengan una caída. Los factores de 31. ¿Cuáles son los síntomas y signos de la osteoporosis?
riesgo para caída son debilidad muscular, visión alterada, altera 32. ¿Cuáles son los factores de riesgo para fractura en un pa
ción del equilibrio, uso de sedantes y factores ambientales. Por ciente con osteoporosis?
ende, las estrategias para prevenir caídas son parte importante 33. ¿Qué tratamientos pueden prevenir la pérdida de hueso?
del método para abordar al paciente que padece osteoporosis.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 509
OSTEOMALACIA a grupos étnicos de piel oscura son en especial vulnerables por
que tienen menos síntesis cutánea de vitamina D en respuesta
a la luz solar. La leche enriquecida es la principal fuente de vita
Etiología mina D en los alimentos, pero a 100 IU/taza de leche, puede ser
La osteomalacia se define como un defecto de la mineralización difícil lograr las 600 a 800 IU/día recomendadas de vitamina D
del hueso. Cuando ocurre en jóvenes, también afecta la mine para adultos. Algunos cereales y otros alimentos se han enriqueci
ralización de cartílago en la placa de crecimiento, trastorno lla do con vitamina D. Además de ingestión insuficiente, la deficien
mado raquitismo. La osteomalacia puede producirse por una cia de vitamina D puede producirse por malabsorción de esta
deficiencia de vitamina D o de fosfato, una deficiencia heredi vitamina liposoluble. El raquitismo grave también sucede como
taria en la fosfatasa alcalina (hipofosfatasia) o agentes que tie parte de tres trastornos hereditarios raros de la acción de la vi
nen efectos adversos sobre el hueso (cuadro 17-12). De modo tamina D: deficiencia de 1α-hidroxilasa renal, en la cual la vita
sorprendente, es raro que la deficiencia de calcio en la dieta dé mina D no se convierte en 1,25-(OH)2D; receptores de vitamina
por resultado osteomalacia, aunque se han informado algunos mutantes con actividad reducida y producción excesiva de una
casos. proteína de unión a elemento de respuesta a hormona que inter
La deficiencia de vitamina D se está haciendo más frecuen fiere con la activación (por el heterodímero receptor de vitamina
te en EUA debido a decremento de la exposición a la luz solar, D-receptor de ácido retinoico) de elementos de respuesta a vita
incremento del uso de pantallas protectoras solares y fuentes de mina D en genes.
vitamina D limitadas en la dieta. Los individuos que pertenecen La deficiencia de fosfato con osteomalacia por lo general se
produce por pérdida renal de fosfato hereditaria o adquirida.
Tres formas hereditarias de pérdida renal de fosfato son el ra
CUADRO 17–12 Causas de osteomalacia quitismo hipofosfatémico, ligado a X (XLH), autosómico domi
nante o autosómico recesivo. La osteomalacia y la hipofosfatemia
Deficiencia de vitamina D también pueden producirse por tumores que de manera carac
terística son de origen mesenquimatoso y a menudo están situa
Nutricional
dos en la región de la cabeza y el cuello. Muchos de estos tumores
Malabsorción sintetizan en exceso FGF-23 (véase antes) e inducen pérdida re
nal de fosfato y concentraciones bajas de 1,25-(OH)2D, lo que al
Raquitismo dependiente de vitamina D hereditario
final lleva a osteomalacia. El gen FGF-23 está mutado en fami
Deficiencia de 1α-hidroxilasa renal lias con raquitismo hipofosfatémico autosómico dominante. Las
familias con raquitismo hipofosfatémico ligado a X tienen mu
Raquitismo resistente a vitamina D hereditario (falta del receptor taciones en el gen PHEX, que codifica para una endopeptida
de vitamina D o defectos del mismo)
sa, PHEX. Esa endopeptidasa está involucrada en la producción
Deficiencia de fosfato de FGF-23 y la degradación del mismo. En el raquitismo hipo
fosfatémico ligado a X, la concentración de FGF-23 está alta, y
Pérdida renal de fosfato
parece ser la causa del fenotipo hipofosfatémico, aunque que
Hipofosfatemia ligada a X da por dilucidar el papel exacto de PHEX en el metabolismo del
FGF-23.
Raquitismo hipofosfatémico autosómico dominante
Raquitismo hipofosfatémico autosómico recesivo
Patogenia
Raquitismo hipofosfatémico hereditario con hipercalciuria La deficiencia de vitamina D causa osteomalacia en etapas. En la
Síndrome de Fanconi etapa temprana, la absorción disminuida de calcio suscita hiper
paratiroidismo secundario, lo que impide hipocalcemia a costas
Acidosis tubular renal (tipo II) de incremento de la excreción renal de fosfato e hipofosfatemia.
Osteomalacia inducida por tumor (adquirida, asociada con tumores
En etapas más tardías, sobreviene hipocalcemia, y la hipofosfate
mesenquimatosos y cáncer de próstata) mia progresa debido a efectos combinados de decremento de la
absorción y la acción fosfatúrica de la PTH. El aporte inadecua
Antiácidos de unión a fosfato do de minerales al hueso (tal vez acoplado con la falta de efectos
Fosfatasa alcalina deficiente: hipofosfatasia hereditaria directos de la vitamina D sobre el hueso) altera la mineralización
de la matriz ósea. Dado que los osteoblastos siguen sintetizando
Toxicidad farmacológica matriz ósea, se acumula matriz u osteoide no mineralizado en
Fluoruro
superficies formadoras de hueso.
Aluminio (enfermedad renal crónica)
Manifestaciones clínicas
Etidronato disódico
Los pacientes con osteomalacia tienen dolor óseo, debilidad
Antiácidos de unión a fosfato muscular y una marcha de pato. Los estudios radiográficos sue
len revelar masa ósea reducida, detectable tanto con radiografías
Enfermedad renal crónica
como con densitometría ósea. Sin embargo, el dato característico
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
510 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
del trastorno es la seudofractura: resorción ósea local que tiene pecto radiográfico de raquitismo o seudofracturas, o una biopsia
el aspecto de una fractura no desplazada, de forma clásica en ósea característica. Si se obtiene biopsia de hueso para histomor
las ramas del pubis, las clavículas o los omóplatos. En niños con fometría cuantitativa, se encuentran costuras osteoides engrosadas
raquitismo los huesos de las piernas están arqueados (osteoma y una disminución del índice de mineralización. El tratamiento
lacia significa “ablandamiento de huesos”), las uniones costo con vitamina D o el reemplazo enérgico de fosfato en aquellos
condrales están agrandadas (“rosario raquítico”), y las placas de pacientes con pérdida renal de fosfato revertirá la osteomalacia o
crecimiento están ampliadas y son irregulares, lo cual refleja el curará el raquitismo. En la enfermedad renal, y en los trastornos
incremento de cartílago no mineralizado que se flexiona bajo mediados por FGF-23, también debe proporcionarse calcitriol
el peso del niño, lo cual da lugar al arqueo. Desde el punto de para mineralizar el hueso, porque en estos trastornos no hay sín
vista bioquímico, los datos característicos de la osteomalacia con tesis endógena (enfermedad renal) o está suprimida (trastornos
deficiencia de vitamina D son hipofosfatemia, hiperparatiroidis del FGF-23).
mo, hipocalcemia variable y disminuciones notorias del calcio
urinario a menos de 50 mg/día. Hay decremento de la concentra
ción de 25-(OH)D, indicativo de reducción de las reservas corpo PUNTO DE CONTROL
rales de vitamina D. En la deficiencia de vitamina D y otras formas
de osteomalacia, se observa incremento de las cifras de fosfatasa 34. ¿Cuáles son las causas de osteomalacia?
alcalina. 35. ¿Cuáles son las dos etapas en las que la deficiencia de vita
Si bien el trastorno puede sospecharse con base en los datos mina D causa osteomalacia?
clínicos, y los cambios bioquímicos que se resumieron antes son 36. ¿Cuáles son los síntomas y signos de osteomalacia?
confirmadores, un diagnóstico firme de osteomalacia exige el as
ESTUDIOS DE CASO
Yeong Kwok, MD
(Véanse las respuestas en el capítulo 25, pág. 729.)
CASO 83
Una mujer de 56 años de edad acude con su médico de aten Preguntas
ción primaria por fatiga, debilidad y dolor óseo difuso, progre
A. ¿Cuáles son algunas causas frecuentes de hipercalcemia? ¿Cuál
sivos. Le comenta que los síntomas han estado empeorando
sospecha en esta paciente y por qué?
en el transcurso de los últimos dos meses. En el historial mé
B. ¿Cuál es la patogenia del hiperparatiroidismo primario? ¿Qué
dico resaltan hipertensión bien controlada y cálculos renales
genes han quedado implicados?
recurrentes. El examen físico no revela datos notorios. Una con
C. ¿Cómo podría diagnosticar hiperparatiroidismo primario?
centración sérica de calcio está alta.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 511
CASO 84
Una mujer de 40 años de edad acude a la clínica para comentar Preguntas
algunas anormalidades inesperadas (aumento leve de las cifras
A. ¿Cuál es el diagnóstico probable en esta paciente?
séricas de calcio), en los análisis de laboratorio practicados como
B. ¿Cuál es la fisiopatología subyacente de este trastorno y cómo
parte de un examen solicitado por la compañía que le otorga
lleva esto al calcio sérico alto?
su seguro de vida. La mujer ha estado sana, sin problemas médi
cos; se siente bien y niega fatiga o dolor. No toma medicamen
tos ni complementos de la dieta. No hay antecedentes familiares
significativos. El examen físico no revela datos notorios. La re
petición de los análisis de laboratorio confirma incremento leve
de la concentración sérica de calcio, pero también muestra ci
fras séricas normales de fósforo, hormona paratiroidea (PTH)
intacta y 1,25-(OH)2D. En una prueba de calcio en orina de 24
horas se informa un resultado bajo, de 60 mg/24 horas.
CASO 85
Un varón de 69 años de edad se presenta con su médico de Preguntas
atención primaria quejándose de fatiga, náuseas, debilidad y
A. ¿Qué tumores suelen producir hipercalcemia? ¿Cuál es el más
dolor óseo difuso. Declara que los síntomas han estado empeo
probable en este paciente?
rando de manera progresiva en el transcurso de los últimos dos
B. ¿Qué cifras séricas de PTH esperaría? ¿De PTHrP sérico? ¿Por
meses. Además, ha notado pérdida de peso alrededor de 6.8 kg
qué?
(15 libras) en el mismo lapso; su esposa, quien lo acompañó,
C. ¿De qué modo la secreción de PTHrP ocasiona hipercalcemia?
señaló que él parece cada vez más desorientado. Los datos que
destacan en su historial médico son hipertensión bien contro
lada y enfermedad pulmonar obstructiva crónica (EPOC). Tiene
un antecedente de tabaquismo de 100 cajetillas por año. En el
examen físico el paciente tiene aspecto de enfermedad crónica
y está delgado. Los signos vitales notorios son presión arterial
de 120/85 mmHg y frecuencia cardiaca de 98 latidos/minuto,
frecuencia respiratoria de 16/minuto. Los pulmones tienen una
fase espiratoria aumentada, con sibilancias espiratorias leves.
Tiene decremento de los ruidos respiratorios en la base izquier
da. El resto del examen no revela datos notorios. Se encuentra
gran incremento de la concentración sérica de calcio y se sos
pecha hipercalcemia de enfermedad maligna.
CASO 86
Una mujer de 32 años de edad acude a la sala de urgencias por Preguntas
espasmos involuntarios en las manos. Declara que mientras es
A. ¿Cuál es el mecanismo por el que la operación de la tiroides pue
taba doblando ropa lavada, tuvo un espasmo intenso y repen
de traducirse en hipocalcemia? ¿Cuál es la causa probable por
tino en la mano derecha, con flexión de los dedos. El espasmo
la que la paciente sólo ahora presenta síntomas?
fue muy doloroso y duró varios minutos; se resolvió de manera
B. ¿En qué consiste el signo de Chvostek? ¿El signo de Trousseau?
espontánea. La paciente tiene seis meses de embarazo; su his
¿Qué representa cada uno?
torial médico por lo demás es notable por estado de tumor ti
C. ¿Qué cifras séricas de fosfato esperaría que tuviera esta pacien
roideo después de tiroidectomía tres años atrás. Está tomando
te? ¿De PTH sérica? ¿Por qué?
hormona tiroidea sintética y un polivitamínico prenatal. No tie
ne antecedentes familiares notorios. En el examen físico hay
signos de Chvostek y Trousseau. El examen por lo demás re
sulta normal. La concentración sérica de calcio es baja. Se sos
pecha hipoparatiroidismo como complicación de intervención
quirúrgica tiroidea.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
512 CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo
CASO 87
Una mujer de 23 años de edad acude con su médico de aten Preguntas
ción primaria quejándose de diarrea profusa y acuosa, que ha
A. ¿Cuál es la causa de la diarrea de esta paciente?, ¿qué provoca
estado empeorando de modo progresivo durante los últimos
el rubor?
dos meses. No ha tenido evacuaciones sanguinolentas ni de
B. ¿De qué manera diagnosticaría carcinoma medular de la tiroi
color negro. La enfermedad no empeora con la alimentación y
des?
no muestra vínculo con fiebre, escalofríos, sudores, náuseas ni
C. ¿Qué otras pruebas desearía solicitar?, ¿por qué?
vómitos. En la revisión de los sistemas, la mujer nota una pér
dida de peso de 2.3 kg (5 libras) durante los últimos tres meses.
También nota rubor ocasional; niega antecedentes familiares
importantes. En el examen físico, la paciente es una mujer de
raza blanca, delgada, que no muestra zozobra aguda. Está afe
bril, con presión arterial de 100/60 mmHg, frecuencia cardiaca
de 100 latidos/minuto y frecuencia respiratoria de 14/minuto.
El examen de la cabeza resulta normal, el del cuello revela nó
dulos duros bilaterales en la tiroides: un nódulo de 2 cm en el
polo superior derecho y uno de 1.5 cm en el polo superior iz
quierdo. Tiene un ganglio linfático de 1 cm, firme, en la cade
na cervical anterior derecha. Los campos pulmonares están
despejados. El examen del corazón muestra taquicardia leve,
con ritmo regular y sin ruidos adicionales. El abdomen tiene
ruidos intestinales hiperactivos y no está distendido, está blan
do, no está hipersensible y no muestra masas. El examen de la
piel no revela exantemas. Se sospecha carcinoma medular de
la tiroides.
CASO 88
Una mujer de 72 años de edad es llevada a la sala de urgencias Preguntas
luego de una caída en su hogar. Se resbaló con agua derrama
A. ¿Cuáles son algunas causas importantes de osteoporosis?
da en la cocina. Le resultó imposible levantarse después de la
B. ¿Cuáles son las causas probables de osteoporosis en esta pa
caída y su hijo, que pasó a visitarla cuando salió de trabajar,
ciente, y la patogenia subyacente de cada una?
la encontró en el piso de la cocina. La mujer se queja de dolor
C. ¿Cuáles son los factores de riesgo para fracturas en pacientes
intenso en la cadera derecha. En el examen, tiene equimosis
con osteoporosis?
sobre la cadera derecha. El rango de movimiento en la cadera
D. ¿Cuáles son las complicaciones frecuentes de las fracturas de
derecha está notoriamente reducido, con dolor con la rotación
cadera?
tanto interna como externa. La radiografía revela una fractura
E. ¿Qué tratamientos están disponibles para prevenir pérdida de
de cadera y tal vez masa ósea baja. El historial suscita preocu
hueso?
pación respecto a osteoporosis.
Biblioteca Médica Virtual
Libros de Medicina en PDF [◢ ◤ BMV ◢ ◤]
CAPÍTULO 17 Trastornos de las paratiroides, y del metabolismo del calcio y fósforo 513
CASO 89
Una mujer de 93 años de edad es llevada a la sala de urgencias Preguntas
en ambulancia porque “está desmejorada”. Hoy, la hija de la
A. ¿Cuáles son las causas de la osteomalacia? ¿Cuál sospecha en
mujer estaba intentando girarla para limpiarla y la paciente
esta paciente? ¿Por qué?
cayó de la cama al piso. Han sido incapaces de comprar medici
B. ¿Cuál es la patogenia de la osteomalacia en esta paciente?
nas durante varios meses. Durante muchos meses, la paciente
C. ¿Qué esperaría observar en una biopsia de hueso, para histo
sólo ha estado comiendo caldos debido a dificultad para mas
morfometría cuantitativa?
ticar y deglutir. En el examen, está pálida, con obesidad central,
emaciación de las extremidades y contracturas en flexión de
las extremidades superiores e inferiores derechas. En el exa
men de la cabeza y el cuello, tiene emaciación temporal, caída
del lado derecho de la cara, conjuntivas pálidas y mucosas se
cas. Los campos pulmonares están despejados a la ausculta
ción. El dato notable en el examen cardiaco es un galope S4. La
paciente gime cuando se palpan sus extremidades. Los infor
mes de laboratorio muestran hipocalcemia, hipofosfatemia y
fosfatasa alcalina alta. Las radiografías de la pelvis revelan masa
ósea baja y “seudofractura” de las ramas del pubis. Se sospecha
osteomalacia.
BIBLIOGRAFÍA Vilardaga JP et al. Molecular basis of parathyroid hormone receptor sig
naling and trafficking: a family B GPCR paradigm. Cell Mol Life Sci.
2011 Jan;68(1):1–13. [PMID: 20703892]
Metabolismo óseo y mineral general,
y vitamina D Hiperparatiroidismo
Chakravarti B et al. Signaling through the extracellular calcium- Bilezikian JP. Primary hyperparathyroidism. Endocr Pract. 2012 Sep–
sensing receptor (CaSR). Adv Exp Med Biol. 2012;740:103–42. Oct;18(5):781–90. [PMID: 22982802]
[PMID: 22453940] Cetani F et al. Molecular pathogenesis of primary hyperparathyroidism.
Christakos S. Recent advances in our understanding of 1,25-dihydroxy J Endocrinol Invest. 2011 Jul;34(7 Suppl):35–9. [PMID: 21985978]
vitamin D(3) regulation of intestinal calcium absorption. Arch Bio Eastell R et al. Diagnosis of asymptomatic primary hyperparathyroi
chem Biophys. 2012 Jul 1;523(1):73–6. [PMID: 22230327] dism: proceedings of the third international workshop. J Clin Endo
Civitelli R et al. Calcium and phosphate homeostasis: concerted inter crinol Metab. 2009 Feb;94(2):340–50. [PMID: 19193909]
play of new regulators. J Endocrinol Invest. 2011 Jul;34(7 Suppl):3–7. Lemos MC et al. Multiple endocrine neoplasia type 1 (MEN1): analy
[PMID: 21985972] sis of 1336 mutations reported in the first decade following iden
Egbuna OI et al. Hypercalcaemic and hypocalcaemic conditions due to tification of the gene. Hum Mutat. 2008 Jan;29(1):22–32. [PMID:
calcium-sensing receptor mutations. Best Pract Res Clin Rheumatol. 17879353]
2008 Mar;22(1):129–48. [PMID: 18328986] Marcocci C et al. Clinical practice. Primary hyperparathyroidism.
Endres DB. Investigation of hypercalcemia. Clin Biochem. 2012 Aug; N Engl J Med. 2011 Dec 22;365(25):2389–97. [PMID: 22187986]
45(12):954–63. [PMID: 22569596] Marcocci C et al. Parathyroid carcinoma. J Bone Miner Res. 2008
Nakashima T et al. New regulation mechanisms of osteoclast differentia Dec;23(12):1869–80. [PMID: 19016595]
tion. Ann NY Acad Sci. 2011 Dec;1240:E13–8. [PMID: 22360322] Mosekilde L. Primary hyperparathyroidism and the skeleton. Clin En
Piret SE et al. Mouse models for inherited endocrine and metabolic di docrinol (Oxf). 2008 Jul;69(1):1–19. [PMID: 18167138]
sorders. J Endocrinol. 2011 Dec;211(3):211–30. [PMID: 21765099] Newey PJ et al. Parafibromin—functional insights. J Intern Med. 2009
Rosen CJ et al. The nonskeletal effects of vitamin D: an Endocrine Jul;266(1):84–98. [PMID: 19522828]
Society scientific statement. Endocr Rev. 2012 Jun;33(3):456–92. Newey PJ et al. Role of multiple endocrine neoplasia type1 mutatio
[PMID: 22596255] nal analysis in clinical practice. Endocr Pract. 2011 Jul–Aug;17
Silva BC et al. Catabolic and anabolic actions of parathyroid hormo (Suppl 3):8–17. [PMID: 21454234]
ne on the skeleton. J Endocrinol Invest. 2011 Nov;34(10):801–10. Pepe J et al. Sporadic and hereditary primary hyperparathyroidism.
[PMID: 2194608 J Endocrinol Invest. 2011 Jul;34(Suppl 7):40–4. [PMID: 21985979]
Biblioteca Médica Virtual
También podría gustarte
- Trastornos en Paratiroides y Metabolismo Del CalcioDocumento33 páginasTrastornos en Paratiroides y Metabolismo Del CalcioLuis A Berzunza ChanAún no hay calificaciones
- Glándulas ParatiroidesDocumento9 páginasGlándulas ParatiroidesEnzon BritoAún no hay calificaciones
- Sistema Endocrino ParatiroideDocumento11 páginasSistema Endocrino ParatiroideQUIMICO CLINICO WILLIANS SANCHEZ100% (1)
- Capitulo 47 PDFDocumento9 páginasCapitulo 47 PDFKaren ReyesAún no hay calificaciones
- Hipoparatiroidismo PDFDocumento8 páginasHipoparatiroidismo PDFStephany Bruiget100% (2)
- Metabolismo Del CalcioDocumento46 páginasMetabolismo Del CalcioFrancisco AbantoAún no hay calificaciones
- Glandula ParatiroidesDocumento14 páginasGlandula ParatiroidesJostein Carvajal ParralesAún no hay calificaciones
- Tema #11G. ParatiroideaDocumento8 páginasTema #11G. ParatiroideaJoselin GalvezAún no hay calificaciones
- El Fósforo o Los Fosfatos FISIOLOGIADocumento4 páginasEl Fósforo o Los Fosfatos FISIOLOGIAVicente Fernando Arizabal CarpioAún no hay calificaciones
- Anatomía de Las Glándulas Paratiroideas (R)Documento9 páginasAnatomía de Las Glándulas Paratiroideas (R)Diego Gutierrez HernandezAún no hay calificaciones
- Hormona Paratifoidea Formas Moleculares y Utilidad DiagnosticoDocumento16 páginasHormona Paratifoidea Formas Moleculares y Utilidad DiagnosticoMaria Camila Patron MontoyaAún no hay calificaciones
- Hormona ParatiroideaDocumento8 páginasHormona ParatiroideagonchigolsAún no hay calificaciones
- Secretor ResumenDocumento6 páginasSecretor ResumenJeanAún no hay calificaciones
- Glándulas ParatiroidesDocumento21 páginasGlándulas ParatiroidesLisbeth Alvarez100% (1)
- Glandula Paratiroides EndocrinoDocumento98 páginasGlandula Paratiroides EndocrinoJorge SolisAún no hay calificaciones
- ParatitoidesDocumento2 páginasParatitoides22080054Aún no hay calificaciones
- HIPOPARATIROIDISMODocumento28 páginasHIPOPARATIROIDISMOanaAún no hay calificaciones
- Paratiroides Regulacion Hormonal Del Calcio y FosfatosDocumento82 páginasParatiroides Regulacion Hormonal Del Calcio y FosfatosUSMP FN ARCHIVOSAún no hay calificaciones
- Para Tiro IdeaDocumento7 páginasPara Tiro IdeaJochiJaramilloAún no hay calificaciones
- CALCITONINADocumento10 páginasCALCITONINAGiuliana DoriaAún no hay calificaciones
- Alteraciones Del CalcioDocumento39 páginasAlteraciones Del CalcioAndres GamaAún no hay calificaciones
- Glándulas ParatiroidesDocumento10 páginasGlándulas ParatiroidesKareftt Jerif FFigueroa RomeroAún no hay calificaciones
- Tema 10 MFH III - 050532Documento3 páginasTema 10 MFH III - 050532Geronimo J D SánchezAún no hay calificaciones
- Artículo Calcio y Metabolismo Del Hueso.Documento8 páginasArtículo Calcio y Metabolismo Del Hueso.Cesar Alberto Alzate SantaAún no hay calificaciones
- CalcioDocumento30 páginasCalcioCarlos Campos100% (1)
- Glándulas Paratireoides, CalcitoninaDocumento22 páginasGlándulas Paratireoides, Calcitoninathais liechyeAún no hay calificaciones
- Expo EndocrinoDocumento15 páginasExpo EndocrinoMorales Quezada Jose JaimeAún no hay calificaciones
- Título AquíDocumento38 páginasTítulo AquíEdwin Adrian RodriguezAún no hay calificaciones
- Metabolismo Calcio, Fosforo, Magnesio: Dra. Liana RomeroDocumento39 páginasMetabolismo Calcio, Fosforo, Magnesio: Dra. Liana RomeroDoany CariasAún no hay calificaciones
- Cuestionario Tiroides y ParatiroidesDocumento1 páginaCuestionario Tiroides y Paratiroidesjosue LaraAún no hay calificaciones
- Hormona Paratiroidea (PTH)Documento24 páginasHormona Paratiroidea (PTH)Bayardo O EspinozaAún no hay calificaciones
- CalcioDocumento2 páginasCalcioddcvvdrq8xAún no hay calificaciones
- OSTEODISTROFIA HG RN 62v08n84a13036956pdf001Documento6 páginasOSTEODISTROFIA HG RN 62v08n84a13036956pdf001OscarDavidGordilloGonzalezAún no hay calificaciones
- Etiologia de HipocalcemiaDocumento24 páginasEtiologia de HipocalcemiaJORGE SEGURAAún no hay calificaciones
- Tarea 1 Bioquimica Diego ParedesDocumento6 páginasTarea 1 Bioquimica Diego ParedesReal MonsterAún no hay calificaciones
- Hipo e HiperparatiroidisimoDocumento10 páginasHipo e HiperparatiroidisimoVerónica Duménez JofréAún no hay calificaciones
- Alteraciones de La Homeostasis FosfocalcicaDocumento3 páginasAlteraciones de La Homeostasis FosfocalcicaGabrielaAún no hay calificaciones
- HIPOCALCEMIADocumento7 páginasHIPOCALCEMIAAileenAún no hay calificaciones
- Hormona Paratiroidea y Metabolismo Del CalcioDocumento5 páginasHormona Paratiroidea y Metabolismo Del Calciobryan fragoso castroAún no hay calificaciones
- Metabolismo Del Calcio y FosforoDocumento9 páginasMetabolismo Del Calcio y FosforoAnatomiaud100% (1)
- Encefalitis Por ArbovirusDocumento58 páginasEncefalitis Por ArbovirusArely ArredondoAún no hay calificaciones
- CALCIODocumento11 páginasCALCIOhectorsuarez8Aún no hay calificaciones
- Paratiroides, Metabolismo Del Calcio y Fisiolog+¡a OseaDocumento42 páginasParatiroides, Metabolismo Del Calcio y Fisiolog+¡a OseaSandy MosqueraAún no hay calificaciones
- Enfermedad de Las Glándulas Paratiroides (María Peña)Documento8 páginasEnfermedad de Las Glándulas Paratiroides (María Peña)Victor MonsalveAún no hay calificaciones
- El Laboratorio Clínico en El Diagnóstico y Seguimiento Del Hiperparatiriodismo PrimarioDocumento25 páginasEl Laboratorio Clínico en El Diagnóstico y Seguimiento Del Hiperparatiriodismo PrimarioMark Sal DontoAún no hay calificaciones
- Metabolismo Fosfo-CalcicoDocumento14 páginasMetabolismo Fosfo-CalcicoGerson Antonio Torres AlmeydaAún no hay calificaciones
- Informe HiperparatiroidismoDocumento11 páginasInforme HiperparatiroidismoFiorela Maclaine Vasquez DiazAún no hay calificaciones
- Calcio fp2 PDFDocumento8 páginasCalcio fp2 PDFERICK ARIEL ARTETA CHOWAún no hay calificaciones
- GENERALIDADESDocumento11 páginasGENERALIDADESAlison PFAún no hay calificaciones
- Hormonas Tiroideas y ParatiroideasDocumento45 páginasHormonas Tiroideas y ParatiroideasMarité Flores MontenegroAún no hay calificaciones
- 2.2. Glándula ParatiroidesDocumento13 páginas2.2. Glándula ParatiroidesMaría Alvarado PachasAún no hay calificaciones
- Cap Tulo 37 GL Ndulas Paratiroideas 2018 Sabiston Tratado de Cirugia Plus Expertconsult 20 Edici NDocumento18 páginasCap Tulo 37 GL Ndulas Paratiroideas 2018 Sabiston Tratado de Cirugia Plus Expertconsult 20 Edici NMayIsa RivAceAún no hay calificaciones
- PARATIROIDESDocumento55 páginasPARATIROIDESALEJANDRO JOSE CABARCAS TORDECILLAAún no hay calificaciones
- 004-Gándulas ParatiroidesDocumento24 páginas004-Gándulas ParatiroidesEmely PortilloAún no hay calificaciones
- Trastornos de Las Glandulas. ParatiroideDocumento38 páginasTrastornos de Las Glandulas. ParatiroideFegenes DessalinesAún no hay calificaciones
- Practica 3Documento16 páginasPractica 3yadira fernandezAún no hay calificaciones
- Calcio, Físico, Híper e Hipo TrastornosDocumento34 páginasCalcio, Físico, Híper e Hipo TrastornosFernanda VAún no hay calificaciones
- GuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisDe EverandGuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisCalificación: 4 de 5 estrellas4/5 (9)
- Hipertensión Pulmonar Arterial: (Ascitis) En Pollos De EngordaDe EverandHipertensión Pulmonar Arterial: (Ascitis) En Pollos De EngordaAún no hay calificaciones
- Causas De Mala Circulación - Basado En Las Enseñanzas De Frank Suarez: Factores Y Desencadenantes De Problemas CirculatoriosDe EverandCausas De Mala Circulación - Basado En Las Enseñanzas De Frank Suarez: Factores Y Desencadenantes De Problemas CirculatoriosAún no hay calificaciones
- Hepatico - Merged (1) - Merged - CompressedDocumento153 páginasHepatico - Merged (1) - Merged - CompressedSaira Alexandra Ullaguari CuencaAún no hay calificaciones
- Casos ClinicosDocumento19 páginasCasos ClinicosSaira Alexandra Ullaguari CuencaAún no hay calificaciones
- Hematologia Clinica 1Documento45 páginasHematologia Clinica 1Saira Alexandra Ullaguari CuencaAún no hay calificaciones
- PielDocumento3 páginasPielSaira Alexandra Ullaguari CuencaAún no hay calificaciones
- Alteraciones Del Metabolismo Fosfocálcico. Hipercalcemia. HiperparatiroidismoDocumento7 páginasAlteraciones Del Metabolismo Fosfocálcico. Hipercalcemia. HiperparatiroidismoManc127Aún no hay calificaciones
- Exámenes Que Incluye El Perfil BioquímicoDocumento2 páginasExámenes Que Incluye El Perfil BioquímicoAlejandro BarrientosAún no hay calificaciones
- HipocalcemiaDocumento7 páginasHipocalcemiaKate CastañoAún no hay calificaciones
- PNFMIC Semana 22 Orientac Estudi y Profesores ASIC 21 Al 26 de SeptiembreDocumento77 páginasPNFMIC Semana 22 Orientac Estudi y Profesores ASIC 21 Al 26 de SeptiembreyeremyAún no hay calificaciones
- CalcemiaDocumento55 páginasCalcemiaCarolina VelizAún no hay calificaciones
- Cuantificacion de Calcio en La Cascara de Huevo PDFDocumento58 páginasCuantificacion de Calcio en La Cascara de Huevo PDFDiana Carolina Zapata Bereche100% (1)
- Polifarmacia 3CIPARDocumento39 páginasPolifarmacia 3CIPARpotolokiss2025Aún no hay calificaciones
- Paraclinicos Normales PDFDocumento25 páginasParaclinicos Normales PDFRick Costa100% (1)
- Resumen Insuficiencia Renal CrónicaDocumento6 páginasResumen Insuficiencia Renal CrónicaDIEGO MUÑOZ MUÑOZAún no hay calificaciones
- 11 Metabolismo Del Calcio y FosfatoDocumento68 páginas11 Metabolismo Del Calcio y FosfatoPaloma Castillo SantanderAún no hay calificaciones
- CalculosDocumento274 páginasCalculosMarco Huerta0% (1)
- Práctica #2 Calcemia y FosfatemiaDocumento7 páginasPráctica #2 Calcemia y FosfatemiaJOSE VALDEMAR OJEDA ROJASAún no hay calificaciones
- Transtornos Del Calcio en GuardiaDocumento9 páginasTranstornos Del Calcio en GuardiailmediciAún no hay calificaciones
- CALCIO ExposicionDocumento5 páginasCALCIO ExposicionVeronica UriiBeAún no hay calificaciones
- Osteoporosis 1Documento16 páginasOsteoporosis 1anthony mera gutierrezAún no hay calificaciones
- CalcemiaDocumento6 páginasCalcemiaConii RengifoAún no hay calificaciones
- HiperparatiroidismoDocumento46 páginasHiperparatiroidismowilpmfmhAún no hay calificaciones
- 1.1 Taller de ERCDocumento7 páginas1.1 Taller de ERCjose Gabriel Iriarte CadrascoAún no hay calificaciones
- Clase 3, Aldosterona y Metabolismo Del Calcio (24-04)Documento10 páginasClase 3, Aldosterona y Metabolismo Del Calcio (24-04)gonzalomanuelAún no hay calificaciones
- Fisio CalcioDocumento4 páginasFisio CalcioCarmem AlbuquerqueAún no hay calificaciones
- Homonas y CalcioDocumento5 páginasHomonas y CalcioMonica WalkerAún no hay calificaciones
- Metabolismo Del Calcio, Fosforo y MagnesioDocumento29 páginasMetabolismo Del Calcio, Fosforo y MagnesioAlbetzy LayaAún no hay calificaciones
- Cirurgia IIIDocumento327 páginasCirurgia IIIPaula de TássiaAún no hay calificaciones
- Calcio - Hipo e Hiper SíntomasDocumento8 páginasCalcio - Hipo e Hiper SíntomasJosé Pérez100% (1)
- Metabolismo Del Calcio y Del Fosforo - pdf3Documento45 páginasMetabolismo Del Calcio y Del Fosforo - pdf3Alexander Salgado ReyesAún no hay calificaciones
- Hiper e HipoparatiroidismoDocumento40 páginasHiper e HipoparatiroidismoTaniaAún no hay calificaciones
- Equilibrio HidroelectrolíticoDocumento24 páginasEquilibrio HidroelectrolíticoStela MarisAún no hay calificaciones
- 11-Fisiología OsteomuscularDocumento54 páginas11-Fisiología OsteomuscularNestor Danilo Rendon DiazAún no hay calificaciones
- Metabolismo Del Calcio ResumenDocumento2 páginasMetabolismo Del Calcio ResumenAna MendezAún no hay calificaciones
- Histologia Del Sistema Endocrino IIDocumento12 páginasHistologia Del Sistema Endocrino IIPedro GonzalezAún no hay calificaciones