Documentos de Académico
Documentos de Profesional
Documentos de Cultura
111 Aspirin A
Cargado por
Monse0 calificaciones0% encontró este documento útil (0 votos)
33 vistas2 páginasSe realizó la síntesis del ácido acetilsalicílico mediante la reacción de acetilación entre el anhídrido acético y el ácido salicílico catalizada por el ácido sulfúrico. El producto se purificó por recristalización y se realizaron pruebas de identificación como cromatografía en placa fina y reacción con cloruro de fierro, aunque esta última indicó la presencia de fenoles, lo que sugiere que la purificación no fue completa.
Descripción original:
Sintesis de acido acetilsalicílico
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoSe realizó la síntesis del ácido acetilsalicílico mediante la reacción de acetilación entre el anhídrido acético y el ácido salicílico catalizada por el ácido sulfúrico. El producto se purificó por recristalización y se realizaron pruebas de identificación como cromatografía en placa fina y reacción con cloruro de fierro, aunque esta última indicó la presencia de fenoles, lo que sugiere que la purificación no fue completa.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
33 vistas2 páginas111 Aspirin A
Cargado por
MonseSe realizó la síntesis del ácido acetilsalicílico mediante la reacción de acetilación entre el anhídrido acético y el ácido salicílico catalizada por el ácido sulfúrico. El producto se purificó por recristalización y se realizaron pruebas de identificación como cromatografía en placa fina y reacción con cloruro de fierro, aunque esta última indicó la presencia de fenoles, lo que sugiere que la purificación no fue completa.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
INTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
PRÁCTICA No. 6 “SÍNTESIS DE ÁCIDO ACETILSALICÍLICO”
RESUMEN: Se realizó la síntesis del ácido acetilsalicílico mediante la reacción de anhídrido acético y
ácido salicílico en un medio con ácido sulfúrico. Posteriormente el producto se purificó con la técnica de
recristalización en etanol-agua y se realizaron pruebas de identificación; cromatografía en placa fina,
reacción con cloruro de fierro y se determinó su punto de fusión.
INTRODUCCIÓN mencionar que no se puede llevar a cabo una
reacción intramolecular entre el grupo –OH y
El ácido acetilsalicílico, también conocido con el ácido carboxílico debido a que si esta
el nombre de aspirina, es un fármaco de la reacción formaría un anillo de cuatro
familia de los salicilatos, usado miembros en donde predominaría la tensión
frecuentemente como antiinflamatorio, angular, siendo de este modo un anillo
inestable. La reacción se realizó en un baño
analgésico, para el alivio del dolor leve o
María debido a que así se favorece la
moderado, antipirético para reducir fiebre y reacción de acetilación evitando la
antiagregante plaquetario indicado para sublimación del ácido salicílico, regulando de
personas con alto riesgo de coagulación temperatura de la reacción.
sanguínea, principalmente individuos que ya
han tenido un infarto agudo de miocardio.
La reacción química de la síntesis de la
aspirina se considera una esterificación. El (1)
ácido salicílico es tratado con anhídrido
acético, un compuesto derivado de un ácido,
lo que hace que el grupo alcohol del salicilato
se convierta en un grupo acetilo. Este proceso
produce aspirina y ácido acético, el cual se
considera un subproducto de la reacción. (2) (3)
DISCUSIÓN DE RESULTADOS
Para llevar a cabo la síntesis del ácido acetil
salicílico se partió de una mezcla de ácido
salicílico, anhídrido acético (2.5 y 5 mL (4)
respectivamente) y ácido sulfúrico (5 gotas),
en donde se efectuó una reacción de
acetilación, que consiste en la formación de Prueba de identificación con FeCl3
un grupo éster, el cual es proporcionado por En esta reacción se produce la
el anhídrido acético. La reacción es catalizada desaparición del carácter fenólico de ácido
por el ácido sulfúrico, para que el anhídrido salicílico, por lo que la pureza se puede ver
acético (agente acetilante) se protone [1] y observando la formación o no del complejo
posteriormente el grupo –OH del ácido color violeta que los fenoles forman con el
salicílico ataque al carbono carbonílico del catión Fe3+.
anhídrido acético [2], formándose un éster Para la realización de esta prueba, en un
debido a una transferencia de un protón de tubo de ensaye se colocó ácido salicílico y
forma intramolecular [3], posteriormente el una gota de FeCl3. En otro tubo se colocó
anhídrido acético se hidroliza y se regenera el una pizca el crudo de reacción disuelta en
catalizador [4] (Mecanismo 1). Cabe etanol y una gota de FeCl3. Finalmente, en
INTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
PRÁCTICA No. 6 “SÍNTESIS DE ÁCIDO ACETILSALICÍLICO”
un tercer tubo se colocó el crudo de
reacción después del cristalizado y una
gota de FeCl3.
En nuestro caso nos dimos cuenta que no
obtuvimos el producto deseado ya que los
tres tubos; tanto el que contenía el ácido
salicílico, como el del crudo de reacción y
el de nuestro producto después de
recristalizar dieron positivo a la prueba,
dando un color violeta. Esto se debe a que
aún hay fenoles presentes en él.
También podría gustarte
- Reporte 5 - Preparacion de Acido Salicilico y Sintesis de La Aspirina!Documento22 páginasReporte 5 - Preparacion de Acido Salicilico y Sintesis de La Aspirina!Ligia FletesAún no hay calificaciones
- Práctica 4 Sintesis de Ácido Acetilsalicilico Grupo DDocumento20 páginasPráctica 4 Sintesis de Ácido Acetilsalicilico Grupo Dmelaniejg100% (1)
- AspirinaDocumento2 páginasAspirinaTanjiro KamadoAún no hay calificaciones
- G2.Ochoa - Síntesis Del Ácido Acetil SalicílicoDocumento7 páginasG2.Ochoa - Síntesis Del Ácido Acetil SalicílicoOchoasusana28Aún no hay calificaciones
- AspirinaDocumento11 páginasAspirinaMaria TorresAún no hay calificaciones
- Obtención Del Ácido Acetilsalicílico Por Medio de Un Proceso de Química VerdeDocumento6 páginasObtención Del Ácido Acetilsalicílico Por Medio de Un Proceso de Química VerdeGänon Abraham50% (2)
- Informe N°2 ParteDocumento3 páginasInforme N°2 PartePiero MirandaAún no hay calificaciones
- Practica 5: "Obtención Del Ácido Acetilsalicílico Por Medio de Un Proceso de Química Verde."Documento5 páginasPractica 5: "Obtención Del Ácido Acetilsalicílico Por Medio de Un Proceso de Química Verde."Isabella Van BuurenAún no hay calificaciones
- Síntesis Ácido AcetilsalicílicoDocumento3 páginasSíntesis Ácido AcetilsalicílicoAlfredo LopezAún no hay calificaciones
- Sintesis Del AAsDocumento4 páginasSintesis Del AAsJose David VeraAún no hay calificaciones
- Practica 6 Preparacion de La AspirinaDocumento9 páginasPractica 6 Preparacion de La AspirinaMateo ValenciaAún no hay calificaciones
- Practica No. 6. Obtención de Ácido Acetilsalicílico (Aspirina)Documento6 páginasPractica No. 6. Obtención de Ácido Acetilsalicílico (Aspirina)Daniel Santos GarciaAún no hay calificaciones
- Quim Ii-Bio Grupo 7practica12Documento5 páginasQuim Ii-Bio Grupo 7practica12Sam ValdiviaAún no hay calificaciones
- LaboratorioDocumento7 páginasLaboratorioRONAL ZUNIGA CAMPOSAún no hay calificaciones
- Síntesis de Ácido Acetil SalicílicoDocumento4 páginasSíntesis de Ácido Acetil SalicílicoLuis Sanchez OreAún no hay calificaciones
- Organica 3 Practica 1Documento7 páginasOrganica 3 Practica 1marielaAún no hay calificaciones
- Muestra de Un ReporteDocumento3 páginasMuestra de Un ReporteCastañeda Zepeda Héctor AlejandroAún no hay calificaciones
- Hidrólisis Ácido AcetilsalicílicoDocumento6 páginasHidrólisis Ácido AcetilsalicílicojhoanaAún no hay calificaciones
- ProyectoDocumento6 páginasProyectoLuisa SalinasAún no hay calificaciones
- ESTERIFICACIÓNDocumento6 páginasESTERIFICACIÓNArmando CarcamoAún no hay calificaciones
- Informe de Sintesis Del AasDocumento16 páginasInforme de Sintesis Del AasMonica CastilloAún no hay calificaciones
- Sintesis de Aspirina (Laboratorio)Documento17 páginasSintesis de Aspirina (Laboratorio)Paola Guillén Morales100% (3)
- Sintesis Extraccion y CCFDocumento6 páginasSintesis Extraccion y CCFJhonda Sequeda DominguezAún no hay calificaciones
- Síntesis de AAS - AdrianaC y JesúsO - Marzo2022Documento2 páginasSíntesis de AAS - AdrianaC y JesúsO - Marzo2022Adriana Paola Colmenares SoaresAún no hay calificaciones
- Sintesis Extraccion y CCFDocumento6 páginasSintesis Extraccion y CCFdavid romeroAún no hay calificaciones
- Síntesis de La AspirinaDocumento8 páginasSíntesis de La AspirinaCamilo100% (1)
- PRAC 6 - Síntesis de AspirinaDocumento4 páginasPRAC 6 - Síntesis de AspirinaJuan AguilarAún no hay calificaciones
- Informe 2 Org II: Síntesis de AspirinaDocumento6 páginasInforme 2 Org II: Síntesis de AspirinaCamilo Colilaf CaroAún no hay calificaciones
- Síntesis AspirinaDocumento3 páginasSíntesis AspirinaRosa Isabel BernalAún no hay calificaciones
- Wa0067.Documento13 páginasWa0067.Luisfer DelcastilloAún no hay calificaciones
- Lab Quim Orgii Practica 4 Sintesis de Aspirina Ot2021Documento6 páginasLab Quim Orgii Practica 4 Sintesis de Aspirina Ot2021farid garcia (superfarid666)0% (1)
- Salicilato de MetiloDocumento4 páginasSalicilato de MetiloJorgeMartin100% (1)
- AasDocumento7 páginasAasNadia De Jesus OrdoñezAún no hay calificaciones
- Preparacion Del Acido AcetilsalicilicoDocumento11 páginasPreparacion Del Acido AcetilsalicilicolizAún no hay calificaciones
- Práctica Ácido AcetilsalicílicoDocumento3 páginasPráctica Ácido AcetilsalicílicoAlexandra maria marin bernalAún no hay calificaciones
- Laboratorio Sintesis de La AspirinaDocumento11 páginasLaboratorio Sintesis de La AspirinaSergio Enrique Alvarez GarciaAún no hay calificaciones
- Síntesis y Caracterizacción Del Ácido AcetilsalicílicoDocumento12 páginasSíntesis y Caracterizacción Del Ácido AcetilsalicílicoMartaYanesSánchezAún no hay calificaciones
- Informe 6 Preparación de Ácido O-AcetilsalicílicoDocumento11 páginasInforme 6 Preparación de Ácido O-AcetilsalicílicoDani SantoyoAún no hay calificaciones
- Muestra de Un Reporte.Documento4 páginasMuestra de Un Reporte.Castañeda Zepeda Héctor AlejandroAún no hay calificaciones
- Practica de Goros 2Documento8 páginasPractica de Goros 2anon_793719390Aún no hay calificaciones
- El Ácido Acetilsalicílico Es Un Éster de Ácido Acético y Ácido SalicílicoDocumento2 páginasEl Ácido Acetilsalicílico Es Un Éster de Ácido Acético y Ácido SalicílicoDiana RodriguezAún no hay calificaciones
- Sintesis de AspirinaDocumento12 páginasSintesis de AspirinaRubén Gonzalo UsnayoAún no hay calificaciones
- Obtencion de Acido AcetilsalicilicoDocumento4 páginasObtencion de Acido AcetilsalicilicoOsnayder Vilardy VarelaAún no hay calificaciones
- Sintesis de AspirinaDocumento7 páginasSintesis de AspirinaGustavo Gutiérrez Gómez50% (2)
- Práctica 10 - Síntesis y Caracterización Del AAS PDFDocumento15 páginasPráctica 10 - Síntesis y Caracterización Del AAS PDFDavid Fabra CarrascoAún no hay calificaciones
- Informe Síntesis 2. Ácido AcetilsalicílicoDocumento10 páginasInforme Síntesis 2. Ácido AcetilsalicílicoDiana HernándezAún no hay calificaciones
- Práctica # 10. Síntesis de AspirinaDocumento7 páginasPráctica # 10. Síntesis de Aspirinaperla batista carrascoAún no hay calificaciones
- Practica 8 Lab Organica IiDocumento6 páginasPractica 8 Lab Organica IiAlan Lopez MoralesAún no hay calificaciones
- Equipo6 E4 FQEDocumento8 páginasEquipo6 E4 FQEQueenAún no hay calificaciones
- AspirinaDocumento3 páginasAspirinaAnonymous GUDFgoaAún no hay calificaciones
- Lab RCA-7 PiridoniosDocumento5 páginasLab RCA-7 PiridoniosSebas IslasAún no hay calificaciones
- AspirinaDocumento9 páginasAspirinaUvuvwevwevwev OsasAún no hay calificaciones
- Practica para Realizar Acido AcetilsalicilicoDocumento11 páginasPractica para Realizar Acido AcetilsalicilicoLuis Vazquez HuanteAún no hay calificaciones
- Esterificacion de Los EsteresDocumento9 páginasEsterificacion de Los EsteresNatalia KlopatosquiAún no hay calificaciones
- AspirinaDocumento10 páginasAspirinajhonatanAún no hay calificaciones
- Pregunta 1 y 2Documento3 páginasPregunta 1 y 2Grecia Obando0% (1)
- Práctica 3 - Ácido Acetil SalicílicoDocumento6 páginasPráctica 3 - Ácido Acetil SalicílicoMARIA0% (1)
- Estatus ácido-base: Conceptos, desequilibrios e interpretaciónDe EverandEstatus ácido-base: Conceptos, desequilibrios e interpretaciónAún no hay calificaciones
- Descubre El Mejor Antiácido Natural - Basado En Las Enseñanzas De Frank Suarez: Restableciendo El Equilibrio Ácido De Manera NaturalDe EverandDescubre El Mejor Antiácido Natural - Basado En Las Enseñanzas De Frank Suarez: Restableciendo El Equilibrio Ácido De Manera NaturalAún no hay calificaciones
- P7 SeminarioDocumento26 páginasP7 SeminarioMonseAún no hay calificaciones
- Diagrama PastasDocumento1 páginaDiagrama PastasMonseAún no hay calificaciones
- COLORANTESDocumento8 páginasCOLORANTESMonseAún no hay calificaciones
- Mapaconceptual7 PDFDocumento1 páginaMapaconceptual7 PDFMonseAún no hay calificaciones
- LIOFOLIZACIONDocumento1 páginaLIOFOLIZACIONMonseAún no hay calificaciones
- 3.membrana Citoplasmica Parte 2 BDocumento11 páginas3.membrana Citoplasmica Parte 2 BMonseAún no hay calificaciones
- 1HIDROLISISDocumento2 páginas1HIDROLISISMonseAún no hay calificaciones
- AAPRACT6HETERODocumento1 páginaAAPRACT6HETEROMonseAún no hay calificaciones
- 1METILPIRAZOLONADocumento1 página1METILPIRAZOLONAMonseAún no hay calificaciones
- Criterios de Selección de Personal Trabajo en AlturaDocumento20 páginasCriterios de Selección de Personal Trabajo en AlturaolivoroAún no hay calificaciones
- Actividad 3 SVEDocumento7 páginasActividad 3 SVEEdwin fernando Aya CortesAún no hay calificaciones
- Protocolo Bioseguridad Muro PiedecuestaDocumento101 páginasProtocolo Bioseguridad Muro PiedecuestaJavierAriasHdezAún no hay calificaciones
- Evaluacion Clinica. PsicopatologicaDocumento108 páginasEvaluacion Clinica. PsicopatologicaPAOLA DEL CARMEN SEPéLVEDA CORREAAún no hay calificaciones
- Informe LaboratorioDocumento4 páginasInforme LaboratorioYeison Ivan SuarezAún no hay calificaciones
- Residuos Sólidos - PMIRSDocumento12 páginasResiduos Sólidos - PMIRSPilar Marin SánchezAún no hay calificaciones
- Cramer Comprension PsicopatologiaDocumento13 páginasCramer Comprension PsicopatologiapanxologoAún no hay calificaciones
- Adaptaciones ParasitariasDocumento9 páginasAdaptaciones ParasitariasIván Hernández ReyesAún no hay calificaciones
- Silabo de Documentacion Sanitaria y Del Laboratorio ClinicoDocumento5 páginasSilabo de Documentacion Sanitaria y Del Laboratorio ClinicoErnesti SanchezAún no hay calificaciones
- Oa-Fr-89 Solicitud Traslado - Evacuación Aeromedica v2Documento2 páginasOa-Fr-89 Solicitud Traslado - Evacuación Aeromedica v2Robinson MenaAún no hay calificaciones
- PROYECTODocumento34 páginasPROYECTOjesusAún no hay calificaciones
- Derecho AmbientalDocumento4 páginasDerecho AmbientalAlonso F GuzmanAún no hay calificaciones
- Patologia Clinica Dr. Carlos A. Javier - Completo PDFDocumento585 páginasPatologia Clinica Dr. Carlos A. Javier - Completo PDFKahiAún no hay calificaciones
- Acuerdo 20Documento386 páginasAcuerdo 20YovaniAún no hay calificaciones
- Envases y EmbalajesDocumento79 páginasEnvases y EmbalajesUgo TmochAún no hay calificaciones
- Los Efectos de La Experiencia Con La Letra Manuscrita en El Desarrollo Funcional Del Cerebro de Ni Os PrealfabetizadosDocumento3 páginasLos Efectos de La Experiencia Con La Letra Manuscrita en El Desarrollo Funcional Del Cerebro de Ni Os PrealfabetizadosVictor Marcelo PiaggioAún no hay calificaciones
- GRAALL2003Documento27 páginasGRAALL2003Milber Enrique Fuentes radaAún no hay calificaciones
- Electroporacion WordDocumento6 páginasElectroporacion WordIrene De La Cruz Rojas100% (1)
- Marco Legal Laboral 2Documento13 páginasMarco Legal Laboral 2fidel ernesto guevara felizAún no hay calificaciones
- DesayunoSaludable DesafioDiarioWhatsApp TodosDocumento7 páginasDesayunoSaludable DesafioDiarioWhatsApp TodosAngie GonzalezAún no hay calificaciones
- Homeóstasis GlucemiaDocumento10 páginasHomeóstasis Glucemiadrcidbaez86% (7)
- TIVA CompletoDocumento109 páginasTIVA CompletoCandy ShaiyaAún no hay calificaciones
- El Peruano 7-9-2023Documento16 páginasEl Peruano 7-9-2023SGC2 Paz LaboratoriosAún no hay calificaciones
- Bosquejo DebateDocumento6 páginasBosquejo Debateapi-429394316Aún no hay calificaciones
- Presentacion GenogramaDocumento26 páginasPresentacion GenogramaLeidy Johana Muñoz ChavezAún no hay calificaciones
- WAGNER Pistola Pintar ElectricaDocumento10 páginasWAGNER Pistola Pintar ElectricaCameron RiosAún no hay calificaciones
- Guia Texto DivulgacionDocumento4 páginasGuia Texto DivulgacionEliziña Muñoz0% (1)
- Procedimiento de Reaccion InmediataDocumento6 páginasProcedimiento de Reaccion InmediataJair DiazAún no hay calificaciones
- Plan de Contingencias VIALDocumento12 páginasPlan de Contingencias VIALRodrigo SeguelAún no hay calificaciones
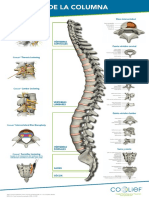
- Anatomia de La Columna VertebralDocumento1 páginaAnatomia de La Columna VertebralAngel Fernandez100% (1)