Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Enlaces Quimicos Primarios y Secundarios
Enlaces Quimicos Primarios y Secundarios
Cargado por
Jheyson Zuasnabar Paucar0 calificaciones0% encontró este documento útil (0 votos)
10 vistas12 páginasTítulo original
36892425 Enlaces Quimicos Primarios y Secundarios
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
10 vistas12 páginasEnlaces Quimicos Primarios y Secundarios
Enlaces Quimicos Primarios y Secundarios
Cargado por
Jheyson Zuasnabar PaucarCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 12
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
UNIVERSIDAD TECNOLOGICA
DE TECAMACHALCO
MANTENIMIENTO REA INDUSTRIAL
INGENIERIA DE MATERIALES
ENLACES QUIMICOS: PRIMARIOS Y SECUNDARIOS
PROFESOR: ING. ISAAC OSUNA MARMOLEJO
ALUMNO: AGUSTIN FLORES ASCENCIN
GRUPO: 4 D
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
ENLACES QUIMICOS PRIMARIOS
ENLACE INICO
El sodio y el cloro unindose inicamente para formar cloruro de sodio.
En qumica, el enlace inico es una unin que resulta de la presencia de fuerza de
atraccin electrosttica entre los iones de distinto signo, es decir uno fuertemente
electropositivo (baja energa de ionizacin) y otro fuertemente electronegativo (alta
afinidad electrnica). As pues se da cuando en el enlace uno de los tomos capta
electrones del otro.
Dado que los elementos implicados tienen elevadas diferencias de electronegatividad,
este enlace suele darse entre un compuesto metlico y uno no metlico. Se produce
una transferencia electrnica total de un tomo a otro formndose iones de diferente
signo. El metal dona uno o ms electrones formando iones con carga positiva o
cationes con una configuracin electrnica estable. Estos electrones luego ingresan en
el no metal, originando un ion cargado negativamente o anin, que tambin tiene
configuracin electrnica estable. Son estables pues ambos, segn la regla del octeto
adquieren 8 electrones en su capa mas exterior. La atraccin electrosttica entre los
iones de carga opuesta causa que se unan y formen un compuesto.
En una unin de dos tomos por enlace inico, un electrn abandona el tomo menos
electronegativo y pasa a formar parte de la nube electrnica del ms electronegativo. El
cloruro de sodio (la sal comn) es un ejemplo de enlace inico: en l se combinan
sodio y cloro, perdiendo el primero un electrn que es capturado por el segundo: De
esta manera se forman dos iones de carga contraria: un catin (de carga positiva) y un
anin (de carga negativa). La diferencia entre las cargas de los iones provoca entonces
una fuerza de interaccin electromagntica entre los tomos que los mantiene unidos.
El enlace inico es la unin en la que los elementos involucrados aceptarn o perdern
electrones.
Enlace inico en el NaCl.
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
ENLACES COVALENTES
Los enlaces covalentes son las fuerzas que mantienen unidos entre s los tomos no
metlicos (los elementos situados a la derecha en la tabla peridica -C, O, F, Cl, ...).
Estos tomos tienen muchos electrones en su nivel ms externo (electrones de
valencia) y tienen tendencia a ganar electrones ms que a cederlos, para adquirir la
estabilidad de la estructura electrnica de gas noble. Por tanto, los tomos no metlicos
no pueden cederse electrones entre s para formar iones de signo opuesto.
En este caso el enlace se forma al compartir un par de electrones entre los dos tomos,
uno procedente de cada tomo. El par de electrones compartido es comn a los dos
tomos y los mantiene unidos, de manera que ambos adquieren la estructura
electrnica de gas noble. Se forman as habitualmente molculas: pequeos grupos de
tomos unidos entre s por enlaces covalentes.
A diferencia de lo que pasa en un enlace inico, en donde se produce la transferencia
de electrones de un tomo a otro, en el enlace qumico covalente, los electrones de
enlace son compartidos por ambos tomos. En el enlace covalente, los dos tomos no
metlicos comparten uno o ms electrones, es decir se unen a travs de sus electrones
en el ltimo orbital, el cual depende del nmero atmico en cuestin. Entre los dos
tomos puede compartirse uno, dos o tres electrones, lo cual dar lugar a la formacin
de un enlace simple, doble o triple. En representacin de Lewis estos enlaces pueden
representarse por una pequea lnea entre los tomos.
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
ENLACE METLICO
Un enlace metlico es un enlace qumico que mantiene unidos los tomos (unin
entre cationes y los electrones de valencia) de los metales entre s. Estos tomos se
agrupan de forma muy cercana unos a otros, lo que produce estructuras muy
compactas. Se trata de redes tridimensionales que adquieren la estructura tpica de
empaquetamiento compacto de esferas. En este tipo de estructura cada tomo
metlico est rodeado por otros doce tomos (seis en el mismo plano, tres por encima
y tres por debajo). Adems, debido a la baja electronegatividad que poseen los
metales, los electrones de valencia son extrados de sus orbitales y tienen la capacidad
de moverse libremente a travs del compuesto metlico, lo que otorga a ste las
propiedades elctricas y trmicas.
El enlace metlico es caracterstico de los elementos metlicos, es un enlace fuerte,
primario, que se forma entre elementos de la misma especie. Los tomos, al estar tan
cercanos uno de otro, interaccionan los ncleos junto con sus nubes electrnicas
empaquetndose en las tres dimensiones, por lo que quedan rodeados de tales nubes.
Estos electrones libres son los responsables que los metales presenten una elevada
conductividad elctrica y trmica, ya que estos se pueden mover con facilidad si se
ponen en contacto con una fuente elctrica. Presentan brillo y son maleables.
Los elementos con un enlace metlico estn compartiendo un gran nmero de
electrones de valencia, formando un mar de electrones rodeando un enrejado gigante
de cationes. Los metales tienen puntos de fusin ms altos por lo que se deduce que
hay enlaces ms fuertes entre los distintos tomos.
La vinculacin metlica es no polar, apenas hay (para los metales elementales puros) o
muy poca (para las aleaciones) diferencia de electronegatividad entre los tomos que
participan en la interaccin de la vinculacin, y los electrones implicados en lo que es la
interaccin a travs de la estructura cristalina del metal. El enlace metlico explica
muchas caractersticas fsicas de metales, tales como fuerza, maleabilidad, ductilidad,
conduccin del calor y de la electricidad, y lustre. La vinculacin metlica es la
atraccin electrosttica entre los tomos del metal o los iones y electrones
deslocalizados. Esta es la razn por la cual se explica un deslizamiento de capas,
dando por resultado su caracterstica maleabilidad y ductilidad.
Los tomos del metal tienen por lo menos un electrn de valencia, no comparten estos
electrones con los tomos vecinos, ni pierden electrones para formar los iones. En
lugar los niveles de energa externos de los tomos del metal se traslapan. Son como
enlaces covalentes identificados.
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
ENLACES QUIMICOS SECUNDARIOS
FUERZAS DE VAN DER WAALS
Cuando se encuentran a una distancia moderada, las molculas se atraen entre s
pero, cuando sus nubes electrnicas empiezan a solaparse, las molculas se repelen
con fuerza.
El trmino "fuerzas de van der Waals" engloba colectivamente a las fuerzas de
atraccin entre las molculas. Son fuerzas de atraccin dbiles que se establecen entre
molculas elctricamente neutras (tanto polares como no polares), pero son muy
numerosas y desempean un papel fundamental en multitud de procesos biolgicos.
Las fuerzas de van der Waals incluyen:
Fuerzas dipolo-dipolo (tambin llamadas fuerzas de Keesom), entre las que se
incluyen los puentes de hidrgeno
Fuerzas dipolo-dipolo inducido (tambin llamadas fuerzas de Debye)
Fuerzas dipolo instantneo-dipolo inducido (tambin llamadas fuerzas de
dispersin o fuerzas de London)
ENLACE METALICO EN EL COBRE
ENLACE METALICO EN EL ALUMINIO
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
FUERZAS DE POLARIDAD (DIPOLO-DIPOLO)
Una molcula es un dipolo cuando existe una distribucin asimtrica de los electrones
debido a que la molcula est formada por tomos de distinta electronegatividad. Como
consecuencia de ello, los electrones se encuentran preferentemente en las
proximidades del tomo ms electronegativo. Se crean as dos regiones (o polos) en la
molcula, una con carga parcial negativa y otra con carga parcial positiva (Figura
inferior izquierda).
Cuando dos molculas polares (dipolos) se aproximan, se produce una atraccin entre
el polo positivo de una de ellas y el negativo de la otra. Esta fuerza de atraccin entre
dos dipolos es tanto ms intensa cuanto mayor es la polarizacin de dichas molculas
polares o, dicho de otra forma, cuanto mayor sea la diferencia de electronegatividad
entre los tomos enlazados.
Los enlaces sern tanto ms polares cuanto mayor sea la diferencia de
electronegatividad entre los tomos enlazados.
El momento dipolar ( ) es un vector (orientado hacia la carga negativa y cuya magnitud
depende de la intensidad de la carga y de la distancia entre los tomos) que permite
cuantificar la asimetra de cargas en la molcula (Figura inferior izquierda). La forma de
la molcula tambin afecta al momento dipolar (Figura inferior derecha).
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
FUERZAS DIPOLO INSTANTNEO-DIPOLO INDUCIDO
Tambin se llaman fuerzas de dispersin o fuerzas de London. En muchos textos, se
identifican con las fuerzas de van der Waals, lo que puede generar cierta confusin.
Las fuerzas de dispersin son fuerzas atractivas dbiles que se establecen
fundamentalmente entre sustancias no polares, aunque tambin estn presentes en las
sustancias polares. Se deben a las irregularidades que se producen en la nube
electrnica de los tomos de las molculas por efecto de la proximidad mutua. La
formacin de un dipolo instantneo en una molcula origina la formacin de un dipolo
inducido en una molcula vecina de manera que se origina una dbil fuerza de
atraccin entre las dos.
En promedio, la
distribucin de cargas en
torno a una molecula
apolar es simtrica y no
hay momento dipolar
Las fuerzas de London
son fuerzas de
atraccin entre dipolos
que surgen de forma
transitoria
Sin embargo, a tiempos
cortos la nube electrnica
puede fluctuar, creando
momentos dipolares
instantneos
Estas fuerzas son mayores al aumentar el tamao y la asimetra de las molculas. Son
mnimas en los gases nobles (He, Ne), algo mayores en los gases diatmicos (H
2
, N
2
,
O
2
) y mayores an en los gases poli atmicos (O
3
, CO
2
).
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
PUENTES DE HIDRGENO
Los puentes de hidrgeno constituyen un caso especial de interaccin dipolo-dipolo (Figura de la
derecha). Se producen cuando un tomo de hidrgeno est unido covalentemente a un elemento
que sea:
muy electronegativo y con dobletes electrnicos sin compartir
de muy pequeo tamao y capaz, por tanto, de
aproximarse al ncleo del hidrgeno
Estas condiciones se cumplen en el caso de los
tomos de F, O y N.
El enlace que forman con el hidrgeno es muy polar y
el tomo de hidrgeno es un centro de cargas
positivas que ser atrado hacia los pares de
electrones sin compartir de los tomos
electronegativos de otras molculas (Figura de la
izquierda). Se trata de un enlace dbil (entre 2 y 10
Kcal/mol). Sin embargo, como son muy abundantes,
su contribucin a la cohesin entre biomolculas es
grande.
La distancia entre los tomos electronegativos unidos
mediante un puente de hidrgeno suele ser de unos 3 . El
hidrgeno se sita a 1 del tomo al que est covalentemente
unido y a 2 del que cede sus e- no apareados (Figura de la
derecha).
Este enlace es fundamental en bioqumica, ya que:
condiciona en gran medida la estructura espacial de las protenas y de los
cidos nucleicos y
est presente en gran parte de las interacciones que tienen lugar entre distintos
tipos de biomolculas en multitud de procesos fundamentales para los seres
vivos
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
Muchas de las propiedades fsicas y
qumicas del agua se deben a los puentes
de hidrgeno. Cada molcula de agua es
capaz de donar 4 puentes de hidrgeno, lo
que explica su elevado punto de ebullicin,
ya que es necesario romper gran cantidad
de puentes de hidrgeno para que una
molcula de agua pase al estado gaseoso.
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
SLIDO AMORFO
El slido amorfo es un estado slido de la materia, en el que las partculas que
conforman el slido carecen de una estructura ordenada. Estos slidos carecen de
formas y caras bien definidas. Esta clasificacin contrasta con la de slidos cristalinos,
cuyos tomos estn dispuestos de manera regular y ordenada formando redes
cristalinas.
Muchos slidos amorfos son mezclas de molculas que no se pueden apilar bien. Casi
todos los dems se componen de molculas grandes y complejas. Entre los slidos
amorfos ms conocidos destaca el vidrio.
Un mismo compuesto, segn el proceso de solidificacin, puede formar una red
cristalina o un slido amorfo. Por ejemplo, segn la disposicin espacial de las
molculas de slice (SiO
2
), se puede obtener una estructura cristalina (el cuarzo) o un
slido amorfo (el vidrio).
Diagrama molecular del cuarzo (SiO
2
) en red
cristalina
Diagrama molecular del vidrio (SiO
2
) en slido
amorfo
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
Artificialmente, existen varios mtodos de obtencin de slidos amorfos. El mtodo ms
antiguo y ms empleado es el de la fundicin templada, del que se conocen algunas
variedades:
Bloque congelado
Esta tcnica necesita de un alto rango de temperaturas
para el enfriamiento y formar una aleacin metlica. Un
chorro de metal fundido es propulsado contra la
superficie de un cilindro de cobre, el cual se encuentra
en rpida rotacin, lo que obliga al lquido a enfriarse (a
temperatura ambiente o menor). Dentro de la tcnica
del bloque congelado, se distingue entre splat-cooling y
el templado giratorio de extraccin.
Templado con lquido
Esta tcnica puede ser utilizada para el enfriamiento de lquidos, utilizando baos de
hielo en los cuales se introducen pequeas cantidades de fundido; permite enfriar con
rangos de velocidad altos.
Templado al aire
Esta tcnica puede ser utilizada para materiales con tendencia a la formacin de
slidos amorfos. Se puede obtener la fundicin con enfriamiento lento, lo cual se
consigue apagando el horno. Slidos amorfos obtenidos mediante este mtodo son
SiO
2
, As
2
S
3
y polietileno.
Condensacin del vapor
Esta tcnica comienza cuando el vapor formado en una cmara de vaco, por la
evaporacin del material, choca con una superficie fra, obtenindose una sustancia
amorfa.
ENLACES QUIMICOS PRIMARIOS Y SECUNDARIOS
CUATRIMESTRE: SEPTIEMBRE-DICIEMBRE SEPTIEMBRE 03 DEL 2010
Bibliografa
Wikipedia.com
Ciencia e Ingeniera de los Materiales, Donald R. Askeland
Editorial, Thompson.
También podría gustarte
- Práctica 6 - Procesos Químicos Y Corriente Eléctrica - Aldo Esaú Xoxocotla SánchezDocumento14 páginasPráctica 6 - Procesos Químicos Y Corriente Eléctrica - Aldo Esaú Xoxocotla Sánchezxozo land100% (1)
- Beer Solucionario-Mecanica-De-Materiales-7ma-Edicion-Beer-Jhonston-1-10-118577-DownloableDocumento11 páginasBeer Solucionario-Mecanica-De-Materiales-7ma-Edicion-Beer-Jhonston-1-10-118577-DownloableMARÍA FERNANDA HERNÁNDEZ GUTIÉRREZ100% (1)
- Taller de EjerciciosDocumento15 páginasTaller de EjerciciosSaray MaldonadoAún no hay calificaciones
- HibridacionDocumento79 páginasHibridacionGabriella ApAún no hay calificaciones
- CONCEPTO AlcanosDocumento4 páginasCONCEPTO AlcanosAlcides Coca MejiaAún no hay calificaciones
- Diferenciación de Isómeros de Alcoholes y Propiedades FísicasDocumento16 páginasDiferenciación de Isómeros de Alcoholes y Propiedades FísicasSarmiento DanielAún no hay calificaciones
- Tratamiento Efectivo Contra La Anemia en Pacientes Con Enfermedad Renal Crónica Usando ClorofilaDocumento4 páginasTratamiento Efectivo Contra La Anemia en Pacientes Con Enfermedad Renal Crónica Usando ClorofilajuanitaAún no hay calificaciones
- Relación Entre Los Enlaces Químicos, Materiales y Sus PropiedadesDocumento14 páginasRelación Entre Los Enlaces Químicos, Materiales y Sus PropiedadesRodrigo Andrés33% (3)
- La Rótula PlásticaDocumento18 páginasLa Rótula PlásticaBraulioLeopoldoFernandezCachiqueAún no hay calificaciones
- Discucion Grupal 2019Documento53 páginasDiscucion Grupal 2019Ibette NorttonAún no hay calificaciones
- AmeboideDocumento2 páginasAmeboideAdrian Urco CastroAún no hay calificaciones
- Regla de MarkovnikovDocumento7 páginasRegla de MarkovnikovFLORES05Aún no hay calificaciones
- Fuerzas Intermoleculares Lab PDFDocumento11 páginasFuerzas Intermoleculares Lab PDFANDERSON FABIER MOJICA LAVERDEAún no hay calificaciones
- Problemario Resuelto Unidad 8 ChangDocumento10 páginasProblemario Resuelto Unidad 8 Changnicol fernanda quispe torresAún no hay calificaciones
- Enlace QuimicoDocumento30 páginasEnlace QuimicoAngela Mendo GuibertAún no hay calificaciones
- Metales Alcalinos y AlcalinotérreosDocumento7 páginasMetales Alcalinos y AlcalinotérreosDavid F RábagoAún no hay calificaciones
- Practica Laboratorio 02Documento10 páginasPractica Laboratorio 02Renán Hector Sánchez Cerna100% (1)
- Sublimacion y Punto de FusionDocumento9 páginasSublimacion y Punto de Fusionsamuel palacioAún no hay calificaciones
- Clase 8. Metabolismo EnergéticoDocumento105 páginasClase 8. Metabolismo EnergéticoJuanCaicedo77Aún no hay calificaciones
- ComplejosDocumento7 páginasComplejosMaggi Condori GuarachiAún no hay calificaciones
- CUESTINARIO CrustaceosDocumento5 páginasCUESTINARIO CrustaceosAdriana SantosAún no hay calificaciones
- Práctica 3 Tabla Periodica y Propiedades PeriodicasDocumento4 páginasPráctica 3 Tabla Periodica y Propiedades PeriodicasMario Edwin Martinez Corona0% (1)
- Fenomenos ElectrostaticosDocumento5 páginasFenomenos ElectrostaticosLaura RiveraAún no hay calificaciones
- Practica 3Documento3 páginasPractica 3CAROLINA HERRERAAún no hay calificaciones
- Informe 2 BotanicaDocumento6 páginasInforme 2 Botanicaangello500Aún no hay calificaciones
- Taller Introducción Al Curso de Bioquímica JoseDocumento6 páginasTaller Introducción Al Curso de Bioquímica JoseJHOJAN RICO ARROYOAún no hay calificaciones
- EnviarDocumento16 páginasEnviaresneider linares romeroAún no hay calificaciones
- Práctica Nº1 - Disección de Una Rata-InformeDocumento13 páginasPráctica Nº1 - Disección de Una Rata-InformeAlexanderSpdpAún no hay calificaciones
- Informe 5 - TinciónDocumento7 páginasInforme 5 - TinciónChristopher Sanchez VegaAún no hay calificaciones
- Informe 2 Quimica OrganicaDocumento3 páginasInforme 2 Quimica OrganicaBernardo SandovalAún no hay calificaciones
- Practica de La Purificacion de La LECTINADocumento8 páginasPractica de La Purificacion de La LECTINACesarAún no hay calificaciones
- Uniones 1Documento1 páginaUniones 1Sofía Torroledo RamírezAún no hay calificaciones
- Uce InformeDocumento9 páginasUce InformeAngel ZevallosAún no hay calificaciones
- Informe 2Documento20 páginasInforme 2Javier MorenoAún no hay calificaciones
- HiperconjugaciónDocumento3 páginasHiperconjugaciónAlejaGoRuAún no hay calificaciones
- Nomenclatura (R) y (S) de Compuestos OrganicosDocumento10 páginasNomenclatura (R) y (S) de Compuestos OrganicosFranklin A.C.Aún no hay calificaciones
- Capitulo 1 - Ensayo Historia de La Biología MolecularDocumento5 páginasCapitulo 1 - Ensayo Historia de La Biología MolecularKimberly Nieto MoreaAún no hay calificaciones
- Estructura Interna y Externa de La FlorDocumento16 páginasEstructura Interna y Externa de La Florbrayan de hoyosAún no hay calificaciones
- S7 - 1 - Estereoisómeros Configuracionales - EMVDocumento41 páginasS7 - 1 - Estereoisómeros Configuracionales - EMVJocelyn Grisel García GonzálezAún no hay calificaciones
- Los Electrodos de MembranaDocumento2 páginasLos Electrodos de MembranaOsborn ArtolaAún no hay calificaciones
- VELOCIDAD DE REACCIÓN ENZIMÁTICA Y DETERMINACIÓN DEL Pi DE UNA PROTEÍNADocumento13 páginasVELOCIDAD DE REACCIÓN ENZIMÁTICA Y DETERMINACIÓN DEL Pi DE UNA PROTEÍNAFernanda CarrilloAún no hay calificaciones
- 12 Mitosis Equipo 4Documento7 páginas12 Mitosis Equipo 4Juan Volta BellamyAún no hay calificaciones
- PRACTICA 1 BioseguridadDocumento9 páginasPRACTICA 1 BioseguridadDiazDenisse0% (1)
- Taller Fisicoquimica 23401 Parte IDocumento5 páginasTaller Fisicoquimica 23401 Parte IKevin PavaAún no hay calificaciones
- Mapa de DestinoDocumento2 páginasMapa de Destinowallesm123Aún no hay calificaciones
- Entalpia de Formacion de Una SalDocumento7 páginasEntalpia de Formacion de Una SalOscar PortilloAún no hay calificaciones
- Introducción A Las Fuerzas IntermolecularesDocumento5 páginasIntroducción A Las Fuerzas IntermolecularesMágicos OchentasAún no hay calificaciones
- OPERONDocumento15 páginasOPERONGineth MaderaAún no hay calificaciones
- Laboratorio 3 BiologiaDocumento14 páginasLaboratorio 3 BiologiaCM35100% (1)
- Obtencion Del MetanoDocumento5 páginasObtencion Del MetanodilsaAún no hay calificaciones
- Informe TerminadoDocumento14 páginasInforme TerminadoGabriel Monzòn LunaAún no hay calificaciones
- Prac6 Las Flores e InflorescenciasDocumento14 páginasPrac6 Las Flores e InflorescenciasIhan Howard Rios LedesmaAún no hay calificaciones
- VOLVOXDocumento3 páginasVOLVOXisaac_pollon95Aún no hay calificaciones
- Citoesqueleto ForoDocumento39 páginasCitoesqueleto ForoClaudia Montes GuerraAún no hay calificaciones
- Cuestionario SemillaDocumento1 páginaCuestionario SemillaDamián Alexander0% (1)
- Informe de AnelidosDocumento11 páginasInforme de AnelidosRigobertoAún no hay calificaciones
- Taller BiologiaDocumento5 páginasTaller Biologiadayanna caballeroAún no hay calificaciones
- Práctica 5 OrgánicaDocumento24 páginasPráctica 5 OrgánicaOlga Tatiana Reyes PayaresAún no hay calificaciones
- Relación Entre Los Enlaces Químicos, Materiales y Sus PropiedadesDocumento14 páginasRelación Entre Los Enlaces Químicos, Materiales y Sus PropiedadesRodrigo AndrésAún no hay calificaciones
- Informe 3Documento14 páginasInforme 3Miguel Angel Chavez GuillenAún no hay calificaciones
- EnlacesDocumento6 páginasEnlacesMichell SanchezAún no hay calificaciones
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseDe EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Momento Amplficado para Columnas-EjemploDocumento7 páginasMomento Amplficado para Columnas-EjemploLuiggi Wilmer Bellota GonzalesAún no hay calificaciones
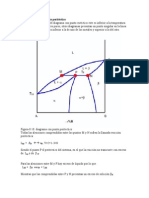
- PeritecticoDocumento3 páginasPeritecticoRenata Figon100% (1)
- Tecnologia de Procesos y Materiales - Metales Ferrosos y No FerrososDocumento12 páginasTecnologia de Procesos y Materiales - Metales Ferrosos y No FerrososArturo MontielAún no hay calificaciones
- Flechas y Ejes Solo en Flexión y TorsiónDocumento27 páginasFlechas y Ejes Solo en Flexión y TorsiónCristiano Alejandro Cortes0% (1)
- Reistencia de MaterialesDocumento21 páginasReistencia de MaterialesDina Flor Chavez CollantesAún no hay calificaciones
- 1 Comp MecDocumento8 páginas1 Comp MecEdgar BenitezAún no hay calificaciones
- Diagramas de EquilibrioDocumento26 páginasDiagramas de Equilibrioninoghg100% (3)
- Pavement Analysis and Design by Yang H. HuangDocumento36 páginasPavement Analysis and Design by Yang H. HuangGabriel Arias Tabraj100% (1)
- Lab Prueba de Tension SimpleDocumento17 páginasLab Prueba de Tension SimpleRuisu Shirayuki Yūka NaAún no hay calificaciones
- 13 AluminioDocumento51 páginas13 AluminioCarloXs Xs MglAún no hay calificaciones
- Compresion Paralela A La Fibra - MaderaDocumento7 páginasCompresion Paralela A La Fibra - MaderaJeiver RodriguezAún no hay calificaciones
- Curvas TTTT Ciencias MaterialesDocumento16 páginasCurvas TTTT Ciencias MaterialesIbeth Henao de AponteAún no hay calificaciones
- Defectos CristalinosDocumento26 páginasDefectos CristalinosAsbleIdis Fernandez MejiaAún no hay calificaciones
- Evaluacion de Vigas de Madera Mediante UltrasonidoDocumento15 páginasEvaluacion de Vigas de Madera Mediante UltrasonidoAly HuaytallaAún no hay calificaciones
- Trabajo Practico Fisica II ComplDocumento20 páginasTrabajo Practico Fisica II ComplGrébneva AlënaAún no hay calificaciones
- Cap 1 Falla Estatica 02 TXTDocumento10 páginasCap 1 Falla Estatica 02 TXTEla HAún no hay calificaciones
- 1pcisia040620150 CañoteDocumento1 página1pcisia040620150 Cañotecarlos muñozAún no hay calificaciones
- 2 Esfuerzo Biaxial y TriaxialDocumento18 páginas2 Esfuerzo Biaxial y TriaxialMiguel Angel Anticona Guillen100% (3)
- Metalografía y Estudio de Los MaterialesDocumento17 páginasMetalografía y Estudio de Los MaterialesFernando Sanz CamachoAún no hay calificaciones
- DEFORMACIONDocumento9 páginasDEFORMACIONAlexis VillalbaAún no hay calificaciones
- Informe de FenomenosDocumento15 páginasInforme de FenomenosMarceloCisternasAún no hay calificaciones
- Concreto MCH 3Documento2 páginasConcreto MCH 3lollydrewAún no hay calificaciones
- Nociones de Resistencia de MaterialesDocumento11 páginasNociones de Resistencia de MaterialesRichard FlemingAún no hay calificaciones
- Rigidez de ArbolesDocumento12 páginasRigidez de Arboleslubeni22Aún no hay calificaciones
- Solucionario Holman Transferencia de Calor KarlekarDocumento4 páginasSolucionario Holman Transferencia de Calor KarlekarJ David Diaz0% (2)
- Curva Esfuerzo Deformación Del AceroDocumento5 páginasCurva Esfuerzo Deformación Del AceroEdisonQuishpe100% (1)
- Examen Diagnostico Diagrama de Fases.Documento10 páginasExamen Diagnostico Diagrama de Fases.Angel DoroteoAún no hay calificaciones
- Resistencia de MaterialesDocumento14 páginasResistencia de MaterialesperezAún no hay calificaciones