Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Formulario Química
Cargado por
her217430 calificaciones0% encontró este documento útil (0 votos)
6 vistas2 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
6 vistas2 páginasFormulario Química
Cargado por
her21743Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
Formulario Química
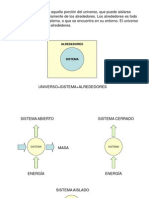
Sistema abierto: intercambio masa y energía en forma de calor
Sistema cerrado: transfiere energía (calor) pero no transfiere masa
Sistema aislado: no transfiere ni masa ni agua.
Endotérmico: +; Exotérmico: -
La suma de los cambios de energía debe ser igual a cero:
ΔUsist +ΔUalred=0
ΔUsist =- ΔUalred
Primera Ley de termodinámica: ΔU= q+w
ΔU: cambio en la energía interna
Q: suma del intercambio de calor entre el sistema y alrededores
W: trabajo realizado sobre o por el sistema
Trabajo: w=F*D
F: fuerza
D: distancia
Trabajo que realiza el gas sobre los alrededores: w=-P ΔV
P: presión atmosférica externa
ΔV cambio de volume
ΔV >0 y por eso la P es una cantidad negativa
1L*atm= 101.3J
Para calcular cambio de energía usar: ΔU= q+w
*Si el problema dice que libera energía, el signo de q es positivo, de lo contrario es
negativo
Entalpía: H= U+PV
U: energía interna del sistema
P: presión
V: volumen
En la entalpía, si la presión se mantiene constante usar: ΔH= ΔU+PΔV
Entalpía de reacción (ΔHreac): ΔH= H(productos)- H (reactivos)
Calcular el cambio de energía interna: ΔU= ΔH- PΔV
Relación entre capacidad calorífica y calor específico: C=ms
M= masa de sustancia en gramos
S= calor específico
Ecuaciones para calcular el cambio de calor: q= msΔt; q= CΔt
M: masa; s: calor específico; Δt: cambio de temp
C: calor específico
Calor de disolución: ΔHdisol= Hdisol- Hcomponentes
Velocidad de onda: u=λv
Λ: longitud de onda (lambda)
V(nu): frecuencia (número de ondas que pasan por un punto particular en un sec)
1Hz= 1 ciclo
Cuando piden encontrar una frecuencia usar: v= c/λ (c: velocidad luz)
Teoría de Planck: E=hv o también E= H* C/ λ
E: energía de un fotón
H: constante de Planck
V: frecuencia
Constante de Planck: 6.63* 10-34 J*S
Para calcular energía cinética:hv=EC+W o también EC= hv-W
EC: energía cinética
W: trabajo
Fuerzas dipolo- dipolo: fuerzas de atracción entre moléculas polares
Fuerzas ion-dipolo: atraen entre sí un ion y una molécula polar
Dipolo inducido: la separación de cargas positva y negativa se debe a la proximidad de un ion o
una molécula polar.
También podría gustarte
- Semana N°3 - Primera Ley de La TermodinámicaDocumento20 páginasSemana N°3 - Primera Ley de La TermodinámicaLesly PeredaAún no hay calificaciones
- Termoquímica (1-41) - 1Documento41 páginasTermoquímica (1-41) - 1Enrique Hernandez LiraAún no hay calificaciones
- Tema 2-TermoDocumento32 páginasTema 2-TermoNoemí DaSilvaAún no hay calificaciones
- 3-Primera LeyDocumento52 páginas3-Primera LeySofi RomeroAún no hay calificaciones
- S01.s1 - TermodinámicaDocumento28 páginasS01.s1 - Termodinámicaluis martin pachas parionaAún no hay calificaciones
- SESION 9-Termoquìmica.Documento29 páginasSESION 9-Termoquìmica.Gabriel Armando Orellana NolascoAún no hay calificaciones
- Primera Ley de TermodinamicaDocumento71 páginasPrimera Ley de TermodinamicaAndreaAún no hay calificaciones
- TERMODINAMICADocumento71 páginasTERMODINAMICAFederico MoralesAún no hay calificaciones
- 1 0 Leyes-TermodinámicasDocumento65 páginas1 0 Leyes-TermodinámicasJandir Nicolás Chigne PlasenciaAún no hay calificaciones
- Tema 2 (Resumen) (1) - TaggedDocumento19 páginasTema 2 (Resumen) (1) - TaggedMohamed NadwiAún no hay calificaciones
- Entalpía TermodinámicaDocumento3 páginasEntalpía TermodinámicaRonaldoAún no hay calificaciones
- Formulas Unidad 4Documento32 páginasFormulas Unidad 4diego leonAún no hay calificaciones
- Balance de MateriaDocumento6 páginasBalance de MateriaCarlos MonarcaAún no hay calificaciones
- Termoqu ImicaDocumento18 páginasTermoqu ImicabarlosAún no hay calificaciones
- Tema - 3 - Termodinámica QuímicaDocumento44 páginasTema - 3 - Termodinámica QuímicaJose GutierrezAún no hay calificaciones
- Unidad 2 Intro. TermoquimicaDocumento31 páginasUnidad 2 Intro. TermoquimicadiegoAún no hay calificaciones
- Unidad Vii Iqu 2016 TermquimicaDocumento67 páginasUnidad Vii Iqu 2016 TermquimicaFernanda Vera-ValverdeAún no hay calificaciones
- 1, 2 y 3 Ley de La TermodinamicaDocumento62 páginas1, 2 y 3 Ley de La Termodinamicaosvaldo denizAún no hay calificaciones
- ppt.S09 - VFDocumento29 páginasppt.S09 - VFKokaAún no hay calificaciones
- Termoquimica Parte IIDocumento45 páginasTermoquimica Parte IIMc Gabo.16Aún no hay calificaciones
- TermodinamicaxxDocumento41 páginasTermodinamicaxxDebo LafuenteAún no hay calificaciones
- Energía InternaDocumento10 páginasEnergía InternaAlejandra MonteverdeAún no hay calificaciones
- Procesos Fisicos de GasesDocumento40 páginasProcesos Fisicos de GasesPaulina SantanaAún no hay calificaciones
- Termo 2021Documento70 páginasTermo 2021singhjudith13Aún no hay calificaciones
- 1era Ley de La Termodinamica-Morales Fuentes Rivera, MiguelDocumento40 páginas1era Ley de La Termodinamica-Morales Fuentes Rivera, MiguelMiguel MfrAún no hay calificaciones
- Wuolah-Capítulo 3Documento9 páginasWuolah-Capítulo 3ksaweryjpcAún no hay calificaciones
- Funciones Auxiliares de TermodinamicaDocumento8 páginasFunciones Auxiliares de TermodinamicaJhoel ChaucaAún no hay calificaciones
- Informe 2 Lab. FisicoquimicaDocumento9 páginasInforme 2 Lab. FisicoquimicaBeimar PeñaAún no hay calificaciones
- S05. s1 - Material de Clase (Termodinamica)Documento31 páginasS05. s1 - Material de Clase (Termodinamica)AaronAún no hay calificaciones
- Gases Ideales Primera LeyDocumento37 páginasGases Ideales Primera LeyJean Carlo GonzalesAún no hay calificaciones
- Equilibrio fisicoquimicoU1-2019NyoEnDocumento18 páginasEquilibrio fisicoquimicoU1-2019NyoEnMarco Daniel ZapataAún no hay calificaciones
- Teoría de La Primera UnidadDocumento15 páginasTeoría de La Primera UnidadZarialmlAún no hay calificaciones
- S09.s1 - Introducción A La TermodinámicaDocumento29 páginasS09.s1 - Introducción A La TermodinámicaMilagros Obregon VilcaAún no hay calificaciones
- Geoquimica Clase 4Documento39 páginasGeoquimica Clase 4Centro de Estudiantes De GeologíaAún no hay calificaciones
- Cambios de Energia en Las Reacciones Quimicas Clase 2Documento34 páginasCambios de Energia en Las Reacciones Quimicas Clase 2DENNIS HERRERAAún no hay calificaciones
- TermoquímicaDocumento13 páginasTermoquímicaalbayance2002Aún no hay calificaciones
- Equilibrio Fisico-Quimico Unidad 1Documento17 páginasEquilibrio Fisico-Quimico Unidad 1Marco Daniel ZapataAún no hay calificaciones
- TERMODINAMICADocumento43 páginasTERMODINAMICAJohan Rosas TaipeAún no hay calificaciones
- Propiedades Termodinamicas de Los FluidosDocumento25 páginasPropiedades Termodinamicas de Los FluidosmichelleAún no hay calificaciones
- Termoquimica 2021 MTDocumento42 páginasTermoquimica 2021 MTDenis GiubiAún no hay calificaciones
- S05.s1 - Material - TermodinámicaDocumento45 páginasS05.s1 - Material - TermodinámicaRoberto Quispe EscarcenaAún no hay calificaciones
- Clase 5 - 1ER PRINC TERMO - ENERGIA INTERNADocumento36 páginasClase 5 - 1ER PRINC TERMO - ENERGIA INTERNABoris HergenretherAún no hay calificaciones
- Unidad IVDocumento6 páginasUnidad IVcanaima linuxAún no hay calificaciones
- TERMOQUIMICADocumento34 páginasTERMOQUIMICAOli Ve RtAún no hay calificaciones
- IsobaricoDocumento2 páginasIsobaricoLuis Yacelga MejíaAún no hay calificaciones
- CAP 6 PRIMER PRINCIPIO DE TERMODINÁMICA. Parte 3 Trabajo en Procesos FísicosDocumento29 páginasCAP 6 PRIMER PRINCIPIO DE TERMODINÁMICA. Parte 3 Trabajo en Procesos FísicosDaniel FeymanAún no hay calificaciones
- Cap 6 Primer Principio de Termodinámica. Parte 3 Trabajo en Procesos FísicosDocumento29 páginasCap 6 Primer Principio de Termodinámica. Parte 3 Trabajo en Procesos FísicosMauricio Carlos Quispe ApazaAún no hay calificaciones
- Termoquímica (Apuntes)Documento12 páginasTermoquímica (Apuntes)JSTCAún no hay calificaciones
- Termodinamica IntroducciónDocumento9 páginasTermodinamica IntroducciónrolyAún no hay calificaciones
- Leyes de La TermodinámicaDocumento19 páginasLeyes de La TermodinámicaRoberto TraconisAún no hay calificaciones
- 1 Ley Termodinámica-Calor V2018-2Documento45 páginas1 Ley Termodinámica-Calor V2018-2Yourladys ElenaAún no hay calificaciones
- Clase 16Documento22 páginasClase 16Juan Carlos Valencia BravoAún no hay calificaciones
- Capitulo 1. TermoquímicaDocumento37 páginasCapitulo 1. TermoquímicaJosé MedinaAún no hay calificaciones
- Colaborativo 1 TermodinamicaDocumento37 páginasColaborativo 1 TermodinamicaHarry RamosAún no hay calificaciones
- TermoquímicaDocumento34 páginasTermoquímicaalvaro luqueAún no hay calificaciones
- Semana 2 2012Documento8 páginasSemana 2 2012quimicocad9891Aún no hay calificaciones
- Leccion 5-4Documento28 páginasLeccion 5-4CONSUELO VICTORIA CARASAS MORIAún no hay calificaciones
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Psicometría. Principios básicos y protocolos experimentales diversosDe EverandPsicometría. Principios básicos y protocolos experimentales diversosAún no hay calificaciones
- Prelab 1 CircuitosDocumento7 páginasPrelab 1 Circuitosher21743Aún no hay calificaciones
- Hoja de Trabajo 2 QuímicaDocumento2 páginasHoja de Trabajo 2 Químicaher21743Aún no hay calificaciones
- Comprobación 6Documento1 páginaComprobación 6her21743Aún no hay calificaciones
- Comprobación 7Documento1 páginaComprobación 7her21743Aún no hay calificaciones