0% encontró este documento útil (0 votos)
47 vistas4 páginasSíndrome de Cushing en hombres
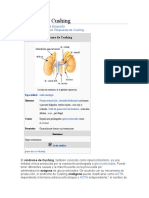
El síndrome de Cushing se produce por una exposición excesiva a las hormonas glucocorticoideas y puede ser endógeno o exógeno. Los síntomas incluyen obesidad central, estrías, hipertensión e hiperglicemia. El tratamiento depende de la causa subyacente y puede incluir cirugía, medicamentos u otros enfoques.
Cargado por
Valentina Gelves CardenasDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
47 vistas4 páginasSíndrome de Cushing en hombres
El síndrome de Cushing se produce por una exposición excesiva a las hormonas glucocorticoideas y puede ser endógeno o exógeno. Los síntomas incluyen obesidad central, estrías, hipertensión e hiperglicemia. El tratamiento depende de la causa subyacente y puede incluir cirugía, medicamentos u otros enfoques.
Cargado por
Valentina Gelves CardenasDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd