Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Apunte Noeli Aminoacidos
Cargado por
borja florezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Apunte Noeli Aminoacidos
Cargado por
borja florezCopyright:
Formatos disponibles
Por Noelí Torres
Metabolismo de aminoácidos
Digestión de proteínas
Las proteasas lisosomales (catepsinas) degradan las proteínas que entran a los lisosomas.
Las proteínas ubiquinizadas (recambio celular), degradadas por el proteasoma. Este proceso
requiere ATP y los aminoácidos liberados son usados para la síntesis de nuevas proteínas o para
obtener energía.
La pepsina es una endopeptidasa que corta en varios puntos dentro de la molécula, aunque tiene
mas especifidad en enlaces peptídicos en las que el grupo carboxilo proviene de un aminoácido
aromático o acídico.
La tripsina es una enzima de origen pancreático, que se sintetiza como tripsinógeno y que es
activada por una enteroquinasa y por autocatálisis. Su acción principal se basa en la hidrólisis de las
proteínas de la dieta, preferentemente sobre aminoácidos básicos y con carácter de endopeptidasa
(aspartil-enzima), actuando a un pH óptimo de 8.
La secretina, es una enterohormona que estimula la secreción pancreática de bicarbonato. La
secretina es sintetizada por las células S de la mucosa del duodeno y yeyuno. Es un pequeño
polipéptido, cuyo estímula para su síntesis es el descenso de pH del duodeno, ante la llegada del
quimo acido del estómago. Principalmente, estimula la secreción de jugo pancreático rico en
bicarbonato, contribuyendo a neutralizar el pH del duodeno, ante la llegada del quimo acido del
estómago. Principalmente, estimula la secreción de jugo pancreático rico en bicarbonato,
contribuyendo a neutralizar el quimo acido que llega del estómago al intestino. Por otra parte inhibe
la secreción gástrica de HCl y retarda el vaciamiento gástrico.
La enteropeptidasa es una proteasa secretada por las células del borde en cepillo del intestino
delgado.
La gastrina es secretada por las células G del estómago, en respuesta a la distensión mecánica del
antro gástrico, la actividad vagal, dietas hiperproteicas y a la elevación del pH de la mucosa. Actúa
por sus cinco aminoácidos terminales (por eso, el nombre de pentagastrina). Su acción fisiológica
radica en un aumento de la secreción de ácido clorhídrico y acción trófica gástrica.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
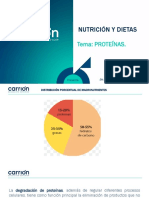
A los distintos aa los podemos dividir en esenciales y no esenciales, es decir los que debemos consumir
de la dieta y los que no es necesario respectivamente.
Una dieta libre de proteínas produce
una pérdida neta de proteínas
corporales de alrededor de 0.34 g/kg
de peso/día. Se recomienda que entre
el 10 al 15% del ingreso calórico
provenga de proteínas.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
Degradación de aminoácidos
Las reacciones de transaminación tienen constantes de equilibrio cercanas a 1, por lo tanto son
fácilmente reversibles.
El NH3 es altamente tóxico sobre todo para el sistema nervioso, pero existen mecanismos de
detoxificación que lo eliminan o lo convierten en metabolitos no tóxicos.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
Paso 1: Transaminación
La mayoría de las transaminasas son citoplasmáticas, aunque también existen mitocondriales y
precisan del fosfato de piridoxal (Vit B6).
Paso 2 : Desaminación oxidativa (súper importante)
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
• ↑ ATP o GTP : la reacción ira hacia glutamato (lo que frena las transaminaciones de los
aminoácidos y pueden ser estos, usados para la síntesis de proteínas).
• ↑ ADP o GDP : la reacción ira hacia α-cetoglutarato que ira al ciclo de Krebs para obtener
energía.
• La glutamato deshidrogenasa es la enzima mas importante en el metabolismo de los
aminoácidos y es una enzima citosólica.
• Como las transaminasas y GDH son reacciones reversibles, cuando aumenta el contenido de
cualquier aminoácido, se alcanzara fácilmente el equilibrio en la reacción de
transdesaminación porque la Keq es cercana a 1, por lo tanto ese grupo amino de ese
aminoácido será transferido al glutamato quien a su vez reversiblemente por la reacción
catalizada por la GDH se transformara en α-cetoglutarato. Pero recordar que aun ante alta
energía y porque la Keq de estas reacciones es cercana a 1, no se puede evitar que algunos
aa se degraden y el resto se usara para la síntesis de proteínas (los que no se degradan).
• Si bien existen transaminasas en todos los tejidos, en el hígado, hay una gran concentración
de estas enzimas, por eso mismo se toma como una medida diagnostica de daño hepático
cuando se encuentra aumentada en sangre.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
• Cuando acoplamos las dos reacciones, tenemos una reacción de transdesaminación.
• Las transaminasas catalizan la transferencia del grupo amino para la formación de L-
glutamato, el cual posteriormente sufrirá la desaminación oxidativa por la enzima glutamato
deshidrogenasa a nivel mitocondrial. Por eso, el proceso global recibe el nombre de
transdesaminación.
• Ítem: paso 1 + paso 2---- TRANSDESAMINACIÓN!!!
Otras reacciones de desaminación
Estas reacciones están catalizadas por una enzima llamada L-aminoácido oxidasas (son de baja
actividad).
En las desaminaciones no oxidativas
no hay una oxidación neta de la
molecula, sino que hay una
distribución intramolecular de los
electrones. Este tipo de reacciones
también requieren de piridoxal
fosfato (vit B6) como cofactor.
Paso 3: Reacciones de detoxificación del amoníaco
▪ Síntesis de Glutamato
▪ Síntesis de Glutamina
▪ Síntesis de Alanina
▪ Síntesis de Urea (súper importante)
a. Síntesis de glutamato
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
b. Síntesis de glutamina: La glutamina al no tener carga neta (el glutamato tiene una carga
neta -), es un buen transportador de amoniaco no toxico y dado que es una molécula neutra,
atraviesa con mayor facilidad las membranas biológicas que el glutamato.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
c. Síntesis de alanina
En el músculo la concentración de ALAT (GPT) es muy alta. Esto favorece el ciclo de Glucosa-Alanina
entre músculo e hígado.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
d. Síntesis de UREA
La urea es el producto final no toxico de eliminación de nitrógeno en el hombre y otros
vertebrados ureotelicos (excretan amoniaco como urea) a diferencia de aves y reptiles que
eliminan el amoniaco como acido urico y por eso se los denomina uricotélicas. Algunos
peces y anfibios eliminan el exceso de nitrógeno en forma de amoniaco y se las llama
amoniotélicas.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
• Ocurre exclusivamente en el Hígado.
• CPS II: Se expresa en el citosol de todos los tipos celulares→ síntesis de pirimidinas.
• CPS I : Se expresa exclusivamente en las mitocondrias hepáticas → ciclo de la urea.
• El aspartato se forma en la mitocondria por transaminación del oxalacetato en una reacción
catalizada por la aspartato aminotransferasa (ASAT), siendo el glutamato el dador del grupo
amino.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
Regulación del ciclo de la urea
▪ Aumenta con dietas ricas en proteínas → Se usan los esqueletos carbonados para obtener
energía. (↑expresión de las 5 enzimas)
▪ Aumenta en estado de ayuno → hay un aumento en el catabolismo de proteínas.
(↑expresión de las 5 enzimas)
▪ Aumenta en DBT no controlada. (↑expresión de las 5 enzimas)
▪ La CPS I es activada alostéricamente por N-acetilglutamato. Este modulador se sintetiza a
partir de glutamato y acetil CoA, en una reacción catalizada por la N-acetilglutamato
sintetasa. Esta enzima, a su vez es activada por arginina, que se acumula cuando la
producción de urea es muy baja.
Balance del ciclo de la urea
▪ HCO3 + NH4+ + 3 ATP + Aspartato + 2 H2O → Urea + 2 ADP + 2 Pi + AMP + PPi + Fumarato
▪ En intestino por la flora intestinal Urea → CO2 + 2 NH3
▪ Las enzimas se encuentran en forma de complejos enzimáticos.
▪ Si la urea llega al tracto intestinal, las bacterias de la flora poseen la enzima ureasa. El NH3
sintetizado por esta enzima, vuelve al hígado donde vuelve a formar parte de la urea
sintetizada en este órgano.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
▪ Las 5 enzimas descriptas aumentan en casos de dietas altas en proteínas y en ayunos
severos.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
Aprovechamiento del esqueleto carbonado por los distintos órganos
SNC: La síntesis de L-glutamina, por medio de la enzima glutamina sintetasa, es un mecanismo
de eliminación de amoníaco importante en tejidos como el hígado, músculo esquelético, riñones
y muy especialmente, el cerebro, el cual es muy sensible a la presencia de amoníaco. Recordar
que en el cerebro no existe formación de urea. En el cerebro el glutamato es el principal
neurotransmisor excitatorio. En las células de sostén la enzima es
Intestino: recambio de bases, por lo tanto los aa que usamos en metabolismo de bases
principalmente.
Hígado: utiliza todos los aminoácidos pero en menor proporción los ramificados
Músculo: aa raminificados
Riñón: glutamina por excelencia. La glutaminasa cataliza la hidrólisis de la L-glutamina con
liberación de L-glutamato y amonio. Se encuentra en el hígado y especialmente, en los túbulos
renales, donde la producción de amonáco y su eliminación por la orina constituyen uno de los
mecanismos más importantes de regulación del equilibrio ácido-base y de conservación de
cationes por parte del riñón.
Productos especiales de aa
1. Catecolaminas
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
Son sintetizadas desde la tirosina, puede venir de la dieta o puede venir del hígado a partir de
fenilalanina.
Cuando hay déficit enzimático de dihidrobiopterina reductasa el producto acumulado es el
fenilpiruvato producto acumulado en la fenilcetonuria.
Cuando hay un defecto en la reacción catalizada por la fanilalanina hidroxilasa, la fenilalanina se
acumula en sangre y se equilibra con su producto de transaminación, fenilpiruvato. Este
compuesto en parte se excreta y también se convierte en fenilactato y fenilacetato por
reducción y descarboxilación oxidativa respectivamente. Estos productos son excretados en la
orina.
La fenilcetonuria es un trastorno hereditario donde el fenilpiruvato es un metabolito
neurotóxico que afecta gravemente al cerebro durante el crecimiento y el desarrollo. Los efectos
de su acumulación causan oligofrenia fenilpirúvica o fenilcetonuria, caracterizada por un
cociente intelectual bajo. Los primeros meses de vida los niños que padecen esta enfermedad
parecen estar sanos. Entre los tres y los seis meses pierden el interés por el entorno, y al año se
evidencia un retraso importante en su desarrollo. Los síntomas suelen ser retraso psicomotor,
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
cuadros psicóticos de tipo autista, convulsiones, convulsiones generalizadas y un eczema facial
muy rebelde. Por lo general su desarrollo físico es bueno, tienden a tener el cabello más claro
que sus hermanos, piel clara, y ojos claros (se afecta también la formación de melanina).
Los destinos metabólicos del aminoácido L-fenilalanina son: a. L-tirosina; b. fenilpiruvato; fenil-
lactato; fenilacetato; por su parte, la L-tirosina tiene como destinos:
a) fumarato y acetoacetato;
b.hormona tiroidea;
c. melanina; d. catecolaminas. La histamina proviene de la L-histidina; la serotonina, del
aminoácido L-triptofano; a su vez, la melatonina se origina de la serotonina. El ácido gamma-
aminobutírico(GABA) se origina de la decarboxilación del L-glutamato.
• CREATINA FOSFATO
La L-arginina por una aminotransferasa se transforma en guanidoacetato, el cual por una metil
transferasa en presencia de S-Adenosil-Metionina forma creatina fosfato.
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
Por Noelí Torres
Regla memo: qiss
Este contenido es parte del Curso Online de Filadd.
Para ver más contenidos como este ingrese a: https://filadd.com/cursos-academia-filadd
consultas@filadd.com + 54 9 3517593395 @filadd_web Filadd
También podría gustarte
- Las Enzimas Teoría Capsula 1Documento8 páginasLas Enzimas Teoría Capsula 1Ariel MojicaAún no hay calificaciones
- Metabolismo de Las ProteínasDocumento10 páginasMetabolismo de Las ProteínasmarimarthaAún no hay calificaciones
- MONOGRAFIADocumento30 páginasMONOGRAFIAJoseph Valdez GarcíaAún no hay calificaciones
- Guía 1 Parcial de FisiologíaDocumento9 páginasGuía 1 Parcial de FisiologíaRivera Gómez América LucíaAún no hay calificaciones
- Guias BioqumicaDocumento25 páginasGuias BioqumicaAbner Eliu LealAún no hay calificaciones
- Metabolismo de ProteinasDocumento56 páginasMetabolismo de ProteinasAngie Lizeth Osma ChAún no hay calificaciones
- Teórico 13 Dra. Rosenstein - Metabolismo de Aminoácidos - 2018Documento24 páginasTeórico 13 Dra. Rosenstein - Metabolismo de Aminoácidos - 2018Nandy PachecoAún no hay calificaciones
- Resumen Unidad 6 201820Documento4 páginasResumen Unidad 6 201820Fernanda BecerraAún no hay calificaciones
- LipidosDocumento5 páginasLipidosKERENAún no hay calificaciones
- Sem 12 File 3Documento26 páginasSem 12 File 3Daniela MatamalaAún no hay calificaciones
- Expo de Aminoácidos 2.0Documento40 páginasExpo de Aminoácidos 2.0Jimmy ArroligaAún no hay calificaciones
- GLUCONEOGÉNESISDocumento15 páginasGLUCONEOGÉNESISNelsys GonzalezAún no hay calificaciones
- Tarea 4 - Metabolismo Celular-Grupo - 35 - BIOQUIMICADocumento24 páginasTarea 4 - Metabolismo Celular-Grupo - 35 - BIOQUIMICAMaida alejandra Ochoa castañedaAún no hay calificaciones
- Temas Examen de Bioquímica IIDocumento9 páginasTemas Examen de Bioquímica IIManuel Alejandro Iza GutierrezAún no hay calificaciones
- Actividad 1Documento11 páginasActividad 1Santiago CastilloAún no hay calificaciones
- 10 Ciclo Urea 23.1Documento38 páginas10 Ciclo Urea 23.1Angel Jeremy Garcia ArroyoAún no hay calificaciones
- Actividad Evaluativa Corte 3 - BioquimicaDocumento12 páginasActividad Evaluativa Corte 3 - Bioquimicavalentina guerreroAún no hay calificaciones
- Biosíntesis de Los AminoácidosDocumento32 páginasBiosíntesis de Los AminoácidosMarco Sanchez Olaya100% (1)
- Tema IV. Vitaminas Parte 2. Bioquímica para MedicinaDocumento58 páginasTema IV. Vitaminas Parte 2. Bioquímica para MedicinaAnnie RodríguezAún no hay calificaciones
- La Creatina Es Un PéptidoDocumento7 páginasLa Creatina Es Un PéptidotiterecchiutoAún no hay calificaciones
- Taller Metabolismo - Carbohidratos FinallDocumento15 páginasTaller Metabolismo - Carbohidratos FinallalejandraAún no hay calificaciones
- Metabolismo de Las ProteínasDocumento40 páginasMetabolismo de Las ProteínasFrank Sánchez Estela100% (1)
- Reacciones Generales de Los AminoácidosDocumento33 páginasReacciones Generales de Los AminoácidosFrancisco Abanto67% (3)
- Capitulo 6 Libro Nutricion de Las AvesDocumento20 páginasCapitulo 6 Libro Nutricion de Las AvesDiego MedinaAún no hay calificaciones
- 17 Procesamiento y Regulación de Proteínas 2Documento39 páginas17 Procesamiento y Regulación de Proteínas 2Estefania Correa RamirezAún no hay calificaciones
- Investigación Bioinformática de GluteninaDocumento12 páginasInvestigación Bioinformática de GluteninaVania OdetteAún no hay calificaciones
- Introduccion Al MetabolismoDocumento11 páginasIntroduccion Al MetabolismoMelissa CazaresAún no hay calificaciones
- Taller Sobre Componentes Quimicos Del Citoplasma BiologiaDocumento11 páginasTaller Sobre Componentes Quimicos Del Citoplasma BiologiaDiana SierraAún no hay calificaciones
- Casos ClínicosDocumento15 páginasCasos ClínicosJosé ÁvilaAún no hay calificaciones
- Cuestionario Biosintesis de AminoacidosDocumento7 páginasCuestionario Biosintesis de AminoacidosLeandro Torres CalabiAún no hay calificaciones
- Metabolismo Proteico Y Destinos Del NitrógenoDocumento171 páginasMetabolismo Proteico Y Destinos Del NitrógenoYohn LópezAún no hay calificaciones
- Metabolismo de Proteínas - T10Documento27 páginasMetabolismo de Proteínas - T10Eric JavierAún no hay calificaciones
- Metabolismo de ProteinasDocumento53 páginasMetabolismo de ProteinasJulio César AcevedoAún no hay calificaciones
- Orientaciones para El Trabajo Grupal Sobre Glucolisis Nilda 2021Documento7 páginasOrientaciones para El Trabajo Grupal Sobre Glucolisis Nilda 2021Patrick Ansport PvAún no hay calificaciones
- Teórico 13 Dra. Rosenstein - Texto Metabolismo de Aminoácidos - 2019-2Documento24 páginasTeórico 13 Dra. Rosenstein - Texto Metabolismo de Aminoácidos - 2019-2Symfora AtlanteAún no hay calificaciones
- Metabolismo de Las ProteinasDocumento5 páginasMetabolismo de Las ProteinasBryan S CalleAún no hay calificaciones
- Cuestionario Metabolismo de LípidosDocumento3 páginasCuestionario Metabolismo de LípidosSamuel Bonilla63% (16)
- CarbohidratosDocumento8 páginasCarbohidratoslavrAún no hay calificaciones
- Taller 06 Grupo 06 - AminoacidosDocumento3 páginasTaller 06 Grupo 06 - AminoacidosOctavio ScappatriccioAún no hay calificaciones
- Compuestos NitrogenadosDocumento192 páginasCompuestos NitrogenadosMilton IsraelAún no hay calificaciones
- Catabolismo de Los AminoácidosDocumento39 páginasCatabolismo de Los AminoácidosEd BozaAún no hay calificaciones
- Taller Final de BioquimicaDocumento22 páginasTaller Final de BioquimicaAndres Camilo Moreno GarciaAún no hay calificaciones
- FISIOLOGÍADocumento12 páginasFISIOLOGÍAyesenia lucy inquilla ariasAún no hay calificaciones
- METABOLISMO FOSFOCÁLCICO ResumenDocumento32 páginasMETABOLISMO FOSFOCÁLCICO ResumenIris zavalaAún no hay calificaciones
- Metabolismo Del Nitrogeno. DegradacionDocumento29 páginasMetabolismo Del Nitrogeno. DegradacionFernando Rodriguez ChavezAún no hay calificaciones
- Investigacion MutacionesDocumento9 páginasInvestigacion MutacionesAndrea sibaja AguirreAún no hay calificaciones
- SEMANA05Documento42 páginasSEMANA05Elías Mindreau GanozaAún no hay calificaciones
- GUIA DE ESTUDIO 15bioquimicaDocumento4 páginasGUIA DE ESTUDIO 15bioquimicaDiana MuñozAún no hay calificaciones
- Trabajo de Sintesis de Glucosa y MetioninaDocumento38 páginasTrabajo de Sintesis de Glucosa y Metioninajhon rosales astoAún no hay calificaciones
- Nutrición EnteralDocumento22 páginasNutrición Enteralcarlitos_cruz_4Aún no hay calificaciones
- VITAMINASDocumento2 páginasVITAMINASLuciana GanozaAún no hay calificaciones
- CarmonaGuzmanSarahy BQN5C TareasprimerparcialDocumento6 páginasCarmonaGuzmanSarahy BQN5C TareasprimerparcialFrancoAún no hay calificaciones
- NUTRICION Y DIETAS. Semana 9Documento17 páginasNUTRICION Y DIETAS. Semana 9cristina delia chombo cutipaAún no hay calificaciones
- Biosíntesis de Ácidos GrasosDocumento5 páginasBiosíntesis de Ácidos GrasosCarlos SosaAún no hay calificaciones
- T 2 - RX Generales de Los AAsDocumento31 páginasT 2 - RX Generales de Los AAslisetAún no hay calificaciones
- Imagen CarbohidratosDocumento35 páginasImagen Carbohidratoswild.addsystemAún no hay calificaciones
- LipidosDocumento14 páginasLipidosFernando Ortiz FrayreAún no hay calificaciones
- Preguntas NutriciónDocumento5 páginasPreguntas NutriciónThais TorresAún no hay calificaciones
- La Ciencia Del Metabolismo: Metabolismo sin rodeosDe EverandLa Ciencia Del Metabolismo: Metabolismo sin rodeosCalificación: 5 de 5 estrellas5/5 (1)
- Dotaciones de AguaDocumento5 páginasDotaciones de AguaRamonAún no hay calificaciones
- Instrumento de AutoevaluacionDocumento207 páginasInstrumento de AutoevaluacionSanti Belarcazar100% (1)
- Aviso Dos DicabiDocumento41 páginasAviso Dos DicabiPalma Hugo EscobarAún no hay calificaciones
- Remodelacion e Implementacion de LabortorioDocumento6 páginasRemodelacion e Implementacion de LabortorioGuillermo Gutierrez50% (2)
- Dextrosa AnhidraDocumento3 páginasDextrosa AnhidraErick LópezAún no hay calificaciones
- CapituloDocumento11 páginasCapituloYanirce Chireno Lizardo100% (1)
- Investigacion OctanajeDocumento6 páginasInvestigacion OctanajeLuis Gustavo Ugarte VallejosAún no hay calificaciones
- Temple y Rockwell FinalDocumento12 páginasTemple y Rockwell FinalStefanyAún no hay calificaciones
- Informe Preliminar Contratos Con Altos Montos Contratados y Tramites ExternosDocumento33 páginasInforme Preliminar Contratos Con Altos Montos Contratados y Tramites ExternosKatherine MartinezAún no hay calificaciones
- Libro Robot Structural EversionDocumento596 páginasLibro Robot Structural Eversionjuan pablo waked100% (1)
- LUNES 07 COMUNICACION - "Dialogamos para Planificar Nuestras Actividades Del Proyecto"Documento5 páginasLUNES 07 COMUNICACION - "Dialogamos para Planificar Nuestras Actividades Del Proyecto"Diana Valenzuela FelixAún no hay calificaciones
- Tipos de Mapaps Valles, Llanuras 6 GradoDocumento23 páginasTipos de Mapaps Valles, Llanuras 6 GradoIsmary EspinalAún no hay calificaciones
- Fundamento de La Motricidad en El Rendimientos Deportivo. Fernandez RomeroDocumento573 páginasFundamento de La Motricidad en El Rendimientos Deportivo. Fernandez RomeroJordi Cañadas LopezAún no hay calificaciones
- Ficha de Seguridad Pybuthrin 33Documento14 páginasFicha de Seguridad Pybuthrin 33HSEQ AGUACHICAAún no hay calificaciones
- Cronologia de La QuimicaDocumento18 páginasCronologia de La Quimicaubaldo enrique quijano tellezAún no hay calificaciones
- Perfiles Hotel Campestre BegoniaDocumento15 páginasPerfiles Hotel Campestre BegoniahotelbegoniaAún no hay calificaciones
- Actividad 1 - Neuropsicología y El Desarrollo Del Sistema Nervioso CentralDocumento5 páginasActividad 1 - Neuropsicología y El Desarrollo Del Sistema Nervioso CentralDelia Imbajoa CabreraAún no hay calificaciones
- Hoja de Datos de Seguridad Del Acido PropanoicoDocumento1 páginaHoja de Datos de Seguridad Del Acido PropanoicoARNULFO MUÑOZAún no hay calificaciones
- Popeadora de Kiwicha Pkt-30x-2Documento4 páginasPopeadora de Kiwicha Pkt-30x-2JB StrahlAún no hay calificaciones
- Frases de Autor Jorge BucayDocumento6 páginasFrases de Autor Jorge BucayLuis Enrique Lara MorenoAún no hay calificaciones
- Balanza de PagosDocumento4 páginasBalanza de Pagosnatalia ballinaAún no hay calificaciones
- Identificacion de Los Factores Que AfectanDocumento18 páginasIdentificacion de Los Factores Que AfectanenersolicAún no hay calificaciones
- Catalogo General Aerotecnica 19-12-2005Documento60 páginasCatalogo General Aerotecnica 19-12-2005YoAún no hay calificaciones
- 09 Tres Puertas-SanguanDocumento2 páginas09 Tres Puertas-SanguanElysenda ValAún no hay calificaciones
- ESPONDADocumento4 páginasESPONDAJoseAngelPalaciosCamposAún no hay calificaciones
- Test NitritosDocumento1 páginaTest NitritosMarceloAún no hay calificaciones
- Producto 6 Msc. Francisco IcazaDocumento4 páginasProducto 6 Msc. Francisco Icazasanty pro1023 IcazaAún no hay calificaciones
- Examen 2008 Jornada 2 Examen Admision Universidad de Antioquia UdeADocumento24 páginasExamen 2008 Jornada 2 Examen Admision Universidad de Antioquia UdeAJorge CanoAún no hay calificaciones
- CalorimetriaDocumento42 páginasCalorimetriaMALCA HIDALGO MARYCIELO ELIZABETHAún no hay calificaciones
- 2 Ficha Tecnica Frescasa FiberglassDocumento8 páginas2 Ficha Tecnica Frescasa Fiberglassno seAún no hay calificaciones