Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Quiz 3 - 2023-1
Cargado por
Angela Lorena DíazDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Quiz 3 - 2023-1
Cargado por
Angela Lorena DíazCopyright:
Formatos disponibles
Universidad de La Sabana
Facultad de Ingeniería
Ingeniería de las Reacciones Químicas – 2023-1
Tercer Quiz - 20% (Nivel introductorio)
Nombre: ____________________________________________ Código: ____________ Fecha:
__________
Docente: Manuel Fernando Valero
1. Resuelva en Excel de manera clara y ordenada los ejercicios que encuentre a continuación. Para cada
uno de los ejercicios, aplique todos los métodos que sea posible de acuerdo con las características de
los datos presentados y concluya cuál de ellos da el resultado más pertinente, cada uno acompañado
de su respectiva gráfica. El orden y claridad de la solución serán criterios de evaluación. Por
supuesto, cualquier sospecha de copia concluirá automáticamente una nota de 0.0.
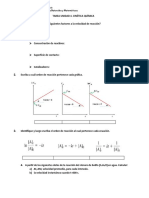
a) El clorato de potasio se descompone térmicamente a través de una reacción que se sabe es de
orden 2. Con los datos de la siguiente tabla, determine los parámetros cinéticos de la reacción.
Se sabe que en una de las muestras hubo contaminación cruzada, ¿a cuál de ellas se lo atribuye?
Muestra Velocidad Concentració Temperatur
(mol/s.L) n (mol/L) a (K)
1 4,90E-04 0,2 700
2 1,10E-04 0,02 750
3 2,10E-03 0,05 800
4 2,20E-02 0,08 850
5 1,18E-01 0,1 900
6 1,82E-02 0,06 950
b) Para estudiar la descomposición fotoquímica de bromo acuoso expuesto a luz solar brillante, se
disolvió una pequeña cantidad de bromo líquido en agua contenida en un frasco de vidrio y se
colocó bajo luz solar directa. Se obtuvieron los siguientes datos a 25°C:
Tiempo (min) 10 20 30 40 50 60
[Br2] (ppm) 2.45 1.74 1.23 0.88 0.62 0.44
Asumiendo condiciones de exposición idénticas, calcule la velocidad de inyección de bromo
(en libras/h) que se requiere en un cuerpo de agua asoleado con un volumen de 25 ,000 galones
con la finalidad de mantener un nivel esterilizante de bromo de 1.0 ppm.
c) La reacción química ¿ ¿ se da en la descomposición de dimetil éter en fase gas, en un reactor
batch a 540°C a volumen constante. Inicialmente solo (CH3)2O está presente. Por medio de un
experimento para determinar el orden de reacción y la constante de velocidad se obtuvieron los
siguientes datos
Tiempo (s) 390 777 1195 3155 ∞
Presión total 408 488 562 799 931
(mmHg)
Encuentre el orden de reacción y la constante de velocidad.
d) La descomposición térmica del cloruro de nitrilo se produciría de acuerdo con la siguiente
ecuación estequiométrica: 2NO2Cl ↔ 2NO2 + Cl2. Algunos de los resultados obtenidos en una
corrida a 180 °C fueron:
Tiempo 0 150 300 450 600 750 900
(s)
CNO2Cl 1.99 1.80 1.63 1.47 1.33 1.21 1.09
(mol/cm3)
Encuentre el orden de reacción y la constante de velocidad respecto al reactivo.
e) La descomposición del hidróxido de aluminio en alúmina y agua se efectuó en un reactor
discontinuo de volumen constante donde se registraron las siguientes medidas de concentración
en función del tiempo.
t (min) [Al(OH)3]
(mol/dm3)
0 2
5 1.6
9 1.35
15 1.1
22 0.87
30 0.70
40 0.53
60 0.35
Encuentre el orden de reacción y la velocidad de reacción específica. Se cree que el técnico
cometió un error de dilución en la concentración medida a los 60 minutos. ¿Qué puede concluir
usted?
f) En la siguiente tabla se muestran los datos cinéticos a 25ºC para la concentración de bromuro de
tert-butilo a alcohol tert-butílico. La reacción es (𝐶𝐻3)3𝐶𝐵𝑟+𝐻2𝑂→(𝐶𝐻3)3𝐶𝑂𝐻+𝐻𝐵𝑟. Proponer
una ecuación de velocidad que se ajuste a estos datos
Tiempo (h) [(CH3)3CBr
] (mol/ L)
0 0,1039
3,15 0,0896
4,1 0,0859
6,2 0,0776
8,2 0,0701
10 0,0639
13,5 0,0529
18,3 0,0353
26 0,027
30 0,0207
g) Un alimento gaseoso puro A, 88mmol/l a 1 atm y 25ºC, entra en un reactor de mezcla completa.
La reacción que ocurre es A → 3R. Determinar el orden de la reacción y la constante de
velocidad a partir de los siguientes datos:
τ (min) 11.4 20.2 31.7 46.7 90.9
CA, (mmol/L) 43 36 32 28 21
También podría gustarte
- Problemas resueltos de Hidráulica de CanalesDe EverandProblemas resueltos de Hidráulica de CanalesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Ejercicios de velocidad de reacciónDocumento2 páginasEjercicios de velocidad de reacciónMichelle PinzonAún no hay calificaciones
- GuiaCINETICA 2023Documento10 páginasGuiaCINETICA 2023lucas juanAún no hay calificaciones
- Tarea Cinética Química AaDocumento4 páginasTarea Cinética Química Aagustavo valdiviesoAún no hay calificaciones
- Taller Velocidad de ReaccionDocumento4 páginasTaller Velocidad de ReaccionJavier ClarosAún no hay calificaciones
- Cinética EjerciciosDocumento7 páginasCinética EjercicioslolazarAún no hay calificaciones
- Tarea ReaccionesDocumento6 páginasTarea ReaccionesNaysha LicuonaAún no hay calificaciones
- Hidrólisis ácida del acetato de etiloDocumento14 páginasHidrólisis ácida del acetato de etiloJazmin LeonAún no hay calificaciones
- Problemas Reacciones Bimoleculares PDFDocumento5 páginasProblemas Reacciones Bimoleculares PDFDanielle Domingueez0% (1)
- 2021 Tarea#4 - Cinética QuímicaDocumento9 páginas2021 Tarea#4 - Cinética QuímicaMartin ErazoAún no hay calificaciones
- Discusion 10Documento4 páginasDiscusion 10Elmer CardonaAún no hay calificaciones
- Repaso PC3Documento4 páginasRepaso PC3BC NandoAún no hay calificaciones
- Discusion 2Documento8 páginasDiscusion 2Dee-Deecita ItiAún no hay calificaciones
- Recovered Word 5Documento12 páginasRecovered Word 5Elvis Caballero TocasAún no hay calificaciones
- Met-2330, Primeros Examenes Parciales PDFDocumento12 páginasMet-2330, Primeros Examenes Parciales PDFRicardo BravoAún no hay calificaciones
- Cálculos cinéticos para diseño de reactores discontinuosDocumento18 páginasCálculos cinéticos para diseño de reactores discontinuosMiguel Angel GutierrezAún no hay calificaciones
- 04 Problemas de Cinética QuímicaDocumento15 páginas04 Problemas de Cinética QuímicaBrenda AJ.Aún no hay calificaciones
- Seminario de Cinetica QuimicaDocumento34 páginasSeminario de Cinetica QuimicaBriggit Gamarra Flores0% (1)
- Determinación de conductividades molaresDocumento11 páginasDeterminación de conductividades molarescristian espinozaAún no hay calificaciones
- Miercoles Saponificación Del Acetato de EtiloDocumento12 páginasMiercoles Saponificación Del Acetato de EtiloAnonymous Mp0qhmAún no hay calificaciones
- Práctica 3er PDocumento3 páginasPráctica 3er PBladimir Alex Quispe RochaAún no hay calificaciones
- RCTR CSTRDocumento11 páginasRCTR CSTRjosephAún no hay calificaciones
- SAPONIFICACI - N-DEL-ACETATO-DE-ETILO - Docx Filename - UTF-8''SAPONIFICACIÓN-DEL-ACETATO-DE-ETILODocumento8 páginasSAPONIFICACI - N-DEL-ACETATO-DE-ETILO - Docx Filename - UTF-8''SAPONIFICACIÓN-DEL-ACETATO-DE-ETILOYuri Ticona RuizAún no hay calificaciones
- Cinetica FinalDocumento1 páginaCinetica FinalLuis Vaca0% (1)
- Cinetica Serie 3Documento4 páginasCinetica Serie 3Angélica OMAún no hay calificaciones
- Practicas Primer Parcial de IngDocumento14 páginasPracticas Primer Parcial de IngramiroAún no hay calificaciones
- Ejercicios Guia 4Documento13 páginasEjercicios Guia 4DORIELYS DAYANA LOPEZ CASTRILLOAún no hay calificaciones
- 03 Balance de Materia Con Reaccion Quimica Hidratacion de Anhidrido AceticoDocumento9 páginas03 Balance de Materia Con Reaccion Quimica Hidratacion de Anhidrido AceticoAlexisEstradaAún no hay calificaciones
- Conductividad Electrica Disoluciones PDFDocumento14 páginasConductividad Electrica Disoluciones PDFFerAún no hay calificaciones
- Cinetica de LixiviacionDocumento5 páginasCinetica de LixiviacionJOAN RODOLFO PURIS CoNDORAún no hay calificaciones
- Villagomez CQC Rep 5Documento12 páginasVillagomez CQC Rep 5Adrián León PachecoAún no hay calificaciones
- Problemas. CineticaDocumento2 páginasProblemas. CineticaAMERICO VICTORIO ANTICONAAún no hay calificaciones
- Práctica 2 - Grupo 22 - EspañolDocumento28 páginasPráctica 2 - Grupo 22 - EspañoltatianaAún no hay calificaciones
- Problemario Segundo Parcial Fisicoquímica IiDocumento4 páginasProblemario Segundo Parcial Fisicoquímica IiLESLIE SILVA SANDOVALAún no hay calificaciones
- IR2 - Deber 2 - Datos Del Reactor BatchDocumento3 páginasIR2 - Deber 2 - Datos Del Reactor BatchSteven MenaAún no hay calificaciones
- Cinética de Reducción Del Ion PermanganatoDocumento6 páginasCinética de Reducción Del Ion PermanganatoCarlos MadridAún no hay calificaciones
- Informe Practica de AdsorciónDocumento7 páginasInforme Practica de AdsorciónYasmin Arteaga VelasquezAún no hay calificaciones
- Ejercicios de Química General - Cinética Química SIN RESOLUCIÓNDocumento7 páginasEjercicios de Química General - Cinética Química SIN RESOLUCIÓNAleAún no hay calificaciones
- Tercer Tutorial - Grupo 5Documento12 páginasTercer Tutorial - Grupo 5Amed Enrique Ortega MonteroAún no hay calificaciones
- Problemas Tarea Cinetica 1Documento83 páginasProblemas Tarea Cinetica 1Marisol BravoAún no hay calificaciones
- Practica No6Documento15 páginasPractica No6Karla Chavolla SalomonAún no hay calificaciones
- Segundo Examen Parcial QMC 1400Documento1 páginaSegundo Examen Parcial QMC 1400Harold Cesar Gabriel HerreraAún no hay calificaciones
- PROBLEMAS PROPUESTOS: TERMODINÁMICA QUÍMICADocumento4 páginasPROBLEMAS PROPUESTOS: TERMODINÁMICA QUÍMICAFlorPerettiAún no hay calificaciones
- Obtención de la ecuación de velocidad para la reacción de saponificación del acetato de etiloDocumento9 páginasObtención de la ecuación de velocidad para la reacción de saponificación del acetato de etilovaleria martinezAún no hay calificaciones
- Taller Cinetica QuimicaDocumento2 páginasTaller Cinetica QuimicaMICHELL FERNANDA VERGEL PEREZAún no hay calificaciones
- Oxidación Del Ion IoduroDocumento12 páginasOxidación Del Ion IoduroIsita AlvarezAún no hay calificaciones
- Ejercicios de Análisis y Diseño de ReactoresDocumento23 páginasEjercicios de Análisis y Diseño de ReactoresAngela SequeraAún no hay calificaciones
- Exame Final K Jueves 2022Documento14 páginasExame Final K Jueves 2022GRECIA PAULA TUESTA BECERRAAún no hay calificaciones
- Laboratorio FisicoquimicaDocumento4 páginasLaboratorio FisicoquimicaPilar GoezAún no hay calificaciones
- Guia de CineticaDocumento3 páginasGuia de CineticaMariana ZamoraAún no hay calificaciones
- Cinetica de LixiviacionDocumento13 páginasCinetica de LixiviacionJesusGlennMaldonadoLlacsahuangaAún no hay calificaciones
- Parciales CineticaDocumento19 páginasParciales CineticaJocelyn BernabeAún no hay calificaciones
- P 6 - Cinetica Quimica MarcelaDocumento3 páginasP 6 - Cinetica Quimica MarcelaDiego MiguelAún no hay calificaciones
- Documento Sin TítuloDocumento5 páginasDocumento Sin TítuloSebastian MerchanAún no hay calificaciones
- Trabajo 2.cinetica QuímicaDocumento5 páginasTrabajo 2.cinetica QuímicaBrenda GutierrezAún no hay calificaciones
- Práctica 1: Cinética de La Hidrólisis Del Acetato de EtiloDocumento13 páginasPráctica 1: Cinética de La Hidrólisis Del Acetato de EtiloSalvador MartínezAún no hay calificaciones
- CQC Rep 5 PDFDocumento12 páginasCQC Rep 5 PDFAdrián León PachecoAún no hay calificaciones
- TP 10 - Cinética QuímicaDocumento3 páginasTP 10 - Cinética QuímicaJuan AramayoAún no hay calificaciones
- Ejercicios de Análisis y Diseño de ReactoresDocumento21 páginasEjercicios de Análisis y Diseño de ReactoresGianna RivasAún no hay calificaciones
- Ejercicios para El Examen de Recuperacion de FisicoquimicaDocumento7 páginasEjercicios para El Examen de Recuperacion de FisicoquimicaAnthony FreireAún no hay calificaciones
- Niyc0717 50-51Documento2 páginasNiyc0717 50-51Angela Lorena DíazAún no hay calificaciones
- Guía Trabajo Final 2021-1Documento1 páginaGuía Trabajo Final 2021-1Ana Maria VallejoAún no hay calificaciones
- Quiz Área de MercadeoDocumento4 páginasQuiz Área de MercadeoAngela Lorena DíazAún no hay calificaciones
- Diapositivas ReposiciónDocumento23 páginasDiapositivas ReposiciónAngela Lorena DíazAún no hay calificaciones
- SecadoDocumento29 páginasSecadoAngela Lorena DíazAún no hay calificaciones
- UntitledDocumento3 páginasUntitledAngela Lorena DíazAún no hay calificaciones
- UntitledDocumento4 páginasUntitledAngela Lorena DíazAún no hay calificaciones
- Ruta EscogidaDocumento4 páginasRuta EscogidaAngela Lorena DíazAún no hay calificaciones
- Aceite Mineral: Q (Gal/min) Ge Viscosidad (KG/MS) P2 (Kpa) Z2 (M) P1 Z1 Densidad Del Aceite MineralDocumento10 páginasAceite Mineral: Q (Gal/min) Ge Viscosidad (KG/MS) P2 (Kpa) Z2 (M) P1 Z1 Densidad Del Aceite MineralAngela Lorena DíazAún no hay calificaciones
- Taller 1. ELVDocumento12 páginasTaller 1. ELVAngela Lorena DíazAún no hay calificaciones
- Parcial 2 - 2022-2Documento1 páginaParcial 2 - 2022-2Angela Lorena DíazAún no hay calificaciones
- (CH CO) O + H O 2Ch CoohDocumento1 página(CH CO) O + H O 2Ch CoohAngela Lorena DíazAún no hay calificaciones
- 2 - Rúbrica - Sustentación - Estudios Técnico Parte 1 - MartesDocumento2 páginas2 - Rúbrica - Sustentación - Estudios Técnico Parte 1 - MartesAngela Lorena DíazAún no hay calificaciones
- IntercambiadoresDocumento32 páginasIntercambiadoresAngela Lorena DíazAún no hay calificaciones
- Quiz 4 - 2023-1Documento2 páginasQuiz 4 - 2023-1Angela Lorena DíazAún no hay calificaciones
- Cálculo de cambios de entropía en procesos industriales usando ecuaciones de la termodinámicaDocumento8 páginasCálculo de cambios de entropía en procesos industriales usando ecuaciones de la termodinámicaKatherine Rodriguez100% (2)
- Miércoles, 16 de Junio de 2021, 14:01 Finalizado Miércoles, 16 de Junio de 2021, 14:26 24 Minutos 42 Segundos de 5,00 (%)Documento2 páginasMiércoles, 16 de Junio de 2021, 14:01 Finalizado Miércoles, 16 de Junio de 2021, 14:26 24 Minutos 42 Segundos de 5,00 (%)Juan Cruz FeresAún no hay calificaciones
- 0.4.formulario Examen AEMT 2018Documento8 páginas0.4.formulario Examen AEMT 2018JenAún no hay calificaciones
- Fisica Ii 2Documento13 páginasFisica Ii 2Andres RasAún no hay calificaciones
- Determinación de Fuerzas Aerodinámicas en Una Esfera y Una Media EsferaDocumento106 páginasDeterminación de Fuerzas Aerodinámicas en Una Esfera y Una Media Esferalidia montemayorAún no hay calificaciones
- Línea de Aducción Uc Ejemplo 1Documento3 páginasLínea de Aducción Uc Ejemplo 1GLENY YSABEL QUISPE BERNEDOAún no hay calificaciones
- Problemas hidráulica riegoDocumento4 páginasProblemas hidráulica riegoCristinaHernández0% (1)
- 5 Valvulas de Equilibrado HidraulicoDocumento20 páginas5 Valvulas de Equilibrado HidraulicoRene Arenas EnecalAún no hay calificaciones
- Aplicación de Las Ecuaciones Diferenciales para Determinar La Velocidad de Una Reacción QuímicaDocumento40 páginasAplicación de Las Ecuaciones Diferenciales para Determinar La Velocidad de Una Reacción QuímicaJEAN PIERRE ROJAS BAEZAún no hay calificaciones
- Craqueo catalítico: proceso de refinaciónDocumento2 páginasCraqueo catalítico: proceso de refinaciónRodolfo Bendezu DiazAún no hay calificaciones
- Oxidos de CarbonoDocumento28 páginasOxidos de CarbonoJorge Jorjais Rojas CabreraAún no hay calificaciones
- Serie 9Documento3 páginasSerie 9Julia SerrattoAún no hay calificaciones
- Fase 6 - Grupo - 211612 - 36 - AndresFelipeGutierrezDocumento13 páginasFase 6 - Grupo - 211612 - 36 - AndresFelipeGutierrezANDRES FELIPE GUTIERREZ HUERTASAún no hay calificaciones
- Intercambiadores de Tubo y CorazaDocumento27 páginasIntercambiadores de Tubo y CorazaDiana LuciaAún no hay calificaciones
- S - 10 Calor y TemperaturaDocumento34 páginasS - 10 Calor y Temperaturaxd xdAún no hay calificaciones
- Parcial 2Documento3 páginasParcial 2zxcvbnbmmnbvcxzAún no hay calificaciones
- Unidad I: Propiedades de Los Fluidos: ResoluciónDocumento99 páginasUnidad I: Propiedades de Los Fluidos: ResoluciónSejas Claure SebastianAún no hay calificaciones
- Practica #9Documento9 páginasPractica #9Gerardo Estefano Sanchez PalominoAún no hay calificaciones
- Clase 11 Ecuacion Conduccion de Calor Radio CriticoDocumento23 páginasClase 11 Ecuacion Conduccion de Calor Radio Criticoalejandra patiñoAún no hay calificaciones
- Práctica 2 (Convección Natural y Convección Forzada) - LABORATORIO IIIDocumento51 páginasPráctica 2 (Convección Natural y Convección Forzada) - LABORATORIO IIIBárbaraAún no hay calificaciones
- Contenido: Excelencia Empresarial Ingenieria en Industria Y MecánicaDocumento26 páginasContenido: Excelencia Empresarial Ingenieria en Industria Y MecánicakevinAún no hay calificaciones
- Comercialización de hidrocarburos y derivadosDocumento35 páginasComercialización de hidrocarburos y derivadosAdith VargasAún no hay calificaciones
- Química Analítica I: Dra. Norma Rodríguez LagunaDocumento65 páginasQuímica Analítica I: Dra. Norma Rodríguez LagunaYazAún no hay calificaciones
- Oferta Académica Lapso 20222 Ingeniería QuímicaDocumento2 páginasOferta Académica Lapso 20222 Ingeniería QuímicajosuegolindanoAún no hay calificaciones
- Diseño de biodigestor autolimpiable para el caserío El Granero LlushcampaDocumento2 páginasDiseño de biodigestor autolimpiable para el caserío El Granero LlushcampaNey CoronelAún no hay calificaciones
- Catálisis - Unidad 3Documento55 páginasCatálisis - Unidad 3Corazon ContentoAún no hay calificaciones
- 4 Presión Requerida para El Transporte de HidrocarburosDocumento30 páginas4 Presión Requerida para El Transporte de HidrocarburosSonya Mamani ChambiAún no hay calificaciones
- Flujo: EnergiaDocumento25 páginasFlujo: EnergiaNaviroAún no hay calificaciones
- Cap. 2 Introducción A La ConducciónDocumento8 páginasCap. 2 Introducción A La ConducciónAlcides Roa RománAún no hay calificaciones
- Cuadro Comparativo Transferencia de Calor SALAZARDocumento1 páginaCuadro Comparativo Transferencia de Calor SALAZARDaniel Salazar Rojas100% (1)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaCalificación: 5 de 5 estrellas5/5 (200)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- La invasión de la pseudociencia: Claves para orientarse en un mundo en donde casi todo es posibleDe EverandLa invasión de la pseudociencia: Claves para orientarse en un mundo en donde casi todo es posibleCalificación: 4.5 de 5 estrellas4.5/5 (15)
- Psiconeuroinmunología para la práctica clínicaDe EverandPsiconeuroinmunología para la práctica clínicaCalificación: 5 de 5 estrellas5/5 (4)
- Disciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreDe EverandDisciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreCalificación: 5 de 5 estrellas5/5 (3)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- Zensorialmente : Dejá que tu cuerpo sea tu cerebroDe EverandZensorialmente : Dejá que tu cuerpo sea tu cerebroAún no hay calificaciones
- Borges y la memoria: De "Funes el memorioso" a la neurona de Jennifer AnistonDe EverandBorges y la memoria: De "Funes el memorioso" a la neurona de Jennifer AnistonCalificación: 5 de 5 estrellas5/5 (4)
- Nunca fuimos modernos: Ensayos de antropología simétricaDe EverandNunca fuimos modernos: Ensayos de antropología simétricaAún no hay calificaciones
- Fisiopatología de las enfermedades cardiovascularesDe EverandFisiopatología de las enfermedades cardiovascularesCalificación: 5 de 5 estrellas5/5 (1)
- Resumen de Pensar rápido pensar despacio de Daniel KahnemanDe EverandResumen de Pensar rápido pensar despacio de Daniel KahnemanCalificación: 4.5 de 5 estrellas4.5/5 (11)
- Investigación de operaciones: Conceptos fundamentalesDe EverandInvestigación de operaciones: Conceptos fundamentalesCalificación: 4.5 de 5 estrellas4.5/5 (2)
- Anatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasDe EverandAnatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasCalificación: 4.5 de 5 estrellas4.5/5 (21)
- Reconstrucción de dientes endodonciados: Pautas de actuación clínicaDe EverandReconstrucción de dientes endodonciados: Pautas de actuación clínicaCalificación: 5 de 5 estrellas5/5 (4)
- Estoicismo y dureza mental: Descubre los secretos psicológicos de la filosofía estoica en la vida moderna. Construir una autodisciplina inquebrantable y hábitos diarios que garanticen el éxitoDe EverandEstoicismo y dureza mental: Descubre los secretos psicológicos de la filosofía estoica en la vida moderna. Construir una autodisciplina inquebrantable y hábitos diarios que garanticen el éxitoCalificación: 4 de 5 estrellas4/5 (23)
- Cálculo infinitesimal: El lenguaje matemático de la naturalezaDe EverandCálculo infinitesimal: El lenguaje matemático de la naturalezaCalificación: 5 de 5 estrellas5/5 (3)
- Interpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasDe EverandInterpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasAún no hay calificaciones
- Teoría de juegos: Una introducción matemática a la toma de decisionesDe EverandTeoría de juegos: Una introducción matemática a la toma de decisionesCalificación: 4 de 5 estrellas4/5 (1)
- Estadística básica: Introducción a la estadística con RDe EverandEstadística básica: Introducción a la estadística con RCalificación: 5 de 5 estrellas5/5 (8)
- Desastres y emergencias. Prevención, mitigación y preparaciónDe EverandDesastres y emergencias. Prevención, mitigación y preparaciónCalificación: 4 de 5 estrellas4/5 (5)